Изобретение относится к медицине, в частности к неврологии, и может быть использовано в лечении болевой формы полинейропатии, в частности диабетической.
Болевая форма периферической (дистальной) диабетической нейропатии (БПДН) является основной причиной ухудшения качества жизни пациентов с сахарным диабетом 2 типа (СД2).
Выраженная нейропатическая боль, проявляющаяся жжением, онемением, покалыванием, стреляющими болями наблюдается не менее чем у 20% пациентов с БПДН [Храмилин В.Н., Давыдов О.С. Болевая диабетическая полинейропатия: диагностика и лечение с позиций доказательной медицины. Российский журнал боли. 2021; 19(4):44-59].
Поражение крупных нервных волокон приводит к возникновению парестезий и ощущению онемения стоп на фоне дистальных нарушений чувства вибрации, суставно-мышечного чувства и ощущения тактильного давления, а также аномальных (явно сниженных или отсутствующих) ахилловых рефлексов. Ощущения покалывания, дистальных нарушений чувства вибрации и жжения отражают поражение мелких волокон, что в конечном итоге приводит к стойкой нейропатической боли, поражающей около 20% пациентов с СД [Рудакова И.Г. Неврологические расстройства при основных клинических формах нарушения углеводного обмена: дис. - Российская медицинская академия последипломного образования, 2003].
Болевой синдром сопровождается гиперпатией (интенсивная боль, персистирующая после прекращения болевой стимуляции), гипералгезией (выраженная боль при нанесении умеренного по интенсивности раздражителя) и аллодинией (появление болевых ощущений под действием неболевых раздражителей - прикосновения покрывала, теплового воздействия и т.д.) [Тора A. et al. Chronic inflammatory demyelinating polyneuropathy mimicking an acute painful diabetic neuropathy // Neurological Sciences. - 2015. - T. 36. - №. 8. - C. 1509-1510.]. Боль может существенно ограничивать ходьбу больного, физическую нагрузку и, как следствие, приводить к увеличению веса. Боль при БПДН обычно более выражена ночью и часто мешает нормальному сну человека.
Боль может сопровождаться необычными ощущениями, такими как чувство отечности стоп или сильное похолодание ног, странными ощущениями при ходьбе, подобными «ходьбе по гальке» или «хождению по горячему песку» и т.д. [Tesfaye S., Boulton A.J. М., Dickenson А.Н. Mechanisms and management of diabetic painful distal symmetrical polyneuropathy // Diabetes care. - 2013. - T. 36. - №. 9. - C. 2456-2465].
Поиск эффективных методов лечения болевой формы периферической диабетической полинейропатии всегда был серьезной проблемой. Основным методом профилактики и лечения БПДН является достижение и длительное поддержание оптимального гликемического контроля у больных с СД. Но, к сожалению, в реальной клинической практике длительное обеспечение целевых значений углеводного обмена возможно лишь у части пациентов. При этом даже улучшение компенсации углеводного обмена и доведение его показателей до целевых значений у больных СД не приводит к достаточному противоболевому эффекту [Танашян М.М., Антонова К.В., Раскуражев А.А. Диабетическая полинейропатия: патогенез, клиника, подходы к персонифицированной коррекции. Медицинский Совет. 2017; (17):72-80].
Классические лекарственные средства, применяемые для терапии нейропатической боли, такие, как антидепрессанты, антиконвульсанты (Карбамазепин, Габапентин, Дулоксетин, Прегабалин и др.), требуют высоких доз для контроля боли, при этом потенцируют развитие существенных системных побочных эффектов [Клинические рекомендации. Сахарный диабет 2 типа у взрослых. 2019. URL: tps://www.endocrincentr.ru/sites/default/files/specialists/science/clinic-recomendations/saharnyy_diabet_2_tipa_u_vzroslyh.pdf]. Пластыри с высокими дозами капсаицина, используемые для местного применения, обладают менее выраженным системным действием.
Для терапии болевого синдрома при диабетической полинейропатии используются также акупунктура и электроакупунктура [doi: 10.1186/1745-6215-14-225 Cite this article as: Lee et al.: Electroacupuncture to treet painful diabetic neuropathy: study protocol for a three-armed, randomized, controlled pilot trial. Trials 2013 14:225]. В рандомизированное контролируемое исследование (Acupuncture in Patients with Diabetic Peripheral Neuropathy-Related Complaints: A Randomized Controlled Clinical Trial // J Clin Med. 2023 Mar; 12(6): 2103. Published online 2023 Mar 7. doi: 10.3390/jcm12062103; https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10055667/) были включены пациенты с СД2 и симптомами нейропатии нижних конечностей. Всего в течение 8 недель было проведено 12 процедур иглоукалывания. Результаты показали, что иглоукалывание приводит к значительному и длительному уменьшению жалоб, связанных с ДПН.
Используются также хирургические методы лечения полинейропатии (которые иногда вызывают ухудшение состояния здоровья больного), например, описанные ниже 1 и 2.
1. Постоянная электростимуляция. Эффективность и безопасность данного способа лечения в настоящее время недостаточно изучены. Кроме того, способ довольно сложен в исполнении при лечении нейропатий [Gtinter, Жан Дельбек & Макс Ортис-Каталан - Журнал нейроинженерии и реабилитации. Номер статьи 13 (2019) - Безопасность долговременной электрической стимуляции периферических нервов: обзор уровня техники].
2. Деструктивные операции в области входных зон задних корешков. Они используются только при отсутствии эффекта от применения других видов лечения и при показателе выраженности болевого синдрома не менее 70 баллов по визуально-аналоговой шкале (ВАШ). Эти методы являются технически сложными и могут выполнятся только специалистами нейрохирургического профиля [Исагулян Э.Д. и др. Нейромодуляция в лечении хронической неонкологической боли (из клинических рекомендаций «Хирургическое лечение хронического нейропатического болевого синдрома») //Клиническая и экспериментальная хирургия. - 2016. - Т. 4. - №. 3(13). - С. 74-88].
При хронических болевых синдромах достаточно широко используют инъекции ботулотоксина типа А (БТА) [Артеменко А. Р. и др. Токсин ботулизма типа А в лечении болевых синдромов //РМЖ. - 2008. - Т. 16. - №. 30. - С. 40-44. https://www.rmj.ru/articles/bolevoy_sindrom/Toksin_botulizma_tipa_A_v_lechenii_bolevyh_sindromov/]. Основанием для этого являются свойства БТА уменьшать ноцицептивную трансдукцию, поскольку, помимо блокирования высвобождения ацетилхолина, он ингибирует высвобождение местных ноцицептивных нейропептидов, таких как субстанция Р, кальцитонин-ген-родственный пептид (CGRP).
Известен «Способ лечения пациентов среднего возраста с хроническим болевым синдромом при дорсопатиях вертеброгенного и невертеброгенного генеза» (патент РФ №2740268, опубл. 12.01.2021), в котором ботулинотерапию используют вместе с лечебной физкультурой и паравертебральной высокоинтенсивной лазеротерапей.
Известно применение ботулотоксина для профилактики хронической мигрени (патент РФ №2549981, опубл. 10.05.2015), для купирования болевого синдрома после эндопротезирования молочных желез (патент РФ №2746035, опубл. 06.04.2021).
Фармацевтическую композицию, включающую ботулинический токсин типов А, В, С, D, Е, F, G в дозе от 0,01 до 250 ЕД, предпочтительно от 0,01 до 20 единиц, в сочетании с гиалуроновой кислотой, применяют для лечения болевого синдрома в стопе при подошвенном фасциите, фасциите стопы, диабете и подагре. Композицию подкожно вводят в подошву 1-2 раза в три месяца (патент РФ №2734159, зарег. 13.10.2020). В описании изобретения приведены примеры применения композиции только на животных.
Опубликован ряд нижеприведенных работ по применению ботулинического токсина при болевой диабетической нейропатии.
1. В исследовании Юань Р.Ю. и др. [Юань Р.Ю. и др. Ботулинический токсин при диабетической нейропатической боли: рандомизированное двойное слепое перекрестное исследование // Неврология. - 2009. - Т. 72. - №. 17. - С. 1473-1478] ботулотоксин типа А (Ботокс) вводился с целью лечения диабетической нейропатии в 12 точек тыльной поверхности каждой стопы внутрикожно по 50 ЕД в стопу в объеме 1,2 мл 0,9%-го хлорида натрия. При этом каждая инъекция составляла приблизительно 4 ЕД (0,10 мл раствора БТА). Инъекции распределялись в виде сетки таким образом, чтобы расстояние между ними было приблизительно равным, обычно на расстоянии от 2 до 3 см друг от друга.
2. В исследовании Шахиназ X., Тамер Э., Менем А. А. «Ботулинический токсин типа А при болезненной диабетической невропатии: открытое исследование» (Египетский журнал неврологии, психиатрии и нейрохирургии. - 2021. - Т. 57. - №. 1) ботулотоксин типа А (Ботокс) вводился с целью лечения диабетической нейропатии внутрикожно в тыльную поверхность стопы по 48 ЕД суммарно в каждую стопу. Точки введения ботулотоксина в исследовании не указаны.
3. В исследовании Ghasemi et al. [Гасеми М., Ансари М., Басири К., Шайганнеджад В. «Влияние внутрикожных инъекций ботулинического токсина типа А на болевые симптомы пациентов с диабетической нейропатией». J Res Med Sci. 2014 Февраль; 19(2):106-11. PMID: 24778662; PMCID: PMC3999594] ботулотоксин типа А (Диспорт) вводился с целью лечения диабетической нейропатии внутрикожно по 8-10 ЕД в 12 точек тыльной поверхности стопы по 100 ЕД в каждую стопу.
4. Taheri et al. [Тахери M., Седагхат M., Солпур А., Ростами П., Сафарпур Лима Б. «Влияние внутрикожных инъекций ботулинического токсина А на болезненную диабетическую полиневропатию. Метаболический синдром диабета». 2020 Ноябрь-декабрь; 14(6):1823-1828. doi: 10.1016/j.dsx.2020.09.019. Epub 2020, 14 сентября. PMID: 32961514] ботулотоксин типа А (Диспорт) вводили с целью лечения диабетической нейропатии внутрикожно с помощью инсулиновых шприцев в подошвенную поверхность стопы по 150 ЕД в 20 точек каждой стопы на расстоянии 1 см. Расположение точек не указано. Общий объем инъекции для каждого пациента был равен 4 мл. Оценка боли по ВАШ значительно улучшилась у пациентов, которым вводили ботулотоксин А, по сравнению с пациентами, которые получали плацебо (0,9% хлорид натрия) (Р<0,001 для всех). Ощущение жара было значительно ниже у тех пациентов, которым ботулотоксин А вводился в обе стопы по сравнению с пациентами, которым в одну стопу вводился ботулотоксин А, а в другую плацебо (Р=0,003).
Несмотря на имеющиеся наработки, ботулинотерапия нуждается в дальнейшем развитии.
Раскрытие сущности изобретения
Определение понятий
1. Стопа - дистальный отдел нижней конечности человека.
2. Подошва, или ступня - часть стопы, непосредственно соприкасающаяся с опорной поверхностью.
3. Точки костной опоры стопы при стоянии - бугор пяточной кости (пяточный бугор) и головки 1-й и 5-й плюсневых костей.
4. Опорные области стопы при стоянии - области под точками костной опоры, а именно, пятка и подушечка стопы; опорные области при ходьбе - те же, а также боковой (наружный) край стопы и область под дистальной фалангой большого пальца.
5. Точки 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 -условные обозначения (условная нумерация) точек введения БТА под кожу подошвы согласно изобретению, принятые (принятая) для удобства описания расположения точек. При осуществлении изобретения нумерация точек не используется.
Предлагаемый способ лечения болевой формы периферической (дистальной) диабетической полинейропатии характеризуется тем, что вводят ботулинический токсин типа А - гемагглютинин комплекс (БТА) подкожно в подошву стопы в точки, расположенные на опорных областях стоп: пятке, подушечке, боковом крае и большом пальце.
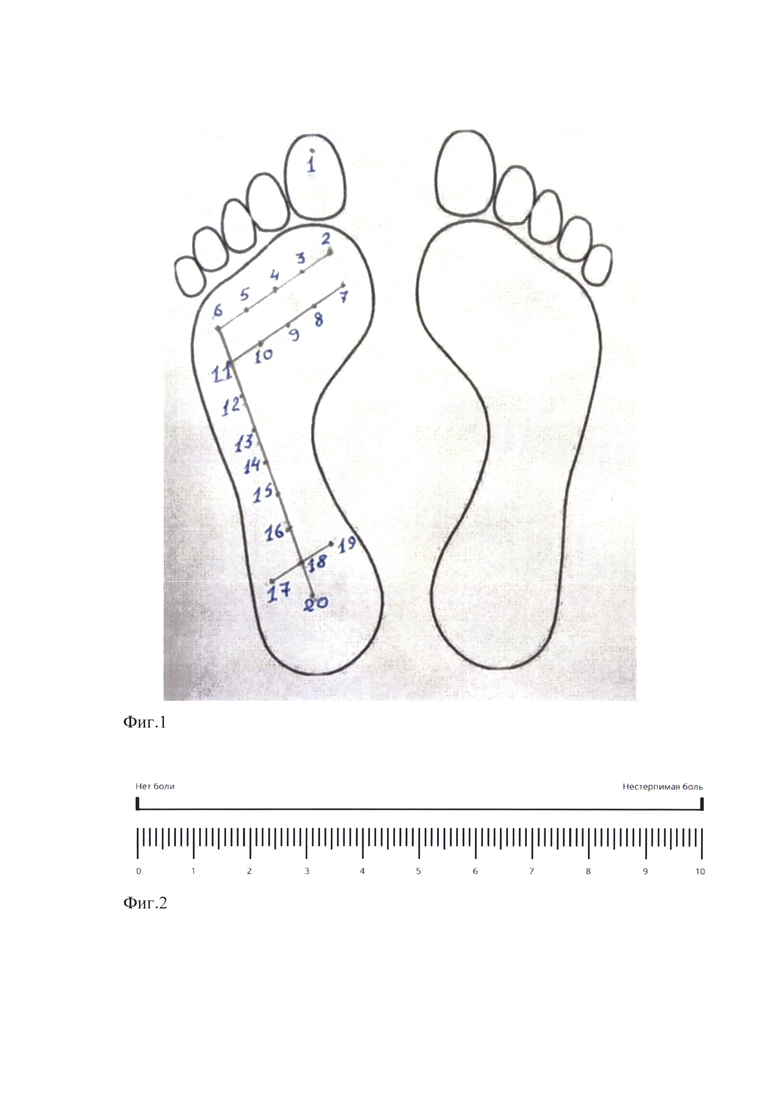
БТА вводят в 20 точек каждой стопы, которые располагают (распределяют) на подошве следующим образом: точку 1 - в центре дистальной фаланги большого пальца, точку 2 - под головкой первой плюсневой кости, точку 6 - под головкой пятой плюсневой кости, точку 20 -под пяточным бугром; на отрезке между точками 2 и 6 располагают на равном расстоянии друг от друга точки 3, 4, 5; на отрезке между точками 6 и 20 располагают на равном расстоянии друг от друга точки 11, 12, 13, 14, 15, 16, 18; на отрезке, параллельном и равном отрезку 2-6, проведенном от него на расстоянии, равном отрезку 6-11, равноудаленно друг от друга располагают точки 7, 8, 9, 10; через точку 18 проводят линию, параллельную отрезку 7-11, и откладывают на ней в обе стороны от точки 18 на расстоянии, равном отрезку 5-6, точки 17 и 19 (фиг. 1).
Технические результаты
1. При диабетической полинейропатии прежде всего повреждаются мелкие нервные волокна, а на подошве они в наибольшей степени травмируются в опорных областях стопы. Предлагаемый способ направлен на обезболивание прежде всего наиболее нагружаемых опорных областей стопы - пятки, подушечки стопы, области дистальной фаланги первого пальца, наружно-боковой части ступни.
2. Почти вся подошва человека иннервируется тремя крупными нервами: болыпеберцовым нервом (Nervus tibialis) и его ветвями - медиальным подошвенным нервом (Nervus plantaris medialis) и латеральным подошвенным нервом (Nervus plantaris lateralis). Точки введения БТА в соответствии с предлагаемым способом охватывают в большей или меньшей степени области иннервации подошвы всеми тремя нервами.
3. Однократное введение препарата в соответствии с предлагаемым способом обеспечивает снижение боли на 12 недель (срок наблюдения).
4. Через 1 неделю после однократного введения БТА интенсивность боли у пациентов по сравнению с ее интенсивностью до введения БТА была ниже на 15 баллов по визуально-аналоговой шкале (ВАШ); через 3 недели - на 28 баллов; через 12 недель - на 30 баллов.
5. Оценка качества жизни пациентов с использованием опросника SF-36 по физическому и по психологическому компоненту здоровья через 12 недель после введения БТА показала достоверное улучшение качества жизни по каждому из компонентов на 16 баллов.
Перечень фигур иллюстративного материала
Фиг. 1. Расположение точек введения БТА в подошву стопы в соответствии с предлагаемым способом.
Фиг. 2. Визуально-аналоговая шкала для оценки интенсивности боли.
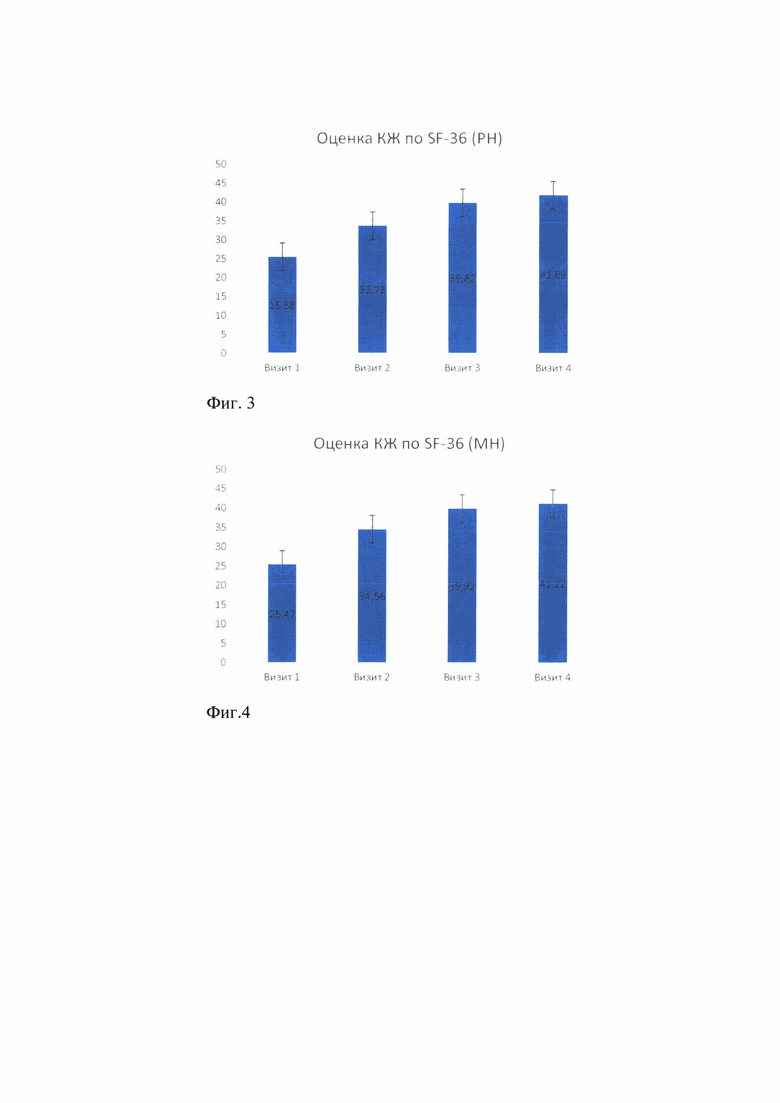
Фиг. 3. Оценка качества жизни по физическому компоненту здоровья (SF-36).
Фиг. 4. Оценка качества жизни по психологическому компоненту здоровья (SF-36).
Группа пролеченных больных включала лиц мужского и женского пола в возрасте 28-89 лет с впервые выявленным сахарным диабетом 2-го типа (СД2) или с СД2 давностью 5 и более лет.
До начала лечения пациенты были всесторонне обследованы.
Пациенты направлялись на консультацию невролога для оценки состоятельности функции периферической нервной системы. Выявлялись клинические признаки периферической дистальной нейропатии (ПДН) как неврологического осложнения хронической гипергликемии.
При обследовании пациентов использовались клинические, лабораторно-инструментальные и статистические методы. В рамках перечисленных были применены следующие методы: клинико-неврологическое обследование, включая классический неврологический осмотр, тестирование (Шкала балльной оценки симптомов нейропатии «Neuropathy Symptom Score» (NSS), Мичиганский инструмент скрининга нейропатии «Michigan Neuropathy Screening Instrument)) (MNSI)).
Нейрофизиологическое исследование включало проведение стимуляционной ЭНМГ с использованием стандартных встроенных программ на четырехканальном электромиографе «Нейро-МВП» аппаратом «Нейрософт МВП4» по стандартной методике. Стимуляционная ЭНМГ проводилась по нервам нижних конечностей с 2-х сторон по стандартной методике с тестированием моторных волокон по п. Peroneus и п. Tibialis, а также сенсорных волокон по п. Suralis и п. Saphenus. Лабораторная диагностика выполнялась по стандартному протоколу обследования пациентов с СД2 и нарушением толерантности к глюкозе, ассоциированных с механизмами повреждения, включая определение уровней интерлейкина-6 (ИЛ-6) и фактора некроза опухоли α (ФНО-α).
После введения БТА проводилось тестирование пациентов с использованием ВАШ, шкалы оценки качества жизни (SF-36). Статистическая обработка результатов осуществлялась с помощью программы IBM SPSS Statistics 21, МС Exel.
Всего было обследовано и пролечено 20 пациентов с длиной стопы 23,5-27 см. Для инъекций использовали препарат БТА российского производства компании «НПО «Микроген» - «Релатокс» - токсин ботулинический типа А в комплексе с гемагглютинином. Препарат «Релатокс» (лиофилизат для приготовления раствора для инъекций) растворяли в 0,9%-м хлориде натрия для инъекций. Во флакон со 100 ЕД препарата «Релатокс» (далее также - БТА) добавляли 2 мл физраствора.
Для введения разведенного препарата БТА использовали инсулиновый шприц объемом 1 мл с интегрированной иглой и одной шкалой U-100. Длина иглы составляла 8 мм, размер 30G. Внешний диаметр иглы составлял 0.3 мм. Шприц содержал 1 мл (50 ЕД) разведенного БТА для обкалывания одной стопы. В обе стопы вводили 100 ЕД БТА, по 0.05 мл раствора БТА в точку инъекции (2.5 ЕД).
Препарат БТА вводили подкожно в 20 точек подошвенной части каждой стопы. Расположение точек описано выше и ниже в клиническом примере, а также показано на фиг.1. Местоположение точек 1, 2, 6 и 20 уточнялось пальпацией с целью учета индивидуальных анатомических особенностей стопы пациента.
Для проведения линий и обозначения точек на подошве использовали зеленку в маркере ЛЕККЕР (зеленка карандаш / спиртовой раствор бриллиантового зеленого 1%, 5 мл).
Оценка нейропатической боли до введения препарата БТА, через неделю, через 3 недели и через 12 недель после однократного введения БТА проводилась с использованием ВАШ.
При оценке по ВАШ используется шкала со значениями от 0 до 10 (в нашем случае - до 100 с учетом промежуточных делений) (фиг. 2), по которой пациент может отметить степень боли или дискомфорта. Значению «0» соответствует «отсутствие боли», а значению «100» - «сильнейшая вообразимая боль».
Результаты оценки интенсивности боли представлены в таблице 1.

Приведенные данные показывают уменьшение интенсивности боли после однократного введения БТА по сравнению с ее интенсивностью до введения БТА на 15,05 баллов по ВАШ (F=7,92, р=0,01) через 1 неделю; на 28,1 балл (F=22,9, р=0,00) - через 3 недели; на 29,65 баллов (F=29,32, р=0,00) через 12 недель. Интенсивность боли снизилась на 30 баллов и более по ВАШ у 45% пациентов через 12 недель после инъекции БТА.
Для сравнения приведем результаты ботулинотерапии из статьи «Ботулинотерапия невропатической боли» Медведевой Л.А., Загорулько О.И., Шевцовой Г.Е. (Российский журнал боли. 2020; 18(2):34 39): через неделю после лечения уменьшение боли по ВАШ составило 8,3 балла, через 12 недель - 25,3 балла. Сравнение показывает, что при лечении по предлагаемому способу через неделю уменьшение боли было на 6,75 балла больше, а через 12 недель на 4,85 балла больше, чем в статье Медведевой Л.А. и соавт.
Результаты оценки качества жизни пациентов с использованием опросника SF-36 по физическому компоненту здоровья РН (максимальный возможный балл 66,32) до введения препарата, через 1, 3, 12 недель после введения БТА по предлагаемому способу представлены в таблице 2.
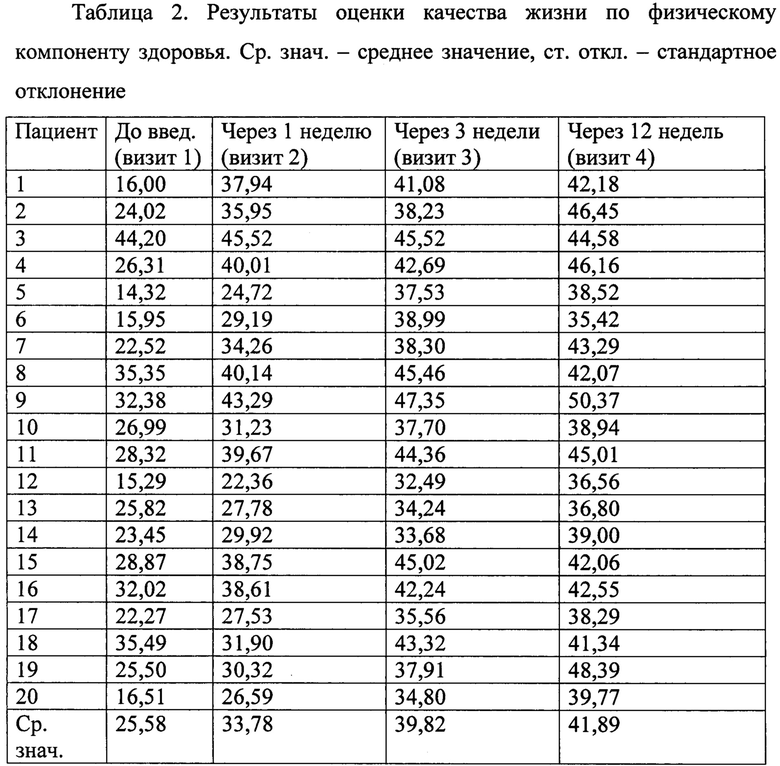
Отмечено достоверное улучшение качества жизни пациентов по РН в сравнении с состоянием до введения препарата на 8,2 балла через неделю после введения БТА (р<0,05); на 14,24 балла (р<0,05) через 3 недели; на 16,31 балла (Р<0,05) через 12 недель. Оценка качества жизни (КЖ) по физическому компоненту здоровья (SF-36) в виде диаграммы представлена на фиг. 3.
Результаты оценки качества жизни пациентов с использованием опросника SF-36 по психологическому компоненту здоровья МН (максимальный возможный балл 69,08) до введения препарата, через 1, 3, 12 недель после введения БТА представлены в таблице 3.
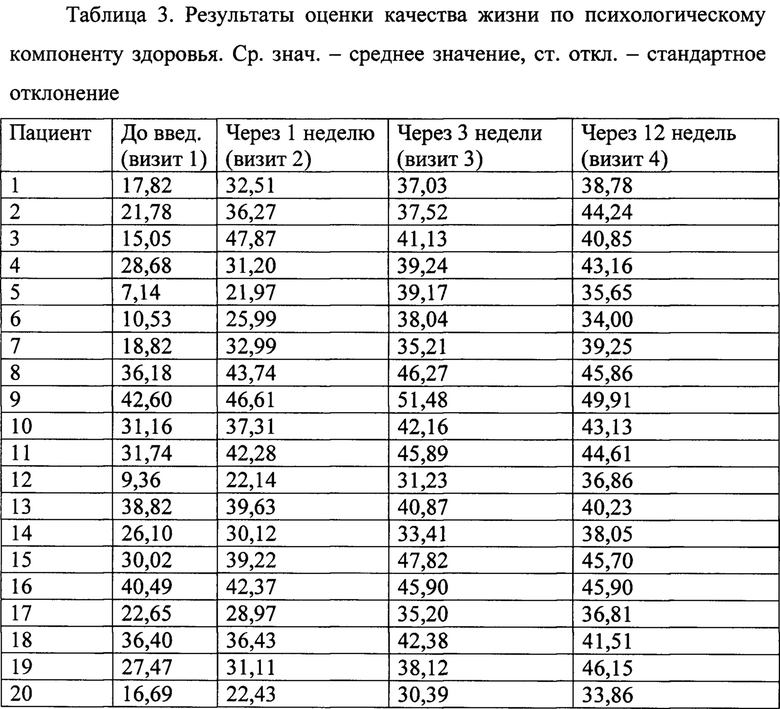

Отмечено достоверное улучшение качества жизни по МН в сравнении с состоянием до введения препарата на 9,09 балла через неделю после введения БТА (р<0,05); на 14,45 балла (р<0,05) через 3 недели; на 15,75 балла (Р<0,05) через 12 недель. Оценка качества жизни по психологическому компоненту здоровья (SF-36) в виде диаграммы представлена на фиг. 4.
Наиболее существенное улучшение качества жизни пациентов, как по РН, так и по МН, отмечалось в период между 2-м и 3-м визитами (р<0,05). В дальнейшем динамика улучшения качества жизни замедлялась, что отражает отсутствие достоверных различий в показателях 3 и 4 визита (р=0,14 для РН и р=0,42 для МН).
Результаты оценки качества жизни соответствуют показателям, полученным при использовании ВАШ, что в совокупности указывает на снижение выраженности болевого синдрома при ПДН и эффективность применения БТА в соответствии с предлагаемым способом.
Клинический пример
Пациент А. Пол: М., возраст: 62 года.
Пациент предъявляет жалобы на боли, онемение в руках и ногах, ощущение «мурашек» в дистальных отделах конечностей. Болевой синдром соответствует 44 мм по ВАШ, мешает повседневной деятельности. Пациент отмечает появившиеся в течение года периодическое чувство жажды, быструю утомляемость, снижение толерантности к физическим нагрузкам. Сопутствующие заболевания: АГ 3 степени; ГБ II стадии, риск 3, компенсированная; целевой уровень АД 130/80. Ожирение II степени. Бессимптомная бактериурия. Артифакия левого глаза (2016 год). Постоянно принимает препараты: таб. Лозартан 25 мг утром, таб. Амлодипин 10 мг вечером, таб. Розувастатин 10 мг вечером, таб. Карбамазепин 200 мг 3 раза в день (антиконвульсанты принимает в терапии болевого синдрома, парестезий в ногах).
При физикальном обследовании выявлено: рост пациента 166 см, вес 101 кг, ИМТ 36,65, что соответствует ожирению II степени, конституционально-алиментарному. Обхват талии 107 см, что соответствует абдоминальному ожирению. АД на момент измерения на правой руке 125/70 мм. рт.ст, на левой - 120/70 мм. рт.ст.
По данным ЭКГ - синусовый ритм с ЧЖС 71 в минуту, умеренные изменения миокарда (соответствуют возрастной норме).
По данным ЭХОКГ - размеры камер сердца в пределах нормальных значений. Уплотнение створок митрального клапана с регургитацией I-II степени. Трикуспидальная регургитация I степени. Сократительная способность миокарда левого желудочка сохранена, фракция выброса 72%.
Показатели, оцениваемые в рамках общего анализа крови, были в пределах нормальных значений. В биохимическом анализе крови отмечено повышение общего холестерина до 6.19 ммоль/л (норма 0-5 ммоль/л), погранично-высокий уровень триглицеридов 1.8 ммоль/л (норма 0.5-1.7 ммоль/л), повышение концентрации мочевины крови до 9.2 ммоль/л (норма 2.8-7.2 ммоль/л), что свидетельствует о дислипидемии и нарушении белкового обмена у пациента. Глюкоза сыворотки крови натощак составила 6,812 ммоль/л (норма 3,5-6,4 ммоль/л), HbA1C был незначительно повышен -6,3% (норма 0-6%).
В гликемическом профиле у пациента отклонений не выявлено.
Учитывая состояние углеводного обмена, который отличается от нормы, но не достигает значений, установленных при СД2, пациенту выставлен диагноз - нарушение толерантности к глюкозе.
Воспалительные маркеры ИЛ-6 и ФНО-α были в пределах нормальных значений.
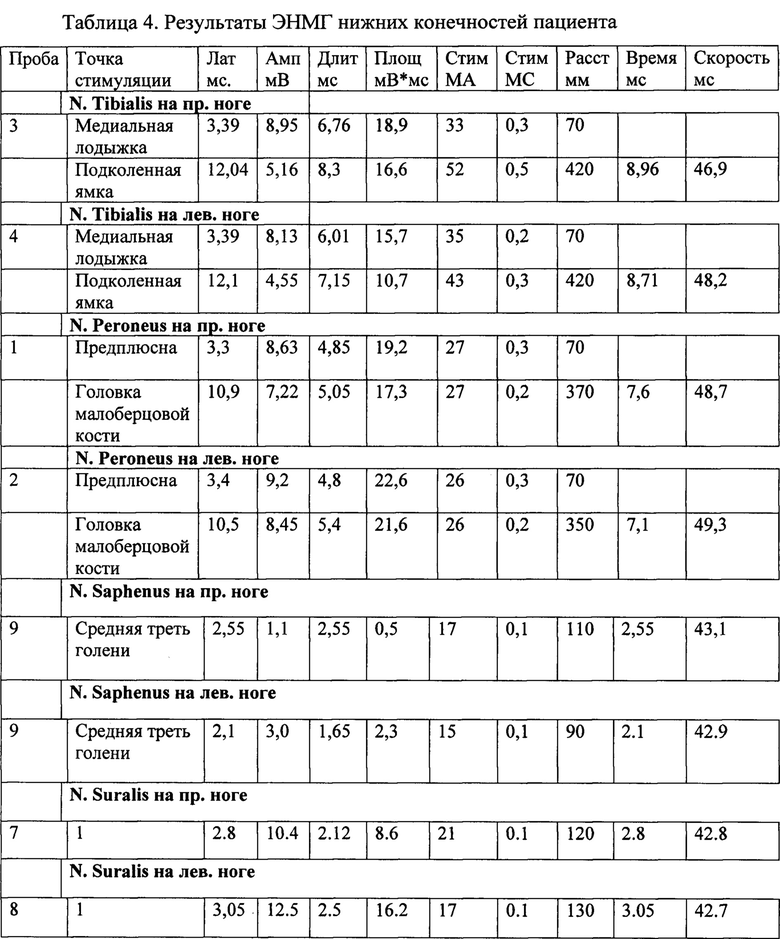
Номер пробы - порядок стимуляции нерва нейрофизиологом.
Заключение: у пациента имеются признаки незначительной дисфункции N. Tibialis в проксимальных отделах по типу аксонопатии, незначительного снижения скоростей проведения по сенсорным волокнам N. Suralis, N. Saphenus в дистальных отделах (сенсорная миелинопатия).
Таким образом, у пациента 62 лет с метаболическим синдромом, ожирением II степени и нарушением толерантности к глюкозе имеют место нарушения нервной проводимости по моторным и сенсорным волокнам периферических нервов нижних конечностей, выявленные методами стимуляционной электронейромиографии. При нарушенных показателях углеводного и липидного обменах на фоне дисметаболических процессов предполагаются нарушения капиллярного кровотока в нижних конечностях, что приводит к возникновению хронической ишемии в тканях, повреждению нервных волокон, возникновению нейропатического болевого синдрома более в дистальных отделах ног, по типу «носок», с явлениями парестезии, дизестезии, гиперестезии, локализованных на подошвенной поверхности стопы, более в пятке, подушечке стопы, пальцах, наружно-боковой части ступни.
Учитывая стойкий нейропатический болевой синдром, соответствующий 44 мм по ВАШ, сопровождающийся парестезиями на фоне приема антиконвульсантов (таб. Карбамазепин 200 мг 3 раза в день), с целью купирования болевого синдрома пациенту выполнена инъекция БТА по предлагаемому способу. Препарат использовали в стандартном разведении 2 мл физиологического раствора натрия хлорида 0,9% на 100 ЕД препарата «Релатокс».
Введение раствора «Релатокс» осуществляли подкожно по 2.5 ЕД препарата в точку инъекции (50 ЕД в каждую ступню, 100 ЕД в обе ступни) в следующие 20 точек каждой ступни, а именно:
- в центр дистальной фаланги большого пальца;
- в точки проекции на подошву головок (далее для краткости - точки под головками) первой и пятой плюсневых костей и в точку проекции на подошву пяточного бугра (далее - точку под пяточным бугром);
- в три равноудаленные друг от друга точки на отрезке под головками первой и пятой плюсневых костей (далее - отрезок А);
- в семь равноудаленных друг от друга точек на отрезке между точкой под головкой пятой плюсневой кости и точкой под пяточным бугром (далее - отрезок Б);
- в четыре точки, полученные от деления на 4 равные части отрезка С, параллельного и равного отрезку А, проведенного от него на расстоянии, равном 1/8 отрезка Б, отмеренном в сторону пятки;
- в две точки на отрезке Д, параллельном отрезку А, проведенном на расстоянии 1/8 отрезка Б, отмеренном в сторону пальцев от точки под пяточным бугром. Указанные две точки отстоят вправо и влево от точки пересечения отрезков Б и Д на расстоянии, равном 1/4 отрезка А.
Произведена оценка динамики болевого синдрома по ВАШ у пациента через 1, 3, 12 недель после введения БТА. Результаты представлены в таблице 5.

Интенсивность боли по ВАШ снизилась на 29,55% от исходного показателя спустя неделю после постановки БТА, на 77,27% спустя 3 недели после введения БТА и оставалась сниженной через 12 недель после введения БТА.
Субъективно пациент отмечает значительное снижение болевых ощущений в стопах, исчезновение парестезий: покалываний, чувства зябкости и жжения, а также увеличение толерантности к физическим нагрузкам.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ мультимодальной ботулинотерапии постампутационных болевых синдромов в конечностях и связанных расстройств | 2023 |
|
RU2825061C1 |
| Способ лечения болей после ампутации конечности | 2023 |
|
RU2823155C1 |
| Способ лечения пациентов с диабетической нейропатией | 2017 |
|
RU2690745C1 |
| СПОСОБ ЛЕЧЕНИЯ ДИАБЕТИЧЕСКИХ АНГИОПАТИЙ НИЖНИХ КОНЕЧНОСТЕЙ | 2017 |
|
RU2644292C1 |
| СПОСОБ ЛЕЧЕНИЯ WEB-СИНДРОМА ПОСЛЕ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВ В ПОДМЫШЕЧНОЙ ОБЛАСТИ | 2019 |
|
RU2715564C2 |
| Способ реабилитации пациентов с послеоперационными рубцами и болевым синдромом в нижней части спины | 2023 |
|
RU2806478C2 |
| Способ реабилитации при периферической полинейропатии, индуцированной цитостатиками | 2022 |
|
RU2775121C1 |
| СПОСОБ ЛЕЧЕНИЯ ДИАБЕТИЧЕСКОЙ ПОЛИНЕЙРОПАТИИ | 2004 |
|
RU2262928C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОССТАНОВЛЕНИЯ ПОВЕРХНОСТНОЙ ЧУВСТВИТЕЛЬНОСТИ ПРИ ЛЕЧЕНИИ ДИАБЕТИЧЕСКОЙ ДИСТАЛЬНОЙ ПОЛИНЕВРОПАТИИ НИЖНИХ КОНЕЧНОСТЕЙ С БОЛЕВЫМ СИНДРОМОМ | 2015 |
|
RU2593227C1 |
| Способ лечения компрессионно-ишемической нейропатии поднадколенниковой ветви подкожного нерва бедра у пациентов с болевым синдромом медиальных отделов коленного сустава с гонартрозом с ультразвук-ассистированной гидродиссекцией | 2023 |
|
RU2818258C1 |
Изобретение относится к медицине, в частности к неврологии, и может быть использовано для лечения болевой формы периферической диабетической полинейропатии нижних конечностей. Осуществляют введение ботулинического токсина типа А - гемагглютинин комплекс подкожно в подошву стоп в двадцать определённых точек. Способ позволяет обезболить наиболее нагруженные опорные области стопы и улучшить качество жизни за счет введения ботулинического токсина в двадцать точек в проекции большеберцового, медиального и латерального подошвенных нервов. 4 ил., 5 табл., 1 пр.
Способ лечения болевой формы периферической диабетической полинейропатии нижних конечностей, характеризующийся тем, что осуществляют введение ботулинического токсина типа А - гемагглютинин комплекс подкожно в подошву стоп, при этом точку введения 1 располагают в центре дистальной фаланги большого пальца, точку введения 2 располагают под головкой первой плюсневой кости, точку введения 6 располагают под головкой пятой плюсневой кости, точку введения 20 располагают под пяточным бугром; точки 3, 4, 5 располагают на равном расстоянии на отрезке между точками 2 и 6; точки 11, 12, 13, 14, 15, 16, 18 располагают на равном расстоянии на отрезке между точками 6 и 20; точки 7, 8, 9, 10 располагают равноудаленно друг от друга на отрезке, параллельном и равном отрезку 2-6, проведенном от него на расстоянии, равном отрезку 6-11; точку 17 располагают на линии, параллельной отрезку 7-11, проведенной через точку 18, медиальнее от точки 18, на расстоянии, равном отрезку 5-6; точку 19 располагают на линии, параллельной отрезку 7-11, проведенной через точку 18, латеральнее от точки 18, на расстоянии, равном отрезку 5-6.
| MEHRDAD T | |||
| et al | |||
| The Effect of Intradermal Botulinum Toxin a injections on painful diabetic polyneuropathy | |||
| Diabetes & Metabolic Syndrome: Clinical Research & Reviews, v | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Электрический поворотный выключатель | 1918 |
|
SU1823A1 |
| Переносный ручной станок для расточки вагонных буксовых подшипников | 1919 |
|
SU1825A1 |
| СПОСОБ ЛЕЧЕНИЯ ДИФТЕРИЙНЫХ ПОЛИНЕЙРОПАТИЙ У ДЕТЕЙ | 1996 |
|
RU2154479C2 |
| Девликамова Ф.И | |||
| Радикулопатия у пациента с диабетической полинейропатией: сложности | |||
Авторы
Даты
2025-05-16—Публикация
2024-04-25—Подача