Предлагаемое изобретение относится к медицине и позволяет оценивать выраженность метаболических нарушений в желчи, на основании которых можно прогнозировать риск литогенеза в желчевыводящих путях и, в том числе, осуществлять выбор эндобилиарных стентов с соответствующими физико-химическими характеристиками, что ведет к снижению частоты инкрустации и обструкции билиарных эндопротезов и увеличивает сроки функционирования стентов у пациентов с механической желтухой различной этиологии с риском развития холелитиаза.
Проблема механической желтухи остается одной из самых актуальных в современной хирургической гастроэнтерологии [Григорьева И.Н., Никитин Ю.П. Распространенность желчнокаменной болезни в разных регионах // Клин. медицина. - 2007. - Т. 85, №9. - С. 27-29]. Число больных, поступающих в хирургические стационары с заболеваниями органов билиопанкреатодуоденальной зоны, осложненные обструкцией желчевыводящих путей и механической желтухой, на протяжении многих лет не снижается [Стойко Ю.М., Левчук А.Л., Бардаков В.Г., Ветшев П.С. Возможности современных методов диагностики и обоснование лечебной тактики при механической желтухе // Вестник хирургической гастроэнтерологии. - 2008. - №2. - С. 24-32]. Механический фактор закупорки желчных протоков чаще всего имеет место при осложненной желчнокаменной болезни, опухолях билиопанкреатодуоденальной зоны и различных формах панкреатита. Значительно реже этиологическими факторами выступают ятрогенные повреждения магистральных структур протоковой системы, развивающиеся в результате операционной травмы, врожденные аномалии развития желчных протоков, паразитарные болезни печени и желчных протоков, а также «низкие» язвы ДПК [Пауткин Ю.Ф., Климов А.Е. Механическая непроходимость желчных путей (механическая желтуха). - М.: Профиль. 2 С., 2010. - 224 с.].
Продолжают изучать основные причины возникновения механической желтухи: распространенность желчнокаменной болезни на основе прогностических исследований заболеваний гепатобилиарной системы [Хохлачева Н.А., Горбунов А.Ю., Вахрушев Я.М. Изучение распространенности желчнокаменной болезни на основе прогностических исследований заболеваний гепатобилиарной системы // Терапевт, арх. - 2012. - №2. - С. 45-49; Paumgartner G. Medical treatment of cholestatic liver diseases: From pathobiology to pharmacological targets // Gastroenterol. - 2006. - №12 (28). - P. 4445-4451], анализа онкологической заболеваемости и летальности органов билиопанкреатодуоденальной зоны в структуре онкопатологии [Казанцева М.В., Тесленко Л.Г., Цокур И.В., Бондарева И.С. Злокачественные новообразования в Краснодарском крае (2009-2013 годы). Состояние онкологической помощи населению. - Краснодар: Изд-во «Флер», 2014. - 280 с.].
При этом отмечается устойчивая тенденция к росту процента больных пожилого и старческого возраста, поступающих в хирургические стационары с клиникой механической желтухи, возникающей на фоне протоковой обструкции, число которых составляет по разным данным 49-68% от всех пациентов с данной патологией [Быстров С.А., Жуков Б.Н., Бизярин В.О. Миниинвазивные операции в лечении желчнокаменной болезни у пациентов с повышенным операционным риском // Хирургия. Журнал им. Н.И. Пирогова. - 2010. - №7. - С. 55-59]. Общее состояние этих больных усугубляется имеющейся общесоматической патологией, что в значительной степени влияет на результаты лечения, увеличивая количество неблагоприятных исходов в несколько раз [Pring С.М., Kelding-Millar L.S. Expectant treatment or cholecustectomy after endoscopic retrograde cholangiopancreatography for choledocholithiasis in patients over 80 years old // Surg. Endoscop. - 2005. - Vol. 19 (3). - P. 337-360].
Современные принципы лечения пациентов с механической желтухой предполагает применение одного из варианта малоинвазивной декомпрессии желчных протоков, в том числе включая применение эндобилиарных стентов [Гусев А.В., Балагуров Б.А., Боровков И.Н., Коньков О.И., Мартинш Ч.Т., Покровский Е.Ж., Раскин А.В., Станкевич A.M. Дренирование и эндопротезирование желчных протоков при механической желтухе // Вестник новых медицинских технологий. - 2008. - Т. 15, №4. - С. 97-98.]. При длительном функционировании стента происходит его постепенная обтурация, что приводит к рецидиву механической желтухи, развитию холангита и вынуждает вновь госпитализировать больных для замены билиарного эндопротеза [Дюжева Т.Г., Савицкая Е.Е., Котовский А.Е., Батин М.А. Биодеградируемые материалы и методы тканевой инженерии в хирургии желчных протоков // Анналы хир. гепатол. - 2012. - №1. - С. 94-99, Котовский А.Е., Глебов К.Г. Эндоскопическое транспапиллярное стентирование желчных протоков // Анналы хир. гепатол. - 2008. - №1. - С. 66-71]. Подобная ситуация характерна для внутренних билиарных стентов независимо от способа их установки. В научной литературе широко обсуждается вопрос по увеличению эффективности желчеоттока через различающиеся по материалам изготовления, физико-химическим характеристикам, диаметрам и конфигурациям стенты [Куликовский В.Ф., Солошенко А.В., Ярош А.Л., Колпаков А.Я., Карпачев А.А., Балакирева О.В., Битенская Е.П., Власюк Ю.Ю. Билиарный стент с алмазоподобным углеродным покрытием // Эндоскопическая хирургия. - 2013. - №3. - С. 16-20]. Реакция организма на имплантат определяется его реактивностью и поверхностными свойствами последнего: структурой, морфологией и химическим составом [Хенч Д., Джонс Д. Биоматериалы, искусственные органы и инжиниринг тканей (под ред. А.А. Лушниковой). Серия «Мир биологии и медицины». - М.: Техносфера, 2007. - 304 с.], в связи с чем представляет интерес разработка биохимического алгоритма для выбора медицинских изделий с измененными физико-химическими параметрами в зависимости от функционального состояния организма на местном уровне, например при изменениях метаболических показателей желчи у больных с механической желтухой. Следует указать, что средний срок функционирования билиарного стента уменьшается при повторном протезировании [Шевченко, Ю.Л., Ветшев, П.С., Стойко, Ю.М. и др. Приоритетные направления в лечении больных с механической желтухой // Анналы хирургической гепатологии. - 2011. - №3. - С. 9-15], что обусловливает необходимость разработки способов лабораторного анализа для определения наиболее оптимальных по перечисленным выше характеристикам эндобилиарных стентов у пациентов с впервые выявленной механической желтухой.
Выпадение в осадок веществ желчи связано с дестабилизацией физико-химического состояния желчи. При этом в наиболее массовой разновидности желчных камней содержание холестерина превышает 50%. На долю таких желчных камней приходится до 90% от их общего количества [Михин И.В., Голуб В.А. Желчнокаменная болезнь. Острый холецистит. Учебное пособие. - Волгоград: Изд-во ВолгГМУ, 2011. - 86 с.], в связи с чем изучение именно показателей липидного обмена является ведущим при оценке риска возникновения холелитиаза.
Известно, что усиление окисления компонентов желчи является интегративным и одним из наиболее ранних местных факторов формирования желчных камней. При самоокислении желчи накапливаются продукты перекисной модификации липидов, что сопровождается агрегацией и агломерацией везикул желчи с последующей кристаллизацией или осаждением макромолекулярных компонентов желчи [Швецова М.М., Барботько А.А. и соавт. Перекисное окисление липидов желчи больных калькулезным и бескаменным холециститом // Терапевтический архив. - 1998 - №5. - С. 33-35; Седов А.П., Парфенов И.П. и соавт. Оценка изменений слизистой оболочки желчных протоков и состава желчи при остром холангите // Анналы хирургической гепатологии. - 2009. - №2. - С. 22-28]. Поэтому химический состав камня определяется, прежде всего, взаимодействием компонентов желчи с продуктами перекисного окисления липидов. В связи с этим физико-химические характеристики желчи целесообразно учитывать при диагностике ранних стадий холелитиаза. Особенно актуально определение прооксидантно-антиоксидантного баланса желчи, позволяющего оценивать как риск развития самоокисления желчи при снижении ее антиокислительной активности, так и вероятность перекисной модификации липидных компонентов, например при усиленной генерации свободных радикалов в условиях развивающегося свободнорадикального патологического процесса (воспаление, опухоль, диспепсия и другие [Cruz A., Padillo F.J., Tunez I. Melatonin protects against renal oxidative stress after obstructive jaundice in rats // Eur. J. Pharmacol. - 2001. - №425 (2). - P. 135-139; Терехина H.A., Заривчатский М.Ф., Владимиров A.A., Хлебников В.В. Показатели антиоксидантной защиты при остром и хроническом холецистите // Клин. лаб. диагностика. - 2008. - №4. - С. 33-41]).
Известен способ определения степени литогенности пузырной желчи [Andrews Е., Schoenheimer R., Hrdina Е. Etiology of gallstones, chemical factors and the role of the gallbladder // Arch. Surg. - 1932. - Vol. 25. - P. 796-805], основанный на расчете холатохолестеринового коэффициента по формуле:
ХХК=ЖК/ХС,
где ХХК - холатохолестериновый коэффициент;
ЖК - суммарная концентрация желчных кислот, ммоль/л;
ХС - концентрация холестерина желчи, ммоль/л.
Считается, что концентрации холестерина и желчных кислот являются определяющими для коллоидной устойчивости желчи. При дисбалансе их соотношения, а именно, снижении концентрации ЖК, повышении ХС, т.е. при снижении ХХК, желчь становится пересыщенной, литогенной, ХС постепенно выпадает в осадок. По данным разных авторов желчь становится литогенной при снижении ХХК до 10 и ниже [Маркидонова А.А., Белобородова Э.И., Бурковская В.А. Состояние желчевыводящей системы и литогенность желчи у больных воспалительными заболеваниями кишечника // Бюллетень сибирской медицины. - 2013. - Т. 12. - №6. - С. 112-119].
Указанный способ имеет следующие недостатки:
а) не учитывают, кроме желчных кислот и холестерина, содержание других липидов (лецитина, фосфатидилэтаноламина, лизолецитина, фосфатидилсерина, составляющих до 22% липидов желчи [Berry W., Reichen J. Bile acid metabolism: its relation to clinical disease // Seminars Liver Dis. - 1983. - Vol. 3. - P. 330-340; Romański K. The role and mechanism of action of bile acids in the digestive system - bile acids in the gut // Adv. Clin. Exp. Med. - 2008. - Vol. 17. - P. 83-89]), обладающих способностью стабилизировать холестерин в составе желчи [Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека: в 2 т. Т. 2. Пер. с англ.: - М.: Мир, 1993. - С. 288-289], что важно при оценке литогенности желчи на начальных этапах желчнокаменной болезни, в том числе при установке эндобилиарных протезов;
б) одной из составляющих этого индекса литогенности является показатель желчных кислот, определение которых достаточно трудоемкое [Рубенс Ю.И., Юрика Э.В., Селезнев Ю.В. Индексы литогенности желчи: методы определения, клиническая доступность, информативность // Клин. медицина. - 1992. - Т. 70, №7-8. - С. 39-41], что снижает пропускную способность данного способа в клинической практике;
в) при расчете этого индекса литогенности не принимают во внимание участие инициирующих факторов камнеобразования, например, при воспалительных процессах в желчевыводящих протоках, приводящих к развитию самоокисления желчи и снижению ее антиоксидантного потенциала на фоне интенсификации процессов свободнорадикального окисления [Виноградова И.С., Мандров С.И., Жданова Л.А., Акайзина А.Э., Акайзин Э.С., Миленина И.В., Томилова И.К. Перекисное окисление липидов и антиоксидантная активность у детей с начальной стадией желчнокаменной болезни // Медицина и образование Сибири. - 2013. - №6.], что играет существенную роль в патогенезе начальных этапов желчнокаменной болезни и может вести к получению ложноотрицательных результатов при диагностике.
Способ неэффективен из-за указанных недостатков, поэтому остается актуальной задачей разработка новых способов определения литогенности желчи, сочетающих все вышеизложенные факторы и обладающих высокой воспроизводимостью полученных.
За ближайший аналог принят способ определения литогенности желчи [Thomas P.J., Hofmann A.F. Letter: a simple calculation of the lithogenic index og bile: expressing biliary lipid composition on rectangular coordinates // Gastroenterology. - 1973. - Vol. 65, №4. - P. 698-700], основанный на расчете индекса литогенности Томаса-Хофмана (Tomas-Hofmann). Этот индекс учитывает все главные билиарные липиды: фосфолипиды, желчные кислоты, холестерин и учитывает молярную долю последнего в рассматриваемой системе липидов желчи. Таким образом, он отражает отношение фактического насыщения желчи холестерином к максимально возможному, то есть рассчитывается по значению максимальной молярной доли холестерина на границе его максимальной растворимости, который может быть растворен в исследуемом образце. Для нахождения значения максимального молярного процента холестерина на границе его максимальной растворимости используют формулы [Рубенс Ю.И., Юрика Э.В., Селезнев Ю.В. Индексы литогенности желчи: методы определения, клиническая доступность, информативность // Клин. медицина. - 1992. - Т. 70, №7-8. - С.39-41]:
y1=4,87+39,45х-86,9х2+53,7х3 (для x≤0,320)
y2=117,4+755,0х+1,756х2-1,377х3 (для x>0,320), где
y - теоретический максимальный молярный процент холестерина, который может быть растворен в данном образце;
x - соотношение, в знаменателе которого находится показатель лецитина данного образца (в ммоль/л), в числителе - сумма показателей лецитина и суммы желчных кислот данного образца (в ммоль/л).
Индекс литогенности Томаса-Хофмана определяют как соотношение молярного процента холестерина исследуемого образца и теоретически найденного максимального молярного процента холестерина (y1 или y2) для этого образца. Если значение индекса литогенности Томаса-Хофмана более 1, то желчь литогенна, если менее 1 - не литогенна.
Указанный способ имеет следующие недостатки:
а) представленный индекс литогенности сложен в расчетах и не отличается, по мнению ряда специалистов, особой информативностью [Рубенс Ю.И., Юрика Э.В., Селезнев Ю.В. Индексы литогенности желчи: методы определения, клиническая доступность, информативность // Клин, медицина. - 1992. - Т. 70, №7-8. - С.39-41], что может сопровождаться получением ложноотрицательных результатов у больных на начальных стадиях заболевания;
б) при расчете этого индекса литогенности не учитывает нарушение прооксидантно-антиоксидантного баланса желчи, так как известно, что перекисное окисление желчи способствует накоплению продуктов перекисной модификации в пузырной желчи, например при остром или хроническом воспалении, и является интегративным и наиболее ранним местным фактором формирования желчных камней [Мараховский Ю.X. Желчнокаменная болезнь: современное состояние проблемы // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. - 2003. - №1. - С.81-91; Седов А.П., Парфенов И.П., Ярош А.Л., Сергеев О.С., Солошенко А.В., Карпачев А.А., Судаков М.В., Балакирева О.В. Оценка изменений слизистой оболочки желчных протоков и состава желчи при остром холангите // Анналы хирургической гепатологии. - 2009. - Т. 14, №2. - С. 22-27], что необходимо учитывать при диагностике желчнокаменной болезни на ранних стадиях заболевания;
в) индекс литогенности не учитывает избыточный супрамицеллярный холестерин, который может содержаться в желчи в физиологических условиях в составе холестерин/лецитиновых-везикул [Рубенс Ю.И., Юрика Э.В., Селезнев Ю.В. Индексы литогенности желчи: методы определения, клиническая доступность, информативность // Клин, медицина. - 1992. - Т. 70, №7-8. - С. 39-41], что может приводить к получению ложноположительных результатов при использовании этого индекса для оценки литогенности желчи у здоровых лиц.
Способ отличается низкой диагностической эффективностью из-за указанных недостатков, так как недостоверен.
Задача - повышение эффективности диагностических мероприятий, выявляющих дисхолию и позволяющих определять риск литогенеза в желчевыводящих путях, путем комплексной оценки метаболических нарушений на местном уровне по показателям липидного обмена и прооксидантно-антиоксидантного баланса в желчи, что позволит, в том числе, осуществлять оптимальный выбор билиарных эндопротезов и своевременно осуществлять полноценную и при необходимости длительную коррекцию холестаза.
Сущностью изобретения является способ биохимической оценки метаболических нарушений в желчи при литогенезе, включающий определение в желчи у обследуемого (i) показателей холестерина (ХС, ммоль/л) в сравнении со средними значениями, принятыми за норму (k), отличающийся тем, что в желчи определяют комплекс общих липидов (ОЛ, г/л) и показателей прооксидантно-антиоксидантного баланса: суммарную антиокислительную активность (АОА) электрохимическим методом (в нА·с), максимум вспышки хемилюминесценции (МВХЛ, в усл. ед.) и площадь хемилюминесценции (ПХЛ, в усл. ед. площади), дополнительно соотносят значения АОА с показателями стандартного аскорбинового эквивалента (AOAvitC), значения МВХЛ - с показателями максимума вспышки стандартного раствора люминола (МВХЛL), значения ПХЛ - с показателями площади стандартного раствора люминола (ПХЛL), далее вычисляют интегральный показатель литогенности желчи (ИПЛi) по формуле:
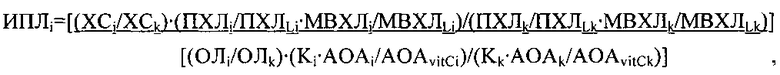
где Ki и Kk - коэффициент разведения - кратность разведения пробы желчи обследуемого и пробы желчи принятой за норму соответственно при определении АОА, и чем выше значение ИПЛi, тем более высокая степень литогенности желчи с риском развития холелитиаза.
Техническим результатом изобретения является:
1) возможность с помощью комплексной оценки интегрально определять показатель литогенности желчи, что важно для прогнозирования риска камнеобразования в желчевыводящих путях, в том числе на ранних этапах развития желчнокаменной болезни и при билиарном эндопротезировании;
2) составляющими индекса литогенности являются значения суммарной антиокислительной активности и интенсивности хемилюминесценции желчи, так как при формировании холелитиаза, прежде всего при воспалительных заболеваниях, определенную значимость имеют активация свободнорадикального окисления и снижение антиоксидантных факторов в желчи, что важно учитывать при лечении таких больных;
3) способ включает определение соотношения холестерина и общих липидов, что увеличивает его чувствительность при диагностике и позволяет выявлять патологические изменения в желчи, сопровождающиеся нарушением ее литогенности на ранних стадиях заболевания или при дисхолии, наблюдающейся при установке эндобилиарных протезов;
4) используемые для определения интегрального показателя литогенности желчи методики являются доступными, информативными, легко воспроизводимыми и не требуют дорогостоящего оборудования и специальной подготовки персонала.
Способ осуществляют следующим образом.
Определение содержания холестерина желчи проводят с помощью набора реактивов «Холестерин-22-Витал» (Витал Диагностике СПб, см. приложение 1). Для этого смешивают 2,0 мл рабочего реагента (содержащего холестеролэстеразу 400 U/л, холестеролоксидазу 250 U/л, пероксидазу 500 U/л и хромогены в фосфатном буферном растворе 100 ммоль/л с 20 ммоль/л фенолом) с 20 мкл супернатанта предварительно центрифугированной желчи в течение 30 минут при 3000 об/мин (опытная проба), 20 мкл стандартного раствора холестерина 5,17 ммоль/л (стандарт) и 20 мкл дистиллированной воды (контрольная проба). Реакционную смесь перемешивают и инкубируют 10 минут при температуре 20-25°C, затем измеряют оптическую плотность опытной пробы и стандарта против контрольного раствора на спектрофотометре в кюветах с длиной оптического пути 10 мм при длине волны 500 нм. Расчет концентрации холестерина проводят по формуле (см. приложение 2):
ХС=(ЕОП/Ек)·5,17, где
ХС - концентрация холестерина желчи, ммоль/л,
ЕОП - оптическая плотность опытной пробы, в единицах оптической плотности;
Ек - оптическая плотность калибровочной пробы (стандарта), в единицах оптической плотности;
5,17 - концентрация холестерина в калибраторе, в ммоль/л.
Определение общих липидов желчи проводят с помощью набора реактивов «Общие липиды» (PLIVA-Lachema Diagnostika s.r.o.). Для этого в трех пробирках смешивают 1,5 мл концентрированной серной кислоты с 20 мкл супернатанта предварительно центрифугированной (30 минут при 3000 об/мин) желчи (опытная проба), 20 мкл стандартного раствора общих липидов 8 г/л (стандарт) и 20 мкл дистиллированной воды (контрольная проба). Полученные растворы перемешивают и нагревают 15 минут на кипящей водяной бане. После охлаждения проточной водой смешивают 100 мкл полученного гидролизата с 1,5 мл 10 ммоль/л раствором ванилина в 11,5 ммоль/л ортофосфорной кислоте. Реакционную смесь инкубируют 50 минут при температуре 15-25°C. Не позднее 60 минут инкубации измеряют оптическую плотность опытной пробы и стандарта против контроля на спектрофотометре, в кювете с длиной оптического пути 10 мм, при длине волны 540 нм. Расчет концентрации общих липидов проводят по формуле (см. приложение 3):
ОЛ=8·(А1/А2), где
ОЛ - концентрация общих липидов, г/л;
A1 - оптическая плотность опытной пробы, в единицах оптической плотности;
А2 - оптическая плотность стандарта, в единицах оптической плотности;
8 - стандартный коэффициент, в г/л.
Для определения антиокислительной активности исследуемую желчь растворяют в специальном элюенте (2,2 мМ раствор ортофосфорной кислоты) в соотношении 1:100. Кратность разведения для каждой пробы желчи в последующем учтена при определении интегрального показателя литогенности. Суммарную антиокислительную активность определяют по методу [Пахомов В.П., Яшин Я.И., Яшин А.Я., Багирова В.Л., Арзамасцев А.П., Кукес В.Г., Ших Е.В. Способ определения суммарной антиоксидантной активности биологически активных веществ. Патент на изобретение №2238554] в модификации [Басов А.А., Федосов С.Р., Канус И.С., Еремина Т.В., Пшидаток Д.В., Малышко В.В. Современные способы стандартизации антиоксидантных лекарственных средств и биологически активных добавок // Современные проблемы науки и образования. - 2006. - №4, прил. 1. - С. 149] и выражают в мг/л по отношению к антиокислительной активности аскорбиновой кислоты. Окисление анализируемого и стандартного вещества проводят электрохимически путем непосредственной поочередной подачи подготовленных проб в термостатируемую электрохимическую ячейку амперометрического детектора с получением сигналов в виде соответствующих импульсов электрического тока, усиление сигналов, регистрацию в виде дифференциальных выходных кривых и расчет площадей полученных пиков анализируемого (S) и стандартного (Sст) веществ. Полученные результаты выражают в виде положительных значений в нА·с. Антиокислительную активность образцов определяют по суммарному содержанию в них природных флавоноидов: катехинов (вещества группы флавана); кверцетина, рутина, дигидрокверцетина (вещества группы флавона); а также витаминов группы А, Е, С и других соединений, способных связывать свободные радикалы. В качестве стандарта используют раствор аскорбиновой кислоты в концентрациях 0,5-8,0 мг/л.
Люминол-зависимую H2O2-индуцированную хемилюминесценцию желчи измеряют на хемилюминотестере ЛТ-1 производства НПО «Люмин» (Ростов-на-Дону) по авторской методике [Павлюченко И.И., Басов А.А., Федосов С.Р. Система лабораторной диагностики окислительного стресса. Патент на полезную модель №54787. - Заявл. 19.01.2006; опубл. 27.07.2006 - Бюл. №21. - 2 с.]. В кювету вносят 2,7 мл 50 мкМ стандартного раствора люминола в 0,1 М трис-HCl буфере (рН=6,8). Затем добавляют 300 мкл исследуемой желчи в кювету. Термостатируют кювету с реакционной системой 500 секунд в сухом термостате (t=37°C). После этого кювету помещают в люминотестер ЛТ-1 и реакцию радикального окисления люминола запускают впрыскиванием с помощью шприца-дозатора через инжектор 0,5 мл 3% H2O2. Интенсивность вспышки хемилюминесценции регистрируют в условных единицах (усл. ед.) хемилюминесценции в виде двух параметров: максимума вспышки хемилюминесценции и площади хемилюминесценции. Изучение динамики процесса хемилюминесценции [Федосов С.Р., Павлюченко И.И., Басов А.А. Способ повышения информативности прибора «Хемилюминотестер LT-1» // Современные проблемы науки и образования. - 2006. - №4, прил. 1. - С. 27-28] производят с помощью собственного аппаратно-программного комплекса с программным обеспечением [Павлюченко И.И., Федосов С.Р., Басов А.А. Программа регистрации сигналов хемилюминотестера ЛТ-1. Свидетельство об официальной регистрации программы для ЭВМ №2006611562. - Заявл. №2006610783; зарег. 10.05.2006.], позволяющим оцифровывать аналоговый сигнал с выхода хемилюминотестера ЛТ-1. Определяют следующие показатели хемилюминесценции: максимум вспышки хемилюминесценции в сравнении с эталоном (рабочий раствор люминола) и площади хемилюминесценции за 25 секунд в сравнении с эталоном (рабочий раствор люминола). В обоих случаях эталоном служит реакционная смесь без исследуемого субстрата. Интенсивность реакций свободнорадикального окисления, определяемая с помощью люминол-зависимой хемилюминесценции по максимуму и площади хемилюминесценции, позволяет определить способность антиоксидантных компонентов желчи перехватывать свободные радикалы, при этом можно оценить как прямой кратковременного антирадикальный эффект желчи - по максимуму вспышки хемилюминесценции, так и ее пролонгированный антирадикальный эффект - по площади хемилюминесценции.
Обоснование полученных результатов
Определение литогенности желчи остается актуальной задачей в хирургической и терапевтической гастроэнтерологии. В ряде исследований показано, что процесс формирования желчных камней проходит три стадии: насыщение, кристаллизация и рост [Иванченкова Р.А. Хронические заболевания желчевыводящих путей. - М.: Атмосфера, 2006. - 415 с.], среди которых наиболее важной является стадия перенасыщения желчи холестерином, наступающая тогда, когда весь холестерин не может быть солюбилизирован везикулами [Вахрушев Я.М., Хохлачева Н.А. Возможности использования кристаллооптических свойств желчи в ранней диагностике желчнокаменной болезни // Экспериментальная и клиническая гастроэнтерология. - 2011. - №4. - С. 26-30], в связи с чем определение соотношения холестерина и общих липидов желчи является одним из важных диагностических критериев при оценки литогенности желчи.
При этом уже на этапах формирования билиарного сладжа в форме взвеси гиперэхогенных частиц и эхонеоднородной желчи со сгустками происходит нарушение сбалансированности в системе свободнорадикального окисления, проявляющееся в повышении антиоксидантной активности, как компенсаторной реакции на развивающийся окислительный стресс. В дальнейшем при формировании замазкообразной желчи накапливаются продукты липопероксидации, и снижается антиоксидантная активность желчи, что ведет к агрегации и агломерации везикул желчи с продуктами липопероксидации и последующей кристаллизации и осаждению макромолекулярных компонентов желчи [Виноградова И.С., Мандров С.И., Жданова Л.А., Акайзина А.Э., Акайзин Э.С., Миленина И.В., Томилова И.К. Перекисное окисление липидов и антиоксидантная активность у детей с начальной стадией желчнокаменной болезни // Медицина и образование Сибири. - 2013. - №6], в связи с чем оценка прооксидантно-антиоксидантного баланса желчи также является одним из основных критериев ее литогенности.
Особенность предлагаемого способа заключается в совместном определении, как соотношения холестерина и общих липидов желчи, что позволяет своевременно выявлять стадию перенасыщения желчи холестерином - его способность участвовать в холелитиазе, так и оценке прооксидантно-антиоксидантного баланса желчи, то есть ее способности к самоокислению и устойчивости к внешним воздействиям, связанным с интенсификацией процессов свободнорадикального окисления, что позволяет с помощью полученных результатов изучать литогенность желчи и оценивать риск камнеобразования в желчевыводящих путях, в том числе и при эндобилиарном протезировании. Таким образом, способ позволяет выявлять метаболические нарушения в желчи, связанные с процессами дисхолии, интенсификацией свободнорадикального окисления и снижением антиоксидантной активности, что особенно актуально для диагностики холелитиаза на ранних стадиях и оценки риска камнеобразования при эндобилиарном стентировании.
В исследованиях, проведенных при поддержке государственного задания Министерства здравоохранения Российской Федерации (от 28.01.2015 г. ч. 1, раздел 1) «Осуществление прикладных научных исследований, в том числе проведение доклинических исследований лекарственных средств и клинических исследований лекарственных препаратов», установлено, что в группе обследуемых (n=18), не имеющих данных за холедохолитиаз, доброкачественные и злокачественные новообразования органов билиопанкреатодуоденальной зоны, интегральный показатель литогенности желчи составил 1,1±0,2 единиц литогенности (ХСk=3,0±0,2 ммоль/л; ОЛk=8,1±0,8 г/л; АОАk=741,6±78,4 нА·с, AOAvitCk=1198,4 нА·с; МВХЛk=1,9±0,3 условных единиц (усл. ед.), МВХЛLk=1,4 усл. ед.; ПХЛk=171,8±21,7 условных единиц площади (усл. ед. пл.), ПХЛLk=72,7 усл. ед. пл.; Kk=100,0).
При этом у пациентов (n=21) с холедохолитиазом без клинических и лабораторных проявлений холангита интегральный показатель литогенности желчи был повышен в 1,4 раза; у пациентов (n=13) с холедохолитиазом, осложненным острым холангитом, интегральный показатель литогенности желчи был повышен в 12,6 раза; у пациентов (n=10) со злокачественными новообразованиями органов билиопанкреатодуоденальной зоны, осложненными острым холангитом, интегральный показатель литогенности желчи был повышен в 65,1 раза.
Пример №1.
В хирургическое отделение №1 ГБУЗ «Научно-исследовательский институт - Краевая клиническая больница №1 имени профессора С.В. Очаповского» МЗКК (г. Краснодар) 12 января 2015 года поступила пациентка К., возраст 88 лет. Диагноз: «ЖКБ. Хронический калькулезный холецистит. Холедохолитиаз. Механическая желтуха». Длительность заболевания желчнокаменной болезнью составляла 25 лет, длительность механической желтухи составила 3 суток. В качестве первого этапа лечения 13.01.15 выполнена эндоскопическая ретроградная холангиография, эндоскопическая папиллосфинктеротомия, частичная механическая литоэкстракция, назобилиарное дренирование по поводу множественных крупных конкрементов общего желчного протока. В общехирургическом лечении больной было отказано по сопутствующей патологии. Проведено обследование с целью оценки выраженности метаболических нарушений желчи и определения риска литогенеза после проведения назобилиарного дренирования, в связи с чем определяли интегральный показатель литогенности желчи.
Для определения интегрального показателя литогенности использовали желчь, забор которой осуществляли при выполнении эндоскопического вмешательства с использованием эндоскопических стерильных катетеров. Затем желчь в объеме 50 мкл добавляли в 5 мл элюента (разведение 1:100, Ki=100,0), после чего проводили измерение суммарной антиокислительной активности исследуемого образца (AOAi, в нА·с) электрохимическим путем на амперометрическом детекторе (AOAi=786,2 нА·с). Далее определяли антиокислительную активность стандартного раствора аскорбиновой кислоты (AOAvitCi) в концентрации 1 мг/л, которая равнялась 1183,5 нА·с.
Кроме того, желчь в объеме 300 мкл вносили в тест-систему с 2,7 мл раствором люминола. Запускали реакцию радикального окисления люминола внесением через инжектор 0,5 мл 3% H2O2 и измеряли на люминотестере с помощью специального программного обеспечения максимум вспышки (МВХЛi=2,1 усл. ед.) и площадь хемилюминесценции (ПХЛi=216,8 усл. ед. пл.). Одновременно измеряли максимум вспышки и площадь хемилюминесценции контрольного раствора люминола без исследуемого субстрата, которые оставили: МВХЛLi=1,4 усл. ед., ПХЛLi=73,9 усл. ед. пл.
Для определения общих липидов центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию общих липидов определяли с помощью набора реактивов «Общие липиды» (PLIVA-Lachema Diagnostika s.r.o.). Оптическая плотность опытной пробы составила 0,219 единиц оптической плотности, оптическая плотность стандарта составила 0,274 единиц оптической плотности, что соответствовало концентрации общих липидов (ОЛi) 6,4 г/л.
Для определения холестерина центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию холестерина определяли с помощью набора реактивов «Холестерин-22-Витал» (Витал Диагностике СПб). Оптическая плотность опытной пробы составила 0,157 единиц оптической плотности, оптическая плотность стандарта составила 0,253 единиц оптической плотности, что соответствовало концентрации холестерина (XCi) 3,2 ммоль/л.
Интегральный показатель литогенности желчи рассчитывали по формуле: 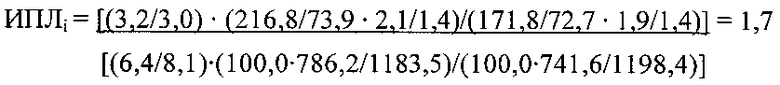
Проведенными исследованиями показано, что повышение интегрального показателя литогенности желчи, рассчитанного по описанной выше формуле, у пациентки с холедохолитиазом было незначительное (ИПЛi составил 1,7 единиц литогенности) в сравнении с данными контрольной группы, в связи с чем 15.01.15 проведено повторное эндоскопическое вмешательство в объеме установки билиарного полимерного стента конфигурации «double pigtail», диаметром 10 Fr, длиной 10 см. В дальнейшем в течение 4-х месяцев у этой пациентки по результатам общеклинических обследований не было зафиксировано данных за обтурацию стента, рецидива механической желтухи и холангита, а проведенное лечение оценили как эффективное и адекватное.
Пример №2.
В хирургическое отделение №2 ГБУЗ «Научно-исследовательский институт - Краевая клиническая больница №1 имени профессора СВ. Очаповского» МЗКК (г. Краснодар) 14 января 2015 года поступила пациентка А., возраст 78 лет. Диагноз: «ЖКБ. Хронический калькулезный холецистит. Холедохолитиаз. Механическая желтуха. Острый холангит» Длительность заболевания желчнокаменной болезнью составляла 12 лет, длительность механической желтухи составила 2 недели. В качестве первого этапа лечения 15.01.15 выполнена эндоскопическая ретроградная холангиография, эндоскопическая папиллосфинктеротомия, частичная механическая литоэкстракция, назобилиарное дренирование по поводу крупного (более 4,0 см), фиксированного конкремента общего желчного протока. В общехирургическом лечении больной было отказано по сопутствующей патологии и тяжести основного заболевания. Проведено обследование с целью оценки выраженности метаболических нарушений желчи и определения риска литогенеза после проведения эндобилиарного стентирования, в связи с чем определяли интегральный показатель литогенности желчи.
Для определения интегрального показателя литогенности использовали желчь, забор которой осуществляли при выполнении эндоскопического вмешательства с использованием эндоскопических стерильных катетеров. Затем желчь в объеме 50 мкл добавляли в 5 мл элюента (разведение 1:100, Ki=100,0), после чего проводили измерение суммарной антиокислительной активности исследуемого образца (AOAi, в нА·с) электрохимическим путем на амперометрическом детекторе (AOAi=249,5 нА·с). Далее определяли антиокислительную активность стандартного раствора аскорбиновой кислоты (AOAvitCi) в концентрации 1 мг/л, которая равнялась 1207,3 нА·с.
Кроме того, желчь в объеме 300 мкл вносили в тест-систему с 2,7 мл раствором люминола. Запускали реакцию радикального окисления люминола внесением через инжектор 0,5 мл 3% H2O2 и измеряли на люминотестере с помощью специального программного обеспечения максимум вспышки (МВХЛi=2,9 усл. ед.) и площадь хемилюминесценции (ПХЛi=257,1 усл. ед. пл.). Одновременно измеряли максимум вспышки и площадь хемилюминесценции контрольного раствора люминола без исследуемого субстрата, которые оставили: МВХЛLi=1,3 усл. ед., ПХЛLi=70,8 усл. ед. пл.
Для определения общих липидов центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию общих липидов определяли с помощью набора реактивов «Общие липиды» (PLIVA-Lachema Diagnostika s.r.o.). Оптическая плотность опытной пробы составила 0,096 единиц оптической плотности, оптическая плотность стандарта составила 0,265 единиц оптической плотности, что соответствовало концентрации общих липидов (ОЛi) 2,9 г/л.
Для определения холестерина центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию холестерина определяли с помощью набора реактивов «Холестерин-22-Витал» (Витал Диагностике СПб). Оптическая плотность опытной пробы составила 0,110 единиц оптической плотности, оптическая плотность стандарта составила 0,270 единиц оптической плотности, что соответствовало концентрации холестерина (XCi) 2,1 ммоль/л.
Интегральный показатель литогенности желчи рассчитывали по формуле: 
Проведенными исследованиями показано, что у пациента с холедохолитиазом, осложненным острым холангитом, было значительное повышение интегрального показателя литогенности желчи (рассчитанного по описанной выше формуле, ИПЛi составил 14,8 единицы литогенности) в сравнении с данными контрольной группы, в связи с чем 20.01.15 проведено повторное эндоскопическое вмешательство в объеме установки билиарного стента со специальными физико-химическими характеристиками покрытия, конфигурации «double pigtail», диаметром 10 Fr, длиной 7 см. В дальнейшем у этой пациентки по результатам общеклинических обследований не было зафиксировано данных за обтурацию стента, рецидива механической желтухи и холангита, больная была подготовлена к общехирургическому лечению, которое было успешно проведено через 3,5 месяца после установки эндопротеза, а проведенное лечение оценили как эффективное и адекватное.
Пример №3.
В хирургическое отделение №1 ГБУЗ «Научно-исследовательский институт - Краевая клиническая больница №1 имени профессора С.В. Очаповского» МЗКК (г. Краснодар) 22 января 2015 года поступила пациентка З., возраст 76 лет. Диагноз: «Рак головки поджелудочной железы. T3NxMx С\п наружной холангиостомии» В общехирургическом лечении больной было отказано в связи с распространенностью процесса. Проведено обследование с целью оценки выраженности метаболических нарушений желчи и определения риска литогенеза после проведения наружной холангиостомии, в связи с чем определяли интегральный показатель литогенности желчи.
Для определения интегрального показателя литогенности использовали желчь, забор которой осуществляли при выполнении эндоскопического вмешательства с использованием эндоскопических стерильных катетеров. Затем желчь в объеме 50 мкл добавляли в 5 мл элюента (разведение 1:100, Ki=100,0), после чего проводили измерение суммарной антиокислительной активности исследуемого образца (AOAi, в нА·с) электрохимическим путем на амперометрическом детекторе (АОАi=304,9 нА·с). Далее определяли антиокислительную активность стандартного раствора аскорбиновой кислоты (AOAvitCi) в концентрации 1 мг/л, которая равнялась 1182,9 нА·с.
Кроме того, желчь в объеме 300 мкл вносили в тест-систему с 2,7 мл раствором люминола. Запускали реакцию радикального окисления люминола внесением через инжектор 0,5 мл 3% H2O2 и измеряли на люминотестере с помощью специального программного обеспечения максимум вспышки (МВХЛi=1,6 усл. ед.) и площадь хемилюминесценции (ПХЛi=238,2 усл. ед. пл.). Одновременно измеряли максимум вспышки и площадь хемилюминесценции контрольного раствора люминола без исследуемого субстрата, которые оставили: МВХЛLi=1,3 усл. ед., ПХЛLi=69,5 усл. ед. пл.
Для определения общих липидов центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию общих липидов определяли с помощью набора реактивов «Общие липиды» (PLIVA-Lachema Diagnostika s.r.o.). Оптическая плотность опытной пробы составила 0,122 единиц оптической плотности, оптическая плотность стандарта составила 0,306 единиц оптической плотности, что соответствовало концентрации общих липидов (ОЛi) 3,2 г/л.
Для определения холестерина центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию холестерина определяли с помощью набора реактивов «Холестерин-22-Витал» (Витал Диагностике СПб). Оптическая плотность опытной пробы составила 0,060 единиц оптической плотности, оптическая плотность стандарта составила 0,259 единиц оптической плотности, что соответствовало концентрации холестерина (XCi) 1,2 ммоль/л.
Интегральный показатель литогенности желчи рассчитывали по формуле: 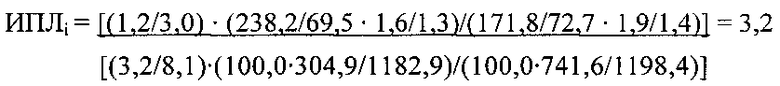
Проведенными исследованиями показано, что у пациента со злокачественным новообразованием головки поджелудочной железы было умеренное повышение интегрального показателя литогенности желчи (рассчитанного по описанной выше формуле, ИПЛi составил 3,2 единицы литогенности) в сравнении с данными контрольной группы, в связи с чем в качестве паллиативного окончательного метода лечения было выполнено эндоскопическое протезирование желчевыводящих путей билиарным стентом диаметром 11,5 Fr и длиной 7 см, удаление наружной холангиостомы. В дальнейшем в течение 4 месяцев у пациентки по результатам общеклинических обследований не было зафиксировано данных за обтурацию стента, рецидива механической желтухи и холангита, а проведенное лечение оценили как эффективное и адекватное.
Пример №4.
В хирургическое отделение №1 ГБУЗ «Научно-исследовательский институт - Краевая клиническая больница №1 имени профессора С.В. Очаповского» МЗКК (г. Краснодар) 23 октября 2014 года поступил пациент М., возраст 56 лет. Диагноз: «Хронический бескаменный холецистит. Холедохолитиаз? Механическая желтуха. Острый холангит». Длительность механической желтухи составила 4 недели. В качестве первого этапа лечения 24.10.14 выполнена эндоскопическая ретроградная холангиография, эндоскопическая папиллосфинктеротомия, браш-биопсия, назобилиарное дренирование по поводу стриктуры терминального отдела холедоха злокачественного генеза. От общехирургического лечения больной категорически отказался. Проведено обследование с целью оценки выраженности метаболических нарушений желчи и определения риска литогенеза после проведения назобилиарного дренирования, в связи с чем определяли интегральный показатель литогенности желчи.
Для определения интегрального показателя литогенности использовали желчь, забор которой осуществляли при выполнении эндоскопического вмешательства с использованием эндоскопических стерильных катетеров. Затем желчь в объеме 50 мкл добавляли в 5 мл элюента (разведение 1:100, Ki=100,0), после чего проводили измерение суммарной антиокислительной активности исследуемого образца (АОАi, в нА·с) электрохимическим путем на амперометрическом детекторе (AOAi=168,1 нА·с). Далее определяли антиокислительную активность стандартного раствора аскорбиновой кислоты (AOAvitCi) в концентрации 1 мг/л, которая равнялась 1192,7 нА·с.
Кроме того, желчь в объеме 300 мкл вносили в тест-систему с 2,7 мл раствором люминола. Запускали реакцию радикального окисления люминола внесением через инжектор 0,5 мл 3% H2O2 и измеряли на люминотестере с помощью специального программного обеспечения максимум вспышки (МВХЛi=3,8 усл. ед.) и площадь хемилюминесценции (ПХЛi=390,4 усл. ед. пл.). Одновременно измеряли максимум вспышки и площадь хемилюминесценции контрольного раствора люминола без исследуемого субстрата, которые оставили: МВХЛLi=1,4 усл. ед., ПХЛLi=74,9 усл. ед. пл.
Для определения общих липидов центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию общих липидов определяли с помощью набора реактивов «Общие липиды» (PLIVA-Lachema Diagnostika s.r.o.). Оптическая плотность опытной пробы составила 0,048 единиц оптической плотности, оптическая плотность стандарта составила 0,296 единиц оптической плотности, что соответствовало концентрации общих липидов (ОЛi) 1,3 г/л.
Для определения холестерина центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию холестерина определяли с помощью набора реактивов «Холестерин-22-Витал» (Витал Диагностике СПб). Оптическая плотность опытной пробы составила 0,072 единиц оптической плотности, оптическая плотность стандарта составила 0,267 единиц оптической плотности, что соответствовало концентрации холестерина (XCi) 1,4 ммоль/л.
Интегральный показатель литогенности желчи рассчитывали по формуле: 
Проведенными исследованиями показано, что у пациента со злокачественным новообразованием дистального отдела холедоха было выраженное повышение интегрального показателя литогенности желчи (рассчитанного по описанной выше формуле, ИПЛi составил 56,3 единицы литогенности) в сравнении с данными контрольной группы, в связи с чем в качестве паллиативного окончательного метода лечения было выполнено эндоскопическое протезирование желчевыводящих путей саморасширяющимся нитиноловым эндопротезом диаметром 10 мм и длиной 5 см. В дальнейшем в течение 7 месяцев у пациента по результатам общеклинических обследований не было зафиксировано данных за обтурацию стента, рецидива механической желтухи и холангита, а проведенное лечение оценили как эффективное и адекватное.
Пример №5.
В хирургическое отделение №2 ГБУЗ «Научно-исследовательский институт - Краевая клиническая больница №1 имени профессора СВ. Очаповского» МЗКК (г. Краснодар) 23 января 2015 года поступил пациент М., возраст 59 лет. Диагноз: «Рак головки поджелудочной железы. T4NxM1. ЖКБ. Хронический калькулезный холецистит. Механическая желтуха. Острый холангит». Длительность механической желтухи составила 3 недели. В качестве первого этапа лечения 24.01.15 выполнена чрескожная-чреспеченочная холангиостомия под ультразвуковыми рентгеноскопическим контролем. В общехирургическом лечении больному было отказано в связи с распространенностью процесса и отдаленным метастазированием. Проведено обследование с целью оценки выраженности метаболических нарушений желчи и определения риска литогенеза после проведения наружной холангиостомии, в связи с чем определяли интегральный показатель литогенности желчи.
Для определения интегрального показателя литогенности использовали желчь, забор которой осуществляли при выполнении эндоскопического вмешательства с использованием эндоскопических стерильных катетеров. Затем желчь в объеме 50 мкл добавляли в 5 мл элюента (разведение 1:100, Ki=100,0), после чего проводили измерение суммарной антиокислительной активности исследуемого образца (AOAi, в нА·с) электрохимическим путем на амперометрическом детекторе (AOAi=226,1 нА·с). Далее определяли антиокислительную активность стандартного раствора аскорбиновой кислоты (AOAvitCi) в концентрации 1 мг/л, которая равнялась 1230,8 нА·с.
Кроме того, желчь в объеме 300 мкл вносили в тест-систему с 2,7 мл раствором люминола. Запускали реакцию радикального окисления люминола внесением через инжектор 0,5 мл 3% H2O2 и измеряли на люминотестере с помощью специального программного обеспечения максимум вспышки (МВХЛi=2,5 усл. ед.) и площадь хемилюминесценции (ПХЛi=471,3 усл. ед. пл.). Одновременно измеряли максимум вспышки и площадь хемилюминесценции контрольного раствора люминола без исследуемого субстрата, которые оставили: МВХЛLi=1,6 усл. ед., ПХЛLi=81,0 усл. ед. пл.
Для определения общих липидов центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию общих липидов определяли с помощью набора реактивов «Общие липиды» (PLIVA-Lachema Diagnostika s.r.o.). Оптическая плотность опытной пробы составила 0,081 единиц оптической плотности, оптическая плотность стандарта составила 0,325 единиц оптической плотности, что соответствовало концентрации общих липидов (ОЛi) 2,0 г/л.
Для определения холестерина центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию холестерина определяли с помощью набора реактивов «Холестерин-22-Витал» (Витал Диагностике СПб). Оптическая плотность опытной пробы составила 0,086 единиц оптической плотности, оптическая плотность стандарта составила 0,262 единиц оптической плотности, что соответствовало концентрации холестерина (XCi) 1,7 ммоль/л.
Интегральный показатель литогенности желчи рассчитывали по формуле: 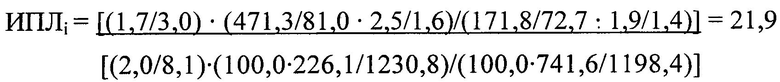
Проведенными исследованиями показано, что у пациента со злокачественным новообразованием поджелудочной железы и сопутствующей ЖКБ было значительное повышение интегрального показателя литогенности желчи (рассчитанного по описанной выше формуле, ИПЛi составил 21,9 единицы литогенности) в сравнении с данными контрольной группы, в связи с чем в качестве паллиативного окончательного метода лечения было выполнено наружно-внутреннее дренирование желчевыводящих путей под рентгеноскопическим контролем. В дальнейшем в течение 3 месяцев до момента летального исхода от прогрессирования основного заболевания у пациента по результатам общеклинических обследований не было зафиксировано данных за обтурацию дренажа, рецидива механической желтухи и холангита, а проведенное лечение оценили как эффективное и адекватное.
Пример №6.
В хирургическое отделение №1 ГБУЗ «Научно-исследовательский институт - Краевая клиническая больница №1 имени профессора С.В. Очаповского» МЗКК (г. Краснодар) 1 марта 2015 года поступил пациент Б., возраст 67 лет. Диагноз: «ЖКБ. Хронический калькулезный холецистит. Холедохолитиаз? Механическая желтуха. Острый холангит». Длительность механической желтухи составила 11 дней. В качестве первого этапа лечения 2.03.15 выполнена эндоскопическая ретроградная холангиография, эндоскопическая папиллосфинктеротомия, назобилиарное дренирование по поводу стриктуры н\3 холедоха, механической желтухи и острого холангита. После дообследования выставлен диагноз: рак холедоха, T2NxMx. В плане проведения общехирургического лечения (второго этапа) больному было рекомендовано в условиях стационара по месту жительства провести коррекцию явлений печеночно-почечной недостаточности и сопутствующей кардиологической патологии. Проведено обследование с целью оценки выраженности метаболических нарушений желчи и определения риска литогенеза после проведения назобилиарного дренирования, в связи с чем определяли интегральный показатель литогенности желчи.
Для определения интегрального показателя литогенности использовали желчь, забор которой осуществляли при выполнении эндоскопического вмешательства с использованием эндоскопических стерильных катетеров. Затем желчь в объеме 50 мкл добавляли в 5 мл элюента (разведение 1:100, Ki=100,0), после чего проводили измерение суммарной антиокислительной активности исследуемого образца (AOAi, в нА·с) электрохимическим путем на амперометрическом детекторе (AOAi=205,0 нА·с). Далее определяли антиокислительную активность стандартного раствора аскорбиновой кислоты (AOAvitCi) в концентрации 1 мг/л, которая равнялась 1214,6 нА·с.
Кроме того, желчь в объеме 300 мкл вносили в тест-систему с 2,7 мл раствором люминола. Запускали реакцию радикального окисления люминола внесением через инжектор 0,5 мл 3% H2O2 и измеряли на люминотестере с помощью специального программного обеспечения максимум вспышки (МВХЛi=7,3 усл. ед.) и площадь хемилюминесценции (ПХЛi=759,8 усл. ед. пл.). Одновременно измеряли максимум вспышки и площадь хемилюминесценции контрольного раствора люминола без исследуемого субстрата, которые оставили: МВХЛLi=1,5 усл. ед., ПХЛLi=70,1 усл. ед. пл.
Для определения общих липидов центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию общих липидов определяли с помощью набора реактивов «Общие липиды» (PLIVA-Lachema Diagnostika s.r.o.). Оптическая плотность опытной пробы составила 0,135 единиц оптической плотности, оптическая плотность стандарта составила 0,300 единиц оптической плотности, что соответствовало концентрации общих липидов (ОЛi) 3,6 г/л.
Для определения холестерина центрифугировали желчь в течение 30 минут при 3000 об/мин. Концентрацию холестерина определяли с помощью набора реактивов «Холестерин-22-Витал» (Витал Диагностике СПб). Оптическая плотность опытной пробы составила 0,087 единиц оптической плотности, оптическая плотность стандарта составила 0,251 единиц оптической плотности, что соответствовало концентрации холестерина (ХСi) 1,8 ммоль/л.
Интегральный показатель литогенности желчи рассчитывали по формуле: 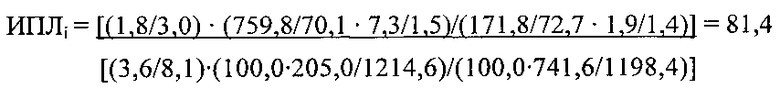
Проведенными исследованиями показано, что у пациента со злокачественным новообразованием поджелудочной железы и сопутствующей ЖКБ было выраженное повышение интегрального показателя литогенности желчи (рассчитанного по описанной выше формуле, ИПЛi составил 81,4 единицы литогенности) в сравнении с данными контрольной группы, в связи с чем в качестве метода длительной предоперационной декомпрессии было выполнено наружное дренирование желчевыводящих путей под УЗИ и рентгеноскопическим контролем. В дальнейшем в течение одного месяца до момента поступления в стационар для проведения второго этапа радикального лечения у пациента по результатам общеклинических и инструментальных исследований были зафиксированы данные за обтурацию наружного дренажа, периодические рецидивы механической желтухи и холангита, что требовало практически ежедневных санаций дренажа с целью профилактики его обтурации сладжированной желчью, тем самым выбор метода декомпрессии желчевыводящих путей и лечения оценили как адекватный данной клинической ситуации.
Таким образом, с помощью предложенного интегрального показателя литогенности желчи можно оценивать выраженность дисхолии и в дальнейшем использовать полученные данные для прогнозирования риска литогенеза и холелитиаза и целесообразности применения различных корригирующих мероприятий, в том числе использования билиарных эндопротезов с различными физико-химическими характеристиками.
Данное изобретение позволяет:
- исследовать в комплексе показатели дисхолии, свободнорадикального окисления и антиокислительной активности желчи, отражающих выраженность метаболических нарушений в желчи и ее литогенность, а следовательно, риск развития холелитиаза,
- определять целесообразность применения различных корригирующих мероприятий, в том числе рациональность проведения билиарного эндопротезирования у пациентов с холестазом,
- проводить мониторинг эффективности лечебных мероприятий, своевременно предотвращая развитие осложнений на местном уровне при выборе метода декомпрессии при обструкции желчевыводящих путей доброкачественного и злокачественного генеза.
Практическим результатом предложения является возможность исследования выраженности метаболических нарушений при заболеваниях билиопанкреатодуоденальной зоны на местном уровне на основании интегрального показателя литогенности желчи и оптимизации выбора метода декомпрессии желчевыводящих путей, направленных на предупреждение ранней инкрустации эндопротезов, за счет включения дополнительных критериев оценки дисхолии и повышения информативности о состояния литогенеза, что позволяет обеспечить адекватную тактику ведения больного и повысить эффективность лечебных мероприятий.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ АНТИОКСИДАНТНО-ЭНЕРГЕТИЧЕСКОГО ПОТЕНЦИАЛА ПИЩЕВЫХ ВЕЩЕСТВ | 2011 |
|
RU2452947C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО МОДЕЛИРОВАНИЯ ОКИСЛИТЕЛЬНОГО СТРЕССА У ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 2011 |
|
RU2455703C1 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ МЕТАБОЛИЗМА В ОРГАНИЗМЕ В УСЛОВИЯХ ОКИСЛИТЕЛЬНОГО СТРЕССА | 2010 |
|
RU2436101C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ХОЛЕЛИТОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 1996 |
|
RU2142814C1 |
| Способ диагностики печеночной недостаточности у больных с наружным дренированием желчевыводящих путей при хирургических заболеваниях гепатопанкреатобилиарной системы в раннем послеоперационном периоде | 2024 |
|
RU2834887C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ГЕПАТОПРОТЕКТОРА И ПРЕБИОТИКА, ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2006 |
|
RU2318538C1 |
| СПОСОБ ОЦЕНКИ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА К ВОЗДЕЙСТВИЮ ПРООКСИДАНТНЫХ ФАКТОРОВ | 2017 |
|
RU2629391C1 |
| СПОСОБ ПРОФИЛАКТИКИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ У ПАЦИЕНТОВ С ЖЕЛЧНОКАМЕННОЙ БОЛЕЗНЬЮ ПОСЛЕ ЛАПАРОСКОПИЧЕСКОЙ ХОЛЕЦИСТЭКТОМИИ | 2017 |
|
RU2657838C1 |
| Способ экспресс-оценки жизнеспособности клеток в тканеинженерных конструкциях | 2016 |
|
RU2662997C2 |
| Способ прогнозирования течения механической желтухи неопухолевого генеза | 2019 |
|
RU2703289C1 |
Изобретение относится к медицине и представляет собой способ оценки литогенности желчи, включающий определение в желчи у обследуемого (i) показателей холестерина (ХС, ммоль/л) в сравнении со средними значениями, принятыми за норму (k), отличающийся тем, что в желчи определяют комплекс общих липидов (ОЛ, г/л), суммарную антиокислительную активность (АОА) электрохимическим методом (в нА·с), максимум вспышки хемилюминесценции (МВХЛ, в усл. ед.) и площадь хемилюминесценции (ПХЛ, в усл. ед. площади), далее вычисляют интегральный показатель литогенности желчи (ИПЛi) по формуле:
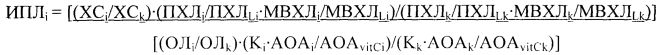
где Ki и Kk - коэффициент разведения - кратность разведения пробы желчи обследуемого и пробы желчи, принятой за норму, с ИПЛ не более 1,1 единиц литогенности - соответственно при определении АОА, и чем выше значение ИПЛi, тем более высокая степень литогенности желчи с риском развития холелитиаза. Способ позволяет оптимизировать выбор метода декомпрессии желчевыводящих путей, направленных на предупреждение ранней инкрустации эндопротезов, что позволяет повысить эффективность лечебных мероприятий. 6 пр.
Способ оценки литогенности желчи, включающий определение в желчи у обследуемого (i) показателей холестерина (ХС, ммоль/л) в сравнении со средними значениями, принятыми за норму (k), отличающийся тем, что в желчи определяют комплекс общих липидов (ОЛ, г/л) и показателей прооксидантно-антиоксидантного баланса: суммарную антиокислительную активность (АОА) электрохимическим методом (в нА·с), максимум вспышки хемилюминесценции (МВХЛ, в усл. ед.) и площадь хемилюминесценции (ПХЛ, в усл. ед. площади), дополнительно соотносят значения АОА с показателями стандартного аскорбинового эквивалента (AOAvitC), значения МВХЛ - с показателями максимума вспышки стандартного раствора люминола (МВХЛL), значения ПХЛ - с показателями площади стандартного раствора люминола (ПХЛL), далее вычисляют интегральный показатель литогенности желчи (ИПЛi) по формуле:
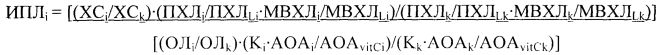
где Ki и Kk - коэффициент разведения - кратность разведения пробы желчи обследуемого и пробы желчи, принятой за норму, с ИПЛ не более 1,1 единиц литогенности - соответственно при определении АОА, и чем выше значение ИПЛi, тем более высокая степень литогенности желчи с риском развития холелитиаза.
Авторы
Даты
2016-08-10—Публикация
2015-07-14—Подача