Изобретение относится к экспериментальной медицине, а именно к моделированию патофизиологического состояния у экспериментальных животных, и может быть использовано для создания окислительного стресса с целью изучения закономерностей его протекания и оценки эффективности антиоксидантной терапии.
Одним из ключевых механизмов, сокращающих продолжительность активной жизнедеятельности человека, принято считать дисбаланс в системах перекисного окисления тканевых субстратов и антиоксидантной защиты в сторону усиления прооксидантного потенциала [Скулачев В.П. Феноптоз: запрограммированная смерть организма // Биохимия. - 1999. - Т.64, №12. - С.1679-1688, Дубинина Е.Е. Роль активных форм кислорода в качестве сигнальных молекул в метаболизме тканей при состояниях окислительного стресса // Вопросы медицинской химии. - 2001. - Т.47, №6. - С.561-581, Владимиров Ю.А. Активные формы кислорода и азота: значение для диагностики профилактики и терапии // Биохимия. - 2004. - Т.69, вып.1. - С.5-7]. Свободные радикалы могут возникать в организме в избыточном количестве вследствие радиоактивного и ультрафиолетового облучения, курения, избыточного потребления жиров и углеводов, при гиподинамии с ее низким уровнем биологического ферментативного окисления, а также под воздействием электромагнитного поля, различных внешних химических веществ, загрязнения воздуха, гипероксии и других факторов. Избыточное количество свободных радикалов наблюдается при снижении поступления антиоксидантов, таких как токоферол, аскорбиновая кислота, флавоноиды, и уменьшении активности антиоксидантных ферментов, что встречается при врожденных энзимопатиях антиоксидантных систем. Важное значение в предупреждении явлений, связанных с нарушением функционирования антиоксидантных систем организма, имеет своевременное и дозированное применение эффективных антиоксидантных средств (витаминов, липоевой кислоты, глутатиона, комбинированных антиоксидантных комплексов) [Балаболкин М.И., Креминская В.М., Клебанова Е.М. Роль окислительного стресса в патогенезе диабетической нейропатии и возможность его коррекции препаратами α-липоевой кислоты. // Проблемы эндокринологии. -2005. - Т.51, №3. - С.22-33, Ивашкин В.Т., Драпкина О.М., Шульпекова Ю.О. Диагностика и лечение неалкогольной жировой болезни печени. // Российские медицинские вести. - 2009. - Т.XIV, №3. - С.1-12].
Проведенные за последние два десятилетия исследования убедительно доказали, что смещение баланса в системе антиоксидантно-прооксидантного равновесия сопровождает многие физиологические и большинство патологических процессов. В частности, рядом авторов доказано, что раневой процесс неизбежно связан с активацией прооксидантной системы [Захаров В.В., Мамедов Л.А., Николаев А.В., Гудзь Т.И., Кудряшов Ю.Б., Гончаренко Е.Н., Рагимов Ч.Р., Городовикова Е.Н., Ковш И.В. Состояние анти- и прооксидантных систем при заживлении асептических и инфицированных ран в эксперименте // Бюллетень экспериментальной биологии и медицины. - 1988. - №6. -С.686-689; Grief R., Akca 0., Horn E.P, Kurz A., Sessler D.I. Supplemental perioperative oxygen to reduce the incidence of surgical-wound infection // New England Journal of Medicine. - 2000. - №342. - P.161-167; Kivisaari J., Vihersaari Т., Renvall S., Niinikoski J. Energy metabolism of experimental wounds at various oxygen environments // Annals of Surgery. - 1975. - №181. - P.823-828, Gordillo G.M., Sen C.K. Revisiting the essential role of oxygen in wound healing // Am. J. Surg. - 2003. - №186. - P.259-263].
Известен способ моделирования окислительного стресса [А.А.Овсепян, Н.И.Венедиктова, М.В.Захарченко, Р.Е.Казаков, М.Н.Кондрашова, Е.Г.Литвинова, И.Р.Саакян, Т.В.Сирота, И.Г.Ставровская, П.М.Шварцбург. Антиоксидантное и иммунопротекторное действие экстракта личинок восковой моли при окислительном стрессе у крыс, вызванном потреблением корма, обогащенного железом // Вестник новых медицинских технологий. - 2010. - №1 (электронное издание)], основанного на пищевой перегрузке железом. Длительное потребление животными корма, обогащенного железом в дозах, близких к принятым в ветеринарии, приводит к развитию окислительного стресса, а также нарушениям иммунных и митохондриальных функций. В частности, для выполнения модели на крысах последним вместе с основным рационом перорально дают препарат железа (1 мл/жив/сут).
Указанный способ имеет следующие недостатки:
а) моделирование окислительного стресса занимает длительное время (10-12 недель), что требует дополнительных материальных затрат на содержание животных и выполнение научно-исследовательской работы;
б) формируемая модель носит хронический вялотекущий характер за счет медленного развития окислительного стресса, что не позволяет исследовать процессы при патологических состояниях с острым течением и апробировать эффективность препаратов с антиоксидантными свойствами, применяемых при неотложной терапии;
в) затруднительно регулирование выраженности окислительного стресса в связи с медленным накоплением и выведением провоцирующего агента (железа), что не позволяет прогнозировать степень нарушений окислительного метаболизма в опытной группе на стадии планирования эксперимента;
г) возможны широкая вариабельность получаемых результатов, обусловленная дозированием провоцирующего препарата в связи с тем, что последний вводят вместе с частью рациона, что может приводить к получению большего количества ложных результатов в опытной группе.
Способ недостаточно эффективен из-за указанных недостатков.
За ближайший аналог принят способ [Н.В.Довженко, А.В.Куриленко, Н.Н.Бельчева, В.П.Челомин. Окислительный стресс, индуцируемый кадмием, в тканях двустворчатого моллюска Modiolus Modiolus // Биология моря. - 2005. - т.31 (№5) - с.358-62], который заключается в том, что используют взрослых особей двустворчатого моллюска Modiolus modiolus, отобранных по размеру (7-10 см), перед опытами выдерживают в аквариумах не менее 7 суток. Затем в аквариумы с экспериментальной группой животных добавляют раствор CdCl2 до концентрации 100 мкг/л. Воду в аквариумах меняют через сутки. Контрольную группу моллюсков содержали в таких же условиях, что и экспериментальную, но без добавления соли металла. Авторами метода установлено, что в данной модели окислительный стресс индуцируется через дезорганизацию антиоксидантной системы. Снижение способности антиоксидантной системы инактивировать свободные радикалы можно рассматривать как вероятную причину формирования окислительного стресса и накопления продуктов перекисного окисления липидов.
Указанный способ имеет следующие недостатки:
а) формируемая модель носит хронический вялотекущий характер за счет медленного развития окислительного стресса, связанного с предварительным хроническим ингибированием активности антиоксидантных ферментов, что может приводить к получению неоднородной опытной группы по интенсивности свободнорадикального окисления, обусловленного различной степенью ингибирования активности ферментов антирадикальной защиты;
б) используется вид животного, который не размножается в неволе и для проведения опытов должен вылавливаться в естественной среде, что затрудняет циклическое проведение лабораторных экспериментов;
в) затягивается время эксперимента в связи с тем, что требуется выполнение карантинных мероприятий, приводящее к повышению расходов на выполнение научно-исследовательской работы;
г) оценка эффективности способов лечения на данной модели затруднена в связи с единственным способом доставки препаратов - путем их растворения в среде обитания моллюска, такой подход оценки антиоксидантной активности зависит в большей степени от растворимости и биодоступности препарата (косвенные показатели), чем от его прямой антиоксидантной активности.
Способ отличается высокой ресурсоемкостью и низкой эффективностью из-за указанных недостатков.
Задача - разработка способа хирургического моделирования окислительного стресса у лабораторных животных, позволяющего с высокой эффективностью вызывать регулируемый дисбаланс между прооксидантной и антиоксидантной системами, имеющего направленную на выздоровление динамику течения модельной патологии, а также являющегося легковоспроизводимым и несложным в техническом выполнении.
Сущностью изобретения является способ хирургического моделирования окислительного стресса у лабораторных животных, включающий введение животному инициирующего окислительный стресс патогенного фактора, отличающийся тем, что после обработки операционного поля спиртовым раствором, под местной анестезией раствором новокаина 0,5% - 20-200 мл вызывают острый процесс - абсцесс мягких тканей - производят разрез, рассекают подкожную клетчатку, поверхностную и пояснично-спинную фасции, собственную фасцию мышцы выпрямителя спины, в рану вводят стерильный марлевый шарик, пропитанный суточной культурой патогенного штамма концентрацией 103/мл-108/мл или 1 мл жидкости, полученной растворением 1 грамма фекалий животного в 1-10 мл 0,9% раствора хлорида натрия, затем рану закрывают путем сшивания краев кожи кисетным швом, через 72-120 часов с момента проведения имплантации инфицированного инородного тела переводят процесс в хронический - формируют гнойную рану - снимают кожные швы, удаляют инородное тело: и выполняют санацию полости абсцесса.
Техническим результатом изобретения является:
1) обеспечение моделирования окислительного стресса с естественной направленностью на выздоровление, включающего в себя острую и хроническую фазы танатогенеза;
2) возможность регулировать тяжесть развивающегося окислительного стресса от легкой до крайне тяжелой (вплоть до потенциально летальной) с помощью штаммов, отличающихся вирулентностью, и внесением различного количества микробного инфекта;
3) высокая степень воспроизводимости окислительного стресса - возможность одновременного получения модели на многих лабораторных животных, с использованием многих штаммов бактерий;
4) технически несложные манипуляции с лабораторными животными для создания модели окислительного стресса (не требует общего наркоза, реанимационных приспособлений, при элементарном знании основ хирургических манипуляций).
Способ осуществляют следующим образом
Лабораторному животному накануне срезают и выбривают шерсть на средней и нижней третях спины. На следующий день после двукратной обработки операционного поля (выбритой зоны) спиртовым раствором под местной анестезией раствором новокаина 0,5% - 20-200 мл производят разрез длиной 1-5 см в зависимости от размера животного. Рассекают подкожную клетчатку, поверхностную и пояснично-спинную фасции, собственную фасцию мышцы выпрямителя спины. В образовавшуюся рану вводят стерильный марлевый шарик диаметром около 10 мм, пропитанный 1 мл жидкости с суточной культурой патогенного штамма, например, Staphylococcus aureus, концентрация 103/мл-108/мл, или 1 мл жидкости, полученной растворением 1 грамма фекалий животного в 1-10 мл 0,9% раствора хлорида натрия. Затем рану закрывают путем сшивания краев кожи над шариком кисетным швом, то есть проводят генерацию с помощью инородного тела острого гнойного заболевания мягких тканей - абсцесса (острая фаза окислительного стресса). Возможно выполнение нескольких ран на одном животном. Через 72-120 часов с момента проведения имплантации инфицированного инородного тела снимают кожные швы, удаляют инородное тело и выполняют санацию полости абсцесса. В результате происходит трансформация абсцесса в хронический гнойный процесс - гнойную рану (хроническая фаза окислительного стресса), которая может подвергаться лечению путем ежедневных перевязок с использованием асептического материала и мазевых препаратов.
Техническим результатом является регулируемая по тяжести и длительности двухфазная по характеру экспериментальная модель окислительного стресса, позволяющая с высокой эффективностью вызывать необходимый дисбаланс между прооксидантной и антиоксидантной системами и имеющая направленную на выздоровление динамику течения.
Технология способа хирургического моделирования окислительного стресса заключается в том, что у лабораторного животного создают абсцесс мягких тканей (острая фаза окислительного стресса), который после снятия швов и удаления инородного тела переводят в гнойную рану (хроническая фаза окислительного стресса).
Обоснование полученных результатов.
Апробацию модели окислительного стресса производили на лабораторных кроликах (24 штуки), контрольную группу составили сопоставимые по возрасту и весу лабораторные кролики, получающие обычный рацион и не подвергшиеся хирургическому вмешательству (11 штук). Кровь из ушной вены забиралась на 1, 3, 5, 7 и 10 сутки от начала эксперимента. Выраженность окислительного стресса определяли по изменению интенсивности хемилюминесценции и способности окисляться под воздействием постоянного электрического тока.
Антиокислительная активность плазмы крови, измеренная амперометрическим методом [Басов А.А., Федосов С.Р., Канус И.С., Еремина Т.В., Пшидаток Д.В., Малышко В.В. Современные способы стандартизации антиоксидантных лекарственных средств и биологически активных добавок // Современные проблемы науки и образования. - 2006. - №4. - Приложение №1, с.149], с 1 до 5 сутки уменьшалась на 38%, с 5 по 7 сутки стабилизировалась, после 7 суток возрастала на 7%.
Динамику процессов свободнорадикального окисления определяли при помощи лабораторной системы [Павлюченко И.И., Басов А.А., Федосов С.Р. Система лабораторной диагностики окислительного стресса. Патент на полезную модель №54787. - Заявл. 19.01.2006; опубл. 27.07.2006 - Б.21] со специальным программным обеспечением [Павлюченко И.И., Федосов С.Р., Басов А.А. Программа регистрации сигналов хемилюминотестера ЛТ-1. Свидетельство об официальной регистрации программы для ЭВМ №2006611562. - Заявл. №2006610783 от 16.03.2006] по максимуму и площади люминол-зависимой Н2O2-индуцированной хемилюминесценции. В ходе экспериментов установлено, что показатели максимума быстрой вспышки хемилюминесценции плазмы крови характеризовались относительным постоянством: наибольшие значения были отмечены до санации полости абсцесса (повышение на 162%), постоянное их снижение - после санации полости абсцесса (на 3-8% в сутки).
По совокупности оцениваемых показателей можно оценить предлагаемую модель окислительного стресса как функционально пригодную со следующими основными показателями: двухфазность, регулируемость тяжести течения, возможность быстрого создания необходимой рабочей модели.
Пример №1. До введения в эксперимент кролика №3 показатель максимума вспышки хемилюминесценции плазмы крови составил 0,481, показатель площади - 9,830, показатель антиокислительной активности - 2907 единиц.
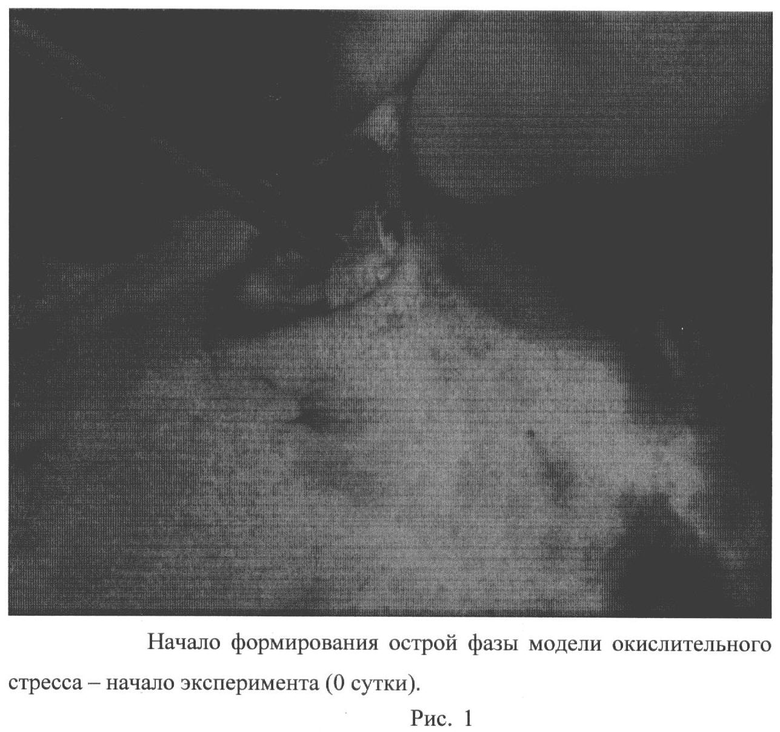
Было выполнено хирургическое моделирование острой фазы окислительного стресса, первый этап которого продемонстрирован на рисунке 1, где показано как в образовавшуюся в ходе операции рану вводят стерильный марлевый шарик диаметром около 10 мм, пропитанный 1 мл жидкости с суточной культурой патогенного штамма (0 сутки начала эксперимента).
После формирования абсцесса мягких тканей (острая фаза окислительного стресса) на 5 сутки показатель максимума вспышки хемилюминесценции плазмы крови составил 1,175 (+124% к исходным показателям), показатель площади - 55,02 (+460% к исходным показателям), показатель антиокислительной активности - 1591 (- 55% от исходных показателей).
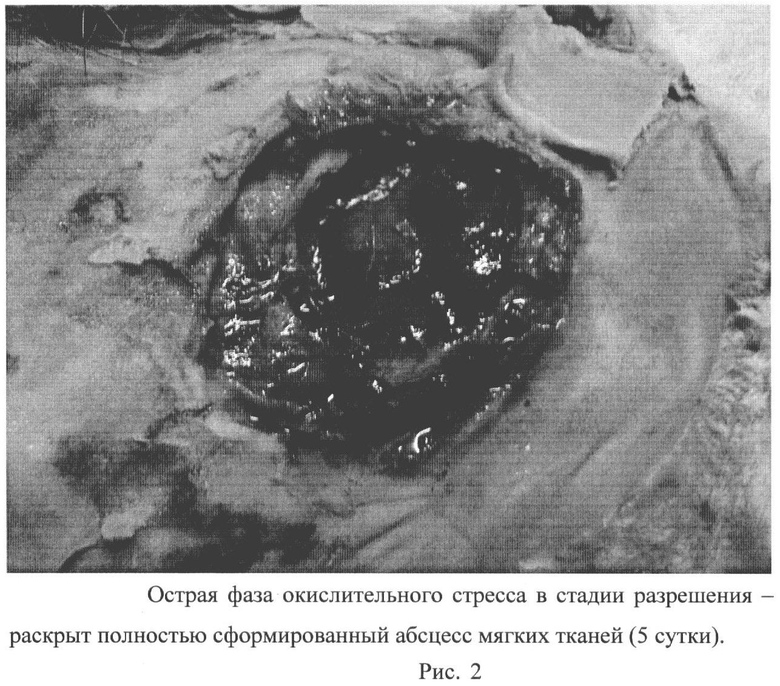
На рисунке 2 показано полное раскрытие абсцесса мягких тканей в стадии разрешения в острую фазу окислительного стресса (5 сутки эксперимента).
К моменту санации гнойного процесса в ране на 12 сутки показатель максимума вспышки хемилюминесценции плазмы крови составил 0,815 (+69% к исходным показателям), показатель площади - 40,82 (+315%), показатель антиокислительной активности -1783 (-39%).
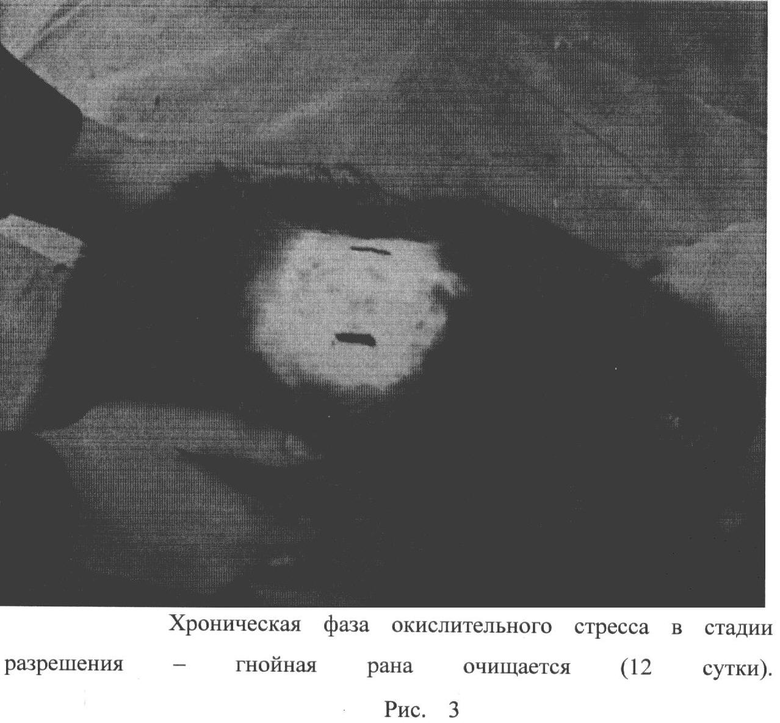
На рисунке 3 показана хроническая фаза окислительного стресса в стадии разрешения - гнойная рана очищается (12 сутки эксперимента).
Данное изобретение позволяет:
- моделировать окислительный стресс у лабораторных животных достаточного размера, любого вида и в необходимых (больших) количествах;
- снизить затраты на введение животного в эксперимент за счет сокращения сроков на формирование патологического процесса с окислительным стрессом в среднем на 35%;
- исследовать особенности течения окислительного стресса по фазам его развития: в острую фазу (до вскрытия абсцесса) и хроническую фазу (после вскрытия абсцесса и формирования гнойной раны), что определяет двухфазный характер экспериментальной модели на одном и том же лабораторном животном, снижая возможность получения ложных результатов при сравнении показателей в процессе дальнейшего анализа и статистической обработки;
- определять эффективность медикаментозного лечения окислительного стресса в зависимости от фазы его развития, что позволит дифференцировать необходимость применения отдельных препаратов с антиоксидантными свойствами в острой или хронической фазе развития окислительного стресса, а следовательно, сделать схемы лечения более рациональными для практического использования.
Практическим результатом предложения является возможность исследовать фазы течения окислительного стресса и эффективность его медикаментозного лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ МЕТАБОЛИЗМА В ОРГАНИЗМЕ В УСЛОВИЯХ ОКИСЛИТЕЛЬНОГО СТРЕССА | 2010 |
|
RU2436101C1 |
| СПОСОБ ОЦЕНКИ АНТИОКСИДАНТНО-ЭНЕРГЕТИЧЕСКОГО ПОТЕНЦИАЛА ПИЩЕВЫХ ВЕЩЕСТВ | 2011 |
|
RU2452947C1 |
| СПОСОБ БИОХИМИЧЕСКОЙ ОЦЕНКИ МЕТАБОЛИЧЕСКИХ НАРУШЕНИЙ В ЖЕЛЧИ ПРИ ЛИТОГЕНЕЗЕ | 2015 |
|
RU2593340C1 |
| СПОСОБ ДИАГНОСТИКИ ОКИСЛИТЕЛЬНОГО СТРЕССА ОРГАНИЗМА ЧЕЛОВЕКА | 2003 |
|
RU2236008C1 |
| СПОСОБ ОЦЕНКИ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА К ВОЗДЕЙСТВИЮ ПРООКСИДАНТНЫХ ФАКТОРОВ | 2017 |
|
RU2629391C1 |
| СПОСОБ КОНТРОЛЯ АНТИОКИСЛИТЕЛЬНОЙ АКТИВНОСТИ ПРОФИЛАКТИЧЕСКИХ И ЛЕЧЕБНЫХ АНТИОКСИДАНТНЫХ СРЕДСТВ | 2001 |
|
RU2182706C1 |
| Способ моделирования хронического травматического остеомиелита | 2015 |
|
RU2622369C1 |
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНОЙ ЯЗВЫ РОГОВИЦЫ | 2015 |
|
RU2602362C1 |
| СПОСОБ ПРОФИЛАКТИКИ И КОРРЕКЦИИ МЕТАБОЛИЧЕСКИХ И ФУНКЦИОНАЛЬНЫХ НАРУШЕНИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ В УСЛОВИЯХ СТРЕССА | 2019 |
|
RU2717107C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОГО ВОЗДЕЙСТВИЯ ПРИ ЛЕЧЕНИИ МЕСТНОГО ОТГРАНИЧЕННОГО ПЕРИТОНИТА В ЭКСПЕРИМЕНТЕ | 2023 |
|
RU2834555C1 |
Изобретение относится к экспериментальной медицине, а именно к моделированию окислительного стресса с целью изучения закономерностей его протекания и оценки эффективности антиоксидантной терапии. Моделирование проводят путем создания острого и хронического повреждения организма. После обработки операционного поля спиртовым раствором, под местной анестезией раствором новокаина 0,5% - 20-200 мл, вызывают острый процесс - абсцесс мягких тканей. Для этого производят разрез кожи, рассекают подкожную клетчатку, поверхностную и пояснично-спинную фасции, собственную фасцию мышцы выпрямителя спины. В рану вводят стерильный марлевый шарик, пропитанный суточной культурой патогенного штамма бактерий концентрацией 103/мл-108/мл или пропитанный 1 мл жидкости, полученной растворением 1 грамма фекалий животного в 1-10 мл 0,9% раствора хлорида натрия. Затем рану закрывают путем сшивания краев кожи кисетным швом. Через 72-120 часов с момента проведения имплантации инфицированного инородного тела переводят процесс в хронический - формируют гнойную рану. Для этого снимают кожные швы, удаляют инородное тело и выполняют санацию полости абсцесса. Способ обеспечивает регулируемую по тяжести и длительности, двухфазную по характеру экспериментальную модель окислительного стресса, позволяющую с высокой эффективностью вызывать необходимый дисбаланс между прооксидантной и антиоксидантной системами и имеющую направленную на выздоровление динамику течения. 3 ил., 1 пр.
Способ хирургического моделирования окислительного стресса у лабораторных животных, включающий введение животному инициирующего окислительный стресс патогенного фактора, отличающийся тем, что после обработки операционного поля спиртовым раствором под местной анестезией раствором новокаина 0,5% - 20-200 мл, вызывают острый процесс - абсцесс мягких тканей, для этого производят разрез, рассекают подкожную клетчатку, поверхностную и пояснично-спинную фасции, собственную фасцию мышцы выпрямителя спины, в рану вводят стерильный марлевый шарик, пропитанный суточной культурой патогенного штамма концентрацией 103/мл - 108/мл или 1 мл жидкости, полученной растворением 1 г фекалий животного в 1-10 мл 0,9%-ного раствора хлорида натрия, затем рану закрывают путем сшивания краев кожи кисетным швом, через 72-120 ч с момента проведения имплантации инфицированного инородного тела переводят процесс в хронический - формируют гнойную рану, для чего снимают кожные швы, удаляют инородное тело и выполняют санацию полости абсцесса.
| GÜRER A, et al | |||
| Tissue oxidative stress level and remote organ injury in two-hit trauma model of sequential bum injury and peritoneal sepsis are attenuated with N-acetylcysteine treatment in rats | |||
| Ulus Travma Acil Cerrahi Derg | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА У КРЫС | 2009 |
|
RU2394281C1 |
| СПОСОБ КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ ДЖОЗАМИЦИНОМ ПРИ L-NAME-ИНДУЦИРОВАННОМ ДЕФИЦИТЕ ОКСИДА АЗОТА | 2007 |
|
RU2353369C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЦЕЛЕСООБРАЗНОСТИ НАЗНАЧЕНИЯ ЭМОКСИПИНА БОЛЬНЫМ РОЖЕЙ | 2003 |
|
RU2232995C1 |
| ПРИСПОСОБЛЕНИЕ К ДАЛЬНОМЕРУ ДЛЯ ОПРЕДЕЛЕНИЯ ВЫСОТЫ ИЛИ ГОРИЗОНТАЛЬНОГО РАССТОЯНИЯ ВОЗДУШНОЙ ЦЕЛИ | 1926 |
|
SU11160A1 |
Авторы
Даты
2012-07-10—Публикация
2011-01-11—Подача