Область изобретения
Настоящее изобретение относится к специфично связывающимся молекулам, в частности к антителам и их фрагментам, которые связываются с аннексином-А1, и к гибридомным линиям клеток, которые производят такие специфично связывающиеся молекулы. Такие специфично связывающиеся молекулы применимы в лечении заболеваний, опосредованных Т-клетками.
Предпосылки создания изобретения
Глюкокортикоиды (ГК) часто применяют для лечения ряда хронических аутоиммунных заболеваний благодаря их способности одновременно блокировать как врожденный, так и приобретенный иммунный ответ. Исследования последних десяти лет, проведенные авторами настоящего изобретения и другими исследовательскими группами, показали, что некоторые из воспалительных эффектов, оказываемых ГК на врожденный иммунный ответ, опосредованы белком Аннексином-1 (Annexin-1, Anx-А1). Было показано, что этот белок осуществляет гомеостатическую регуляцию многих типов клеток, в том числе нейтрофилов, макрофагов и клеток эндотелия. Однако одним аспектом, которому не уделяли никакого внимания, является роль Anx-А1 в адаптивном иммунном ответе. Это вызывает удивление, с учетом того, что, как предполагается, Anx-А1 является одним из вторичных посредников фармакологического действия ГК.
Авторы данного изобретения ранее показали, что Anx-А1 играет гомеостатическую роль в Т-клетках, за счет модулировния интенсивности передачи сигналов рецептором Т-клеток (TCR) (D'Acquisto et al., Blood 109: 1095-1102, 2007). Более того, авторы настоящего изобретения показали, что высокий уровень Anx-А1 снижает порог активации Т-клеток и способствует их дифференцировке в клетки Th1, в то время как у мышей, дефицитных по Anx-А1, наблюдают нарушение активации Т-клеток и более интенсивную дифференцировку в клетки Th2 (D'Acquisto et al., Eur. J. Immunol. 37: 3131-3142, 2007).
В публикации WO 2005/027965 описан механизм, за счет которого апоптотические нейтрофилы доставляют противовоспалительные сигналы к дендритным клеткам, а также идентифицированы антитела, которые препятствуют этому процессу.
Краткое описание изобретения
Авторами настоящего изобретения было идентифицировано моноклональное антитело, обладающее превосходными свойствами в плане специфичного ингибирования активации Т-клеток без каких-либо неблагоприятных цитотоксических эффектов. Такое антитело применимо в лечении заболеваний, опосредованных Т-клетками, например ревматоидного артрита или рассеянного склероза.
Соответственно, настоящее изобретение обеспечивает специфично связывающуюся молекулу, направленную против белка человека Anx-А1, имеющую аминокислотную последовательность, представленную на Фигуре 2А.
Определения
При использовании в настоящей заявке термина «специфично связывающаяся молекула» относится к члену пары молекул, обладающих специфичностью связывания по отношению друг к другу. Члены пары молекул со специфичным связыванием могут быть природными или полностью или частично синтетическими. Один из членов указанной пары молекул имеет на своей поверхности область, которая может представлять собой выступ или полость, которая специфично связывается и, следовательно, является ей комплементарной, с определенной пространственной и полярной структурой другого члена указанной пары молекул. Таким образом, члены такой пары обладают свойством специфичного связывания друг с другом. Примеры типов пар со специфичным связыванием включают антиген-антитело, биотин-авидин, гормон-рецептор гормона, рецептор-лиганд, фермент-субстрат. Настоящее изобретение в целом относится к реакциям типа антиген-антитело. Специфично связывающаяся молекула согласно настоящему изобретению связывается с Anx-A1c большим сродством, чем с другими молекулами, то есть специфично связывается с Anx-А1. Специфично связывающиеся молекулы, которые связываются с Anx-А1, включают антитела к Anx-А1 и их аптамеры. Специфично связывающиеся молекулы согласно настоящему изобретению, как правило, представляют собой антитела. Антитела к Anx-А1 согласно настоящему изобретению функционируют, блокируя активацию Т-клеток и, таким образом, при введении в организм, их можно применять для лечения заболеваний, опосредованных Т-клетками, которые обычно обусловлены аберрантной активацией Т-клеток.
Термин «антитело», используемый в настоящей заявке, относится к молекулам иммуноглобулина и иммунологически активным участкам молекул иммуноглобулина, то есть молекулам, содержащим сайт связывания антигена, который специфично связывается с антигеном, который является природным или частично или полностью получен синтетически. Этот термин также охватывает любой полипептид или белок, имеющий связывающий домен, который представляет собой связывающий домен антитела или гомологичен ему. Антитела могут быть получены из природных источников, или они могут быть частично или полностью синтетическими. Антитела представляют собой полипептиды, которые обычно содержат две идентичные тяжелые цепи и две идентичные легкие цепи, которые меньше, чем тяжелые цепи. У млекопитающих существуют два типа легких цепей, которые называют лямбда (λ) и каппа (κ). Каждая из тяжелых цепей и каждая из легких цепей состоит из вариабельной области и константной области. Вариабельную область тяжелой цепи обозначают как область VH, а вариабельную область легкой цепи обозначают как область VL. В случае легкой цепи каппа область VL может обозначаться как область VK. Каждая из вариабельных областей тяжелых и легких цепей включает в себя три гипервариабельных участка (участка, определяющих комплементарность, complementarity determining regions, CDR), CDR1, CDR2 и CDR3. Их обозначают как VLCDR1, VLCDR2, VLCDR3, VHCDR1, VHCDR2 и VHCDR3 соответственно. Примерами антител являются изотипы иммуноглобулинов (например, IgG, IgE, IgM, IgA и IgD) и их изотипические подклассы; фрагменты, содержащие антигенсвязывающий домен, такие как Fab, F(ab')2, Fv, scFv, dAb, Fd и диатела. Антитела могут быть поликлональными или моноклональными. Моноклональные антитела упоминаются в настоящей заявке как «МАТ».
Подробное описание изобретения
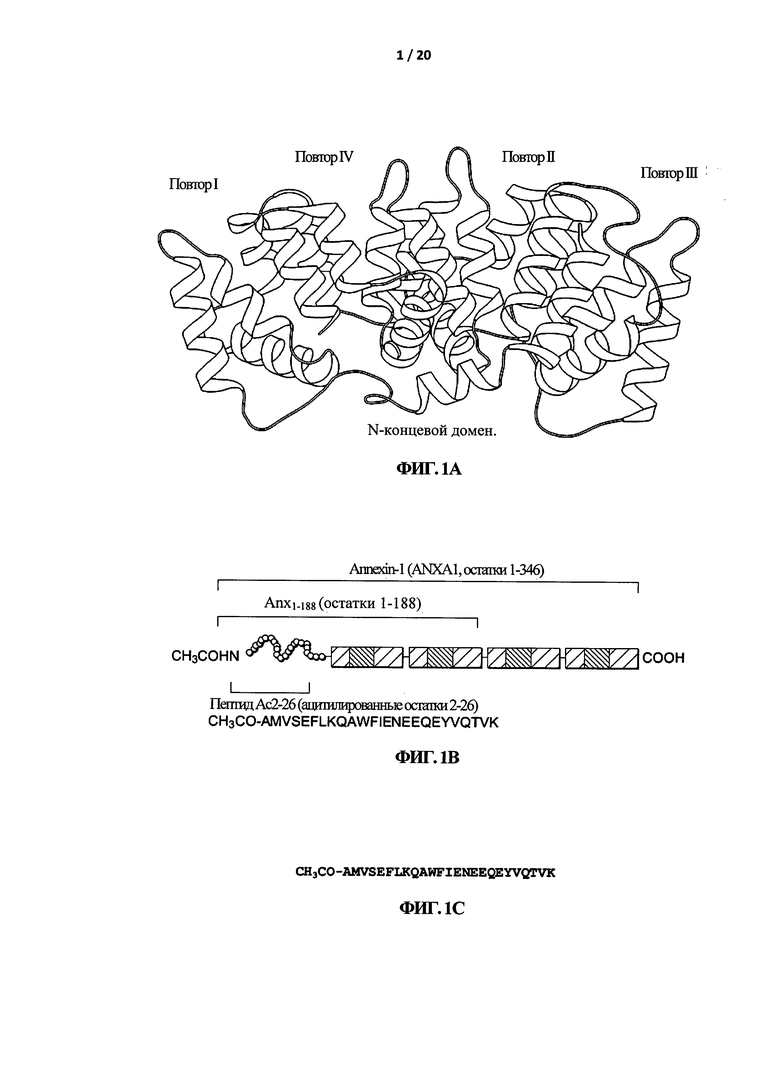
Аннексины представляют собой группу кальций- и фосфолипид-связывающих клеточных белков, также известных как липокортины. Семейство аннексинов состоит из 13 членов, включая Аннексин А1, Аннексин А2 и Аннексин А5. Аннексин А-1 также известен как Аннексин-1 и в данной заявке обозначен "Anx-А1". Аннексин-1 (Anx-А1) представляет собой белок с молекулярной массой 37 кДа, который изначально был описан как посредник действия глюкокортикоидов. За последние несколько лет появились доказательства того, что Anx-А1 выполняет гомеостатическую функцию в приобретенном иммунном ответе, в частности в Т-клетках, за счет изменения интенсивности сигналинга от Т-клеточного рецептора (TCR). Anx-А1 действует как эндогенный ингибитор воспаления в клетках системы врожденного иммунитета in vivo. На Фигуре 1А представлена ленточная диаграмма трехмерной структуры Anx-А1.
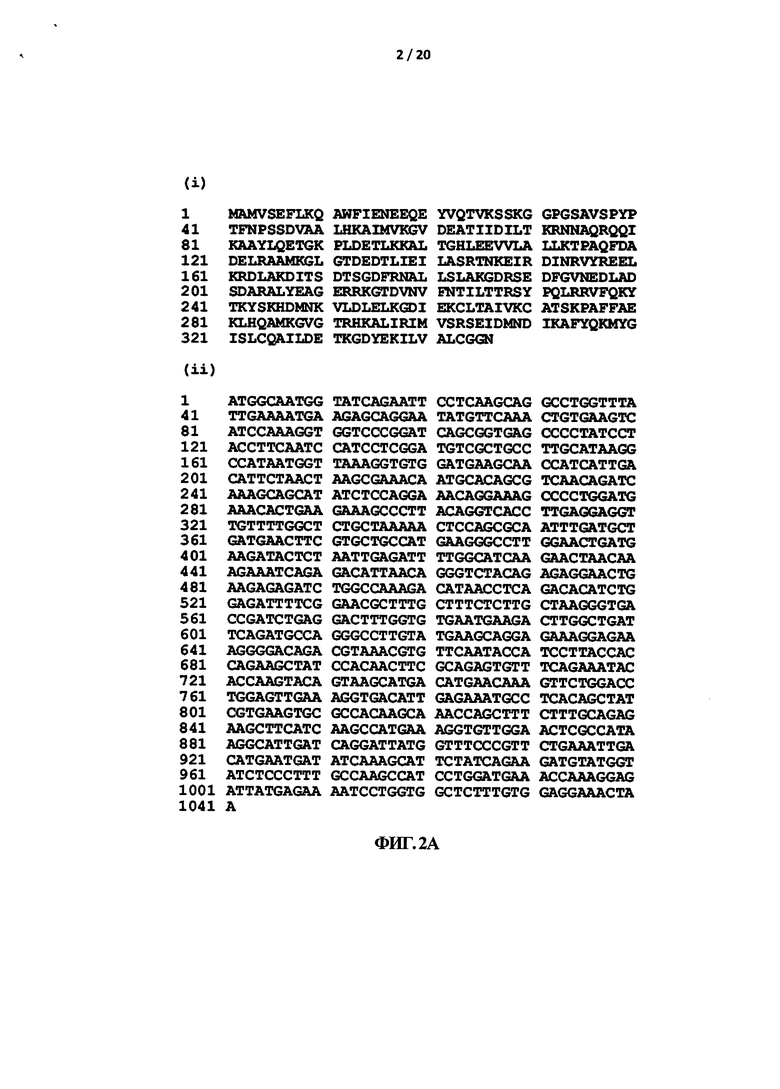
У человека присутствуют 8 нуклеотидных последовательностей, кодирующих Anx-А1. Из них транслируются только четыре, и, таким образом, существует четыре изоформы Anx-А1, обозначаемые как ANXA1-002, ANXA1-003, ANXA1-004 и ANXA1-006. Эти последовательности доступны на сайте Ensembl (www.ensembl.org) и обозначены как OTTHUMT00000052664 (ANXA1-002), OTTHUMT00000052665 (ANXA1-003), OTTHUMT00000052666 (ANXA1-004) и OTTHUMT00000052668 (ANXA1-006). Аминокислотная и нуклеотидная последовательности одной из изоформ человеческого Аннексина-1 (Anx-A1), ANXA1-003 приведены на Фигуре 2а. Аминокислотные и нуклеотидные последовательности изоформ ANXA1-002, ANXA1-004 и ANXA1-006 приведены на Фигурах 2b, 2с и 2d соответственно. Как можно видеть на Фигуре 2, изоформы ANXA1-002, ANXA1-004 и ANXA1-006 являются короткими спланированными вариантами ANXA1-003 или вариантами ANXA1-003 с небольшим числом аминокислотных замен.
В ряде исследований показано, что N-концевой пептид Anx-А1, называемый Ас.2-26, действует как биологически активный суррогат целого белка (см., напр., Lim et ah, Ргос Natl Acad Sci USA 95, 14535-9, 1998).
На Фигуре 1B схематично представлены повторы в составе аннексина и локализация такой биологически активной последовательности. Пептид Ас.2-26 представляет собой ацетилированный пептид с последовательностью аминокислотных остатков 2-26 из полноразмерной аминокислотной последовательности Anx-А1, показанной на Фигуре 2. Последовательность пептида Ас.2-26 показана на Фигуре 1С:
СН3СО-AMVSEFLKQAWFIENEEQEYVQTVK.
Биологическое действие Anx-А1 и его производных N-концевых биологически активных пептидов опосредовано членами семейства рецепторов формильных пептидов (FPR, formyl peptide receptor). Anx-A1 оказывает контррегуляторное действие на экстравазацию нейтрофилов и врожденный иммунитет за счет непосредственного связывания и активации одного из членов этого семейства, белка, подобного рецептору формильных пептидов-1 (Formyl Peptide Receptor-Like-1, FPRL-1). Авторами настоящего изобретения ранее было обнаружено, что стимуляция Т-клеток в присутствии hrAnx-A1 повышает уровень активации Т-клеток за счет стимуляции FPRL-1 (D'Acquisto et al., Blood 109: 1095-1102, 2007).
Специфично связывающиеся молекулы согласно настоящему изобретению связываются с Аннексином-1 (Anx-A1). Anx-А1, с которым связывается указанная специфично связывающаяся молекула в основном представляет собой Anx-А1 человека, имеющий полипептидную последовательность, приведенную на Фигуре 2А.
В первом своем аспекте настоящее изобретение обеспечивает специфично связывающуюся молекулу, направленную против белка Anx-А1 человека, имеющего аминокислотную последовательность, приведенную на Фигуре 2А.
Этот аспект настоящего изобретения также распространяется на специфично связывающиеся молекулы, которые содержат гипервариабельные участки (CDR) VLCDR1, VLCDR2, VLCDR3, VHCDR1, VHCDR2 и VHCDR3 специфично связывающейся молекулы согласно первому аспекту настоящего изобретения или аминокислотную последовательность, по меньшей мере на 70% идентичной каждому из соответствующих CDR. Специфично связывающаяся молекула, как правило, представляет собой антитело.
В одном из вариантов реализации специфично связывающаяся молекула содержит гипервариабельные участки (CDR) VLCDR1, VLCDR2, VLCDR3, VHCDR1, VHCDR2 и VHCDR3, каждый из которых имеет соответствующую аминокислотную последовательность, как указано ниже, где
VLCDR1 представляет собой KASENVVTYVS,
VLCDR2 представляет собой GASNRYT,
VLCDR3 представляет собой GQGYSYPYT,
VHCDR1 представляет собой GYTFTNYWIG,
VHCDR2 представляет собой DIYPGGDYTNYNEKFKG,
VHCDR3 представляет собой WGLGYYFDY,
или аминокислотную последовательность, по меньшей мере на 70% идентичную ей.
CDR обозначены в соответствии с комбинацией определения на основе консервативности последовательностей (Kabat et al in "Sequences of Proteins of Immunological Interest", Nat'l. Inst. Health, Bethesda, MD (1987)) и структурного определения (Chothia and Lesk J. Mol Biol. 196:901-17(1987)). Эти варианты определений также впоследствии были описаны в работе Carter et al, Proc Nat'l Acad Sci USA. 89:4285-9 (1992).
Настоящее изобретение также относится к вариантам пептидных последовательностей, упомянутых выше. Используемый в настоящей заявке термин «вариант» относится к белкам, которые имеют сходные аминокислотные последовательности и/или которые сохраняют одинаковые функции. В частности, термин «вариант» охватывает белки или полипептиды, которые содержат одну и более аминокислотную вставку, делецию, замену и т.п. Примером варианта согласно настоящему изобретению является белок, такой как гибридный белок, содержащий пептид, являющийся таким как определено выше, за исключением того, что в нем заменены одна или более аминокислот на одну или более других аминокислот. Как известно специалисту, различные аминокислоты обладают похожими свойствами. Одна или более таких аминокислота в веществе часто может быть заменена на другую одну или более других таких аминокислот с сохранением желаемой активности такого вещества.
Так, аминокислоты глицин, аланин, валин, лейцин и изолейцин часто могут заменять друг друга (аминокислоты с алифатическими боковыми цепями). Среди возможных замен предпочтительны замены, при которых замещают друг друга глицин и аланин (поскольку они имеют относительно короткие боковые цепи) или валин, лейцин и изолейцин (они имеют большие алифатические боковые цепи, которые обладают свойством гидрофобности). Другими аминокислотами, которые часто могут заменять друг друга, являются фенил аланин, тирозин и триптофан (аминокислоты, содержащие ароматические боковые цепи); лизин, аргинин и гистидин (аминокислоты с основными боковыми цепями); аспарагин и глутамин (аминокислоты, с кислыми боковыми цепями) и цистеин и метионин (аминокислоты с серосодержащими боковыми цепями).
Замены такого рода часто называют «консервативными» или «полуконсервативными» аминокислотными заменами. Настоящее изобретение, таким образом, распространяется также на специфично связывающиеся молекулы, содержащие CDR, имеющие аминокислотные последовательности, описанные выше, но включающие одну или более консервативную замену в CDR, такую, что аминокислотные последовательности CDR по меньшей мере на 70% идентичны последовательностям, описанным выше. Например, каждый CDR может содержать 1, 2, 3, 4 или 5 консервативных замен (в зависимости от конкретного CDR), по сравнению с аминокислотной последовательностью CDR, указанной выше. Например, в аминокислотной последовательности VLCDR1, приведенной выше, может содержаться 1, 2 или 3 консервативных замены, в аминокислотной последовательности VLCDR2, приведенной выше, может содержаться 1 или 2 консервативные замены, в аминокислотной последовательности VLCDR3, приведенной выше, может содержаться 1 или 2 консервативные замены, в аминокислотной последовательности VHCDR1, приведенной выше, может содержаться 1, 2 или 3 консервативные замены, в аминокислотной последовательности VHCDR2, приведенной выше, может содержаться 1, 2, 3, 4 или 5 консервативные замены, и в аминокислотной последовательности VHCDR3, приведенной выше, может содержаться 1, 2 или 3 консервативные замены, и последовательность при этом будет сохранять по меньшей мере 70% идентичности последовательностям CDR, приведенным выше.
Для аминокислот используются следующие трехбуквенные и однобуквенные обозначения: глицин (G или Gly), аланин (А или Ala), валин (V или Val), лейцин (L или Leu), изолейцин (I или Ile), пролин (Р или Pro), фенилаланин (F или Phe), тирозин (Y или Tyr), триптофан (W или Trp), лизин (К или Lys), аргинин (R или Arg), гистидин (Н или His), аспарагиновая кислота (D или Asp), глутаминовая кислота (Е или Glu), аспарагин (N или Asn), глутамин (Q или Gln), цистеин (С или Cys), метионин (М или Met), серии (S или Ser) и треонин (Т или Thr). В случае, если аминокислотный остаток может представлять собой аспарагиновую кислоту или асапарагин, могут использоваться обозначения Asx или В. В случае, если аминокислотный остаток может представлять собой глутаминовую кислоту или глутамин, могут использоваться обозначения Glx или Z. Аспарагиновая кислота также подразумевает аспартат, а глутаминовая кислота - глутамат, если в тексте не обозначено иначе.
Указанная выше последовательность белка, например гибридного белка, упомянутого выше, также может содержать делеции или вставки аминокислот. Так, например, аминокислоты, удаление которых не оказывает значительного влияния на активность белка или по меньшей мере не уничтожает указанную активность, могут быть удалены. Такие делеции могут быть выгодны, в случае если они уменьшают общую длину и молекулярный вес полипептида при сохранении его активности. Это может позволить уменьшить количество белка, необходимого для конкретной цели, например могут быть уменьшены размеры доз.
Также можно осуществлять вставки аминокислот в последовательность химерного белка. Это может быть сделано для изменения свойств вещества согласно настоящему изобретению (например, для облегчения идентификации, очистки или экспрессии, как описано выше в отношении гибридных белков).
Также вышеописанная последовательность может содержать аминокислотные замены, которые можно осуществлять для изменения свойств белка (например, для облегчения его определения, очистки или экспрессии). Аминокислотные замены можно осуществлять с использованием любой подходящей техники, например, с помощью направленного мутагенеза или твердофазного синтеза.
Необходимо учитывать, что аминокислотные замены или вставки в рамках данного изобретения можно осуществлять с применением как природных, так и неприродных аминокислот. Вне зависимости от того, используется ли природная или неприродная аминокислота, предпочтительно присутствие только L-аминокислот.
«Идентичность», как известно в данной области, обозначает схожесть двух или более полипептидных последовательностей или двух или более полинуклеотидных последовательностей, которое определяют путем сравнения последовательностей. В данной области идентичность также означает степень родства между полипептидными или полинуклеотидными последовательностями, в зависимости от обстоятельств, которую определяют по совпадению цепей таких последовательностей. Хотя существует целый ряд способов для оценки идентичности между двумя полипептидными или двумя полинуклеотидными последовательностями, способы, обычно применяемые для определения идентичности, представлены в виде компьютерных программ. Популярные компьютерные программы для определения идентичности двух последовательностей включают, но не ограничены перечисленными, пакет программ GCG (Devereux, et al., Nucleic Acids Research, 12, 387 (1984), BLASTP, BLASTN и FASTA (Atschul et al., J. Molec. Biol. 215, 403 (1990)).
Для сравнения аминокислотных последовательностей можно использовать такую программу, как CLUSTAL. Эта программа сравнивает аминокислотные последовательности и находит оптимальное выравнивание за счет введения разрывов в любую из последовательностей при необходимости. Возможно рассчитать идентичность или сходство (идентичность, а также сохранение типа аминокислоты) для оптимального выравнивания. Такие программы, как BLASTx, выравнивают наиболее длинный участок со сходными последовательностями и оценивают уровень идентичности. Таким образом, можно сравнить найденные области со сходными последовательностями, каждая из которых имеет свой уровень идентичности. В данном изобретении рассмотрены оба типа анализа идентичности.
Процент идентичности двух аминокислотных последовательностей или двух нуклеотидных последовательностей определяют при помощи выравнивания последовательностей с целью оптимального сравнения (например, в первую последовательность можно ввести разрывы для лучшего сравнения с другой последовательностью) и для сравнения аминокислотных остатков или нуклеотидов в позициях, соотносящихся друг с другом. «Наилучшее выравнивание» - это такое выравнивание двух последовательностей, которое приводит к максимальному проценту идентичности. Процент идентичности определяется как число одинаковых аминокислотных или нуклеотидных остатков в сравниваемых последовательностях (т.е. % идентичности = число идентичных позиций/общее число позиций × 100).
Определение процента идентичности двух последовательностей может быть усовершенствовано за счет использования математического алгоритма, известного специалистам в данной области техники. Одним из примеров математического алгоритма для сравнения двух последовательностей представляет собой алгоритм Карлина и Альтшула (Karlin and Altschul (1990) Proc. Natl. Acad. Sci. USA 87:2264-2268), модифицированный Карлином и Альтшулом в 1993 (Karlin and Altschul (1993) Proc. Natl. Acad. Sci. USA 90:5873-5877. Программы NBLAST и XBLAST (Altschul, et al. (1990) J. Mol. Biol. 215:403-410) включают такой алгоритм. Для получения нуклеотидных последовательностей, гомологичных нуклеиновым кислотам данного изобретения, нуклеотидный поиск BLAST может осуществляться с помощью программы NBLAST, счет = 100, длина слова = 12. Для получения аминокислотных последовательностей, гомологичных белковым молекулам данного изобретения, поиск белков BLAST может осуществляться с помощь программы XBLAST, счет = 50, длина слова = 3. Для получения выравниваний с пропусками с целью сравнения можно использовать Gapped BLAST, как описано у Альтшула и др. (Altschul et al. (1997) Nucleic Acids Res. 25:3389-3402). В качестве альтернативы можно использовать PSI-Blast для проведения повторного поиска, который выявляет отдаленные сходства между молекулами (Id). При использовании программ BLAST, Gapped BLAST и PSI-Blast можно использовать параметры по умолчанию в соответствующих программах (например, XBLAST и NBLAST). См. http://www.ncbi.nlm.nih.gov. Другим примером математического алгоритма, используемого для сравнения последовательностей, представляет собой алгоритм Миерса и Миллера (Myers and Miller, CABIOS (1989)). Программа ALIGN (версия 2.0), которая представляет собой часть пакета программ выравнивания последовательностей CGC, включает в себя этот алгоритм. Другие алгоритмы для анализа последовательностей, известные в данной области техники, включают ADVANCE ADAM, как описано у Тореллиса и Роботти (Torellis и Robotti (1994) Comput. Appl. Biosci., 10:3-5); и FASTA, описанный у Пирсона и Липмана (Pearson и Lipman (1988) Proc. Natl. Acad. Sci. 85:2444-8). В FASTA параметр ktup представляет собой контрольную опцию, которая позволяет настраивать чувствительность и скорость поиска.
Как правило, аминокислотная последовательность участков CDR специфично связывающейся молекулы согласно настоящему изобретению по меньшей мере на 70% идентична аминокислотным последовательностям CDR, описанным выше, при анализе с использованием параметров по умолчанию компьютерной программы BLAST (Atschul et al., J. Mol. Biol. 215, 403-410 (1990)), предоставленной HGMP (Human Genome Mapping Project), на аминокислотном уровне. Как правило, каждая из последовательностей CDR имеет по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или по меньшей мере 99% идентичности на уровне аминокислот с последовательностями, приведенными выше. Как правило, каждая из последовательностей CDR специфично связывающейся молекулы согласно настоящему изобретению имеет уровень идентичности аминокислотной последовательности CDR, как указано выше. Кроме того, любой 1, 2, 3 4 или 5 из участков CDR специфично связывающейся молекулы согласно настоящему изобретению имеет такой уровень идентичности аминокислотных последовательностей CDR, как указано выше.
Специфично связывающаяся молекула согласно настоящему изобретению, как правило, представляет собой антитело, в большинстве случаев, моноклональное антитело. В одном варианте реализации моноклональное антитело согласно настоящему изобретению является гуманизированным.
Моноклональное антитело согласно настоящему изобретению может быть гуманизировано за счет модификации его аминокислотной последовательности. Способы уменьшения иммуногенности специфично связывающихся молекул настоящего изобретения могут включать пересадку CDR на каркасную часть подходящего антитела или ремоделирование остатков поверхности вариабельной области, например, за счет сайт-направленного мутагенеза и других стандартно используемых технологий молекулярной биологии (Roguska et al Protein Eng. 9895-904 (1996)).
Другие применимые способы включают идентификацию возможных эпитопов для Т-клеток в составе молекулы и их последующее удаление, например, с помощью сайт-направленного мутагенеза (деиммунизация). Если предполагается применять специфично связывающуюся молекулу в качестве терапевтического средства, может потребоваться ее гуманизация. Если необходимо, можно провести гуманизацию участков CDR или окружающей их каркасной последовательности.
Существуют технологии рекомбинантной ДНК, позволяющие на основе моноклональных и других антител получать другие антитела или химерные молекулы, которые сохраняют специфичность исходного антитела. Такие способы могут включать присоединение ДНК, кодирующей вариабельную область иммуноглобулина или гипервариабельный участок (CDR) антитела к константным областям или к константным областям вместе с каркасными участками других иммуноглобулинов. См., например, ЕР-А-184187, GB 2188638 А или ЕР-А-239400. Гибридому или другие клетки, продуцирующие антитела, можно подвергнуть генетической мутации или другим изменениям, которые могут изменять или могут не изменять специфичность связывания продуцируемых антител.
Поскольку антитела могут быть модифицированы различными способами, термин «антитело» должен охватывать любые специфично связывающиеся молекулу или вещество, имеющие связывающий домен с требуемой специфичностью. Таким образом, этот термин охватывает фрагменты антитела, производные, функциональные эквиваленты и гомологи антител, гуманизированные антитела, в том числе любой полипептид, содержащий связывающий домен иммуноглобулина, либо природные, либо полностью или частично синтетические. Таким образом, в объем данного термина также входят химерные молекулы, содержащие связывающий домен иммуноглобулина, или его эквивалент, «слитый» с другим полипептидом. Клонирование и экспрессия химерных антител описаны в патентах ЕР-А-0120694 и ЕР-А-0125023. Гуманизированное антитело может представлять собой модифицированное антитело, имеющее вариабельные области нечеловеческого, например мышиного антитела, и константную область человеческого антитела. Способы получения гуманизированных антител описаны, например, в патенте США №5225539.
Специфично связывающаяся молекула согласно настоящему изобретению может представлять собой фрагмент антитела. Было показано, что фрагменты целого антитела могут выполнять функцию связывания антигенов. Примерами связывающихся фрагментов являются (I) Fab-фрагмент, состоящий из доменов VL, VH, CL и CH1; (II) Fd-фрагмент, состоящий из доменов VH и CH1; (III) Fv-фрагмент, состоящий из областей VL и VH одного антитела; (IV) фрагмент dAb (Ward, E.S. et al, Nature 341:544-546 (1989)), который состоит из домена VH; (V) изолированные участки CDR; (VI) Р(ab')2-фрагменты, бивалентный фрагмент, состоящий из двух связанных Fab-фрагментов, (VII) одноцепочечные молекулы Fv (scFv), в которых домен VH и домен VL связаны между собой пептидным линкером, благодаря которому два домена ассоциируют с образованием сайта связывания антигена (Bird et al., Science 242:423-426 (1988); Huston et al., PNAS USA 85:5879-5883 (1988)); (VIII) биспецифичные одноцепочечные димеры Fv (PCT/US 92/09965) и (IX) «диатела», мультивалентные или мультиспецифичные фрагменты, сконструированные в результате «слияния» генов (WO 94/13804; P. Hollinger et al., Proc. Natl. Acad. Sci. USA 90: 6444-6448 (1993)). Как правило, фрагмент представляет собой Fab-фрагмент, F(ab')2- или Fv-фрагмент или молекулу scFv.
Диатела представляют собой мультимеры полипептидов, каждый из которых содержит первый домен, содержащий связывающую область легкой цепи иммуноглобулина и второй домен, содержащий связывающую область тяжелой цепи иммуноглобулина, при этом эти два домена связаны (например, посредством пептидного линкера), но не способны ассоциировать друг с другом с образованием антигенсвязывающего сайта: антигенсвязывающий сайт образуются в результате ассоциации первого домена одного полипептида в составе мультимера со вторым доменом другого полипептида в составе такого мультимера (WO 94/13804).
В случае применения биспецифичных антител они могут представлять собой обычные биспецифичные антитела, которые могут быть получены различными способами (Hollinger & Winter, Current Opinion Biotechnol. 4:446-449 (1993)), например получены химическим способом или от гибридных гибридом, или могут представлять собой любой из биспецифичных фрагментов антител, упомянутых выше. Может быть предпочтительно применение димеров scFv или диател, а не целых антител. Диатела и scFv могут быть сконструированы без области Fc, с применением только вариабельных доменов, что потенциально снижает эффект анти-идиотипических реакций. Другие формы биспецифичных антител включают одноцепочечные «Янусины» (Janusins), описанные в работе Traunecker et al., EMBO Journal 10:3655-3659 (1991).
Также можно применять биспецифичные диатела, в противоположность биспецифичным целым антителам, поскольку их легко можно сконструировать и экспрессировать в E. coli. Диатела (и многие другие полипептиды, такие как фрагменты антител) с соответствующей специфичностью связывания можно легко отобрать из библиотек с помощью фагового дисплея (WO 94/13804). Если одна ветвь диатела должна оставаться постоянной, например со специфичностью, направленной против антигена X, то можно создать библиотеку, в которой варьируют другую ветвь, и осуществить селекцию антитела с соответствующей специфичностью.
Моноклональное антитело VJ-4B6 продуцируется клеточной линией гибридомы VJ-4B6-E5-B10-D4, депонированной 3 июня 2010 года в Европейской коллекции клеточных культур (ЕСАСС), Агентство по охране здоровья, Центр аварийной готовности и реагирования, Портон, Солсбери, SP4 0JG, Соединенное Королевство, в соответствии с Будапештским договором, под номером доступа 10060301.
Депонирование было осуществлено Фульвио Д'Аквисто (Fulvio D'Acquisto, Queen Магу and Westfield College, Centre for Biochemical Pharmacology, Charterhouse Square, London EC1M 6BQ). Депозитор уполномочил Заявителя сослаться на депонированный материал в настоящей заявке и дал свое безоговорочное и безотзывное согласие на то, чтобы депонированный материал стал доступным для общественности в соответствии с Правилом 31 (l)(d) Европейской патентной конвенции.
Клеточная линия гибридомы VJ-4B6-E5-B10-D4 продуцирует моноклональные антитела VJ-4B6, которые специфично связываются с Аннексином-А1. Моноклональные антитела VJ-4B6 согласно настоящему изобретению относятся к изотипу IgG2b.
Антитело VJ-4B6 было получено против полноразмерного белка Anx-А1 человека, имеющего аминокислотную последовательность, приведенную на Фигуре 2А.
Последовательность ДНК и аминокислотная последовательность вариабельной области легкой цепи антитела VJ-4B6 приведена на Фигуре 11. На Фигуре 12 показана аминокислотная последовательность вариабельной области легкой цепи VJ-4B6 с обозначенными участками CDR. На Фигуре 12 также показаны несколько первых аминокислот константной области легкой цепи VJ-4BO.
Последовательность ДНК и аминокислотная последовательность вариабельной области тяжелой цепи антитела VJ-4B6 приведена на Фигуре 13. На Фигуре 14 приведена последовательность аминокислот вариабельной области тяжелой цепи из VJ-4B6 с обозначенными участками CDR. На Фигуре 14 также показаны несколько первых аминокислот константной области тяжелой цепи VJ-4B6.
Гипервариабельные участки (CDR) антитела VJ-4B6 являются следующими:
VLCDR1 представляет собой KASENVVTYVS,
VLCDR2 представляет собой GASNRYT,
VLCDR3 представляет собой GQGYSYPYT,
VHCDR1 представляет собой GYTFTNYWIG,
VHCDR2 представляет собой DIYPGGDYTNYNEKFKG,
VHCDR3 представляет собой WGLGYYFDY.
Настоящее изобретение охватывает специфично связывающиеся молекулы, которые имеют участки CDR антитела VJ-4B6, как описано в настоящей заявке, а также специфично связывающиеся молекулы, которые имеют CDR, по меньшей мере на 70% идентичные одному или более CDR антитела VJ-4B6, как описано в настоящей заявке.
Настоящее изобретение также охватывает специфично связывающие молекулы, которые имеют либо вариабельную область легкой цепи, вариабельную область тяжелой цепи, или как вариабельную область легкой цепи, так и вариабельную область тяжелой цепи антитела VJ-4B6.
Таким образом, в конкретном варианте реализации настоящее изобретение обеспечивает специфично связывающиеся молекулы в соответствии с первым аспектом изобретения, включающие полипептид, имеющий аминокислотную последовательность, приведенную на Фигуре 11 и/или Фигуре 13.
В этом варианте реализации настоящее изобретение также охватывает некоторые фрагменты антител, включающие вариабельную область легкой цепи, которая имеет аминокислотную последовательность, показанную на Фигуре 11, и/или вариабельную область тяжелой цепи с аминокислотной последовательностью, показанной на Фигуре 13. Например, этот вариант реализации охватывает фрагменты Fab, F(ab')2 или Fv и молекулы scFv.
Настоящее изобретение также охватывает специфично связывающиеся молекулы в соответствии с первым аспектом настоящего изобретения, включающие полипептид, имеющий последовательность аминокислот, как показано на Фигуре 12 и/или Фигуре 14.
В конкретном варианте реализации настоящее изобретение обеспечивает специфично связывающуюся молекулу в соответствии с первым аспектом настоящего изобретения, продуцируемую клеточной линией гибридомы, депонированной в Европейской коллекции клеточных культур (ЕСАСС) 3 июня 2010 года под номером 10060301.
Во втором аспекте настоящее изобретение относится к клеточной линии гибридомы, которая продуцирует специфично связывающуюся молекулу, направленную против белка Anx-А1 человека, имеющую аминокислотную последовательность, приведенную на Фигуре 2А.
В конкретном варианте реализации настоящее изобретение относится к клеточной линии гибридомы в соответствии со вторым аспектом настоящего изобретения, депонированной в Европейской коллекции клеточных культур (ЕСАСС) 3 июня 2010 года полномером 10060301.
В третьем своем аспекте настоящее изобретение относится к фармацевтической композиции, содержащей специфично связывающуюся молекулу согласно настоящему изобретению.
Композиция в соответствии с этим аспектом изобретения может быть приготовлена для применения любым удобным способом. Фармацевтическая композиция согласно настоящему изобретению наряду со специфично связывающейся молекулой согласно настоящему изобретению обычно содержит фармацевтически приемлемый носитель, эксципиент, разбавитель, адъювант, наполнитель, буфер или стабилизатор. Такие носители включают, но не ограничены перечисленными, физиологический раствор, буферный раствор, декстрозу, липосомы, воду, глицерин, полиэтиленгликоль, этанол и их комбинации. Такой фармакологический препарат может быть в любой приемлемой форме, в зависимости от желаемого способа введения ее пациенту.
Фармацевтическая композиция может быть обеспечена в единичной дозированной форме, как правило, представленной в запечатанном контейнере, и может представлять собой часть набора. Такой набор, как правило (хотя и необязательно), включает инструкции по применению. Он может включать в себя некоторое количество указанных лекарственных форм.
Фармацевтическая композиция может быть адаптирована для введения любым подходящим способом, например путем перорального (в том числе буккального или подъязычного), ректального, назального, местного (в том числе буккального, подъязычного или трансдермального), вагинального или парентерального (в том числе подкожного, внутримышечного, внутривенного или внутрикожного) способа. Такие фармакологические препараты могут быть получены любым способом, известным в области фармацевтики, например путем смешивания активного ингредиента с носителем (носителями) или наполнителем (наполнителями) в стерильных условиях.
Фармацевтические композиции, адаптированные для перорального введения могут быть представлены в виде отдельных форм, таких как капсулы или таблетки; в виде порошков или гранул, в виде растворов, сиропов или суспензий (в водных или неводных жидкостях; или как съедобная пена, крем или эмульсия).
Подходящие эксципиенты для таблеток или твердых желатиновых капсул включают лактозу, кукурузный крахмал или его производные, стеариновую кислоту или ее соли.
Подходящие эксципиенты для применения в мягких желатиновых капсулах включают, например, растительные масла, воск, жиры, полутвердые или жидкие полиолы и т.п.
Эксципиенты, которые можно использовать для приготовления растворов и сиропов, включают, например, воду, полиолы и сахара. Для приготовления суспензий можно применять масла (например, растительные масла) (для получения суспензии масла в воде или воды в масле).
Фармацевтические композиции, адаптированные для трансдермального приема, могут быть представлены в виде отдельных пластырей, предназначенных для того, чтобы оставаться в тесном контакте с эпидермисом реципиента в течение продолжительного периода времени. Например, активный ингредиент может доставляться из пластыря через ионтофорез, как в целом описано в журнале «Фармакологические исследования» (Pharmaceutical Research, 3(6):318 (1986)).
Фармакологические препараты, адаптированные для местного приема, могут быть представлены в виде мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел. Для инфекций глаза или других наружных тканей, например полости рта и кожи, предпочтительно локальное применение препаратов в виде мази или крема. Если активный ингредиент входит в состав мази, его можно применять с парафиновой или водорастворимой мазевой основой. В качестве альтернативы, активный ингредиент может входить в состав крема с кремовой основой в виде масла в воде или воды в масле. Фармакологические препараты, адаптированные для местной доставки в глаза, включают глазные капли, в которых активный ингредиент растворен или суспендирован в подходящем переносчике, главным образом - в водном растворителе. Фармакологические препараты, адаптированные для местной доставки в ротовую полость включают леденцы, пастилки и бальзамы для полости рта.
Фармакологические препараты, предназначенные для ректального приема, могут быть представлены в виде свечей или клизм.
Фармакологические препараты, предназначенные для приема назально с твердым носителем, включают крупнозернистый порошок, имеющий размер частиц, например, от 20 до 500 микрон, который принимается так же, как нюхательный табак, т.е. за счет быстрого вдыхания через носовые ходы порошка из контейнера, который подносят к носу. Подходящие препараты, в которых носитель является жидким, для приема в виде назального спрея или назальных капель, включают водные или масляные растворы активного ингредиента.
Фармакологические препараты, адаптированные для приема через ингаляцию, включают пудру или аэрозоли, которые могут генерироваться с помощью разнообразных типов герметичных дозированных аэрозолей, распылителей или инжекторов.
Фармакологические препараты, адаптированные для вагинальной доставки, могут быть представлены в виде маточных колец, тампонов, кремов, гелей, паст, пен или спреев.
Фармакологические препараты, адаптированные для парентеральной доставки включают водные или неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатические факторы и растворы, которые делают препарат по существу изотоничным крови предполагаемого реципиента; а также водные или неводные стерильные суспензии, которые могут включать суспензирующие агенты и загустители. Эксципиенты, которые могут быть использованы в растворах для инъекций, включают, в частности, воду, спирты, полиолы, глицерин и растительные масла. Препараты могут быть представлены в виде единичных доз или многодозовых контейнеров, например, запаянных ампул и бутылочек, и могут храниться в условиях сухой заморозки (лиофилизации); в этом случае требуется лишь добавить стерильный жидкий носитель, например, воду для инъекций, непосредственно перед применением. Растворы и суспензии инъекций для немедленного приема могут быть приготовлены из стерильных порошков, гранул и таблеток.
Фармакологические препараты могут содержать консервирующие, солюбилизирующие, смачивающие вещества, эмульгаторы, подстастители, красители, ароматизаторы, соли, (вещества согласно настоящему изобретению могут сами быть предоставлены в форме фармацевтически приемлемой соли), буферы, вещества для оболочки или антиоксиданты.
Фармацевтические композиции согласно настоящему изобретению могут также содержать один или более других терапевтически активный агент в дополнение к молекуле согласно настоящему изобретению.
В некоторых вариантах реализации активный концентрат препарата может содержать фармацевтически приемлемый агент, регулирующий тоничность, буферный агент и фармацевтически приемлемое поверхностно-активное вещество.
Кроме того, препарат может содержать активный ингредиент вместе с фосфатом натрия, однозамещенным, двузамещенным фосфатом натрия, хлоридом натрия, полисорбатом 80 или полисорбатом 20 (поверхностно-активное вещество для минимизации риска агрегации, вызванной встряхиванием) и водой (USP/Ph.Eur), при этом значение рН может составлять от 6,0 до 7,0, например около 6,5.
Активный концентрат препарата может быть лиофилизирован или может быть не лиофилизирован.
Другие препараты могут содержать ацетат натрия тригидрат в качестве буферного агента, хлорид натрия в качестве модификатора тоничности, уксусную кислоту для подведения рН и воду для инъекций.
Дозировка препарата согласно настоящему изобретению может варьировать в широком пределе, в зависимости от заболевания или расстройства, подлежащего лечению, возраста и состояния человека, подлежащего лечению, и т.д., и в конечном счете врач определяет необходимую для применения дозу.
Дозирование можно повторять так часто, как необходимо. Если развиваются побочные эффекты, количество или частоту приемов можно уменьшать, в соответствии с обычной клинической практикой.
При назначении млекопитающему, в частности человеку, ожидается, что дневная доза активного вещества будет составлять от 1 мкг/кг веса до 10 мг/кг веса, обычно около 10 мкг - 1 мг на 1 кг веса. В любом случае, врач определяет необходимую дозу, которая лучше всего подходит для данного индивидуума и которая зависит от возраста, веса, пола и индивидуального ответа. Дозы, представленные выше, являются характерными для среднего случая. Конечно же, возможны случаи, когда необходимы большие или меньшие дозы, и такие случаи также охвачены настоящим изобретением.
Специфично связывающуюся молекулу настоящего изобретения можно применять в медицине, например, для лечения заболеваний, опосредованных Т-клетками.
В четвертом аспекте настоящее изобретение обеспечивает специфично связывающуюся молекулу согласно настоящему изобретению для применения в медицине.
В пятом своем аспекте настоящее изобретение обеспечивает специфично связывающуюся молекулу согласно настоящему изобретению для применения при лечении заболеваний, опосредованных Т-клетками. В этом аспекте настоящее изобретение также включает способ лечения заболевания, опосредованного Т-клетками, у субъекта, как правило, субъекта, нуждающегося в таком лечении, такой способ включает введение указанному субъекту специфично связывающейся молекулы согласно настоящему изобретению. Таким образом, настоящее изобретение также охватывает применение специфично связывающейся молекулы настоящего изобретения в производстве лекарственного средства для применения при лечении заболевания, опосредованного Т-клетками заболеваний, или, как альтернатива, применение специфично связывающейся молекулы согласно настоящему изобретению в производстве лекарственного средства для лечения заболевания, опосредованного Т-клетками. Указанный способ лечения может быть предназначен для человека или животного, и настоящее изобретение в равной степени распространяется на применение для человека и/или в области ветеринарии. Специфично связывающуюся молекулу согласно настоящему изобретению предпочтительно вводят индивидууму в «терапевтически эффективном количестве», которое является достаточным для оказания благоприятного эффекта на указанного индивидуума. При использовании в настоящей заявке «лечение» включает любой режим, который может принести пользу человеку или животному, отличному от человека, предпочтительно млекопитающему. Лечение может быть направлено на существующее патологическое состояние или может быть профилактическим (предупреждающее лечение).
В этом аспекте настоящего изобретения специфично связывающуюся молекулу согласно настоящему изобретению можно применять для лечения широкого спектра заболеваний, опосредованных Т-клетками. В данном контексте «заболевание, опосредованное Т-клетками» обозначает любое заболевание или патологическое состояние, в патогенезе и развитии которого Т-клетки играют некоторую роль. Заболевания, опосредованные Т-клетками, как правило, вызваны аберрантной активацией Т-клеток. Соответственно, такие заболевания можно лечить, предотвращая активацию Т-клеток, путем блокирования активности Anx-А1, что, как показано в настоящей заявке, может быть осуществлено с помощью моноклональных антител VJ-4B6. Как правило, заболевания, опосредованные Т-клетками, подлежащие лечению в соответствии с настоящим изобретением, представляют собой заболевания, в которые вовлечены клетки Тh1.
Заболевания, опосредованные Т-клетками, включают, но не ограничены перечисленными, заболевание «трансплантат против хозяина», отторжение трансплантата, атеросклероз, ВИЧ и/или СПИД, псориаз и некоторые аутоиммунные заболевания. Аутоиммунные заболевания, которые можно лечить согласно настоящему изобретению, включают ревматоидный артрит (РА), рассеянный склероз (PC), системную красную волчанку (СКВ), болезнь Аддисона, болезнь Грейвса (базедову болезнь), склеродермию, полимиозит, некоторые формы сахарного диабета (например, ювенильный диабет), аутоиммунный увеоретинит, язвенный колит, обыкновенную пузырчатку, воспалительную болезнь кишечника, аутоиммунный тиреоидит, увеит, болезнь Бехчета и синдром Шегрена. Типичные заболевания, опосредованные Т-клетками - это ревматоидный артрит, рассеянный склероз, системная красная волчанка или атеросклероз, ВИЧ, СПИД или псориаз. Наиболее типичное заболевание, опосредованное Т-клетками - это ревматоидный артрит или рассеянный склероз.
Заболевания, опосредованные Т-клетками, как определено в настоящей заявке, также включают выкидыш. Как оговорено в настоящей заявке, лечение может быть профилактическим (предупреждающее лечение). Специфично связывающуюся молекулу настоящего изобретение можно применять для предотвращения выкидыша. Неконтролируемой ответ Th1-клеток, как известно, вовлечен в выкидыш, и увеличение ответа Th2-клеток способствует благоприятному течению беременности.
Типичное заболевание, опосредованное Т-клетками представляет собой ревматоидный артрит. Считается, что при ревматоидном артрите (РА) Т-клетки распознают и взаимодействуют с антиген-презентирующими клетками в синовиальной оболочке. Будучи активированными, эти клетки продуцируют цитокины и эффекторные молекулы; эта последовательная, расширяющаяся продукция цитокинов составляет «цитокиновый каскад», который приводит к активации макрофагов и индукции воспалительного процесса, итогом которого является деградация и резорбция хрящей и костей. С течением времени может происходить эрозия костей, разрушение хряща и полная потеря целостности сустава. В конечном счете, могут быть поражены многие системы органов.
В другом варианте реализации заболевание, опосредованное Т-клетками, представляет собой рассеянный склероз (PC).
В другом варианте реализации типичным заболеванием, опосредованным Т-клетками, является атеросклероз. Воспаление играет ключевую роль в заболевании коронарной артерии и других проявлениях атеросклероза. Клетки иммунитета управляют ранними атеросклеротическими повреждениями; их эффекторные молекулы ускоряют развитие повреждений, а активация воспаления может вызвать острые коронарные синдромы. Приобретенный иммунитет также тесно связан с атерогенезом, поскольку было показано, что он взаимодействует с метаболическими факторами риска, вызывая, распространяя и активируя повреждения в артериальном дереве.
В другом варианте реализации в качестве заболевания, опосредованного Т-клетками, выступает системная красная волчанка (СКВ).
Настоящее изобретение можно также применять в связи со способностью Anx-А1 стимулировать дифференцировку клеток Th, например, для ограничения неконтролируемых защитных клеточных (Th) ответов, направленных против внутриклеточных патогенов и для лечения внеклеточных инфекций (ответ Th2) за счет подавления дифференцировки Тh1 и стимуляции дифференцировки Th2.
Предпочтительные признаки указанных второго и последующих аспектов настоящего изобретения, являются такими же, как для первого аспекта, с Соответствующими изменениями.
В одном варианте реализации настоящее изобретение обеспечивает специфично связывающиеся молекулы, полученные против полноразмерного белка Anx-А1 человека, имеющего аминокислотную последовательность, приведенную на Фигуре 2А.
Одним из примеров такой специфично связывающейся молекулы является моноклональное антитело VJ-4B6, продуцируемое клеточной линией гибридомы, депонированной в Европейской коллекции клеточных культур (ЕСАСС) 3 июня 2010 года под номером доступа 10060301.
В одном варианте реализации настоящее изобретение обеспечивает специфично связывающуюся молекулу, которая имеет гипервариабельные участки (CDR) моноклонального антитела VJ-4B6, которое имеет следующие аминокислотные последовательности:
VLCDR1 представляет собой KASENVVTYVS,
VLCDR2 представляет собой GASNRYT,
VLCDR3 представляет собой GQGYSYPY,T
VHCDR1 в GYTFTNYWIG,
VHCDR2 в DIYPGGDYTNYNEKFKG,
VHCDR3 представляет собой WGLGYYFDY.
В одном из вариантов реализации настоящее изобретение обеспечивает специфично связывающуюся молекулу, имеющую области VH и/или VL от моноклонального антитела VJ-4B6, которые приведены на Фигурах 11 и 13, соответственно.
В одном варианте реализации настоящее изобретение относится к клеточной линии гибридомы VJ-4B6-E5-B10-D4, депонированной в Европейской коллекции клеточных культур (ЕСАСС) 3 июня 2010 года под номером доступа 10060301.
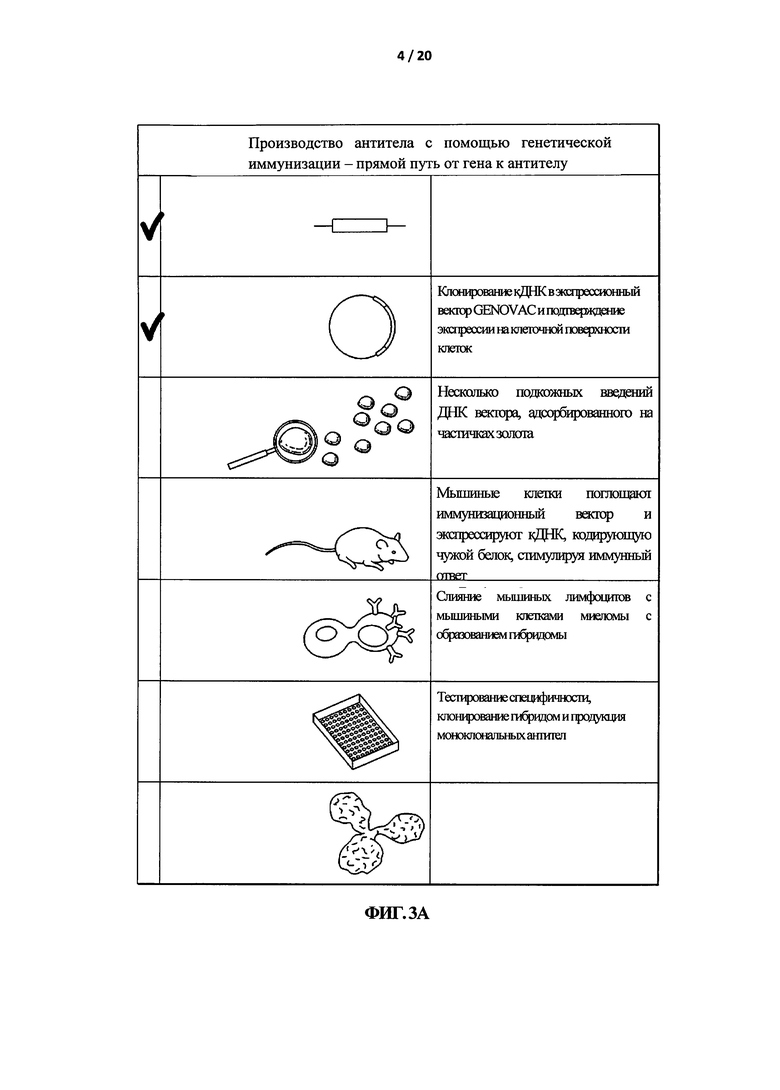
Моноклональное антитело VJ-4B6 продуцируется согласно способу, описанному на Фигуре 3А. Кратко, кДНК, кодирующую полноразмерный белок Anx-А1 человека, имеющий последовательности, приведенную на Фигуре 2А, клонировали в векторе для экспрессии и подтверждали экспрессию белка на клеточной поверхности. Мышам осуществляли несколько раз внутрикожное введение векторной ДНК, адсорбированной на частицах золота. Мышиные клетки поглощали вектор для иммунизации и экспрессировали белок, кодируемой полученной кДНК, что стимулировало иммунный ответ. Мышиные лимфоциты затем «сливали» с мышиными клетками миеломы для получения гибридом. Затем проводили тестирование на специфичность, гибридомы клонировали и продуцировали моноклональные антитела.
Таким образом, в подходе, применяемом для получения моноклонального антитела VJ-4B6, применяются клетки, траснфицированные кДНК Anx-А1, которые экспрессируют на своей поверхности его полную молекулу, и, таким образом, белок находится в той же форме, в какой он находится в природных, то есть в своей нативной четвертичной структуре. Этот подход к получению антител отличается от продукции других коммерчески доступных антител к Anx-А1, которые были получены путем иммунизации мышей пептидом Anx-А1 или денатурированным полноразмерным белком.
Антитело согласно настоящему изобретению, в частности, применимо в лечении заболеваний, опосредованных Т-клетками, таких как ревматоидный артрит и рассеянный склероз.
Настоящее изобретение в дальнейшем описано при помощи ссылок на последующие примеры и Фигуры, которые представлены в настоящей заявке лишь с целью иллюстрации. В Примерах даны ссылки на ряд Фигур, где:
Фигура 1А представляет собой ленточную диаграмму структуры Аннексина-1, демонстрирующую четыре аннексиновых повтора и N-концевой домен. Фигура 1В - это схема, показывающая аннекиновые повторы и локализацию биологически активной последовательности Аннексина-1, пептида Ас.2-26. На Фигуре 1С приведена аминокислотная последовательность пептида Ас.2-26, который является ацетилированным N-концевым пептидным фрагментом Anx-А1.
На Фигуре 2А приведена (i) аминокислотная последовательность и (и) нуклеотидная последовательность Аннексина-1 человека (Anx-А1), изоформы ANXA1-003. На Фигуре 2 В приведена аминокислотная последовательность Аннексина-1 человека (Anx-А1), изоформы ANXA1-002. На Фигуре 2С приведена аминокислотная последовательность Аннексина-1 человека (Anx-А1), изоформы ANXA1-004. На Фигуре 2D показана аминокислотная последовательность Аннексина-1 человека (Anx-A1), изоформы ANXA 1-006.
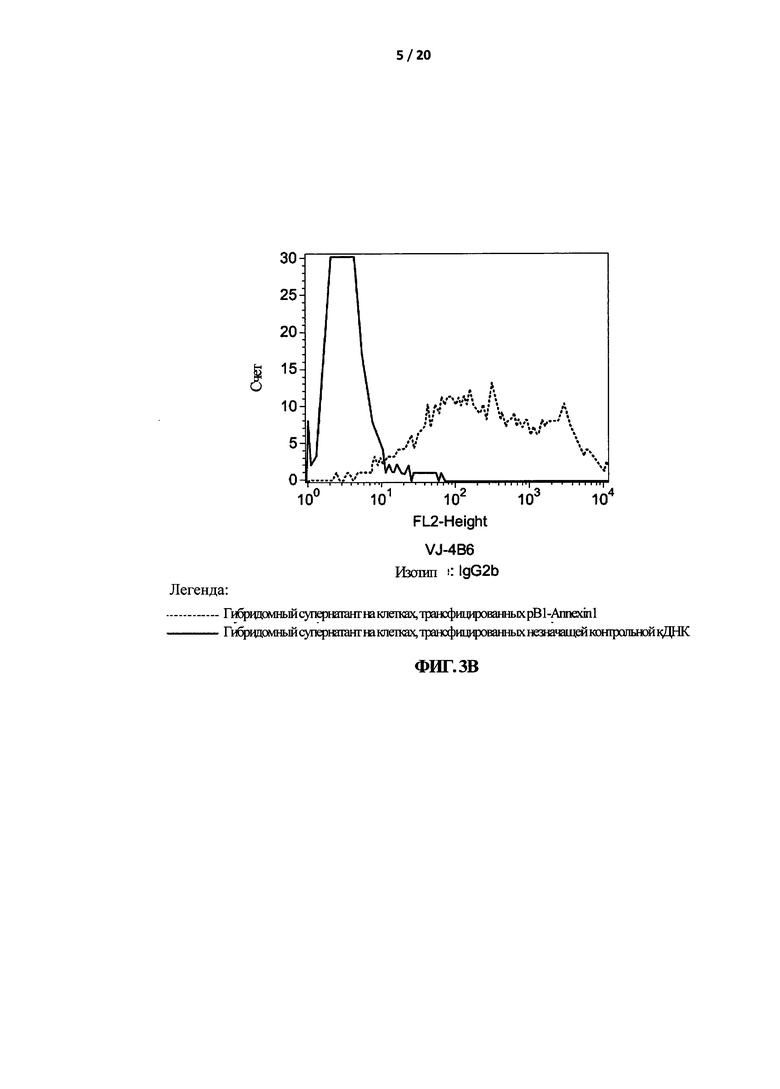
На Фигуре 3 показано получение VJ-4B6. (А) Схематическое изображение стратегии, используемой для изоляции и продукции VJ-4B6. (В) Гистограмма показывает окрашивание на VJ-4B6 клеточных линий, стабильно трансфицированных кДНК Аннексином-1 (зеленая линия; правый пик), или контрольной кДНК (красная линия, левый пик).
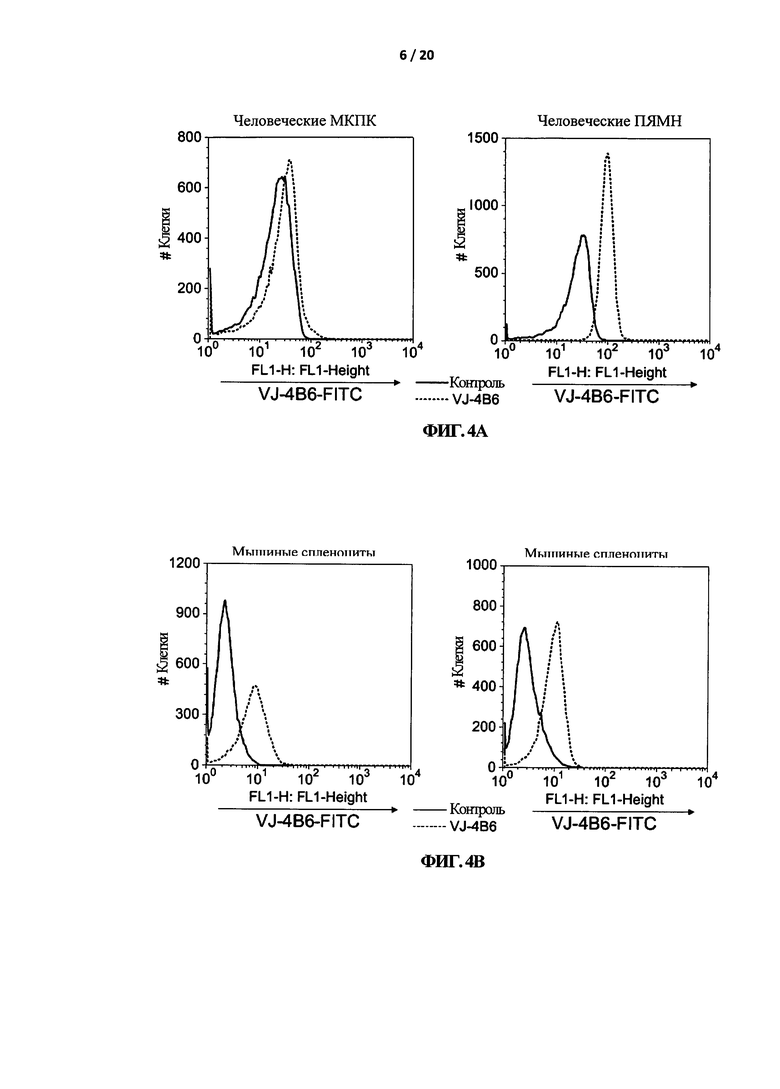
На Фигуре 4 показана проверка VJ-4B6. (А) Окрашивание пермеабилизированных мононуклеарных клеток периферической крови (МКПК) человека или полиморфно-ядерных мононуклеарных клеток (ПЯМН) с помощью VJ-4B6 (50 нг/мл). (В) Окрашивание пермеабилизованных мышиных спленоцитов или резидентных перитонеальных макрофагов с помощью VJ-4B6 (50 нг/мл). Во всех тестах клетки фиксировали 4% параформальдегидом, а затем пермеабилизировали с помощью 0,02% сапонина в буфере FACS. Клетки инкубировали с биотинилированным VJ-4B6 в течение ночи при 4°С, а затем окрашивали в течение 1 часа с помощью стрептавидин-FITC конъюгированных антител (разбавление 1:200). На всех графиках левый пик относится к контролю, а правый пик - к VJ-4B6. Приведенные данные взяты из одного эксперимента и являются репрезентативными для двух других экспериментов с аналогичными результатами.
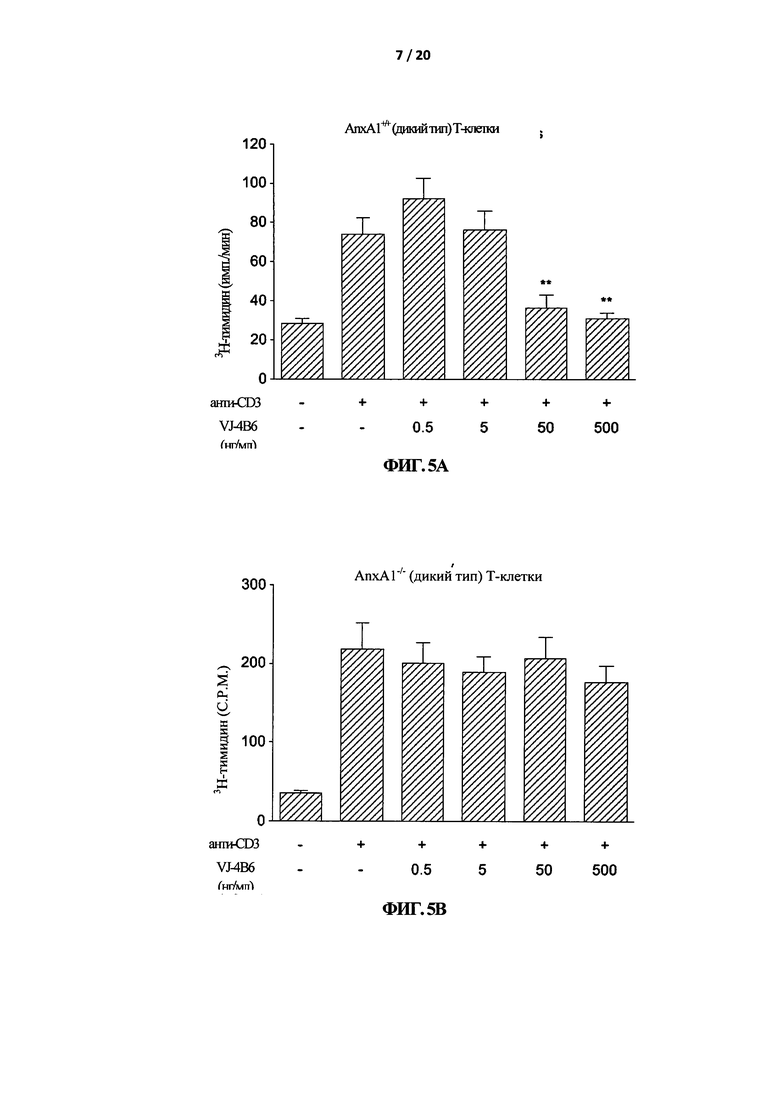
На Фигуре 5 показано, что VJ-4B6 ингибирует анти-CD3-индуцированную пролиферацию Т-клеток. Т-клетки из селезенки и лимфатических узлов мышей AnxA1 +/+ (А) и AnxA1 -/- (В) стимулировали с помощью антител к CD3 (анти-CD3), связанных с планшетом (1 мкг/мл) в присутствии указанных концентраций VJ-4B6. После 18-20 часов в клетки импульсно вводили 3Н-тимидин (1 мкКи) в течение 12 часов и затем обрабатывали с помощью коллектора клеток для измерения уровня 3Н-тимидина. Приведенные данные взяты из одного эксперимента и являются репрезентативными для двух других экспериментов с аналогичными результатами.
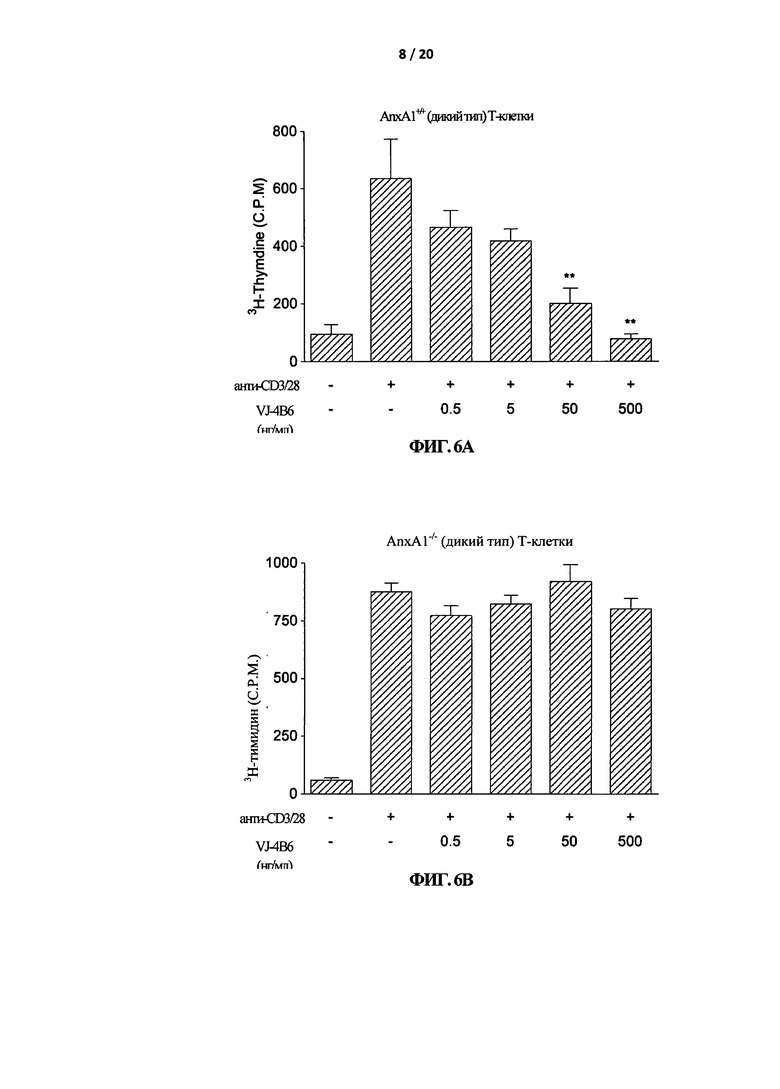
На Фигуре 6 показано, что VJ-4B6 ингибирует анти-CD3/СВ28-индуцированную пролиферации Т-клеток. Т-клетки из селезенки и лимфатических узлов мышей AnxA1 +/+ (А) и AnxA1 -/- (В) стимулировали с помощью связанных с планшетом антител к CD3 (анти-CD3) (1 мкг/мл) и антител к CD8 (анти-CD8) (1 мкг/мл) в присутствии указанных концентраций VJ-4B6. После 18-20 часов в клетки импульсно вводили 3Н-тимидин (1 мкКи) в течение 12 часов и затем обрабатывали с помощью коллектора клеток для измерения уровня 3Н-тимидина. Приведенные данные взяты из одного эксперимента и являются репрезентативными для двух других экспериментов с аналогичными результатами.
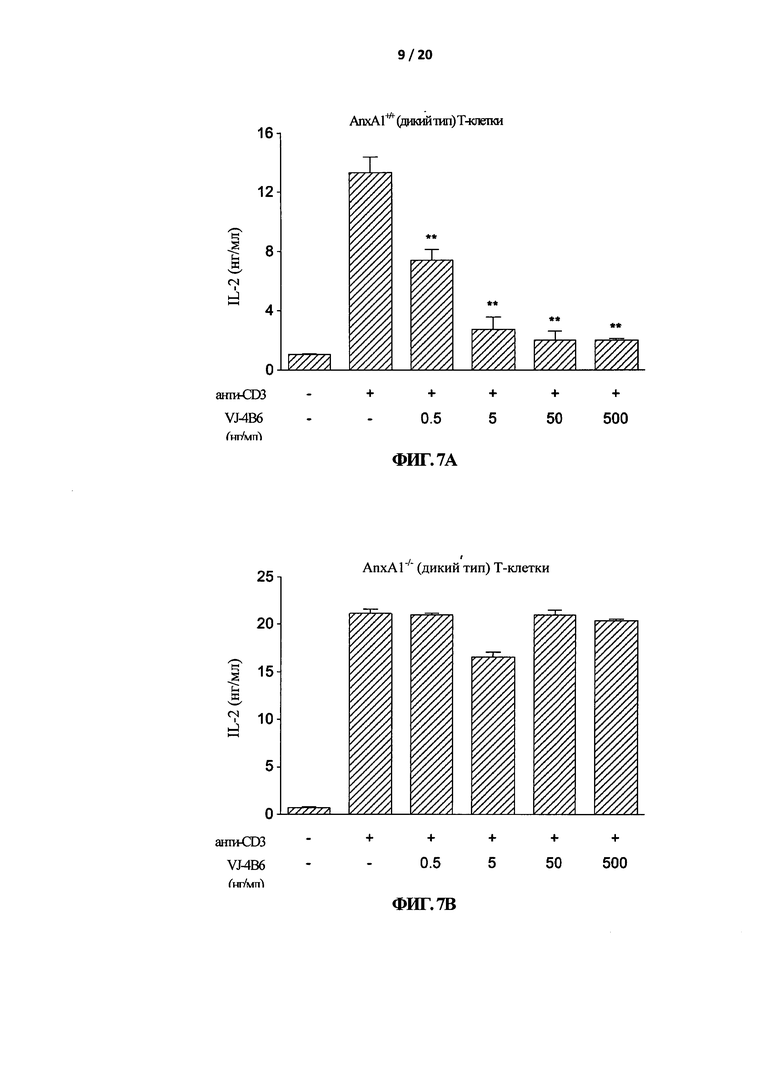
На Фигуре 7 показано, что VJ-4B6 ингибирует анти-CD3-индуцированную продукцию IL-2. Т-клетки из селезенки и лимфатических узлов мышей AnxA1 +/+ (А) и AnxA1 -/- (В) стимулировали с помощью антител к CD3 (анти-CD3), связанных с планшетом (1 мкг/мл) в присутствии указанных концентраций VJ-4B6. После 20-24 часов клеточные супернатанты собирали и анализировали в них уровень IL-2 способом ИФА. Приведенные данные взяты из одного эксперимента и являются репрезентативными для двух других экспериментов с аналогичными результатами.
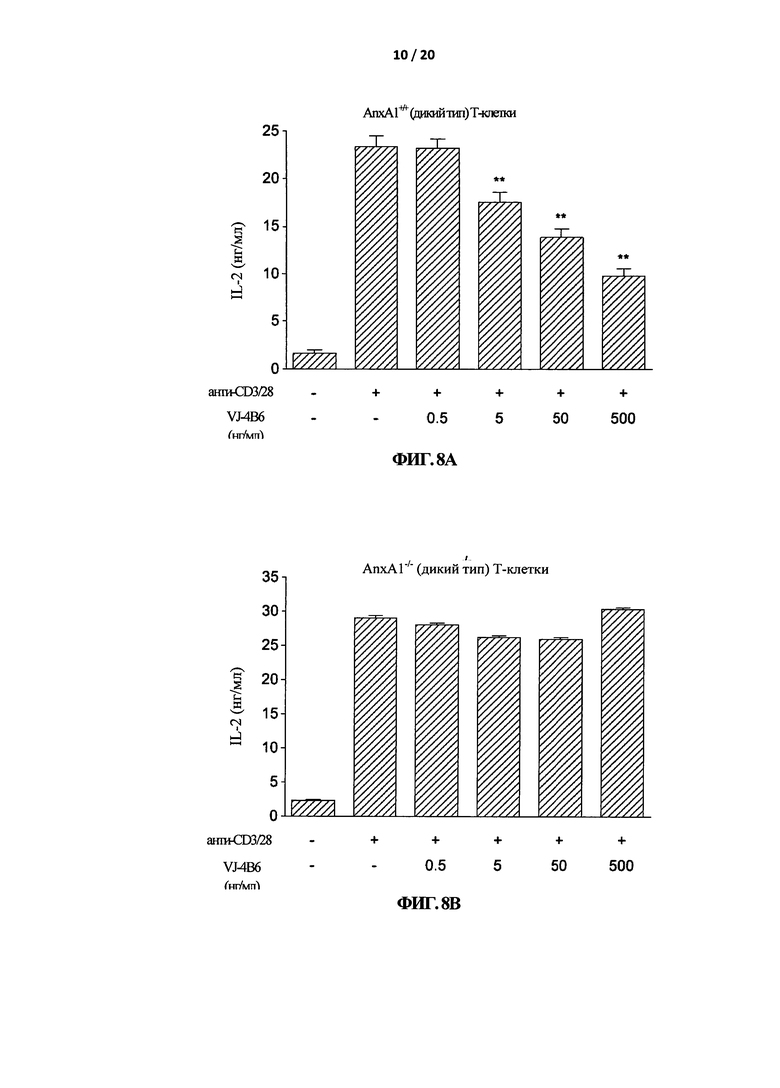
На Фигуре 8 показано, что VJ-4B6 тормозит анти-CD3/CD28-индуцированную продукцию IL-2. Т-клетки из селезенки и лимфатических узлов мышей AnxA1 +/+ (А) и AnxA1 -/- (В) стимулировали с помощью связанных с планшетом антител к CD3 (анти-CD3) (1 мкг/мл) и антител к CD28 (анти-CD28) (1 мкг/мл) в присутствии указанных концентраций VJ-4B6. После 20-24 часов клеточные супернатанты собирали, и анализировали в них уровень IL-2 способом ИФА. Приведенные данные взяты из одного эксперимента и являются репрезентативными для двух других экспериментов с аналогичными результатами.
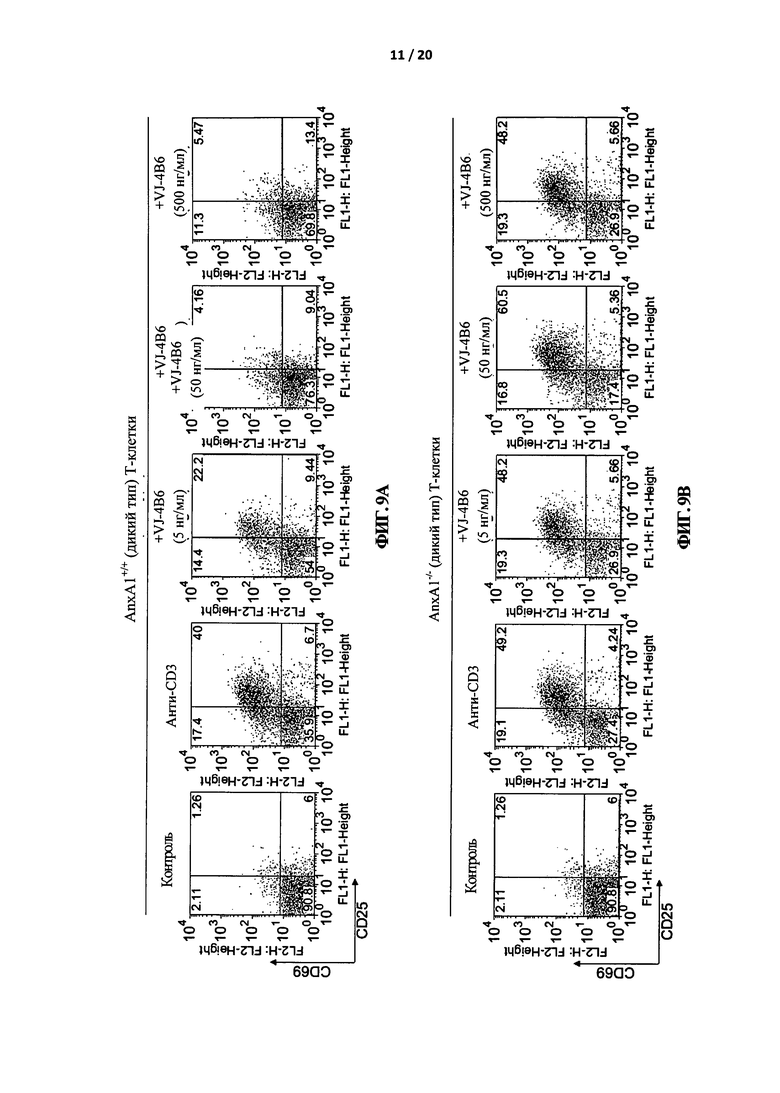
На Фигуре 9 показано, что VJ-4B6 ингибирует анти-CD3-индуцированную активацию CD25/CD69. Т-клетки из селезенки и лимфатических узлов мышей AnxA1 +/+ (А) и AnxA1 -/- (В) стимулировали с помощью антител к CD3 (анти-CD3), связанных с планшетом (1 мкг/мл) в присутствии указанных концентраций VJ-4B6. После 18-20 часов клетки собирали и окрашивали с помощью анти-CD25 с FITC вместе с анти-СБ69 РЕ. Образцы собирали с помощью FACSCalibur и анализировали с помощью программы FlowJo. Приведенные данные взяты из одного эксперимента и являются репрезентативными для двух других экспериментов с аналогичными результатами.
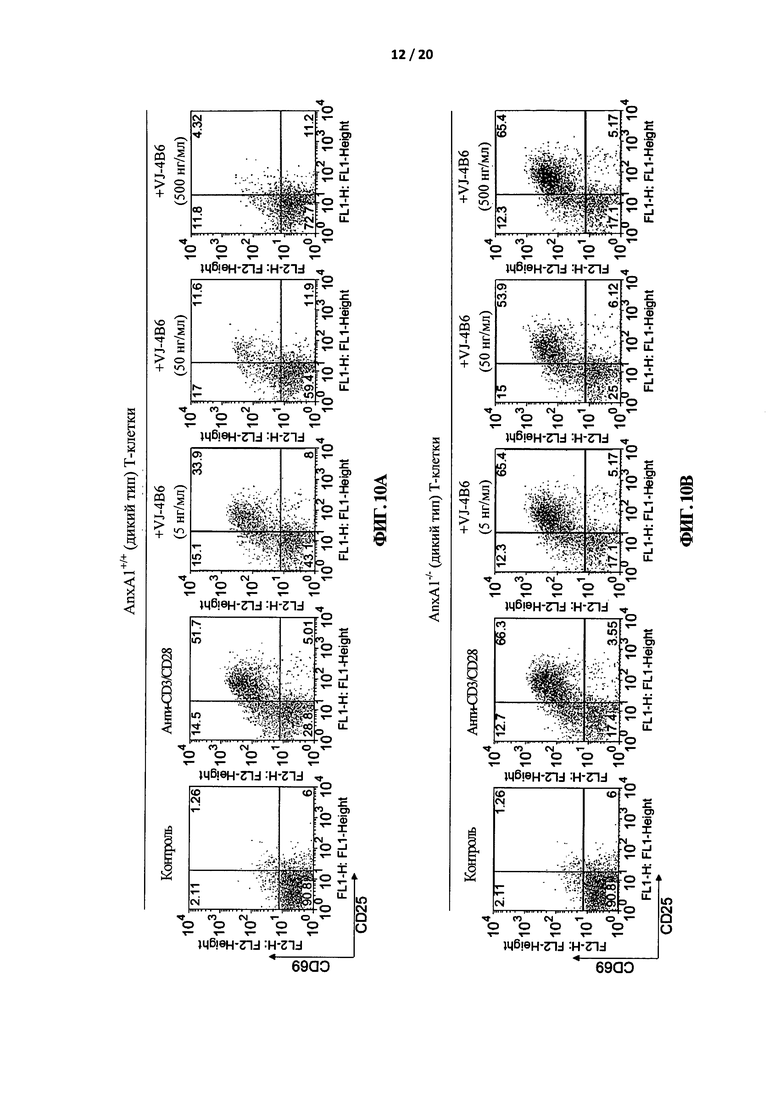
На Фигуре 10 показано, что VJ-4B6 ингибирует анти-CD3/CD28-индуцированную активацию CD25/CD69. Т-клетки из селезенки и лимфатических узлов мышей AnxA1 +/+ (А) и AnxA1 -/- (В) стимулировали с помощью связанных с планшетом антител к CD3 (анти-CD3) (1 мкг/мл) и антител к CD28 (анти-CD28) (1 мкг/мл) в присутствии указанных концентраций VJ-4B6. После 18-20 часов клетки собирали и окрашивали с помощью анти-CD25 с FITC вместе с анти-CD69 РЕ. Образцы собирали с помощью FACSCalibur и анализировали с помощью программы FlowJo. Приведенные данные взяты из одного эксперимента и являются репрезентативными для двух других экспериментов с аналогичными результатами.
На Фигуре 11 приведены последовательности ДНК и аминокислот вариабельной области легкой цепи VJ-4B6.
На Фигуре 12 приведена аминокислотная последовательность вариабельной области легкой цепи из VJ-4B6 с обозначенными участками CDR. Выделены CDR1, CDR2, CDR3 и начало константной области. Нумерация и порядок CDR даны в соответствии с определением Kabat.
На Фигуре 13 приведены последовательности ДНК и аминокислот последовательность вариабельной области тяжелой цепи VJ-4B6.
На Фигуре 14 приведена аминокислотная последовательность вариабельной области тяжелой цепи VJ-4B6 с обозначенными участками CDR. Выделены CDR1, CDR2, CDR3 и начало константной области. Нумерация и порядок CDR даны в соответствии с определением Kabat. В вариабельной области тяжелой цепи остатки с 26 по 29, хотя и не являются частью гипервариабельного участка в соответствии с определением Kabat, являются частью петли CDR в соответствии с определением Chothia (Chothia and Lesk, 1987). Положения во вставках 52, 52а, 82, 82а, 82b, 82с, 100 и 100а обозначены как 52а, 82abc, 100а.
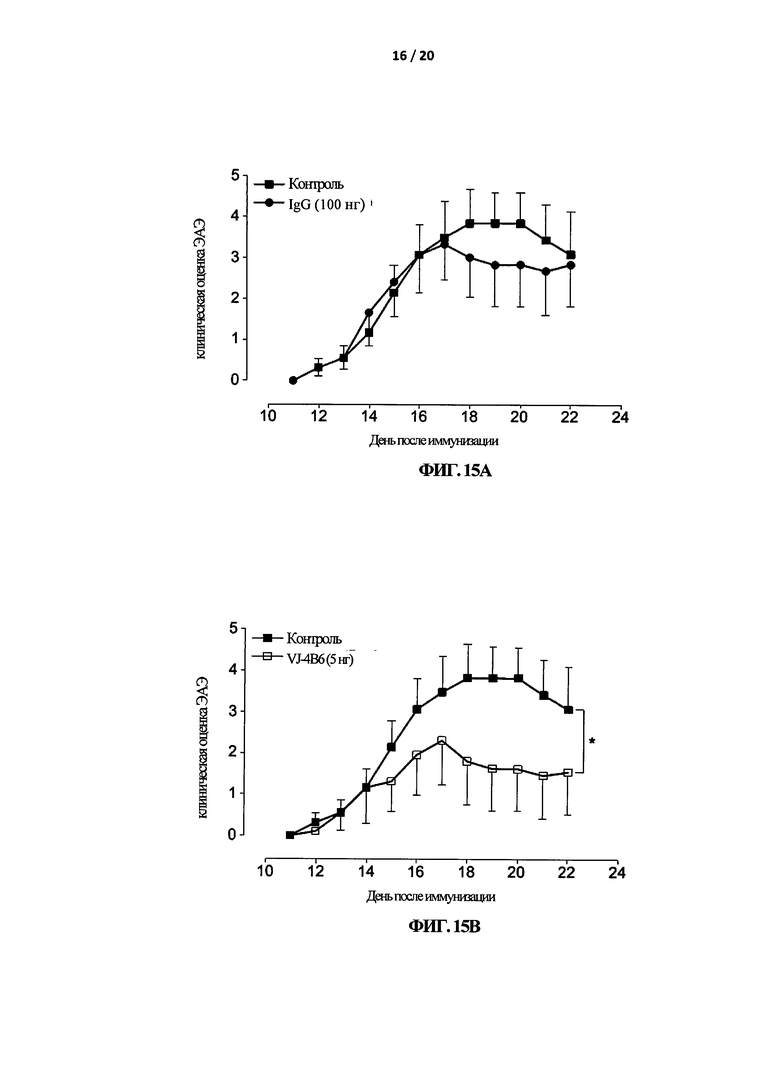
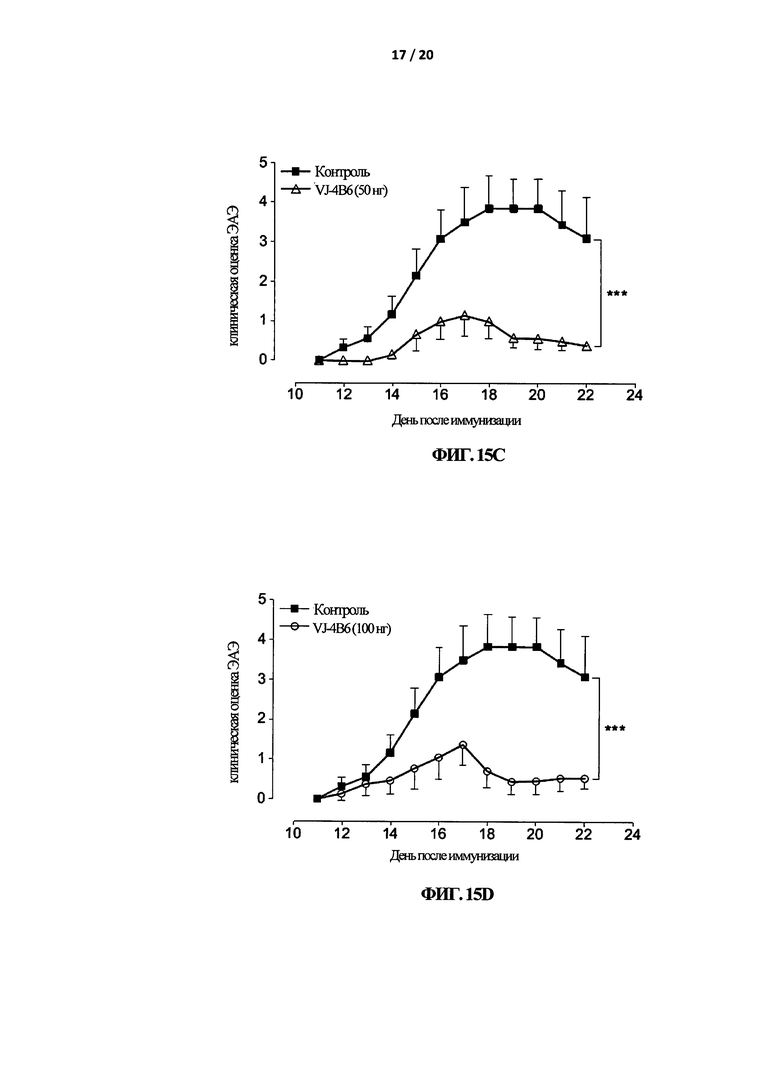
На Фигуре 15 показано, что VJ-4B6 ингибирует развитие ЭАЭ. Мышей C57BL/6 иммунизировали MOG35-55 в CFA и ежедневно наблюдали за признаками ЭАЭ в течение 22 дней. На 6-й день после иммунизации мыши получали и.п. инъекцию 100 нг IgG (А) или 5 (В), 50 (С), 100 ng (D) VJ-4B6 (в 100 мкл ФСБ) каждые шесть дней. Результаты представляют собой средние значения ± СОС (n=6/группа). ∗p<0,05, ∗∗∗р<0,001.
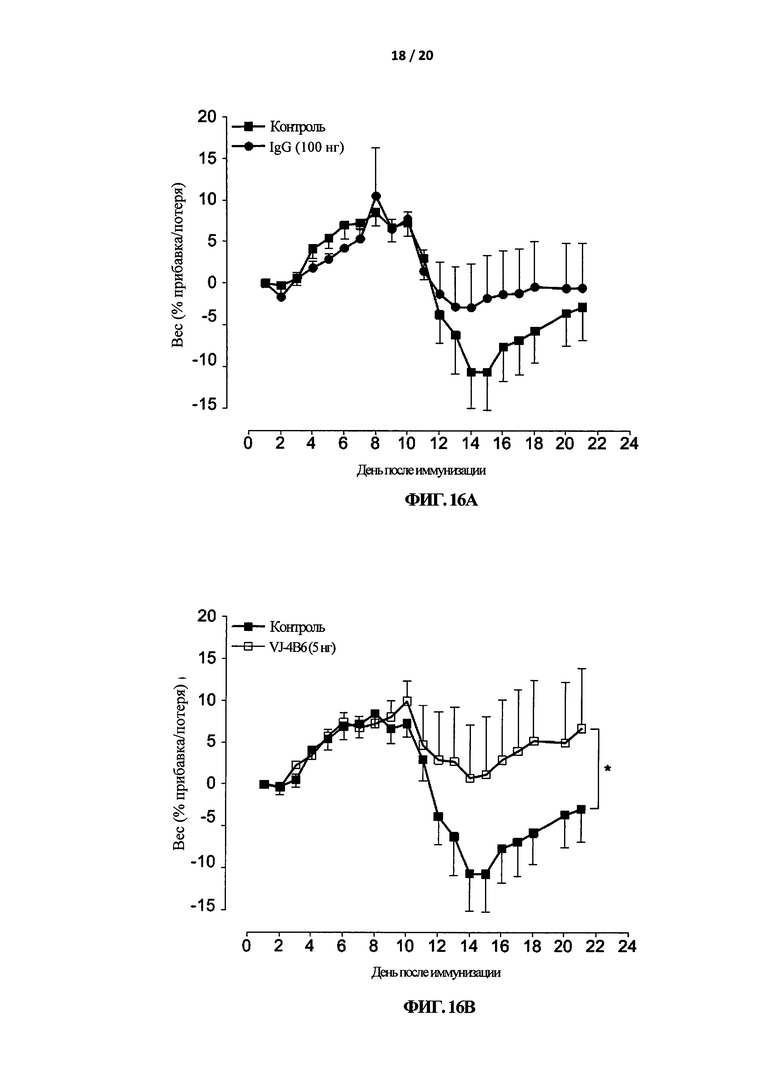
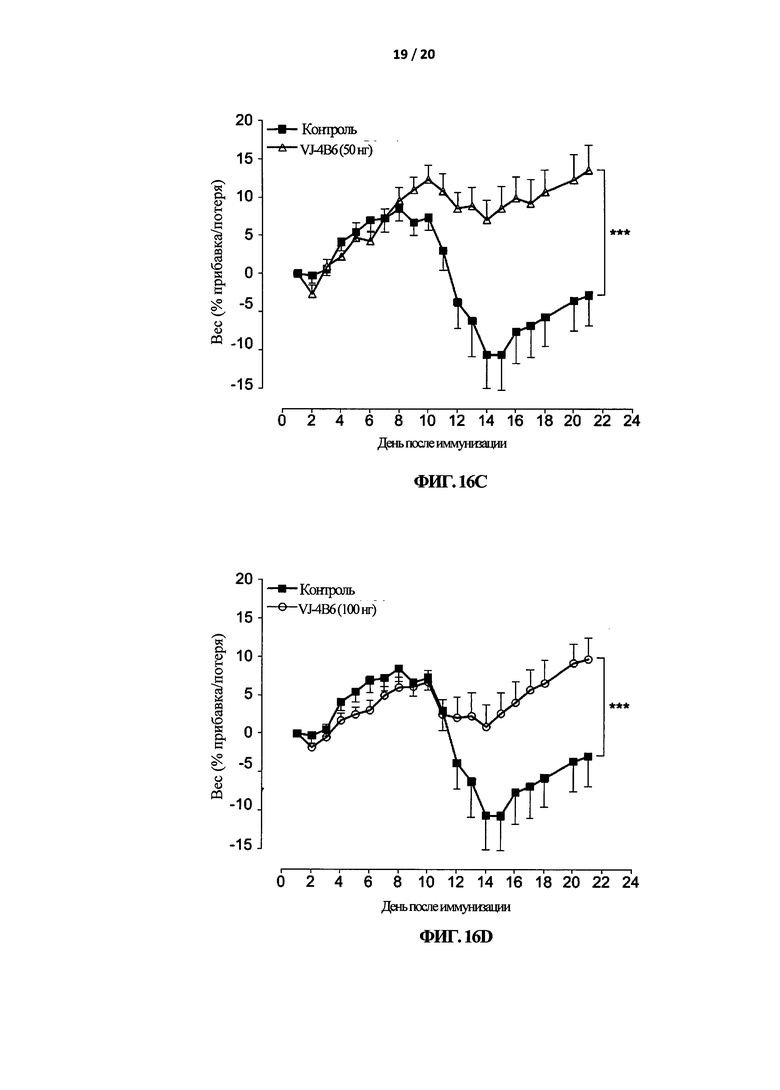
На Фигуре 16 показано, что VJ-4B6 снижает потерю веса, связанную с развитием ЭАЭ. Мышей C57BL/6 иммунизировали MOG35-55 в CFA и ежедневно наблюдали за увеличением/уменьшением веса в течение 22 дней. На 6-й день после иммунизации мыши получали и.п. инъекцию 100 нг IgG (А) или 5 (В), 50 (С), 100 ng (D) VJ-4B6 (в 100 мкл ФСБ) каждые шесть дней. Результаты представляют собой средние значения ± СОС (n=6/группа). ∗р<0,05, ∗∗∗р<0,001.
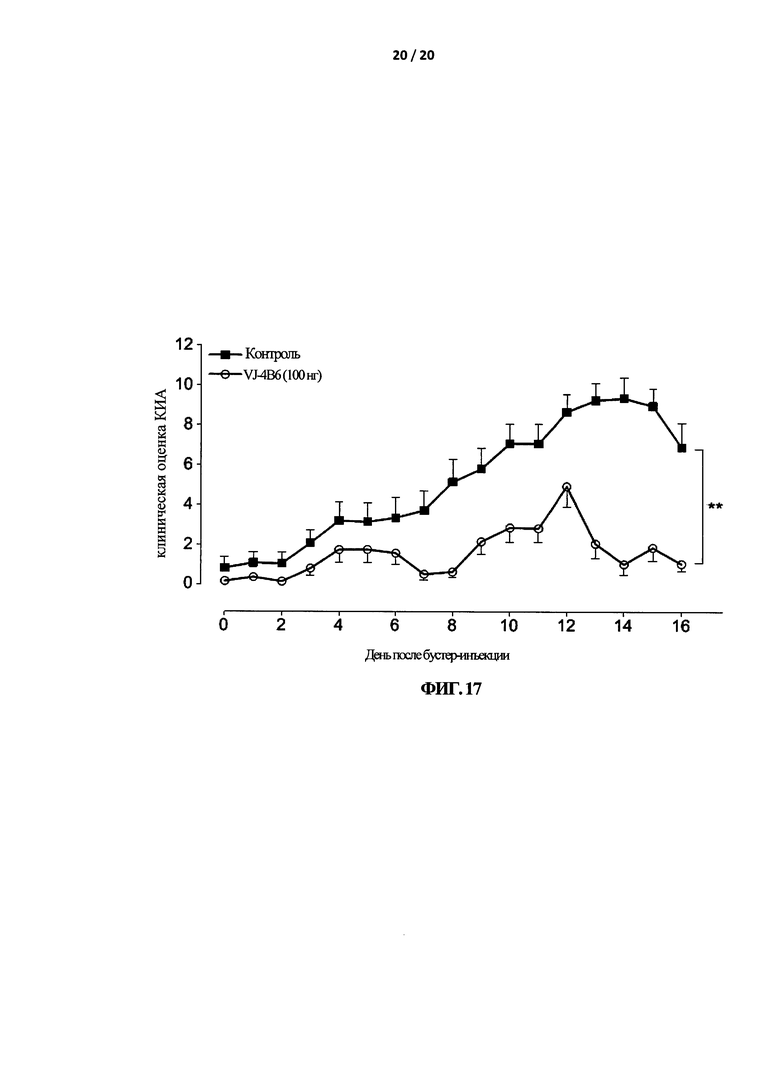
На Фигуре 17 показано, что VJ-4B6 уменьшает развитие КИА. Мышей DBA/1 иммунизировали бычьим коллагеном II типа в CFA. На 21 день после первичной иммунизации мыши получали (п.к.) вторичную инъекцию 200 мкг бычьего коллагена II типа в CFA и ежедневно наблюдали за проявлением симптомов заболевания в течение 20 дней. В день вторичной инъекции мыши получали и.п. инъекцию 100 нг VJ-4B6 (в 100 мкл ФСБ) каждые шесть дней. Результаты представляют собой средние значения ± СОС (n=6/группа). ∗∗∗р<0,001.
Пример 1. VJ-4B6 специфично ингибирует Т-клеточную активацию у Аннексин-1содержащих Т-клеток
МАТЕРИАЛЫ И МЕТОДЫ
Мыши (мыши, используемые в экспериментах, результаты которых представлены на Фигурах 4В, 5, 6, 7, 8, 9 и 10)
Мыши Balb/C были получены из В&К Universal (Гримстон, Англия). Мыши AnxA1-/- были выведены в лаборатории авторов настоящего изобретения и выращены в беспатогенных условиях в В&К Universal. Все мыши, использованные в этих исследованиях, были в возрасте от 6 до 8 недель. Работа с животными была выполнена в соответствии с правилами МВД Великобритании (United Kingdom Home Office, Руководство по проведению опытов с животными, Акт научных процедур 1986) и директивами Европейского Союза.
Выделение мышиных Т-клеток (клетки, использованные в экспериментах, результаты которых представлены на Фигурах 4В, 5, 6, 7, 8, 9 и 10)
Селезенку и лимфатические узлы (подмышечные, паховые и кишечные) выделяли из мышей в возрасте 6-8 недель и обрабатывали путем мягкой дезинтеграции тканей сквозь 50 мкм фильтр (BD) с помощью поршня шприца, как описано ранее. Клеточную суспензию наслаивали поверх фиколла для получения мононуклеаров, затем собирали и отмывали с помощью среды (RPMI) (Gibco).
Анализ пролиферации Т-клеток (данные на Фигуре 5 и 6)
Выделенные из лимфатических узлов Т-клетки (105 кл/мл) стимулировали с помощью прикрепленных к планшету антител к CD3 (анти-CD3) (клон 145-2С11; eBioscience) или с помощью анти-CD3 и анти-CD28 (клон 37.51; eBioscience) в 96-луночных планшетах. После 18-20 ч в культуру импульсно вводили 1 мкКи [3Н]-тимидина в течение 12 ч (Amersham Pharmacia Biothech) и включенную радиоактивность измеряли с помощью автоматического сцинтилляционного счетчика (Packard).
Продукция IL-2 (данные на Фигуре 7 и 8)
Выделенные из лимфатических узлов Т-клетки (105 клеток/мл) стимулировали с помощью прикрепленных к планшету анти-CD3 (клон 145-2С11; eBioscience) или с помощью анти-CD3 и анти-CD28 (клон 37.51; eBioscience) в 96-луночных планшетах. После 20-24 ч культуры супернатантов собирали и анализировали на содержание IL-2 с помощью набора для оценки мышиного IL-2 способом ИФА (mouse IL-2 ELISA kit, eBioscience) согласно инструкции производителя.
Анализ способом проточной цитометрии (Фигура 9 и 10)
Клетки ресуспендировали в FACS-буфере (ФСБ, содержащий 1% FCS и 0.02% NaN2). Лимфоциты в концентрации 1×106/мл окрашивали в 100 мкл FACS-буфера и захватывали с помощью FACScalibur с использованием программы CellQuestTM (Becton Dickinson). Использовали антитела к CD25 с FITC (клон РС61, eBioscience) и РЕ-коньюгированные антитела к CD69 (клон H1.2F3). Клетки предварительно инкубировали в FACS-буфере, содержащем антитела к CD 16/32 в течение 30 минут при 4°С, чтобы предотвратить неспецифическое связывание, и затем метили с помощью соответствующей концентрации коньюгированных антител в течение 30 минут при 4°С. После мечения клетки отмывали и анализировали. Передний и боковой рассеиватели настраивали так, чтобы исключить эритроциты и мертвые клетки, и, по меньшей мере, 2×104 лимфоцитов было проанализировано в каждом образце. Во всех экспериментах захват окрашенных клеток получали с помощью проточного цитометра FACScalibur и анализировали их, используя программное обеспечение FlowJo.
Проверка VJ-4B6 с помощью анализа способом проточной цитометрии (Фигура 4)
Человеческие МКПК и ПЯМК или мышиные спленоциты и брюшинные макрофаги первоначально ресуспендировали в FACS-буфере, содержащем 4% параформальдегид, в течение 10 минут, и после этого в FACS-буфере, содержащем 4% параформальдегид и 0.02% сапонин, в течение 15 минут. Клетки инкубировали с 50 нг/мл биотинизированным VJ-4B6 в течение 12 ч при 4°С. Затем клетки инкубировали со стрептавидином-FITC (разведение 1:200; eBioscience) в течение 1 ч при комнатной температуре. После мечения клетки отмывали и анализировали. Передний и боковой рассеиватели были настроены так, чтобы исключить эритроциты и мертвые клетки, и по меньшей мере 2×104 лимфоцитов было проанализировано для каждого образца. Во всех экспериментах окрашенные клетки захватывали с помощью FACScalibur проточного цитометра и анализировали с помощью программного обеспечения FlowJo.
Лейкоциты периферической крови человека (клетки, использованные в эксперименте, результаты которого приведены на Фигуре 4А)
Донорами крови были 20-35 летние здоровые мужчины и женщины, которые имели отрицательный ответ на ВИЧ, гепатит В и гепатит С. Дальнейшими критериями исключения были проявление инфекций в течение последних 4 недель, жар, симптоматические аллергии, ненормальное количество кровяных клеток, увеличение уровня ферментов печени или прием лекарства любого рода. Свежую венозную кровь собирали у здоровых волонтеров и немедленно переносили в пробирки, содержащие 3.2% цитрат натрия (разведение 1:10). Затем клетки разделяли, используя метод градиента плотности: 3 мл фиколла Histopaque-10771 наносили слоем поверх 3 мл Фиколл Histopaque-11911 (оба от Sigma) для создания дискретных слоев, после чего поверх Histopaque наносили слой 6 мл крови (разведение 1:1 в среде RPMI). После центрифугирования при 1500 об/мин при комнатной температуре в течение 30 минут МПКП и ПЯМК отсасывали из соответствующих слоев, используя стерильную пипетку Пастера, и промывали средой RPMI три раза.
Статистический анализ
Все статистические анализы проводили с помощью программного обеспечения Prism (программа GraphPad). Все значения представлены в виде средних значений ± СО. Статистический анализ оценивали с помощью t-критерия Стьюдента или с помощью однофакторного дисперсионного анализа в случае необходимости. Вероятность Р<0.05 принимали за значимую.
РЕЗУЛЬТАТЫ
Новое антитело к AnxA1 было получено с помощью генетической иммунизации, как показано на схеме на Фигуре 3А (Genovac GmbH, Германия). Анализировали сыворотки из нескольких иммунизированных мышей и трех мышей, клетки которых проявляли положительную реакцию на узнавание IgG, трансфицировали с помощью кДНК AnxA1. Спленоциты от таких мышей «сливали» с клетками миеломы для получения клеток гибридомы. Только один из трех гибридомных клонов был успешно субклонирован и размножен. Эти гибридомные клетки были названы VJ-4B6-E5-B10-D4. Очищенная фракция IgG2b из клеток гибридомы узнавала клетки, трансфицированные кДНК AnxA1 (Фигура 3В, зеленая линия; пик справа), но не клетки, трансфицированные несоответствующей кДНК (Фигура 3В, красная линия; пик слева).
Для подтверждения специфичности VJ-4B6 анализировали экспрессию AnxA1 с помощью ФСК в пермеабилизованных человеческих и мышиных клетках, в которых, как было известно, белок экспрессируется на разных уровнях. Как показано на Фигуре 4А, человеческие ПЯМК проявляли в более высокой степени положительную реакцию на окрашивание VJ-4B6, по сравнению с человеческими МКПК (Фигура 4А, пик справа, правая и левая панель, соответственно). Это согласуется с первоначальными наблюдениями (D'Acquisto et al., неопубликованные результаты), согласно которым в ПЯМК AnxA1 экспрессируется на значительно более высоком уровне, по сравнению с МКПК. Также, окрашивание мышиных макрофагов с помощью VJ-4B6 выявило высокий уровень экспрессии AnxA1, по сравнению со спленоцитами (Фигура 4В, пик справа, правая и левая панель, соответственно). Вместе эти результаты показывают, что VJ-4B6 узнают как человеческий, так и мышиный AnxA1.
На следующем этапе был проанализирован эффект и специфичность VJ-4B6 на активацию Т-клеток. Для этого сначала оценили воздействие VJ-4B6 на анти-CD3-индуцированную пролиферацию клеток (методом включения Н3-тимидина), используя Т-клетки от мышей AnxA1+/+ или AnxA1-/-. На Фигуре 5 показано увеличение включения Н3-тимидина как в AnxA1+/+, так и в AnxA1-/- Т-клетки, после стимуляции с помощью анти-CD3 (Фигура 5А и 5В, соответственно). Добавление VJ-4B6 к простимулированным культурам вызывает зависимое от концентрации ингибирование включения Н3-тимидина в AnxA1+/+, но не в AnxA1-/-клетки. Похожие результаты были получены при стимулировании Т-клеток с помощью анти-CD3 и анти-CD-28 (Фигура 6А и 6В, соответственно).
Для дальнейшего подтверждения этих результатов было исследовано воздействие VJ-4B6 на другие классические маркеры пролиферации Т-клеток, например на продукцию интерлейкин-2 (IL-2) и активацию CD25/CD69. Т-клетки, простимулированные либо с помощью анти-CD3, либо с помощью анти-CD3 и анти-CD28, продуцируют большее количество IL-2 (Фигура 7 и 8, соответственно). Добавление VJ-4B6 в значительной степени и зависимым от концентрации способом ингибировало продукцию IL-2 в AnxA1+/+, но не в AnxA1-/- Т-клетках. Похожие результаты были получены для активации CD25/CD69. Активация Т-клеток либо с помощью анти-CD3, либо с помощью анти-CD3 и анти-CD28 вызывала заметное увеличение процента CD25/CD69 двойных позитивных Т-клеток (вторая панель слева, Фигура 9 и 10, соответственно). Стимуляция в присутствии VJ-4B6 в значительной степени и зависимым от концентрации способом ингибировала индукцию CD25/CD69 (и экспрессию) в AnxA1+/+, но не в AnxA1-/- Т-клетках.
В совокупности эти результаты показывают, что VJ-4B6 достоверно ингибирует пролиферацию Т-клеток, продукцию IL-2 и активацию CD25/CD69, индуцированную с помощью компонентов сигнального каскада, индуцированного либо анти-CD3, либо анти-CD3 и анти-CD28. Кроме того, этот эффект является специфичным вследствие нейтрализации AnxA1 с помощью VJ-4B6, т.к. этот эффект не наблюдается в AnxA1+/+ Т-клетках. Это согласуется с первоначальными наблюдениями авторов настоящего изобретения, что активированные Т-клетки выделяют эндогенный AnxA1, что могло бы быть, в свою очередь, необходимым для правильной активации Т-клеток (D'Acquisto et al, Blood 109: 1095-1102, 2007; D'Acquisto etal, Eur. J. Immunol. 37: 3131-3142, 2007).
Таким образом, полученные данные показывают, что VJ-4B6 ингибирует анти-CD3-индуцируемую активацию CD25 и CD69 (маркеры активации Т-клеток) зависимым от концентрации способом. Схожий ингибирующий эффект наблюдали по отношению к продукции IL-2 и пролиферации Т-клеток. Наиболее важно, что это воздействие не наблюдали в Аннексин-1-дефицитных Т-клетках, что указывает на то, что ингибирование является специфичным и что антитела не вызывают какого-либо неблагоприятного цитотоксического воздействия.
Пример 2. Секвенирование VJ-4B6
Целью данного Примера было клонирование генов вариабельной области тяжелой и легкой цепей антитела из клеток гибридомы, и определение последовательности ДНК и местоположения гипервариабельных участков (CDR), а также других характеристик.
Клонирование и секвенирование вариабельных областей антитела
Тотальную РНК выделяли из 1 пробирки клеток гибридомы с помощью набора Qiagen RNeasy mini kit (кат.номер 74104). РНК элюировали 50 мкл воды и проверяли в 1,2% агарозном геле.
кДНК VH и VK (вариабельная область легкой цепи каппа) получали с помощью обратной транскриптазы и праймеров к IgG и константной области каппа. Первую цепь кДНК амплифицировали с помощью ПЦР, используя большой набор праймеров с сигнальными последовательностями. Амплифицированную ДНК выделяли из геля и клонировали в вектор pGem® Т Easy (Promega). Полученные клоны VH и VK проверяли на наличие вставок ожидаемого размера. Последовательность ДНК отобранных клонов определяли в обоих направлениях с помощью автоматического секвенирования ДНК. Местоположение гипервариабельных участков (CDR) в последовательностях определяли относительно последовательностей других антител (Kabat ЕА et al., 1991).
Результаты
Легкая цепь VJ-4B6
Была определена последовательность ДНК единичной VK и вычисленная аминокислотная последовательность для VJ-4B6 VK показана на Фигуре 11. Вычисленная белковая последовательность с аннотированными CDR показана на Фигуре 12. Девять клонов (семь независимых) из двух независимых этапов амплификации демонстрировали идентичную последовательность V-области. Неэффективная аберрантная последовательность VK, образовавшаяся из партнера гибридомного слияния, была также представлена в ряде клонов, и присутствовал один клон с делецией внутри последовательности.
Тяжелая цепь VJ-4B6
Была идентифицирована единичная последовательность VH. Последовательность ДНК и рассчитанная аминокислотная последовательность для VH VJ-4B6 показана на Фигуре 13. Одна и та же последовательность V-области была обнаружена в девяти независимых клонах. Два клона имели одиночные замены, один клон имел делецию одной нуклеотидной пары и одну нуклеотидную замену, и один клон имел две нуклеотидные замены.
Каждая из 5 одиночных нуклеотидных замен имела место только в одном клоне. Оставшиеся пять клонов имели идентичные последовательности. Выведенная белковая последовательность с аннотированными участками CDR показана на Фигуре 14.
Ссылки
Chothia С and Lesk AM. Cannonical structures for the hypervariable regions of immunoglobulins. J Mol Biol. 196: 901-17, 1987.
Kabat EA, Wu TT, Perry HM, Gottesman KS, Foeller C. Sequences of proteins of Immunological Interest, US Department of Health and Human Services, 1991.
Пример 3. Иммуносупрессивное воздействие JV-4B6
Для исследования иммуносупрессорного эффекта VJ-4B6 in vivo были выбраны две классические модели аутоиммунных заболеваний: MOG33-35-индуцированный экспериментальный аутоиммунный энцефаломиелит (ЭАЭ; модель рассеянного склероза мыши) и коллаген-индуцированный артрит (КИА; модель ревматоидного артрита мыши).
Методы
Экспериментальные аутоиммунные энцефаломиелиты. Мышей иммунизировали подкожно на 0 день с помощью 300 мкл эмульсии, содержащей 300 мкг MOG33-35 в ФСБ, объединенный с равным количеством CFA (полный адъювант Фрейнда), содержащим 300 мкг инактивированных нагреванием М. tuberculosis H37Ra. Эмульсия вводили в оба бока и вслед за ней осуществляли внутрибрюшинное введение токсина В. pertusis (500 нг/100 мкл) в 100 мкл солевого раствора на 0 и 2 день. За мышами наблюдали ежедневно на предмет признаков ЭАЭ и потери веса. Тяжесть болезни оценивали по 6-бальной шкале: 0 = отсутствие болезни, 1 = частично вялый хвост; 2 = полностью вялый хвост; 3 = нарушение основных рефлексов; 4 = частичный паралич задних конечностей; 5 = полный паралич задних конечностей; 6 = умирающее или мертвое животное.
Коллаген-индуцированный артрит. Шесть-восемь мышиных самцов DBA/1 (в возрасте 8-12 недель) инъецировали подкожно у основания хвоста 200 мкг коллагена II типа, эмульгированного в полном адъюванте Фрейнда (CFA; Hooke labs.). На 21 день после первой иммунизации мышей повторно иммунизировали (п.к.) с помощью 200 мкг коллагена II типа в IFA (Hooke labs). Мышей обследовали на предмет появления признаков наступления артрита, используя два клинических параметра: опухание лапы и клиническую оценку. Опухание лапы оценивали, измеряя толщину пострадавших задних лап с помощью плетизмометра. Клинический артрит оценивали в соответствии с рекомендациями производителя (http://hookelabs.com/protocols/ciaInductionDBAl/ciaInduction_DBAl.html). Каждую конечность оценивали, выставляя максимально возможный балл из 12 для каждого животного.
Результаты
Самцов мышей C57/BL6 иммунизированы с помощью MOG33-35/CFA, как было описано ранее (Paschalidis et al., J Neuroinflammation. 2009; 6:33). Мыши получали внутрибрюшинную (и.п.) инъекцию VJ-4B6 (5, 50 и 100 нг/100 мкл), контрольного IgG (100 нг/мкл) или носителя ФСБ (контроль) каждые 6 дней, начиная с 6 дня после иммунизации с помощью MOG33-35/CFA. Как показано на Фигуре 15, мыши, обработанные 5, 50 и 100 нг VJ-4B6, демонстрировали статистически значимое дозозависимое уменьшение признаков болезни, по сравнению с контрольными мышами (Фигура 15В, С и D, соответственно), в то время как введение контрольного IgG не оказывало никакого эффекта (Фигура 15А). Площадь под кривой (ППК) для каждой обработки и процент ингибирования в отношении контроля (27,29 ППК) были следующими: IgG 100 нг, 24,17 ППК, 11.4%; VJ-4B6 5 нг, 15,04 ППК, 44,8%; VJ-4B6 50 нг, 5,87 ППК, 78,5%; VJ-4B6 100 нг, 7,04 ППК, 74.2%.
Изучение животных моделей ЭАЭ показало, что критическая фаза болезни совпадает с потерей веса, что вероятно связанно с анорексией и недостаточным поглощением жидкости. Измерение веса обработанных мышей коррелировало с тяжестью клинической оценки и показывало дозозависимое уменьшение потери веса, с 18 дня и далее, у мышей, которым вводили VJ-4B6-, но не у мышей, получавших IgG, по сравнению с контролями (Фигура 16).
Для подтверждения терапевтического потенциала VJ-4B6 как иммунодепрессанта in vivo, протестировали его эффект на модели КИА. Самцов мышей DBA/1 иммунизировали бычьим коллагеном II типа в CFA, как было описано ранее (D'Acquisto et al., Blood. 2007; 109(3):1095-102). Мыши получали и.п. инъекцию VJ-4B6 (100 нг/100 мкл) или носитель ФСБ (контроль) каждые шесть дней, начиная с 0 дня после бустер-инъекции коллагеном. Согласно данным, полученным для ЭАЭ, введение VJ-4B6 значительно уменьшает развитие признаков болезни (ОПК 26,75; 67,9%), по сравнению с контрольными мышами (ОПК 83,50) (Фигура 17).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ АУТОИММУННОГО ЗАБОЛЕВАНИЯ ПУТЕМ МОДУЛИРОВАНИЯ АКТИВНОСТИ АННЕКСИНА-1 (ЛИПОКОРТИНА-1) | 2009 |
|
RU2554801C2 |
| АГЕНТЫ ДЛЯ ЛЕЧЕНИЯ ЭКСПРЕССИРУЮЩИХ КЛАУДИН РАКОВЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2678127C2 |
| АНТИТЕЛА ПРОТИВ ОХ40 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2562874C1 |
| АНТИ-СD3-АНТИТЕЛО И МОЛЕКУЛА, СОДЕРЖАЩАЯ ЭТО АНТИТЕЛО | 2017 |
|
RU2790326C2 |
| АНТИТЕЛА, РАСПОЗНАЮЩИЕ СОДЕРЖАЩИЙ УГЛЕВОДЫ ЭПИТОП НА CD-43 И СЕА, ЭКСПРЕССИРУЕМЫХ НА ЗЛОКАЧЕСТВЕННЫХ КЛЕТКАХ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2461572C2 |
| СПОСОБЫ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ АНТАГОНИСТАМИ DLL4 | 2011 |
|
RU2587620C2 |
| АНТИТЕЛА, РАСПОЗНАЮЩИЕ СОДЕРЖАЩИЙ УГЛЕВОДЫ ЭПИТОП НА CD-43 И СЕА, ЭКСПРЕССИРУЕМЫХ НА ЗЛОКАЧЕСТВЕННЫХ КЛЕТКАХ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2616868C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ДИАБЕТА АНТАГОНИСТАМИ DLL4 | 2011 |
|
RU2587624C2 |
| БИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ АГЕНТЫ С МЕЖВИДОВОЙ СПЕЦИФИЧНОСТЬЮ | 2008 |
|
RU2535992C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ С УСТОЙЧИВОСТЬЮ К РАСТВОРИМОМУ СЕА | 2010 |
|
RU2573893C2 |




Настоящее изобретение относится к биохимии, в частности к антителу против аннексина (Аnх-А1) человека, имеющему следующие гипервариабельные участки (CDR): VLCDR1 представляет собой KASENVVTYVS, VLCDR2 представляет собой GASNRYT, VLCDR3 представляет собой GQGYSYPYT, VHCDR1 представляет собой GYTFTNYWIG, VHCDR2 представляет собой DIYPGGDYTNYNEKFKG, и VHCDR3 представляет собой WGLGYYFDY. Кроме того, настоящее изобретение раскрывает клеточную гибридому, депонированную в Европейской коллекции клеточных культур (ECACC) под номером 10060301, которая продуцирует указанное антитело. Антитело согласно настоящему изобретению используют в качестве активного ингредиента в композиции для ингибирования активации Т-клеток, а также для получения лекарственного средства для лечения заболеваний, вызванных аберрантной активацией Т-клеток, таких как, например, ревматоидный артрит или рассеянный склероз. Настоящее изобретение обеспечивает новое моноклональное антитело, специфично ингибирующее активацию Т-клеток без каких-либо неблагоприятных цитотоксических эффектов. 5 н. и 13 з.п. ф-лы, 17 ил., 4 пр.
1. Антитело или фрагмент указанного антитела, направленные против белка Anx-А1 человека, где указанный белок имеет аминокислотную последовательность SEQ ID NO: 8, при этом указанное антитело или фрагмент указанного антитела содержат гипервариабельные участки (CDR) VLCDR1, VLCR2, VLCDR3, VHCDR1, VHCDR2 и VHCDR3, каждый из которых имеет соответствующую аминокислотную последовательность, как указано ниже: VLCDR1 представляет собой KASENVVTYVS,
VLCDR2 представляет собой GASNRYT,
VLCDR3 представляет собой GQGYSYPYT,
VHCDR1 представляет собой GYTFTNYWIG,
VHCDR2 представляет собой DIYPGGDYTNYNEKFKG,
VHCDR3 представляет собой WGLGYYFDY.
2. Антитело или фрагмент указанного антитела по п. 1, отличающееся тем, что указанное антитело представляет собой моноклональное антитело.
3. Антитело или фрагмент указанного антитела по п. 2, отличающееся тем, что указанное моноклональное антитело является гуманизированным.
4. Антитело или фрагмент указанного антитела по п. 1, отличающееся тем, что указанный фрагмент представляет собой Fab, F(ab′)2 или Fv-фрагмент или молекулу scFv.
5. Антитело или фрагмент указанного антитела по п. 1, включающее полипептид, имеющий аминокислотную последовательность, приведенную в SEQ ID NO: 15 и/или SEQ ID NO: 19.
6. Антитело или фрагмент указанного антитела по п. 1, продуцируемое клеточной линией гибридомы, депонированной в Европейской коллекции клеточных культур (ЕСАСС) под номером доступа 10060301.
7. Антитело или фрагмент указанного антитела по п. 1 для применения в медицине.
8. Антитело или фрагмент указанного антитела по п. 1 для применения для лечения заболевания, вызванного аберрантной активацией Т-клеток.
9. Антитело или фрагмент указанного антитела по п. 8, отличающееся тем, что указанное заболевание выбрано из группы, состоящей из заболевания «трансплантат против хозяина», отторжения трансплантата, атеросклероза, ВИЧ, СПИД, псориаза, выкидыша и аутоиммунных заболеваний.
10. Антитело или фрагмент указанного антитела по п. 9, отличающееся тем, что указанное аутоиммунное заболевание выбрано из группы, состоящей из ревматоидного артрита (РА), рассеянного склероза (PC), системной красной волчанки (СКВ), болезни Аддисона, болезни Грейвса, склеродермии, полимиозита, диабета, аутоиммунного увеоретинита, язвенного колита, обыкновенной пузырчатки, воспалительного заболевания кишечника, аутоиммунного тиреоидита, увеита, болезни Бехчета и синдрома Шегрена.
11. Антитело или фрагмент указанного антитела по п. 10, отличающееся тем, что указанное аутоиммунное заболевание выбрано из группы, состоящей из ревматоидного артрита (РА), рассеянного склероза (PC) и системной красной волчанки (СКВ).
12. Антитело или фрагмент указанного антитела по п. 11, отличающееся тем, что указанное аутоиммунное заболевание представляет собой ревматоидный артрит (РА) или рассеянный склероз (PC).
13. Антитело или фрагмент указанного антитела по п. 9, отличающееся тем, что указанное заболевание выбрано из группы, состоящей из атеросклероза, ВИЧ, СПИД и псориаза.
14. Клеточная линия гибридомы, продуцирующая антитело или фрагмент указанного антитела по любому из пп. 1-6, при этом указанная клеточная линия гибридомы депонирована в Европейской коллекции клеточных культур (ЕСАСС) под номером доступа 10060301.
15. Фармацевтическая композиция для ингибирования активации Т-клеток, содержащая терапевтически эффективное количество антитела или фрагмента указанного антитела по любому из пп. 1-6.
16. Фармацевтическая композиция по п. 15, дополнительно содержащая другой терапевтически активный агент.
17. Применение антитела или фрагмента указанного антитела по любому из пп. 1-6 для получения лекарственного средства для применения для лечения заболевания, вызванного аберрантной активацией Т-клеток.
18. Способ лечения заболевания, вызванного аберрантной активацией Т-клеток, у субъекта, нуждающегося в этом, включающий введение указанному субъекту антитела или фрагмента указанного антитела по любому из пп. 1-6.
| PEPINSKY et al., Monoclonal antibodies to lipocortin-1 as probes for biological function, FEBS LETTERS, 1990, vol.261, no.2, pp.247-252 | |||
| D`ACQUISTO et al., Glucocorticoid treatment inhibits annexin-1 expression in rheumatoid arthritis CD4 T cells, Rheumatology 2008, 47, pp.636-639 | |||
| OHNO et | |||
| al., Antigen-binding specificities of |
Авторы
Даты
2016-09-10—Публикация
2011-06-09—Подача