Настоящая заявка имеет приоритет в соответствии с предварительной патентной заявкой США №61/096,488, поданной 12 сентября 2008 г., и японской патентной заявкой №2009-184806, поданной 7 августа 2009 г., содержание которых включено сюда посредством ссылки во всей своей полноте.
Здесь раскрыты композиции и способы, относящиеся к областям органической химии, фармацевтической химии, биохимии, молекулярной биологии и медицины. В частности, варианты осуществления изобретения, раскрытые здесь, относятся к агентам и способам визуализации клетки и/или части ткани, например, клетки и/или ткани, характеризующихся фиброзом, а также к агентам и способам для определения и/или диагностики фиброзных заболеваний.
Предшествующий уровень техники
Фиброз, или развитие избытка фиброзной соединительной ткани в теле, связан с рядом заболеваний и нарушений, таких как гепатитный фиброз, панкреатический фиброз, рубцы голосовых связок и многочисленные формы рака. Фиброзные заболевания являются группой заболеваний, характеризующихся таким фиброзом, который может встречаться в различных тканях, таки как печень. Например, гепатитный фиброз, который является одним из фиброзных заболеваний, вызывается, например, гепатитными звездчатыми клетками (HSC), активированными в результате заживления ран после повреждения ткани внутри печени вследствие вирусного гепатитного заболевания, вызванного вирусом гепатита В или С, неалкогольного стеатогепатита, диабета, связанного с недостаточностью питания, паразитов, инфекционных заболеваний, таких как туберкулез или сифилис, внутрипеченочной закупорки в связи с сердечным заболеванием, или нарушения в желчном протоке, и т.д., которые в свою очередь чрезмерно продуцируют и секретируют внеклеточный матрикс (ЕСМ), например, множество типов коллагеновых молекул и фибронектина, который откладывается на интерстициальной ткани. Конечная стадия гепатитного фиброза представляет собой гепатитный цирроз, который может вызывать гепатитное повреждение, гепатоклеточную карциному и т.д.
Применяли различные подходы в попытке ингибировать фиброз в органе или ткани. Один подход может ингибировать активацию одной или более звездчатых клеток, где активация таких клеток характеризуется повышенным продуцированном внеклеточного матрикса (ЕСМ). Другие подходы могут относиться к ингибированию продуцирования коллагена, например, способствуя деградации коллагена или контролируя метаболизм коллагена. Однако способа восстановления фиброзной ткани еще не существует, и когда большая часть ткани замещена фиброзной тканью до такой степени, что пораженная ткань не может нормально функционировать, действительно нет других вариантов, кроме трансплантации для восстановления такой ткани. Следовательно, важно обнаружить фиброзное заболевание на ранней стадии и обеспечить противофиброзное лечение.
Диагностирование фиброзных заболеваний обычно проводят биопсией ткани, для которой предполагается фиброз. Однако так как биопсия является высоко инвазивным методом, который может вызывать осложнения, такие как инфекцию, кровоизлияние, боль и повреждение другой ткани, проводятся различные исследования, относящиеся к неинвазивным диагностическим методам фиброзных заболеваний. Например, сообщают о попытке коррелировать аналитические значения диффузионных-взвешенных МР-томограмм с наличием цирроза (Aube et al., J Radiol. 2004; 85(3):301-6), попытке определить наличие цирроза детектированием его характерных признаков, например, морфологических изменений печени путем КТ, МРТ или ультразвукового исследования (Kudo et al., In tervirology. 2008; 51 Suppl 1: 17-26) и о попытке определить наличие цирроза при помощи биохимических индикаторов, таких как гиалуронат и протромбиновый индекс (Oberti et al., Gastroenterology. 1997; 113(5): 1609-16). Однако ни один из таких способов не является удовлетворимым, и необходима разработка дополнительных способов диагностики.
Кроме того, JP, А, 2009-518372 раскрывает синтез ретиноил-ПЭГ(12)-Lys-ОН в качестве диагностического контрастного агента, пригодного для диагностической визуализации фиброза, но не описывает, что это вещество действительно было пригодно в качестве контрастных агентов.
Краткое содержание изобретения Техническая задача
Настоящее изобретение главным образом направлено на обеспечение визуализирующего агента для фиброзных заболеваний, способа визуализации фиброзного заболевания, использующего указанный визуализирующий агент, диагностического агента фиброзного заболевания, содержащего указанный визуализирующий агент, диагностического способа фиброзного заболевания, использующего указанный диагностический агент и т.д.
Решение задачи
При исследовании нового диагностического способа для фиброзных заболеваний авторы обнаружили, что фиброзные заболевания могут обнаруживаться неинвазивно in vivo путем введения визуализирующего агента, который содержит ретиноид и детектируемую метку, достигая цели настоящего изобретения. Хотя известно, что носитель, содержащий витамин А, доставляет лекарства к гепатитным звездчатым клеткам (WO 2006/068232), вовсе не было известно, что фиброзные заболевания могут неинвазивно детектироваться in vivo при помощи визуализирующего агента, который содержит ретиноид и детектируемую метку.
Настоящее изобретение относится к:
(1) Визуализирующий агент для клетки и/или тканей, характеризующихся фиброзом, содержащий ретиноид и детектируемую метку.
(2) Визуализирующий агент (1), где ретиноид содержит ретинол.
(3) Визуализирующий агент (1) или (2), где визуализирующий агент служит для визуализации in vivo.
(4) Визуализирующий агент по любому из (1)-(3), где визуализирующий агент служит для визуализации фиброзного заболевания.
(5) Визуализирующий агент по любому из (1)-(4), содержащий полимерный конъюгат, содержащий по меньшей мере одно повторяющееся звено, выбранное из формул (I), (II), (III) и (IV):
[Схем. 1]

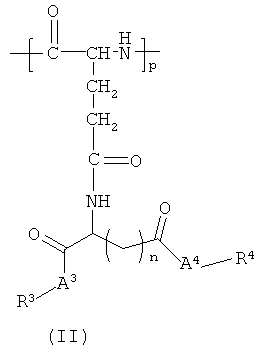
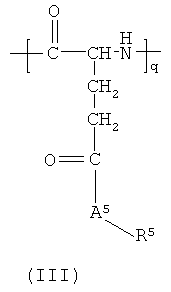

где:
m означает независимо 1 или 2;
n означает независимо 1 или 2;
А1 и А2 каждый независимо означают кислород или NR7;
А3 и А4 каждый независимо означают кислород или NR8;
А5 и А6 каждый независимо означают кислород или NR9;
R1, R2, R3, R4, R5 и R6 каждый независимо выбраны из группы, состоящей из при необходимости замещенного C1-10 алкила, при необходимости замещенного С6-20 арила, аммония, щелочного металла, ретиноида и группы, которая содержит детектируемую метку;
R7, R8 и R9 каждый независимо являются водородом или C1-4 алкилом;
о, р, q и r каждый независимо являются 0, 1 или более, где сумма о, р, q и r означает 2 или более; и
при условии, что по меньшей мере один из R1, R2, R3, R4, R5 и R6 означает группу, которая содержит детектируемую метку, и по меньшей мере один из R1, R2, R3, R4, R5 и R6 означает ретиноид.
(6) Полимерный конъюгат, содержащий по меньшей мере одно повторяющееся звено, выбранное из формул (I), (II), (III) и (IV):
[Схем. 2]




где:
m означает независимо 1 или 2;
n означает независимо 1 или 2;
А1 и А2 каждый независимо означают кислород или NR7;
А3 и А4 каждый независимо означают кислород или NR8;
А5 и А6 каждый независимо означают кислород или NR9;
R1, R2, R3, R4, R5 и R6 каждый независимо выбраны из группы, состоящей из при необходимости замещенного С1-10 алкила, при необходимости замещенного С6-20 арила, аммония, щелочного металла, ретиноида и группы, которая содержит детектируемую метку;
R7, R8 и R9 каждый независимо означают водород или С1-4 алкил;
о, р, q и r каждый независимо означают 0,1 или более, где сумма о, р, q и r означает 2 или более; и
при условии, что по меньшей мере один из R1, R2, R3, R4, R5 и R6 означает группу, которая содержит детектируемую метку, и по меньшей мере один из R1, R2, R3, R4, R5 и R6 означает ретиноид.
(7) Полимерный конъюгат согласно (6), где полимер также содержит по меньшей мере одно повторяющееся звено формулы (V):
[Схем. 3]

где:
s независимо означает 1 или 2;
А7 и А8 каждый независимо означают кислород или NR12;
R12 означает водород или C1-4 алкил;
R10 и R11 каждый независимо выбраны из группы, состоящей из при необходимости замещенного С1-10 алкила, при необходимости замещенного С6-20 арила, аммония и щелочного металла.
(8) Полимерный конъюгат согласно (6) или (7), где полимер также содержит по меньшей мере одно повторяющееся звено формулы (VI):
[Схем. 4]
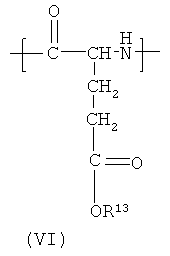
где R13 означает водород, аммоний или щелочной металл.
(9) Полимерный конъюгат по любому из (6)-(8), где детектируемая метка содержит металл, выбранный из группы, состоящей из Gd(III), иттрия-88 и индия-111.
(10) Полимерный конъюгат по любому из (6)-(9), где детектируемая метка содержит лиганд, выбранный из группы, состоящей из: диэтилентриаминпентауксусная кислота (DTPA), тетраазациклододекан-1,4,7,10-тетрауксусная кислота (DOTA), (1,2-этандиилдинитрило)тетраацетат (EDTA), этилендиамин, 2,2′-бипиридин (bipy), 1,10-фенантролин (phen), 1,2-бис(дифенилфосфино)этан (DPPE), 2,4-пентандион (асас) и этандиоат(ox).
(11) Полимерный конъюгат по любому из (6)-(10), где детектируемая метка содержит лиганд, выбранный из группы, состоящей из: диэтилентриаминпентауксусная кислота (DTPA) и тетраазациклодекан-1,4,7,10-тетрауксусная кислота (DOTA).
(12) Полимерный конъюгат по любому из (6)-(11), где детектируемая метка представляет собой хелат парамагнитного металла.
(13) Полимерный конъюгат согласно (12), где хелат парамагнитного металла содержит
[Схем. 5]
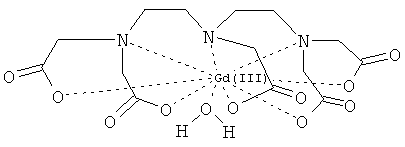 или
или 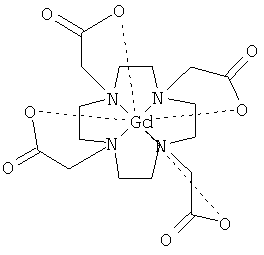 .
.
(14) Полимерный конъюгат по любому из (6)-(11), где детектируемая метка представляет собой краситель.
(15) Полимерный конъюгат согласно (14), где краситель содержит Техасский красный.
(16) Полимерный конъюгат по любому из (6)-(15), где m означает 1.
(17) Полимерный конъюгат по любому из (6)-(15), где m означает 2.
(18) Полимерный конъюгат по любому из (6)-(17), где n означает 1.
(19) Полимерный конъюгат по любому из (6)-(17), где n означает 2.
(20) Полимерный конъюгат по любому из пп.(7)-(19), где s означает 1.
(21) Полимерный конъюгат по любому из пп.(7)-(19), где s означает 2.
(22) Способ получения полимерного конъюгата по любому из (6)-(21), предусматривающий растворение или частичное растворение полимерного реагента, содержащего по меньшей мере одно повторяющееся звено формулы (VII) и повторяющееся звено формулы (VIII), в растворителе с образованием растворенного или частично растворенного полимерного реагента;
[Схем. 6]


где:
z означает 1 или 2;
А9 и А10 являются кислородом; и
R14, R15 и R16 каждый независимо выбраны из группы, состоящей из водорода, аммония и щелочного металла; и
реакцию растворенного или частично растворенного полимерного реагента со вторым реагентом, где второй реагент содержит группу, содержащую детектируемую метку или ретиноид; и
добавление третьего реагента, где третий реагент содержит группу, содержащую детектируемую метку, лиганд или ретиноид; при условии, что если второй реагент содержит группу, содержащую детектируемую метку или лиганд, то третий реагент содержит ретиноид, и если второй реагент содержит ретиноид, тогда третий реагент содержит группу, которая содержит детектируемую метку или лиганд.
(23) Способ согласно (22), где второй реагент содержит ретиноид.
(24) Способ согласно (22) или (23), где третий реагент содержит группу, которая содержит детектируемую метку.
(25) Способ согласно (22) или (23), где третий реагент содержит лиганд.
(26) Способ согласно (25), где лиганд выбран из группы, состоящей из: диэтилентриаминпентауксусной кислоты (DTPA), тетраазациклододекан-1,4,7,10-тетрауксусной кислоты (DOTA), (1,2-этандиилдинитрило)тетраацетата (EDTA), эти-лендиамина, 2,2′-бипиридина (bipy), 1,10-фенантролина(phen), 1,2-бис(дифенилфосфино)этана (DPPE), 2,4-пентандиона (acac) и этандиоата (ох).
(27) Способ по любому из (22)-(26), также предусматривающий добавление четвертого реагента, где четвертый реагент содержит метал.
(28) Способ согласно (27), где метал выбирают из группы, состоящей из Gd(III), иттрия-88 и индия-111.
(29) Диагностическое средство для фиброзного заболевания, содержащее визуализирующий агент по любому из (1)-(5) и/или полимерный конъюгат по любому из (6)-(21).
(30) Композиция, содержащая визуализирующий агент по любому из (1)-(5) и/или полимерный конъюгат по любому из (6)-(21) и/или диагностическое средство согласно (29), и по меньшей мере один, выбранный из фармацевтически приемлемых наполнителя, носителя и разбавителя.
(31) Способ доставки детектируемой метки к части ткани, предусматривающий контактирование части ткани или клетки с по меньшей мере одним визуализирующим агентом по любому из (1)-(5), и/или полимерным конъюгатом по любому из (6)-(21), и/или диагностическим агентом согласно (29), и/или композицией согласно (30).
(32) Способ визуализации части ткани, предусматривающий контактирование части ткани или клетки с по меньшей мере одним визуализирующим агентом по любому из (1)-(5), и/или полимерным конъюгатом по любому из (6)-(21), или композицией по (30).
(33) Способ диагностирования заболевания или состояния, предусматривающий контактирование части ткани или клетки с по меньшей мере одним полимерным конъюгатом по любому из (6)-(21), и/или диагностическим агентом по (29), и/или композицией по (30).
(34) Способ по любому из (31)-(33), где ткань представляет собой фиброзную ткань.
(35) Способ визуализации фиброзного заболевания, предусматривающий стадию введения эффективного количества визуализирующего агента по любому из (1)-(5), полимерного конъюгата по любому из (6)-(21) и/или композиции (30) субъекту, нуждающемуся в этом, и стадию детектирования метки, содержащейся во введенном визуализирующем агенте, полимерном конъюгате или композиции.
(36) Способ определения фиброзного заболевания, предусматривающий стадию сравнения интенсивности сигнала и/или распределения сигнала метки, детектируемой у субъекта, которому вводили визуализирующий агент по любому из (1)-(5), и/или полимерный конъюгат по любому из (6)-(21), и/или диагностическое средство согласно (29), и/или композицию согласно (30), с интенсивностью контрольного сигнала и/или распределением контрольного сигнала.
(37) Способ контроля фиброзного заболевания, предусматривающий стадию сравнения интенсивности сигнала и/или распределения сигнала, детектируемого в первый момент времени у субъекта, которому вводят визуализирующий агент по любому из (1)-(5), и/или полимерный конъюгат по любому из (6)-(21), и/или диагностическое средство согласно (29), и/или композицию согласно (30), с интенсивностью сигнала и/или распределением сигнала метки, детектируемой во второй момент времени, который является более поздним, чем первый момент времени у указанного субъекта.
Способ определения эффекта лечения фиброзного заболевания, предусматривающий стадию сравнения интенсивности сигнала и/или распределения сигнала метки, детектируемой в первый момент времени у субъекта, которому вводится визуализирующий агент по любому из (1)-(5), и/или полимерный конъюгат по любому из (6)-(21), и/или диагностическое средство согласно (29), и/или композиция согласно (30), с интенсивностью сигнала и/или распределением сигнала метки, детектированной во второй момент времени, который является более поздним, чем первый момент времени для указанного субъекта, где первый момент времени имеет место перед тем, как субъект получит лечение фиброзного заболевания, а второй момент времени имеет место после того, как субъект получил лечение фиброзного заболевания, или, альтернативно, первый момент времени имеет место после того, как субъект получил первое лечение фиброзного заболевания, а второй момент времени имеет место после того субъект получил второе лечение фиброзного заболевания, которое осуществлялось после первого лечения фиброзного заболевания.
Некоторые варианты осуществления изобретения, описанные здесь, относятся к полимерному конъюгату, который может включать по меньшей мере одно повторяющееся звено, выбранное из формул (I), (II), (III) и (IV), как здесь установлено далее.
Другие варианты осуществления изобретения, описанные здесь, относятся к способу доставки детектируемой метки к части ткани или клетке, который может включать контактирование части ткани или клетки с по меньшей мере одним из полимерных конъюгатов, описанных здесь.
Еще одни варианты осуществления, описанные здесь, относятся к способу визуализации части ткани или клетки, который может включать контактирование части ткани или клетки с по меньшей мере одним из полимерных конъюгатов, описанных здесь.
Другие варианты осуществления, описанные здесь, относятся к способу диагностирования заболевания или состояния, такого как болезнь или состояние, характеризующиеся фиброзом, который может включать контактирование части тканей с по меньшей мере одним из полимерных конъюгатов, описанных здесь.
Некоторые варианты осуществления изобретения, описанные здесь, относятся к применению по меньшей мере одного или полимерных конъюгатов, описанных здесь, для доставки детектируемой метки к части ткани или клетке.
Другие варианты осуществления изобретения, описанные здесь, относятся к применению по меньшей мере одного из полимерных конъюгатов, описанных здесь, для визуализации части ткани или клетки.
Еще одни варианты осуществления изобретения, описанные здесь, относятся к применению по меньшей мере одного из полимерных конъюгатов, описанных здесь, для диагностирования заболевания или состояния, таких как болезнь или состояние, характеризующиеся фиброзом.
Некоторые варианты осуществления изобретения, описанные здесь, относятся к полимерному конъюгату, описанному здесь, для доставки детектируемой метки к части ткани или клетке.
Другие варианты осуществления изобретения, описанные здесь, относятся к полимерному конъюгату, описанному здесь, для визуализации части ткани или клетки.
Еще одни варианты осуществления изобретения, описанные здесь, относятся к диагностированию заболевания или состояния, таких как заболевание или состояние, характеризующиеся фиброзом.
Полезный эффект изобретения
Хотя точный механизм визуализирующего агента настоящего изобретения не был полностью объяснен, предполагают, что ретиноид функционирует как направленный (targeting) агент для клеток, положительных по альфа-SMA (гладкомышечный альфа-актин) и продуцирующих ЕСМ (внеклеточный матрикс), таких как активированные звездчатые клетки, и дает возможность детектировать указанные клетки путем доставки к ним метящего вещества.
Так как визуализирующий агент согласно настоящему изобретению позволяет недеструктивно, предпочтительно неинвазивно детектировать фиброзные заболевания in vivo, риск осложнений вследствие традиционной биопсии уменьшается, и, следовательно, можно значительно уменьшить нагрузку на исследуемого субъекта. Дополнительно, поскольку это может расширить диапазон исследуемых субъектов, облегчается раннее обнаружение фиброзных заболеваний, что позволяет эффективно замедлять прогрессирование указанных заболеваний. Таким образом, настоящее изобретение делает значительный вклад в лекарственные препараты для человека и ветеринарные препараты.
Кроме того, визуализирующий агент по настоящему изобретению позволяет недеструктивно, предпочтительно неинвазивно обнаруживать фиброзное заболевание in vivo в течение времени у одного и того же индивидуума, что приводит к оценке лечения указанного заболевания с высокой точностью.
Эти и другие варианты осуществления изобретения описаны более подробно ниже.
Краткое описание чертежей
[фиг.1] Фиг.1 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, полиглутамат и тетраазациклододекан-1,4,7,10-тетрауксусную кислоту (DOTA), ретиноид-PGA-DOTA. [фиг.2] Фиг.2 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, полиглутамат и диэтилентриаминпентауксусная кислоту (DTPA), ретиноид-PGA-DTPA.
[фиг.3] Фиг.3 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, поли(L-гамма-глутамилглутамин) и тетраазациклододекан-1,4,7,10-тетрауксусную кислоту (DOTA), ретиноид-PGGA-DOTA.
[фиг.4] Фиг.4 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, поли(L-гамма-глутамилглутамин) и диэтилентриаминпентауксусную кислоту (DTPA), ретиноид-PGGA-DTPA.
[фиг.5] Фиг.5 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, полиглутамат и тетраазациклододекан-1,4,7,10-тетрауксусную кислоту (DOTA)Gd(III), ретиноид-PGA-[DOTA)Gd(III)].
[фиг.6] Фиг.6 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, полиглутамат и диэтилентриаминпентауксусную кислоту (DTPA)Gd(III), ретиноид-PGA-[(DTPA)Gd(III)].
[фиг.7] Фиг.7 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, поли(L-гамма-глутамилглутамин) и тетраазациклододекан-1,4,7,10-тетрауксусную кислоту (DOTA)Gd(III), ретиноид-PGGA-[(DOTA)Gd(III)].
[фиг.8] Фиг.8 иллюстрирует реакционную схему получения полимерного конъюгата, который включает ретиноид, поли(L-гамма-глутамилглутамин) и диэтилентриаминпентауксусную кислоту (DTPA)Gd(III), ретиноид-PGGA-[(DTPA)Gd(III)].
[фиг.9] Фиг.9 является графиком, иллюстрирующим поглощение клетками техасского красного(TR)-полиглутамата (РСА)-ретиноида, TR-PGA-ретиноида, по сравнению с техасским красным(TR)-полиглутаматом (РСА)-холестерином, техасским красным-PGA-холестерином.
[фиг.10] Фиг.10 демонстрирует ЯМР-изображения крысиных DMA-моделей с течением времени.
[фиг.11] Фиг.11 является графиком относительной оптической плотности Gd(III) из PGGA-[(DPTA)Gd(III)] и ретиноида-PGGA-[(DPTA)Gd(III)] в печени крысиных DMA-моделей с течением времени. Количество Gd(III) из ретиноида-PGGA-[(DPTA)Gd(III)], обнаруженное в печени крыс, составляло намного больше, чем количество Gd(III) из PGGA-[(DPTA)Gd(III)], обнаруженное в печени фиброзных крысиных DMA-моделей.
[фиг.12] Фиг.12 демонстрирует интенсивность и распределение флуоресцентного сигнала у цирротической мыши (слева) и нормальной мыши (справа) через 5 мин (вверху) и 90 мин (внизу) после введения визуализирующего агента. Интенсивность флуоресцентного сигнала показана как среднее значение излучения (Сред. излуч., фотоны/сек/см2/стерадиан).
[фиг.13] Фиг.13 представляет собой график, показывающий изменение с течением времени интенсивности флуоресцентного сигнала в печени (слева) и кишечнике (справа) цирротической мыши (закрашенные кружочки) и нормальной мыши (закрашенные квадратики) через 5-90 мин после введения визуализирующего агента.
[фиг.14] Фиг.14 демонстрирует локализацию флуоресцентного сигнала в ткани печени цирротической мыши (слева) и нормальной мыши (справа) через 90 мин после введения визуализирующего агента с (верхние группы) или без (нижние группы) VA.
[фиг.15] Фиг.15 является диаграммой, демонстрирующей отношение Су™ 5.5/ФИТС (флуоресцеин изотиоцианат) двойной положительной области к суммарной Су™ 5.5-положительной области в печени цирротической мыши и обычной мыши через 90 мин после введения визуализирующего агента (среднее из 8 случайных полей).
[фиг.16] Фиг.16 является диаграммой, демонстрирующей отношение количества двойных положительных клеток по Су™ 5.5/ПТС к общему количеству Су™ 5.5-положительных клеток в печени цирротической мыши и обычной мыши через 90 мин после введения визуализирующего агента (среднее из 8 случайных полей).
Описание вариантов осуществления изобретения
Раннее диагностирование фиброза может обеспечить более высокие возможности обнаружения подходящего лечения. В настоящее время клинически доступным одобренным способом диагностирования фиброза является только биопсия. Однако биопсия требует забора ткани для исследования. Неинвазивный способ минимизировал бы необходимость удалять ткань и риски, связанные с наличием инородного предмета, вводимого субъекту. Такой неинвазивный способ разрешает вопросы, связанные с неудовлетворенным выбором средств для диагностирования фиброза.
Если не указано иное, все технические и научные термины, использованные здесь, имеют те же значения, которые обычно понятны специалисту в данной области техники. Все упомянутые здесь патенты, заявки, опубликованные заявки и другие публикации включены сюда путем ссылки во всей своей полноте, если не указано иное.
В том случае, если существует множество определений для термина, превалируют те, которые указаны в этом разделе, если не определено другое.
Термин "сложный эфир" используется здесь в своем обычном значении, и соответственно включает химический фрагмент с формулой -(R)n-COOR′, где R и R′ независимо выбраны из группы, состоящей из алкила, циклоалкила, арила, гетероарила (связанного через углерод кольца) и гетероалициклических структур (связанных через углерод кольца или гетероатом), и где n означает 0 или 1.
Термин "амид" используется здесь в своем обычном значении и, соответственно, включает химический фрагмент с формулой -(R)n-C(O)NHR′ или -(R)n-NHC(O)R′, где R и R′ независимо выбраны из группы, состоящей из алкила, циклоалкила, арила, гетероарила (связанного через углерод кольца) и гетероалициклических структур (связанных через углерод кольца или гетероатом), и где n означает 0 или 1. Амид может включаться в аминокислотную или пептидную молекулу, присоединенную к молекул лекарственного средства, как описано здесь, формируя таким образом пролекарство.
Любые амин, гидрокси-группа или карбоксильная боковая цепь на соединениях, раскрытых здесь, могут быть эстерифицирована или амидирована. Процедуры и специфические группы, используемые для достижения этого результата, известны специалистам в данной области техники и могут быть легко обнаружены в справочных материалах, таких как Greene and Wuts, Protective Groups in Organic Synthesis, 3rd Ed., John Wiley & Sons, New York, NY, 1999, которая включена сюда во всей своей полноте.
При использовании здесь "алкил" относится к прямой или разветвленной углеводородной цепи, которая содержит полностью насыщенную (без двойных или тройных связей) углеводородную группу. Алкильная группа может иметь от 1 до 20 углеродных атомов (при любом здесь упоминании область числовых значений, такая как "1-20", относится к каждому целому числу в данном диапазоне; например, "1-20 углеродных атомов" означает, что алкильная группа может состоять из 1 атома углерода, 2 атомов углерода, 3 атомов углерода и т.д., вплоть до и включая 20 углеродных атомов, хотя настоящее определение также охватывает случай употребления термина "алкил", когда область числовых значений не обозначена). Алкильная группа также может быть алкилом среднего размера, имеющим от 1 до 10 атомов углерода. Алкильная группа также может быть низшим алкилом, имеющим 1-5 атомов углерода. Алкильная группа соединений может обозначаться как "C1-C4 алкил" или подобными обозначениями. Только в качестве примера, "C1-C4 алкил" указывает, что существуют 1-4 атомов углерода в алкильной цепи, т.е., алкильная цепь выбирается из метила, этила, пропила, изопропила, н-бутила, изобутила, втор-бутила и трет-бутила. Типичные алкильные группы включают, но не ограничиваются этим, метил, этил, пропил, изопропил, бутил, изобутил, третичный бутил, петил, гексил и т.п.
Алкильная группа может быть замещенная или незамещенная. В случае, когда она замещенная, группа(ы)-заместитель(и) является(ются) одной или более групп, по отдельности и независимо выбранных из алкенила, алкинила, циклоалкила, циклоалкенила, циклоалкинила, арила, гетероарила, гетероалициклила, аралкила, гетероаралкила, (гетероалициклил)алкила, гидрокси, защищенного гидроксила, алкокси, арилокси, ацила, сложного эфира, меркапто, алкилтио, арилтио, циано, галогена, карбонила, тиокарбонила, O-карбамила, N-карбамила, O-тиокарбамила, N-тиокарбамила, С-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, С-карбокси, защищенного С-карбокси, O-карбокси, изоцианато, тиоцианато, изотиоцианато, нитро, силила, сульфенила, сульфинила, сульфонила, галогеналкила (например, моно-, ди- и тригалогеналкила), галогеналкокси (например, моно-, ди- и тригалогеналкокси), тригалогенметансульфонила, тригалогенметансульфонамидо и амино, включая моно - и дизамещенные аминогруппы, и их защищенные производные. Где бы заместитель ни описывался как "при необходимости замещенный", он представляет собой заместитель, который может быть замещен одним из вышеупомянутых заместителей.
При использовании здесь "арил" относится к карбоциклической (только атомы углерода в кольце) моноциклической или мультициклической ароматической кольцевой системе, которая имеет полностью делокализованную пи-электронную систему. Примеры арильных групп включают, но не ограничиваются этим, бензол, нафталин и азулен. Арильная группа по этому изобретению может быть замещена или незамещена. В том случае, когда она замещена, атомы водорода замещаются группой(ами)-заместителем(ями), которая(ые) является(ются) одной или более групп, независимо выбранных из алкила, алкенила, алкинила, циклоалкила, циклоалкенила, циклоалкинила, арила, гетероарила, гетероалициклила, аралкила, гетероаралкила, (гетероалициклил)алкила, гидрокси, защищенного гидрокси, алкокси, арилокси, ацила, сложного эфира, меркапто, пиано, галогена, тиокарбонила, O-карбамила, N-карбамила, O-тиокарбамила, N-тиокарбамила, С-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, С-карбокси, защищенного С-карбокси, O-карбокси, изоцианато, тиоцианато, изотиоцианато, нитро, силила, сульфенила, сульфинила, сульфонила, галогеналкила (например, моно-, ди- и тригалогеналкила), галогеналкокси (например, моно-, ди- и тригалогеналкокси), тригалогенметансульфонила, тригалогенме-тансульфонамидо и амино, включая моно- и дизамещенные аминогруппы, и их защищенные производные, если не указаны другие группы-заместители.
"Хелат парамагнитного металла " означает комплекс, где лиганд связан с ионом парамагнитного металла. Примеры включают, но не ограничиваются этим, 1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусную кислоту (DOTA)-Gd(III), DOTA-иттрий-88, DOTA-индий-111, диэтилентриаминпентауксусная кислота (DTPA)-Gd(III), DTPA-иттрий-88, DTPA-индий-111.
"Ретиноид" является представителем класса соединений, состоящих из четырех изопреноидных единиц, соединенных способом голова-к-хвосту, см. G.P.Moss, "Biochemical Nomenclature and Related Documents," 2nd Ed. Portland Press, pp.247-251 (1992). "Витамин А" является общим идентификатором для ретиноидов, проявляющих качественно биологическую активность ретинола. При использовании здесь ретиноид относится к природным и синтетическим ретиноидам, включающим первое поколение, второе поколение и третье поколение ретиноидов. Примеры встречающихся в природе ретиноидов включают, но не ограничиваются этим, (1) 11-цис-ретиналь, (2) полностью транс-ретинол, (3) ретинилпальмитат, (4) полностью транс-ретиноевую кислоту и (5) 13-цис-ретиноевые кислоты. Кроме того, термин "ретиноид" охватывает ретинолы, ретинали и ретиноевые кислоты.
"Фиброз" используется здесь в своем обычном значении и относится к развитию фиброзной рубцовообразной соединительной ткани в органе или ткани как часть репаративного или реактивного процесса. "Аномальный фиброз" относится к развитию фиброзной рубцовообразной соединительной ткани в органе или ткани до такой степени, что это ухудшает функционирование органа или ткани. "Фиброзное заболевание" относится здесь к любым заболеваниям, характеризующимся фиброзом тканей, и включает, но не ограничивается этим, например, гепатитный фиброз, гепатитный цирроз, рубцы голосовых связок, фиброз слизистой оболочки голосовых связок, фиброз гортани, фиброз легких, миелофиброз, инфаркт миокарда и фиброз миокарда после инфаркта миокарда. В целях настоящего изобретения фиброзные заболевания обычно представляют собой те, в которые вовлечены клетки, положительные по альфа-SMA и продуцирующие внеклеточный матрикс, такие как гепатитные звездчатые клетки,
При использовании здесь "линкер" и "связывающая группа" относятся к одному или более атомов, которые соединяют один химический фрагмент с другим химическим фрагментом. Примеры связывающих групп включают группы с относительно низкой молекулярной массой, такие как амид, сложный эфир, карбонат и простой эфир, а также связывающие группы с более высокой молекулярной массой, такие как полиэтиленгликоль (ПЭГ).
При этом в любом соединении, описанном здесь, имеющем один или более хиральных центров, если абсолютная стереохимия не указана четко, тогда каждый центр может независимо иметь или R-конфигурацию, или S-конфигурацию, или их смесь. Таким образом, соединения, предоставляемые здесь, могут быть энантиомерно чистыми или представлять собой стереоизомерные смеси. Дополнительно, при этом в любом соединении, описанном здесь, имеется одна или более двойных связей, генерирующих геометрические изомеры, которые могут быть определены как Е или Z, при этом каждая двойная связь может быть независимо Е или Z, или их смесью. Также предполагается, что включены все таутомерные формы.
При использовании здесь аббревиатуры для любых защитных групп, аминокислот и других соединений приводятся, если не указано иное, согласно их общепринятому использованию, общепризнанными аббревиатурами или Комиссии по биохимической номенклатуре IUPAC-IUP (See, Biochem. 11:942-944 (1972)).
Один из объектов настоящего изобретения относится к визуализирующему агенту фиброзных заболеваний, содержащему ретиноид и детектируемую метку.
Ретиноид в настоящем изобретении может воздействовать на клетки, положительные по альфа-SMA и продуцирующие ЕСМ, такие как активированные звездчатые клетки, которые вовлечены в фиброзное заболевание. Хотя механизм, по которому ретиноид воздействует на клетки, положительные по альфа-SMA и продуцирующие ЕСМ, не объяснен полностью, предполагается, например, что ретиноид, специфически связанный с RBP (ретинол-связывающий белок), связывается с и/или поглощается указанными клетками через определенный тип рецептора на их поверхности.
Ретиноид, который может использоваться в настоящем изобретении, включает, но не ограничивается этим, производные ретиноида, такие как ретинол, ретиналь, ретиноевая кислота, сложный эфир ретинола и жирной кислоты, сложный эфир алифатического спирта и ретиноевой кислоты, этретинат, третиноин, изотретиноин, адапален, ацитретин, тазаротен и пальмитат ретинола, и аналоги витамина А, такие как фенретинид (4-HPR) и бексаротен. Ретиноид также включает рексиноиды, т.е. ретиноидные соединения, которые являются селективными для рецепторов ретиноида Х (RXR), такие как бексаротен.
Из них ретинол, ретиналь, ретиноевая кислота, сложный эфир ретинола и жирной кислоты (например, ретинил ацетат, ретинил пальмитат, ретинил стеарат и ретинил лаурат) и сложный эфир алифатического спирта и ретиноевой кислоты (например, этилретиноат) являются предпочтительными с точки зрения эффективности специфического нацеливания указанных ЕСМ-продуцирующих клеток. В другом предпочтительном варианте осуществления ретиноид в настоящем изобретении не включает ретиноевую кислоту и/или производные ретиноевой кислоты. Таим образом, предпочтительный ретиноид в этих вариантах осуществления включает ретинол, ретиналь, сложный эфир ретинола и жирной кислоты и т.д.
Для цели настоящего изобретения ретиноид также включает все изомеры ретиноида, такие как цис/транс изомеры. Специфические примеры таких изомеров включают, но не ограничиваются этим, например, полностью-транс ретинол, полностью-транс ретиноевую кислоту, 11-цис-ретиналь и 13-цис-ретиноевую кислоту. Ретиноид может быть замещен одним или более заместителей. Ретиноид в настоящем изобретении включает ретиноид в выделенном состоянии, а также в растворе или смешанном состоянии со средой, которая может растворять или сохранять ретиноид.
Детектируемая метка (или просто обозначаемая как "метка") в настоящем изобретении включает любые метки, которые могут обнаруживаться любыми существующими средствами детектирования. Средства детектирования включают, но не ограничиваются этим, например, невооруженный глаз, устройство для оптического исследования (такое как оптический микроскоп, флуоресцентный микроскоп, фазово-контрастный микроскоп, визуализирующее устройство in vivo), рентгеновскую установку (такую как обычная рентгеновская установка, аппарат для компьютерной томографии), аппарат для МРТ (магнитно-резонансной томографии), аппарат для радионуклидного исследования (такой как сцинтиграфический аппарат, аппарат для PET (позитронно-эмиссионной томографии), аппарат для SPECT (однофотонной эмиссионной компьютерной томографии)), ультрасонографический аппарат и термографический аппарат. Метки, пригодные для каждого средства детектирования, известны специалистам в данной области техники и описаны, например, в Lecchi et al., Q J Nucl Med Mol Imaging. 2007; 51(2): 111-26.
Метка, подходящая для детектирования невооруженным глазом и устройством для оптического исследования, включает, например, различные флуоресцентные метки и люминесцентные метки. Специфическая флуоресцентная метка, которая может использоваться, включает, но не ограничивается этим, например, серию Cу™ (например, Cу™ 2, 3, 5, 5.5, 7), серию DyLight™ (например. DyLight™ 405, 488, 549, 594, 633, 649, 680, 750, 800), серию Alexa Fluor(R) (например, Alexa Fluor(R) 405, 488, 549, 594, 633, 647, 680, 750), серию HiLyte Fluor™ (например, HiLyte Fluor™ 488, 555, 647, 680, 750), серию АТТО (например, АТТО 488, 550, 633, 647N, 655, 740), FAM (карбоксифлуоресцеин), FITC (изотиоцианат флуоресцеина), техасский красный, GFP (зеленый флуоресцентный белок), RFP (красный флуоресцентный белок) и Qdot. В настоящем изобретении флуоресцентные метки, подходящие для визуализации in vivo, представляют собой, например, те, которые испускают флуоресценцию с длиной волны, которая является высоко проходящей через живой организм и менее чувствительной к автономной флуоресценции, такой как флуоресценция с длиной волны ближней инфракрасной области, или те, которые проявляют сильную интенсивность флуоресценции. Такие флуоресцентные метки включают, но не ограничиваются ими, например, серию Cу™, серию DyLight™, серию Alexa Fluor(R), серию HiLyte Fluor™, серию АТТО, техасский красный, GFP, RFP, Qdot и их производные.
Специфическая люминесцентная метка, которая может использоваться, включает, но не ограничивается этим, например, люминол, люциферин, люцигенин и экворин. Подходящая метка для детектирования посредством рентгеновской установки включает, например, различные контрастные агенты. Специфический контрастный агент, который может использоваться, включает, но не ограничивается этим, например, атом йода, ионы йода и йодсодержащие соединения.
Подходящая метка для детектирования посредством аппарата МРТ включает, например, различные атомы металла и соединения, содержащие указанный(е) атом(ы) металла, такие как комплексы указанного(ых) атома(ов). Конкретно, она может использовать, но не ограничивается этим, например, гадолиний (III) (Gd(III)), иттрий-88 (88Y), индий-111 (111In), комплексы атома(ов) таких металлов и лиганда, такого как диэтилентриаминпентауксусная кислота (DTPA), тетраазациклододекан-1,4,7,10-тетрауксусная кислота (DOTA), (1,2-этандиилдинитрило)тетраацетат (EDTA), этилендиамин, 2,2′-бипиридин (bipy), 1,10-фенантролин (phen), 1,2-бис(дифенилфосфино)этан (DPPE), 2,4-пентандион (acac) и этандиоат (ох), суперпарамагнитный оксид железа (SPIO) и оксид марганца (MnO).
Группа, которая включает хелат парамагнитного металла, является одним примером подходящей метки для детектирования аппаратом МРТ. В некоторых вариантах осуществления изобретения хелат парамагнитного металла может включать одну из следующих групп:
[Схем.7]
 или
или  .
.
Подходящая метка для детектирования посредством аппарата для радионуклидного исследования включает, например, различные радиоизотопы и соединения, содержащие указанный(е) радиоизотоп(ы), такие как комплексы указанного(ых) радио-изотопа(ов). Радиоизотопы, которые могут использоваться, включают, но не ограничиваются этим, например, технеций-99m (99mTc), индий-111 (111In), йод-123 (123I), йод-124 (123I), йод-125 (125I), йод-131 (131I), таллий-201 (201Tl), углерод-11 (11С), азот-13 (13N), кислород-15 (15О), фтор-18 (18F), медь-64 (64Cu), галлий-67 (67Ga), криптон-81m (81mKr), ксенон-133 (133Хе), стронций-89 (89Sr) и иттрий-90 (90Y). Соединения, содержащие радиоизотоп, включают, но не ограничиваются этим, например, 123I-IMP, 99mTc-HMPAO, 99mTc-ECD, 99mTc-MDP, 99mTс-тетрофосмин, 99mTc-MIBI, 99mTcO4-, 99mТс-МАА, 99mTc-MAG3, 99mTc-DTPA, 99mTc-DMSA и 18F-FDG1.
Подходящая метка для детектирования ультрасонографическим аппаратом, который может использоваться, включает, но не ограничивается этим, например, наночастицы и липосомы.
Визуализирующий агент по настоящему изобретению может быть образован только из вышеупомянутых ретиноида и метки или может быть образован связыванием этих двух компонентов с носителем, или их заключением в носитель, который является отличным от указанных компонентов. Следовательно, визуализирующий агент по настоящему изобретению может включать носитель, отличный от ретиноида и метки. Такой носитель не особо ограничивают, и любой носитель, известный в медицинской и фармацевтической областях, может использоваться, но предпочтительны те, которые могут включать в себя ретиноид или связываться с ним.
Примеры такого носителя включают липид, например, фосфолипид, такой как глицерофосфолипид, сфинголипид, такой как сфингомиелин, стерин, такой как холестерин, растительное масло, такое как соевое масло или маковое масло, минеральное масло, лецитин, такой как лецитин из яичного желтка, полимеры, и носители, содержащие лиганд, который не ограничивается полимером, но примеры этим не ограничиваются. Среди них предпочтительны те, что могут образовывать липосомы, например, природный фосфолипид, такой как лецитин, полусинтетический фосфолипид, такой как димиристоилфосфатидилхолин (DMPC), дипальмитоилфосфатидилхолин (DPPC) или дистеароилфосфатидилхолин (DSPC), диолеилфосфатидилэтаноламин (DOPE), дилауроилфосфатидилхолин (DLPC) и холестерин. Лиганд может быть монодентатным лигандом или полидентатньш лигандом, который может формировать хелат.
Особенно предпочтительным носителем является носитель, который может избежать захвата ретикулоэндотелиальной системой, и его примеры включают катионные липиды, такие как N-(альфа-триметиламмониоацетил)-дидодецил-D-глутамат хлорид (TMAG), N,N′,N″,N′″-тетраметил-N,N′,N″,N′″-тетрапальмитилспермин (TMTPS), 2,3-диолеилокси-N-[2(сперминкарбоксамидо)этил]-N,N-диметил-1-пропанаминий триф-торацетат (DOSPA), N-[l-(2,3-диолеилокси)пропил]-N,N,N-ттриметиламмоний хлорид (DOTMA), диоктадецилдиметиламмоний хлорид (DODAC), дидодециламмоний бромид (DDAB), 1,2-диолеилокси-3-триметиламмониопропан (DOTAP), 3b-[N-(N′,N′-диметиламиноэтан)карбамоил]холестерин (DC-Chol), 1,2-димиристоилоксипропил-3-диметилгидроксиэтиламмоний (DMRIE) и O,O′-дитетрадеканоил-N-(альфа-триметиламмониоацетил)диэтаноламин хлорид (DC-6-14).
Связывание ретиноида и/или метки с носителем по настоящему изобретению или заключение в него ретиноида и/или метки также возможно посредством связывания ретиноида и/или метки с носителем или заключения ретиноида и/или метки в носитель путем химического и/или физического способа. Например, ретиноид и/или метка могут непосредственно присоединяться к носителю. В одном из вариантов осуществления ретиноид и/или метка могут непосредственно присоединяться к носителю через кислород, серу, азот и/или атом углерода ретиноида и/или метки. В других вариантах осуществления ретиноид и/или метка могут дополнительно включать лин-керную группу. В варианте осуществления изобретения ретиноид и/или метка могут присоединяться к носителю через линкерную группу. Линкерная группа может быть относительно небольшой. Например, линкерная группа может содержать амин, амид, простой эфир, сложный эфир, гидроксильную группу, карбонильную группу или тиоэфирную группу. Альтернативно, линкерная группа может быть относительно большой. Например, линкерная группа может содержать алкильную группу, арильную группу, арил(С1-6 алкильную) группу (например, фенил-(СН2)1-4-), гетероарильную группу или гетероарил(С1-6 алкильную)группу. В одном из вариантов осуществления линкер может являться -NH(CH2)1-4-NH-. В другом варианте осуществления линкер может являться -(CH2)1-4-арил-NH-. В качестве примера, линкерная группа может быть присоединена вместо водорода на углероде ретиноида и/или метки. Линкерная группа может быть добавлена к носителю, используя способы, известные специалисту в данной области техники.
Альтернативно, связывание ретиноида и/или метки с носителем или заключение ретиноида и/или метки в носитель может также проводиться путем смешивания ретиноида и/или метки и носителя при получении настоящего визуализирующего агента. Альтернативно, если носитель содержит лиганд, который не ограничивается полимером, возможно получить метку, детектируемую магнитно-резонансным визуализированием или радионуклидным исследованием, которая закреплена указанным лигандом.
Количество ретиноида в визуализирующем агенте по настоящему изобретению может составлять предпочтительно 1-10000 наномоль/микролитр (нмоль/мкл), более предпочтительно 10-1000 нмоль/мкл. Количество метки может быть известно в данной области техники, но может быть соответствующим образом увеличено или уменьшено, учитывая различные условия, такие как количество ретиноида и природа носителя. Связывание ретиноида с носителем или заключение ретиноида в носитель может проводиться перед тем, как метка нанесена на носитель, может проводиться одновременно со смешиванием носителя, ретиноида и метки или может проводиться смешиванием ретиноида с носителем, на который метка уже нанесена. Следовательно, настоящее изобретение также относится к способу получения визуализирующего агента фиброзных заболеваний, при этом способ включает стадию связывания ретиноида с любым существующим меченным составом.
Форма носителя по настоящему изобретению может быть любой формой, при условии, что метка может переноситься к клетке-мишени, продуцирующей внеклеточный матрикс, и, не ограничиваясь этим, примеры ее включают макромолекулярную мицеллу, липосому, эмульсию, микросферы и наносферы. Когда носитель находится в форме липосомы, молярное соотношение ретиноида и липида, образующего липосому, в качестве носителя составляет предпочтительно 8:1-1:4, более предпочтительно 4:1-1:2, учитывая эффективность связывания ретиноида с носителем или заключения ретиноида в носитель.
Носитель визуализирующего агента по настоящему изобретению может содержать метку в своей внутренней части, может присоединять ее к наружной части или может смешиваться с меткой, при условии, что ретиноид присутствует в такой конфигурации, что он может функционировать как направленный агент. При упоминании здесь "функционирование как направленный агент" означает, что визуализирующий агент, содержащий ретиноид, достигает и/или принимается клеткой-мишенью, т.е., клеткой, продуцирующей внеклеточный матрикс, более быстро, эффективно и/или в более высоком количестве, чем в случае визуализирующего агента, не содержащего ретиноид, и это может быть легко подтверждено, например, добавлением визуализирующего агента по настоящему изобретению к культуре клеток-мишеней и анализом сайтов, на которых метка присутствует, через заранее определенный период времени. Структурно, вышеуказанные требования могут удовлетворяться, например, если ретиноид по меньшей мере частично экспонирован на наружной части визуализирующего агента не позднее, чем он достигнет клетки-мишени. Экспонирован ли ретиноид по меньшей мере частично на наружной части визуализирующего агента или нет, можно оценить контактированием визуализирующего агента с веществом, которое специфически связывается с ретиноидом, таким как ретинол-связывающий белок (RBP), и исследованием его связывания с визуализирующим агентом. Экспонирование ретиноида на наружной части визуализирующего агента по меньшей мере частично не позднее, чем он достигнет клетки-мишени, можно осуществить, например, регулированием соотношения ретиноида и метки и/или при необходимости носителя в составе.
В одном из вариантов осуществления носителем является полимер, который может содержать повторяющееся звено Формулы (V):
[Схем. 8]

где: s может означать независимо 1 или 2; А7 и А8 могут означать каждый независимо кислород или NR12; R12 может означать водород или C1-4 алкил; R10 и R11 могут быть каждый независимо выбраны из при необходимости замещенного C1-10 алкила, при необходимости замещенного С6-20 арила, аммония и щелочного металла; и/или повторяющееся звено Формулы (VI):
[Схем. 9]

где R13 может означать водород, аммоний или щелочной металл. Когда группа R13 означает водород, тогда повторяющееся звено Формулы (VI) представляет собой повторяющееся звено глутаминовой кислоты.
В одном варианте осуществления по меньшей мере один из R10, R11 и R13 может быть замещен ретиноидом и/или детектируемой меткой, так что и ретиноид, и детектируемая метка содержатся в визуализирующем агенте. Другими словами, ретиноид и детектируемая метка могут быть связаны с А7 и/или А8 Формулы (V) или с атомом О, связанным с C=O Формулы (VI). Однако ретиноид и детектируемая метка могут быть связаны с другой частью полимера. В предпочтительном варианте осуществления изобретения по меньшей мере один из R10, R11 и R13 замещен детектируемой меткой, и по меньшей мере один из R10, R11 и R13 замещен ретиноидом.
Следовательно, визуализирующий агент по настоящему изобретению может содержать или состоять из полимерного конъюгата, как определено ниже. Дополнительно, один из аспектов настоящего изобретения относится к указанному полимерному конъюгату сам по себе. Полимерный конъюгат может включать по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV):
[Схем. 10]




где: m может означать независимо 1 или 2; n может означать независимо 1 или 2; А1 и А2 могут означать каждый независимо кислород или NR7; А3 и А4 могут означать каждый независимо кислород или NR8; А5 и А6 могут означать каждый независимо кислород или NR9; R1, R2, R3, R4, R5 и R6 могут выбираться независимо каждый из при необходимости замещенного С1-10 алкила, при необходимости замещенного С6-20 арила, аммония, щелочного металла, ретиноида и группы, которая содержит детектируемую метку; R7, R8 и R9 могут означать каждый независимо водород или С1-4 алкил; о, p, q и r могут каждый означать независимо 0, 1 или более, где сумма о, p, q и r означает 2 или более; и при условии, что по меньшей мере один из R1, R2, R3, R4, R5 и R6 означают группу, которая содержит детектируемую метку, и по меньшей мере один из R1, R2, R3, R4, R5 и R6 означает ретиноид. Примеры щелочного металла включают литий (Li), натрий (Na), калий (К), рубидий (Rb) и цезий (Cs). В одном из вариантов осуществления щелочной металл означает натрий.
Широкий ряд других повторяющихся звеньев может включаться в полимерный конъюгат, содержащий по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV). В некоторых вариантах осуществления полимерный конъюгат, описанный здесь, может дополнительно включать повторяющееся звено Формулы (V):
[Схем. 11]

где: s может независимо означать 1 или 2; А7 и А8 могут каждый независимо означать кислород или NR12; R12 может означать водород или С1-4 алкил; R10 и R11 могут каждый независимо выбираться из при необходимости замещенного С1-10 алкила, при необходимости замещенного С6-20 арила, аммония и щелочного металла.
Вариант осуществления изобретения обеспечивает полимерный конъюгат, как описано здесь, который также может включать повторяющееся звено Формулы (VI):
[Схем. 12]

где R13 может означать водород, аммоний или щелочной металл. Если группа R13 означает водород, тогда повторяющееся звено Формулы (VI) означает повторяющееся звено глутаминовой кислоты.
Различные детектируемые метки могут являться частью полимерных конъюгатов, описанных здесь, например, полимерного конъюгата, содержащего по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV). В некоторых вариантах осуществления изобретения детектируемая метка может включать металл. Например, металл может выбираться из Gd(III), иттрия-88 и индия-111. В некоторых вариантах осуществления изобретения детектируемая метка может включать лиганд. Подходящие лиганды включают, но не ограничиваются этим, диэтилентриаминпентауксусную кислоту (DTPA), тетраазациклододекан-1,4,7,10-тетрауксусную кислоту (DOTA), (1,2-этандиилдинитрило)тетраацетат (EDTA), этилендиамин, 2,2′-бипиридин (bipy), 1,10-фенантролин (phen), 1,2-бис(дифенилфосфино)этан (DPPE), 2,4-пентандион (acac) и этандиоат (ох). В варианте осуществления изобретения детектируемая метка может включать лиганд, выбранный из диэтилентриаминпентауксусной кислоты (DTPA) и тетраазациклододекан-1,4,7,10-тетрауксусную кислоту (DOTA).
Группа, которая включает хелат парамагнитного металла, представляет собой один пример подходящей детектируемой метки. В некоторых вариантах осуществления изобретения хелат парамагнитного металла может включать одну из следующих групп:
[Схем. 13]
 или
или  .
.
Другой пример подходящей детектируемой метки означает краситель, такой как техасский красный или его производное.
[Схем. 14]
 .
.
Различные ретиноиды могут использоваться в полимерных конъюгатах, описанных здесь, например, полимерном конъюгате, содержащем по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV). Подходящие ретиноиды включают ретинол, ретиналь, ретиноевую кислоту, рексиноид или их производные или аналоги. Типичные ретинолы включают витамин А, полностью-транс ретинол, ретинил пальмитат и ретинил ацетат. Один пример ретиналя представляет собой 11-цис-ретиналь. Рексиноиды представляют собой ретиноидные соединения, которые селективны в отношении ретиноидных Х рецепторов (RXR). Типичный рексиноид представляет собой ретиноид бексаротен. Другие ретиноидные производные и аналоги включают этретинат, ацитретин, тазаротен, бексаротен, адапален и фенретинид. В некоторых вариантах осуществления изобретения ретиноид может выбираться из ретинола, ретиналя, ретиноевой кислоты, полностью-транс ретинола, полностью-транс ретиноевой кислоты, ретинил пальмитата, 11-цис-ретиналя и 13-цис-ретиноевой кислоты. В варианте осуществления изобретения ретиноид может включать витамин А. В другом варианте осуществления изобретения ретиноид может включать ретинол.
Группа, которая включает детектируемую метку, может быть конъюгирована с полимером множеством различных способов. В варианте осуществления изобретения группа, которая содержит детектируемую метку, может непосредственно присоединяться к полимеру. Например, группа, которая содержит детектируемую метку, может непосредственно присоединяться к повторяющемуся звену Формулы (I), (II), (III) и/или (IV). В одном варианте осуществления группа, которая содержит детектируемую метку, может непосредственно присоединяться к полимеру через атом кислорода, серы, азота и/или углерода группы, которая включает детектируемую метку. В других вариантах осуществления группа, которая включает детектируемую метку, может также включать линкерную группу. В варианте осуществления изобретения группа, которая включает детектируемую метку, может присоединяться к полимеру, например, к повторяющемуся звену Формулы (I), (II), (III) и/или (IV), через линкерную группу. Линкерная группа может быть относительно небольшой. Например, линкерная группа может содержать амин, амид, простой эфир, сложный эфир, гидроксильную группу, карбонильную группу или тиоэфирную группу. Альтернативно, линкерная группа может быть относительно большой. Например, линкерная группа может содержать алкильную группу, арильную группу, арил(С1-6 алкильную) группу (например, фенил-(СН2)1-4-), гетероарильную группу или гетероарил(С1-6 алкильную) группу. В одном варианте осуществления изобретения линкер может быть -NH(CH2)1-4-NH-. В другом варианте осуществления изобретения линкер может быть -(СН2)1-4-арил-NH-. В качестве примера линкерная группа может присоединяться вместо водорода к углероду группы, которая включает детектируемую метку. Линкерная группа может быть добавлена к полимеру, например, к повторяющемуся звену Формулы (I), (II), (III) и/или (IV), используя методы, известные специалистам в данной области техники.
Как и в случае группы, которая включает детектируемую метку, ретиноид может быть конъюгирован с полимером множеством различных путей. В одном варианте осуществления ретиноид может непосредственно присоединяться к полимеру. Например, ретиноид может непосредственно присоединяться к повторяющемуся звену Формулы (I), (II), (III) и/или (IV). В одном варианте осуществления изобретения ретиноид может непосредственно присоединяться к полимеру через атом кислорода, серы, азота и/или углерода ретиноида. Ретиноид может также конъюгироваться с полимером, например, полимером, который включает по меньшей мере одно повторяющееся звено Формулы (I), (II), (III) и/или (IV), через линкерную группу. Линкерные группы, описанные здесь, в отношении группы, которая включает детектируемую метку, могут также быть использованы с ретиноидом. Линкерная группа может добавляться к полимеру, например, к повторяющемуся звену Формулы (I), (II), (III) и/или (IV), и/или ретиноиду, используя способы, известные специалисту в данной области техники.
В некоторых вариантах осуществления изобретения m в Формуле (I) может означать 1. В варианте осуществления изобретения m в Формуле (I) может означать 2. В некоторых вариантах осуществления n в Формуле (II) может означать 1. В варианте осуществления изобретения n в Формуле (II) может означать 2. В некоторых вариантах осуществления изобретения s в Формуле (III) может означать 1. В других вариантах осуществления изобретения s в Формуле (III) может означать 2.
В некоторых вариантах осуществления полимерные конъюгаты, описанные здесь, могут включать щелочной металл, например, литий (Li), натрий (Na), калий (К), рубидий (Rb) и цезий (Cs). В варианте осуществления изобретения щелочной металл может означать натрий или калий. В варианте осуществления изобретения щелочной металл может означать натрий.
Полимеры, которые включают по меньшей мере два различных повторяющихся звена Формулы (I), (II), (III) и/или (IV), представляют собой сополимеры. Кроме того, полимеры, содержащие по меньшей мере одно из повторяющихся звеньев Формулы (I), (II), (III) и (IV), могут являться сополимерами, которые содержат другие повторяющиеся звенья, которые не представляют собой Формулу (I), (II), (III) и/или (IV).
Ряд повторяющихся звеньев Формулы (I) и ряд повторяющихся звеньев Формулы (II) могут каждый выбираться независимо и могут варьироваться в широком диапазоне. В варианте осуществления изобретения число повторяющихся звеньев Формулы (I) может находиться в пределах от около 50 до около 5000, и более предпочтительно от около 100 до около 2000. Также, в некоторых вариантах осуществления изобретения число повторяющихся звеньев Формулы (II) может находиться в диапазоне от около 50 до около 5000, и более предпочтительно от около 100 до около 2000.
Подобным образом, число повторяющихся звеньев Формулы (III) и число повторяющихся звеньев Формулы (IV) могут выбираться каждый независимо и могут варьировать. В варианте осуществления изобретения число повторяющихся звеньев Формулы (III) может находиться в диапазоне от около 50 до около 5000, и более предпочтительно от около 100 до около 2000. В некоторых вариантах осуществления изобретения число повторяющихся звеньев Формулы (IV) может находиться в диапазоне от около 50 до около 5000, и более предпочтительно от около 100 до около 2000.
Процентное содержание повторяющихся звеньев Формулы (I) в полимерном конъюгате по отношению к общему числу повторяющихся звеньев может изменяться в широком диапазоне. В одном варианте осуществления изобретения полимерный конъюгат может включать до около 99 мольн.% повторяющегося звена Формулы (I) по отношению к суммарным молям повторяющихся звеньев в полимерном конъюгате. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 99 мольн.% повторяющегося звена Формулы (I) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 50 мольн.% повторяющегося звена Формулы (I) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 30 мольн.% повторяющегося звена Формулы (I) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 20 мольн.% повторяющегося звена Формулы (I) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В другом варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 10 мольн.% повторяющегося звена Формулы (I) по отношению к общим молям повторяющихся звеньев полимерного конъюгата.
Процентное содержание повторяющихся звеньев Формулы (II) в полимерном конъюгате по отношению к общему числу повторяющихся звеньев может также изменяться в широком диапазоне. В одном варианте осуществления полимерный конъюгат может включать до около 99 мольн.% повторяющегося звена Формулы (II) по отношению к суммарным молям повторяющихся звеньев в полимерном конъюгате. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 99 мольн.% повторяющегося звена Формулы (II) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 50 мольн.% повторяющегося звена Формулы (II) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 30 мольн.% повторяющегося звена Формулы (II) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 20 мольн.% повторяющегося звена Формулы (II) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В другом варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 10 мольн.% повторяющегося звена Формулы (II) по отношению к общим молям повторяющихся звеньев полимерного конъюгата.
Процентное содержание повторяющихся звеньев Формулы (III) в полимерном конъюгате по отношению к общему числу повторяющихся звеньев может изменяться в широком диапазоне. В одном варианте осуществления полимерный конъюгат может включать до около 99 мольн.% повторяющегося звена Формулы (III) по отношению к суммарным молям повторяющихся звеньев в полимерном конъюгате. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 99 мольн.% повторяющегося звена Формулы (III) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 50 мольн.% повторяющегося звена Формулы (III) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 30 мольн.% повторяющегося звена Формулы (III) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 20 мольн.% повторяющегося звена Формулы (III) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В другом варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 10 мольн.% повторяющегося звена Формулы (III) по отношению к общим молям повторяющихся звеньев полимерного конъюгата.
Подобным образом, процентное содержание повторяющихся звеньев Формулы (IV) в полимерном конъюгате по отношению к общему числу повторяющихся звеньев может изменяться в широком диапазоне. В одном варианте осуществления полимерный конъюгат может включать до около 99 мольн.% повторяющегося звена Формулы (IV) по отношению к суммарным молям повторяющихся звеньев в полимерном конъюгате. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 99 мольн.% повторяющегося звена Формулы (IV) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 50 мольн.% повторяющегося звена Формулы (IV) по отношению к суммарным молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 30 мольн.% повторяющегося звена Формулы (IV) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 20 мольн.% повторяющегося звена Формулы (IV) по отношению к общим молям повторяющихся звеньев полимерного конъюгата. В варианте осуществления изобретения полимерный конъюгат может включать от около 1 мольн.% до около 10 мольн.% повторяющегося звена Формулы (IV) по отношению к общим молям повторяющихся звеньев полимерного конъюгата.
Если одно или более повторяющихся звеньев Формулы (V) присутствуют в полимерном конъюгате, процентное содержание повторяющихся звеньев Формулы (V) в полимерном конъюгате по отношению к общему числу повторяющихся звеньев может варьировать в широком диапазоне. Подобным образом, если одно или более повторяющихся звеньев Формулы (VI) присутствуют в полимерном конъюгате, процентное содержание повторяющихся звеньев Формулы (VI) в полимерном конъюгате по отношению к общему числу повторяющихся звеньев может варьировать в широком диапазоне. Типичные примеры осуществления изобретения представлены в Таблице 1.
Мольные проценты основаны на суммарных молях повторяющихся звеньев полимерного конъюгата.
В одном варианте осуществления изобретения детектируемая метка может являться нековалентно инкапсулированной или частично инкапсулированной в полимерную матрицу описанного здесь полимерного конъюгата. Например, полимерные конъюгаты, описанные здесь, могут присутствовать в различных формах, включая форму частиц, хлопьев, стержней, волокон, пленок, пен, суспензий (в жидкости или газе), геля, твердого вещества или жидкости. Размер и форма этих различных форм не ограничены. Свободная(ые) и неконъюгированная(ые) детектируемая(ые) метка(и), такие как описанные выше, могут смешиваться с полимерным конъюгатом, описанным здесь, который формирует матрицу, и нековалентно инкапсулироваться или частично инкапсулироваться в него. Похожим образом, ретиноид может нековалентно инкапсулироваться или частично инкапсулироваться в полимерную матрицу или полимерный конъюгат, описанный здесь.
Количество детектируемой метки в полимерном конъюгате может изменяться в широком диапазоне. В варианте осуществления изобретения полимерный конъюгат может включать суммарное количество детектируемой метки в диапазоне от около 0.5% до около 50% (масс./масс.), исходя из массового соотношения детектируемой метки и полимерного конъюгата (масса детектируемой метки вычисляется в полимерном конъюгате). В варианте осуществления изобретения полимерный конъюгат может включать количество детектируемой метки в диапазоне от около 1% до около 40% (масс./масс.) в расчете на массовое соотношение детектируемой метки и полимерного конъюгата (то же основание). В варианте осуществления изобретения полимерный конъюгат может включать количество детектируемой метки в диапазоне от около 1% до около 30% (масс./масс.) в расчете на массовое соотношение детектируемой метки и полимерного конъюгата (то же основание). В варианте осуществления изобретения полимерный конъюгат может включать количество детектируемой метки в диапазоне от около 1% до около 20% (масс./масс.) в расчете на массовое соотношение детектируемой метки и полимерного конъюгата (то же основание). В варианте осуществления изобретения полимерный конъюгат может включать количество детектируемой метки в диапазоне от около 1% до около 10% (масс./масс.) в расчете на массовое соотношение детектируемой метки и полимерного конъюгата (то же основание).
Количество ретиноида, присутствующего в полимерном конъюгате, может также изменяться в широком диапазоне. В некоторых вариантах осуществления изобретения ретиноид может составлять от около 1% до около 50% (масс./масс.) от общей массы полимерного конъюгата (где масса ретиноида включена в общую массу полимерного конъюгата). В других вариантах осуществления изобретения ретиноид может составлять от около 10% до около 30% масс./масс. от общей массы полимерного конъюгата (то же основание). В других вариантах осуществления изобретения ретиноид может составлять от около 20% до около 40% масс./масс. от общей массы полимерного конъюгата (то же основание).
Количество детектируемой метки, количество ретиноида и процентные количества повторяющихся звеньев Формулы (I), (II), (III) и/или (IV) могут предпочтительно выбираться, чтобы обеспечить растворимость полимерного конъюгата, которая составляет больше, чем у сопоставимого конъюгата полиглутаминовой кислоты, который по существу содержит такое же количество такого (таких) же агента(ов). В варианте осуществления изобретения растворимость полимерного конъюгата выше, чем у сравнимого конъюгата полиглутаминовой кислоты. Растворимость измеряют, получая раствор полимерного конъюгата, содержащий по меньшей мере 5 мг/мл полимерного конъюгата в 0.9 масс.% водного NaCl при около 22 градусов Цельсия (°С), и определяя оптическую прозрачность. Оптическую прозрачность можно определить турбидиметрически, например, визуальным наблюдением или с помощью соответствующих инструментальных способов, известных специалистам в данной области техники. Сравнение полученной растворимости с раствором конъюгата полиглутаминовой кислоты, полученной подобным образом, демонстрирует улучшенную растворимость, которая подтверждена более высокой оптической прозрачностью в более широком диапазоне значений рН. Таким образом, растворимость полимерного конъюгата выше, чем у сопоставимого конъюгата полиглутаминовой кислоты, который содержит по существу такое же количество агента, когда раствор тестируемого полимерного конъюгата, содержащий по меньшей мере 5 мг/мл полимерного конъюгата в 0.9 масс.% водного NaCl при около 22°С имеет более высокую оптическую прозрачность в более широком диапазоне рН, чем раствор сопоставимого тестируемого конъюгата полиглутаминовой кислоты. Специалистам в данной области техники будет понятно, что "сопоставимый" конъюгат полиглутаминовой кислоты является контрольным материалом, в котором полимерная часть конъюгата имеет молекулярную массу, которая является приблизительно такой же, как у рассматриваемого полимерного конъюгата (содержащего повторяющееся звено Формулы (I), (II), (III) и/или (IV)), с которым он сравнивается.
Полимерный конъюгат может содержать один или более хиральных атомов углерода. Хиральный углерод (который может обозначаться звездочкой*) может иметь rectus (правовращающую) или sinister (левовращающую) конфигурацию, и таким образом повторяющееся звено может быть рацемическим, энантиомерным или энантиомерно обогащенным. Символы "n" и "*" (обозначающие хиральный углерод), при использовании здесь в другом месте, могут иметь одинаковое значение, как указано выше, если не установлено другое.
Полимерные конъюгаты, содержащие по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV), могут быть получены различными способами. В одном варианте осуществления первый полимерный реагент может быть растворен или частично растворен в растворителе с образованием первого растворенного или частично растворенного полимерного реагента. Первый растворенный или частично растворенный полимерный реагент может затем реагировать со вторым реагентом с образованием второго полимерного реагента. В варианте осуществления изобретения второй реагент может включать группу, которая содержит детектируемую метку. В другом варианте осуществления ретиноид может быть ретинолом или его производным. Еще в одном другом варианте осуществления изобретения второй реагент может включать лиганд, такой как диэтилентриаминпентауксусная кислота (DTPA), тетраазациклододекан-1,4,7,10-тетрауксусная кислота (DOTA), (1,2-этандиилдинитрило)тетраацетат (EDTA), этилендиамин, 2,2′-бипиридин (bipy), 1,10-фенантролин (phen), 1,2-бис(дифенилфосфино)этан (DPPE), 2,4-пентандион (асас) и этандиоат (ох). В варианте осуществления изобретения второй реагент может включать заместитель, выбранный из гидрокси-группы и амина.
Первый полимерный реагент может включать любой подходящий материал, способный к формированию полимера, содержащего по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV). В одном варианте осуществления изобретения полимерный реагент может включать повторяющееся звено Формулы (VII):
[Схем. 15]

где z может означать независимо 1 или 2; А9 и А10 могут каждый означать кислород; и R14, и R15 могут каждый независимо выбираться из водорода, аммония и щелочного металла.
В другом варианте осуществления первый полимерный реагент может включать повторяющееся звено Формулы (VIII):
[Схем. 16]

где R16 может выбираться из водорода, аммония и щелочного металла.
Второй полимерный реагент может затем реагировать с третьим реагентом с образованием промежуточного продукта или, в некоторых вариантах осуществления, полимера, содержащего по меньшей мере одно повторяющееся звено Формулы (I), (II), (III) и (IV). Если необходимо или желательно, второй полимерный реагент может растворяться или частично растворяться в растворителе с образованием второго растворенного иди частично растворенного полимерного реагента. В варианте осуществления изобретения третий реагент может включать группу, которая содержит детектируемую метку. В другом варианте осуществления третий реагент может включать ретиноид. В варианте осуществления ретиноид может быть ретинолом или его производным. В других еще вариантах осуществления третий реагент может включать лиганд, например, как описанные в отношении второго реагента. В варианте осуществления изобретения второй реагент может включать заместитель, выбранный из гидрокси и амина.
Если второй или третий реагент означают лиганд, четвертый реагент может быть добавлен после добавления лиганда, когда четвертый реагент включает металл. Типичные металлы включают, но не ограничиваются этим, Gd(III), иттрий-88 и индий-111.
Смеси свободных детектируемых меток и/или ретиноидов с полимерными конъюгатами, описанными здесь, могут формироваться различными путями, например, с образованием матрицы, в которой несколько или все детектируемые метки и/или ретиноиды являются нековалентно инкапсулированными или частично инкапсулированными. Такая смесь может содержать, например, как конъюгированную(ые), так и неконъюгированную(ые) метку(и) и/или ретиноид(ы).
Полимерные реагенты могут растворяться или частично растворяться в ряде растворителей, подготавливая их для смешивания с группой, которая содержит детектируемую метку, ретиноид и/или лиганд. В варианте осуществления изобретения растворитель может включать гидрофильный растворитель, такой как полярный растворитель. Подходящие полярные растворители включают протонсодержащие растворители, такие как вода, метанол, этанол, пропанол, изопропанол, бутанол, муравьиная кислота и уксусная кислота. Другие подходящие полярные растворители включают апротонные растворители, например, ацетон, ацетонитрил, диметилформамид, диметилсульфоксид, тетрагидрофуран и 1,4-диоксан. В варианте осуществления изобретения растворитель может быть водным растворителем, например, водой.
Растворению или частичному растворению полимерных реагентов в растворителе можно дополнительно помочь, используя стандартные механические методики. Например, полимерный конъюгат можно встряхивать или перемешивать в растворителе, чтобы вызвать растворение или частичное растворение. В варианте осуществления изобретения полимер и растворитель обрабатывают ультразвуком. Обработка ультразвуком является действием, связанным с применением звуковой энергии, например, ультразвуковой энергии, чтобы перемешивать частицы в образце. Обработка ультразвуком может происходить, например, при использовании, например, ультразвуковой ванны или ультразвукового зонда. Степень, до которой растворяется полимер, может контролироваться путем изменения интенсивности и длительности механического встряхивания, или перемешивания, или условий ультразвуковой обработки. Встряхивание, перемешивание или ультразвуковая обработка могут происходить в течение любого временного интервала. Например, смесь можно обрабатывать ультразвуком в течение периода времени, находящегося в интервале от нескольких секунд до нескольких часов. В одном из вариантов осуществления изобретения полимерный конъюгат может обрабатываться ультразвуком в растворителе в течение периода времени, находящегося в интервале от 1 минуты до 10 минут. В одном из вариантов осуществления изобретения полимерный конъюгат может обрабатываться ультразвуком в растворителе в течение около 5 минут.
В одном из вариантов осуществления изобретения группа, которая содержит детектируемую метку и/или лиганд, может добавляться в раствор полимерного конъюгата. Группа, которая содержит детектируемую метку и/или лиганд, может или нет растворяться или частично растворяться в растворителе(ях) перед ее смешиванием с полимерным конъюгатом. Если группа, которая содержит детектируемую метку и/или лиганд, растворяется или частично растворяется в растворителе, растворитель может включать гидрофильный растворитель, например, полярный растворитель. Подходящие полярные растворители включают протонные растворители, такие как вода, метанол, этанол, пропанол, изопропанол, бутанол, муравьиная кислота, уксусная кислота и ацетон. Другие подходящие полярные растворители включают апротонные растворители, такие как ацетон, ацетонитрил, диметилформамид, диметилсульфоксид, тетрагидрофуран и 1,4-диоксан.
Подобным образом, в одном из вариантов осуществления изобретения ретиноид может добавляться к раствору полимерного реагента. Ретиноид может или нет растворяться или частично растворяться в растворителе(ях) перед тем, как он смешивается с полимерным реагентом. Если ретиноид растворяется или частично растворяется в растворителе, растворитель может включать гидрофильный растворитель, такой как полярный растворитель. Подходящие полярные растворители включают протонные растворители, такие как вода, метанол, этанол, пропанол, изопропанол, бутанол, муравьиную кислоту, уксусную кислоту и ацетон. Другие подходящие полярные растворители включают апротонные растворители, такие как ацетон, ацетонитрил, диметилформамид, диметилсульфоксид, тетрагидрофуран и 1,4-диоксан.
После того как группу, которая содержит группу, которая содержит детектируемую метку, ретиноид и/или лиганд, добавляют к раствору полимерного реагента, например, с использованием пипетки, можно проводить дополнительное перемешивание. Например, раствор, содержащий полимерный реагент и группу, которая содержит детектируемую метку, можно встряхивать или перемешивать. В одном из вариантов осуществления изобретения раствор, содержащий полимерный конъюгат и группу, которая содержит детектируемую метку, может обрабатываться ультразвуком. Встряхивание, перемешивание или обработка ультразвуком могут происходить в течение любого временного интервала. Например, смесь может обрабатываться ультразвуком в течение периода времени в интервале от нескольких секунд до нескольких часов.
В одном из вариантов осуществления изобретения полимерный реагент и группа, которая содержит детектируемую метку, ретиноид и/или лиганд, смешивают вместе перед тем, как оба растворяют в растворителе. В одном из вариантов осуществления изобретения растворитель или смесь растворителей могут добавляться к смеси полимерного реагента и группе, которая содержит детектируемую метку, ретиноид и/или лиганд. После того, как растворитель или смесь растворителей добавляют к полимерному реагенту и группе, которая содержит детектируемую метку, ретиноид и/или лиганд, один или более из полимерного реагента и группы, которая содержит детектируемую метку, ретиноид и/или лиганд, могут растворяться или частично растворяться. Растворитель или смесь растворителей может включать один или более из воды, метанола, этанола, пропанола, изопропанола, бутанола, муравьиной кислоты, уксусной кислоты, ацетона, ацетонитрила, диметилформамида, диметилсульфоксида, тетрагидрофурана и 1,4-диоксана. В одном из вариантов осуществления изобретения смесь растворителей может включать спирт и воду. В одном из вариантов осуществления изобретения смесь растворителей может включать этанол и воду.
При необходимости полимерный конъюгат, содержащий группу, которая содержит детектируемую метку и ретиноид, может затем быть выделен и/или очищен. Подходящие способы, известные специалистам в данной области техники, могут использоваться для выделения и/или очистки полимерных конъюгатов, описанных здесь. Полимерные конъюгаты могут затем высушиваться любым подходящим способом, известным специалистам в данной области техники. Например, в одном из вариантов осуществления изобретения полимерный конъюгат может быть лиофилизирован. Условия лиофилизации композиции могут меняться. В одном из вариантов осуществления изобретения смесь может быть лиофилизирована при температуре в диапазоне от около -30°С до около -10°С. В одном из вариантов осуществления изобретения смесь может быть лиофилизирована при температуре около -20°С. После того как полимерный конъюгат, содержащий группу, которая содержит детектируемую метку и ретиноид, при необходимости выделили и высушили, его можно затем хранить при соответствующих условиях. Например, состав может храниться при температуре, подходящий для лиофилизации, как указано выше.
Реакция с третьим реагентом может происходить перед, одновременно или после того, как растворенный или частично растворенный полимерный реагент прореагирует со вторым реагентом. В некоторых вариантах осуществления изобретения растворенный или частично растворенный полимерный реагент может реагировать с по меньшей мере частью второго реагента перед реакцией с третьим реагентом. В одном из вариантов осуществления изобретения промежуточное соединение, которое образуется после добавления по меньшей мере части второго реагента, может быть выделено перед добавлением третьего реагента. В другом варианте осуществления изобретения третий реагент может добавляться без выделения промежуточного соединения, которое образуется после добавления второго реагента. В других вариантах осуществления растворенный или частично растворенный полимерный реагент может реагировать с по меньшей мере частью второго реагента примерно в то же самое время, в которое происходит реакция с третьим реагентом. В одном из вариантов осуществления изобретения растворенный или частично растворенный полимерный реагент может реагировать с по меньшей мере частью второго реагента после проведения реакции с третьим реагентом. В одном из вариантов осуществления изобретения промежуточное соединение, которое образуется после добавления по меньшей мере части третьего реагента, может быть выделено перед добавлением второго реагента.
Если добавляют четвертый реагент, который включает металл, в некоторых вариантах осуществления изобретения четвертый реагент может быть добавлен примерно в то же самое время, что и третий и/или второй реагент. В одном варианте осуществления четвертый реагент может добавляться после третьего и/или второго реагента.
В одном из вариантов осуществления изобретения промежуточное соединение с лигандом, таким как описанные здесь, может выделяться перед добавлением четвертого реагента. В другом варианте осуществления изобретения четвертый реагент может добавляться к промежуточному соединению с лигандом без выделения промежуточного соединения.
В одном из вариантов осуществления изобретения способ получения полимерного конъюгата может включать реакцию растворенного или частично растворенного полимерного реагента со вторым реагентом и/или третьим реагентом в присутствии агента сочетания. Любой подходящий агент сочетания может использоваться. В одном из вариантов осуществления изобретения агент сочетания выбирают из 1-этил-3-(3-диметиламинопропил)-карбодиимида (EDC), 1,3-дициклогексилкарбодиимида (DCC), 1,1′-карбонилдиимидазола (CDI), N,N′-дисукцинимидилкарбоната (DSC), N-[(диметиламино)-1Н-1,2,3-триазоло-[4,5-b]пиридин-1-ил-метилен]-N-метилметанаминия гексафторфосфата N-оксида (HATU), 2-[(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметиламиния гексафторфосфата (HBTU), 2-[(6-хлор-1Н-бензотриазол-1-ил)-1,1,3,3-тетраметиламиния гексафторфосфата (HCTU), бензотриазол-1-ил-окси-трис-пирролидино-фосфония гексафторфосфата (PуBOP(R)), бром-трис-пирролидино-фосфония гексафторфосфата (PyBroP(R)), 2-[(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметиламиния тетрафторбората (TBTU) и бензотриазол-1-ил-окси-трис-(диметиламино)фосфония гексафторфосфата (ВОР).
Может использоваться любой подходящий растворитель, который позволяет проводить реакцию. В одном из вариантов осуществления изобретения растворитель может являться полярным апротонным растворителем. Например, растворитель может выбираться из N,N-диметилформамида (DMF), диметилсульфоксида (DMSO), N-метил-2-пиридона (NMP) и N,N-диметилацетамида (DMAc).
В другом варианте осуществления изобретения реакция может дополнительно включать проведение реакции растворенного или частично растворенного полимерного реагента в присутствии катализатора. Может использоваться любой катализатор, который способствует реакции. В одном из вариантов осуществления изобретения катализатор может содержать 4-диметиламинопиридин (DMAP).
В одном из вариантов осуществления изобретения полимер, содержащий по меньшей мере одно повторяющееся звено, выбранное из Формулы (I) и Формулы (II), может получаться, исходя из полиглутаминовой кислоты и аминокислоты, такой как аспарагиновая и/или глутаминовая кислота. Альтернативно, в другом варианте осуществления полимер может создаваться путем первого превращения материала исходной полиглутаминовой кислоты в форму ее соли. Форма соли полиглутаминовой кислоты может получаться реакцией полиглутаминовой кислоты с подходящим основанием, например, бикарбонатом натрия. Аминокислотный фрагмент может быть присоединен к боковой группе карбоновой кислоты полиглутаминовой кислоты. Среднемассовая молекулярная масса полиглутаминовой кислоты может изменяться в широком диапазоне, но предпочтительно составлять от около 10000 до около 500000 дальтон, и более предпочтительно от около 25000 до около 300000 дальтон. Такая реакция может использоваться для создания поли-(гамма-L-аспартил-глутамин) или поли-(гамма-L-глутамил-глутамин).
В одном из вариантов осуществления аминокислота защищается защитной группой перед присоединением к полиглутаминовой кислоте. Один пример защищенного аминокислотного фрагмента, подходящего для этой реакции, представляет собой гидрохлорид ди-трет-бутилового сложного эфира L-аспарагиновой кислоты, показанный ниже:
[Схем. 17]

Реакция полиглутаминовой кислоты с аминокислотой происходит в присутствии любого подходящего растворителя. В одном из вариантов осуществления изобретения растворитель может быть апротонным растворителем. В предпочтительном варианте осуществления изобретения растворитель может являться N,N′-диметилформамидом.
В одном из вариантов осуществления изобретения агент сочетания, такой как EDC, DCC, CDI, DSC, HATU, HBTU, HCTU, PуBOP(R), PyBroP(R), TBTU и BOP, могут использоваться. В других вариантах осуществления изобретения полиглутаминовая кислота и аминокислота могут реагировать с использованием катализатора (например, DMAP).
После завершения реакции, если атомы кислорода аминокислоты защищены, защитные группы могут удаляться с использованием известных способов, такие как применение подходящей кислоты (например, трифторуксусной кислоты). При желании форма соли полимера, полученного реакцией полиглутаминовой кислоты с аминокислотой, может быть получена обработкой кислой формы полимера подходящим растворителем-основанием, например, раствором бикарбоната натрия.
Полимер может быть извлечен и/или очищен способами, известными специалистам в данной области техники. Например, растворитель может быть удален подходящими методами, например, на роторном испарителе. Дополнительно, реакционная смесь может фильтроваться в кислый водный раствор для получения осадка. Полученный осадок затем можно отфильтровать и промыть водой.
В других вариантах осуществления изобретения полимер, содержащий по меньшей мере одно повторяющееся звено, выбранное из Формулы (I) и Формулы (II), может также включать повторяющуюся структурную единицу Формулы (VI), как указано выше. Один способ для образования такого полимера осуществляется, исходя из полиглутаминовой кислоты и путем ее реакции с аминокислотой, такой как аспарагиновая и/или глутаминовая кислота, в количестве, которое составляет менее чем 1.0 эквивалент аминокислоты по отношению к полиглутаминовой кислоте. Например, в одном из вариантов осуществления изобретения 0.7 эквивалентов аминокислоты в расчете на полиглутаминовую кислоту может реагировать с полиглутаминовой кислотой таким образом, что около 70% повторяющихся звеньев конечного полимера содержит аминокислоту. Как обсуждало выше, атомы кислорода аминокислоты могут быть защищены путем использования подходящей защитной группы. В одном варианте осуществления изобретения аминокислота может являться L-аспарагиновой кислотой или L-глутаминовой кислотой. В другом варианте осуществления изобретения атомы кислорода аминокислоты могут защищаться трет-бутиловыми группами. Если атомы кислорода аминокислоты защищены, защитные группы могут удаляться, используя известные способы, например, подходящую кислоту (например, трифторуксусную кислоту).
В некоторых вариантах осуществления изобретения полимер, содержащий по меньшей мере одно повторяющееся звено, выбранное из Формулы (III) и Формулы (IV), может быть получен, начиная с полиглутаминовой кислоты. Как описано ранее, полимер, содержащий по меньшей мере одно повторяющееся звено, выбранное из Формулы (III) и (IV), может также включать повторяющееся звено Формулы (V). Способ получения такого полимера осуществляется, исходя из полиглутаминовой кислоты и/или ее соли, и путем добавления менее чем 1.0 эквивалента аминокислоты, такой как L-аспарагиновая кислота или L-глутаминовая кислота.
Полимеры, содержащие повторяющиеся звенья из одного или более повторяющихся звеньев, выбранных из Формулы (I), (II), (III), (IV), (V) и (VI), могут быть синтезированы с применением различных соответствующих исходных мономеров, используя методы, известные специалистам в данной области техники.
Конъюгация группы, которая содержит детектируемую метку, с полимерной кислотой или ее солевой формой может проводиться различными способами, например, ковалентно связывая группу, содержащую детектируемую метку, с различными полимерами. Подобным образом, ретиноид может быть конъюгирован с полимерной кислотой или ее солью различными путями. Один способ для конъюгирования вышеуказанных групп с полимером осуществляется путем использования тепла (например, тепла, полученного при использовании микроволнового способа). Альтернативно, конъюгирование может происходить при комнатной температуре. Соответствующие растворители, агенты сочетания, катализаторы и/или буферы, такие как в общем известные специалистам в данной области техники и/или описанные здесь, могут использоваться для образования полимерного конъюгата.
В одном из вариантов осуществления полимер, описанный здесь (например, полимер, содержащий повторяющееся звено, выбранное из Формулы (I), (II), (III) и/или (IV)), может быть конъюгирован с детектируемой меткой, такой как описанные здесь. В одном из вариантов осуществления детектируемая метка может являться техасским красным-NH2.

В одном частном варианте осуществления изобретения полимер, содержащий по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), Формулы (II) и Формулы (V), может реагировать с DCC, красителем техасским красным-NH2, пиридином и 4-диметиламинопиридином. Смесь могут нагревать, используя микроволновой способ. В одном из вариантов осуществления изобретения реакцию можно нагревать вплоть до температуры в диапазоне около 100°С-150°С. В другом варианте осуществления время, в течение которого материалы могут нагреваться, находится в диапазоне от 5 до 40 минут. При желании реакционная смесь может охлаждаться до комнатной температуры. Подходящие способы, известные специалистам в данной области техники, могут использоваться для выделения и/или очистки полимерного конъюгата. Например, реакционная смесь может фильтроваться в кислый водный раствор. Любой осадок, который образуется, может затем фильтроваться и промываться водой. При необходимости осадок можно очистить любым подходящим способом. Например, осадок может переноситься в ацетон и растворяться, и полученный раствор может фильтроваться снова в раствор бикарбоната натрия. При желании полученный реакционный раствор может диализироваться в воду, используя целлюлозную мембрану, и полимер может лиофилизироваться и выделяться.
Альтернативно, группа, которая содержит детектируемую метку и/или ретиноид, может реагировать с аминокислотой, такой как глутаминовая кислота и/или аспарагиновая кислота, в которой группа, которая содержит детектируемую метку и/или ретиноид, связывается (например, ковалентно связывается) с аминокислотой. Соединение аминокислота-метка и/или аминокислота-ретиноид может затем реагировать с полиглутаминовой кислотой или ее солью с образованием полимерного конъюгата, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I) и Формулы (II). Группа, которая содержит детектируемую метку и/или ретиноид, может также присоединяться к мономеру, который будет использоваться для образования части полимерного конъюгата, такого как полимерный конъюгат, который включает повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV). Мономер затем полимеризуют, используя способы, известные специалистам в данной области техники, для образования полимерного конъюгата. Например, группа, которая содержит детектируемую метку и/или ретиноид, может присоединяться к глутаминовой кислоте перед полимеризацией. Подобным образом, группа, которая содержит детектируемую метку и/или ретиноид, может присоединяться к L-гамма-глутамилглутамину и/или гамма-L-аспартилглутамину. Полученный мономер с присоединенной группой, которая содержит детектируемую метку и/или ретиноид, может затем полимеризоваться, используя способы, известные специалистам в данной области техники, для формирования полимерного конъюгата.
После образования полимерного конъюгата может также быть измерено любое количество агента, не связанного ковалентно с полимером. Способы, известные специалистам в данной области техники, могут использоваться для подтверждения значительного отсутствия свободной детектируемой метки и/или ретиноида.
Полимерные конъюгаты, описанные выше, могут формироваться в наночастицы в водном растворе. Полимерные конъюгаты (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)), могут формироваться в наночастицы подобным образом. Такие наночастицы могут использоваться, чтобы предпочтительно доставлять детектируемую метку к выбранной ткани.
Визуализирующий агент и соединение (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV)), по настоящему изобретению может использоваться для диагностики фиброзного заболевания. Таким образом, настоящее изобретение также относится к диагностическому агенту фиброзного заболевания, содержащему визуализирующий агент и/или соединение по изобретению, а также к способу диагностирования фиброзного заболевания, предусматривающему стадию введения эффективного количества визуализирующего агента, соединения или указанного диагностического агента по изобретению субъекту, который нуждается в этом, и стадию детектирования метки, содержащейся во введенном визуализирующем агенте, соединении или диагностическом агенте.
Вариант осуществления изобретения обеспечивает композицию, которая может включать агент (например, визуализирующий агент или диагностический агент) и/или соединение (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV)), описанных здесь, и по меньшей мере один, выбранный из фармацевтически приемлемого наполнителя, носителя или разбавителя. В некоторых вариантах осуществления предоставляются пролекарства, метаболиты, стереоизомеры, гидраты, сольваты, полиморфы и фармацевтически приемлемые соли соединений, раскрытых здесь (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)).
"Пролекарство" относится к агенту, который превращается в исходное лекарственное средство in vivo. Пролекарства часто полезны, поскольку в некоторых ситуациях они могут более легко вводиться, чем исходное лекарство. Они могут, например, являться биодоступными при пероральном введении, тогда как исходные не могут. Пролекарство может также иметь улучшенную растворимость в фармацевтических композициях по отношению к исходному лекарственному средству. Примером, без ограничения, пролекарства может являться соединение, которое вводится в виде сложного эфира ("пролекарства"), чтобы облегчить прохождение через клеточную мембрану, где растворимость в воде нежелательна для перемещения, но которое затем метаболически гидролизуется до карбоновой кислоты, активного соединения, уже внутри клетки, где растворимость в воде является полезной. Дополнительный пример пролекарства может представлять собой короткий пептид (полиаминокислота), связанный с кислотной группой, где пептид метаболизируется, высвобождая активный фрагмент. Стандартные процедуры для выбора и получения подходящих пролекарственных производных описаны, например, в Design of Prodrugs, (ed. H.Bundgaard, Elsevier, 1985), которая включена здесь путем ссылки во всей своей полноте.
Термин "сложный эфир пролекарства" относится к производным соединений, раскрытых здесь, полученных добавлением любой из нескольких групп, образующих сложный эфир, которые гидролизуются в физиологических условиях. Примеры сложноэфирных групп пролекарств включают пивалоилоксиметил, ацетоксиметил, фталидил, инданил и метоксиметил, а также другие такие группы, известные в данной области техники, включая (5-R-2-оксо-1,3-диоксолен-4-ил)метильную группу. Другие примеры сложноэфирных групп пролекарств могут быть обнаружены, например, в Т.Higuchi and V.Stella, in "Pro-drugs as Novel Delivery Systems", Vol.14, A.C.S. Symposium Series, American Chemical Society (1975); и "Bioreversible Carriers in Drug Design: Theory and Application", edited by E.B.Roche, Pergamon Press: New York, 14-21 (1987) (предоставляющих примеры сложных эфиров, используемых как пролекарства для соединений, содержащих карбоксильные группы). Каждая из вышеуказанных ссылок включена сюда путем ссылки во всей своей полноте.
Термин "фармацевтически приемлемая соль" относится к соли соединения, которая не вызывает значительного раздражения в организме, в который она вводится, и не аннулирует биологическую активность и свойства соединения. В некоторых вариантах осуществления изобретения соль означает кислую аддитивную соль соединения. Фармацевтические соли могут быть получены реакцией соединения с неорганическими солями, такими как галогенводородная кислота (например, соляная кислота или бромистоводородная кислота), серная кислота, азотная кислота, фосфорная кислота и т.п. Фармацевтические соли могут быть также получены реакцией соединения с органической кислотой, такой как алифатическая или ароматическая карбоновая или сульфоновая кислоты, например, уксусная, янтарная, молочная, яблочная, винная, лимонная, аскорбиновая, никотиновая, метансульфоновая, этансульфоновая, п-толуолсульфоновая, салициловая или нафталинсульфокислота. Фармацевтические соли могут быть также получены реакцией соединения и основанием с образованием соли, такой как аммониевая соль, соль щелочного металла, такая как натриевая или калиевая соль, соль щелочно-земельного металла, такая как соль кальция или магния, соль органических оснований, такая как дициклогексиламин, N-метил-D-глюкамин, трис(гидроксиметил)метиламин, C1-C7 алкиламин, циклогексиламин, триэтаноламин, этилендиамин, и соли с аминокислотами, такими как аргинин, лизин и т.п.
Если производство фармацевтических составов включает тщательное перемешивание фармацевтических наполнителей и активного компонента в его солевой форме, тогда может быть желательным применять фармацевтические наполнители, которые являются неосновными, т.е. или кислыми, или нейтральными наполнителями.
В различных вариантах осуществления изобретения агенты или соединения, раскрытые здесь (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)), могут использоваться по отдельности, в комбинации с другими агентами или соединениями, раскрытыми здесь, или в комбинации с одними или более другими агентами, активными в терапевтических областях, описанных здесь.
В другом аспекте настоящее раскрытие относится к фармацевтической композиции, содержащей один или более физиологически приемлемых поверхностно-активных агентов, носителей, разбавителей, наполнителей, разглаживающих агентов (smoothing agents), суспендирующих агентов, пленкообразующих веществ и покрывающих вспомогательных средств, или их комбинации; и агент и/или соединение (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)), описанные здесь. Приемлемые носители и разбавители для терапевтического применения хорошо известны в фармацевтической области и описаны, например, в Remington′s Pharmaceutical Sciences, 18th Ed., Mack Publishing Co., Easton, PA (1990), которая включена сюда путем ссылки во всей своей полноте. Консерванты, стабилизаторы, красители, подсластители, отдушки, вкусовые добавки и т.п. могут обеспечиваться в фармацевтической композиции. Например, бензоат натрия, аскорбиновая кислота и сложные эфиры п-гидроксибензойной кислоты могут добавляться как консерванты. Дополнительно, могут использоваться антиоксиданты и суспендирующие агенты. В различных вариантах осуществления изобретения спирты, сложные эфиры, сульфатированные алифатические спирты и подобные могут использоваться как поверхностно-активные агенты; сахароза, глюкоза, лактоза, крахмал, кристаллическая целлюлоза, маннит, безводный легкий силикат, алюминат магния, алюминат метасиликат магния, синтетический силикат алюминия, карбонат кальция, кислый карбонат натрия, вторичный кислый фосфат кальция, карбоксиметилцеллюлоза кальция и подобные могут использоваться как наполнители; стеарат магния, тальк, гидрогенизированное масло и подобные могут использоваться как разглаживающие агенты; кокосовое масло, оливковое масло, кунжутное масло, арахисовое масло, соя могут использоваться как суспендирующие агенты или смазывающие вещества; ацетатфталат целлюлозы в качестве производного углевода, такого как целлюлоза или сахар, или метилацетат-метакрилат сополимер в качестве производного поливинила могут использоваться как суспендирующие агенты; и пластификаторы, такие как сложные эфиры фталаты и подобные могут использоваться как суспендирующие агенты.
Термин "фармацевтическая композиция" относится к смеси агента и/или соединения, раскрытого здесь (например, полимерного конъюгата, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)), с другими химическими компонентами, такими как разбавители или носители. Фармацевтическая композиция способствует введению агента и/или соединения в организм. Множество методик введения агента и/или соединения существует в данной области техники, включая, но не ограничиваясь этим, пероральное, инъекционное, аэрозольное, парентеральное и местное введение. Фармацевтические композиции могут также получать реакцией агентов и/или соединений с неорганическими или органическими кислотами, такими как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота и т.п.
Термин "носитель", использованный по отношению к фармацевтической композиции, относится к химическому соединению, которое способствует включению агента и/или соединения в клетки или ткани. Например, диметилсульфоксид (DMSO) представляет собой широко применяемый носитель, так как он способствует введению многих органических соединений в клетки или ткани организма.
Термин "разбавитель" относится к химическим соединениям, разбавленным в воде, которые растворяют агент и/или интересующее соединение (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)), а также стабилизируют биологически активную форму агента и/или соединения. Соли, растворенные в забуференных растворах, используются как разбавители в данной области техники. Одним широко применяемым забуференным раствором является забуференный фосфатом физиологический раствор, т.к. он имитирует солевые свойства крови человека. Так как буферные соли могут контролировать рН раствора при низких концентрациях, забуференный разбавитель редко модифицирует биологическую активность агента и/или соединения. Термин "физиологически приемлемый" относится к носителю или разбавителю, которые не аннулируют биологическую активность и свойства агента и/или соединения.
В агенте настоящего изобретения метка может содержаться во внутренней части агента, может присоединяться к его внешней части или может смешиваться с ним, поскольку ретиноид присутствует в такой конфигурации, что он может функционировать как направленная молекула. Следовательно, настоящий агент может покрываться соответствующим материалом, таким как, например, энтеросолюбильное покрытие или материал, который распадается с течением времени, или может включаться в соответствующую систему высвобождения лекарства.
Фармацевтические композиции, описанные здесь, могут вводиться человеку-пациенту per se или в фармацевтических композициях, где они смешиваются с другими активными ингредиентами, как в комбинированной терапии, или с подходящими носителями или наполнителем(ями). Методики для подготовки и введения агента и/или соединений рассматриваемой заявки могут быть обнаружены, например, в "Remington′s Pharmaceutical Sciences," Mack Publishing Co., Easton, PA, 18th edition, 1990, and Hyojun Yakuzaigaku (Standard Pharmaceutics), Ed. by Yoshiteru Watanabe et al., Nankodo, 2003.
Подходящие пути введения могут, например, включать пероральное, ректальное, трансмукозальное, трансдермальное, трансназальное, внутриушное, местное или интестинальное введение; парентеральная доставка, включая внутримышечное, подкожное, внутривенное, внутриартериальное, интрапортальное, внутрилимфатическое введение, введение в лимфатические узлы, интрамедуллярное, интратекальное, прямое внутрижелудочковое, интрацеребровентрикулярное, внутрибрюшинное, интраназальное, интрацеребральное введение, внутриокулярные инъекции, а также внутрилегочное введение, введение через дыхательные пути, внутритрахеальное, внутрибронхиальное, внутриматочное или внутритрахеальное введение. В некоторых вариантах осуществления изобретения агент и/или соединения (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)) могут вводиться в виде лекарственных форм с контролируемым или замедленным высвобождением, включая инъекции веществ замедленного всасывания, осмотические насосы, пилюли, трансдермальные (включая электротранспортные) пластыри и подобные, для пролонгированного и/или регулируемого во времени, прерывистого введения при заранее установленной скорости.
Фармацевтические композиции могут быть представлены в виде лекарственной формы, подходящей для каждого пути введения. Такая лекарственная форма и способ приготовления лекарственного средства могут выбираться как подходящие из любых известных форм и способов.
Примеры лекарственных форм, подходящих для перорального введения, включают, но не ограничиваются этим, порошок, гранулы, таблетку, капсулу, жидкость, суспензию, эмульсию, гель и сироп, и примеры лекарственной формы, подходящей для парентерального введения, включают инъекции, например, инъекционный раствор, инъекционную суспензию, инъекционную эмульсию и инъекцию в форме, которую получают во время применения. Составы для парентерального введения могут быть в форме, например, водного или безводного изотонического асептического раствора или суспензии.
Фармацевтические композиции могут быть изготовлены способом, который известен сам по себе, например, посредством процессов стандартного смешивания, растворения, гранулирования, изготовления драже, растирания в порошок, эмульгирования, инкапсулирования, включения или таблетирования.
Фармацевтические композиции могут быть изготовлены стандартным способом, используя один или два физиологически приемлемых носителя, содержащих наполнители и вспомогательные вещества, которые облегчают переработку активных соединений в препараты, которые могут использоваться фармацевтически. Подходящий состав зависит от выбранного пути введения. Любые из известных методик, носителей и наполнителей могут использоваться как подходящие и как предполагаемые в данной области техники, например, в Remington′s Pharmaceutical Sciences и в Standard Pharmaceutics выше.
Инъекционные средства могут быть получены в стандартных формах, или как жидкие растворы, или суспензии, твердые формы, подходящие для раствора или суспензии в жидкой форме перед инъекцией, или как эмульсии. Подходящие наполнители представляют собой, например, воду, физиологический раствор, декстрозу, маннит, лактозу, лецитин, альбумин, глутамат натрия, гидрохлорид цистеина и т.п. Дополнительно, если желательно, инъекционные фармацевтические композиции могут содержать небольшие количества нетоксичных вспомогательных веществ, таких как смазывающие вещества, рН буферные вещества и т.п. Физиологически совместимые буферы включают, но не ограничиваются этим, раствор Хенкса, раствор Рингера или физиологический буфер. При желании могут использоваться препараты, усиливающие абсорбцию (например, липосомы).
Для трансмукозального введения в составе могут использоваться пенетранты, подходящие для барьера, через который нужно проникнуть.
Фармацевтические составы для парентерального введения, например, посредством болюсной инъекции или непрерывной инфузии, включают водные растворы активных соединений в водорастворимой форме. Дополнительно, суспензии активных соединений могут быть получены в виде подходящих масляных инъекционных суспензий. Подходящие липофильные растворители или носители включают жирные масла, такие как кунжутное масло или другие органические масла, например, соевое масло, грейпфрутовое или миндальные масла, или синтетические сложные эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Водные инъекционные суспензии могут содержать вещества, которые повышают вязкость суспензии, такие как карбоксиметилцеллолоза натрия, сорбит или декстран. При необходимости, суспензия может также содержать подходящие стабилизаторы или агенты, которые повышают растворимость соединений, давая возможность получения высоко концентрированных растворов. Составы для инъекций могут быть представлены в единичной лекарственной форме, например, в ампулах или упаковках лекарственных средств для многократного приема, с добавленным консервантом. Композиции могут принимать такие формы как суспензии, растворы или эмульсии в масляных или водных разбавителях, и могут содержать вспомогательные вещества, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может быть в порошкообразной форме для разбавления подходящим разбавителем, например, стерильной апирогенной водой, перед использованием.
Для перорального введения из агента и/или соединений (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)), могут быть легко приготовлены составы посредством комбинирования агента и/или активных соединений с фармацевтически приемлемыми носителями, хорошо известными в данной области техники. Такие носители дают возможность приготовления агента и/или соединений по изобретению в виде таблеток, пилюль, драже, жидкостей, гелей, сиропов, взвесей, суспензий и т.п., для перорального приема пациентом, подвергаемым лечению. Фармацевтические препараты для перорального применения можно получать комбинированием агента и/или активных соединений с твердым наполнителем, при необходимости измельчая полученную смесь и обрабатывая смесь гранул после добавления подходящих вспомогательных веществ, при желании, для получения сердцевин таблеток или драже. Подходящие вспомогательные вещества представляют собой, в частности, наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит, целлюлозные препараты, такие как, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовую камедь, метилцеллюлозу, гидроксипропилметилцеллюлозу, карбоксиметилцеллюлозу натрия и/или поливинилпирролидон (PVP). При желании, дезинтегрирующие агенты, такие как сшитый поливинилпирролидон, агар, или альгиновая кислота, или ее соль, например, альгинат натрия. Сердцевины драже предоставляются с подходящими покрытиями. Для этой цели можно использовать концентрированный сахарный раствор, который может при необходимости содержать гуммиарабик, тальк, поливинилпирролидон, карбополовый гель, полиэтиленгликоль и/или диоксид титана, растворы глазури и подходящие органические растворители или смеси растворителей. Красящие вещества или пигменты могут быть добавлены в покрытия таблеток или драже для идентификации или чтобы охарактеризовать различные комбинации доз активного вещества.
Фармацевтические препараты, которые могут использоваться перорально, включают твердые (push-fit) капсулы, сделанные из желатина, а также мягкие запаянные капсулы, сделанные из желатина и пластификатора, например, глицерина и сорбита. Твердые (push-fit) капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связующие, такие как крахмалы, и/или смазывающие вещества, такие как тальк или стеарат магния, и при необходимости стабилизаторы. В мягких капсулах агент и/или активные соединения могут растворяться или суспендироваться в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли. Кроме того, могут добавляться стабилизаторы. Все составы для перорального введения должны быть в дозировках, подходящих для такого введения.
Для буккального введения композиции могут принимать форму таблеток или таблеток для рассасывания, изготовленных стандартным способом.
Для введения ингаляцией агент и/или соединения (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)) легко доставляются в форме аэрозольного спрея из баллонов под давлением или небулайзера с применением подходящего пропеллента, например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа. В случае аэрозоля под давлением единичная доза может определяться путем обеспечения клапана для доставки отмерянного количества. Капсулы и катриджи, например, из желатина для применения в ингаляторе или инсуффляторе могут быть выполнены содержащими порошкообразную смесь агента и/или соединения и подходящей порошкообразной основы, такой как лактоза или крахмал.
Также здесь раскрыты различные фармацевтические композиции, хорошо известные в фармацевтической области, для применений, которые включают интраокулярную, интраназальную и внутриушную доставку. Подходящие пенетранты для этих применений обычно известны в данной области техники. Фармацевтические композиции для интраокулярной доставки включают водные офтальмологические растворы агента и/или активных соединений в водорастворимой форме, такие как глазные капли, или в геллановой камеди (Shedden et al., Clin. Ther., 23(3): 440-50 (2001)), или гидрогелях (Mayer et al., Ophthalmologica, 210(2): 101-3 (1996)); офтальмологические мази; офтальмологические суспензии, например, микрочастицы, небольшие полимерные частицы, содержащие лекарственное средство, которые суспендированы в жидкой среде-носителе (Joshi, A., J.Ocul. Pharmacol., 10(1): 29-45 (1994)), жирорастворимые составы (Alm et al., Prog. Clin. Biol. Res., 312: 447-58 (1989)) и микросферы (Mordenti, Toxicol. Sci., 52(1): 101-6 (1999)); и глазные линзы. Все из вышеперечисленных ссылок включены сюда путем ссылки во всей своей полноте. Такие подходящие фармацевтические составы чаще всего и предпочтительно изготавливаются стерильными, изотоническими и забуференными для стабильности и удобства. Фармацевтические композиции для интраназальной доставки могут также включать капли и спреи, часто приготовленные таким образом, чтобы имитировать по многим аспектам назальные выделения, чтобы обеспечить поддержание нормальной цилиарной активности. Как раскрыто в Remington′s Pharmaceutical Sciences, 18th Ed., Mack Publishing Co., Easton, PA (1990), которая включена сюда путем ссылки во всей своей полноте, и хорошо известно специалистам в данной области техники, подходящие составы чаще всего и предпочтительно являются изотоническими, слегка забуференными для поддержания рН от 5.5 до 6.5, и чаще всего и предпочтительно включают антимикробные консерванты и подходящие стабилизаторы лекарственных средств. Фармацевтические составы для внутриушной доставки включают суспензии и мази для местного применения в ухе. Обычные растворители для таких ушных составов включают глицерин и воду.
Агент и/или соединения (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)) могут быть заключены в ректальные композиции, такие как ректальные суппозитории или удерживающие клизмы, например, содержащие стандартные суппозиторные основы, такие как масло какао или другие глицериды.
В дополнение к составам, описанным ранее, агент и/или соединения (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)) могут быть заключены в состав, такой как депо-препарат. Такие составы долговременного действия могут вводиться путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Таким образом, агент и/или соединения могут быть получены в виде составов с подходящими полимерными или гидрофобными материалами (например, в виде эмульсии в подходящим масле) или ионообменными смолами, или как труднорастворимые производные, например, как труднорастворимая соль.
Для гидрофобного агента или соединений подходящим фармацевтическим агентом может являться система сорастворителей, содержащая бензиловый спирт, неполярное поверхностно-активное вещество, водорастворимый органический полимер и водную фазу. Стандартная использованная система сорастворителей представляет собой систему сорастворителей VPD, которая является раствором 3% масс./об. бензилового спирта, 8% масс./об. неполярного поверхностно-активного вещества Polysorbate 80™ и 65% масс./об. полиэтиленгликоля 300, доведенного до необходимого объема абсолютным этанолом. Естественно, пропорции системы сорастворителей можно значительно изменять без уничтожения ее характеристик растворимости и токсичности. Кроме того, может изменяться сущность компонентов сорастворителей: например, могут использоваться другие низкотоксичные неполярные поверхностно-активные вещества вместо POLYSORBATE 80™; может изменяться марка полиэтиленгликоля; другие биосовместимые полимеры могут заменять полиэтиленгликоль, например, поливинилпирролидон; и другие сахара или полисахариды могут заменять декстрозу.
Альтернативно, могут использоваться другие системы доставки гидрофобного фармацевтического агента или соединений. Липосомы и эмульсии являются хорошо известными примерами разбавителей или носителей для доставки гидрофобных лекарственных средств. Определенные органические растворители, такие как диметилсульфоксид, также могут использоваться, хотя обычно ценою более высокой токсичности. Дополнительно, агент и/или соединения могут доставляться путем использования системы с замедленным высвобождением, например, полупроницаемых матриц твердых гидрофобных полимеров, содержащих терапевтический агент. Различные материалы для замедленного высвобождения установлены и хорошо известны специалистам в данной области техники. Капсулы с замедленным высвобождением могут в зависимости от их химической природы высвобождать агент и/или соединения в течение от нескольких часов или недель вплоть до в течение 100 дней. В зависимости от химической природы и биологической стабильности терапевтического реагента могут использоваться дополнительные стратегии стабилизации белков.
Агенты, которые предполагается вводить внутриклеточно, могут быть введены, используя методики, хорошо известные специалистам в данной области техники. Например, такие агенты могут инкапсулироваться в липосомы. Все молекулы, присутствующие в водном растворе во время образования липосом, включаются в водную внутреннюю часть. Липосомальное содержимое и защищено от внешней микросреды, и, поскольку липосомы сливаются с клеточными мембранами, эффективно доставляется в клеточную цитоплазму. Липосома может быть покрыта тканеспецифическим антителом. Липосомы могут быть нацеленными и поглощаться селективно желательным органом. Альтернативно, небольшие гидрофобные органические молекулы могут непосредственно вводиться внутриклеточно.
Дополнительные терапевтические или диагностические агенты могут вводиться в фармацевтические композиции. Альтернативно или дополнительно фармацевтические композиции могут комбинироваться с другими композициями, которые содержат другие терапевтические или диагностические агенты.
Агент и/или соединения (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)) или их фармацевтические композиции могут вводиться пациенту любым подходящим способом. Неограничивающие примеры способов введения включают среди прочих (а) введение пероральным путем, которое включает введение в капсуле, таблетке, грануле, спрее, сиропе или других подобных формах; (b) введение через непероральный путь, такой как ректальный, вагинальный, интрауретральный, интраокулярный, интраназальный или внутриушной, которые включают введение в виде водной суспензии, масляного препарата или т.п. или в виде капель, спрея, суппозитория, бальзама, мази или т.п.; (с) введение через инъекцию, подкожно, внутрибрюшинно, внутривенно, внутримышечно, внутрикожно, интраорбитально, внутрикапсулярно, интраспинально, интрастернально или т.п., включая доставку через инфузионный насос; (d) введение локально, такое как инъекция непосредственно в область почек или сердца, например, депо-имплантацией; а также (е) введение местно; как предполагается подходящим специалистами в данной области техники для приведения активного соединения в контакт с живой тканью.
Фармацевтические композиции, подходящие для введения, включают композиции, где активные ингредиенты содержатся в количестве, эффективном для достижения намеченной цели. Эффективное количество раскрытых здесь соединений, требуемое в виде дозы, будет зависеть от пути введения, типа животного, включая человека, подвергаемого лечению, и физических характеристик конкретного рассматриваемого животного. Доза может быть приспособлена для достижения требуемого эффекта, но будет зависеть от таких факторов как масса, рацион, сопутствующая лекарственная терапия и другие факторы, которые будут понятны специалистам в данной области техники. Более конкретно, эффективное количество означает количество соединения, эффективного для предотвращения, смягчения или облегчения симптомов заболевания или продления продолжительности существования субъекта, подвергаемого лечению. Определение эффективного количества находится вполне в пределах способностей специалистов в данной области техники, в особенности в свете подробного раскрытия, представленного здесь.
Как будет легко видно специалисту в данной области техники, применение in vivo вводимой дозировки и специфического метода введения может изменяться в зависимости от возраста, массы и вида обрабатываемого млекопитающего, используемых конкретного агента и/или соединений, и специфического применения, для которого используются эти агенты и/или соединения. Определение эффективных уровней дозировки, которые являются уровнями дозировки, необходимыми для достижения требуемого результата, может выполняться специалистом в данной области техники с использованием обычных фармакологических методов. Обычно клинические применения продуктов для человека начинаются на более низких уровнях дозировок, при этом уровень дозировки увеличивается до достижения требуемого эффекта. Альтернативно, допустимые исследования in vitro могут использоваться для установления пригодных доз и путей введения композиций, идентифицируемых настоящими методами с использованием установленных фармакологические способы.
В исследованиях на животных, которые не являются человеком, применения потенциальных продуктов начинаются при более высоких уровнях дозировки, при этом доза уменьшается до тех пор, пока требуемый эффект более не достигается или исчезают побочные эффекты. Дозировка может изменяться в широких пределах, в зависимости от требуемых эффектов и терапевтического показания. Обычно дозировки могут составлять от около 10 микрограмм/килограмм (мкг/кг) до 100 мг/кг массы тела, предпочтительно от около 100 мкг/кг до 10 мг/кг массы тела. Альтернативно, дозировки могут основываться и рассчитываться на площадь поверхности тела пациента, что понятно специалистам в данной области техники.
Точный состав, путь введения и дозировка фармацевтических композиций, описанных здесь, могут выбираться персональным врачом, принимая во внимание состояние пациента. (Смотри, например, Fingl et al. 1975, in "The Pharmacological Basis of Therapeutics", которая включена здесь путем ссылки во всей своей полноте, особенно Глава 1, стр.1). Обычно диапазон дозы композиции, введенной пациенту, может составлять от около 0.5 до 1000 мг/кг массы тела пациента. Доза может быть единичной или серией из двух или более, даваемых в течение одного или более дней, как это необходимо пациенту. Например, если дозировки для человека в отношении агента и/или соединений установлены по меньшей мере для некоторого состояния, настоящее изобретение будет использовать те же дозировки или дозировки, которые составляют между около 0.1% и 500%, более предпочтительно между около 25% и 250% установленной дозировки для человека. Если не установлена дозировка для человека, как это может быть в случае новых фармацевтических композиций, подходящая дозировка для человека может быть выведена из значений ED5o или ID5o, или других соответствующих значений, полученных из исследований in vitro или in vivo, например, полученных из исследований на животных токсичности и эффективности.
Следует отметить, что лечащий врач, вероятно, знал бы как и когда заканчивать, прерывать или корректировать введение из-за токсичности или дисфункций органов.
В свою очередь, лечащий врач, вероятно, также знал бы, как довести лечение до более высоких уровней, если клинический ответ не являлся адекватным (препятствующая токсичность). Величина введенной дозы при лечении интересующего нарушения может изменяться в соответствии со сложностью состояния, подвергаемого лечению, и пути введения. Сложность состояния может, например, оцениваться частично стандартными прогностическими методами оценки. Кроме того, доза и возможно частота дозы будут также изменяться согласно возрасту, массе тела и реакции отдельного пациента. Программа, сравнимая с обсуждаемой выше, может использоваться в ветеринарии.
Хотя точная дозировка может определяться в зависимости от конкретного лекарственного средства, в большинстве случаев могут быть сделаны некоторые обобщения, касающиеся дозировки. Ежедневная схема приема для пациента - взрослого человека может представлять собой, например, пероральную дозу между 0.1 мг и 2000 мг каждого активного ингредиента, предпочтительно между 1 мг и 500 мг, например 5-200 мг. В других вариантах осуществления изобретения используется внутривенная, подкожная или внутримышечная доза каждого активного ингредиента между 0.01 мг и 100 мг, предпочтительно между 0.1 мг и 60 мг, например, 1-40 мг. В случаях введения фармацевтически приемлемой соли дозировки могут быть вычислены в расчете на свободное основание. В некоторых вариантах осуществления изобретения композиция вводится от 1 до 4 раз в день. Альтернативно, композиции по изобретению могут вводиться непрерывным внутривенным вливанием, предпочтительно при дозе для каждого активного ингредиента вплоть до 1000 мг на день. Как будет понятно специалистам в данной области техники, в определенных ситуациях может быть необходимо вводить агент и/или соединения, раскрытые здесь, в количествах, которые превышают или даже в значительной степени превышают вышеуказанный предпочтительный диапазон дозировок, для того, чтобы эффективно и интенсивно лечить особенно агрессивные заболевания или инфекции. В некоторых вариантах осуществления изобретения агент и/или соединения можно вводить в период непрерывной терапии, например, в течение недели или более, или в течение месяцев или лет.
Величина дозировки и интервал могут регулироваться индивидуально, чтобы обеспечить концентрации активного фрагмента в плазме крови, которые достаточны для поддержания регулирующих эффектов или минимальной эффективной концентрации (МЕС). МЕС может изменяться для каждого агента и/или соединения, но может оцениваться по данным in vitro. Дозировки, необходимые для достижения МЕС, будут зависеть от индивидуальных характеристик и пути введения. Однако анализы или биоанализы ВЭЖХ могут использоваться для определения концентраций в плазме.
Интервалы дозировок могут также определяться, используя величину МЕС. Композиции следует вводить, используя режим, который поддерживает концентрации в плазме крови выше, чем МЕС, в течение 10-90% времени, предпочтительно между 30-90% и наиболее предпочтительно между 50-90%.
В случаях локального введения или селективного поглощения эффективная локальная концентрация лекарственного средства может быть не связана с концентрацией в плазме крови.
Количество вводимой композиции может зависеть от субъекта, подвергаемого лечению, массы субъекта, тяжести заболевания, способа введения и заключения лечащего врача.
Агент и/или соединения, раскрытые здесь (например, полимерный конъюгат, который включает по меньшей мере одно повторяющееся звено, выбранное из Формулы (I), (II), (III) и (IV)), могут оцениваться на эффективность и токсичность, используя известные способы. Например, токсикология конкретного агента и/или соединения, или подгруппы агента и/или соединений, совместно использующих определенные химические фрагменты, может быть установлена путем определения токсичности in vitro по отношению к клеточной линии, такой как клеточная линия млекопитающего, предпочтительно, человека. Результаты таких исследований часто предсказывают токсичность у животных, таких как млекопитающие, или более конкретно, люди. Альтернативно, токсичность конкретного агента и/или соединений в отношении животной модели, такой как мыши, крысы, кролики или обезьяны, можно определить, используя известные методы. Эффективность конкретного агента и/или соединения можно установить, используя несколько общепризнанных методов, таких как методы in vitro, животные модели или клинические исследования на людях. Общепризнанные модели in vitro существуют почти для каждого класса состояния, включая, но не ограничиваясь этим, рак, сердечно-сосудистое заболевание и различные иммунные дисфункции. Аналогично, приемлемые животные модели могут использоваться для установления эффективности химикатов для лечения таких условий. Выбирая модель для определения эффективности специалист в данной области техники может руководствоваться уровнем техники для выбора подходящих модели, дозы и пути введения, и режима. Конечно, клинические исследования на людях могут также использоваться для определения эффективности агента и/или соединения для человека.
Агент или композиция согласно настоящему изобретению могут поставляться в любой форме, но с точки зрения стабильности при хранении, могут предоставляться в форме, которую готовят во время использования, например, в форме, которая дает возможность доктору и/или фармацевту, медицинской сестре, иному парамедику и т.д. готовить ее в месте проведения лечения или поблизости от него. В этом случае агент или композиция настоящего изобретения предоставляется в виде одного или более контейнеров, содержащих по меньшей мере один основной составляющий элемент, и приготовление проводится перед применением, например, за 24 ч до применения, предпочтительно за 3 ч перед применением и более предпочтительно непосредственно перед применением. При осуществлении приготовления реагент, растворитель, оборудование для приготовления и т.д., которые обычно доступны в месте приготовления, могут использоваться соответствующим образом.
Следовательно, настоящее изобретение также относится к набору для получения для агента, соединения или композиции, раскрытых здесь, при этом набор включает один или более контейнеров, содержащих отдельно или в комбинации ретиноид и/или детектируемую метку, и/или при необходимости вещество, составляющее носитель, и/или при необходимости другой(ие) компонент(ы), необходимый(е) для получения агента, соединения или композиции. Настоящее изобретение также относится к составляющему элементу, необходимому для агента, соединения или композиции, предоставляемых в форме такого набора. Набор согласно настоящему изобретению может содержать, в дополнение к вышесказанному, инструкции, электронный носитель, такой как CD или DVD, относящийся к способу получения агента, соединения или композиции согласно настоящему изобретению или способу введения, и т.д. Кроме того, набор согласно настоящему изобретению может включать все составляющие элементы для комплектования агента, соединения или композиции по настоящему изобретению, но нет необходимости всегда включать все составляющие элементы. Следовательно, набор согласно настоящему изобретению не требует включения реагента или растворителя, который обычно доступен в месте проведения медицинского лечения, экспериментального оборудования и т.д., такого как, например, стерильная вода, физиологический раствор или раствор глюкозы.
Агенты, соединения и композиции, при желании, могут быть представлены в упаковке или диспенсере (раздаточном устройстве), которые могут содержать одну или более единичных лекарственных форм, содержащих активный ингредиент. Упаковка может, например, содержать металлическую или полимерную пленку, такую как блистерная упаковка. Упаковка или диспенсер могут сопровождаться инструкциями для введения. Упаковка или диспенсер могут также сопровождаться уведомлением, соединенным с контейнером, в форме, предписанной государственным органом, регулирующим производство, применение или продажу лекарственных средств, и это уведомление отражает разрешение данного органа на введение человеку или ветеринарное введение формы лекарственного средства. Таким уведомлением, например, может быть маркировка, утвержденная Управлением по контролю за пищевыми продуктами и лекарственными средствами для лекарств, отпускаемых по рецептам, или утвержденный листок-вкладыш. Композиции, содержащие агент и/или соединение согласно настоящему изобретению, заключенные в совместимый фармацевтический носитель, также могут быть получены, помещены в соответствующий контейнер, маркированный для лечения указанного состояния.
Агент, соединение и композиция согласно настоящему изобретению подходят для определения фиброзных заболеваний in vivo. Таким образом, они подходят для недеструктивного, предпочтительно неинвазивного детектирования фиброзных заболеваний. Термин "недеструктивный", как здесь подразумевается, относится к неразрушающейся ткани, подвергнутой детектированию. Например, когда ткань, подвергнутая детектированию, представляет собой печень, этот термин подразумевает, что печень подвергают лапаротомии, или получают изображения поверхности печени, используя эндоскоп, но не означает разрезание печени и исследование ее внутренней части. С другой стороны, термин "неинвазивно", как здесь подразумевается, относится к обнаружению метки, содержащейся в визуализирующем агенте, без умышленного повреждения живого организма, и обычно включает детектирование снаружи живого организма, но также охватывает детектирование метки путем вставления детектора, такого как эндоскоп или ультразвуковой зонд, через естественное отверстие, например, ротовую полость, назальную полость, анальное отверстие, уретру, слуховой проход и влагалище.
Агент, соединение, например, полимеры и сополимеры, содержащие по меньшей мере одно повторяющееся звено, выбранное из Формул (I), (II), (III) и (IV), и композиция согласно настоящему изобретению могут иметь множество различных применений. В некоторых вариантах осуществления изобретения агент, соединение или композиция, описанные здесь, могут использоваться для доставки детектируемой метки к участку ткани или клетке. В одном из вариантов осуществления изобретения агент, соединение или композиция, описанные здесь, могут использоваться для диагностирования заболевания или состояния, таких как заболевание или состояние, характеризуемые фиброзом. В еще одном варианте осуществления изобретения агент, соединение или композиция, описанные здесь, могут использоваться для получения изображения участка ткани или клетки. В некоторых вариантах осуществления изобретения ткань может являться фиброзной тканью.
В одном из вариантов осуществления изобретения настоящее изобретение относится к способу визуализации фиброзных заболеваний, причем этот способ включает стадию введения эффективного количества агента, соединения или композиции изобретения субъекту, нуждающемуся в этом, и стадию детектирования метки, содержащейся во введенном агенте, соединении или композиции. Эффективное количество, упомянутое здесь, означает, например, количество, которое позволяет детектировать метку по меньшей мере на одном участке тела по меньшей мере в один момент времени после введения. Также предпочтительным является количество, которое не вызывает побочного эффекта, который превышает пользу от введения. Такое количество можно определить при необходимости тестом in vitro, используя культивируемые клетки, или тестом на животных моделях, таких как мышь, крыса, собака или свинья, и такие методы испытаний хорошо известны специалисту в данной области техники. Примеры таких тестов уже обсуждались здесь. Кроме того, доза ретиноида, метки и при необходимости носителя, содержащихся в визуализирующем агенте, соединении или композиции по изобретению хорошо известны специалисту в данной области техники или могут быть определены при необходимости вышеуказанными тестами и т.д.
Что касается пути введения, существуют различные пути, включающие и пероральное, и парентеральное введение, и их примеры включают пероральный, внутривенный, внутримышечный, подкожный, локальный, внутрилегочный, в дыхательные пути, внутритрахеальный, внутрибронхиальный, трансназальный, ректальный, внутриартериальный, интрапортальный, внутрижелудочковый, интрамедуллярный пути, введение в лимфатические узлы, внутрилимфатический, интрацеребральный, интратекальный, интрацеребровентрикулярный, трансмукозальный, чрескожный, интраназальный, внутрибрюшинный и внутриматочный путь.
В одном варианте осуществления настоящее изобретение обеспечивает способ определения фиброзного заболевания, предусматривающий стадию сравнения интенсивности сигнала и/или распределения сигнала метки, обнаруживаемой у субъекта, которому вводятся агент, соединение или композиция согласно настоящему изобретению, с контрольной интенсивностью сигнала и/или контрольным распределением сигнала.
Интенсивность сигнала метки, как здесь подразумевается, относится к интенсивности или сходному значению измерения различных сигналов, испускаемых меткой, например, флуоресцентного сигнала, люминесцентного сигнала, магнитного сигнала и радиоактивного сигнала, и обычно измеряется соответствующими средствами детектирования, конкретные примеры которых уже обсуждались выше. Интенсивность сигнала можно получать из целого объекта или из специфического участка или области субъекта. Интенсивность сигнала может также быть средней величиной или суммарной величиной по отношению к площади или объему измеряемого участка. В том случае, если интенсивность сигнала изменяется с течением времени, интенсивность сигнала согласно настоящему способу может быть представлена для определенного момента времени или может суммироваться для данного периода времени.
Распределение сигнала метки, как здесь подразумевается, относится к информации о положении сигнала, испускаемого меткой, в субъекте, и может быть двумерным или трехмерным. Сравнивая распределение сигнала с соответствующим анатомическим положением органов или структурной информацией о ткани, такой как КТ-изображение, МРТ-изображение или ультразвуковое изображение, можно идентифицировать, из какой ткани идет сигнал. В том случае, если распределение сигнала изменяется по времени, распределение сигнала согласно настоящему способу может относиться к определенному моменту времени или суммироваться для данного периода времени. В настоящем способе можно оценить комбинацию интенсивности сигнала и распределения сигнала. Одновременная оценка и интенсивности, и положения сигнала позволяет более точное определение.
Интенсивность контрольного сигнала и/или распределение контрольного сигнала, как здесь подразумевается, относятся к интенсивности сигнала и/или распределению сигнала метки, измеренным у субъекта, который, как известно, не имеет фиброзного заболевания, и которому вводится агент, соединение или композиция согласно настоящему изобретению (также указывается как "негативная интенсивность сигнала и/или негативное распределение сигнала"), или к интенсивности сигнала и/или распределению сигнала метки, измеренным у субъекта, который, как известно, имеет фиброзное заболевание, и которому вводится агент, соединение или композиция согласно настоящему изобретению (также указывается как "положительная интенсивность сигнала и/или положительное распределение сигнала"). Например, если интенсивность сигнала и/или распределение сигнала метки, обнаруженной у исследуемого субъекта, представляют собой/похожи на (например, незначительно отличаются от) негативную интенсивность сигнала и/или негативное распределение сигнала, субъект может быть определен как негативный по фиброзному заболеванию, а если интенсивность сигнала у субъекта значительно выше, чем негативная интенсивность сигнала, и/или если распределение сигнала у субъекта значительно больше, чем негативное распределение сигнала, субъект может быть определен как положительный по фиброзному заболеванию. Кроме того, если интенсивность сигнала и/или распределение сигнала метки, обнаруженной у исследуемого субъекта, представляют собой/похожи на (например, незначительно отличаются от) положительную интенсивность сигнала и/или положительное распределение сигнала, субъект может определяться как положительный по фиброзному заболеванию.
Настоящее изобретение также относится к способу контроля фиброзного заболевания, предусматривающему стадию сравнения интенсивности сигнала и/или распределения сигнала метки, обнаруженных в первый момент времени у субъекта, которому вводится агент, соединение или композиция согласно настоящему изобретению, с интенсивность сигнала и/или распределения сигнала метки, обнаруживаемых во второй момент времени, который позже, чем первый момент времени, у субъекта, которому вводится агент, соединение или композиция согласно настоящему изобретению. Например, если интенсивность сигнала во второй момент времени ниже, чем в первый момент времени, для фиброзного заболевания может быть определено улучшение, и наоборот, если интенсивность сигнала во второй момент времени выше, чем в первый момент времени, для фиброзного заболевания может быть определено ухудшение. Кроме того, например, если распределение сигнала во второй момент времени уже, чем в первый момент времени, для фиброзного заболевания может быть определено улучшение, и наоборот, если распределение сигнала во второй момент времени шире, чем в первый момент времени, для фиброзного заболевания может быть определено ухудшение.
Настоящий способ может предусматривать стадию введения агента, соединения или композиции согласно настоящему изобретению субъекту, и/или стадию детектирования метки, содержащейся во введенных агенте, соединении или композиции в по меньшей мере два различных момента времени, и/или стадию определения интенсивности сигнала и/или распределения сигнала детектируемой метки, перед вышеуказанной стадией сравнения.
Настоящее изобретение также относится к способу определения эффекта лечения фиброзного заболевания, предусматривающего стадию сравнения интенсивности сигнала и/или распределения сигнала метки, обнаруженной в первый момент времени у субъекта, которому вводятся агент, соединение или композиция согласно настоящему изобретению, с интенсивностью сигнала и/или распределением сигнала метки, обнаруженной во второй момент времени, который позже, чем первый момент времени, у субъекта, которому вводятся агент, соединение или композиция согласно настоящему изобретению, где первый момент времени имеет место перед тем, как субъект получает лечение фиброзного заболевания, и второй момент времени имеет место после того, как субъект получил лечение фиброзного заболевания, или, альтернативно, первый момент времени имеет место после того, как субъект получил первое лечение фиброзного заболевания, и второй момент времени имеет место после того, как субъект получил второе лечение фиброзного заболевания, которое было проведено после первого лечения фиброзного заболевания. Например, если интенсивность сигнала во второй момент времени ниже, чем в первый момент времени, для фиброзного заболевания может быть определено улучшение, и таким образом лечение является удачным, и наоборот, если интенсивность сигнала во второй момент времени выше, чем в первый момент времени, для фиброзного заболевания может быть определено ухудшение, и таким образом лечение является менее удачным или неудачным. Кроме того, например, если распределение сигнала во второй момент времени является уже, чем в первый момент времени, для фиброзного заболевания может быть определено улучшение, и таким образом лечение является удачным, и наоборот, если распределение сигнала во второй момент времени шире, чем в первый момент времени, для фиброзного заболевания может быть определено ухудшение, и таким образом лечение является менее удачным или неудачным.
Настоящий способ может содержать стадию лечения фиброзного заболевания у субъекта, и/или стадию введения субъекту агента, соединения или композиции согласно настоящему изобретению, и/или стадию детектирования метки, содержащейся во введенных агенте, соединении или композиции, по меньшей мере в два различных отдельных момента времени, и/или стадию определения интенсивности сигнала и/или распределения сигнала детектируемой метки, перед вышеуказанной стадией сравнения.
В способах настоящего изобретения, раскрытых здесь, подразумевается, что термин "субъект" относится к любому живому организму, предпочтительно к животному, более предпочтительно, к млекопитающему или еще более предпочтительно, к человеку. В настоящем изобретении субъект может быть здоровым или страдать каким-либо нарушением, и когда предполагается визуализация, диагностирование, определение или контроль фиброзного заболевания, это обычно означает, что субъект страдает или подозревается в том, что страдает фиброзным заболеванием, и когда предполагается определение эффекта лечения фиброзного заболевания, это обычно означает субъекта, который получил или будет получать лечение фиброзного заболевания.
В способах настоящего изобретения, раскрытых здесь, термин "лечение" включает все типы приемлемых с медицинской точки зрения превентивных и/или терапевтических вмешательств с целью лечения, временной ремиссии или предупреждения нарушения. Например, термин "лечение" включает приемлемое с медицинской точки зрения вмешательство с различными целями, включая задержку или остановку прогрессирования фиброзного заболевания, регрессию или исчезновение повреждений, предупреждение начала фиброзного заболевания и предупреждение рецидива.
Специалистам в данной области техники будет понятно, что многочисленные и различные модификации могут быть сделаны без отступления от сущности настоящего изобретения. Следовательно, необходимо ясно понимать, что формы настоящего изобретения являются только иллюстративными и не предполагают ограничение объема настоящего изобретения.
Примеры
Следующие примеры представлены с целями дополнительного описания представленных здесь вариантов осуществления и не ограничивают объем этого изобретения.
ПРИМЕР 1
Синтез Ретиноид-PGA-DOTA
Полимерный конъюгат Ретиноид-PGA-DOTA получают согласно общей схеме, представленной на Фиг.1, следующим образом: PGA (150 мг) растворяют в диметилформамиде (DMF) (15 мл). Добавляют ретинол (10 мг), дихлорэтан (EDC) (50 мг) и диметиламинопиридин (DMAP) (50 мг). Смесь перемешивают в течение 24 часов. Затем добавляют pNH2-Bn-DOTA (10 мг), EDC (50 мг) и DMAP (50 мг). Полученную смесь перемешивают в течение 24 ч. Затем добавляют разбавленный раствор НСl (0.2 М), чтобы вызвать выпадение осадка. Смесь перемешивают в течение 2 минут и центрифугируют при 10000 об/мин в течение 15 минут. Твердый осадок собирают, промывают водой и повторно растворяют в растворе бикарбоната натрия (0.5 М). Смесь диализируют в воде в течение 24 ч. Продукт, полимерный конъюгат Ретиноид-PGA-DOTA, лиофилизируют. Идентичность продукта подтверждена 1Н-ЯМР.
Пример 2
Синтез Ретиноид-PGA-DTPA
Полимерный конъюгат Ретиноид-PGA-DTPA получают согласно общей схеме, представленной на Фиг.2, следующим образом: PGA (150 мг) растворяют в DMF (15 мл). Добавляют ретинол (10 мг), EDC (50 мг) и DMAP (50 мг). Смесь перемешивают в течение 24 ч. Затем добавляют pNH2-Bn-DTPA (10 мг), EDC (50 мг) и DMAP (50 мг). Полученную смесь перемешивают в течение 24 ч. Затем добавляют разбавленный раствор НСl (0.2М), чтобы вызвать преципитацию. Смесь перемешивают в течение 2 минут и центрифугируют при 10000 об/мин в течение 15 минут. Твердый осадок собирают, промывают водой и повторно растворяют в растворе бикарбоната натрия (0.5 М). Смесь диализируют в воде в течение 24 ч. Продукт, полимерный конъюгат Ретиноид-PGA-DTPA, лиофилизируют. Идентичность продукта подтверждают 1Н-ЯМР.
ПРИМЕР 3
Синтез Ретиноид-PGGA-DOTA
Полимерный конъюгат Ретиноид-PGGA-DOTA получают согласно общей схеме, представленной на Фиг.3, следующим образом: поли(L-гамма-глутамилглутамин) (PGGA, 150 мг) растворяют в DMF (15 мл). Добавляют ретинол (10 мг), EDC (50 мг), и DMAP (50 мг). Смесь перемешивают в течение 24 ч. Затем добавляют pNH2-Bn-DOTA (10 мг), EDC (50 мг) и DMAP (50 мг). Полученную смесь перемешивают в течение 24 ч. Затем добавляют разбавленный раствор НСl (0.2М), чтобы вызвать выпадение осадка. Смесь перемешивают в течение 2 минут и центрифугируют при 10000 об/мин в течение 15 минут. Твердый осадок собирают, промывают водой и повторно растворяют в растворе бикарбоната натрия (0.5 М). Смесь диализируют в воде в течение 24 ч. Продукт, полимерный конъюгат Ретиноид-PGGA-DOTA, лиофилизируют. Идентичность продукта подтверждают 1Н-ЯМР.
ПРИМЕР 4
Синтез Ретиноид-PGGA-DTPA
Полимерный конъюгат Ретиноид-PGGA-DTPA получают согласно общей схеме, представленной на Фиг.4, следующим образом: поли(L-гамма-глутамилглутамин) (PGGA, 150 мг) растворяют в DMF (15 мл). Добавляют ретинол (15 мг), EDC (50 мг) и DMAP (50 мг). Смесь перемешивают в течение 24 ч. Затем добавляют pNH2-Bn-DTPA (10 мг), EDC (50 мг) и DMAP (50 мг). Полученную смесь перемешивают в течение 24 ч. Разбавленный раствор НСl (0.2М) затем добавляют, чтобы вызвать выпадение осадка. Смесь перемешивают в течение 2 минут и центрифугируют при 10000 об/мин в течение 15 минут. Собирают твердый осадок, промывают водой и повторно растворяют раствором бикарбоната натрия (0.5 М). Смесь диализируют в воде в течение 24 ч. Продукт, полимерный конъюгат Ретиноид-PGGA-DTPA, лиофилизируют. Идентичность продукта подтверждена 1Н-ЯМР.
ПРИМЕР 5
Синтез Ретиноид-PGA-[(DOTA)Gd(III)]
Полимерный конъюгат Ретиноид-РСА-[DOTA)Gd(III)] получают согласно общей схеме, представленной на Фиг.5, следующим образом: Ретиноид-PGA-[(DOTA) (45 мг) растворяют в EDTA буфере (10 мл). Добавляют раствор Gd(III) (5 мг) в EDTA (1 мл). Смесь перемешивают в течение 4 ч и выливают в раствор бикарбоната натрия (50 мл) и диализируют в воде. Продукт, Ретиноид-PGA-[(DOTA)Gd(III)], лиофилизируют.
ПРИМЕР 6
Синтез Ретиноид-PGA-[(DTPA)Gd(III)]
Полимерный конъюгат Ретиноид-PGA-[(DTPA)Gd(III)] получают согласно общей схеме, представленной на Фиг.6, следующим образом: Ретиноид-PGA-[(DTPA)] (45 мг) растворяют в EDTA буфере (10 мл). Добавляют раствор Gd(III) (5 мг) в EDTA (1 мл). Смесь перемешивают в течение 4 ч и выливают в раствор бикарбоната натрия (50 мл) и диализируют в воде. Продукт, Ретиноид-PGA-[(DTPA)Gd(III)], лиофилизируют.
ПРИМЕР 7
Синтез Ретиноид-PGGA-[(DOTA)Gd(III)]
Полимерный конъюгат Ретиноид-PGGA-[(DOTA)Gd(III)] получают согласно общей схеме, представленной на Фиг.7, следующим образом: Ретиноид-PGA-[(DOTA) (45 мг) растворяют в EDTA буфере (10 мл). Добавляют раствор Gd(III) (5 мг) в EDTA (1 мл). Смесь перемешивают в течение 4 ч и выливают в раствор бикарбоната натрия (50 мл) и диализируют в воде. Продукт, Ретиноид-PGGA-[(DOTA)Gd(III)], is лиофилизируют.
EXAMPLE 8
Синтез Ретиноид-PGGA-[(DPTA)Gd(III)]
Полимерный конъюгат Ретиноид-PGGA-[(DTPA)Gd(III)] получают согласно общей схеме, представленной на Фиг.8, следующим образом: Ретиноид-PGGA-[(DTPA)] (45 мг) растворяют в EDTA буфере (10 мл). Добавляют раствор Gd(III) (5 мг) в EDTA (1 мл). Смесь перемешивают в течение 4 ч и выливают в раствор бикарбоната натрия (50 мл) и диализируют в воде. Продукт, Ретиноид-PGGA-[(DTPA)Gd(III)], лиофилизируют. Количество Gd(III) в PGGA-[(DTPA)Gd(III)], определенное ICP-MS (масс-спектрометрия с индуктивно связанной плазмой), составляло 8%.
Синтез PGGA-[(DPTA)Gd(III)]
PGGA-[(DTPA)] (45 мг) растворяли EDTA буфере (10 мл). Добавляли раствор Gd(III) (5 мг) в EDTA (1 мл). Смесь перемешивали в течение 4 ч и выливали в раствор бикарбоната натрия (50 мл) и диализировали в воде. Продукт, PGGA-[(DTPA)Gd(III)], лиофилизировали. Количество Gd(III) в PGGA-[(DTPA)Gd(III)], определенное масс-спектрометрией с индуктивно связанной плазмой (ICP-MS), составляло 3%.
ПРИМЕР 9
Синтез Техасский красный-поли(L-глутаминовая кислота)-ретиноида (TR-PGA-ретиноид)
Поли-L-глутаминовую кислоту (PGA, 95.6 мг) помещали в 50 мл круглодонную колбу. В колбу добавляли безводный DMF (15 мл), и суспензию перемешивали в течение 30 минут. Добавляли ретинол (5.5 мг), EDC (12.7 мг) и незначительное количество DMAP. Смесь перемешивали в течение 40 ч. Техасский красный (1 мг в 1 мл DMF), EDC (300 мкл, 5 мг/мл DMF) и HOBt (300 мкл, 1 мг/мл DMF) добавляли в реакционную смесь. Смесь перемешивали в течение 15 ч. Реакционную смесь затем выливали в 0.2 н НСl водный раствор (75 мл). Полученную смесь переносили в центрифужные пробирки и центрифугировали. Супернатант удаляли. Твердое вещество растворяли в 0.5 н NaHCO3 водном растворе (приблизительно 60 мл). Раствор затем диализировали против деионизированной воды, фильтровали через 0.45 мкм целлюлозно-ацетатный шприцевой фильтр и лиофилизировали. Получали TR-PGA-ретиноид (93 мг) и характеризовали 1Н-ЯМР и спектроскопией в ультрафиолетовой и видимой области (UV-Vis).
ПРИМЕР 10
Синтез Техасский красный-поли(L-гамма-глутамилглутамин)-ретиноида (TR-PGGA-Ретиноид)
Поли(L-гамма-глутамилглутамин) (PGGA, 95.5 мг) помещали в 50 мл круглодонную колбу. Добавляли безводный ДМФ (6 мл) в колбу и суспензию перемешивали в течение 30 минут. Добавляли ретинол (5.0 мг), EDC (16.3 мг) и незначительное количество DMAP. Смесь перемешивали в течение 40 ч. Техасский красный (TR) (1 мг в 1 мл DMF), EDC (300 мкл, 5 мг/мл DMF) и HOBt (300 мкл, 1 мг/мл DMF) добавляли в реакционную смесь. Смесь перемешивали в течение 15 ч. Реакционную смесь затем выливали в 0.2 н НСl водный раствор (75 мл). Полученную смесь переносили в центрифужные пробирки и центрифугировали. Супернатант удаляли. Твердое вещество растворяли в 0.5 н НаНСО3 водном растворе (приблизительно 60 мл). Раствор диализировали против деионизированной воды, фильтровали через 0.45 мкм целлюлозно-ацетатный шприцевой фильтр и лиофилизировали. Получали TR-PGGA-ретиноид (91 мг) и характеризовали 1Н-ЯМР и UV-Vis спектроскопией.
Пример 11
Синтез Техасский красный-поли(L-глутаминовая кислота)-холестерина (TR-PGA-холестерин)
Поли(L-глутаминовую кислоту) (PGA, 99.7 мг) помещали в 50 мл круглодонную колбу. Добавляли безводный DMF (15 мл) и суспензию перемешивали в течение 30 минут. Добавляли холестерин (5.9 мг), EDC (10.7 mg) и незначительное количество DMAP. Смесь перемешивали в течение 40 ч. Техасский красный (1 мг в 1 мл DMF), EDC (300 мкл, 5 мг/мл DMF) и HOBt (300 мкл, 1 мг/мл DMF) добавляли к реакционной смеси. Смесь перемешивали в течение 15 ч. Реакционную смесь затем выливали в 0.2 н НСl водный раствор (75 мл). Полученную смесь переносили в центрифужные пробирки и центрифугировали. Супернатант удаляли. Твердое вещество растворяли в 0.5 н NaHCO3 водном растворе (приблизительно 60 мл). Раствор диализировали против деионизированной воды, фильтровали через 0.45 мкм целлюлозно-ацетатный шприцевой фильтр и лиофилизировали. Получали TR-PGA-холестерин (90 мг) и характеризовали 1Н-ЯМР и спектроскопией UV-Vis.
ПРИМЕР 12
Поглощение ретиноидных соединений клетками HSC-T6 Клетки HSC-T6, которые экспрессируют рецептор витамин А-связывающего белка, высевали за день до процедуры в 96-луночный планшет (100 мкл культуральной среды на лунку). TR-PGA-ретиноид, TR-PGGA-ретиноид и TR-PGA-холестерин, как, например, полученные в Примерах 9-11, растворяли в воде с получением приблизительно 2-4 мг/мл маточных растворов. Растворы разбавляли культуральной средой и инкубировали в течение 15 минут при комнатной температуре. Добавляли 15 мкл в клетки. После инкубирования клеток в растворе культуральную среду удаляли. Клетки промывали один раз DPBS (фосфатно-солевой буфер Дюльбекко) и добавляли свежую культуральную среду (100 мкл культуральной среды на ячейку). Поглощение (длины волны возбуждения и излучения составляли соответственно 560 нм и 590 нм) считывали при помощи флуоресцентного ридера для 96-луночных планшетов BioTek FLx800 и регистрировали. Результаты показаны на Фиг.8.
Фиг.8 сравнивает поглощение клетками техасский красный-некатионный полимерный носитель-ретиноида с поглощением клетками техасский красный-некатионный полимерный носитель-холестерина. Большее поглощение означает большую оптическую плотность и большее поглощение клетками. Таким образом. Фиг.8 демонстрирует, что ретиноидные композиции приводят к большему клеточному поглощению, чем холестериновая композиция.
ПРИМЕР 13
Визуализирование с помощью магнитного резонанса Изображения мышей получали на сканере GE 3Т MR, используя катушку для колена, до и после введения контраста. Следующие параметры получения изображений представляли собой ТЕ: мин. наполн., TR=250 мс, FOV: 8 и 24 срезов/проход (slab), и толщина коронального среза 1.0 мм. Дозы инъекций тестируемых соединений, Ретиноид-PGGA-[(DPTA)Gd(III)] и PGGA-[(DPTA)Gd(III)], полученных как описано в Примере 8, составляют 0.05 ммоль иона металла/кг крысиных DMA-моделей с фиброзом печени (n=3 для каждого момента времени для каждого соединения). Соединения вводили инъекцией через хвостовую вену в анестезированных мышей и изображения получали до инъекции и через 5 минут, 15 минут и 60 минут после инъекции контрастных агентов (см. Фиг.9). Получали среднюю относительную оптическую плотность Gd(III) и демонстрировали как на Фиг.10.
Пример 14
Визуализация in vivo для мышиных моделей цирроза
Мышиная модель, имеющая цирроз, вызванный тетрахлоридом углерода (далее упоминаемая также как "цирротическая мышь"), и нормальная мышь использовались для неинвазивного исследования очагов снаружи организма.
В качестве цирротической мыши использовали 4-недельного самца мыши C57BL/6J (Charles River), которому внутрибрюшинно инъецировали CCl4 (1 мкл/г массы тела), разбавленный оливковым маслом 1:10, дважды в неделю в течение 28 недель. Что касается нормальной мыши (контрольная группа), использовали 20-недельного самца мыши C57BL/6J.
За 2 недели до исследования мышей кормили, как обычно, кормом, не содержащим люцерну, для того, чтобы уменьшить эффект автономной флуоресценции, получаемой из корма в желудочно-кишечном тракте. Для того чтобы уменьшить степень снижения сигнала из-за кожи с шерстью, шерсть с живота и спины удаляют.
В качестве флуоресцентного зонда для детектирования сигналов внутри организма использовали Cу™ 5.5-меченную scramble siRNA (смысловая: 5′-Cу™ 5.5-CUUACGCUGAGUACUUCGATT-3′ (SEQ ID NO: 1), антисмысловая: 5′-Cу™ 5.5-UCGAAGUACUCAGCGUAAGTT-3′ (SEQ ID NO: 2); далее также упоминаемую как "siRNA scr-Cу™ 5.5"). В качестве носителя использовали Lipotrust SR (Hokkaido System Science Co., Ltd.) (далее также упоминается как "липосома"). В качестве предварительной смеси готовили 100 мМ витамина А (ретинол (Sigma), далее также упоминается как VA, растворенный в диметилсульфоксиде), 1 мМ Lipotrust SR (растворенного в воде, не содержащей нуклеаз) и siRNA scr-Cу™ 5.5, разбавленной до 10 мкг/мкл в воде, не содержащей нуклеаз. Сначала, Lipotrust SR и VA смешивали в соотношении 1:1 (мол./мол.), перемешивали встряхиванием 15 с, затем оставляли стоять при комнатной температуре, защищая от света, в течение 5 мин для образования комплекса. К этому комплексу добавляли 10 мкг/мкл siRNA scr-Cу™ 5.5 и осторожно перемешивали, получая визуализирующий агент (VA-Lip-Cу) согласно настоящему изобретению. Композиция полученного визуализирующего агента содержала по отношению к 100 мкл визуализирующего агента, 100 нмоль (28.6 мг) ретинола, 100 нмоль (62.6 мг) катионного липида, образующего липосому, и 10 мкг Cу™ 5.5-меченной siRNA. Этот визуализирующий агент является таким, в котором по меньшей мере часть ретиноида экспонирована снаружи визуализирующего агента перед тем, как он достигнет клеток-мишеней. Визуализирующий агент без VA (Lip-Cу) получали аналогичным образом. Эти визуализирующие агенты медленно вводили мышам, имеющим массу тела 30 г, через хвостовую вену под анестезией газом изофлураном в количестве 100 мкл на мышь.
Перед введением и через 5-90 мин после введения флуоресцентные участки мыши обнаруживали с течением времени, используя визуализирующую систему IVIS (XENOGEN, IVIS(R)200), и измеряли флуоресцентные сигналы. Для количественного анализа измеряли физическую величину (фотон/сек; далее также выражаемую как ф/с), основываясь на теории модели диффузии в ткани, вместо интенсивности люминесценции (импульсы), и измерения численно выражали средней интенсивностью излучения (сред. излучение, ф/с/см2/ср) и строили график после поправки на источник света возбуждения (выражено через среднюю эффективность (сред. эффективность)). Здесь "ф/с/см2/ср" является аббревиатурой "фотонов на секунду на квадратный сантиметр на стерадиан", где стерадиан означает единицу телесного угла. На 90 мин после введения мышь умерщвляли и удаляли печень, фиксировали 4% параформальдегидом и заливали парафином, получая образец в виде тонкого среза. Образец окрашивали альфа-SMA-FITC (Sigma, F3777) для подтверждения внутриклеточной локализации сигналов siRNA scr-Cу™ 5.5. Дополнительно анализировали соотношение области, положительной и по Cу™ 5.5, и по FITC, по отношению к общей Cу™ 5.5-положительной области (альфа-SMA объед./Cу™ 5.5 положительная область), и соотношение числа клеток, положительных и по Cу™ 5.5, и по FITC по отношению к общему числу Cу™ 5.5-положительных клеток (альфа-SMA объед./Cу™ 5.5 положительные клетки).
Как у цирротической мыши, которой вводили VA-Lip-Cу (Цирроз), так и у нормальной мыши) (Нормал.) сигналы обнаруживали в печени (Печень) через 5 мин после начала введения, но сигналы были значительно сильнее у цирротической мыши, чем у нормальной мыши. В отличие от этого, сигналы в кишечном тракте (Кишечник) у цирротической мыши не демонстрировали почти никаких изменений, тогда как у нормальной мыши демонстрировали постепенное увеличение через 30 мин после начала введения (Фиг.12 и 13).
Из результата окрашивания образцов печени можно увидеть, что число клеток, положительных и по альфа-SMA (FITC), и по siPHK (Cу™ 5.5), у цирротической мыши, которой вводили VA-Lip-Cу (VA(+)), значительно больше, чем у цирротической мыши, которой вводили Lip-Cу (VA(-)), или у нормальной мыши, которой вводили VA-Lip-Cу (Фиг.14-16).
Эти результаты демонстрируют, что у цирротической мыши визуализирующий агент согласно настоящему изобретению специфически метит активированные звездчатые клетки, положительные по альфа-SMA, и остается в фиброзном очаге, тогда как у нормальной мыши визуализирующий агент согласно настоящему изобретению не остается в печени, а перемещается в кишечный тракт. Соответственно, путем наблюдения и количественного анализа такой метки снаружи организма могут быть определены или диагностированы неинвазивно и легко присутствие/отсутствие фиброзного заболевания и его тяжесть. Кроме того, неинвазивное и временное наблюдение за отдельным индивидуумом становится возможным, таким образом давая возможность оценки терапии с высокой точностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ ПОЛИГЛУТАМАТ-АМИНОКИСЛОТА И СПОСОБЫ | 2006 |
|
RU2472812C2 |
| ХЕЛАТНЫЕ АМФИФИЛЬНЫЕ ПОЛИМЕРЫ | 2009 |
|
RU2519713C2 |
| НОСИТЕЛИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2008 |
|
RU2505315C2 |
| АНТАГОНИСТЫ GRPR ДЛЯ ОБНАРУЖЕНИЯ, ДИАГНОСТИКИ И ЛЕЧЕНИЯ GRPR-ПОЗИТИВНОГО ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2013 |
|
RU2693465C2 |
| АНТАГОНИСТЫ GRPR ДЛЯ ОБНАРУЖЕНИЯ, ДИАГНОСТИКИ И ЛЕЧЕНИЯ GRPR-ПОЗИТИВНОГО ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2013 |
|
RU2821944C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ЛИЗИЛОКСИДАЗОПОДОБНЫМ ФЕРМЕНТОМ-2 (LOXL2), И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2549684C2 |
| НОВЫЕ ПСА-СВЯЗЫВАЮЩИЕ АГЕНТЫ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2787105C2 |
| СПОСОБЫ ИДЕНТИФИКАЦИИ САЙТОВ ДЛЯ КОНЪЮГАЦИИ IgG | 2010 |
|
RU2569186C2 |
| КОНЪЮГАТ, ВКЛЮЧАЮЩИЙ ЛИГАНД, СПЕЙСЕР, ПЕПТИДНЫЙ ЛИНКЕР И БИОМОЛЕКУЛУ | 2020 |
|
RU2807081C2 |
| СПЕЦИФИЧЕСКИЕ К ОПУХОЛИ АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2595403C2 |

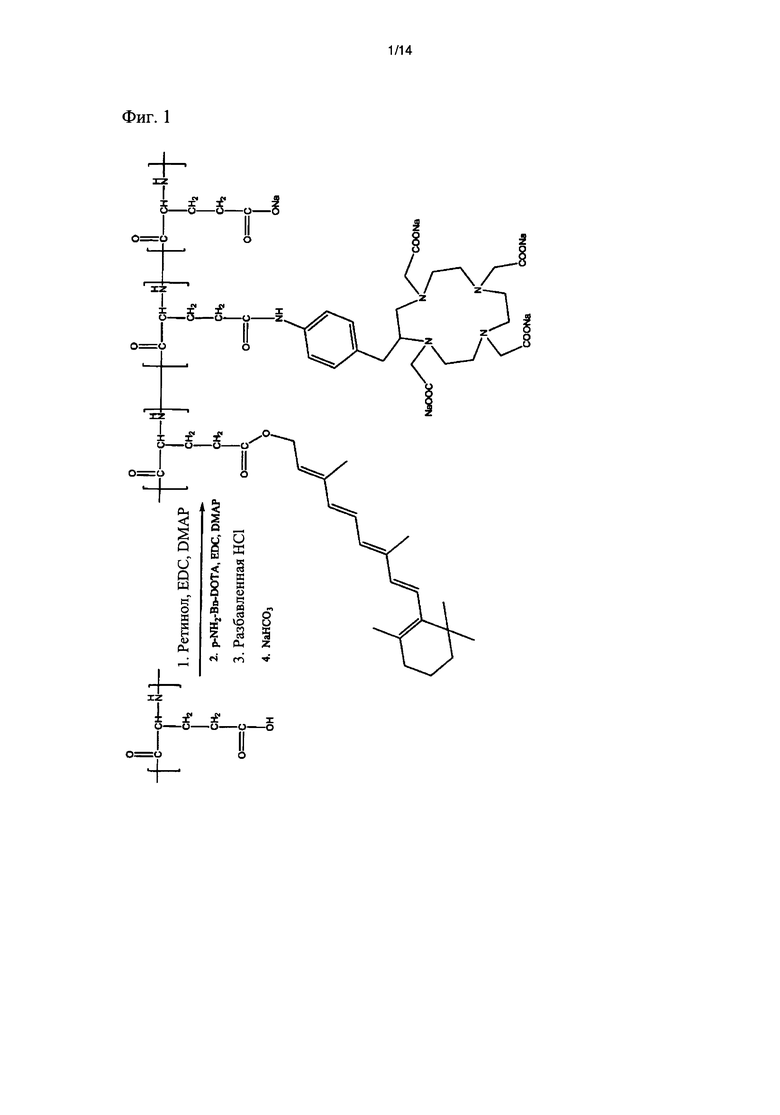
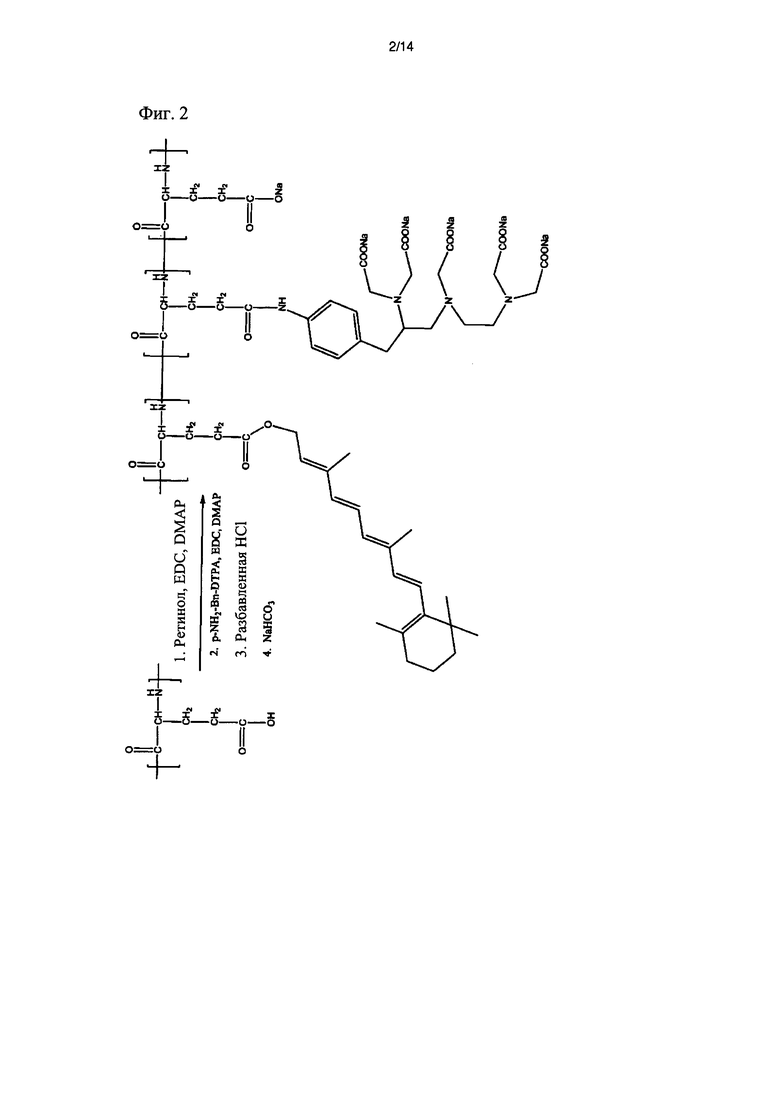

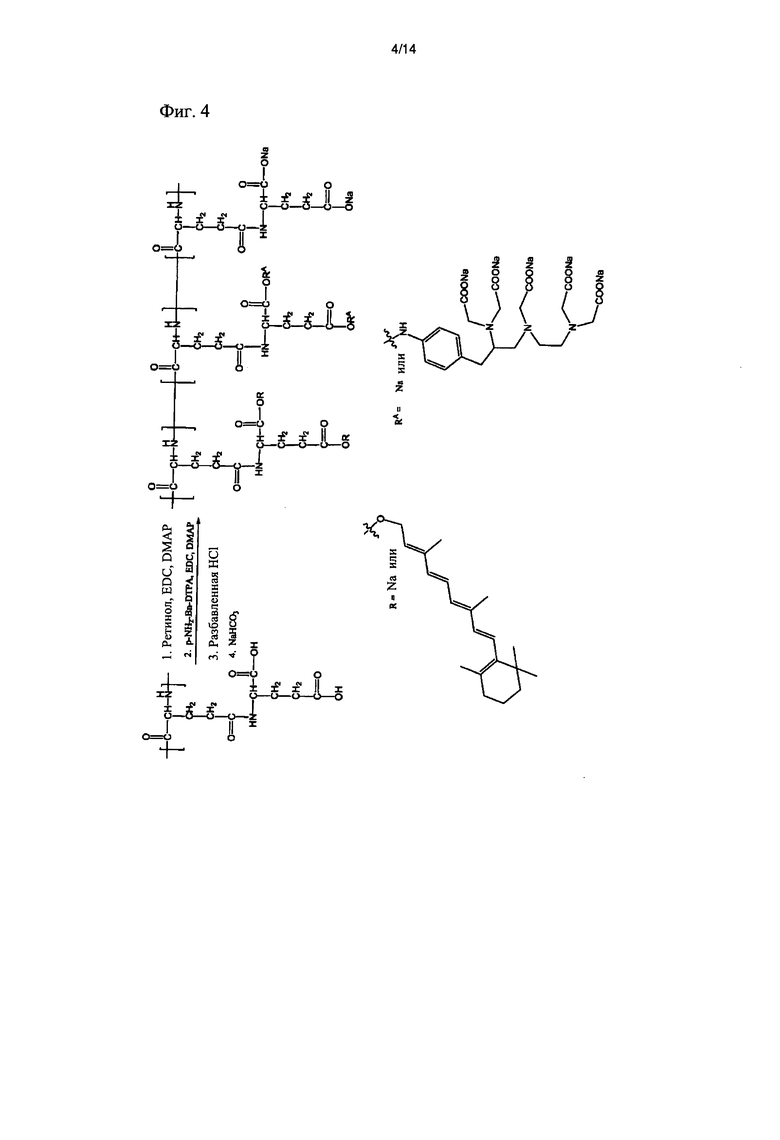
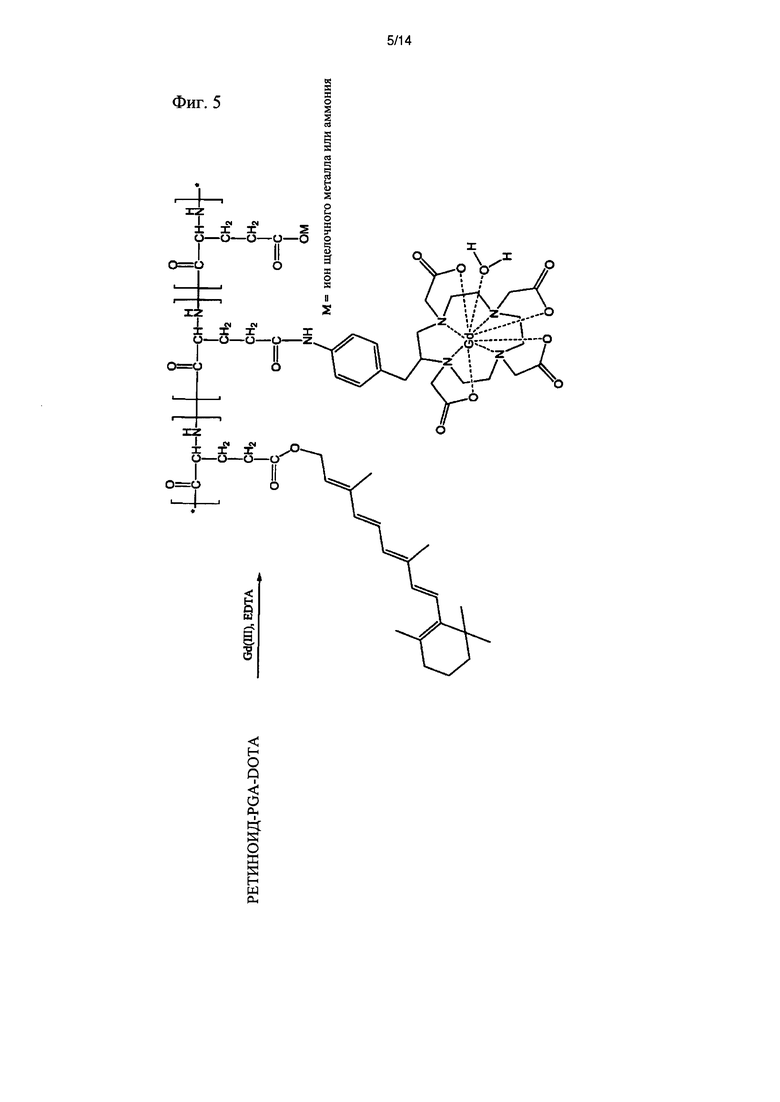
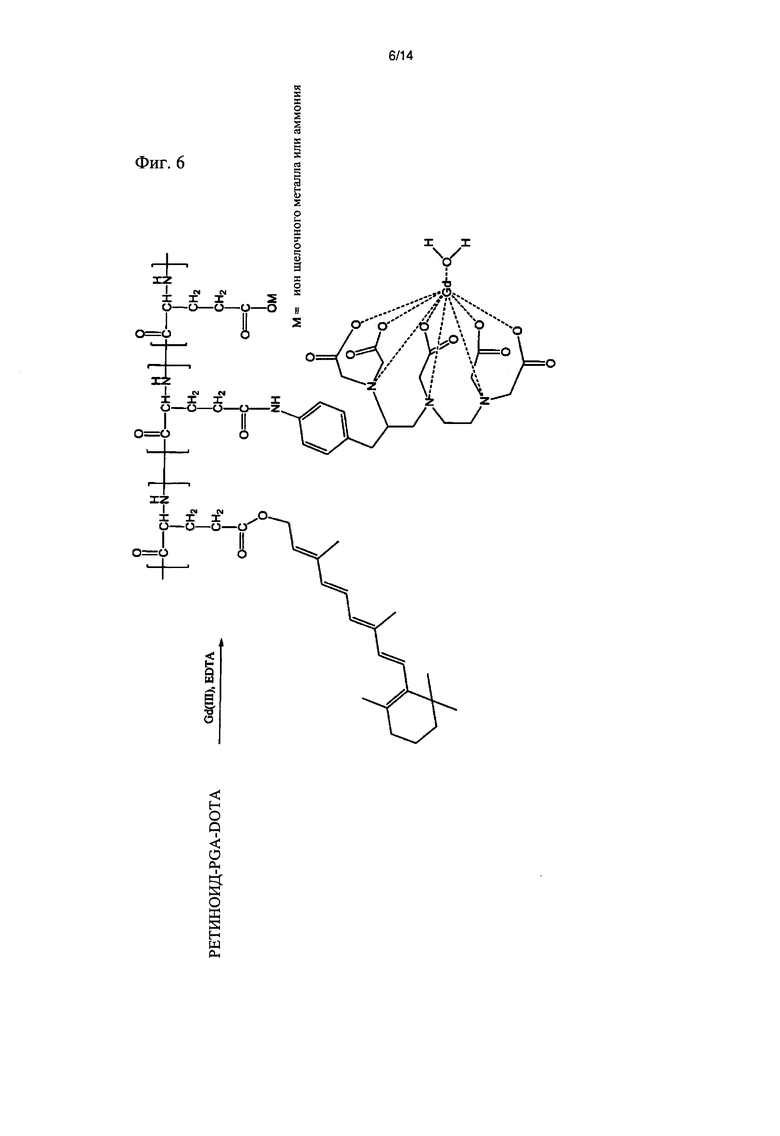
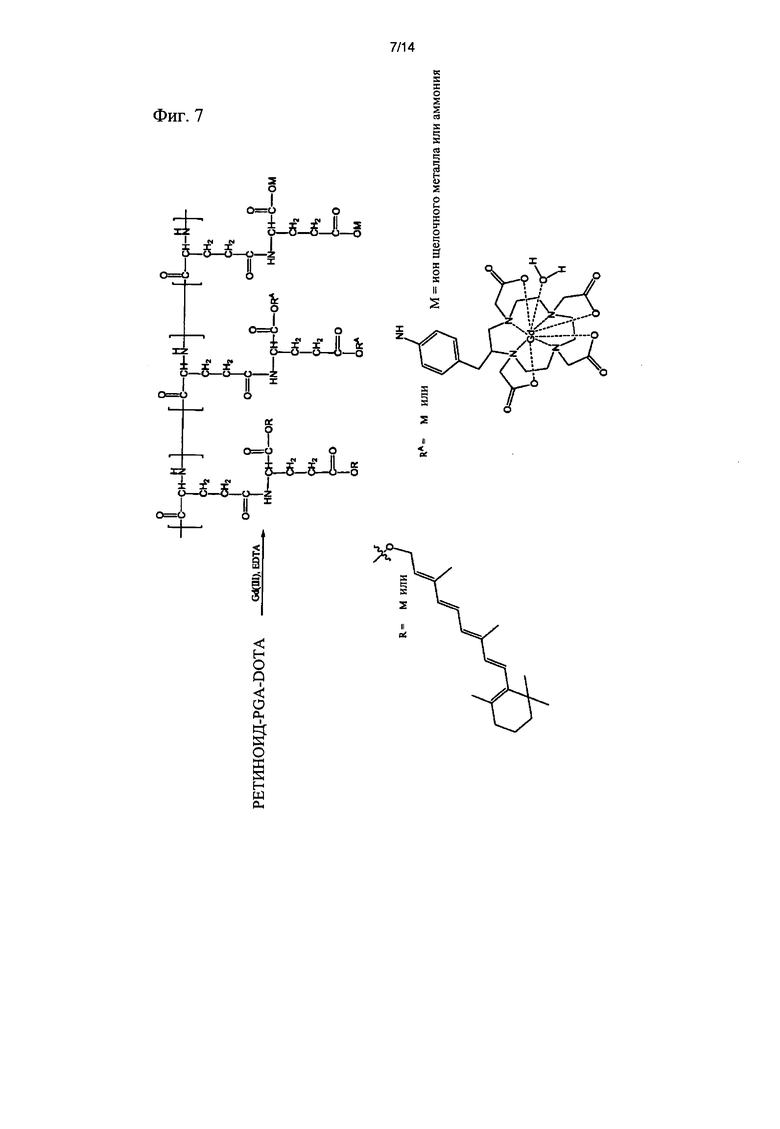





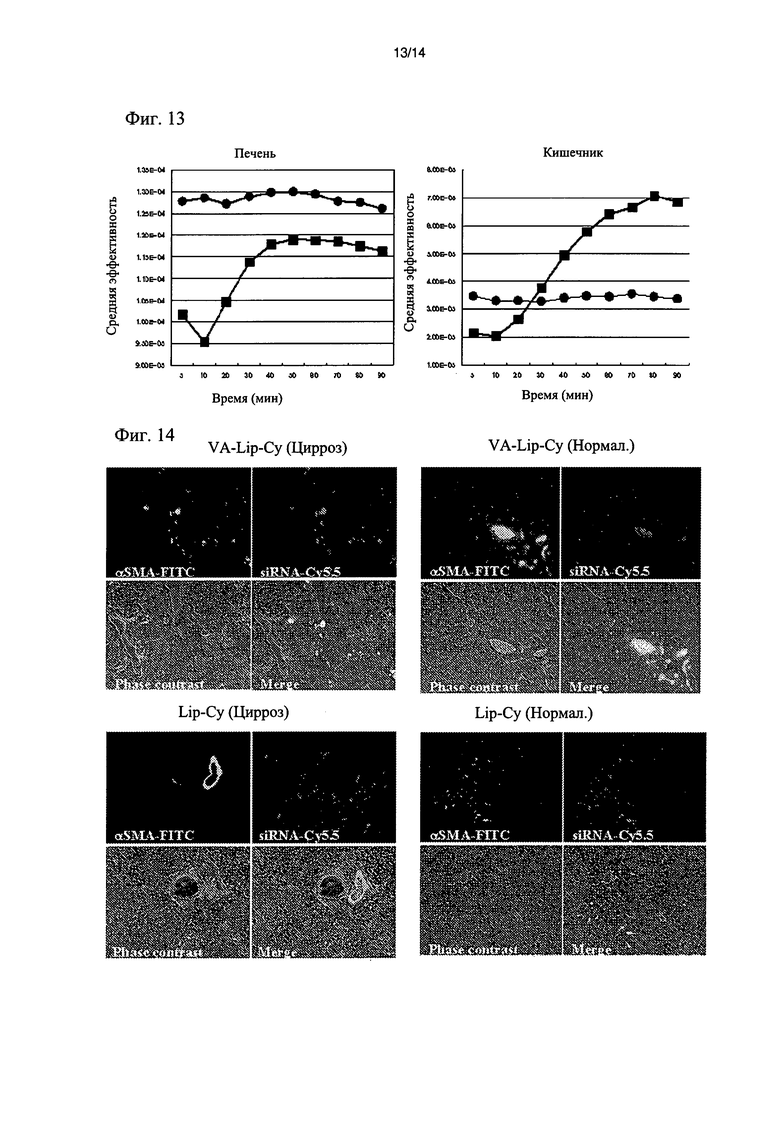

Изобретение касается визуализирующих агентов, используемых в неинвазивных способах диагностики фиброзного заболевания, контроля фиброзного заболевания и способа определения эффекта лечения фиброзного заболевания. Способ диагностики включает стадию введения in vivo визуализирующего агента, содержащего ретиноид и детектируемую метку, тестируемому субъекту и контрольному субъекту и стадию сравнения изменения через 5-90 минут после введения интенсивности сигнала и/или распределения сигнала метки, детектируемой у тестируемого субъекта, с изменением через 5-90 минут после введения интенсивности контрольного сигнала и/или распределения контрольного сигнала метки, детектируемой у контрольного субъекта. Способы контроля и определения эффекта лечения включают стадию введения in vivo визуализирующего агента, содержащего ретиноид и детектируемую метку, субъекту и стадию сравнения интенсивности сигнала и/или распределения сигнала метки, детектируемой в первый момент времени у субъекта, с интенсивностью сигнала и/или распределением сигнала метки, детектируемой у указанного субъекта во второй момент времени, который является более поздним, чем первый момент времени. 3 н. и 6 з.п. ф-лы, 14 пр., 16 ил.
1. Способ диагностики фиброзного заболевания, включающий стадию введения in vivo визуализирующего агента, содержащего ретиноид и детектируемую метку, тестируемому субъекту и контрольному субъекту и стадию сравнения изменения через 5-90 минут после введения интенсивности сигнала и/или распределения сигнала метки, детектируемой у тестируемого субъекта, с изменением через 5-90 минут после введения интенсивности контрольного сигнала и/или распределения контрольного сигнала метки, детектируемой у контрольного субъекта, где когда изменение через 5-90 минут после введения интенсивности сигнала и/или распределения сигнала метки, обнаруженной у тестируемого субъекта, соответствует изменению через 5-90 минут после введения интенсивности контрольного сигнала и/или распределения контрольного сигнала у контрольного субъекта, который не страдает фиброзным заболеванием, тестируемый субъект определяется как негативный по фиброзному заболеванию, или когда изменение через 5-90 минут после введения интенсивности сигнала и/или распределения сигнала метки, обнаруженной у тестируемого субъекта, соответствует изменению через 5-90 минут после введения интенсивности контрольного сигнала и/или распределения контрольного сигнала у контрольного субъекта, который страдает фиброзным заболеванием, тестируемый субъект определяется как положительный по фиброзному заболеванию, и где детектируемая метка может быть обнаружена средствами детектирования, выбранными из группы, включающей невооруженный глаз, устройство для оптического исследования, рентгеновскую установку, аппарат для МРТ, аппарат для радионуклидного исследования, ультрасонографический аппарат и термографический аппарат, где детектируемая метка представляет собой хелат парамагнитного металла, который содержит
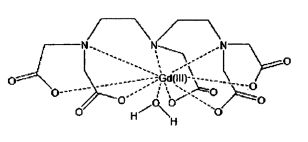 или
или  .
.
2. Способ по п. 1, где ретиноид содержит ретинол.
3. Способ по п. 1, где способ осуществляется неинвазивно.
4. Способ контроля фиброзного заболевания, содержащий стадию введения in vivo визуализирующего агента, содержащего ретиноид и детектируемую метку, субъекту и стадию сравнения интенсивности сигнала и/или распределения сигнала метки, детектируемой в первый момент времени у субъекта, с интенсивностью сигнала и/или распределением сигнала метки, детектируемой у указанного субъекта во второй момент времени, который является более поздним, чем первый момент времени, где если интенсивность сигнала во второй момент времени ниже, чем в первый момент времени, для фиброзного заболевания может быть определено улучшение, и наоборот, если интенсивность сигнала во второй момент времени выше, чем в первый момент времени, для фиброзного заболевания может быть определено ухудшение, или если распределение сигнала во второй момент времени уже, чем в первый момент времени, для фиброзного заболевания может быть определено улучшение, и наоборот, если распределение сигнала во второй момент времени шире, чем в первый момент времени, для фиброзного заболевания может быть определено ухудшение, и где детектируемая метка может быть обнаружена средствами детектирования, выбранными из группы, включающей невооруженный глаз, устройство для оптического исследования, рентгеновскую установку, аппарат для МРТ, аппарат для радионуклидного исследования, ультрасонографический аппарат и термографический аппарат, где детектируемая метка представляет собой хелат парамагнитного металла, который содержит
 или
или  .
.
5. Способ по п. 4, где ретиноид содержит ретинол.
6. Способ по п. 4, где способ осуществляется неинвазивно.
7. Способ определения эффекта лечения фиброзного заболевания, содержащий стадию введения in vivo визуализирующего агента, содержащего ретиноид и детектируемую метку, субъекту и стадию сравнения интенсивности сигнала и/или распределения сигнала метки, детектируемой в первый момент времени у субъекта, с интенсивностью сигнала и/или распределением сигнала метки, детектируемой у указанного субъекта во второй момент времени, который является более поздним, чем первый момент времени, где первый момент времени имеет место перед тем, как субъект получит лечение фиброзного заболевания, а второй момент времени имеет место после того, как субъект получил лечение фиброзного заболевания, или, альтернативно, первый момент времени имеет место после того, как субъект получил первое лечение фиброзного заболевания, а второй момент времени имеет место после того, как субъект получил второе лечение фиброзного заболевания, которое осуществлялось после первого лечения фиброзного заболевания, где если интенсивность сигнала во второй момент времени ниже, чем в первый момент времени, лечение является удачным, и наоборот, если интенсивность сигнала во второй момент времени выше, чем в первый момент времени, лечение является неудачным, или если распределение сигнала во второй момент времени является уже, чем в первый момент времени, лечение является удачным, и наоборот, если распределение сигнала во второй момент времени шире, чем в первый момент времени, лечение является неудачным, и где детектируемая метка может быть обнаружена средствами детектирования, выбранными из группы, включающей невооруженный глаз, устройство для оптического исследования, рентгеновскую установку, аппарат для МРТ, аппарат для радионуклидного исследования, ультрасонографический аппарат и термографический аппарат, где детектируемая метка представляет собой хелат парамагнитного металла, который содержит
 или
или  .
.
8. Способ по п. 4, где ретиноид содержит ретинол.
9. Способ по п. 4, где способ осуществляется неинвазивно.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| EP 1842557 A1, 10.10.2007 | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2016-09-10—Публикация
2009-09-11—Подача