Изобретение относится к химико-фармацевтической промышленности, в частности к способу количественного определения стеринов в корневищах с корнями крапивы двудомной (Urtica dioica L.), и может быть использовано в центрах контроля качества лекарственных средств и контрольно-аналитических лабораториях при проведении анализа стеринов в сырье данного растения.
Действующая система контроля качества требует постоянного усовершенствования подходов к стандартизации биологически активных соединений (БАС) с использованием современных методов анализа и актуальных данных об их свойствах, позволяющих селективно определять конкретные группы БАС.
В России лекарственным сырьем крапивы двудомной являются листья как источник витамина К1. Кроме того, известно, что за рубежом применяются корневища с корнями, в качестве источника препаратов для урологической практики, обладающих противоопухолевой активностью (Простафортон, Базотон) (1, 2). Несмотря на положительный европейский опыт в применении корневищ с корнями крапивы двудомной, в нашей стране до сих пор не выпускаются препараты на основе корневищ с корнями крапивы двудомной. Это связано с тем обстоятельством, что в настоящее время отсутствует фармакопейная статья на указанный вид сырья, а также препараты на его основе.
Химический состав корневищ с корнями крапивы двудомной достаточно богат и содержат стерины, полисахариды, лектины и другие соединения (2). В то же время до сих пор остается неясным, какая именно группа БАС обладает антинеопластической активностью. При этом большинство авторов склоняются к мысли, что этим свойством обладают стерины (1, 2, 3). Необходимым условием для проверки правильности этого предположения является выделение индивидуальных БАС из корневищ с корнями крапивы двудомной и исследование их свойств.
В качестве прототипа нами выбран спектроскопический метод количественного определения стеринов и сапонинов, основанный на галохромной реакции в серной кислоте (4, 5). Однако данный метод не позволяет селективно определить спектральные характеристики стеринов, отличается многостадийной пробоподготовкой, в ходе которой анализируемая проба перед растворением в серной кислоте досуха высушивается. Это существенно увеличивает время анализа, может приводить к деструкции анализируемых БАС и к искажению результатов анализа (ошибка единичного определения составляет ±5,60%).
Ранее нами с помощью колоночной хроматографии был выделен один из доминирующих компонентов корневищ с корнями крапивы двудомной. С помощью 1Н-ЯМР, ТСХ, и масс-спектрометрии было установлено, что выделенное вещество является эргостерином (6).
Таким образом, целью изобретения является разработка 1 метода количественного определения суммы стеринов в корневищах с корнями крапивы двудомной.
Техническим результатом является улучшение способа количественного анализа стеринов в корневищах с корнями крапивы двудомной.
Технический результат достигается тем, что извлечения стеринов из лекарственного растительного сырья осуществляется с помощью спирта этилового 70%, с последующим определением стеринов по оптической плотности в концентрированной серной кислоте, на фоне концентрированной серной кислоты при аналитической длине волны 328 нм, при этом расчет содержания стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
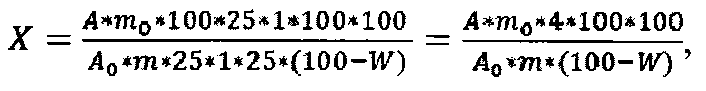
где А - оптическая плотность испытуемого раствора;
Ao - оптическая плотность раствора стандартного образца;
m - точная навеска сырья, г;
mo - точная навеска эргостерина, г;
W - влажность сырья, %.
В случае отсутствия рабочего стандартного образца эргостерина используют значение удельного показателя поглощения его раствора - 800; расчет содержания стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
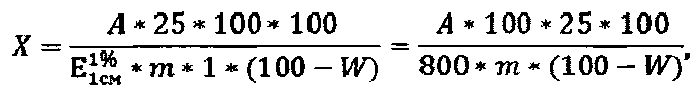
где А - оптическая плотность испытуемого раствора;
m - точная навеска анализируемого образца, г;
W - влажность сырья, %.
800 - удельный показатель поглощения эргостерина.
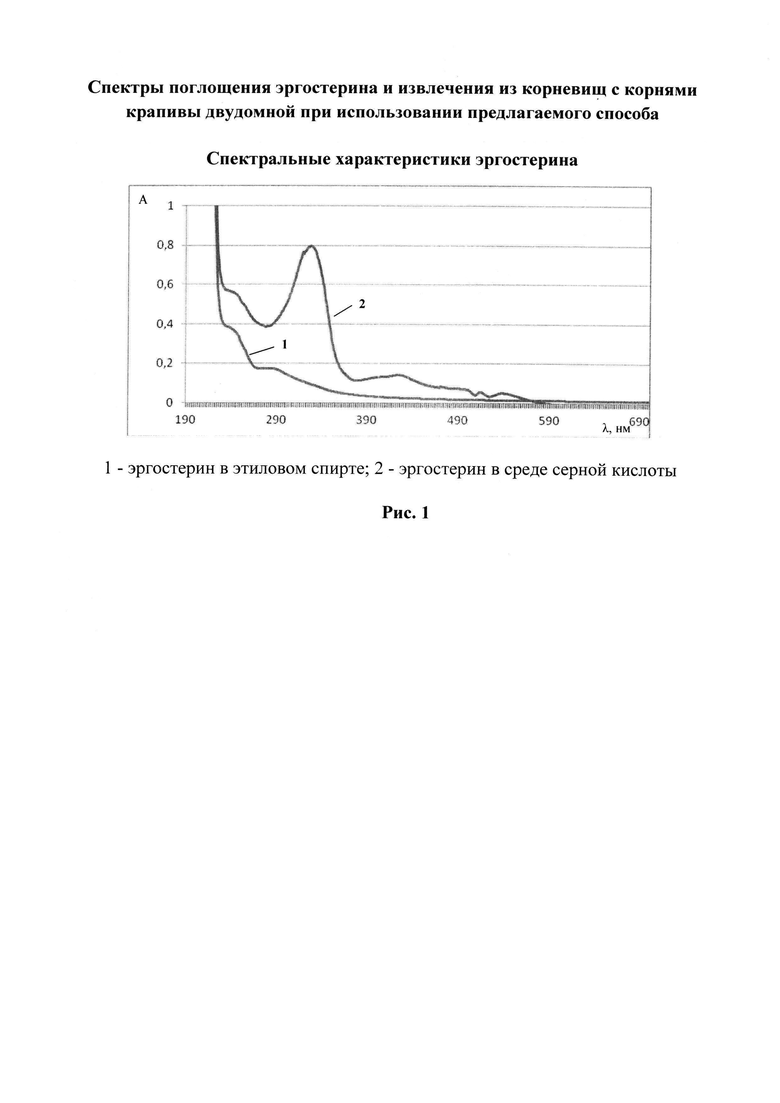
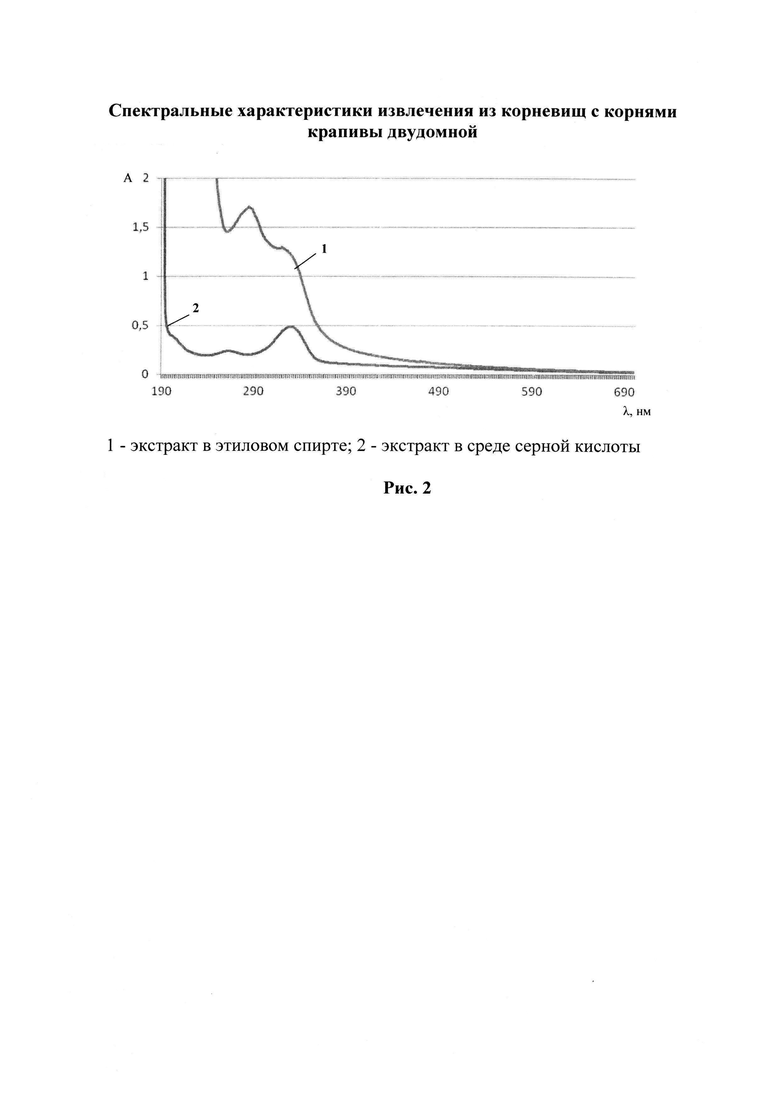
В качестве раствора стандартного образца целесообразно использовать раствор эргостерина или значение его удельного показателя поглощения в концентрированной серной кислоте, так как результаты спектрофотометрического исследования растворов эргостерина и извлечений из корневищ с корнями крапивы двудомной, представленные на рис. 1 и 2, показывают наличие одинаковых максимумов поглощения при аналитической длине волны 328 нм (рис. 1, 2). В результате происходит уменьшение риска термического разложения химических соединений, продолжительности, уменьшения числа технологических стадий, сокращается время анализа и повышается точность метода количественного определения стеринов в лекарственном растительном сырье.
Способ реализуется следующим образом.
Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. Около 1 г измельченного сырья (точная навеска) помещают в коническую колбу со шлифом вместимостью 200 мл, добавляют 100 мл 70% этилового спирта. Колбу закрывают пробкой и взвешивают на тарирных весах с точностью до ±0,01 г. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане (умеренное кипение) в течение 30 мин, затем закрывают той же пробкой, охлаждают до комнатной температуры, после чего колбу снова взвешивают и восполняют недостающий экстрагент до первоначальной массы. Извлечение перемешивают и фильтруют через бумажный фильтр. 1 мл полученного извлечения помещают в градуированную пробирку на 10 мл, добавляют осторожно по каплям 4 мл серной кислоты концентрированной и нагревают на водяной бане при температуре 70°С в течение 1 часа. Затем содержимое пробирки количественно переносят в мерную колбу вместимостью 25 мл и объем доводят концентрированной серной кислотой до метки (испытуемый раствор А). Измерение оптической плотности проводят сразу после приготовления раствора при аналитической длине волны 328 нм. Параллельно измеряют оптическую плотность раствора стандартного образца эргостерина.
Приготовление раствора эргостерина. Около 0,01 г (точная навеска) стандартного образца эргостерина помещают в мерную колбу вместимостью 25 мл, растворяют в 10 мл в концентрированной серной кислоты, нагревают в водяной бане при температуре 70°С в течение 1 часа, охлаждают до комнатной температуры, доводят объем раствора до метки концентрированной серной кислотой и перемешивают. 1 мл полученного раствора помещают в мерную колбу вместимостью 25 мл, доводят до метки концентрированной серной кислотой, перемешивают и измеряют оптическую плотность сразу после приготовления раствора при аналитической длине волны 328 нм. При этом в качестве раствора сравнения используют концентрированную серную кислоту.
Расчет количественного содержания стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
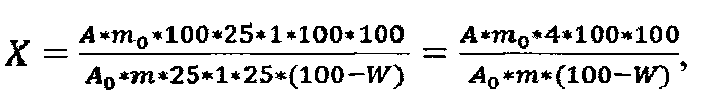
где А - оптическая плотность испытуемого раствора;
Ao - оптическая плотность раствора стандартного образца;
m - точная навеска сырья, г;
mo - точная навеска эргостерина, г;
W - влажность сырья, %.
В случае отсутствия рабочего стандартного образца эргостерина используют значение удельного показателя поглощения его раствора - 800; расчет содержания стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
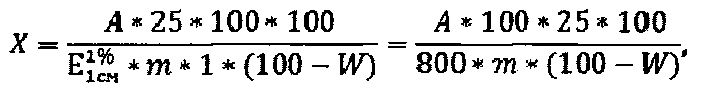
где А - оптическая плотность испытуемого раствора;
m - точная навеска анализируемого образца, г;
W - влажность сырья, %.
800 - удельный показатель поглощения эргостерина.
Предлагаемый способ поясняется следующими примерами.
Пример 1
Аналитическую пробу корневищ с корнями крапивы двудомной, заготовленного в Ботаническом саду в 2014 г., измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. Около 1 г сырья (точная навеска) воздушно-сухого сырья помещают в коническую колбу со шлифом вместимостью 200 мл, добавляют 100 мл 70% этилового спирта. Колбу закрывают пробкой и взвешивают на тарирных весах с точностью до ±0,01 г. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане (умеренное кипение) в течение 30 мин. Затем закрывают той же пробкой, охлаждают до комнатной температуры. После чего колбу снова взвешивают и восполняют недостающий экстрагент до первоначальной массы. Извлечение перемешивают и фильтруют через бумажный фильтр. 1 мл полученного извлечения помещают в градуированную пробирку на 10 мл, добавляют осторожно по каплям 4 мл серной кислоты концентрированной и нагревают на водяной бане при температуре 70°С в течение 1 часа. Затем содержимое пробирки количественно переносят в мерную колбу вместимостью 25 мл и объем доводят концентрированной серной кислотой до метки (испытуемый раствор А). Измерение оптической плотности проводят на спектрофотометре при длине волны 328 нм. Параллельно измеряют оптическую плотность раствора эргостерина. Определяем значение оптической плотности испытуемого раствора А=0,924629, раствора эргостерина А0=0,701958, массу сырья m=1,0050 и стандартного образца эргостерина m0=0,0056.
Содержание суммы стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
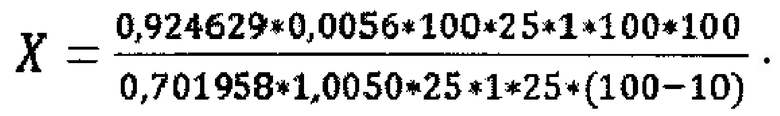
Содержание стеринов X=3,26%.
Испытание проведено в нескольких повторностях. Все данные были статистически обработаны. Ошибка единичного определения с доверительной вероятностью 95% составляет ±1,54%.
Пример 2
Аналитическую пробу корневищ с корнями крапивы двудомной, заготовленных в с. Большая Черниговка в 2014 г., измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. Около 1 г сырья (точная навеска) воздушно-сухого сырья помещают в коническую колбу со шлифом вместимостью 200 мл, добавляют 100 мл 70% этилового спирта. Далее процесс проводят в соответствии с примером 1.
Для расчета содержания стеринов использовали удельный показатель поглощения эргостерина, который равен 800, определили значение оптической плотности испытуемого раствора А=0,942034, массу сырья m=1,0070.
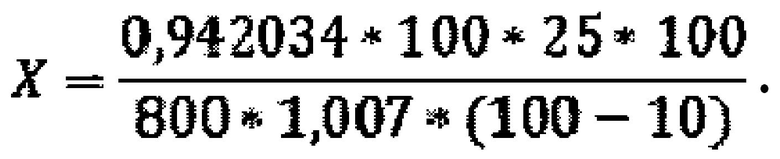
Содержание суммы стеринов Х=3,25%.
Испытание проведено в нескольких повторностях. Все данные были статистически обработаны. Ошибка единичного определения с доверительной вероятностью 95% составляет ±1,54%.
Таким образом, заявленный способ количественного определения стеринов в корневищах с корнями крапивы двудомной разработан впервые для анализа данной группы БАС и обладает следующими преимуществами:
1) позволяет селективно анализировать выбранную группу БАС в корневищах с корнями крапивы двудомной;
2) существенно сокращает время анализа сырья: с 4 часов (прототип) до 3 часов;
3) сокращается количество технологических стадий: с 11 (прототип) до 7;
4) уменьшается ошибка единичного определения: с±5,60% (прототип) до ±1,54%.
Источники информации
1. Кукес В.Г. Фитотерапия с основами клинической фармакологии / Под ред. В.Г. Кукеса. - М.: Медицина, - 1999. - 192 с.
2. Куркин В.А. Фармакогнозия: Учебник для студентов фармацевтических вузов / Изд. 2-е, перераб. и доп. - Самара: ООО «Офорт», ГОУ ВПО «СамГМУ», - 2007. - 1239 с.
3. American herbal pharmacopoeia® botanical pharmacognosy - microscopic characterization of botanical medicines - CRC Press is an imprint of Taylor & Francis Group, an Informa business, - 2011.
4. Генкина Г.Л, Мжельская Л.Г. Спектрофотометрия гликозидов олеаноловой кислоты и хедерагенина в концентрированной серной кислоте // Химия природных соединений, - 1977. - №2. - с. 220-227.
5. Пономарев В.Д., Оганесян Э.Т. Спектры поглощения пентациклических тритерпеноидов в серной кислоте // Химия природных соединений, -1971. - №2. с. 147-150.
6. Балагозян Э.А., Рыжов В.М. Исследование стериновых соединений густого экстракта корневищ с корнями крапивы двудомной // Сборник материалов IV Всероссийской научной конференции студентов и аспирантов с международным участием «Молодая фармация - потенциал будущего», Санкт-Петербург, 2014 г. - СПб.: Изд-во СПХФА, - 2014. C. 406-408.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЕНИЛПРОПАНОИДОВ В КОРНЕВИЩАХ И КОРНЯХ ЭЛЕУТЕРОКОККА КОЛЮЧЕГО | 2022 |
|
RU2797411C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ САПОНИНОВ В ТРАВЕ ГИНОСТЕММЫ ПЯТИЛИСТНОЙ | 2022 |
|
RU2790821C1 |
| Способ идентификации и раздельного количественного определения танина и галловой кислоты при совместном присутствии в растительном сырье и фитопрепаратах без предварительного разделения | 2015 |
|
RU2613878C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГИПОГЛИКЕМИЧЕСКОЙ И ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2506091C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2141841C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНТОЦИАНОВ В ЛЕКАРСТВЕННОМ РАСТИТЕЛЬНОМ СЫРЬЕ | 2013 |
|
RU2557953C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КАЛЬЦИЯ И МАГНИЯ В ЛЕКАРСТВЕННОМ РАСТИТЕЛЬНОМ СЫРЬЕ | 2011 |
|
RU2466387C1 |
| СБОР ЛЕКАРСТВЕННЫХ РАСТЕНИЙ "ГАЛЕЧЕР", ОБЛАДАЮЩИЙ ГИПОГЛИКЕМИЧЕСКИМ ДЕЙСТВИЕМ (ВАРИАНТЫ) | 2006 |
|
RU2331431C1 |
| Способ количественного определения суммы флавоноидов в почках дуба черешчатого | 2021 |
|
RU2782618C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ТРАВЕ ЧЕРНУШКИ ПОСЕВНОЙ | 2022 |
|
RU2786440C1 |
Изобретение относится к области аналитической химии и касается способа количественного определения стеринов в корневищах с корнями крапивы двудомной. Сущность способа заключается в том, что извлекают стерины из корневищ с корнями крапивы 70% этиловым спиртом и рассчитывают количественное содержание стеринов по оптической плотности в концентрированной серной кислоте при максимуме поглощения 328 нм в пересчете на эргостерин, и абсолютно сухое сырье в процентах (X) вычисляют по формуле
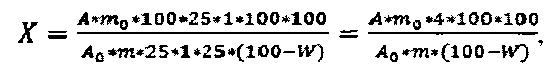
где A - оптическая плотность испытуемого раствора;
Aо - оптическая плотность раствора стандартного образца;
M - точная навеска сырья, г;
mo - точная навеска эргостерина, г;
W - влажность сырья, %.
В случае отсутствия рабочего стандартного образца эргостерина используют значение удельного показателя поглощения его раствора - 800; расчет содержания стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
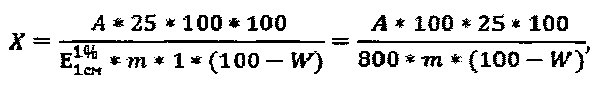
где A - оптическая плотность испытуемого раствора;
m - точная навеска анализируемого образца, г;
W - влажность сырья, %.
800 - удельный показатель поглощения эргостерина.
Использование способа позволяет с высокой точностью определять стерины в корневищах крапивы двудомной. 2 ил., 2 пр.
Способ количественного определения стеринов в корневищах с корнями крапивы двудомной с помощью спектрофотометрии, отличающийся тем, что экстракцию из корневищ с корнями крапивы двудомной осуществляют 70% спиртом этиловым, пробоподготовку проводят без стадии выпаривания и расчет количественного содержания стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
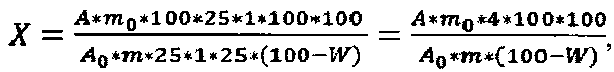
где А - оптическая плотность испытуемого раствора;
Аo - оптическая плотность раствора стандартного образца;
m - точная навеска сырья, г;
mo - точная навеска эргостерина, г;
W - влажность сырья, %,
в случае отсутствия рабочего стандартного образца эргостерина используют значение удельного показателя поглощения его раствора - 800; расчет содержания стеринов в пересчете на эргостерин и абсолютно сухое сырье в процентах (X) вычисляют по формуле
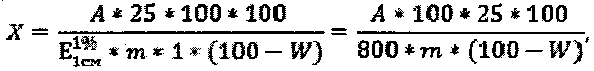
где А - оптическая плотность испытуемого раствора;
m - точная навеска анализируемого образца, г;
W - влажность сырья, %.
800 - удельный показатель поглощения эргостерина.
| Руководство по методам контроля качества и безопасности биологически активных добавок к пище | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ определения концентрации стерина | 1982 |
|
SU1070119A1 |
| ЛЕОНОВА М.В | |||
| и КЛИМОЧКИН Ю.Н | |||
| Экстракционные методы изготовления лекарственных средств из растительного сырья | |||
| Учебно-методическое пособие // Самара, 2012, СГТУ, | |||
Авторы
Даты
2016-10-10—Публикация
2015-08-26—Подача