Изобретение относится к медицине, так как может быть использовано для лечения рака кожи. Композиция представляет собой гель, содержащий ниосомальный доксорубицин, стабильный при длительном хранении. Гель способен трансдермально проникать в организм, создавая депо противоопухолевого препарата, и доставлять в ткань опухоли терапевтическую дозу доксорубицина без резких скачков концентрации, снижая таким образом нейро- и кардиотоксическое действие по сравнению со свободным доксорубицином за счет пролонгированного действия, обусловленного инкапсулированием в ниосомы кремнийорганической природы. Гель обеспечивает создание такой ниосомальной формы доксорубицина, которая увеличивает время циркуляции препарата в кровяном русле в несколько раз.
Доксорубицин представляет собой хорошо известный противоопухолевый антибиотик антрациклинового ряда, химическое его название (8S-цис)-10-(3-амино-2,3,6-тридезокси-альфа-L-ликсогексопиранозил)окси-7,8,9,10-тетра-гидро-6,8,11-тригидрокси-8-(гидроксилацетил)-1-метокси-5,12-афтацендион, брутто-формула C27H29NO1. Молекула доксорубицина состоит из тетрациклического антрахиноидногоагликона доксорубицинона, соединенного гликозидной связью с аминосахаром даунозамином. Доксорубицин уже более 30 лет используется при лечении как гематологических онкологических заболеваний, так и солидных опухолей различной локализации. Доксорубицин применяется только в виде растворов для внутривенного и внутрипузырного введения. В печени он метаболизируется с образованием активного метаболита доксорубицинола. Период полувыведения доксорубицина 20-48 часов, при этом 40% его выводится с желчью в неизмененном виде в течение 7 дней, с мочой в течение 5 дней выводится 5-12% доксорубицина и его метаболитов.
Ограничением для терапевтического использования доксорубицина является его токсичность по отношению к здоровым тканям, в первую очередь кардиотоксичность, проявляющаяся в выраженной сердечной недостаточности. Эффективным способом ее снижения считается использование доксорубицина не в свободной форме, а в составе лекарственных композиций: доксорубицин и переносчик (транспортная система), влияющих на биораспределение лекарства в организме и, в частности, снижающих возможность его поступления в сердце. В связи с этим в последние годы именно доксорубицину посвящено большое количество исследований и разработок новых лекарственных средств.
Широкое применение на сегодняшнее время находят такие формы доксорубицина, которые обеспечивают сохранение или увеличение терапевтического противоопухолевого действия при снижении побочных эффектов. Наиболее распространенные системы доставки - липосомальные формы, основанные на фосфолипидах. Преимущества липосомальной формы в настоящее время хорошо известны и связаны в первую очередь с улучшенной фармакокинетикой и снижением побочных эффектов. Для доксорубицина такая форма оказывается весьма продуктивной, так как инкапсулированное в липосомы лекарство практически не попадает в здоровые ткани, проникая лишь через дефектные капилляры опухолей, а амфифильная фосфолипидная мембрана липосом, взаимодействуя с мембраной клетки, может способствовать взаимодействию лекарства с клеткой-мишенью, повышая тем самым его действие.
Известно несколько липосомальных форм доксорубицина со средним диаметром от 40 до 200 нм, которые представляют собой новые группы препаратов. Патент РФ №2359700 предполагает использовать липосомы, стабилизированые полиэтиленгликолем, однако в этой заявке не учитывается возможное взаимодействие липосом с макрофагами организма. В патенте РФ на полезную модель №42953 предлагается использовать липосомальный доксорубицин, однако инъекционная форма использования существенно снижает спектр применения препарата в ряде случаев, например при раке кожи.
Наиболее близким к заявляемому изобретению является липосомальный препарат доксорубицина, который авторами патента РФ №2411935 предлагается использовать при включении доксорубицина в состав фосфолипидных наночастиц (НФ-доксорубицин), что снижает процент лекарства, связанного с форменными элементами крови. Это повышает относительную долю свободного лекарства, которое может оказывать терапевтическое действие. Оптимизированная пропись позволяет выгодно использовать низкие дозы препарата для достижения терапевтического действия. Однако использование лиофилизации и криопротекторов существенно повышает стоимость препарата. Кроме того, избыток фосфолипидов может запустить механизм интенсивного деления клеток и повлиять на цитотоксичность доксорубицина.
Таким образом, каждая из имеющихся на рынке липосомальных форм доксорубицина обладает определенными недостатками: низкая стабильность, высокая себестоимость или дополнительные побочные действия. Однако недостатком выше приведенной липосомальной нанокапсулы - прототипа является также быстрое выведение липосом из крови, которое связано с поглощением их ретикуло-эндотелиальной системой (РЭС) печени и селезенки, чему способствует их относительно большой размер - выше 150 нм, в сочетании с незащищенной поверхностью.
Целью предлагаемого изобретения является создание такой формы доксорубицина, которая увеличивала бы время ее циркуляции в кровяном русле в несколько раз. С учетом того, что в зоне пораженной опухолью ткани кожи имеют быть место ишемические процессы, особенно необходима трансдермальная пролонгированная доставка лекарственного препарата. Эта задача решается за счет инкапсулирования доксорубицина в кремнийорганические нановезикулы - ниосомы, имеющие размер до 100 нанометров. По отношению к прототипу, заявляемое изобретение отличает то, что в отличие от липосом, ниосомы обладают рядом преимуществ. В частности, ниосомы кремнийорганической природы, являясь неионогенным поверхностно-активным веществом, обладают большей проникающей способностью, чем липосомы. Они структурно сходны с липосомами в наличии бислоя, однако кремнийорганические компоненты, используемые для приготовления ниосом, сделали их более стабильными. Молекулы ниосом, как правило, ориентируются таким образом, что гидрофильные концы неионогенного поверхностно-активного вещества направлены наружу, а гидрофобные концы обращены друг к другу, чтобы сформировать бислой. Ниосомы являются осмотически активными, их химическая стабильность обусловила более длительный срок хранения по сравнению с липосомами. Они могут повысить терапевтическую эффективность молекул лекарственного вещества, защищая препарат от клеток ретикуло-эндотелиальной системы, так как их размер менее 100 нанометров делает их невидимыми для этих клеток. Это улучшает доступность ниосом к клеткам-мишеням и возможность контролируемой доставки лекарственных средств. Таким образом, их главное достоинство, как целевых носителей, заключается в длительной циркуляции в кровотоке, и как следствие - пролонгированной доставке доксорубицина.
Сущность изобретения
Конструирование предлагаемого лекарственного геля заключается в иммобилизации противоопухолевого препарата доксорубицина в кремнийорганические ниосомы, обладающие доказанной высокой трансдермальной проникающей способностью. Данная рецептура позволяет плавно наращивать терапевтическую дозу и повысить эффективность препарата за счет депонирования препарата и невозможности связываться с форменными элементами крови. Встраивание доксорубицина в кремнийорганические ниосомы, обладающие значительной липофильностью, позволяет ему не попадать в здоровые ткани, проникая лишь через дефектные капилляры опухоли кожи и повышая тем самым его действие. Трансдермальный путь введения доксорубицина позволяет снизить кардиотоксический эффект препарата, диспепсические реакции, уменьшить вероятность некрозов в местах введения, что существенно расширяет использование препарата среди пациентов, страдающих сердечной недостаточностью и заболеваниями желудочно-кишечного тракта.
Предлагаемое противоопухолевое средство представляет собой стабильный, однородный гель красного цвета со слабым специфическим запахом для наружного применения.
Осуществление изобретения
В качестве поверхностно активного соединения для формирования ниосом использовали ПЭГ-12 диметикон. Предварительно точную навеску 500 мг доксорубицина, из расчета 0,5 мг в 1 мл фармацевтического геля, растворяли при перемешивании в воде для инъекций. В полученный раствор для формирования ниосом поэтапно добавляли 100 мл ПЭГ-12 диметикона и 400 мл воды. Начальный процесс образования ниосом и инкапсулирования в них доксорубицина проводили при комнатной температуре и интенсивном механическом встряхивании на шейкере в течение 5 минут. Стадия формирования ниосом более мелких размеров происходила при интенсивном механическом перемешивании смеси с использованием АПВ гомогенизатора. Формирование ниосом с размерами 100-140 нм проводили следующим образом. Предварительно полученную дисперсию ниосом с инкапсулированным лекарственным веществом помещали в сосуд для ультразвуковой обработки. Режим озвучивания: частота - 20 кГц, мощность - 200 Вт. Для экспозиции использовали временные интервалы в 15, 30 и 45 минут. В результате повышалась эффективность включения доксорубицина в ниосомы. Для того, чтобы физико-химические характеристики ниосом были постоянными, использовали 50 мл гелеобразователя Covacryl MV 60 в жидком виде, который образовывал трехмерную объемную «сетку», при добавлении 20 мл триэтаноламина. Общий объем геля доводили до 1000 мл очищенной водой.
Состав геля:
Для оценки пролонгированности и устойчивости терапевтического действия полученного фармацевтического геля с ниосомальным доксорубицином изучали концентрацию лекарственного препарата в крови методом обращенно-фазовой высокоэффективной хроматографией с флуориметрической детекцией (ОФ-ВЭЖХ) на экспериментальных животных.
Условия ОФ-ВЭЖХ: система жидкостной хроматографии UltiMate - 3000 (Dionex, США), колонка ReproSil Pur C18 - AQ, 250×4,6 мм, 5 мкм; предколонка Teknokroma Novafix С18, 1×0,4 см; подвижная фаза (ПФ): ПФ 1 - ацетонитрил, ПФ 2 - 0,06 М раствор натрия гидрофосфата (Na2HPO4) с триэтиламином (0,05% по объему), доведенный до рН 4,6 0,03 М раствором кислоты лимонной. Скорость ПФ 0,50 мл/мин. Проводили хроматографию в изократическом режиме при соотношении подвижных фаз 35:65 (ПФ 1 : ПФ 2) в течение 10 минут. Объем вводимой пробы 25 мкл. Температура термостата колонки 35°С; детекция - флуоресцентный детектор (UltiMate 3000 Series, экс. 254 нм, эм. 560 нм, чувствительность 1). Для вычисления времени удерживания, площадей хроматографических пиков при детектировании и графического представления хроматограмм использовали программу «Chromeleon» (Dionex, США). Линеаризацию кривой проводили с помощью программы «Microsoft Excel» (Microsoft Corporation).
Идентификацию компонентов на хроматограммах исследуемых образцов осуществляли путем сравнения со временем удерживания стандарта доксорубицина. Для определения концентрации использовали калибровочную кривую зависимости площади пика от количества не менее 3 соответствующих стандартных образцов субстанции в диапазоне 50-500 нг/мл. Осуществляли не менее пяти измерений для каждого раствора. Время удерживания анализируемого пика доксорубицина 6,30±0,10 мин.
В эксперименте ниосомальный гель с доксорубицином наносился на кожу животных в концентрации, согласно общепринятой схеме лечения для пациентов по 10-20 мг/м2. Через стандартные промежутки времени (6 часов, 12 часов, 24 часов и 48 часов) у кроликов забирали венозную кровь (из ушной вены) в количестве 0,3 мл. В ходе центрифугирования получали плазму, которая использовалась для определения концентрации в ней доксорубицина методом ВЭЖХ. В качестве контроля исследовали плазму крови животных, получавших свободный доксорубицин.
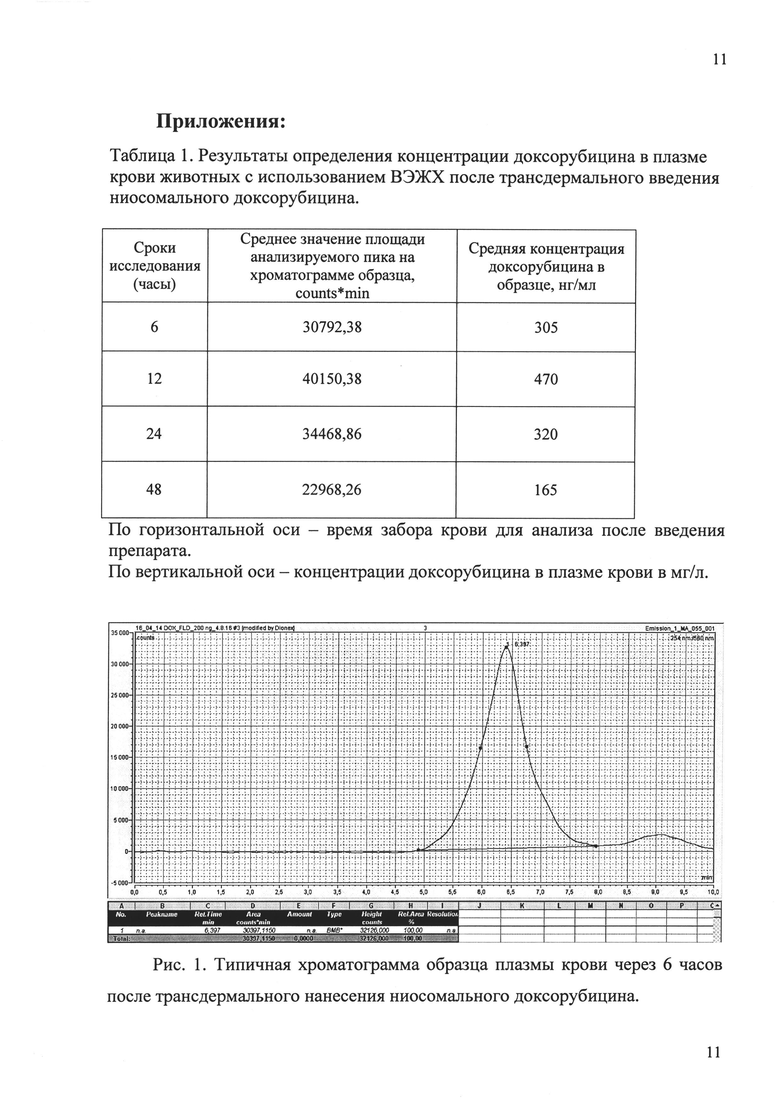
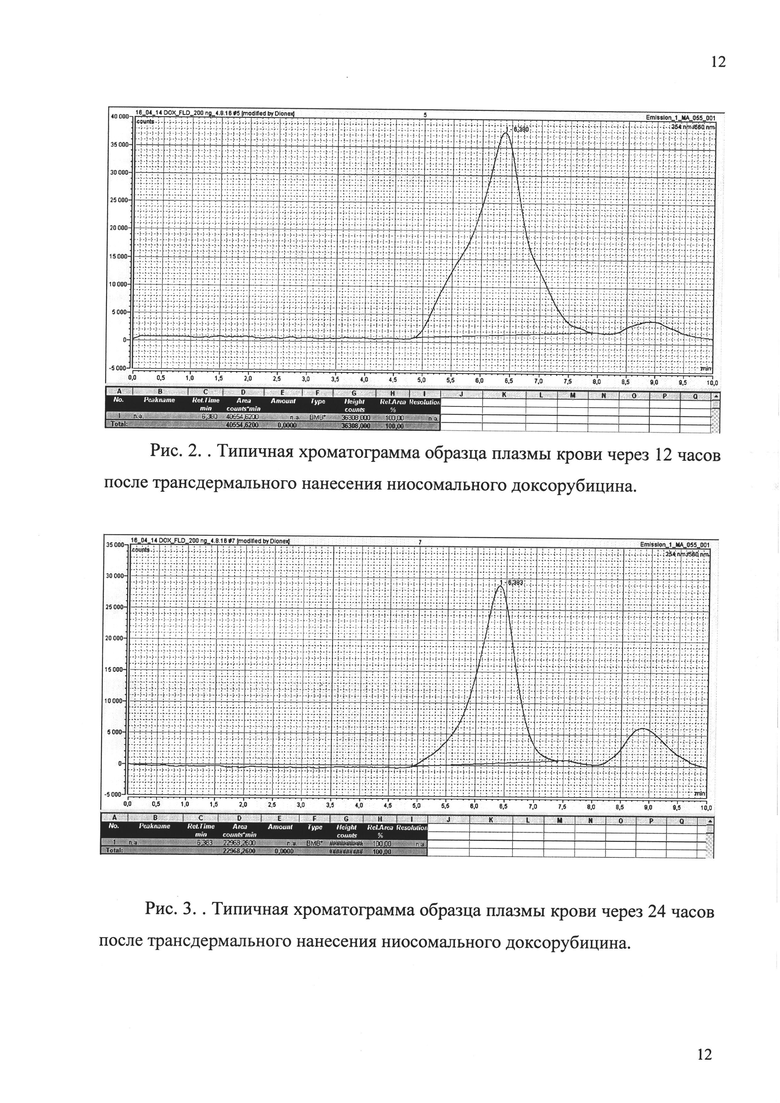
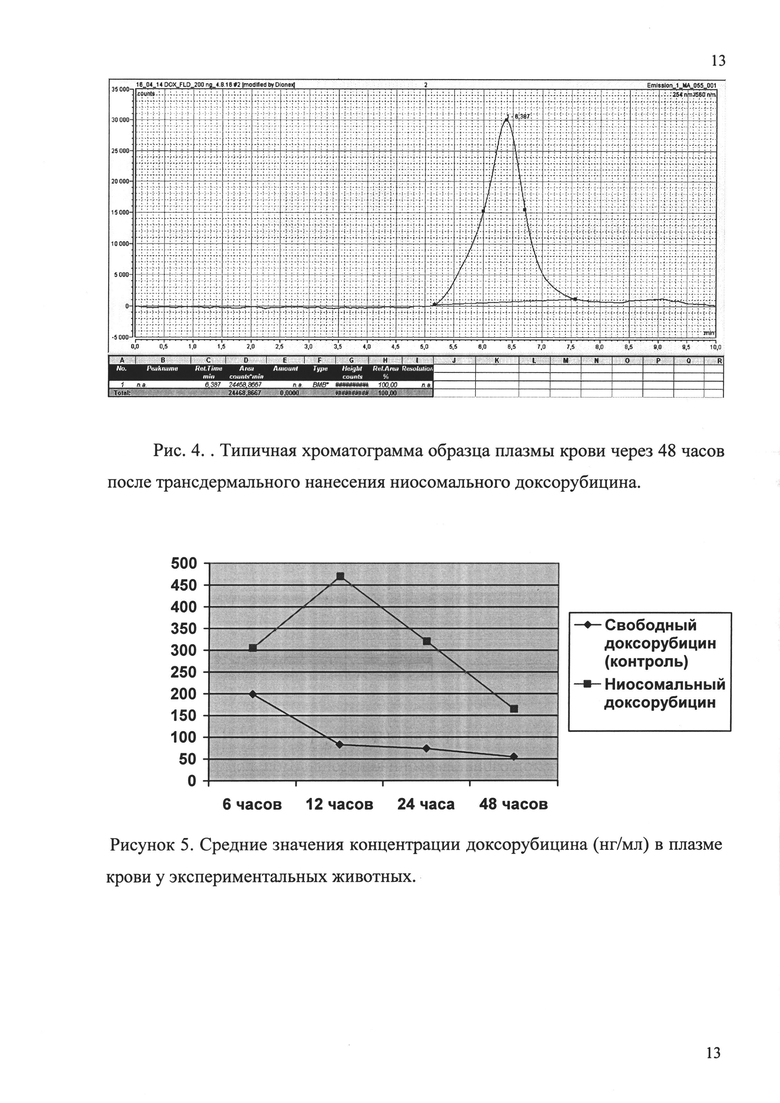
Типичные хроматограммы исследуемых образцов представлены в приложении на рисунках 1-4. Результаты сравнительного определения концентрации ниосомального и свободного доксорубицина в образцах сыворотки с использованием ВЭЖХ представлены на рисунке 5.
Установлено (табл. 1, в Приложении), что ниосомы обеспечили большую биологическую доступность доксорубицина и заметно пролонгировали время сохранения его концентрации в крови. По сравнению с контрольной группой, концентрация препарата в крови при трансдермальной доставке ниосомальной формы доксорубицина была максимальной через 12 часов. Именно ниосомы обеспечили большую биологическую доступность антибиотика и заметно пролонгировали время сохранения концентрации антибиотика в крови. Даже через 48 часов концентрация препарата в крови после введения в ниосомальной форме превышала значения свободной формы доксорубицина в три раза.
Эксперимент показал высокую эффективность ниосомальной формы доксорубицина. Как свидетельствуют экспериментальные данные, ниосомальная форма доксорубицина при трансдермальном использовании обладала плавным повышением терапевтической дозы наряду с длительным постоянным содержанием препарата в крови, необходимым для устойчивого терапевтического действия. Это послужило основанием для рекомендации способа применения ниосомального противоопухолевого геля трансдермально по 1-3 мл 1 раз в неделю или чаще согласно общепринятой схеме лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЙ НИОСОМАЛЬНЫЙ ГЕЛЬ НА ОСНОВЕ ВЕЩЕСТВА N-гидрокси-2-(2-(нафтален-2-ил)-1H-индол-3-ил)-2-фенилацетамид С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ К ГЛИОБЛАСТОМЕ | 2015 |
|
RU2627449C2 |
| ТРАНСДЕРМАЛЬНОЕ АНТИГЕЛЬМИНТНОЕ СРЕДСТВО НА ОСНОВЕ КРЕМНИЙОРГАНИЧЕСКИХ НИОСОМ С АЛЬБЕНДАЗОЛОМ | 2013 |
|
RU2541156C1 |
| СПОСОБ ТРАНСДЕРМАЛЬНОГО ПЕРЕНОСА АКТИВНЫХ СУБСТАНЦИЙ С ИСПОЛЬЗОВАНИЕМ НИОСОМ НА ОСНОВЕ ПЭГ-12 ДИМЕТИКОНА | 2012 |
|
RU2539396C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТРАНСДЕРМАЛЬНОГО ПЛАСТЫРЯ, СОДЕРЖАЩЕГО НИОСОМЫ НА ОСНОВЕ ПЭГ-12 ДИМЕТИКОНА | 2012 |
|
RU2539397C2 |
| НИОСОМАЛЬНЫЙ АНТИМИКРОБНЫЙ ГЕЛЬ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТИЧЕСКИХ ЯЗВ, РАН, ОЖОГОВ, В ТОМ ЧИСЛЕ ИНФИЦИРОВАННЫХ АНТИБИОТИКО-РЕЗИСТЕНТНЫМИ МИКРООРГАНИЗМАМИ | 2021 |
|
RU2781402C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИОСОМАЛЬНОЙ ФОРМЫ ОФЛОКСАЦИНА | 2014 |
|
RU2583135C1 |
| СТОМАТОЛОГИЧЕСКИЙ ГЕЛЬ С НИОСОМАМИ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ И ДИСТРОФИЧЕСКИХ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2013 |
|
RU2582290C2 |
| АНТИМИКРОБНЫЙ ГЕЛЬ ДЛЯ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ РАН, ОЖОГОВ И ТРОФИЧЕСКИХ ЯЗВ | 2017 |
|
RU2655522C1 |
| ЛИПОСОМНЫЕ КОМПОЗИЦИИ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2005 |
|
RU2574926C2 |
| КРЕМНИЙОРГАНИЧЕСКИЕ НИОСОМЫ С БАКТЕРИЦИДНЫМИ И ПАРАМАГНИТНЫМИ СВОЙСТВАМИ | 2016 |
|
RU2625722C1 |
Изобретение относится к медицине и представляет собой фармацевтический противоопухолевый гель, содержащий 0,5 г доксорубицина, 100 мл ПЭГ 12 диметикона, 50 мл гелеобразователя, 20 мл триэтаноламина и воду очищенную до 1000,0 мл. Гель содержит доксорубицин, инкапсулированный в ниосомы, сформированные с помощью ПЭГ 12 диметикона. Технический результат заключается в повышении эффективности доксорубицина и снижении его кардиотоксичности за счет инкапсулирования в ниосомы. 1 табл., 5 ил.
Фармацевтический противоопухолевый гель, содержащий:
характеризующийся тем, что содержит доксорубицин, инкапсулированный в ниосомы, сформированные с помощью ПЭГ 12 диметикона.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ДОКСОРУБИЦИНА И ФОСФОЛИПИДНЫХ НАНОЧАСТИЦ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2411935C1 |
| UCHEGBU IF et al., Distribution, metabolism and tumoricidal activity of doxorubicin administered in sorbitan monostearate (Span 60) niosomes in the mouse, Pharm Res | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| UCHEGBU IF et al., Drug distribution and a pulmonary adverse effect of | |||
Авторы
Даты
2016-10-20—Публикация
2014-11-17—Подача