Изобретение относится к медицине, так как может быть использовано для доставки лекарственных средств к очагам поражения. Развитие биомедицинской науки и биотехнологий привело к созданию новых методов доставки лекарственных веществ. В частности, используется инкапсулирование лекарственных веществ в наноконтейнеры с модификацией поверхности магнитными наночастицами. Существенное отличие новых типов лекарственных форм состоит в возможности реализации на их основе технологий адресной доставки лекарств к определенным тканям, клеткам и внутриклеточным органеллам.
Известна методика инкапсулирования серебра в биоинертные матрицы с целью снижения возможного токсичного воздействия магнитной фазы, повышения ее физико-химической устойчивости и создания серебросодержащих лекарственных препаратов [Shahverdy AR, Fakhimi A, Minaian S. (2007) Nanovedicine-Nanotechnology biology and medicine 3(2) 168-171]. Однако эти матрицы с расположенными внутри серебросодержащими частицами не имеют возможности адресно доставлять лекарственные вещества.
Наиболее близким по назначению и совокупности существенных признаков является патент по использованию ниосом кремнийорганической природы для трансдермальной доставки лекарственных веществ (Патент на изобретение RUS 2539397 от 22.10.2014). Однако в этих системах доставки не использованы антимикробные и парамагнитные свойства атомов серебра.
Целью предлагаемого изобретения является создание кремнийорганических ниосом с бактерицидными и парамагнитными свойствами для адресной доставки лекарств.
По отношению к прототипу заявляемое изобретение отличает то, что применяется адсорбции атомов серебра на поверхность ниосом, имеющих размер до 100 нанометров. По отношению к прототипу заявляемое изобретение отличает то, что в отличие от интактных ниосом серебряные ниосомы обладают рядом преимуществ. В частности, серебряные ниосомы обладают бактерицидным действием. Известно, что серебро является не только хорошим обеззараживающим средством, но и жизненно необходимым элементом. Этот микроэлемент необходим для нормального функционирования всех органов и систем. В малых дозах атомы серебра улучшают физиологические показатели крови и благотворно влияют на протекание биохимических процессов в организме. При этом отмечается стимуляция кроветворных органов, увеличивается число лимфоцитов, моноцитов, эритроцитов, гемоглобина, а также замедляется СОЕ. Высокая биологическая активность серебра в организме связана с участием в синтезе ферментов, витаминов и гормонов [1].
Сущность изобретения
Предлагается использовать ниосомы кремнийорганической природы размером 30-80 нанометров, на поверхность которых адсорбировали атомы серебра. Восстанавливали атомы серебра из раствора нитрата серебра химическим способом. Для этого использовали медную посуду или медные стержни. Адсорбцию восстановленного серебра на ниосомы проводили ультразвуковым воздействием. Это позволило повысить сорбционную активность восстановленного серебра на оксид кремния в составе поверхностного слоя ниосом. Серебрение ниосом придало им высокую бактерицидную активность, на что указывала величина зоны задержки при изучении их чувствительности к бактериям, выделенным с поверхности кожи. Помимо этого, серебрение ниосом придало им парамагнитные свойства для адресной доставки лекарственных средств.
Осуществление изобретения
Для серебрения ниосом использовали 0,14 мМ раствор AgNO3. Серебро восстанавливали в реакции по формуле 1. Для этого реакцию восстановления проводили в химически чистой медной посуде. После образования на стенках медной чашки белого налета остатки жидкости сливали и добавляли суспензию ниосом. Сорбция серебра на ниосомы проходила при ультразвуковой обработке реакционной смеси. Режим озвучивания: частота - 20 кГц, мощность - 200 Вт, экспозиция - 10-15 минут.
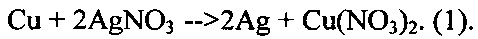
Содержание серебра в ниосомах определяли атомно-адсорбционным методом на атомно-адсорбционном спектрофотометре (AAS, тип-1N, Германия).
Сорбционная способность ниосом рассчитывалась по формуле 2:
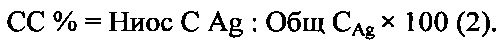
Где СС% - сорбционная способность ниосом, Ниос С Ag - концентрация серебра в ниосомах, Общ CAg - концентрация серебра, вносимого в реакционную смесь.
При использовании медной посуды в нейтральной среде (рН 7) в нашей реакции восстанавливается до 80% сорбированного ионного серебра до металла. Этот процесс длится 10-15 минут. Анализ сорбционной способности ниосом по формуле 2 показал, что около 80% участвовавшего в реакции серебра переходило в ниосомы. За счет этого мы можем визуализировать ниосомы при изучении их с помощью светового и электронного микроскопов (рис. 1).
Высокую сорбционную способность ниосом мы связываем с наличием функционально активных групп в молекуле диметикона. Ковалентные связи Si-O-Si в гидрофобной части молекулы полидиметилсилоксановой основы обладают большой эластичностью и реакционной способностью, что позволяет осаждать атомы серебра на поверхности ниосом. Ниосомы представляют собой гибрид кремния (диметикона) и углерода (полиэтиленгликоля). СН3 - (метальные) группы образуют «облако» вокруг атомов Si и создают условия для длительного взаимодействия Ag с ниосомами, что обеспечивает стабильность серебренных ниосом.
Длина связи Si-О длиннее связи С-С, поэтому молекулы ниосом эластичнее фосфолипидов, используемых при формировании липосом. В связи с этим, ниосомы образуются без значительных энергетических усилий. Высокая адсорбционная активность в отношении атомов серебра обеспечивается за счет длины и угла связи Si-OSi. Эта группа вращается и поэтому обладает большой эластичностью, что способствует взаимодействию серебра, находящегося на поверхности ниосом, с мембранами бактериальных клеток
Исследование бактерицидной активности посеребренных ниосом осуществляли дискодиффузионный методом (ДДМ) при изучении их чувствительности к бактериям, выделенным с поверхности кожи. Предварительно пропитывали бумажные диски посеребренными ниосомами. Затем их наносили на суспензию бактерий, выросших сплошным слоем на агаровой чашке Петри. При изучении антимикробной активности для большей достоверности получаемых результатов испытание с каждой культурой производили параллельно на трех чашках. Засеянные чашки оставляли при комнатной температуре на 1-2 часа, а затем на 16-18 часов помещали в термостат при 36±1°С вверх дном, чтобы избежать попадания конденсационной воды на поверхность посевов. Посеребренные ниосомы диффундировали в агар, формируя вокруг диска зону лизиса (угнетения роста) чувствительных к нему бактерий, четко выделяющуюся на фоне сплошного микробного роста. Величина зоны лизиса определяла степень чувствительности микроба к дискам, пропитанным посеребренными ниосомами. Измерение лизиса производили с помощью миллиметровой бумаги с точностью до 0,1 мм. Между степенью чувствительности микроба к дискам и размером диаметра зоны лизиса использовали следующие соотношения: менее 10 мм - слабая чувствительность; 10 мм - умеренная чувствительность; более 10 мм - высокая чувствительность.
Полученные цифровые величины диаметров зон задержки роста микроорганизмов обрабатывались общепринятыми статистическими методами: рассчитывали значения средней арифметической (X) и стандартного отклонения среднего (Sx). При оценке достоверности различий между сравниваемыми величинами применялся непараметрический критерий Манна-Уитни. Уровень достоверности различий принимался при Р≤0,05.
Серебрение ниосом придает им высокую бактерицидную активность, на что указывает величина зоны задержки (табл. 1, рис. 2). В нашем случае, зона задержки роста микроорганизмов ниосомами, содержащими 50 мкМ и 100 мкМ серебра, составила 16,9±0,5 и 17,1±0,2 мм соответственно, что свидетельствует о высокой бактерицидной активности посеребренных ниосом. Следует отметить, что бактерицидная активность серебра, адсорбированного на ниосомах, при снижении ее концентрации вдвое в нашем эксперименте практически не изменяется (табл. 1), что может в дальнейшем послужить для подбора оптимальной бактерицидной дозы и снижения побочных эффектов действия серебра на кожу и слизистые. Согласно литературным данным одним из механизмов бактерицидного действия серебра является его способность реагировать с клеточной мембраной бактерий, состоящей из особых бактериальных белков пептидогликанов - гетерополимеров N-ацетилглюкозамина и N-ацетил-мурамовой кислоты - обеспечивающих механическую прочность и структурно-функциональные свойства мембран бактерий и простейших. В этом процессе ионы серебра взаимодействуют с пептидогликанами, изменяя их структуру и способность транспортировать кислород О2 внутрь бактериальной клетки, что приводит к кислородному голоданию и последующей гибели микроорганизма [8].
Ранее нами было показано, что ниосомы способствуют пролонгированному эффекту применяемого лекарственного средства за счет постепенного высвобождения препарата, что позволяет длительно поддерживать высокую концентрацию лекарственных веществ в крови [5, 6].
На рис. 2 продемонстрирована пролонгированность действия посеребренных ниосом, связанная с электростатическим действием на клеточные стенки бактерий. Особенность задержки роста бактерий в виде двух зон соответствует литературным данным, согласно которым механизм действия серебра на бактериальную клетку приводит к потере ее жизнеспособности в результате взаимодействия электростатических сил, возникающих между обладающей отрицательным зарядом клеточной мембраной и положительно заряженными ионами серебра [8]. Модифицированная ниосома проявляет свою бактерицидную активность при взаимодействии серебра с функциональными группами Si-О-Si поверхностного слоя, приобретая частично положительный заряд, который приводит к антимикробному эффекту.
Литература
1. Вайнар А.И. (1960) Биологическая роль микроэлементов в организме животных и человека. М.: Наука, 236 с.
2. Shahverdy AR, Fakhimi A, Minaian S. (2007) Nanovedicine-Nanotechnology biology and medicine 3(2) 168-171.
3. Базиков И.А. Патент на изобретение RUS 2539396 от 29.08.2014.
4. Базиков И.А. Патент на изобретение RUS 2539397 от 22.10.2014.
5. Базиков И.А., Чекрыгина Е.В., Климанович И.В., Мальцев А.Н. (2015) Медицинский Вестник Северного Кавказа. Ставрополь, 10 (2) 163-166.
6. Базиков И.А., Омельянчук П.А., Хатков Э.М., Гукасян А.Л., Сеираниду З.А. (2012) Вестник Российской Академии Естественных наук, 1,81-83.
7. Базиков И.А., Климанович И.В., Пенькова Н.И., Магонов М.М., Авакова Т.А., Лысогора Л.В., Хатков Э.М., Сеираниду З.А., Гукасян А.Л., Деряженцева М.А., Калинкина Н.И., Базиков Ф.И. (2013) Медицинский вестник Северного Кавказа, 29 (3) 14-18.
8. Государственная фармакопея. (2007) XII (1) Научный центр экспертизы средств медицинского применения. М., 697 с.
9. Silvestry-Rodriguez N, Bright KR, Uhlmann DR, Gerba CP, (2007) Environmental Science and health 42(11) 67-84.
10. Rami Pedahzur, Ovadia Lev, Badri Fattal and Hillel I. Shuval (1995) Water Science and Technology, 31 (5) 123-129.
11. Благитко E.M., Бурмистров B.A., Колесников А.П., Михайлов Ю.И., Родионов П.П. (2004) Серебро в медицине, Наука-Центр, Новосибирск, 254 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИМИКРОБНЫЙ ГЕЛЬ ДЛЯ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ РАН, ОЖОГОВ И ТРОФИЧЕСКИХ ЯЗВ | 2017 |
|
RU2655522C1 |
| СЫВОРОТКА "РЕГЕНЕРИН" ДЛЯ НАРУЖНОГО ПРИМЕНЕНИЯ С ПРОТИВОВОСПАЛИТЕЛЬНЫМ И РЕГЕНЕРИРУЮЩИМ ЭФФЕКТОМ | 2011 |
|
RU2469704C1 |
| СТОМАТОЛОГИЧЕСКИЙ ГЕЛЬ С НИОСОМАМИ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ И ДИСТРОФИЧЕСКИХ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2013 |
|
RU2582290C2 |
| Препарат для лечения и профилактики субклинического мастита у коров | 2020 |
|
RU2739112C1 |
| НИОСОМАЛЬНЫЙ АНТИМИКРОБНЫЙ ГЕЛЬ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТИЧЕСКИХ ЯЗВ, РАН, ОЖОГОВ, В ТОМ ЧИСЛЕ ИНФИЦИРОВАННЫХ АНТИБИОТИКО-РЕЗИСТЕНТНЫМИ МИКРООРГАНИЗМАМИ | 2021 |
|
RU2781402C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ГЕЛЬ НА ОСНОВЕ ДОКСОРУБИЦИНА И КРЕМНИЙОРГАНИЧЕСКИХ НАНОЧАСТИЦ-НИОСОМ ДЛЯ ЛЕЧЕНИЯ РАКА КОЖИ | 2014 |
|
RU2600164C2 |
| Способ получения ниосомальной формы гентамицина | 2023 |
|
RU2805933C1 |
| СОЛНЦЕЗАЩИТНЫЙ ГЕЛЬ ДЛЯ ЛИЦА "SUN FIGHT" SPF 35 | 2007 |
|
RU2376981C2 |
| СПОСОБ ПОЛУЧЕНИЯ НИОСОМАЛЬНОЙ ФОРМЫ ОФЛОКСАЦИНА | 2014 |
|
RU2583135C1 |
| АНТИВИРУСНЫЙ ФИЛЬТРУЮЩИЙ МАТЕРИАЛ | 2010 |
|
RU2437707C1 |


Изобретение относится к медицине и предназначено для создания новых методов доставки лекарственных веществ к очагам поражения с помощью модифицированных ниосом с антимикробными и парамагнитными свойствами. Заявленные кремнийорганические ниосомы размером 30-80 нанометров модифицированы атомами серебра в концентрации 100 мкМ и могут использоваться для инкапсулирования лекарственных веществ. Адсорбция восстановленного химическим способом серебра на поверхность ниосом проводится ультразвуковым воздействием. Функциональная группа оксида кремния в составе поверхностного слоя ниосом является хорошим адсорбентом для серебра. Исследование посеребренных ниосом дискодиффузионным методом показало их антимикробную активность к бактериям, выделенным с поверхности кожи. Изобретение улучшает характеристики кремнийорганических ниосом, придавая им анимикробную активность и адресность доставки лекарственных веществ. 2 ил.
Ниосомы кремнийорганической природы, отличающиеся тем, что поверхностный слой содержат атомы восстановленного серебра в концентрации 100 мкМ для придания антимикробных и парамагнитных свойств.
Авторы
Даты
2017-07-18—Публикация
2016-01-19—Подача