Настоящее изобретение относится к новому режиму приема N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида формулы (I):

или его соли присоединения с фармацевтически приемлемой кислотой или основанием, отдельно или в сочетании с хирургическим вмешательством, химиотерапией, гормональной терапией или лучевой терапией, для лечения рака.
N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид является сильным ингибитором деацетилазы гистонов (HDAC), описанным в патентной заявке WO 2004/092115. Он обеспечивает ингибирование роста клеток и вызывает апоптоз в культивируемых клетках опухолей in vitro, и он ингибирует рост опухоли in vivo ксенотрансплантатах опухоли (Buggy et al., Mol. Cancer Ther 2006 5 (5) 1309). Его фармакологический профиль расценивается как главная терапевтическая ценность при лечении рака.
В настоящем изобретении было установлено, что N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид формулы (I) обладает весьма выгодным терапевтическим индексом при лечении рака, если его вводят в течение 4 дней подряд, за этим периодом следуют 3 дня подряд без всякого введения соединения формулы (I).
Более конкретно, было выявлено, что максимально переносимая доза N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида была существенно увеличена у пациентов, которые страдают от рака, если его вводили в течение 4 дней подряд, за этим периодом следуют 3 дня подряд без всякого применения соединения формулы (I). Этот цикл введения повторяют столько раз, сколько необходимо для лечения рака. Альтернативно, эти недельные циклы введения периодически могут быть прерваны неделей без всякого лечения.
Данный режим приема делает возможным предусмотреть более эффективное применение N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида в том отношении, что возможно свести к минимуму эффект токсичности тромбоцитов, присущий продукту, при этом обеспечивая достаточное воздействие для лечения рака.
Настоящее изобретение относится к N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамиду формулы (I):
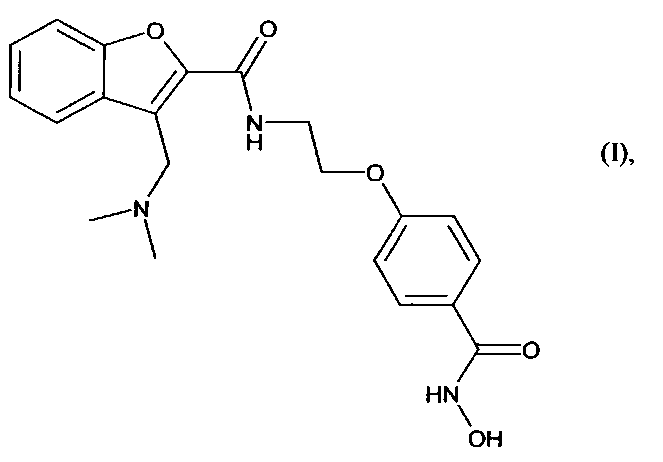
или его солям присоединения с фармацевтически приемлемой кислотой или основанием, отдельно или в сочетании с хирургическим вмешательством, химиотерапией, гормональной терапией или лучевой терапией, для применения в лечении рака, который отличается тем, что его вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без всякого применения соединения формулы (I), при условии, что химиотерапия не представляет собой FOLFOX (оксалиплатин/фолиновая кислота/5-фторурацил).
В контексте настоящего изобретения предпочтение отдается применению N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида в виде гидрохлорида.
N-Гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид преимущественно вводят в течение 4 дней подряд при норме в 2 приема в сутки, за которыми следует 3 дня подряд без всякого применения соединения формулы (I).
В некоторых вариантах осуществления рак, подлежащий лечению в соответствии с режимом приема согласно изобретению, может представлять собой карциному, опухоль, неоплазму, лимфому, меланому, глиому, саркому или бластому. Режим приема в соответствии с изобретением является в особенности пригодным при лечении солидных опухолей, и еще более предпочтительно при лечении рака молочной железы. Также в особенности он может быть направлен на эпителиальную карциному яичников, карциному фаллопиевой трубы и первичную перитонеальную карциному.
Предпочтительно N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид вводят в соответствии с режимом приема согласно изобретению в сочетании с химиотерапией, или гормональной терапией, или лучевой терапией.
В некоторых вариантах осуществления, N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид вводят в течение 4 дней подряд, тот период, за которым следуют 3 дня подряд без всякого другого введения этого соединения, в сочетании с химиотерапевтическим лечением, выбранным из доксорубицин, пегилированный липосомный доксорубицин, цисплатин, циклофосфамид, паклитаксел, карбоплатин, карбоплатин/паклитаксел, цисплатин/доксорубицин/циклофосфамид, пегилированный липосомный доксорубицин/цисплатин. Более предпочтительно ассоциированное химиотерапевтическое лечение представляет собой доксорубицин, пегилированный липосомный доксорубицин или цисплатин.
Альтернативным образом N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид вводят в течение 4 дней подряд, тот период, за которым следуют 3 дня подряд без всякого другого введения этого соединения, в сочетании с тамоксифеном в качестве гормональной терапии.
В предпочтительном варианте осуществления N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид вводят перорально.
Приемлемая дозировка варьируется в зависимости от пола, возраста и веса пациента, способа введения, природы рака и любых ассоциированных лечений и колеблется от 30 мг/м2 до 210 мг/м2 гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида в сутки. В общем приемлемая дозировка колеблется от 20 мг до 480 мг N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензо-фуран-2-илкарбониламино]этокси}бензамида, выраженного в качестве эквивалентного основания в сутки.
Клиническое исследование 1: (N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид в монотерапии)
Клиническое исследование осуществляли для того, чтобы проверить токсичность и эффективность гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида. В это исследование были вовлечены и подвергались лечению 36 пациентов с солидными опухолями. Первый режим приема проверяли в течение цикла из трех недель, включающих 14 дней подряд 2 пероральных применения с интервалом в 4 часа, за которым следовала неделя без лечения. Последовательно были протестированы четыре уровня дозировки от 30 до 75 мг/м2 (дозы выражены в виде соли гидрохлорида) два раза в день.
Переносимость различных уровней дозы N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида оценивали (в особенности, гематологические токсические эффекты) в конце первого цикла.
Результаты показали, что все токсические эффекты, которые ограничивали увеличение дозы, имели 4 степень тромбопении (уровень тромбоцитов в крови менее 25 гигалитр), которые были обратимыми после прекращения лечения N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамидом (см. фигуру 1). Максимальная переносимая доза согласно этому первому режиму приема была установлена в количестве 75 мг/м2 дважды в сутки.
Для того чтобы избежать существенных снижений числа тромбоцитов, наблюдаемых с помощью такого режима, протокол исследования был изменен, чтобы предложить новый режим приема: 4 дня подряд 2 пероральных приема с интервалом в 4 часа и затем 3 дня без лечения, этот режим применяют в течение каждых из 3 недель, соответствующих циклу приема. Этот цикл можно повторять столько раз, сколько необходимо для лечения рака. Данный новый режим показал меньшее токсическое воздействие на тромбоциты, чем предыдущий режим, и позволил лечить пациентов при более высоких уровнях доз (от 90 до 105 мг/м2 дважды в сутки). Путем сравнения фигура 2 показывает, что второй режим приема является в значительной степени менее вредным, чем первый относительно уровня тромбоцитов в крови в дозе 75 мг/м2 дважды в сутки.
При втором режиме приема рекомендованная доза и максимально переносимая доза были установлены в количестве 90 мг/м2 и 105 мг/м2 дважды в сутки соответственно.
Клиническое исследование 2: (N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид в комбинации с цисплатином)
Фазу I клинического исследования для тестирования сочетания гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида с цисплатином осуществляют на примерно сорока пациентах с различными солидными опухолями. Пациенты получают максимально шесть циклов лечения в сочетании, каждый из циклов протекает следующим образом: гидрохлорид N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без лечения, который осуществляют в течение первых двух недель цикла из трех недель. Цисплатин вводят на третий день каждого цикла лечения. В течение третьей недели цикла лечение не проводят.
В соответствующие дни суточная доза гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида составляет от 80 до 320 мг включительно (выражено в виде эквивалентного основания), содержащая два пероральных введения с интервалом в 4 часа. Цисплатин вводят в фиксированной дозе в 75 мг/м2.
В конце цикла лечения оценивают токсическое воздействие протокола, сочетающего гидрохлорид N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид и цисплатин. Если не наблюдается чрезмерной токсичности, то пациент продолжает лечение. Каждые два цикла эффективность лечения оценивают посредством определения ответа опухоли (сканирование КТ, МРТ, …). Также оценивается профиль приемлемости (в особенности, гематологические и сердечные эффекты токсичности). Пациенты продолжают комплексное лечение в течение максимально шести циклов.
Клиническое исследование 3: (N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид в комбинации с доксорубицином)
Фазу I клинического исследования для тестирования сочетания гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида с доксорубицином при лечении запущенных солидных опухолей осуществляют на примерно сорока пациентах. Пациенты получают максимально шесть циклов лечения с сочетанием, каждый из циклов протекает следующим образом: N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид гидрохлорид вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без лечения, который осуществляют в течение первых трех недель цикла из четырех недель. Доксорубицин вливают на третий день первых трех недель цикла. В течение четвертой недели цикла лечение не проводят.
В соответствующие дни суточная доза гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида составляет от 60 до 150 мг/м2 включительно (дозы выражены в виде соли гидрохлорида), содержит два пероральных введения с интервалом в 4 часа. Доксорубицин вводят в фиксированной дозе в 25 мг/м2.
В конце цикла лечения оценивают токсическое воздействие протокола, сочетающего гидрохлорид N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид и доксорубицин. Если не наблюдается чрезмерной токсичности, то пациент продолжает лечение. Каждые два цикла эффективность лечения оценивают посредством определения ответа опухоли (сканирование КТ, МРТ, …). Также оценивается профиль приемлемости (в особенности, гематологические и сердечные эффекты токсичности). Пациенты продолжают комплексное лечение в течение максимально шести циклов.
Клиническое исследование 4: (N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид в комбинации с пегилированным липосомным доксорубицином)
Фазу I клинического исследования для тестирования сочетания гидрохлорида N-гидрокси-4-{2-[3-{N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида с пегилированным липосомным доксорубицином при лечении первичной устойчивой к платине и частично чувствительной к платине эпителиальной карциномы яичников, карциномы фаллопиевой трубы или первичной перитонеальной карциномы осуществляют на примерно семидесяти пациентах. Пациентов подвергают циклам лечения из пяти недель в сочетании. Были протестированы две схемы:
- Схема 1: гидрохлорид N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без лечения, это осуществляют в течение первых трех недель цикла из четырех недель. Пегилированный липосомный доксорубицин вливают на третий день первой недели цикла. Во время четвертой недели цикла не проводят никакого лечения.
- Схема 2: N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид гидрохлорид вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без лечения в первую неделю цикла из четырех недель. Пегилированный липосомный доксорубицин вливают на третий день первой недели цикла. В течение трех последних недель цикла не проводят никакого лечения.
В соответствующие дни суточная доза гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида составляет от 60 до 150 мг/м2 включительно (дозы выражены в виде соли гидрохлорида), содержит два пероральных введения с интервалом в 4 часа. Пегилированный липосомный доксорубицин вводят в фиксированной дозе в 40 мг/м2.
В конце цикла лечения оценивают токсическое воздействие протокола, сочетающего гидрохлорид N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида и пегилированный липосомный доксорубицин. Если не наблюдается чрезмерной токсичности, то пациент продолжает лечение. Каждые два цикла эффективность лечения оценивают посредством определения ответа опухоли (сканирование КТ, МРТ, …). Также оценивается профиль приемлемости (в особенности, гематологические и сердечные эффекты токсичности).
Клиническое исследование 5: (N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид в комбинации с тамоксифеном)
Фазу I клинического исследования для тестирования сочетания гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида с тамоксифеном при лечении запущенного рака молочной железы осуществляют на примерно сорока пациентах. Пациентов подвергают циклам лечения в сочетании, каждый из циклов протекает следующим образом: гидрохлорид N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без лечения. Тамоксифен вводят ежедневно во время всей продолжительности лечения.
В соответствующие дни суточная доза гидрохлорида N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида составляет от 160 и 320 мг включительно (выражено в эквивалентном основании), содержит два пероральных введения с интервалом в 4 часа. Тамоксифен вводят ежедневно в фиксированной дозе в 20 мг.
В конце двух циклов лечения оценивают токсическое воздействие протокола, сочетающего гидрохлорид N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида и тамоксифен. Если не наблюдается чрезмерной токсичности, то пациент продолжает лечение. Каждые два цикла эффективность лечения оценивают посредством определения ответа опухоли (сканирование КТ, МРТ, …). Также оценивается профиль приемлемости (в особенности, гематологические и сердечные эффекты токсичности).
Указанные выше различные клинические исследования показывают, что режим приема, в котором N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамид вводят в течение 4 дней подряд, этот период сопровождается 3 днями подряд без всякого введения, позволяет свести к минимуму токсический эффект тромбоцитов, присущий продукту, и таким образом увеличить терапевтическую дозу для лечения рака.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННЫЕ ФОРМЫ ИНГИБИТОРА ГИСТОНДИАЦЕТИЛАЗЫ В КОМБИНАЦИИ С БЕНДАМУТИНОМ И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2609833C2 |
| СПОСОБЫ ПРИМЕНЕНИЯ (+)-1,4-ДИГИДРО-7-[(3S, 4S)-3-МЕТОКСИ-4-(МЕТИЛАМИНО)-1-ПИРРОЛИДИНИЛ]-4-ОКСО-1-(2-ТИАЗОЛИЛ)-1,8-НАФТИРИДИН-3-КАРБОНОВОЙ КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2006 |
|
RU2592231C2 |
| СПОСОБЫ ПРИМЕНЕНИЯ (+)-1,4-ДИГИДРО-7-[(3S,4S)-3-МЕТОКСИ-4-(МЕТИЛАМИНО)-1-ПИРРОЛИДИНИЛ]-4-ОКСО-1-(2-ТИАЗОЛИЛ)-1,8-НАФТИРИДИН-3-КАРБОНОВОЙ КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2006 |
|
RU2428983C2 |
| ТЕРАПЕВТИЧЕСКИЕ КОМБИНАЦИИ, СОДЕРЖАЩИЕ АНТИ-FOLR1 ИММУНОКОНЪЮГАТЫ | 2016 |
|
RU2749865C2 |
| СЕЛЕКТИВНЫЕ АНТАГОНИСТЫ РЕЦЕПТОРА EP4 ДЛЯ ЛЕЧЕНИЯ РАКА | 2010 |
|
RU2563817C2 |
| КОМБИНАЦИЯ И СПОСОБ ПРЕДУПРЕЖДЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2002 |
|
RU2322981C2 |
| ЛЕЧЕНИЕ РАКА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2018 |
|
RU2792690C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ И НАРУШЕНИЙ, СВЯЗАННЫХ С LSD1, ИНГИБИТОРАМИ LSD1 | 2020 |
|
RU2826217C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2801665C2 |
| СПОСОБ ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО РАКА АНАЛЬНОГО КАНАЛА | 2011 |
|
RU2459644C1 |


Изобретение относится к области медицины, а именно к онкологии, и предназначено для лечения рака. N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино] этокси}бензамид формулы (I):
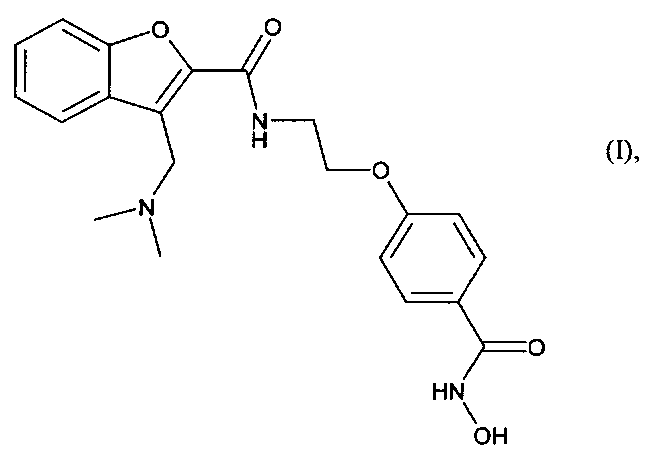
или его соль присоединения с фармацевтически приемлемой кислотой или основанием, отдельно или в сочетании с хирургическим вмешательством, химиотерапией, гормональной терапией или лучевой терапией вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без всякого применения указанного соединения, при этом химиотерапия не представляет собой FOLFOX. Использование изобретения позволяет повысить эффективность лечения рака у человека. 9 з.п. ф-лы, 2 ил.
1. Применение N-гидрокси-4-{2-[3-(N,N-диметиламинометил)бензофуран-2-илкарбониламино]этокси}бензамида формулы (I):
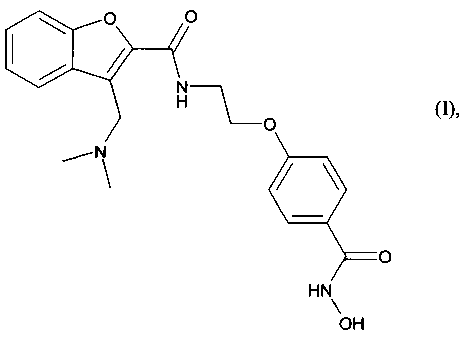
или его соли присоединения с фармацевтически приемлемой кислотой или основанием, отдельно или в сочетании с хирургическим вмешательством, химиотерапией, гормональной терапией или лучевой терапией, для лечения рака у человека, которое отличается тем, что соединение формулы (I) вводят в течение 4 дней подряд, за которыми следуют 3 дня подряд без всякого применения соединения формулы (I), при условии, что химиотерапия не представляет собой FOLFOX (оксалиплатин/фолиновая кислота/5-фторурацил).
2. Применение по п. 1, которое отличается тем, что соединение формулы (I) применяют в виде гидрохлорида.
3. Применение по п. 1 или 2, которое отличается тем, что соединение формулы (I) вводят в течение 4 дней подряд с нормой 2 приема в сутки, за которым следует 3 дня подряд без всякого введения соединения формулы (I).
4. Применение по п. 1 или 2, вводимое в сочетании с химиотерапией, или гормональной терапией или лучевой терапией.
5. Применение по п. 1 или 2 для лечения карциномы, опухолей, неоплазмы, лимфомы, меланомы, глиомы, саркомы или бластомы.
6. Применение по п. 1 или 2 для лечения солидных опухолей.
7. Применение по п. 1 или 2 для лечения рака молочной железы.
8. Применение по п. 1 или 2 для лечения эпителиальной карциномы яичников, карциномы фаллопиевой трубы или первичной перитонеальной карциномы.
9. Применение по п. 1 или 2, отличающееся тем, что химиотерапевтическое лечение представляет собой цисплатин, доксорубицин или пегилированный липосомный доксорубицин.
10. Применение по п. 1 или 2, отличающееся тем, что гормональная терапия представляет собой тамоксифен.
| WO 2004092115 A, 28.10.2004 | |||
| JOSEPH J | |||
| BUGGY et al | |||
| Устройство для введения уточной нити в ткацкий челнок | 1929 |
|
SU24781A1 |
| Molecular Cancer Therapeutics, 2006, vol | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| GONZALO LOPEZ et al | |||
| Устройство для введения уточной нити в ткацкий челнок | 1929 |
|
SU24781A1 |
Авторы
Даты
2016-10-27—Публикация
2012-09-07—Подача