Изобретение относится к медицине, в частности к офтальмологии, и может быть использовано для лечения эндотелиально-эпителиальной дистрофии (ЭЭД) роговицы и ранней буллезной кератопатии.
В настоящее время разработаны различные методы хирургического лечения ЭЭД роговицы и ранней буллезной кератопатии: сквозная кератопластика с замещением роговой оболочки аллотрансплантантом (Копаева В.Г. Субтотальная сквозная кератопластика при дистрофии роговой оболочки. Оптикореконструктивные операции и аллопластика в офтальмологии. М., 1974), послойная кератопластика с пересадкой задних слоев роговицы (Волков В.В. К разработке хирургического метода лечения энтотелиально-эпителиальной дистрофии роговицы. Первый съезд офтальмологов Закавказья: Тез. докл. Тбилиси: 1976), интерламеллярная пересадка задней капсулы хрусталика (авторское свидетельство СССР N810235, кл. A61F 9/007, 1981), послойная кератопластика с использованием желатиновой пленки (Дронов М.М., Каранов К.С., Бобырь А.Б. Способ лечения буллезной кератопатии. Патент России №2082364, приоритет от 27.06.1997).
Однако перечисленные способы имеют ряд существенных недостатков: техническая сложность операции, высокая частота развития осложнений, вероятность иммунного конфликта с последующим отторжением донорского материала, рецидив заболевания.
Все вышеизложенное послужило основанием для создания нового способа хирургического лечения ЭЭД роговицы и ранней буллезной кератопатии путем внутрикамерного введения аутологичных мононуклеаров крови.
Наиболее близким к предлагаемому является способ лечения отека роговицы и других проявлений ранней буллезной кератопатии путем проведения интракамеральной локальной экспресс-аутоцитокинотерапии (ЛЭАЦКТ) (Каспаров А.А., Каспарова Е.А., Павлюк А.С. Патент России №2357743, приоритет от 13.10.2009).
Согласно этому способу, в переднюю камеру больного глаза вводят активированные полуданом аутологичные мононуклеарные клетки крови пациента. Забор крови у пациента производят с соблюдением правил асептики и антисептики в условиях процедурного кабинета. Кровь берут из локтевой вены пациента в количестве 5,0 мл. Содержимое 2 флаконов полудана растворяют в 2,0 мл раствора воды для инъекций, и водный раствор полудана переносят в стерильную пробирку с 5,0 мл крови. Содержимое пробирки тщательно перемешивают путем переворачивания. Далее пробирку помещают в термостат на 2-4 часа. После окончания инкубирования пробирку со свернувшейся кровью центрифугируют в течение 5-10 минут при 500-1000 об/мин. Далее на границе сыворотки и сгустка свернувшейся крови пипеткой собирают клеточную взвесь. В условиях операционной после обработки операционного поля и ретробульбарной анестезии больного глаза пациента вблизи лимба лезвием производят парацентез роговицы. В переднюю камеру постепенно осуществляют инфузию суспензии аутологичных мононуклеаров крови в количестве 1,0-2,0 мл вплоть до полного замещения ею влаги передней камеры. В зоне парацентеза роговицы накладывают супрамидный шов. Сразу после операции больной должен принять положение лицом вниз и лежать в течение 1 часа, чтобы введенные клетки контактировали с эндотелием роговицы. Сеансы ЛЭАЦКТ проводят с интервалом 3-6 дней в количестве от 1 до 4 раз.
Недостатками этого метода являются: длительность и трудоемкость получения аутологичных мононуклеаров крови, активированных с помощью полудана, необходимость повторения клеточной терапии с интервалом 3-7 дней в количестве до 4 раз.
Новый технический результат - сокращение сроков лечения и осложнений, связанных с излишней травматизацией тканей глаза, отеком роговицы.
Для достижения нового технического результата в способе лечения эндотелиально-эпителиальной дистрофии роговицы, включающем введение взвеси аутологичных мононуклеаров крови во внутреннюю камеру глаза через парацентез, выполненный вблизи лимба до полного замещения ею влаги передней камеры, отличающийся тем, что выполняют два парацентеза размером 1,2 мм, на 7 и 11 часах, в один из которых устанавливают ирригационную систему в виде канюли для подачи стерильного воздуха в переднюю камеру под давлением до 0,2 атм, при этом через второй парацентез с помощью шприца в переднюю камеру на границе между внутренней поверхностью роговицы и пузырем воздуха однократно вводят 96-98% клеточную суспензию аутологичных мононуклеаров крови, выделенную методом фракционирования в градиенте плотности на разделяющем растворе фиколл-верографина, после чего ирригационную систему удаляют, края парацентезов гидратируют.
Благодаря подобному способу применения аутологичных мононуклеаров крови значительно уменьшается отек ткани роговицы, что способствует восстановлению ее прозрачности и улучшению сниженных вследствие заболевания зрительных функций.
Способ осуществляют следующим образом.
Аутологичные мононуклеарные клетки из крови экспериментального животного выделяют методом фракционирования в градиенте плотности на разделяющем растворе фиколл-верографин. Кровь, взятую в количестве 4,0-5,0 мл, помещают в стерильную пробирку, содержащую 1,0 мл раствора гепарина. Гепаринизированную кровь разбавляют в 2 раза изотоническим раствором хлорида натрия. Полученную суспензию наслаивают на 3,0 мл смеси фиколла-верографина. Пробы центрифугируют при комнатной температуре в течение 15 мин при 800 g (2000 об/мин). После центрифугирования интерфазный слой, содержащий мононуклеарные клетки и располагающийся между плазмой и градиентом, забирают пастеровской пипеткой. Добавляют 1,0 мл изотонического раствора хлорида натрия, и полученную суспензию вновь центрифугируют в течение 7 мин при 400 g (1550 об/мин). Чистота мононуклеаров, полученных на градиенте фиколл-верографин, составляет до 96-98%. Жизнеспособность клеточного материала оценивают в тесте с трипановым синим следующим способом: предварительно на основе раствора Рингера готовят 0,1% раствор эозина. Далее на основе дистиллированной воды готовят 0,1% раствор трипанового синего. После этого к капле клеточной суспензии добавляют 1-2 капли свежей смеси растворов, приготовленных ранее красителей, взятых в равных объемах. Полученную смесь помещают в камеру Горяева. При подсчете клеток процент окрашенных (погибших) элементов должен составлять 1,5-2%, что не превышало бы допустимое (не более 3%) количество. Жизнеспособность клеточного материала в тесте с трипановым синим составляет 97-98%.
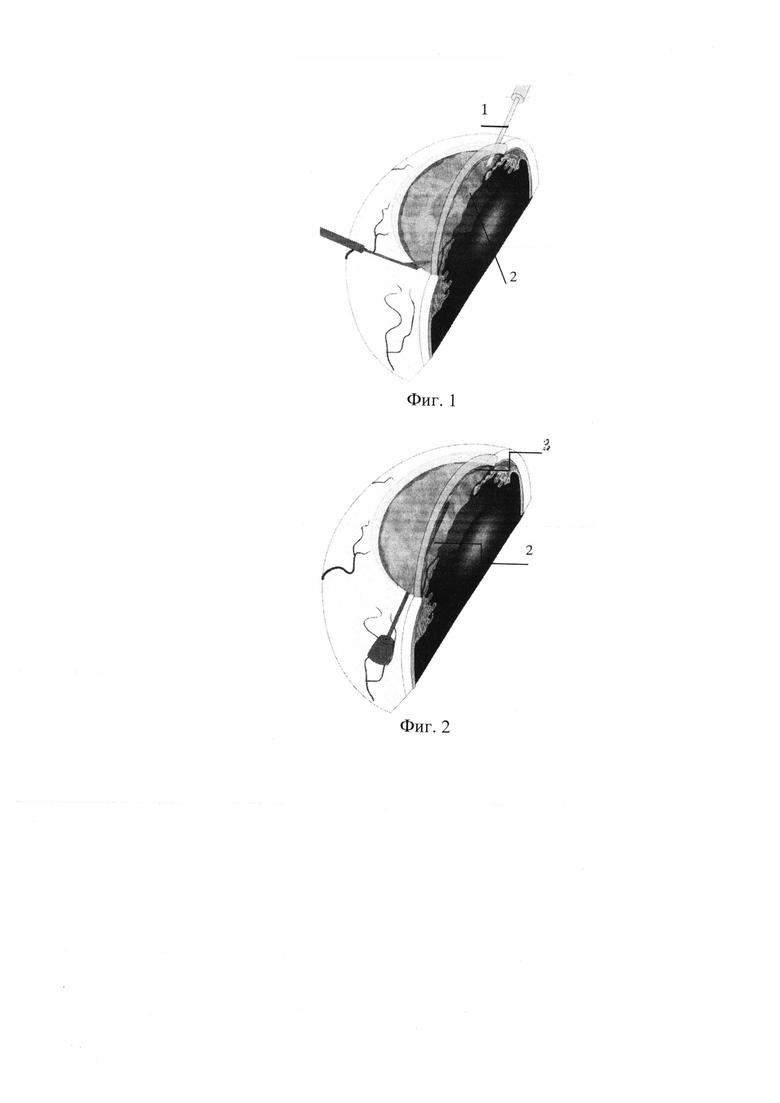
В условиях операционной после наркоза и обработки операционного поля с соблюдением правил асептики и антисептики, экспериментальным животным с предварительно моделированной ЭЭД, проводят оперативное вмешательство. В роговице выполняют два парацентеза размером 1,2 мм, на 7 и 11 часах, в один их которых устанавливают ирригационную систему в виде канюли с подачей стерильного воздуха с давлением до 0,2 атм в переднюю камеру (фиг. 1). С помощью шприца через второй парацентез в переднюю камеру на границе между внутренней поверхностью роговицы и пузырем воздуха на эндотелий наслаивают клеточную суспензию (фиг. 2). Ирригационную систему удаляют, края парацентезов гидратируют.
Способ апробирован на 16 крысах породы Wistar весом 200-250 г.
Обзор экспериментального материала: общая продолжительность эксперимента - 21 сутки. На I этапе каждому животному в условиях операционной предварительно моделировали ЭЭД путем механического повреждения и удаления эндотелия роговицы одного из глаз. На II этапе спустя 2 недели после развития патологического процесса в роговой оболочке осуществляли внутрикамеральное введение аутологичных мононуклеаров крови описанным способом.
В ходе эксперимента проводили наружный осмотр, фоторегистрацию, гистологическое исследование. Забор материала производили на 3, 7, 14, 21 сутки от начала эксперимента.
Для оценки морфологических изменений энуклеированные глаза фиксировали в 12% нейтральном формалине в течение 24 часов. Затем объекты, после 24-часового промывания в проточной воде, подвергали обезвоживанию в спиртах восходящей концентрации, просветляли в О-ксилоле и заливали в парафин. После приготовления срезов толщиной 4-6 мкм, препараты окрашивали гематоксилином и эозином, а также гематоксилином и пикрофуксином по Ван-Гизону.
В ходе морфологических исследований выявлено следующее.
Через 3 суток после внутрикамерного введения суспензии аутологичных мононуклеаров крови передний эпителий роговицы сохранен и представлен пластом многослойного плоского неороговевающего эпителия. Передняя пограничная мембрана четко не определялась.
Собственное вещество роговицы представлено рыхло расположенными коллагеновыми волокнами, которые местами имели повышенно извитой ход (фиг. 3). Задняя пограничная мембрана визуализировалась хорошо, однако окрашивалась неравномерно. Задний эндотелий отсутствовал (фиг. 4).
Через 7 суток после введения суспензии клеток передний эпителий роговицы сохранял обычное строение, передняя пограничная мембрана визуализировалась недостаточно четко.
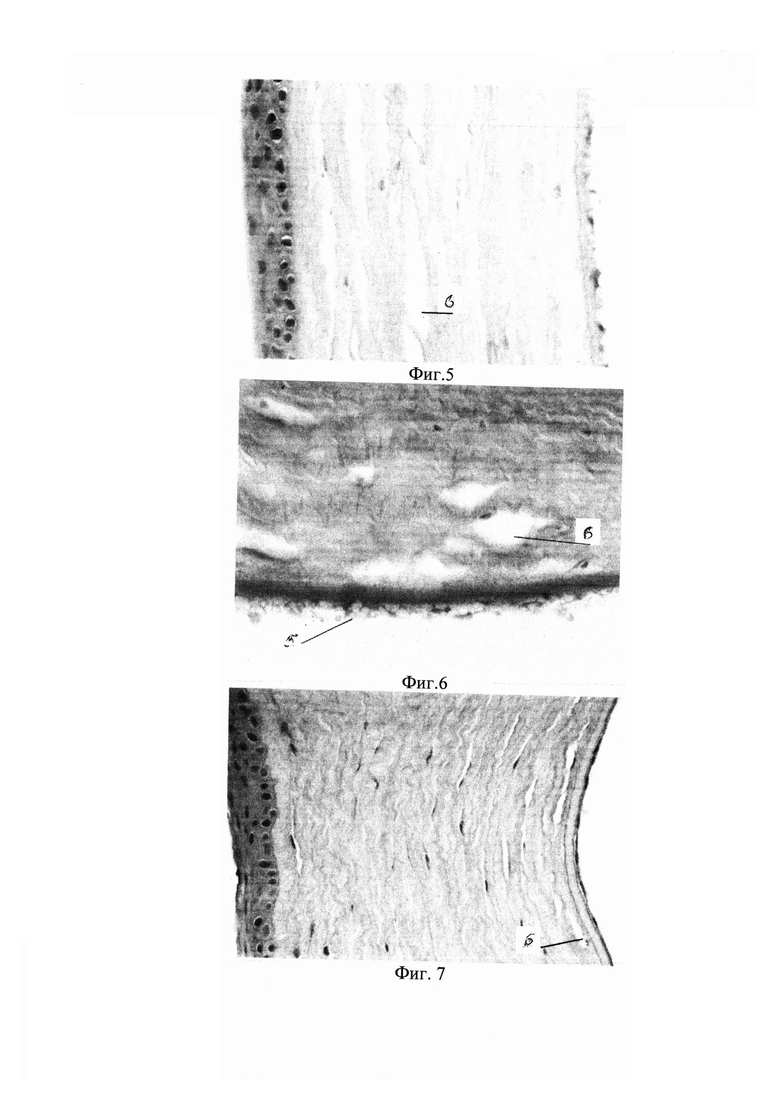
Собственное вещество роговицы характеризовалось выраженным отеком, наиболее распространенным в задней трети. Коллагеновые волокна собственного вещества имели повышенно извитой ход (фиг. 5).
Задняя пограничная мембрана гомогенна, границы ее четко не определялись. При окраске пикрофуксином мембрана характеризовалась незначительным нарушением тинкториальных свойств.
Со стороны эндотелия обнаруживалась выраженная пролиферация клеток отростчатой формы (фиг. 6).
Через 14 суток после введения популяции аутологичных мононуклеаров передний эпителий не изменен, количество слоев сохранено. Передняя пограничная мембрана четко не визуализировалась не вполне четко.
Собственное вещество роговицы имело компактное строение. Коллагеновые волокна в задней трети основного вещества, вблизи от места воздействия, незначительно раздвинуты отечной жидкостью (фиг. 7). При окраске пикрофуксином нарушений тинкториальных свойств не выявлено.
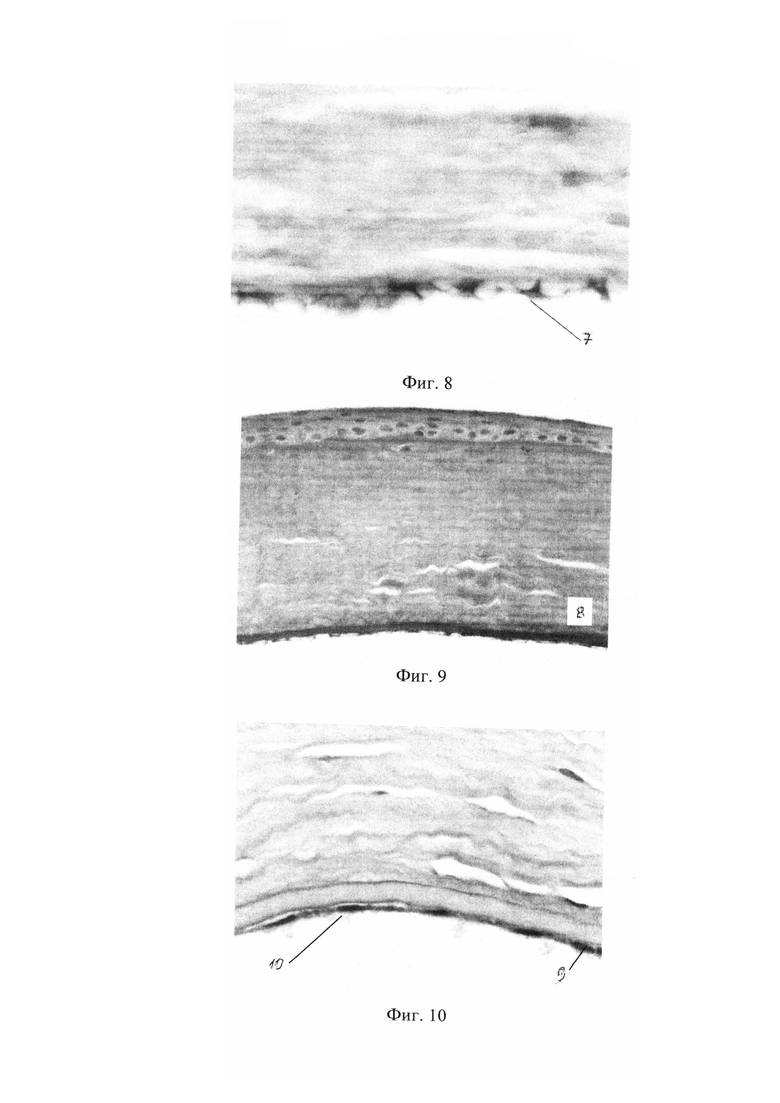
Задняя пограничная мембрана гомогенна, хорошо визуализировалась на всем протяжении. Эндотелий представлен одним слоем плоских отростчатых клеток (фиг. 8).
Через 21 сутки после интракамерального введения суспензии клеток передний передний эпителий роговицы сохранял обычное строение. Передняя пограничная мембрана четко не определялась.
Собственное вещество роговицы компактно, его тинкториальные свойства не нарушены (фиг. 9).
Задняя пограничная мембрана хорошо визуализирована, гомогенна. Эндотелий представлен одним слоем клеток (фиг. 10).
Современные представления о биологической роли мононуклеаров основываются на их функциональной гетерогенности, включающей фагоцитарные, регуляторные и эффекторные свойства (Земсков В.М., Николаева Е.Н., Родионов С.В. Гетерогенность мононуклеарных фагоцитов // Успехи совр. биологии. - 1993. - Т. 113, №3. - С. 336-349). Однако в последние годы, наряду с подробно изученными функциями миграции и хемотаксиса, эндоцитоза и внутриклеточного переваривания, большое внимание исследователей привлекает секреторная функция мононуклеарных фагоцитов. Учение И.И. Мечникова о макрофагальных ферментах - цитазах - переросло в концепцию о монокинах - продуктах секреции моноцитов/макрофагов, которые вместе с лимфокинами получили название «цитокины». Современная трактовка мононуклеаров как секретирующих клеток основывается на их способности продуцировать и выделять более 75 различных видов молекул (Фрейдлин И.С. Дефекты цитокиновой сети и принципы их коррекции // Иммунология. - 1998. - №6. - С. 23-25). Посредством цитокинов мононуклеары влияют на миграцию и пролиферацию гранулоцитов, эндотелиальных клеток, индуцируют хемотаксис и пролиферацию фибробластов, влияют на продукцию коллагена (Маянский А.Н., Пикуза О.И. Клинические аспекты фагоцитоза. - Казань: «Магариф», 1993. - С. 192).
Мононуклеары представляют собой источник многочисленных биорегуляторов - цитокинов, участвующих в формировании и регуляции защитных реакций организма (Шубич М.Г., Авдеева М.Г. Медиаторные аспекты воспалительного процесса // Арх. патологии. - 1997. - Т. 59, №2. - С. 3-8). Цитокины представляют сложную сеть иммуномедиаторов, которые регулируют и определяют природу иммунного ответа. Регуляторная роль цитокинов в организме ограничивается не только иммунным ответом: они принимают участие в процессах регенерации для восстановления поврежденных тканей (Симбирцев А.С. Цитокины - новая система регуляции защитных реакций организма // Цитокины и воспаление. - 2002. - №1. - С. 9-16).
Локальная деструкция тканей в результате повреждения эндотелиального слоя роговицы ведет к синтезу и секреции клетками моноцитарно-макрофагального ряда таких цитокинов, как IL-6, фактора некроза опухоли-α (TNF-α), трансформирующий ростовой фактор бета (TGF-beta). IL-6 является главным индуктором конечной дифференцировки макрофагальных клеток на тканевом повреждении. Трансформирующий ростовой фактор бета (TGF-beta) является белком, контролирующим пролиферацию и клеточную дифференцировку макрофагальных клеток. Фактор некроза опухоли-α (TNF-α) влияет не только на липидный метаболизм и стимуляцию IL-6, IL-8, но и на функционирование эндотелия - однослойного пласта клеток мезенхимного происхождения, отвечающего за контроль диффузии воды, ионов в ткани роговицы.
Размер парацентеза 1,2 мм не требует наложения роговичного шва за счет самогерметизации тканей роговицы при уменьшении травматичности хирургической манипуляции. Клеточную суспензию получают на градиенте плотности смеси фиколл-верографин, что способствует получить 98% чистоту клеточной культуры. Также сроки лечения сокращаются за счет однократного введения суспензии мононуклеаров.
Экзогенное введение аутологичных мононуклеаров периферической крови в переднюю камеру, продуцирующих вышеописанные цитокины, при эндотелиально-эпителиальной дистрофии роговицы позволяет создать локально высокую концентрацию клеток данной популяции в очаге деструкции и направленно воздействовать на патологический процесс, тем самым способствуя пролиферации поврежденного эндотелиального слоя.
Таким образом, результаты экспериментального исследования показали, что внутрикамеральное введение аутологичных мононуклеаров крови с последующим их наслоением на внутреннюю поверхность роговой оболочки при ЭЭД и ранней буллезной кератопатии способствует регенерации эндотелиального слоя роговицы.
Благодаря этому компенсируется нарушенная функция эндотелия роговицы и, как следствие, уменьшается отек ткани роговой оболочки и восстанавливается ее прозрачность.
Фигура 1 - установка ирригационной системы в паразентез с подачей стерильного воздуха:
1 - ирригационная система;
2 - пузырь воздуха.
Фигура 2 - введение суспензии аутологичных мононуклеаров крови в переднюю камеру на границе внутренней поверхностью роговицы и пузырем воздуха:
3 - суспензия аутологичных мононуклеаров крови;
2 - пузырь воздуха.
Фигура 3 - отек собственного вещества роговицы, повышенно извитой ход и нарушение тинкториальных свойств коллагеновых волокон через 3 суток после воздействия. Окраска гематоксилином и пикрофуксином по Ван-Гизону, ×400:
4 - отек стромы роговицы.
Фигура 4 - слущивание эндотелия через 3 суток после воздействия. Окраска гематоксилином и эозином, ×400:
5 - эндотелий роговицы.
Фигура 5 - выраженный отек собственного вещества роговицы через 7 суток после воздействия. Окраска гематоксилином и эозином, ×400:
6 - отек собственного вещества роговицы.
Фигура 6 - отек собственного вещества роговицы, нечеткие границы задней пограничной мембраны, пролиферация заднего эпителия роговицы через 7 суток после воздействия. Окраска гематоксилином и пикрофуксином по Ван-Гизону, ×600:
6 - отек собственного вещества роговицы;
5 - эндотелий роговицы.
Фигура 7 - незначительный отек собственного вещества роговицы через 14 суток после воздействия. Окраска гематоксилином и эозином, ×400:
6 - отек собственного вещества роговицы.
Фигура 8 - отростчатые клетки заднего эпителия роговицы через 14 суток после воздействия. Окраска гематоксилином и эозином, ×600:
7 - отростчатые клетки эндотелия.
Фигура 9 - компактное расположение коллагеновых волокон, равномерное восприятие красителя в собственном веществе роговицы через 21 сутки после воздействия. Окраска гематоксилином и пикрофуксином по Ван-Гизону, ×400:
8 - коллагеновые волокна.
Фигура 10 - задняя пограничная мембрана и задний эпителий роговицы через 21 сутки после воздействия. Окраска гематоксилином и эозином, ×600:
9 - задняя пограничная мембрана;
10 - задний эпителий роговицы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЭНДОТЕЛИАЛЬНО-ЭПИТЕЛИАЛЬНОЙ ДИСТРОФИИ РОГОВИЦЫ | 2017 |
|
RU2674237C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛУБОКИХ СТРОМАЛЬНЫХ КЕРАТИТОВ | 2010 |
|
RU2440801C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭНДОТЕЛИАЛЬНО-ЭПИТЕЛИАЛЬНОЙ ДИСТРОФИИ РОГОВИЦЫ | 2015 |
|
RU2594447C1 |
| СПОСОБ ЛЕЧЕНИЯ ЯЗВ РОГОВИЦЫ | 2006 |
|
RU2324488C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ОТЕКА РОГОВИЦЫ И ДРУГИХ ПРОЯВЛЕНИЙ РАННЕЙ БУЛЛЕЗНОЙ КЕРАТОПАТИИ | 2008 |
|
RU2357743C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПРОЛИФЕРАТИВНОЙ ВИТРЕОРЕТИНОПАТИИ | 2000 |
|
RU2182369C2 |
| Способ хирургического лечения кератэктазий различного генеза | 2022 |
|
RU2780273C1 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ МОНОНУКЛЕАРОВ КРОВИ in vitro | 2002 |
|
RU2221039C1 |
| Способ лечения воспалительных или дистрофических заболеваний глаз | 2019 |
|
RU2714193C1 |
| СПОСОБ ЛЕЧЕНИЯ БУЛЛЕЗНОЙ КЕРАТОПАТИИ | 2013 |
|
RU2544306C2 |

Изобретение относится к медицине, а именно к офтальмологии, и предназначено для лечения эндотелиально-эпителиальной дистрофии (ЭЭД) роговицы. Для осуществления способа вводят взвесь аутологичных мононуклеаров крови через парацентез вблизи лимба во внутреннюю камеру глаза до полного замещения ею влаги передней камеры. При этом выполняют два парацентеза размером 1-2 мм, на 7 и 11 часах, в один из которых устанавливают ирригационную систему в виде канюли для подачи стерильного воздуха в переднюю камеру под давлением до 0,2 атм, и через второй парацентез с помощью шприца в переднюю камеру на границе между внутренней поверхностью роговицы и пузырем воздуха однократно вводят 96-98% клеточную суспензию аутологичных мононуклеаров крови. После чего ирригационную систему удаляют, края парацентезов гидратируют. Суспензию аутологичных мононуклеаров крови получают путем выделения методом фракционирования в градиенте плотности на разделяющем растворе фиколл-верографина. Использование изобретения позволяет сократить сроки лечения и осложнений, связанных с излишней травматизацией тканей глаза, отека роговицы. 10 ил.
Способ лечения эндотелиально-эпителиальной дистрофии роговицы, заключающийся во введении взвеси аутологичных мононуклеаров крови через парацентез вблизи лимба во внутреннюю камеру глаза до полного замещения ею влаги передней камеры, отличающийся тем, что выполняют два парацентеза размером 1,2 мм, на 7 и 11 часах, в один из которых устанавливают ирригационную систему в виде канюли для подачи стерильного воздуха в переднюю камеру под давлением до 0,2 атм, при этом через второй парацентез с помощью шприца в переднюю камеру на границе между внутренней поверхностью роговицы и пузырем воздуха однократно вводят 96-98% клеточную суспензию аутологичных мононуклеаров крови, выделенную методом фракционирования в градиенте плотности на разделяющем растворе фиколл-верографина, после чего ирригационную систему удаляют, края парацентезов гидратируют.
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ОТЕКА РОГОВИЦЫ И ДРУГИХ ПРОЯВЛЕНИЙ РАННЕЙ БУЛЛЕЗНОЙ КЕРАТОПАТИИ | 2008 |
|
RU2357743C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛУБОКИХ СТРОМАЛЬНЫХ КЕРАТИТОВ | 2010 |
|
RU2440801C1 |
| СПОСОБ ЛЕЧЕНИЯ МАКУЛЯРНОГО РАЗРЫВА | 2003 |
|
RU2258491C2 |
| ЕЛЕГЕЧЕВА О.Н | |||
| Применение аутологичных мононуклеаров крови в комплексном лечении гнойных язв роговицы (экспериментально-клиническое исследование) | |||
| Дисс | |||
| к.м.н., 2009, Томск, с.34-43 | |||
| ЗАПУСКАЛОВ И.В | |||
| и др | |||
| Динамика воспалительно-регенераторных процессов при | |||
Авторы
Даты
2016-11-10—Публикация
2015-07-30—Подача