Изобретение относится к медицине, в частности к офтальмологии, и может быть использовано для лечения первичных и вторичных кератэктазий.
Кератэктазия - мультифакториальное заболевание роговой оболочки, в основе которого лежит потеря структурной целостности и истончение стромы роговицы с формированием ее выпячивания. Причинами развития заболевания могут быть ранее выполненные кераторефракционные и кератореконструктивные операции, травмы роговицы. Появление эктазии роговой оболочки сопровождается развитием симптомов роговичного синдрома, значительным снижением остроты зрения и существенным ухудшением качества жизни пациентов [1, 2].
В настоящее время существуют различные методы лечения данного заболевания. Так, например, на начальной стадии кератэктазии используются коррекция жесткими контактными линзами и ультрафиолетовый кросслинкинг роговой оболочки в различных модификациях, в далеко зашедших стадиях – сквозная и послойная кератопластика [3, 4]. Однако, учитывая полиэтиологичность заболевания и патоморфологические особенности его течения, проблема лечения кератэктазий различного генеза остается нерешенной до настоящего времени. Особый интерес, на наш взгляд, представляет клеточная терапия, применение которой стимулирует репаративные процессы в дистрофически измененной роговой оболочке.
Известен способ медикаментозного лечения кератоконуса, заключающийся в эпибульбарном введении раствора лейкинферона [5]. Препарат инстиллируют в конъюнктивальную полость больного глаза по 1-2 капле 2 раза в день в одно и тоже время в течение 10 дней. Согласно клиническим наблюдениям, на фоне применения данного метода лечения подавляется апопотоз кератоцитов пораженной роговицы за счет антиоксидантных свойств лейкинферона. Однако необходимо отметить, данный метод лечения кератэктазии все же не обеспечивает должной глубины воздействия на роговую оболочку, оказывая терапевтическое влияние, преимущественно, на поверхностные слои роговицы. Кроме того, данный метод лечения эффективен лишь на начальной стадии заболевания, обеспечивая временный результат с последующим прогрессирующим выпячиванием роговой оболочки.
Известен также способ лечения начальной стадии кератоконуса [6], предполагающий субконъюнктивальное – вблизи лимба пораженной роговицы - введение диспергированного биоматериала Аллоплант. Препарат предварительно разводят в физиологическом растворе натрия хлорида в соотношении 30 мг биоматериала на 0,5-1,5 мл раствора с добавлением 0,5 мл раствора дексаметазона, после чего выполняют субконъюнктивальные инъекции Аллопланта в 4-6 точках вокруг лимба дистрофически измененной роговицы с интервалом 1 раз в 6-12 месяцев. Недостатками данного метода является необходимость повторных инъекций для поддержания терапевтического эффекта, а также аллогенность вводимого препарата с риском развития аллергической и аутоиммунной реакций.
Наиболее близким к заявляемому техническому решению по технической сущности и достигаемому техническому результату является способ лечения начального кератоконуса с использованием материала «Биоплант», пропитанным препаратом Суперлимф [7].
Данный способ лечения осуществляется следующим образом. Используют материал «Биопласт», пропитанный иммунотропным препаратом Суперлимф - комплекс естественных цитокинов – интерлейкин – 1, 2, 6, фактор некроза опухоли и т.д., оказывающий активирующее действие на клетки лимбальной зоны роговицы. Из материала «Биопласт» вырезают полоску ткани длиной 8,0 мм и шириной 3,0 мм, которую затем пропитывают в растворе Суперлимф в течение 15 минут. Далее подготовленную полоску материала «Биопласт» вводят в субтеноново пространство пораженного глаза через разрез конъюнктивы склеры длиной 2,0 мм на расстоянии 3,0 мм от лимба, вблизи зоны эктазии роговицы.
Недостатками представленного способа лечения является аллогенность препарата Суперлимф, травматичность хирургического вмешательства, существенный риск развития интра- и послеоперационных осложнений (дислокация биоматериала, присоединение вторичной инфекции). Кроме того, полоска материала «Биопласт», расположенная в 3,0 мм от лимба, не может в полной мере обеспечить достаточно эффективного воздействия на пораженную роговицу вследствие удаленности от нее. Необходимо также отметить, что данный способ лечения, согласно рекомендациям авторов, показан для лечения только начальной стадии кератоконуса.
В основу настоящего изобретения положена задача создания нового способа хирургического лечения кератэктазий различного генеза с использованием клеточных технологий, применение которого обеспечит высокую и стабильную клинико-функциональную эффективность на различных стадиях заболевания.
Для решения поставленной задачи разработан новый способ хирургического лечения кератэктазий различного генеза, включающий однократное введение свежевыделенной суспензии аутологичных мононуклеарных лейкоцитов крови в строму пораженной роговой оболочки.
Способ осуществляется следующим образом. Аутологичные мононуклеарные клетки из крови пациента выделяют непосредственно перед операцией методом фракционирования в градиенте плотности на разделяющем растворе фиколл-верографин. Выделение аутологичных мононуклеаров осуществляют следующим образом: предварительно в условиях процедурного кабинета с соблюдением условий асептики и антисептики производят забор крови из локтевой вены пациента в количестве 4,0-5,0 мл. Кровь помещают в стерильную пробирку, содержащую 1,0 мл раствора гепарина. Гепаринизированную кровь разводят в 2,0 раза изотоническим раствором хлорида натрия. Полученную суспензию наслаивают на 3,0 мл смеси фиколла-верографина (12 частей 9% фиколла и 5 частей 33,9% верографина с плотностью 1,067-1,077 г/мл). Соотношение объемов градиента и разделяемой суспензии составляет 1:3 - 1:4.
Пробирку центрифугируют при комнатной температуре в течение 15 мин при 800g (2000 об/мин). После центрифугирования интерфазный слой, содержащий мононуклеарные лейкоциты и располагающийся между плазмой и градиентом, забирают пастеровской пипеткой. Добавляют 1,0 мл изотонического раствора хлорида натрия, и полученную суспензию вновь центрифугируют в течение 7 мин при 400g (1500 об/мин) для отмывания клеточной взвеси.
Чистота мононуклеаров, полученных на градиенте фиколл-верографин, составляет 96-98%. Жизнеспособность клеточного материала оценивается в тесте с трипановым синим следующим способом: предварительно на основе раствора Рингера готовится 0,1% раствор эозина. Далее на основе дистиллированной воды готовится 0,1% раствор трипанового синего. После этого к капле клеточной суспензии добавляют 1-2 капли свежей смеси растворов, приготовленных ранее красителей, взятых в равных объемах. Полученную смесь помещают в камеру Горяева. При подсчете клеток процент окрашенных (погибших) элементов должен составлять 1,5-2%, что не превышало бы допустимое (не более 3%) количество. Жизнеспособность клеточного материала в тесте с трипановым синим составляла 97-98%.
В условиях операционной после обработки операционного поля и анестезии больного глаза пациента с помощью инстилляций в конъюнктивальную полость 1-2 капель 0,4% раствора оксибупракаина, ретробульбарной анестезии 2,0 мл 2% раствора лидокаина гидрохлорида вокруг зоны эктазии роговицы под углом 30 градусов к поверхности роговой оболочки на уровне передней трети ее стромы вводят иглу калибра 25G, надетую на 1,0 мл шприц со свежевыделенной суспензией аутологичных мононуклеарных лейкоцитов крови. Далее, вводя по 0,2 мл клеточной суспензии в 4 секторах вокруг зоны кератэктазии, добиваются появления четко выраженной инфильтрации передней трети стромы пораженной роговицы. Затем под конъюнктиву склеры больного глаза пациента вводят раствор антибиотика широкого спектра действия в стандартном разведении и накладывают монокулярную повязку на 1 сутки. В послеоперационном периоде проводят инстилляции глазных капель антибиотика широкого спектра действия в конъюнктивальную полость больного глаза по стандартной схеме.
Сущность заявляемого технического решения поясняется чертежами. Ниже представлено краткое описание приложенных фигур, используемых для описания осуществления изобретения.
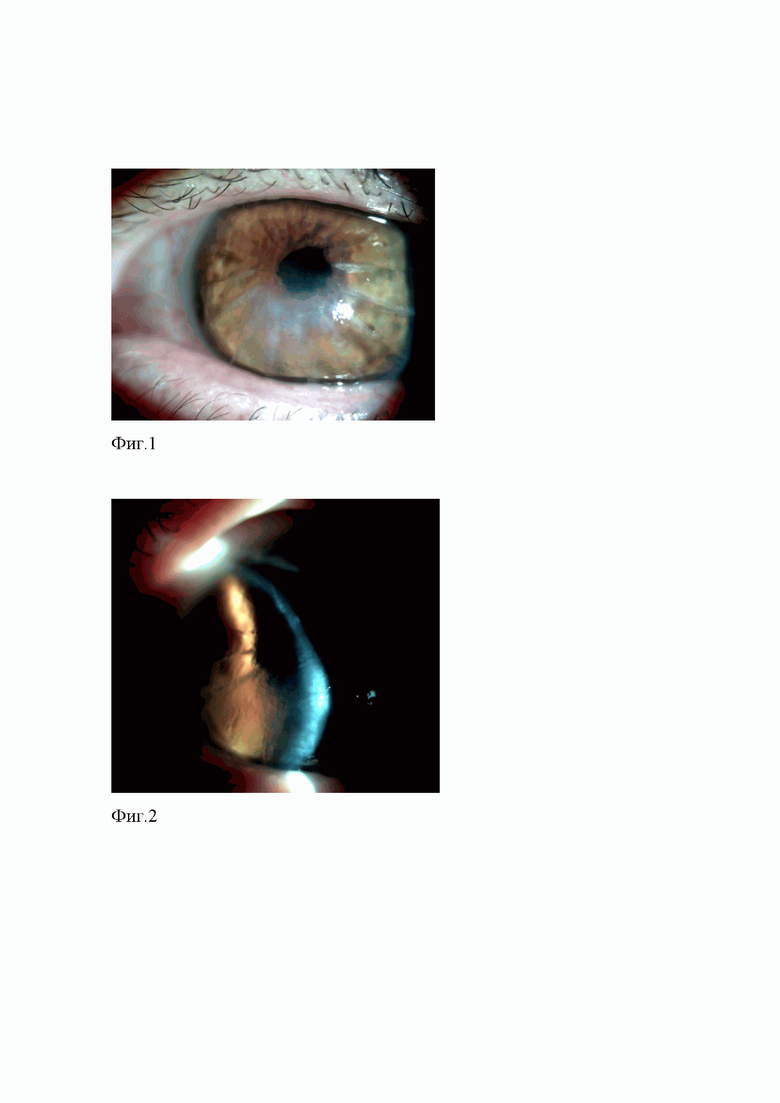
На фиг.1 представлена биомикроскопическая картина роговой оболочки больного глаза пациентки с вторичной кератэктазией при поступлении;
на фиг.2 показан оптический срез роговой оболочки больного глаза пациентки с вторичной кератэктазией при поступлении;
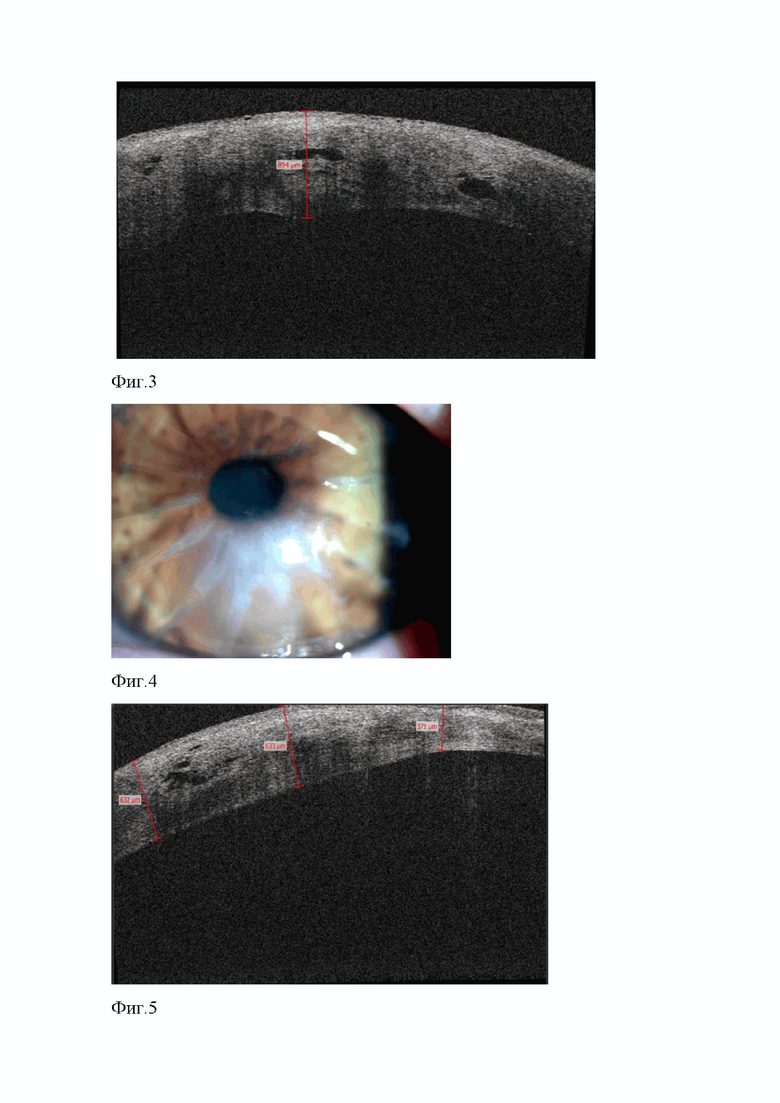
на фиг.3 представлена ОКТ-томограмма роговицы больного глаза пациентки с вторичной кератэктазией при поступлении;
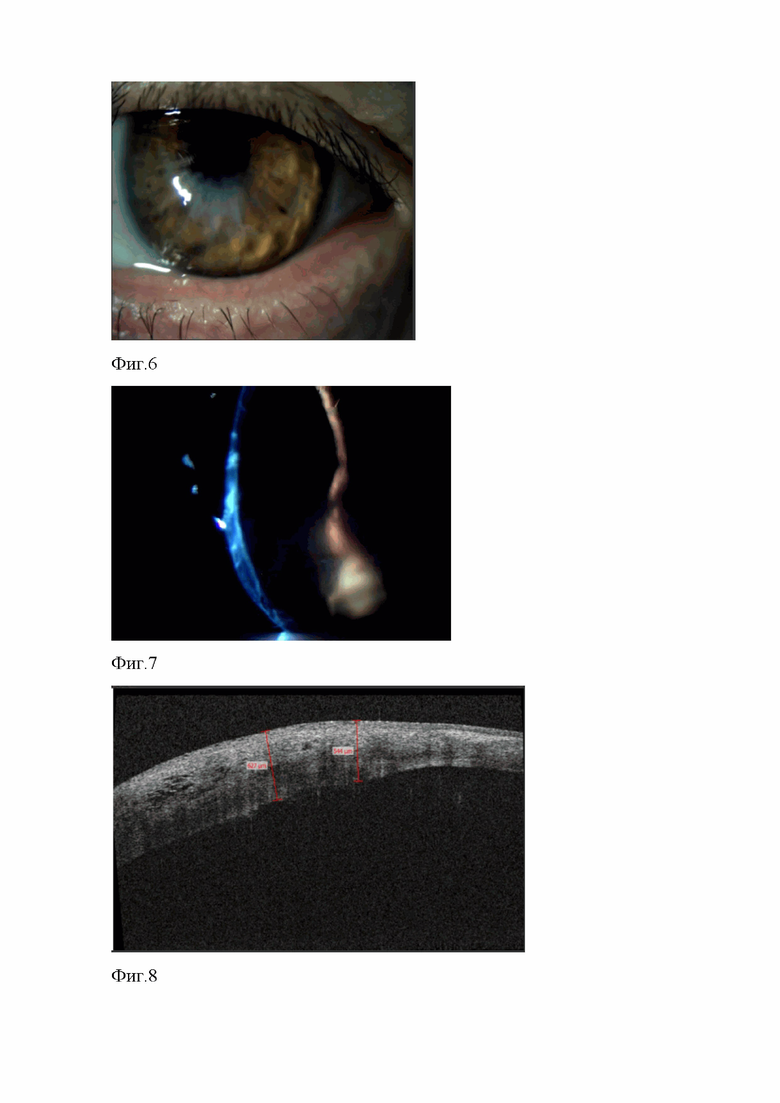
на фиг.4 представлена биомикроскопическая картина роговой оболочки больного глаза пациентки с вторичной кератэктазией на 3-и сутки после операции;
на фиг.5 представлена ОКТ-томограмма роговицы больного глаза пациентки с вторичной кератэктазией на 3-и сутки после операции;
на фиг.6 представлена биомикроскопическая картина роговой оболочки больного глаза пациентки с вторичной кератэктазией на 10-е сутки после операции;
на фиг.7 показан оптический срез роговой оболочки больного глаза пациентки с вторичной кератэктазией на 10-е сутки после операции;
на фиг.8 представлена ОКТ-томограмма роговицы больного глаза пациентки с вторичной кератэктазией на 10-е сутки после операции;
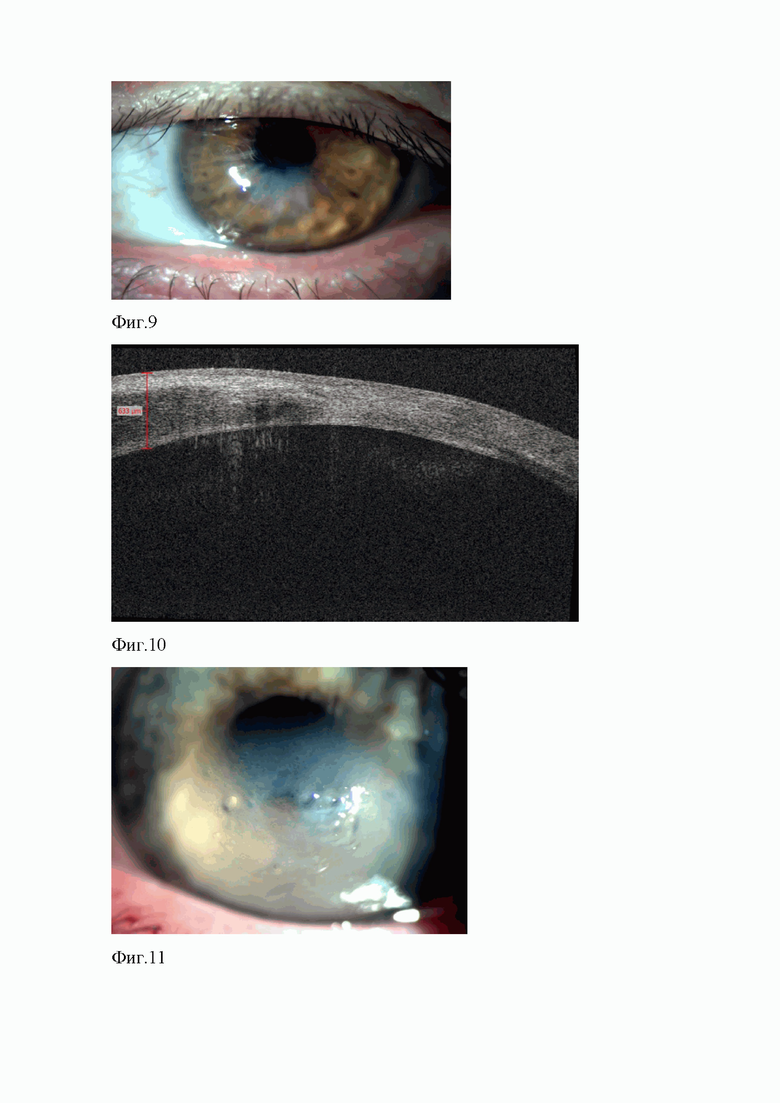
на фиг.9 представлена биомикроскопическая картина роговой оболочки больного глаза пациентки с вторичной кератэктазией через 1 месяц после операции;
на фиг.10 представлена ОКТ-томограмма роговицы больного глаза пациентки с вторичной кератэктазией через 1 месяц после операции;
на фиг.11 представлена биомикроскопическая картина роговой оболочки больного глаза пациента с начальным кератоконусом при поступлении;
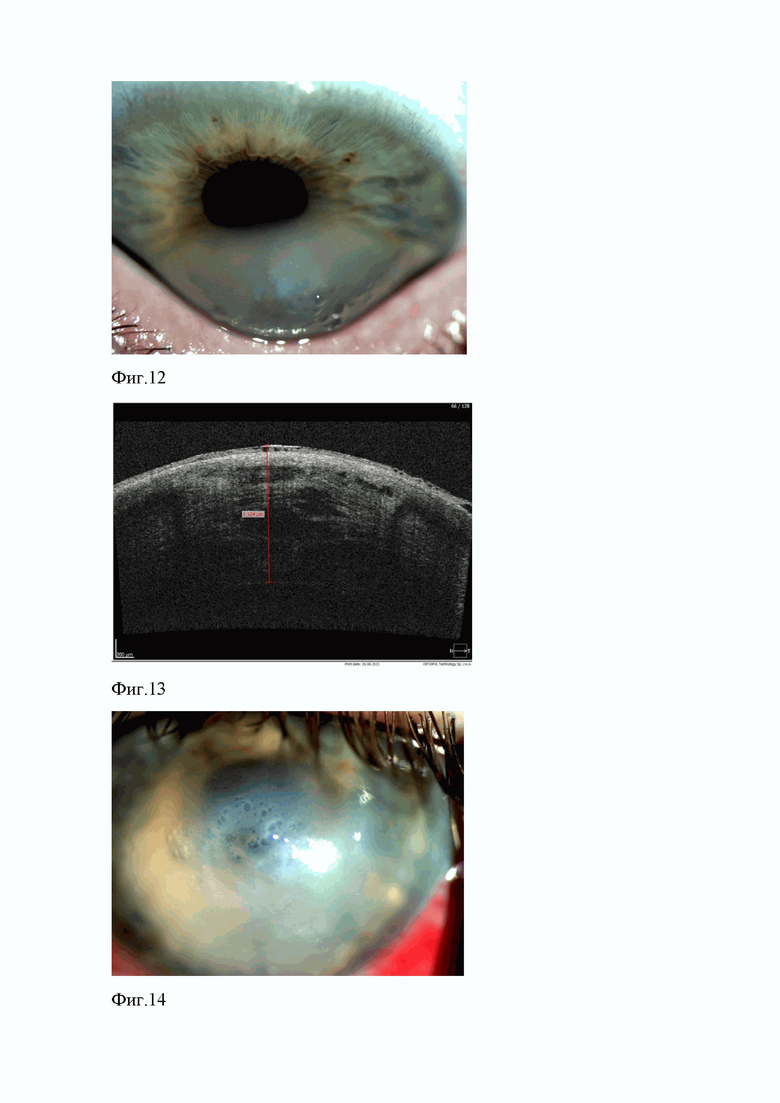
на фиг.12 показан внешний вид роговой оболочки больного глаза пациента с начальным кератоконусом при взгляде книзу при поступлении;
на фиг.13 представлена ОКТ-томограмма роговицы больного глаза пациента с начальным кератоконусом при поступлении;
на фиг.14 представлена биомикроскопическая картина роговой оболочки больного глаза пациента с начальным кератоконусом на 3-и сутки после операции;
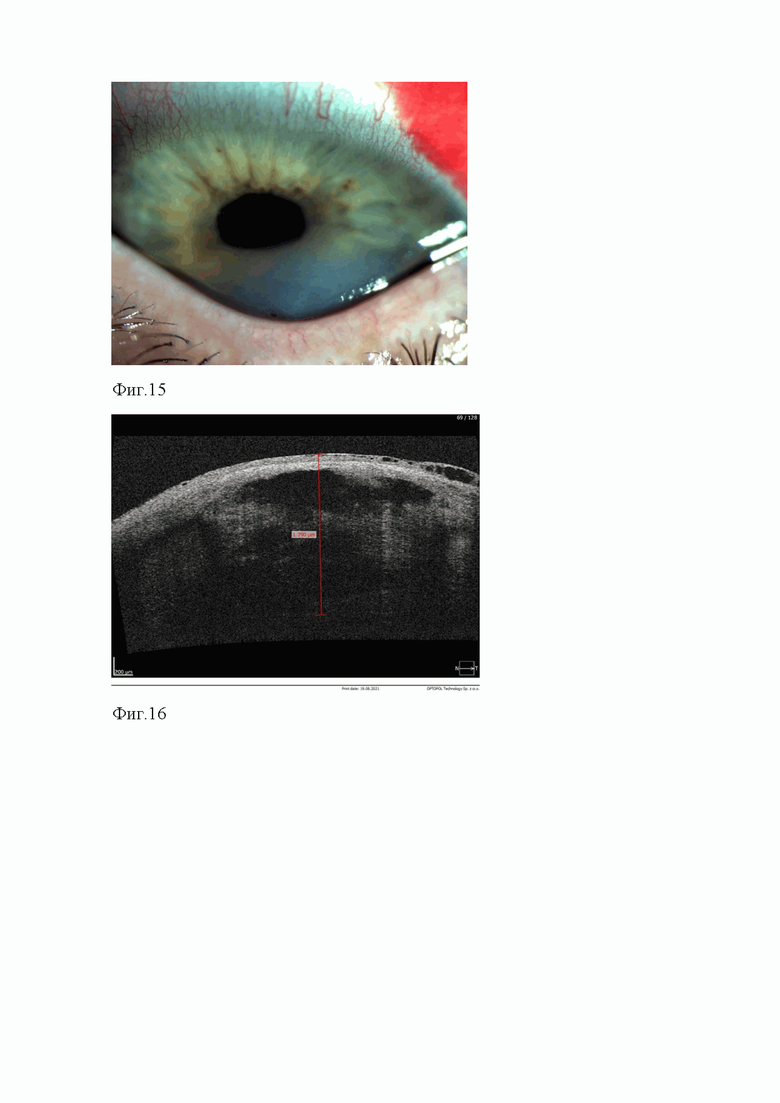
на фиг.15 представлен внешний вид роговой оболочки больного глаза пациента с начальным кератоконусом при взгляде книзу на 3-и сутки после операции;
на фиг.16 представлена ОКТ-томограмма роговицы больного глаза пациента с начальным кератоконусом на 3-и сутки после операции;
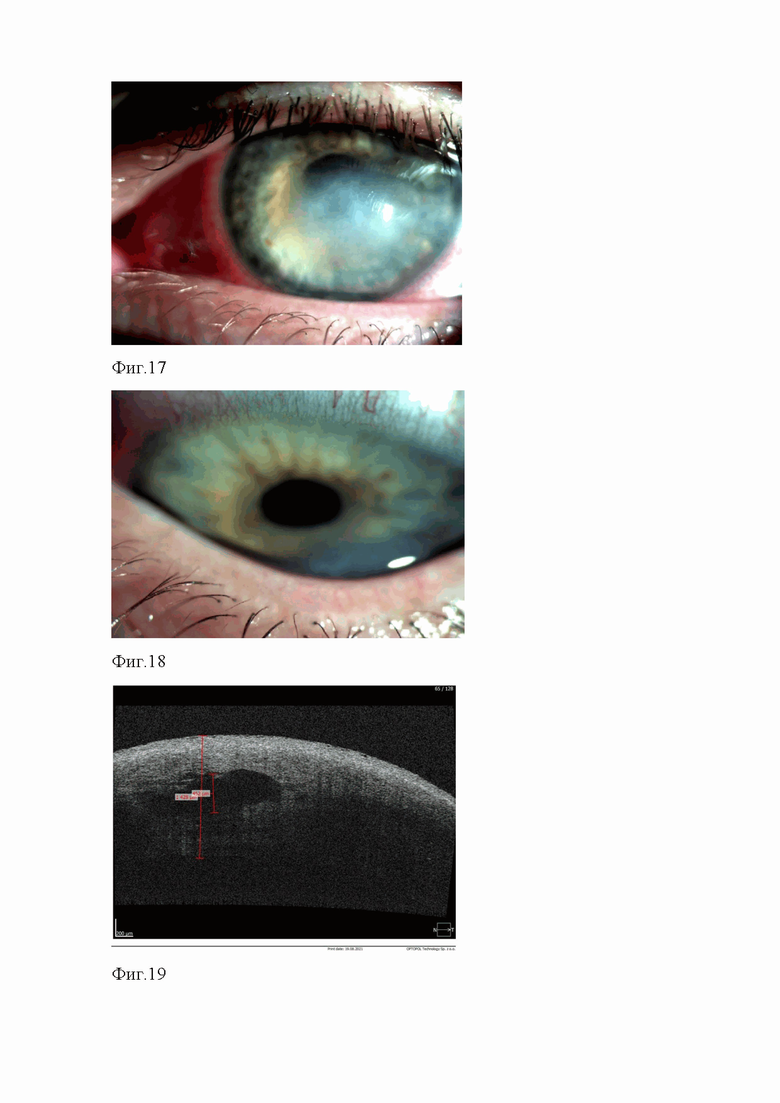
на фиг.17 представлена биомикроскопическая картина роговой оболочки больного глаза пациента с начальным кератоконусом на 10-е сутки после операции;
на фиг.18 представлен внешний вид роговой оболочки больного глаза пациента с начальным кератоконусом при взгляде книзу на 10-е сутки после операции;
на фиг.19 представлена ОКТ-томограмма роговицы больного глаза пациента с начальным кератоконусом на 10-е сутки после операции;
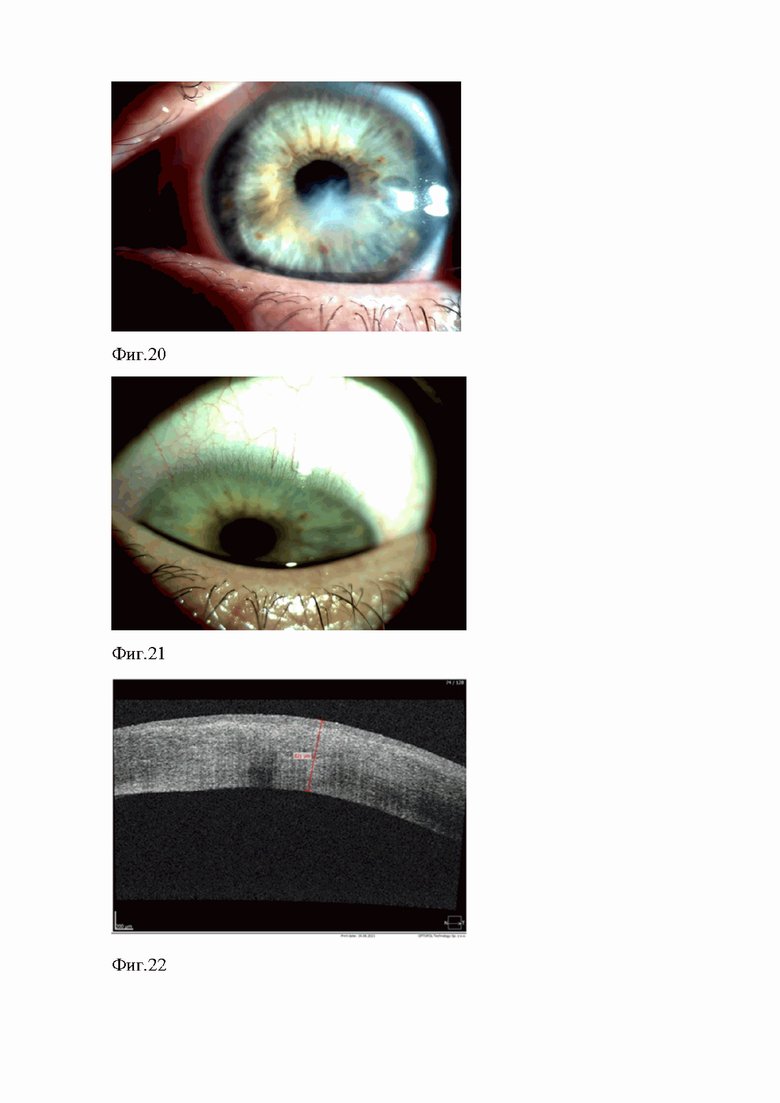
на фиг.20 представлена биомикроскопическая картина роговой оболочки больного глаза пациента с начальным кератоконусом через 1 месяц после операции;
на фиг.21 представлен внешний вид роговой оболочки больного глаза пациента с начальным кератоконусом при взгляде книзу через 1 месяц после операции;
на фиг.22 представлена ОКТ-томограмма роговицы больного глаза пациента с начальным кератоконусом через 1 месяц после операции;
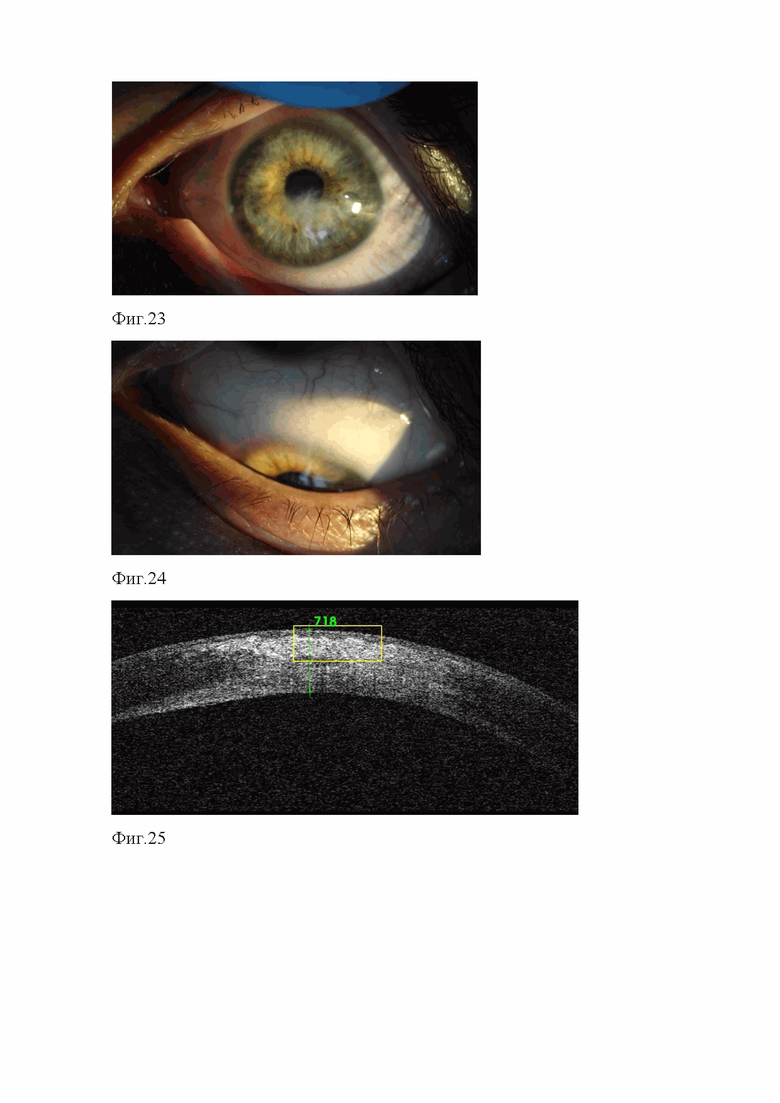
на фиг.23 представлена биомикроскопическая картина роговой оболочки больного глаза пациента с начальным кератоконусом через 3 месяца после операции;
на фиг.24 представлен внешний вид роговой оболочки больного глаза пациента с начальным кератоконусом при взгляде книзу через 3 месяца после операции;
на фиг.25 представлена ОКТ-томограмма роговицы больного глаза пациента с начальным кератоконусом через 3 месяца после операции.
Преимуществами разработанного нового способа хирургического лечения кератэктазий различного генеза являются:
- использование суспензии клеток аутологичного происхождения из крови пациента, что исключает риск развития аутоиммунной реакции, а также передачи трансмиссивных инфекций;
- использование свежевыделенной клеточной суспензии не требует ее консервации и обеспечения дополнительных специальных условий хранения (температурный режим, влажность, уровень оксигенации, стерильность), что существенно снижает финансово-экономические затраты лечебно-профилактического учреждения;
- рекомендуется однократное введение свежевыделенной суспензии аутологичных мононуклеарных лейкоцитов крови в строму пораженной роговой оболочки в ходе лечения кератэктазий различного генеза;
- методика введения клеточной суспензии в переднюю треть пораженной роговицы отличается технической простотой в сравнении с представленными прототипами и не требует владения специальными микрохирургическими навыками;
- введение суспензии аутологичных мононуклеарных лейкоцитов крови в переднюю треть роговицы больного глаза обеспечивает высокую концентрацию биологически активных веществ в непосредственной близости от зоны кератэктазии, обеспечивая более быструю стабилизацию патологического процесса;
- использование предлагаемого способа хирургического лечения кератэктазий различного генеза возможно на различных стадиях заболевания, в том числе, и развитой.
Клинический пример № 1
Пациентка Л., 64 года. Обратилась с жалобами на боль, светобоязнь, значительное снижение зрения левого глаза. Указанные жалобы беспокоили 2 недели, в связи с чем пациентка обратилась к офтальмологу, было назначено лечение в виде инстилляций в конъюнктивальную полость больного глаза антибактериальных, противовоспалительных и репаративных средств. Спустя несколько дней состояние глаза ухудшилось, в связи с чем пациентке была рекомендована экстренная госпитализация в офтальмологический стационар. В ходе сбора анамнеза жизни пациентки установлено, что около 30-ти лет назад ей была выполнена радиальная кератотомия по поводу миопии высокой степени обоих глаз.
Диагноз при поступлении в офтальмологическую клинику: вторичная кератэктазия левого глаза. Оперированная миопия высокой степени обоих глаз.
При поступлении:
Vis OD = 0,7 не корригирует (н/к)
Vis OS= 0,005 н/к
Уровень внутриглазного давления (ВГД)
OD=18 мм рт.ст., OS = 22 мм рт.ст.
При биомикроскопии: OD – глаз спокоен, на периферии роговице в поверхностных слоях стромы обнаруживаются беловатые, линейной формы радиально расположенные рубцы после кератотомии. Передняя камера средней глубины, влага прозрачная, реакция зрачка на свет сохранена, в хрусталике определялись начальные помутнения в передней и задней коре. Со стороны глазного дна патологии не выявлено.
OS - умеренные светобоязнь и слезотечение, блефароспазм, смешанная инъекция глазного яблока. Оптический срез роговицы неравномерный по толщине, в нижней половине роговой оболочки визуализируется выраженный отек эпителия и конической формы выпячивание стромы со значительным ее истончением на вершине, перифокально обнаруживается неравномерный отек и инфильтрация основного вещества, складки десцеметовой оболочки. Радиально на периферии роговицы, в поверхностных слоях стромы – беловатые, линейной формы рубцы после кератотомии (фиг.1, фиг.2). Передняя камера средней глубины, влага прозрачная, зрачок средней ширины, реакция на свет «живая», в хрусталике - начальные помутнения в передней и задней коре. Со стороны глазного дна патологии не выявлено.
По данным оптической когерентной томографии (ОКТ) переднего отрезка левого глаза, толщина роговицы в зоне эктазии составляла 595 мкм, вокруг зоны выпячивания роговой оболочки - 894 мкм, в строме роговицы обнаруживались скопления кистозных полостей (фиг.3).
Пациентке проведено хирургическое лечение вторичной кератэктазии левого глаза разработанным способом, включающим интрастромальное введение суспензии аутологичных мононуклеарных лейкоцитов крови в переднюю треть стромы дистрофически измененной роговой оболочки. Операция выполнена по представленной методике, без осложнений.
В послеоперационном периоде выполнялись инстилляции в конъюнктивальную полость оперированного глаза глазных капель антибиотика широкого спектра действия по стандартной схеме.
В ходе наблюдения пациентки в послеоперационном периоде выявлена следующая динамика клинической картины заболевания.
На 3-и сутки после оперативного вмешательства:
Vis OS=0,1 н/к, пальпаторно уровень ВГД OS – в норме.
При биомикроскопии левого глаза - незначительные блефароспазм и смешанная инъекция бульбарной конъюнктивы. Оптический срез роговицы неравномерный за счет эктазии в нижней половине, отек переднего эпителия несколько уменьшился, сохранялись отек и инфильтрация стромы вокруг зоны эктазии, складки десцеметовой оболочки (фиг.4). По данным ОКТ роговицы левого глаза, толщина роговой оболочки в зоне эктазии уменьшилась до 423 мкм, вокруг зоны эктазии - до 673 мкм за счет значительного уменьшения количества кистозных полостей в толще основного вещества, сокращения их по площади и объему (фиг.5). Со стороны глубже лежащих отделов оперированного левого глаза – без отрицательной динамики.
На 10-е сутки после операции пациентка отметила отсутствие светобоязни левого глаза и лишь незначительную болезненность, а также некоторое улучшение остроты зрения оперированного глаза.
Vis OS=0,2 н/к, уровень ВГД OS = 21 мм рт. ст.
При биомикроскопии левого глаза – передний эпителий роговой оболочки спокоен, зона эктазии в нижней трети роговицы значительно уменьшилась по площади и степени выпячивания, вокруг патологической зоны роговицы сохранялись незначительные отек и инфильтрация стромы, тонкие складки десцеметовой оболочки (фиг.6, фиг.7). По данным ОКТ роговицы левого глаза, толщина роговой оболочки в зоне эктазии составляла 414 мкм, вокруг нее – 653 мкм с единичными щелевидным кистозными полостями в строме оболочки (фиг.8).
Через 1 месяц после хирургического лечения вторичной кератэктазии левого глаза пациентки новым предлагаемым способом пациентка отмечала отсутствие жалоб со стороны оперированного глаза.
Vis OS=0,5 н/к, уровень ВГД OS = 20 мм рт.ст.
При биомикроскопии левого глаза - отмечалась незначительная неравномерность оптического среза роговой оболочки за счет остаточной эктазии в нижней трети роговицы, передний эпителий и строма роговой оболочки спокойны, определялись единичные тонкие складки десцеметовой оболочки (фиг.9). По данным ОКТ роговицы левого глаза, в зоне эктазии толщина роговой оболочки составляла 394 мкм, перифокально – 633 мкм, при этом строма роговицы в зоне эктазии и вокруг нее была однородная, без признаков отека и кистозных полостей (фиг.10).
Через 3, 6 месяцев и 1 год после хирургического лечения вторичной кератэктазии левого глаза пациентки новым предлагаемым способом клинико-функциональные результаты лечения соответствовали показателям, достигнутым через 1 месяц после операции.
Каких-либо осложнений со стороны оперированного глаза в течение всего периода наблюдения (1 год) выявлено не было.
Клинический пример № 2
Пациент М., 31 год. Обратился с жалобами на боль, светобоязнь, резкое снижение зрения левого глаза. Указанные жалобы появились около 2-х дней назад на фоне относительного здоровья. Пациент обратился в кабинет неотложной офтальмологической помощи и после осмотра дежурным врачом-офтальмологом был экстренно госпитализирован в офтальмологическую клинику.
Диагноз при поступлении: острый кератоконус левого глаза, начальный кератоконус правого глаза.
При поступлении:
Vis OD= 0,3 с sph +1,5 cyl -2,5 Ax 54=0,8
Vis OS= 0,05 н/к
Уровень ВГД OD=17 мм рт.ст., OS – норма пальпаторно.
При биомикроскопии: OD – глаз спокоен, роговица прозрачная, передняя камера средней глубины, влага прозрачная, реакция зрачка «живая», хрусталик прозрачный. При осмотре глазного дна – патологии не выявлено.
OS - умеренные светобоязнь и слезотечение, блефароспазм, смешанная инъекция конъюнктивы глазного яблока. Оптический срез роговицы неравномерный по толщине, зона эктазии захватывает до 2/3 роговой оболочки, перифокально отмечаются отек и инфильтрация основного вещества, складки десцеметовой оболочки (фиг.11, фиг.12). Передняя камера средней глубины, влага прозрачная, реакция зрачка на свет сохранена, хрусталик прозрачный. Осмотр глазного дна затруднен из-за изменений роговой оболочки, рефлекс с глазного дна розовый.
Согласно данным В-сканирования левого глаза, патологии глазного дна выявлено. По данным ОКТ роговой оболочки левого глаза, средняя толщина роговицы в зоне эктазии составляла 1594 мкм, в основном веществе обнаруживались отек и кистозные полости (фиг.13).
Пациенту проведено хирургическое лечение острого кератоконуса левого глаза новым разработанным способом. Операция выполнена по представленной методике, осложнений во время хирургического вмешательства не наблюдалось.
В послеоперационном периоде выполнялись инстилляции глазных капель антибиотика широкого спектра действия в конъюнктивальную полость оперированного глаза по стандартной схеме.
В ходе наблюдения пациента в послеоперационном периоде выявлена следующая динамика клинической картины заболевания.
На 3-и сутки после хирургического лечения:
Vis OS=0,05 н/к, уровень ВГД OS – пальпаторно в норме.
При биомикроскопии левого глаза - незначительные блефароспазм и смешанная инъекция бульбарной конъюнктивы. Оптический срез роговицы неравномерный за счет эктазии в нижней половине оболочки, в зоне эктазии, в толще основного вещества, определялась крупная полость. Перифокально, вокруг зоны эктазии обнаруживались отек и инфильтрация стромы, складки десцеметовой оболочки (фиг.14, фиг.15). По данным ОКТ роговицы оперированного глаза, толщина оболочки в зоне эктазии составляла 1790 мкм (фиг.16). Со стороны остальных отделов оперированного глаза – без отрицательной динамики.
На 10-е сутки после интрастромального введения суспензии аутологичных мононуклеарных лейкоцитов пациент М. отметил значительное уменьшение боли в левом глазу и светобоязни, а также некоторое улучшение остроты зрения больного глаза.
Vis OS= 0,08 н/к. Уровень ВГД OS =18 мм рт.ст.
При биомикроскопии левого глаза – передний эпителий роговой оболочки спокоен, зона эктазии в нижней трети роговицы значительно уменьшилась по степени выпячивания, полость в толще стромы оболочки уменьшилась по высоте. Вокруг эктазии сохранялись незначительные отек и инфильтрация основного вещества, тонкие складки десцеметовой оболочки (фиг.17, фиг.18). По данным пахиметрии роговицы левого глаза, толщина роговой оболочки составляла 1428 мкм. Согласно ОКТ переднего отрезка левого глаза, в строме основного вещества роговой оболочки определялись единичные кистозными полости, значительно уменьшившиеся по величине при сравнении с исходными данными (фиг.19).
Через 1 месяц после проведенного хирургического лечения острого кератоконса новым разработанным способом пациент отметил отсутствие жалоб со стороны оперированного глаза и улучшение остроты и качества зрения левого глаза.
Vis OS=0,1 н/к. Уровень ВГД OS = 21 мм рт.ст.
При биомикроскопии левого глаза - незначительная неравномерность оптического среза роговой оболочки за счет остаточной эктазии в нижней трети роговицы. Передний эпителий и строма роговой оболочки спокойны, определялись единичные тонкие складки десцеметовой оболочки (фиг.20, фиг.21). Показатель пахиметрии роговицы оперированного глаза составлял 821 мкм. По данным ОКТ роговицы левого глаза, строма роговой оболочки была однородная, без признаков отека и кистозных полостей (фиг.22).
Через 3 месяца после хирургического лечения пациента новым предлагаемым способом жалобы отсутствовали.
Vis OS = 0,1 с sph -1,5 cyl -4,0 Ax 111=0,2-0,3
Уровень ВГД OS = 19 мм рт.ст.
При биомикроскопии левого глаза - в нижней половине роговой оболочки определялось умеренной интенсивности помутнение неправильной формы с четкими границами, окружающая ткань роговицы была спокойная. Эктазии роговой оболочки не отмечалось (фиг.23, фиг.24). При проведении ОКТ роговицы оперированного глаза, показатель пахиметрии составлял 718 мкм, при этом строма роговой оболочки была однородная, без признаков отека и кистозных полостей (фиг.25). Со стороны глазного дна – без особенностей.
Через 6 и 12 месяцев после хирургического лечения острого кератоконуса у пациента новым разработанным способом клинико-функциональные результаты оставались на уровне, достигнутом через 3 месяца после лечения.
В течение всего срока наблюдения (1 год) каких-либо осложнений у пациента не выявлено.
Согласно общепризнанному мнению [8], в основе действия клеточной терапии при лечении воспалительных и дистрофических заболеваний роговицы лежит, прежде всего, трофический эффект за счет секреторного потенциала вводимых клеток. Так, например, мононуклеарные лейкоциты крови, по данным ученых [8, 9], обладают способностью к синтезу и секреции ряда противовоспалительных цитокинов - трансформирующий фактор роста β-1, интерлейкин-1, -10 и т.д. Благодаря действию указанных биологически активных веществ в зоне патологически измененной роговой оболочки происходит стимуляция пролиферации клеток различных популяций, в первую очередь, эпителиальной природы, а также усиление продукции коллагена.
Другим механизмом действия клеточной терапии при лечении воспалительных и дистрофических заболеваний роговицы является заместительный эффект – вводимые клетки фактически заполняют имеющиеся тканевые дефекты в зонах поврежденной роговой оболочки.
Результатом комбинации указанных эффектов клеточной терапии при лечении воспалительных и дистрофических заболеваний роговицы является стимуляция репаративной регенерации поврежденных роговичных структур с постепенным улучшением формы и кривизны патологически измененной роговой оболочки. Это, в свою очередь, способствует устранению роговичного синдрома и улучшению зрительных функций у пациентов данной категории.
Техническим результатом является новый способ хирургического лечения кератэктазий различного генеза с использованием клеточных технологий, обладающий более высокой клиническо-функциональной эффективностью.
Изобретение позволяет исключить использование аллогенного, а также донорского материала при хирургическом лечении кератэктазий различного генеза. Представленный способ хирургического лечения характеризуется минимальной травматизацией глазной поверхности оперируемого глаза, что позволяет значительно снизить риски интра- и послеоперационных осложнений. Новый способ хирургического лечения отличается технической простотой и не требует владения специальными микрохирургическими навыками.
Применение разработанного способа хирургического лечения кератэктазий обеспечивает стабильные клинико-функциональные результаты в послеоперационном периоде, хорошо переносится пациентами и не вызывает осложнений.
Источники информации
1. Балашевич Л.И., Качанов А.Б., Головатенко С.П. Офтальмохирургия. 2009; 6:4-8,
2. Said A., Hamade I.H., Tabbara K.F. Saudi J. Ophthalmol. 2011; 25: 225–230
3. Солодкова Е.Г., Ремесников И.А. Современные подходы в лечении прогрессирующей кератэктазии // Практическая медицина. - 2012. – Т. 4, № 59. – С. 75-79.
4. Иомдина Е.Н. Биомеханические аспекты кераторефракционной хирургии и корнеального кросслинкинга // Российская педиатрическая офтальмология. - 2015-№ 4. – С. 32-37.
5. Патент RU2171659 «Способ медикаментозного лечения кератоконуса», МПК A61F 9/00, опубл. 10.08.2001 г.
6. Патент RU2421195, «Способ лечения начального кератоконуса», МПК А61F 9/00, A 61K 35/32, A61P 27/02, опубл.20.06.2011г.
7. Патент RU2325141, «Способ лечения начального кератоконуса», МПК А61F 9/007, опубл.27.05.2008г.
8. Аветисов С.Э., Суббот А.М., Антохин А.И., Каспарова Е.А., Каспаров А.А., Павлюк А.С. Персонализированная клеточная терапия в офтальмологии (II): цитокиновый профиль аутогенного клеточного продукта // Клеточная трансплантология и тканевая инженерия. - 2012. – Т. 7, № 1. С. 49-53.
9. Kado M, Tanaka R, Arita K, Okada K, Ito-Hirano R, Fujimura S, Mizuno H. Human peripheral blood mononuclear cells enriched in endothelial progenitor cells via quality and quantity controlled culture accelerate vascularization and wound healing in a porcine wound model. Cell Transplant.2018 Jul;27 (7):1068-1079. doi: 10.1177/0963689718780307. Epub 2018 Jul 5. PMID: 29974793; PMCID: PMC6158547.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГИПООСМОТИЧЕСКОЕ ОФТАЛЬМОЛОГИЧЕСКОЕ СРЕДСТВО ДЛЯ УЛЬТРАФИОЛЕТОВОГО КРОССЛИНКИНГА ТОНКИХ РОГОВИЦ | 2016 |
|
RU2631604C1 |
| Способ ускоренного локального кросслинкинга роговицы при кератэктазии | 2023 |
|
RU2804716C1 |
| Способ комплексного хирургического лечения начальных стадий кератоконуса у детей | 2024 |
|
RU2831914C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЭНДОТЕЛИАЛЬНО-ЭПИТЕЛИАЛЬНОЙ ДИСТРОФИИ РОГОВИЦЫ | 2017 |
|
RU2674237C1 |
| Способ лечения кератоконуса I-II стадии | 2022 |
|
RU2819801C2 |
| СПОСОБ ЛЕЧЕНИЯ КЕРАТЭКТАЗИЙ МЕТОДОМ ИМПУЛЬСНОГО АКСЕЛЕРИРОВАННОГО УЛЬТРАФИОЛЕТОВОГО КРОССЛИНКИНГА РОГОВИЦЫ | 2017 |
|
RU2682494C1 |
| Способ коррекции аметропии у пациентов со стабилизированным кератоконусом II-III стадий после имплантации интрастромальных роговичных сегментов и УФ-кросслинкинга | 2024 |
|
RU2832529C1 |
| Способ фемтосекундной сквозной кератопластики у пациентов с кератэктазиями со значительным истончением периферии роговицы | 2021 |
|
RU2773105C1 |
| СПОСОБ БИОПОКРЫТИЯ ПОРАЖЕННОЙ РОГОВИЦЫ | 2023 |
|
RU2813951C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСТРУЗИИ СЕГМЕНТОВ ПОСЛЕ ИМПЛАНТАЦИИ ИНТРАСТРОМАЛЬНЫХ РОГОВИЧНЫХ СЕГМЕНТОВ ПРИ КЕРАТЭКТАЗИЯХ | 2012 |
|
RU2525671C2 |
Изобретение относится к медицине, в частности к офтальмологии, и может быть использовано для хирургического лечения кератэктазий различного генеза. Для этого вокруг зоны выпячивания роговицы, в переднюю треть стромы роговой оболочки, под углом 30 градусов к поверхности роговой оболочки вводят по 0,2 мл свежевыделенной суспензии аутологичных мононуклеарных лейкоцитов крови с помощью иглы калибра 25G. Клеточную суспензию вводят в 4 сектора вокруг зоны кератэктазии до появления четко выраженной инфильтрации передней трети стромы пораженной роговицы. Процедура выполняется однократно. Способ обеспечивает стабильные клинико-функциональные результаты в послеоперационном периоде и хорошую переносимость пациентами разработанного лечения при минимальной травматизации глазной поверхности оперируемого глаза, что значительно снижает риск интра- и послеоперационных осложнений. 2 пр., 25 ил.
Способ хирургического лечения кератэктазий различного генеза, заключающийся в локальном введении свежевыделенной суспензии аутологичных мононуклеарных лейкоцитов крови, отличающийся тем, что суспензию клеток по 0,2 мл однократно вводят в переднюю треть стромы роговой оболочки вокруг зоны ее выпячивания с помощью иглы калибра 25G под углом 30 градусов к поверхности роговицы в 4 секторах вокруг зоны кератэктазии до появления четко выраженной инфильтрации передней трети стромы пораженной роговицы.
| Способ лечения хронического кератоконуса | 1983 |
|
SU1171030A1 |
| СПОСОБ ЛЕЧЕНИЯ НАЧАЛЬНОГО КЕРАТОКОНУСА | 2006 |
|
RU2325141C1 |
| US 0009937033 B1, 10.04.2018 | |||
| СУРКОВА В.К | |||
| и др., Кератэктазии и современные методы их лечения, Точка зрения | |||
| Восток - Запад, N2 2021, с.84-88 | |||
| ЩУКО А.Г | |||
| и др., Современные представления об этиологии, патогенезе и механизмах лечения первичных и вторичных кератэктазий, Практическая медицина N9 | |||
Авторы
Даты
2022-09-21—Публикация
2022-02-18—Подача