Настоящее изобретение относится к способам повышения выживаемости без прогрессирования заболевания пациента, страдающего от рака желудочно-кишечного тракта, в частности, метастатического колоректального рака (мКРР), с помощью бевацизумаба (Авастин, Avastin®) в комбинации с химиотерапией и с помощью определения уровня экспрессии одного или более из VEGFA (Vascular endothelial growth factor А, фактор роста эндотелия сосудов A), HER2 (Human Epidermal Growth Factor Receptor 2, человеческий рецептор эпидермального фактора роста 2), и нейропилина относительно контрольного уровня экспрессии у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, метастатического колоректального рака (мКРР).
Соответственно, настоящее изобретение связано с идентификацией и селекцией биомаркеров рака желудочно-кишечного тракта, в частности, метастатического колоректального рака (мКРР), которые коррелируют с чувствительностью или наличием ответной реакции на ингибиторы ангиогенеза, например, бевацизумаб (Avastin®), в комбинации с химеотерапевтическим лечением, например, химиотерапии на основе оксалиплатина. В этом аспекте, изобретение связано с применением опухоль-специфичного профиля (профилей) одного или более из VEGFA, HER2 и нейропилина относительно контроля у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, для выявления пациентов, чувствительных или реагирующих на добавление ингибиторов ангиогенеза, например, бевацизумаба (Avastin®), к стандартной химиотерапии. Кроме того, изобретение относится к способам повышения выживаемости без прогрессирования заболевания пациента, страдающего раком желудочно-кишечного тракта, в частности, мКРР, с помощью добавления ингибиторов ангиогенеза, например, бевацизумаба (Avastin®), к стандартной химиотерапии, например, к оксалиплатиновой химиотерапии, с помощью определения опухоль-специфичного уровня (уровней) экспрессии при опухоли одного или более из VEGFA, HER2 и нейропилина, по сравнению с контролем (контролями) у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, метастатического колоректального рака. В качестве альтернативы или дополнения к определению уровня экспрессии одного или более из VEGFA, HER2 и нейропилина в соответствии со способами, описанными в настоящей заявке, может быть определено число сосудов в опухолевом образце относительно контрольного уровня (уровней) у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, как биомаркер, указывающий на пациента, чувствительного или реагирующего на добавление ингибиторов ангиогенеза например, бевацизумаба (Avastin®), к стандартной химиотерапии. Изобретение также предусматривает наборы и композиции для выявления пациентов, чувствительных или реагирующих на ингибиторы ангиогенеза, в частности, бевацизумаб (Avastin®), установленных и определенных в соответствии со способами настоящего изобретения.
Ангиогенез является необходимым для развития рака, при этом он регулирует не только размер первичной опухоли и рост, но также влияет на инвазивный и метастатический потенциал. Соответственно, механизмы, опосредующие процессы ангиогенеза были исследованы как потенциальные мишени для направленной антираковой терапии. Ранее при изучении модуляторов ангиогенеза было показано, что сигнальный путь фактора роста эндотелия сосудов (англ. vascular endothelial growth factor, VEGF) преимущественно регулирует активность ангиогенеза в различных типах рака, и были разработаны различные способы терапии для модулирования различных этапов этого пути. Среди прочего, такие способы терапии включают бевацизумаб, сунитиниб, сорафениб и ваталаниб. Хотя применение ингибиторов ангиогенеза в клинической практике оказалось успешным, не все пациенты реагируют или полностью реагируют на терапию с помощью ингибиторов ангиогенеза. Механизм (механизмы), лежащий в основе такого неполного ответа, не известен. Таким образом, существует растущая потребность выявления подгрупп пациентов, чувствительных или реагирующих на антиангиогенезную раковую терапию.
Хотя известен целый ряд ингибиторов ангиогенеза, наиболее выдающимся ингибитором ангиогенеза является бевацизумаб (Авастин, Avastin®). Бевацизумаб представляет собой рекомбинантное гуманизированное моноклональное антитело lgG1, которое специфично связывается и блокирует биологическое действие VEGF (фактора роста эндотелия сосудов). VEGF является ключевым фактором опухолевого ангиогенеза - ключевого процесса, требующегося для роста опухоли и образования метастазов, т.е. распространения опухоли в другие части тела. Авастин® был одобрен в Европе для лечения поздних стадий четырех наиболее распространенных типов рака: колоректального рака, рака молочной железы, немелкоклеточного рака легких (НРЛ) и рака почки, которые в совокупности вызывают более 2,5 миллионов смертей в год. В США Авастин® был первым антиангиогенезным терапевтическим средством, утвержденным FDA, и в настоящее время одобрен для лечения пяти типов опухолей: колоректального рака, немелкоклеточного рака легких, рака молочной железы, рака головного мозга (глиобластомы) и рака почки (почечно-клеточный рак). К настоящему времени более полумиллиона пациентов прошли лечение Авастином, и существует крупномасштабная исследовательская программа, включающая более 450 клинических исследований, направленная на изучение дальнейшего применения Авастина для лечения различных типов рака (в том числе колоректального рака, рака молочной железы, немелкоклеточного рака легких, рака головного мозга, рака желудка, рака яичников и простаты) в различных условиях (например, на поздней или ранней стадии заболевания). Важно отметить, что Авастин® продемонстрировал перспективность применения в качестве сотерапевтического средства, демонстрируя эффективность в сочетании с широким спектром химиотерапевтических препаратов и других противораковых способов лечения. Из литературы известны исследования фазы III, демонстрирующие положительный эффект сочетания бевацизумаба со стандартными схемами химиотерапии (см, например, Saltz et al., 2008, J. Clin. Oncol., 26:2013-2019; Yang et al., 2008, Clin. Cancer Res., 14:5893-5899; Hurwitz et al., 2004, N. Engl. J. Med., 350:2335-2342). Однако, как и в предыдущих исследованиях ингибиторов ангиогенеза, некоторые из этих исследований фазы III показали, что часть пациентов не полностью реагируют на добавление бевацизумаба (Авастин®) к химиотерапевтическому режиму лечения.
Соответственно, существует потребность в способах определения тех пациентов, которые реагируют или могут реагировать на комбинированную терапию, содержащую ингибиторы ангиогенеза, в частности, бевацизумаб (Avastin®). Таким образом, техническая проблема, лежащая в основе настоящего изобретения, представляет собой создание способов и средств идентификации пациентов, страдающих или предрасположенных к развитию рака желудочно-кишечного тракта, в частности мКРР, которые могут извлечь пользу от добавления ингибиторов ангиогенеза, в частности бевацизумаба (Avastin®), к химиотерапевтическим схемам лечения, например, лечению с помощью ингибиторов на основе оксалиплатина.
Техническая проблема решена с помощью вариантов воплощения настоящего изобретения, охарактеризованных в пунктах формулы изобретения.
Настоящее изобретение, таким образом, обеспечивает способ улучшения лечебного эффекта химиотерапии у пациента, страдающего раком желудочно-кишечного тракта, в частности, мКРР, с помощью добавления бевацизумаба к вышеупомянутой схеме химиотерапии, при этом указанный способ включает:
(а) определение уровня экспрессии одного или более из VEGFA, HER2 и нейропилина; и
(б) введение бевацизумаба в комбинации с химиотерапевтическим режимом лечения пациенту, имеющему повышенный уровень VEGFA, и/или пониженный уровень HER2 и/или нейропилина, относительно контрольных уровней, определенных у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР.
Настоящее изобретение относится к способу улучшения лечебного эффекта химиотерапии у пациента, страдающего раком желудочно-кишечного тракта, в частности, мКРР, с помощью добавления бевацизумаба к химиотерапевтическому режиму лечения, при этом указанный способ включает:
(а) получение образцов тканей от указанного пациента;
(б) определение уровня экспрессии одного или более из VEGFA, HER2, и нейропилина;и
(в) введение бевацизумаба в комбинации с химиотерапевтическим режимом лечения пациенту, имеющему повышенный уровень VEGFA, и/или пониженный уровень HER2 и/или нейропилина относительно контрольных уровней, определенных у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР.
Настоящее изобретение, таким образом, обеспечивает способ повышения выживаемости без прогрессирования заболевания у пациента, страдающего раком желудочно-кишечного тракта, в частности, мКРР, с помощью добавления бевацизумаба к схеме химиотерапии, при этом указанный способ включает:
(а) определение уровня экспрессии одного или более из VEGFA, HER2 и нейропилина; и
(б) введение бевацизумаба в комбинации с химиотерапевтическим режимом лечения пациентам, имеющим повышенный уровень VEGFA, и/или пониженный уровень HER2 и/или нейропилина относительно контрольных уровней, определенных у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР.
Настоящее изобретение, таким образом, представляет способ повышения выживаемости без прогрессирования заболевания пациента, страдающего раком желудочно-кишечного тракта, в частности, мКРР, с помощью добавления бевацизумаба к схеме химиотерапии, при этом указанный способ включает:
(а) получение образцов тканей от вышеупомянутых пациентов;
(б) определение уровня экспрессии одного или более из VEGFA, HER2, и нейропилина; и
(в) введение бевацизумаба в комбинации с химиотерапевтическим режимом лечения пациентам, имеющим повышенный уровень VEGFA, и/или пониженный уровень HER2 и/или нейропилина относительно контрольных уровней, определенных у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР.
В другом варианте воплощения, настоящее изобретение относится к способу in vitro определения у пациента чувствительности или способности реагировать на добавление бевацизумаба к химиотерапевтической схеме, при этом указанный способ включает:
(а) получение образцов ткани пациентов, страдающих или предрасположенных к раку желудочно-кишечного тракта, в частности, к мКРР; и
(б) определение уровня экспрессии одного или более из VEGFA, HER2 и нейропилина;
при этом увеличение уровня VEGFA и/или понижение уровня HER2 и/или нейропилина относительно контрольного уровня, определенного у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, свидетельствует о чувствительности пациента к добавлению бевацизумаба к вышеупомянутой схеме лечения.
В качестве альтернативы или дополнения к определению уровня экспрессии одного или более из VEGFA, HER2 и нейропилина согласно способам, описанным в настоящей заявке, число сосудов в образце опухоли, относительно контрольного уровня (уровней), определенного у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, может быть определено как биомаркер, указывающий на пациента, чувствительного или реагирующего на добавление ингибиторов ангиогенеза, например, бевацизумаба (Авастин®), к стандартной химиотерапии. Таким образом, способы реализации настоящего изобретения включают определение числа сосудов в указанном образце, при этом определение количества сосудов известно или может быть известным специалисту, например, из образцов твердых тканей, таких как биоптаты тканей и/или образцов, взятых при резекции тканей. Определение числа сосудов может быть выполнено любым способом, описанным в настоящей заявке или известным в данной области техники для подобных измерений. Примером способа определения числа сосудов является детекция маркеров эндотелиальных клеток с помощью одного или более антител, специфичных к одному или более маркерам эндотелиальных клеток. В предпочтительных вариантах реализации биомаркер эндотелиальных клеток не экспрессируется в опухолевых клетках. Так как структура сосуда формируется из эндотелиальных клеток, один или более маркеров эндотелиальных клеток характеризует структуру сосуда из опухоли, что позволяет быстро определить число сосудов. Специалист, например, патологоанатом, сможет быстро определить оба антитела, применимых для детекции/распознавания эндотелиальных клеток (в частности, относящихся к опухолевым клеткам), а также способы выявления подобных антител и последующий анализ образца. Анализ образца в соответствии со способами настоящего изобретения может быть ручным, например, выполненным специалистом, например, патологоанатомом, как известно в данной области техники, или может быть автоматизирован с применением коммерчески доступного программного обеспечения для обработки и анализа картин патологий, например, для определения числа сосудов или для другого анализа тканей биопсии или резекций (например, MIRAX SCAN, Carl Zeiss AG, Jena, Germany).
Типичным антигеном, узнаваемым в качестве маркера эндотелиальных клеток, применяемым для определения числа сосудов в соответствии со способами настоящего изобретения, является CD31. Антиген CD31 узнается, например, с помощью антител клона JC70A из Dako A/S (Glostrup, Denmark) под номером М0823, применение которых входит в способы по настоящему изобретению. Таким образом, изобретение включает определение опухоль-специфичного уровня экспрессии или паттерна экспрессии CD31 в образцах тканей пациентов (1) в качестве показателя чувствительности или реагирования вышеупомянутых пациентов на добавление бевацизумаба к схеме химиотерапии, или (2) как часть способа повышения выживаемости без прогрессирования заболевания вышеупомянутого пациента, при этом такой пациент страдает или предположительно страдает от рака желудочно-кишечного тракта, в частности, мКРР. Поскольку CD31 маркирует эндотелиальные клетки, и большее число сосудов коррелирует с большим числом эндотелиальных клеток, число сосудов в образце также напрямую связано с опухоль-специфичным уровнем экспрессии CD31. Таким образом, изобретение включает способы повышения выживаемости без прогрессирования болезни пациента, страдающего раком желудочно-кишечного тракта, включающие определение опухоль-специфичного числа сосудов и/или опухоль-специфичного уровня экспрессии CD31 у вышеупомянутых пациентов и применение бевацизумаба в комбинации со схемой химиотерапии пациента, имеющего увеличенное число сосудов (и/или повышенную экспрессию CD31) относительно контрольного уровня, определенного у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР. Кроме того, изобретение включает способ in vitro выявления пациента, реагирующего или чувствительного к добавлению бевацизумаба к схеме химиотерапии, включающий определение опухоль-специфичного числа сосудов и/или опухоль-специфичного уровня экспрессии CD31 у вышеупомянутого пациента, в соответствии с которым повышенное число сосудов (и/или повышенный уровень экспрессии CD31) в опухолевых образцах вышеупомянутого пациента относительно контрольного уровня, определенного у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, является ииндикатором чувствительности пациента к добавлению бевацизумаба к вышеупомянутой схеме.
Соответственно, настоящее изобретение решает определенные технические проблемы, неожиданно показавшие, что опухоль-специфичный уровень экспрессии одного или более из VEGFA, HER2 и нейропилина у конкретного пациента относительно контрольного уровня, определенного у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, коррелирует с лечебным эффектом у пациентов, которым вводили ингибитор ангиогенеза в комбинации со схемой химиотерапии. В частности, неожиданно было выявлено, что изменение опухоль-специфичного уровня экспрессии VEGFA, HER2 и/или нейропилина является маркером/предвестником повышения выживаемости без прогрессирования болезни у пациентов с раком желудочно-кишечного тракта в ответ на добавление бевацизумаба (Авастин®) к оксалиплатиновой схеме химиотерапии. Было обнаружено, что у пациентов, проявляющих ответ или чувствительность к добавлению бевацизумаба (Авастин®) к схеме химиотерапии, наблюдается повышенная экспрессия VEGFA и/или пониженная экспрессия нейропилина и пониженная экспрессия HER2 относительно контрольных уровней, определенных в образцах, полученных от пациентов с диагнозом метастатический рак желудочно-кишечного тракта. Более того, в дополнение к измененной экспрессии одного или более из VEGFA, HER2 и/или нейропилина, как описано в настоящей заявке, было неожиданно установлено, что увеличение опухоль-специфичного числа сосудов у конкретного пациента (которое коррелирует с опухоль-специфичным уровнем экспрессии одного или более маркеров эндотелиальных клеток, например, CD31) относительно контрольного уровня, определенного у пациентов с диагнозом рак желудочно-кишечного тракта, в частности мКРР, коррелирует с уровнем (1) одного из маркеров/предвестников для повышения выживаемости без прогрессирования заболевания, и/или (2) одного из маркеров/ предвестников, который коррелирует с лечебным эффектом у пациентов с раком желудочно-кишечного тракта, получавшим ингибиторы ангиогенеза в комбинации со схемой химиотерапии. Термины "маркер" и "предвестник" могут быть использованы как взаимозаменяемые и относятся к уровням экспрессии одного или более из VEGFA, HER2 и/или нейропилина, как описано в настоящей заявке. В дополнение к уровню экспрессии одного или более из VEGFA, HER2 и/или нейропилина, в настоящем изобретении также используются термины "маркер" и "предвестник", относящиеся к опухоль-специфичному числу сосудов и/или опухоль-специфичному уровню экспрессии маркеров эндотелиальных клеток, например, CD31, в соответствии с описанными в настоящей заявке способами. Изобретение также включает использование терминов "маркер" и "предвестник" в отношении комбинирования любых двух или более опухоль-специфичных уровней экспрессии VEGFA, HER2 и/или нейропилина и опухоль-специфичного числа сосудов.
В контексте настоящего изобретения "VEGFA" относится к белковому фактору роста эндотелия сосудов А, примером которого является SEQ ID NO:1, показанная на Фигуре 6. Термин "VEGFA" включает белок, имеющий аминокислотную последовательность SEQ ID NO:1, а также его гомологи и изоформы. Термин "VEGFA" также включает известные изоформы, например, VEGF121, VEGF145, VEGF165, VEGF189 и VEGF206, а также варианты, гомологи и их изоформы. В контексте настоящего изобретения термин "VEGFA" также включает белки, имеющие не менее 85%, не менее 90% или не менее 95% гомологии аминокислотной последовательности SEQ ID NO:1, или аминокислотным последовательностям вариантов и/или их гомологов, также фрагменты последовательностей, при условии, что различные белки (включая изоформы), гомологичные белки и/или фрагменты узнаются одним или несколькими VEGFA-специфичными антителами, такими как антитела клона SP28, доступные от Abeam, Inc (Cambridge, Massachusetts, U.S.A.).
В контексте настоящего изобретения "HER2" относится к трансмембранному белку первого типа, известному также как c-erbB2, ErbB2 или Neu, принадлежащему к семейству рецепторов эпидермального фактора роста, примером которого является аминокислотная последовательность SEQ ID NO:2, показанная на Фигуре 7. В контексте настоящего изобретения термин "HER2" также включает гомологов, варианты и изоформы, в том числе сплайсированные изоформы HER2. Термин "HER2" также включает белки, имеющие не менее 85%, не менее 90% или не менее 95% гомологии аминокислотной последовательности SEQ ID NO:2 или последовательности одного или нескольких HER2 гомологов, вариантов и изоформ, а также фрагменты последовательностей, при условии, что варианты белков (включая изоформы), гомологичные белки и/или фрагменты узнаются одним или несколькими НЕР2-специфичными антителами, например, поставляемыми в виде препарата Herceptest™, доступного от Dako A/S (Glostrup, Denmark). НЕР2-специфичные антитела, например, в указанном препарате Herceptest™, являются аффинно очищенными антителами кролика к синтетическому C-концевому внутрицитоплазматическому фрагменту человеческого белка HER2 (иммуноген объединен с гемоцианином моллюска). Другие примеры антител к HER2, которые являются коммерчески доступными и удобными для применения согласно способам настоящего изобретения, включают, но не ограничены перечисленными: клон 4 В5, доступный от Ventana Medical Systems S.A. (Illkirch, France); один или несколько клонов СВ11, 5А2, 10А7, и СВЕ, доступных от Novocastra/Leica GmbH (Wetzler, Germany); клон SP3, доступный от Thermo Fisher Scientific (Fremont, CA, USA) и клон ТАВ250, доступный от Invitrogen™ (Carslbad, CA, USA).
В контексте настоящего изобретения "нейропилин" относится к белку нейропилину-1, мембранному белку типа I, известному также как NRP-1, примером которого является аминокислотная последовательность SEQ ID NO:3, показанная на Фигуре 8. При использовании в настоящей заявке, "нейропилин" может также относиться к нейропилину-2/МРР-2, который имеет 44% гомологии с NRP-1, как известно в данной области техники. В контексте настоящего изобретения термин "нейропилин" также включает гомологов, варианты и изоформы NRP-1 и/или NRP-2. Кроме того, термин "нейропилин" включает белки, имеющие не менее 85%, не менее 90% или не менее 95% гомологии аминокислотной последовательности SEQ ID NO:1 или последовательности одного или нескольких NRP-1 и/или NRP-2 гомологов, вариантов и изоформ, включая сплайсированные изоформы, а также фрагменты последовательностей при условии, что различные белки (включая изоформы), гомологичные белки и/или фрагменты узнаются с помощью одного или более специфичных к NRP-1 и/или NRP-2 антитела, например, клон 446915, доступный из R&D Systems, Inc. (Minneapolis, Minnesota, U.S.A.).
В качестве альтернативы или дополнения к определению опухоль-специфичного уровня экспрессии одного или более из VEGFA, HER2 и нейропилина, изобретение также включает определение числа сосудов как один из биомаркеров для применения в способах, описанных в настоящей заявке. Как известно в данной области и как описано здесь, число сосудов в образце ткани пациента, например, в образце, содержащем опухолевые ткани, может быть, например, изучено с помощью иммуно-гистохимических методов детекции одного или нескольких маркеров эндотелиальных клеток, например, CD31. CD31 известен как маркер эндотелиальных клеток, который можно применять для определения числа сосудов в опухолевых образцах тканей и, обычно, его выявляют с применением специфичных антител, таких как например антитело к CD31, доступное от Dako A/S (Glostrup, Denmark) клона JC70A под номером М0823. В качестве альтернативы или в дополнение к определению опухоль-специфичного уровня экспрессии одного или более из VEGFA, HER2 и нейропилина, настоящее изобретение, помимо того, включает применение Dako A/S антител клона JC70A (product number M0823) для определения числа сосудов, идентификации эндотелиальных клеток и/или определения уровня экспрессии маркеров эндотелиальных клеток в соответствии со способами, описанными в настоящей заявке.
Соответственно, настоящее изобретение включает определение уровней экспрессии белков, включающих аминокислотные последовательности, описанные в настоящей заявке, но не ограничивается ими. В этом контексте настоящее изобретение включает определение гомологов, вариантов и изоформ одного или более из VEGFA, HER2 и нейропилина; вышеупомянутые изоформы или варианты могут в числе других включать аллельные варианты или сплайсированные варианты. Предусмотрено также определение белков, которые являются гомологичными одному или более из VEGFA, HER2 и нейропилина, описанных в настоящей заявке, или их фрагментам, например, имеющих по меньшей мере 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичности аминокислотным последовательностям SEQ ID NO:1, SEQ ID NO:2 или SEQ ID NO:3 или их фрагментам. В качестве альтернативы или дополнения, настоящее изобретение включает определение уровней экспрессии белков, кодируемых нуклеотидными последовательностями или их фрагментами, которые по меньшей мере на 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% и 99% идентичны нуклеотидным последовательностям, кодирующим SEQ ID NO:1, SEQ ID NO:2 или SEQ ID NO:3 или их фрагментам, вариантам или изоформам. В контексте настоящего изобретения термин "вариант" означает, что аминокислотная последовательность VEGFA, HER2 и/или нейропилина или нуклеотидная последовательность, кодирующая указанную аминокислотную последовательность, отличается от определенной последовательности, идентифицированной как SEQ ID NO:1, SEQ ID NO:2 или SEQ ID NO:3 и/или доступной под вышеуказанными номерами доступа в базе GenBank, и образуется в результате мутаций, например, делеций, добавлений, замен, инверсий и т.д. Кроме того, термин "гомолог" относится к молекулам, имеющим по меньшей мере 60%, предпочтительно по меньшей мере 80% и наиболее предпочтительно по меньшей мере 90% идентичности последовательности одного или нескольких полипептидов, как показано в SEQ ID NO:1, SEQ ID NO:2 или SEQ ID NO:3 или их фрагменту (фрагментам).
Кроме того, изобретение включает определение числа сосудов в образцах ткани пациентов, которое коррелирует с опухоль-специфичной экспрессией маркеров эндотелиальных клеток, известных в данной области техники, например, опухоль-специфичным уровнем экспрессии CD31. В этом контексте настоящее изобретение включает выявление гомологов, вариантов и изоформ одного или нескольких маркеров эндотелиальных клеток или их вариантов, и может, в частности, включать аллельные варианты или сплайсированные варианты маркеров эндотелиальных клеток. Предусмотрено также выявление белков, которые являются гомологичными одному или нескольким маркерам эндотелиальных клеток, известных в данной области, например, имеющим по меньшей мере 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% и 99% идентичности с аминокислотной последовательностью, известной в качестве маркера эндотелиальных клеток, или ее фрагменту, например, CD31 или его фрагменту. В качестве альтернативы или дополнения настоящее изобретение также включает определение уровней экспрессии белков, кодируемых нуклеотидными последовательностями или их фрагментами, которые являются по меньшей мере на 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны нуклеотидной последовательности, кодирующей маркер эндотелиальных клеток, например, CD31 или его фрагмент, вариант или изоформу.
Для определения степени идентичности аминокислотной или нуклеотидной последовательности к аминокислотной или нуклеотидной последовательности, описанной в настоящей заявке, профессионал может использовать средства и методы, известные для этих целей в данной области техники, например, выравнивание, либо вручную, либо с помощью компьютерных программ, широко известных или описанных в настоящей заявке.
В соответствии с настоящим изобретением термин "идентичность" или "процент идентичности" в контексте двух или нескольких аминокислотных или нуклеотидных последовательностей относится к двум или нескольким последовательностям или подпоследовательностям, которые являются схожими (например, 60% или 65% идентичности, предпочтительно 70-95% идентичности, предпочтительно по меньшей мере 95% идентичности аминокислотным последовательностям, например, SEQ ID NO:1, SEQ ID NO:2 или SEQ ID NO:3, или последовательностям, которые известны как маркеры эндотелиальных клеток, например, CD31) при сравнении и выравнивании с максимальным соответствием в окне сравнения или в обозначенной области, измеренной с помощью используемого последовательного алгоритма сравнения, общеизвестного в данной области, или с помощью ручного выравнивания или с помощью визуальной проверки. Последовательности, имеющие, например, от 60% до 95% или более идентичности, считаются в значительной степени идентичными. Такое определение распространяется также на последовательность, которая комплементарна анализируемой. Предпочтительно описанная идентичность существует в пределах участка, длина которого составляет по меньшей мере от 15 до 25 аминокислот или нуклеотидов, более предпочтительно, от 50 до 100 аминокислот или нуклеотидов. Специалистам в данной области техники известно, каким образом можно определить процент идентичности между/среди последовательностями, с помощью, например, алгоритмов, основанных к примеру на алгоритме CLUSTALW (Thompson Nucl. Acids Res. 2 (1994), 4673-4680) или FASTDB (Brutlag Сотр. Арр. Biosci. 6 (1990), 237-245) компьютерных программ, как известно в данной области техники.
Хотя алгоритм FASTDB обычно не учитывает внутренние несовпадающие делеции или добавления в последовательностях, то есть пробелы в расчетах, это можно исправить вручную во избежание завышенного % идентичности. ClustalW, наоборот, учитывает пробелы в последовательностях при расчете идентичности. Также специалистам в данной области доступны алгоритмы BLAST (от англ. Basic Local Alignment Search Tool, средство поиска основного локального выравнивания) и BLAST 2,0 (Altschul, 1997, Nucl. Acids Res. 25:3389-3402; Altschul, 1993 J. Mol. Evol. 36:290-300; Altschul, 1990, J. Mol. Biol. 215:403-410). Программа BLASTN для нуклеотидных последовательностей использует по умолчанию значение длины слова (W, word length), равное 11, ожидание (Е, expectation), равное 10, М=5, N=4 и сравнение обеих цепей. Для аминокислотных последовательностей программа BLASTP использует по умолчанию значение длины слова (W), равное 3, и ожидание (Е), равное 10. В расчетной матрице BLOSUM62 (Henikoff (1989) PNAS 89:10915) используется выравнивание (В), равное 50, ожидание (Е), равное 10, М=5, N=4 и сравнение обоих цепей.
Алгоритмы BLAST, рассмотренные выше, проводят выравнивание как аминокислотных, так и нуклеотидных последовательностей для определения сходства последовательностей. Благодаря локальному характеру выравниваний, BLAST является особенно полезным в определении точных совпадений или выявлении сходных последовательностей. Основной единицей алгоритма BLAST является пара сегментов с максимальным сходством (англ. High-scoring Segment Pair, HSP). HSP состоит из двух фрагментов последовательности произвольной, но одинаковой длины, выравнивание которых является максимальным и для которых расчет выравнивания соответствует или превышает пороговое значение, или минимально допустимый уровень, заданный пользователем. Подход BLAST предназначен для поиска HSP между анализируемой последовательностью и последовательностью из базы данных, для оценки статистической значимости найденных совпадений и сообщения только тех совпадений, которые удовлетворяют пороговым значениям, выбранным пользователем. Параметр Е устанавливает статистически значимый порог для сообщения совпадающих последовательностей из базы данных. Е определяют как верхнюю границу ожидаемой частоты вероятности возникновения HSP (или серий HSP) в контексте поиска по всей базе данных. Любая база данных последовательностей, сопоставление которой удовлетворяет Е, отмечается на выходных данных программы.
Аналогичные техники вычислений, использующие BLAST, можно применять для поиска идентичных или родственных молекул в белковых или нуклеотидных базах данных, таких как GenBank или EMBL. Этот анализ является более быстрым, чем множественные мембранные гибридизации. Кроме того, чувствительность компьютерного поиска можно модифицировать, чтобы определить относится ли конкретное совпадение к категории точных или схожих. В основе поиска лежит счет (балловый показатель), который определяется как:
% идентичности последовательности х % максимального счета BLAST 100
и учитывает как степень сходства между двумя последовательностями, так и длину совпадающей последовательности. Например, при определенном счете, равном 40, совпадение будет точным в пределах 1-2% ошибки, а при счете, равном 70, совпадение будет точным. Схожие молекулы обычно определяют, выбирая те последовательности, которые характеризуются счетом (балловым показателем) от 15 и 40, хотя и более низкий счет также может определить родственные молекулы. Другой пример программы, способной осуществлять выравнивание последовательностей, является компьютерная программа на основе CLUSTALW (Thompson, 1994, Nucl. Acids Res. 2:4673-4680) или FASTDB (Brutlag, 1990, Сотр. App.Biosci. 6:237-245), общеизвестная в данной области техники.
Опухоль-специфичные уровни экспрессии VEGFA, HER2 и/или нейропилина можно рассматривать отдельно как индивидуальные маркеры, или в группах из двух или более маркеров как экспрессионный профиль, для предсказания чувствительности пациента на добавление бевацизумаба к схеме химиотерапии. Таким образом, способы настоящего изобретения включают определение экспрессионного профиля, основанного на уровне экспрессии одного или нескольких маркеров. В качестве альтернативы или в дополнение к определению уровня экспрессии одного или нескольких VEGFA, HER2 и нейропилина в соответствии со способами, описанными в настоящей заявке, число сосудов в опухолевом образце ткани, относительно контрольного уровня (уровней), определенного у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, можно также применять как один или более биомаркер, указывающий на пациента, чувствительного или реагирующего на добавление ингибиторов ангиогенеза, например, бевацизумаба (Авастина®), к стандартной химиотерапии.
В соответствии с настоящим изобретением было неожиданно обнаружено в популяции N01966, что более высокий эффект лечения бевацизумабом связан с более высоким уровнем экспрессии CD31 (большим числом сосудов), более высоким уровнем экспрессии VEGFA, более низким уровнем экспрессии нейропилина и более низким уровнем экспрессии HER2 в опухолевых клетках
Уровень экспрессии одного или нескольких маркеров из VEGFA, HER2 и нейропилина может быть оценен любым способом, известным в данной области техники, подходящим для определения специфичного уровня белка в образце ткани пациента, и предпочтительно их определяют с помощью иммуно-гистохимических (ИГХ) методов, использующих антитела, специфичные для одного или более из VEGFA, HER2, нейропилина и/или CD31. Такие способы хорошо известны и являются стандартными в данной области, и соответствующие коммерческие антитела и/или наборы легкодоступны. Например, коммерчески доступные антитела/тестовые наборы для VEGFA, HER2, нейропилина и CD31 можно приобрести у Abeam, Inc (Cambridge, Massachusetts, U.S.A.) как клон SP28, у Dako A/S (Glostrup, Denmark) как Herceptest™, из R&D Systems, Inc. (Minneapolis, Minnesota, U.S.A.) как клон 446915, и у Dako A/S (Glostrup, Denmark) как клон JC70A, соответственно. Предпочтительно уровни экспрессии маркера/ индикаторных белков настоящего изобретения оценивают с использованием реагентов и/или протоколов, рекомендованных изготовителем антител или коммерческих наборов. Специалисту также известны другие способы определения уровня экспрессии одного или более из VEGFA, HER2, нейропилина с помощью ИГХ методов. Таким образом, уровень экспрессии одного или нескольких маркеров/индикаторов настоящего изобретения может быть рутинно и воспроизводимо определен специалистами в данной области без особых трудностей. Тем не менее, для обеспечения точных и воспроизводимых результатов изобретение также включает тестирование образцов тканей пациентов в специализированной лаборатории, в которой могут обеспечить проверку процедур тестирования.
Предпочтительно уровень экспрессии одного или более из VEGFA, HER2, нейропилина оценивают в биологическом образце, который содержит или, как предполагается, содержит раковые клетки. Образец может представлять собой образец, полученный при резекции желудочно-кишечных тканей, биоптат желудочно-кишечных тканей или метастатического поражения, полученный от пациента, страдающего или предположительно страдающего, или с диагнозом рак желудочно-кишечного тракта, в частности, мКРР. Предпочтительно образец представляет собой образец ткани прямой кишки, полученный при резекции образец или биоптат опухолевой ткани прямой кишки, установленного или предполагаемого метастатического раком желудочно-кишечного тракта поражение или срез, или пробу крови, например, пробу периферической крови, точно или предположительно содержащей циркулирующие раковые клетки, например, желудочно-кишечные раковые клетки. Образец может включать как раковые клетки, т.е. клетки опухоли, так и нераковые клетки, и, в предпочтительном варианте, включающий раковые и нераковые клетки. В аспектах изобретения, включающих определение числа сосудов в образце, образец содержит раковые/опухолевые клетки и нераковые клетки, представляющие собой эндотелиальные клетки. Специалист, например, патологоанатом, может быстро отличить раковые клетки от нераковых, например, эндотелиальных клеток, а также определить число сосудов в образце, например, с помощью окрашивания образца для детекции маркеров эндотелиальных клеток, например, CD31. В качестве альтернативы или в дополнение к прямому определению числа сосудов, может также быть определен уровень экспрессии одного или нескольких маркеров эндотелиальных клеток, например, CD31, который коррелирует с числом сосудов. Методы получения биологических образцов, включающих образцы, полученные при резекции тканей, биоптаты и жидкости организма, например, образцы крови, содержащие раковые/опухолевые клетки, хорошо известны в данной области техники.
В контексте настоящего изобретения бевацизумаб следует вводить в качестве дополнения или совместного лечения с одним или несколькими химиотерапевтическими агентами, вводимыми как часть стандартной химиотерапевтической схемы, известными в данной области. Примеры таких химиотерапевтических агентов включают 5-фторурацил, лейковорин, иринотекан, гемцитабин-эрлотиниб, капецитабин и химиотерапевтические агенты на основе платины, такие как паклитаксел, карбоплатин и оксалиплатин. Пример стандартной химиотерапевтической схемы лечения с комбинацией иринотекана, 5-фторурацила и лейковорина, также известной как IFL. Как показано в прилагаемых примерах, добавление бевацизумаба к оксалиплатиновой схеме химиотерапии влияет на повышение выживаемости без прогрессирования болезни пациентов и/или популяции пациентов, определенной и выбранной в соответствии с уровнем экспрессии одного или более из VEGFA, HER2, нейропилина и CD31.
Таким образом, бевацизумаб может быть комбинирован с оксалиплатиновой схемой химиотерапии. Примеры оксалиплатиновой схемы химиотерапии включают комбинацию оксалиплатина, лейковорина и 5-фторурацила, известные как схемы FOLFOX4 (см., например, de Gramont et al., 2000, J. Clin. Oncol. 18:2938-2947) и комбинацию оксалиплатина и капецитабина, известные как схемы XELOX (см., например, Cassidy et al., 2004, J. Clin. Oncol. 22:2084-2091). В некоторых аспектах изобретения пациента, выявленного в соответствии со способами настоящего изобретения, лечат бевацизумабом в комбинации со схемами FOLFOX4 или XELOX. Общие способы введения включают парентеральное введение в виде болюсной дозы или как инфузию в течение установленного периода времени, например, введение общей суточной дозы в течение 10 мин, 20 мин, 30 мин, 40 мин, 50 мин, 60 мин, 75 мин, 90 мин, 105 мин, 120 мин, 3 час., 4 час.. 5 час или 6 часов. Например, 7.5 мг/кг бевацизумаба (Авастина®) могут быть введены пациенту с раком ободочной и прямой кишки в виде внутривенной инфузии в течение от 30 до 90 минут каждые три недели как часть XELOX схемы, или доза 5 мг/кг как внутривенная инфузия в течение 2 часов каждые две недели как часть FOLFOX4 схемы (см., например, Saltz et al., 2008, J. Clin. Oncol. 26:2013-2019). Специалисту в данной области техники очевидно, что дальнейшие способы введения бевацизумаба включены в изобретение и определяются для конкретного пациента и химиотерапевтической схемы, и что конкретный способ введения и терапевтическая доза лучше всего определяется лечащим врачом в соответствии с методами, общеизвестными в этой области.
Пациентов, выбранных в соответствии со способами настоящего изобретения, лечат бевацизумабом в комбинации с химиотерапевтической схемой, и они могут впоследствии дополнительно получить одну или несколько противораковых терапий. В некоторых аспектах изобретения одной или несколькими противораковыми терапиями является облучение.
В предпочтительных вариантах реализации образцы от пациентов собирают до начала любых других химиотерапевтических схем или терапий, например, терапия лечения рака или управление, или улучшение его симптомов. Таким образом, в предпочтительном варианте реализации образцы собирают перед введением химиотерапевтических агентов или перед началом химиотерапевтической схемы.
Настоящее изобретение также относится к диагностической композиции или набору, включающему олигонуклеотиды или полипептиды, применимые для определения уровня экспрессии одного или более из VEGFA, HER2 и нейропилина. В качестве альтернативы или дополнительно к олигонуклеотидам или полипептидам, применимым для определения уровня экспрессии одного или более из VEGFA, HER2 и нейропилина, как описано в настоящей заявке, набор или диагностическая композиция настоящего изобретения может также содержать олигонуклеотиды или полипептиды для определения и/или детекции маркера эндотелиальных клеток, например, CD31, в качестве средства определения числа сосудов, как описано в настоящей заявке. Как детально описано в настоящей заявке, олигонуклеотиды, такие как зонды на основе ДНК, РНК или смеси ДНК и РНК можно применять для детекции уровней мРНК маркеров/индикаторных белков, тогда как полипептиды можно применять для обнаружения непосредственно уровней маркеров/индикаторных белков с помощью специфических белок-белковых взаимодействий. В предпочтительных аспектах изобретения полипептиды, используемые как зонды для определения уровней экспрессии одного или более из VEGFA, HER2 и нейропилина (и/или одного или нескольких маркеров эндотелиальных клеток, например, CD31) и входящие в состав наборов или диагностических композиций, описанных в настоящей заявке, представляют собой антитела, специфичные для этих белков, или специфичные для гомологов и/или их укороченных вариантов.
Соответственно в дальнейшем воплощении настоящее изобретение предусматривает наборы, применимые для осуществления способов, описанных в настоящей заявке, включающих олигонуклеотиды или полипептиды, способные определять уровень экспрессии одного или более из VEGFA, HER2 и нейропилина (и/или маркеров эндотелиальных клеток, например, CD31).
Предпочтительно олигонуклеотиды содержат праймеры и/или зонды, специфичные к мРНК, кодирующей один или несколько маркеров/индикаторов, описанных в настоящей заявке, а полипептиды содержат белки, способные специфически взаимодействовать с маркером/индикаторными белками, например, маркером/индикатором специфических антител или фрагментов антител.
В еще одном в арианте настоящее изобретение относится к применению бевацизумаба для повышения выживаемости без прогрессирования болезни пациентов, страдающих раком желудочно-кишечного тракта, в частности, мКРР, включающего следующие этапы:
(а) получение образцов тканей от указанных пациентов;
(б) определение уровня экспрессии одного или более из VEGFA, HER2 и нейропилина; и
(в) введение бевацизумаба в комбинации со схемой химиотерапии пациентам с повышенным уровнем VEGFA и/или CD31, и/или пониженным уровнем HER2 и/или нейропилина относительно контрольных уровней, определенных у пациентов, страдающих раком желудочно-кишечного тракта, в частности, мКРР.
Как показано в прилагаемых примерах, настоящее изобретение решает определенные технические проблемы, неожиданно было обнаружено, что уровни экспрессии одного или более из VEGFA, HER2 и нейропилина у конкретного пациента относительно контрольных уровней, определенных у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, коррелируют с лечебным эффектом у пациентов, принимающих бевацизумаб в комбинации с оксалиплатиновой схемой химиотерапии. В контексте изобретения было также установлено, что повышенное число опухоль-специфичных сосудов относительно контрольных уровней, определенных у пациентов с диагнозом рак желудочно-кишечного тракта, в частности, мКРР, также коррелирует с лечебным эффектом у пациентов, получающих бевацизумаб в комбинации с оксалиплатиновой схемой химиотерапии.
Термин "реагировать на" в контексте настоящего изобретения указывает на то, что субъект/пациент, страдающий, предположительно страдающий или предрасположенный к раку желудочно-кишечного тракта, в частности, мКРР, проявляет ответную реакцию на химиотерапевтическую схему, включающую дополнительно бевацизумаб. Специалист легко определит, есть ли реакция у человека, получающего лечение бевацизумабом в соответствии со способами настоящего изобретения. Например, ответ может отражать снижение страданий от рака желудочно-кишечного тракта, таких как уменьшение и/или остановка роста опухоли, уменьшение размера опухоли и/или облегчение одного или нескольких симптомов рака желудочно-кишечного тракта, например, кровотечения желудочно-кишечного тракта, боли, анемии. Предпочтительно ответ может отражать снижение или уменьшение показателей метастатических образований рака желудочно-кишечного тракта или индексов мКРР, например, предотвращение образования метастазов или сокращение численности или размера метастазов.
Термин "чувствительность" в контексте настоящего изобретения указывает на то, что субъект/пациент, страдающий, предположительно страдающий или предрасположенный к раку желудочно-кишечного тракта, в частности, мКРР, показывает в некотором роде положительную реакцию в ответ на бевацизумаб в комбинации с химиотерапевтической схемой. Реакция пациента может быть менее выражена по сравнению с пациентом "реагирующим на", как было описано выше. Например, пациент может испытывать меньше страданий, связанных с болезнью, хотя и без снижения роста опухоли или метастатического показателя и/или реакция пациента на бевацизумаб в комбинации с химиотерапией может иметь лишь переходный характер, т.е. рост опухоли и/или метастазы может быть временно уменьшен или приостановлен.
Термин "пациент, страдающий от" в соответствии с изобретением относится к пациенту, имеющему клинические признаки рака желудочно-кишечного тракта, в частности, мКРР, Термин "быть восприимчивым к" или "быть предрасположенным к " в контексте рака желудочно-кишечного тракта относится к указаниям на болезнь пациента, основанную, например, на генетической предрасположенности, до или при возможном воздействии опасных и/или канцерогенных соединений или воздействия канцерогенных физических факторов, таких как радиация.
Термин "выживаемость без прогрессирования заболевания" в контексте настоящего изобретения относится к отрезку времени, в ходе и после лечения, в течение которого согласно оценке лечащего врача или исследователя, болезнь пациента не ухудшается, т.е. не прогрессирует. Специалист сможет оценить, является ли выживаемость без прогрессирования болезни пациента улучшенной или усиленной, если у пациента в течение долгого отрезка времени заболевание не прогрессирует по сравнению со средним значением или опытным значением времени выживаемости без прогрессирования болезни в контрольной группе таких же пациентов.
Термин "введение", используемый в настоящей заявке, означает введение ингибитора ангиогенеза, например, бевацизумаба (Авастина®) и/или фармацевтической композиции/лечебной схемы, включающей ингибитор ангиогенеза, такой как бевацизумаб (Авастин®), пациенту, нуждающемуся в таком лечении или в медицинском вмешательстве, любым подходящим для введения терапевтических антител способом, известным в данной области техники,. Не ограниченные перечисленными способы введения включают оральное, внутривенное, внутрибрюшинное, подкожное, внутримышечное, местное, интраназальное или внутрибронхиальное введение (например, путем ингаляции). Особенно предпочтительным в контексте настоящего изобретения является парентеральное введение, например, внутривенное введение. Касательно бевацизумаба (Авастина®) для лечения рака прямой кишки, предпочтительными дозами в соответствии с ЕМЕА являются дозы 5 мг/кг или 10 мг/кг массы тела один раз каждые 2 недели или 7.5 мг/кг или 15 мг/кг массы тела один раз каждые 3 недели (более подробную информацию см. http://www.ema. europa.eu/docs/en_GB/document_library/EPAR_-_Product_lnformation/human/000582/WC500029271.pdf (см. 2 стр, снизу, ранее доступная ссылка http://www.emea.europa.eu/humandocs/PDFs/EPAR/avastin/emea-combined-h582en.pdf).
Термин "антитело" в настоящей заявке используется в широком смысле и включает, но не ограничен перечисленными, моноклональные и поликлональные антитела, полиспецифичные антитела (например, двухспецифичные антитела), химерные антитела, антитела с пересаженными гипервариабельными участками, гуманизированные антитела, камелизированные антитела, одноцепочечные антитела и фрагменты антител, и сконструированные фрагменты, например, F(ab')2 фрагменты, Fab-фрагменты, Fv-фрагменты, одноцепочечные Fv-фрагменты (scFvs), двухспецифичные scFvs, диатела (diabodies), однодоменные антитела (dAbs) и минитела, которые проявляют желаемую биологическую активность, в частности, специфическое связывание с одним или более из VEGFA, HER2, нейропилина и CD31, или с их гомологами, вариантами, фрагментами и/или их изоформами.
Используемый в настоящей заявке термин "химиотерапевтическое средство" включает любой активный агент, который может обеспечить противораковый терапевтический эффект и может представлять собой химический агент или биологический агент, в частности, который способен влиять на раковые или опухолевые клетки. Предпочтительно активными агентами являются те, которые выступают в качестве антинеопластичных (хемотоксических и хемостатических) агентов, которые ингибируют или предотвращают развитие, созревание и распространение злокачественных клеток. Не ограниченные перечисленными примерами химиотерапевтические агенты включают алкилирующие агенты, такие как азотистый иприт (например, мехлоретамин, циклофосфамид, ифосфамид, мелфалан и хлорамбуцил), нитрозомочевину (например, кармустин (BCNU), ломустин (CCNU), и семустин (метил-CCNU)), этиленимины/метилмеламины (например, триэтиленмеламин (ТЕМ), триэтилен, тиофосфор амид (тиотепа), гексаметилмеламин (НММ, альтретамин)), алкил сульфонаты (наприм, бусульфан) и триазины (например, дакарбазин (DTIC)); антиметаболиты, такие как аналоги фолиевой кислоты (например, метотрексат, триметрексат), аналоги пиримидина (например, 5-фторурацил, фтордезоксиуридин, гемцитабин, цитозинарабинозид (AraC, цитарабин), 5-азацитидин, 2,2'-дифтордезоксицитидин) и аналоги пурина (например, 6-меркаптопурин, 6-тиогуанин, азатиоприн, 2'-дезоксикоформицин (пентостатин), эритрогидроксинониладенин) (EHNA), флударабин фосфат и 2-хлородезоксиаденозин (кладрибин, 2-CdA); антимитотические препараты, выделенные из натуральных продуктов (например, паклитаксел, алкалоиды барвинка (например, винбластин (VLB)), винкристин и винорелбин), таксотер, эстрамустин и эстрамустин фосфат), эпиподофилотоксин (например, этопозид, тенипозид), антибиотики (например, актиномицин Д, дауномицин (рубидомицин), доксорубицин, митоксантрон, идарубицин, блеомицин, пликамицин (митрамицин), митомицин С, актиномицин), ферменты (например, L-аспарагиназа) и модуляторы биологической активности (например, интерферон-альфа, IL-2, G-CSF, GM-CSF), различные агенты, включая координационные соединения платины (например, цисплатин, карбоплатин), антраценедионы (например, митоксантрон), замещенные мочевины (т.е. гидроксимочевины), метилгидразиновые производные (например, N-метилгидразин (MIH), прокарбазин), адренокортикальные супрессанты (например, митотан (o,p'-DDD), аминоглутетимид), гормоны и антагонисты, включая адренокортикостероидные антагонисты (например, преднизон и его эквиваленты, дексаметазон, аминоглутетимид), прогестины (например, гидрогсипрогестерона капроат, медроксипрогестерона ацетат, мегестрола ацетат), эстрогены (например, диэтилстилбестрол, этинил эстрадиол и их эквиваленты), антиэстрогены (например, тамоксифен), андрогены (например, тестостерон пропионат, флюоксиместерон и их эквиваленты), антиандрогены (например, флутамид, аналог гонадотропин-рилизинг-гормона, лейпролид) и нестероидные антиандрогены (например, флутамид).
В контексте настоящего изобретения под "гомологией" относящейся к аминокислотной последовательности понимают идентичность последовательностей, составляющую по меньшей мере 80%, в частности, идентичность по меньшей мере 85%, предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95% по всей длине к последовательности, определенной в SEQ ID NOs настоящей заявки. В контексте настоящего изобретения, как понятно для специалиста, гомология включает дальнейшие аллельные варианты маркеров/индикаторных белков в различных популяциях и этнических группах.
В настоящей заявке термин "полипептид" относится к пептиду, белку, олигопептиду или полипептиду, который включает аминокислотные цепи заданной длины, в которых аминокислотные остатки связаны ковалентными пептидными связями. Кроме того, изобретением также предусмотрены пептидомиметики таких белков/полипептидов, в которых аминокислота (аминокислоты) и/или пептидная связь (связи) заменены на функциональные аналоги, например, на другой аминокислотный остаток, не относящийся к 20 кодируемым генами аминокислотам, например, селенцистеин. Пептиды, олигопептиды и белки могут быть названы полипептидами. Термины полипептид и белок используются в настоящей заявке взаимозаменяемо. Термин полипептид также относится и не исключает модификации полипептида, например, гликозилированию, ацетилированию, фосфорилированию и тому подобному. Такие модификации хорошо описаны в монографиях, а также в огромном количестве исследовательской литературы.
Термины "лечение" используют в настоящей заявке относительно реабилитации, улучшения, уменьшения тяжести симптомов или сокращения времени течения болезни или любого параметра, или его симптомов. Предпочтительно вышеупомянутый пациент является человеком и рассматриваемая болезнь является раком желудочно-кишечного тракта, в частности, мКРР. Термины "определение" или "оценка" такого пациента относятся к способам определения уровня экспрессии одного или нескольких маркеров/ индикаторных белков, описанных в настоящей заявке, включая VEGFA, HER2, нейропилин и CD31, и/или к селекции пациентов, основанной на уровнях экспрессии таких маркеров/индикаторных белков относительно контрольных уровней, полученных у пациентов с диагнозом метастатический рак ободочной и прямой кишки.
В дополнение к способам, описанным выше, изобретение также включает дальнейшие иммуногистохимические способы оценки уровня экспрессии одного или нескольких VEGFA, HER2 и нейропилина, с помощью Вестерн-блот-анализа и твердофазного ИФА. Подобные способы можно применять в качестве альтернативных или дополнительных способов определения числа сосудов, включая определение опухоле-специфичного уровня одного или нескольких маркеров эндотелиальных клеток, например, CD31. Как известно в данной области техники, уровень экспрессии маркера/индикаторного белка изобретения может также быть оценен на уровне мРНК с помощью любого удобного метода, известного в этой области, таких как Нозерн-блот, ПЦР в реальном времени и ОТ-ПЦР. Иммуногистохимические методы, системы и методы детекции мРНК являются известными в данной области и могут быть почерпнуты из стандартных учебников, таких как Lottspeich (Bioanalytik, Spektrum Akademisher Verlag, 1998) или Sambrook и Russell (Molecular Cloning: A Laboratory Manual, CSH Press, Cold Spring Harbor, NY, U.S.A., 2001). Описанные способы, в частности, применимы для определения уровней экспрессии VEGFA, HER2, нейропилина и/или CD31 у пациента или групп пациентов по сравнению с контрольными уровнями, определенными для популяции с диагнозом метастатический рак прямой кишки.
Уровень экспрессии одного или нескольких из VEGFA, HER2 и нейропилина (и/или одного или нескольких маркеров эндотелиальных клеток, например, CD31) может быть также определен на белковом уровне с помощью методов иммуноагглютинации, иммунопреципитации (например, иммунодиффузии, иммуноэлектрофореза, иммунной фиксации), методом Вестерн-блота (например, (in situ) иммуногистохимии, (in situ) иммуноцитохимии, аффинной хромотографии, иммуноферментного анализа) и подобных им.
Количество очищенного полипептида в растворе может также быть определено с помощью физических методов, например, фотометрии. Методы количественного анализа отдельного полипептида в смеси обычно относятся к специфическому связыванию, например, антител. Специфическая детекция и количественные методы, использующие специфические антитела, включают, например, иммуногистохимию (in situ). Например, концентрация/количество маркера/индикаторного белка настоящего изобретения в клетках или тканях может быть определена с помощью твердофазного иммуноферментного анализа (ИФА). Кроме того, может быть проведен Вестерн-блот-анализ или иммуногистохимическое окрашивание. Вестерн-блот сочетает разделение смеси белков с помощью электрофореза и специфическую детекцию антителами. Электрофорез может быть многомерным, таким как 2D электрофорез. Обычно, полипептиды разделяют с помощью 2D электрофореза, по их молекулярной массе в одном измерении и по их изоэлектрической точке в другом измерении.
Как отмечено выше, уровень экспрессии маркера/индикаторных белков в соответствии с настоящим изобретением может также отражаться в уменьшении экспрессии соответствующего гена (-ов), кодирующих VEGFA, HER2 и/или нейропилин (и/или один или несколько маркеров эндотелиальных клеток, например, CD31, для определения числа сосудов, как описано в настоящей заявке). Таким образом, количественная оценка продукта гена перед трансляцией (например, сплайсированной, несплайсированной или частично сплайсированной мРНК) может быть осуществлена в виде оценки экспрессии соответствующего гена (генов). Специалистам в данной области известны стандартные методы, которые можно применять в данном контексте или они могут найти такие методы в стандартных учебниках (например, Sambrook, 2001, цит. здесь). Например, количественные данные, соответствующие концентрации/количеству мРНК, кодирующей один или более из VEGFA, HER2 и нейропилин (и/или один или несколько маркеров эндотелиальных клеток, например, CD31, для определения числа сосудов, как описано в настоящей заявке) может быть получено с помощью Нозерн-блота, ПЦР в реальном времени и т.п.
В другом аспекте набор настоящего изобретения можно успешно применять для осуществления способа настоящего изобретения и он может быть, в частности, задействован в различных приложениях, например, в диагностике или как исследовательский инструмент. Части набора изобретения могут быть упакованы индивидуально в ампулы или в комбинации в контейнерах или в мультиконтейнерные единицы. Производство набора предпочтительно соответствует стандартным процедурам, которые известны специалистам в этой области. Набор или диагнотическую композицию можно применять для детекции уровня экспрессии одного или нескольких VEGFA, HER2 и нейропилина (и/или одного или нескольких маркеров эндотелиальных клеток, например, CD31, для определения числа сосудов, как описано в настоящей заявке) в соответствии с описанными в настоящей заявке способами изобретения, включающих, например, иммуногистохимические техники, описанные в настоящей заявке.
Хотя настоящее изобретение проиллюстрировано на примере применения бевацизумаба, настоящее изобретение включает применение других ингибиторов ангиогенеза, известных в данной области техники для применения в комбинации со стандартной схемой химиотерапии. Термин "ингибитор ангиогенеза", используемый в настоящей заявке, относится ко всем агентам, которые изменяют ангиогенез (например, процесс формирования кровеносных сосудов) и включает агенты, которые блокируют формирование и/или останавливают, или замедляют рост кровяных сосудов. Не ограниченные перечисленными примеры ингибиторов ангиогенеза включают, в дополнение к бевацизумабу, пегаптаниб, сунитиниб, сорафениб и ваталаниб. Предпочтительным ингибитором ангиогенеза для применения в соответствии со способами настоящего изобретения является бевацизумаб. Как используется в настоящей заявке, термин "бевацизумаб" включает все соответствующие анти-VEGF антитела или фрагменты анти-VEGF антител, которые отвечают требованиям, необходимым для получения авторизации в маркетинге в качестве идентичных или биологически похожих продуктов в стране или на территории, выбранной из группы стран, состоящей из США, Европы и Японии.
Для применения в способах детекции, описанных в настоящей заявке, специалист может маркировать полипептиды или олигонуклеотиды, включенные в настоящее изобретение. Как обычно практикуется в данной области техники, гибридизационные зонды для детекции уровней мРНК и/или антител, или фрагментов антител для применения в методах ИГХ, могут быть помечены и визуализированы в соответствии со стандартными методами, известными в этой области, неограниченные перечисленными примеры которых, наиболее часто используемые, включают использование радиоактивного мечения, энзимных меток, флуоресцентных мишеней, биотин-авидиновых комплексов, хемилюминисценции и тому подобных.
Специалист в данной области, например, лечащий врач, способен легко вводить бевацизумаб в комбинации с химиотерапевтической схемой пациенту/группе пациентов, выбранному, как описано в настоящей заявке. В определенном контексте лечащий врач может изменять или корректировать схемы введения бевацизумаба и схему химиотерапии в соответствии с его/ее профессиональным опытом.
Таким образом, в некоторых аспектах настоящего изобретения предусмотрены способы лечения или повышения выживаемости без прогрессирования болезни пациента, страдающего или предрасположенного к раку желудочно-кишечного тракта с помощью бевацизумаба в комбинации со схемой химиотерапии, при котором вышеупомянутый пациент/группа пациентов охарактеризован по биологическому образцу (в частности полученного в результате резекции желудочной ткани, биопсии желудочной ткани или метастатического повреждения), при этом вышеупомянутый образец демонстрирует один или несколько эффектов из: повышение уровня экспрессии VEGFA, уменьшение уровня экспрессии нейропилина и уменьшение уровня экспрессии HER2 относительно контрольных уровней, полученных у пациентов с диагнозом метастатического колоректального рака. Настоящее изобретение также предусматривает применение бевацизумаба в подготовке фармацевтической композиции для лечения пациента, страдающего или предположительно страдающего от рака желудочно-кишечного тракта, в частности, мКРР, где пациенты отобраны или охарактеризованы с помощью выявленного в настоящей заявке белкового маркера/индикаторного (т.е. одного или нескольких эффектов из повышенного уровня экспрессии VEGFA, пониженного уровня экспрессии нейропилина и пониженного уровня экспрессии HER2 относительно контрольных уровней, определенных у пациентов с диагнозом метастатический рак ободочной и прямой кишки). Изобретение также включает в качестве альтернативы или дополнения использование VEGFA, нейропилина и/или HER2 как маркеров, описанных в настоящей заявке, для определения опухоль-специфичного числа сосудов (которое может, например, быть охарактеризовано с помощью повышения уровня одного или нескольких маркеров эндотелиальных клеток, например, CD31), где увеличенное вышеупомянутое число сосудов (и/или уровень экспрессии одного или нескольких маркеров эндотелиальных клеток) указывает на пациента, чувствительного или реагирующего на добавление бевацизумаба к схеме химиотерапии, или позволяет выделить популяцию пациентов, на которую направлены описанные в настоящей заявке способы.
ОПИСАНИЕ ФИГУР
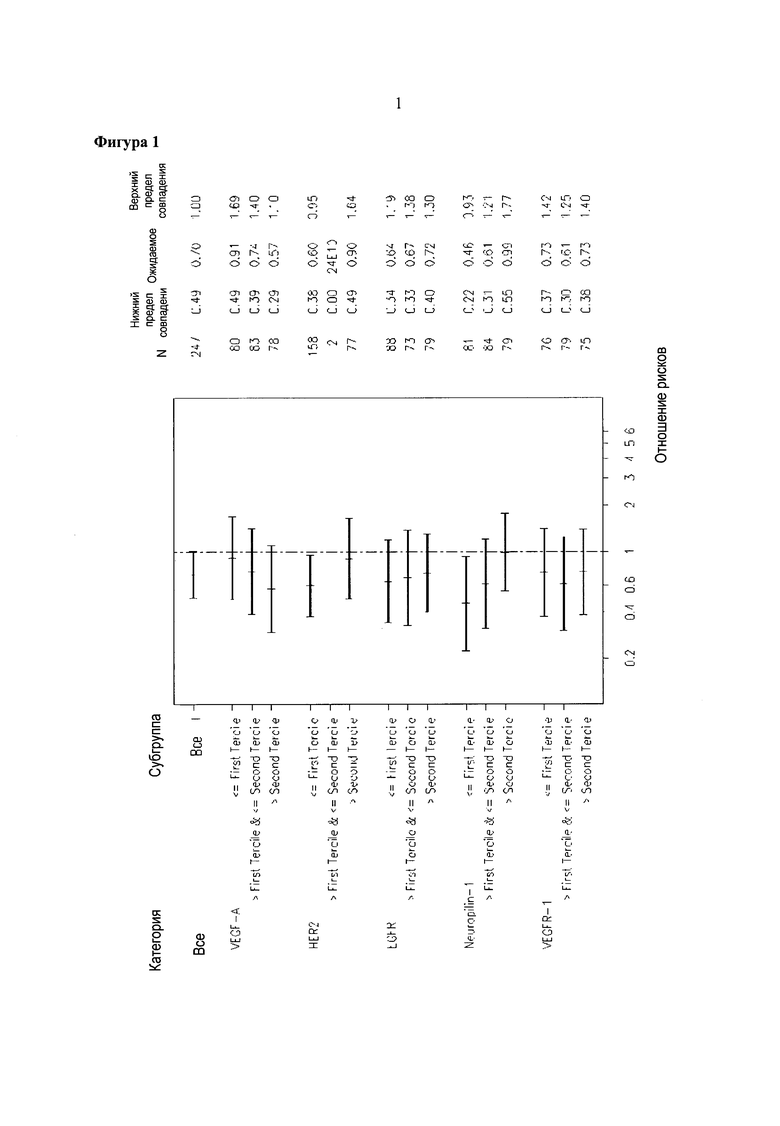
Фигура 1. Диаграмма, иллюстрирующая время до прогрессирования болезни или до смерти для пациентов, получавших бевацизумаб, относительно контроля в соответствии с опухолевыми клеточными биомаркерами субгруппы.
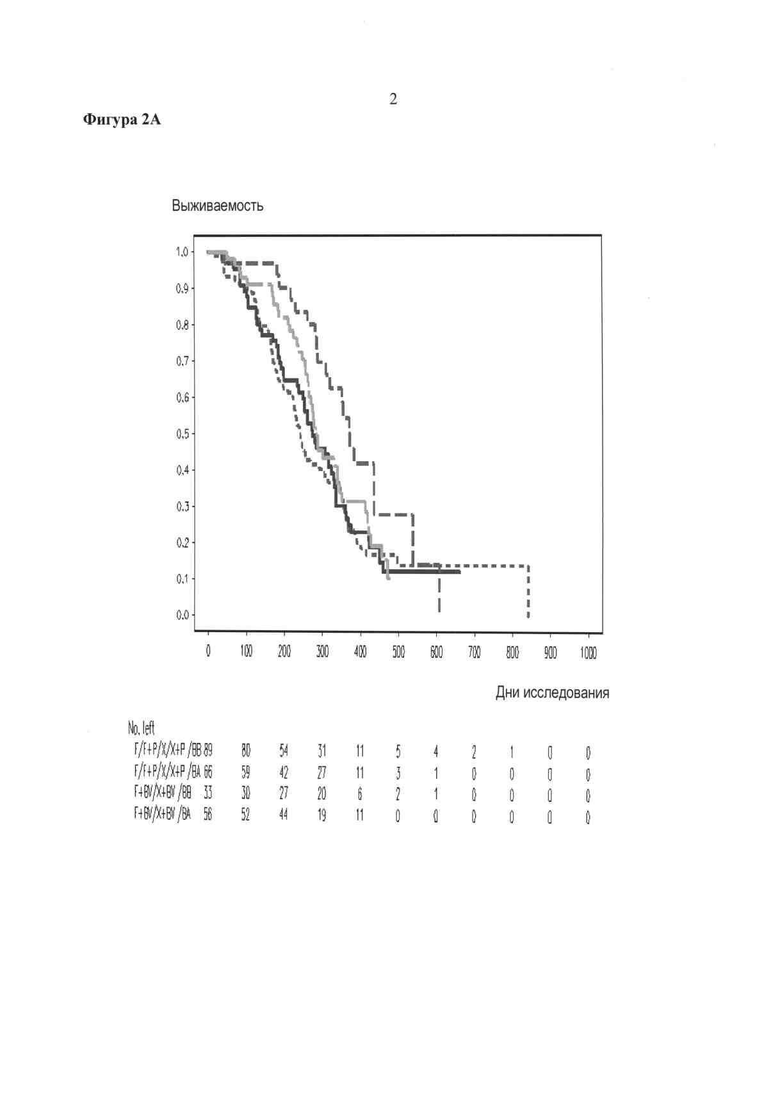
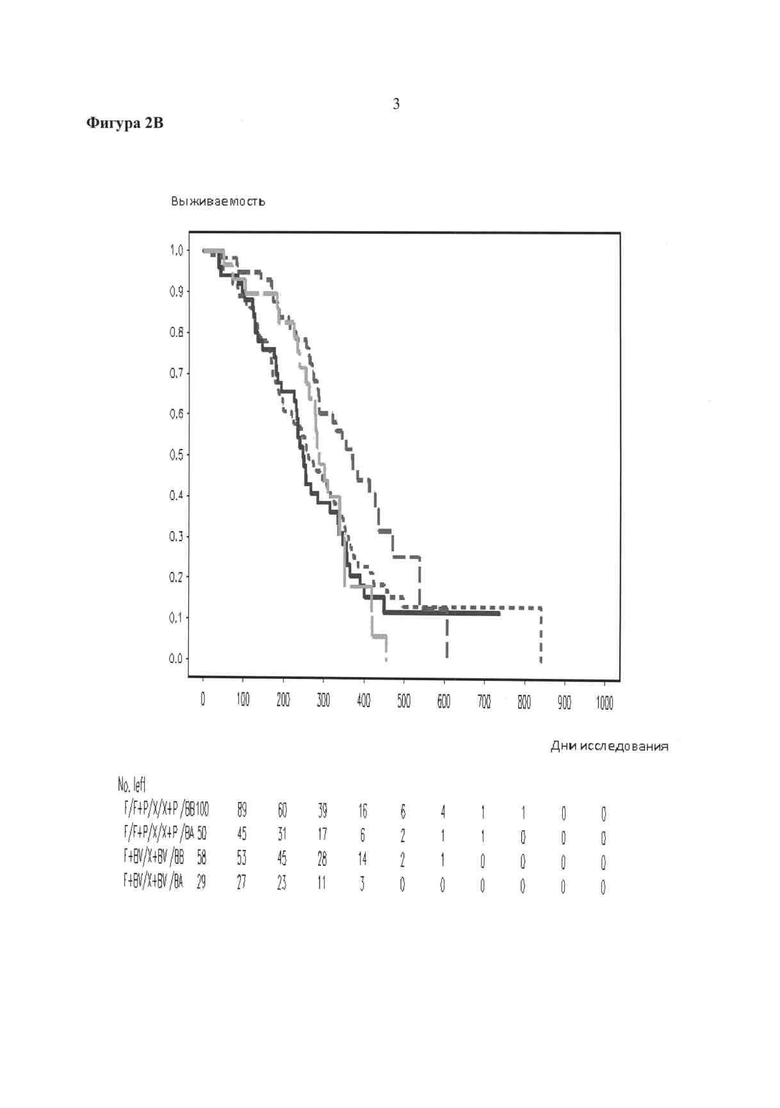
Фигура 2. Корреляция данных об опухолевых биомаркерах с течением времени до прогрессирования болезни или до смерти (в среднем сечении) для нейропилина (Фиг.2А), для HER2 (Фиг.2В) и для VEGFA (Фиг.2С). Для каждой фигуры сплошная черная линия: плацебо (F/F+P/X/X+P) и экспрессия биомаркера над медианой (ВА); длинный пунктир (серого цвета): терапия бевацизумабом (BV) (F+BV/X+BV) и экспрессия биомаркера над медианой (ВА); пунктир: бевацизумабовая терапия (F+BV/X+BV) и экспрессия биомаркера ниже медианы (ВВ); короткий пунктир: плацебо (F/F+P/X/X+P) и экспрессия биомаркера ниже медианы (ВВ).
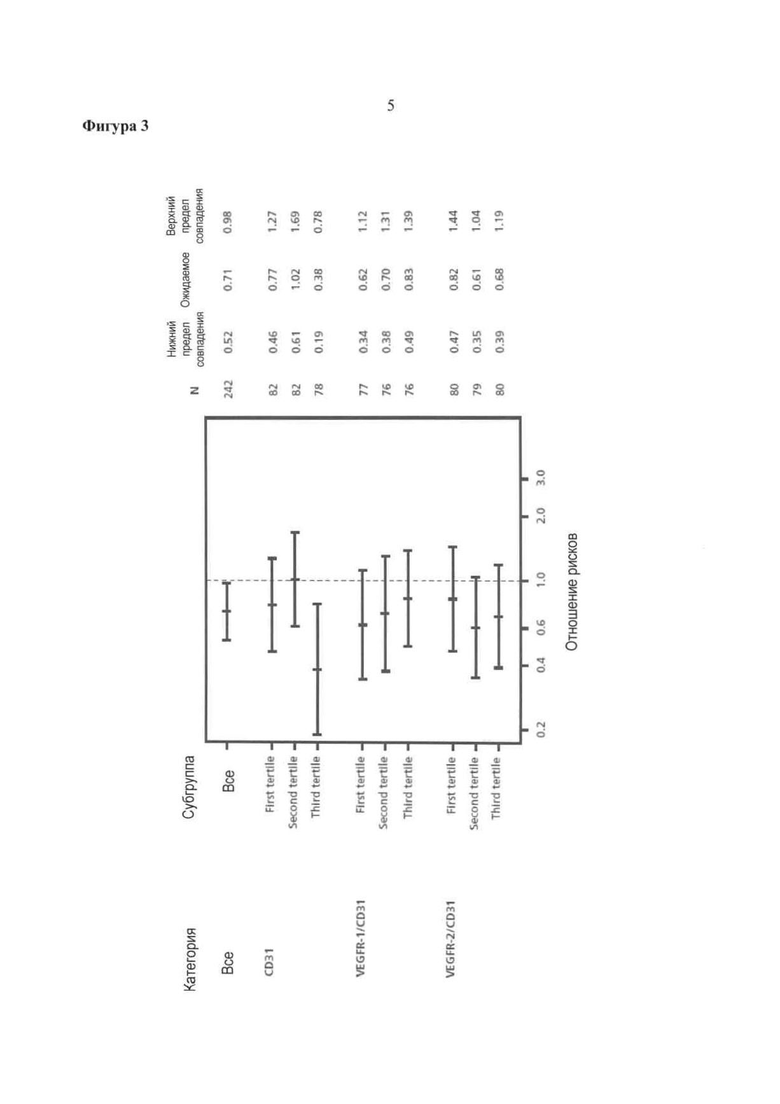
Фигура 3. Диаграмма, иллюстрирующая время до прогрессирования болезни или до смерти для пациентов, получающих бевацизумаб в соответствии с эндотелиальными биомаркерами субгруппы.
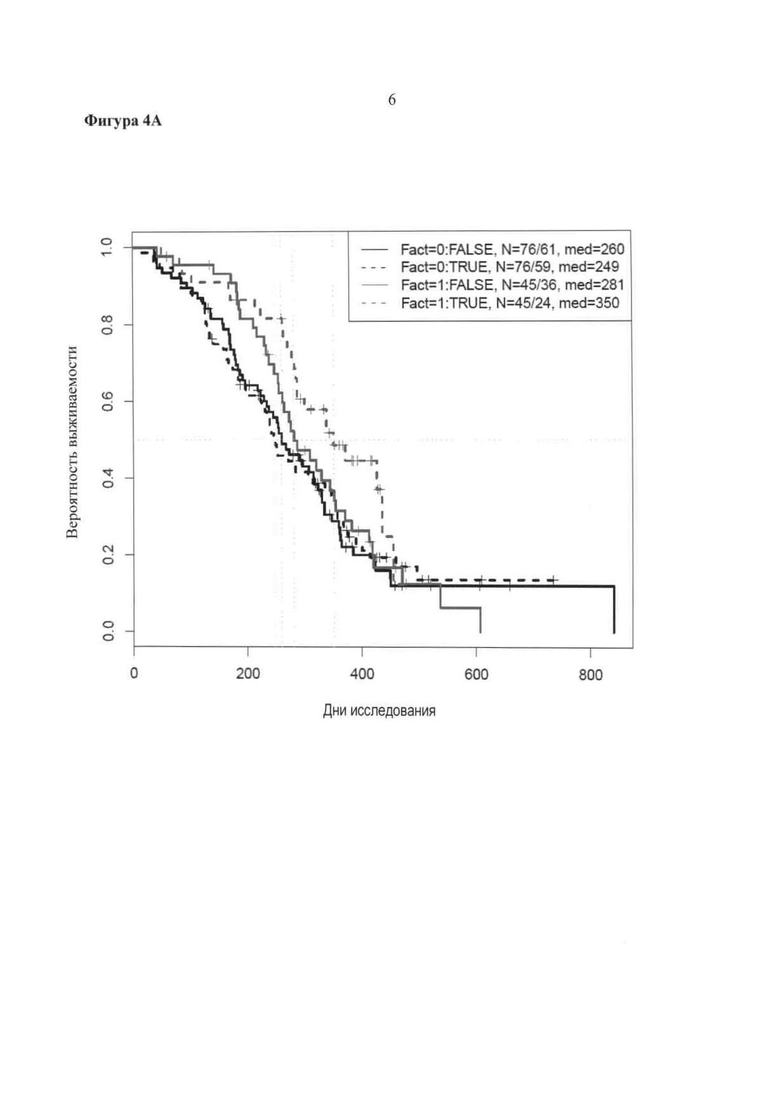
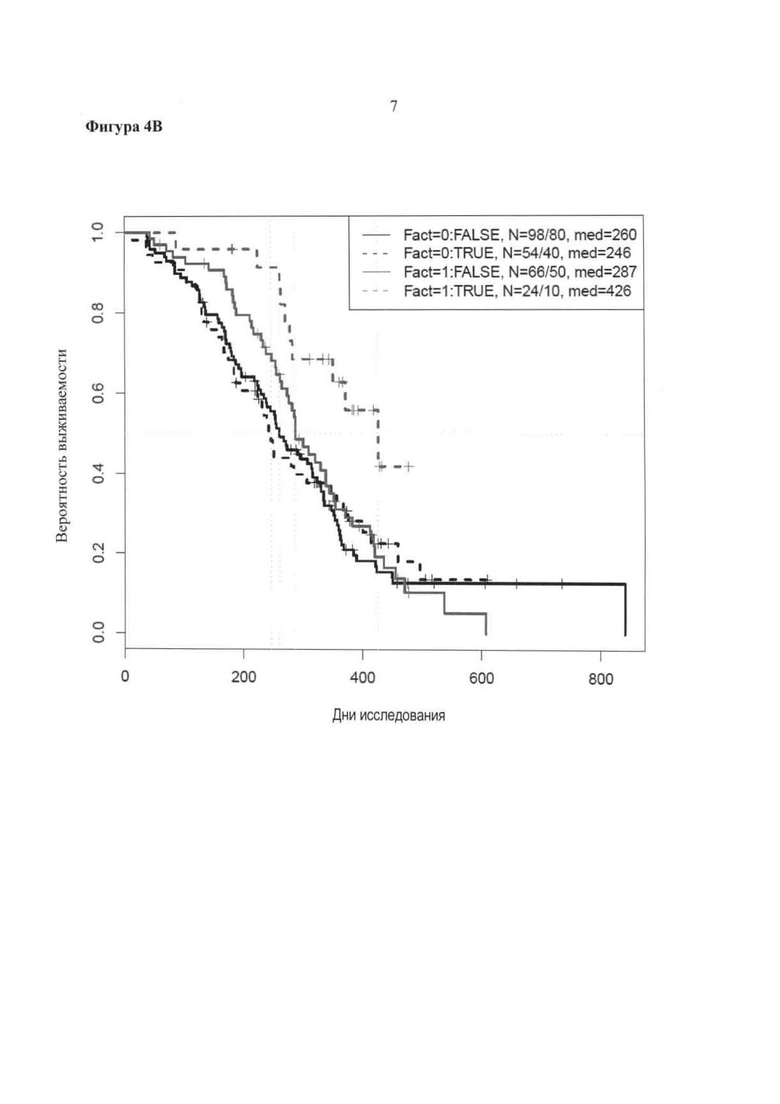
Фигура 4. Корреляция данных эндотелиальных маркеров с течением времени до прогрессирования болезни или до смерти (среднее сечение) для CD31; С031>медианы (Фиг.4А), CD31>2готертиля (Фиг.4В). Для каждой фигуры черная сплошная линия (заканчивающаяся около 610 дня по x-оси; Fact=1 в правом верхнем углу): бевацизумабовая терапия и низкая экспрессия CD31; серый пунктир (Fact=1 в верхнем правом углу) бевацизумабовая терапия и высокая экспрессия CD31; черная сплошная линия (заканчивающаяся на 85 дне по оси x; Fact=0 в верхнем правом углу): плацебо и низкая экспрессия CD31; черный пунктир (выравнивание вероятности выживания около 0.14 по оси y; Fact=0 в верхнем правом углу): плацебо и высокая экспрессия CD31.
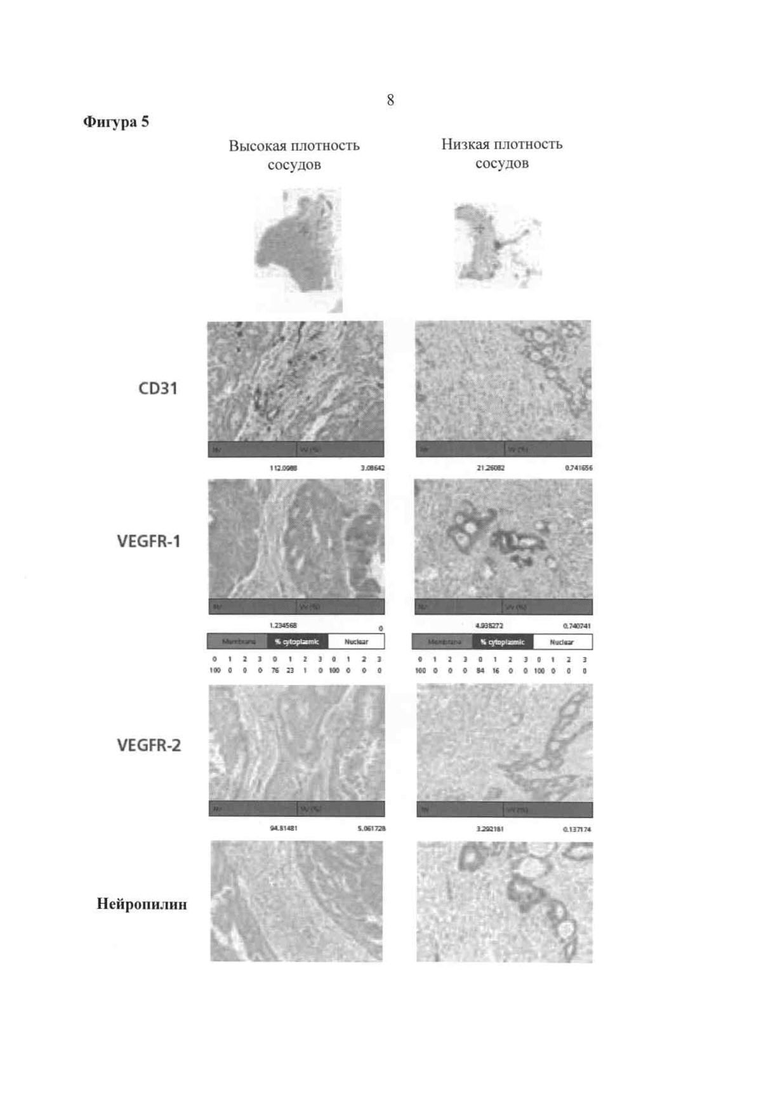
Фигура 5. ИГХ окрашивание опухоли и эндотелиальных клеток у представленных пациентов с высокой и низкой плотностью микрососудов. Nv, число сосудов; W, объем сосудов.
Фигура 6. SEQ ID NO:1, Пример последовательности аминокислот VEGFA.
Фигура 7. SEQ ID NO:2, Пример последовательности аминокислот HER2.
Фигура 8. SEQ ID NO:3, Пример последовательности аминокислот NRP-1.
Настоящее изобретение в дальнейшем проиллюстрировано с помощью не ограничивающих это изобретение примеров.
ПРИМЕР 1
Образцы тканей были взяты у пациентов, участвующих в рандомизированном исследовании фазы III, для сравнения результатов добавления бевацизумаба к первоочередным оксалиплатиновым схемам химиотерапии XELOX и FOLFOX4 для лечения метастатического рака ободочной и прямой кишок (исследование N016966, см., Saltz et al., 2008, J. Clin. Oncol. 26:2013-2019 ("Saltz") и Hurwitz et al., 2004, N. Engl. J. Med. 350:2335-2342 ("Hurwitz")). Исследование состояния биомаркеров связанных с ангиогенезом и опухолегенезом показало, что уровни экспрессии четырех биомаркеров относительно контрольных уровней, определенных для всей популяции пациентов, коррелируют с усовершенствованием параметров лечения. В частности пациенты выявившие один или несколько из следующих эффектов: повышение уровеня экспрессии VEGFA, повышение уровеня экспрессии CD31, понижение уровеня экспрессии HER2 и понижение уровеня экспрессии нейропилина, относительно контрольных уровней, определенных для всей популяции пациентов, демонстрируют увеличение выживаемости без прогрессирования болезни пациента при добавлении бевацизумаба либо к XELOX, либо к FOLFOX4 схеме.
Пациенты и иммуногистохимические методы
В общей сложности 1401 пациент участвовал в исследовании NO 169966 и опухолевые образцы из 247 пациентов были доступны для анализа биомаркеров. Исходные характеристики анализа биомаркеров 247 пациентов представлены в Таблице 1, которые как правило, были схожи с характеристиками для общей популяции (see, Saltz; supra).
Иммуногистохимический анализ проводили на 5 мкм срезах, зафиксированных в формалине парафинизированных тканей. После депарафинизации и регидратации извлечение антигена выполняли с помощью цитратного буфера рН 6.0 при 95°С в течение 30 минут в РТ модуле или СС1 буфере в Benchmark-XT (Ventana, Tucson, AZ, USA).
В таблице 2 представлены семь маркеров, которые были выбраны для иммуногистохимического анализа, основанного на общеизвестных опухолевых и ангиогенных активностях.
Срезы окрашивали с помощью Autostainer или Benchmark-XT (для VEGFR-1), и первичные антитела инкубировали в течение 1 часа. Связывание первичных антител визуализировали с помощью системы Envision (DAKO, Glostrup, Denmark) или Ultraview (Ventana, Tucson, AZ USA). Все срезы были обработаны контрастно гематоксилином Майера.
Проверка отчетов, показывающих точность, специфичность, линейность и ясность (повторяемость и воспроизводимость) доступна для каждого 1НС анализа. Окрашивание внешних контрольных срезов и внутренних контрольных элементов было запротоколировано.
Статистический анализ
Общее распределение биомаркеров было описано с помощью Н-оценки для опухолевых маркеров. Число рассматриваемых маркеров было ограничено и каждый из них был поддержан с помощью биологического обоснования, для множественного тестирования не было формальной коррекции. Первоначальное отсечение было использовано для белкового уровня экспрессии: медиана (ниже, выше) и тертиль (ниже, средний, выше).
Лечебные эффекты были оценены в субгруппах пациентов, определенных уровнем биомаркера. PFS была выбрана в качестве первичной конечной точки и первичного описательного анализа, проводимого с использованием анализа субгрупп. Лечебный тест с помощью взаимодействий биомаркеров (среднее сечение) также представляет вторичный анализ.
Результаты
Маркеры опухоли
Опухолевые клетки, ассоциированные с экспрессией выбранных ИГХ маркеров в выбранной популяции, представлены в Таблице 3.
Исключительно в образцах опухолевых клеток не наблюдали окрашивания на VEGFR-2; однако VEGFR-2 экспрессировался в эндотелиальных клетках. Почти не наблюдали окрашивание на VEGFR-1 в мембранах опухолевых клеток, однако, позитивное окрашивание для этих белков наблюдали в цитоплазме. Несколько образцов также демонстрировали отсутствие экспрессии EGFR и HER2 в опухолевых клетках: 37% образцов не демонстрировали окрашивание для EGFR и 67% образцов не демонстрировали окрашивание для HER2.
Диаграмма, иллюстрирующая время до прогрессирования болезни или до смерти с помощью опухолевых клеточных биомаркеров в субгруппах показана на Фигуре 1. Согласно с отношением рисков, все субгруппы пациентов получили пользу от лечения бевацизумабом, однако, пациенты с опухолевыми клетками, имеющими более высокий уровень VEGFA и/или низкий уровень нейропилина, демонстрировали увеличение пользы, в то время как пациенты, имеющие HER2 положительные опухоли, демонстрировали уменьшение пользы.
Кривая Каплан-Мейера для времени до прогрессирования или до смерти для этих субгрупп показана на Фигуре 2.
Эндотелиальные маркеры
Эндотелиальные клетки, связанные с экспрессией выбранных ИГХ маркеров в выбранной популяции представлены в Таблице 4.
Эндотелиальное VEGFR-1 окрашивание было ниже, чем эндотелиальное VEGFR-2 окрашивание.
Диаграмма, иллюстрирующая время до прогрессирования болезни или до смерти с помощью эндотелиальных биомаркеров субгрупп показана на Фигуре 3. Кривая Каплан-Мейер для времени до прогрессирования болезни или до смерти для CD31 субгрупп показана на Фигуре 4А-В. Пациенты, имеющие опухоли с высокой экспрессией CD31, которая коррелировала с большим числом кровяных сосудов, показывали увеличение пользы в результате лечения бевацизумабом.
Фигура 5 представляет собой изображение ИГХ окрашенных образцов опухоли и эндотелиальных клеток в образцах, имеющих высокую и низкую плотность микрососудов.
Данные, представленные выше, были представлены в виде реферата №374 на симпозиуме, посвященном проблеме рака желудочно-кишечного тракта, 2010 ASCO Gastrointestinal Cancers Symposium в Orlando Florida (January 22 to 24, 2010).
















Группа изобретений относится к области медицины, а именно к онкологии, и предназначена для повышения выживаемости без прогрессирования болезни у пациента, страдающего метастатическим раком ободочной и прямой кишок. Для осуществления способа получают образцы ткани от указанного пациента, определяют уровень экспрессии VEGFA и/или CD31 и вводят бевацизумаб в комбинации со схемой химиотерапии пациенту. При этом пациент имеет повышенный уровень VEGFA и/или CD31 относительно контрольных уровней, определенных у пациентов с диагнозом метастатического рака ободочной и прямой кишок. Указанная схема химиотерапии представляет собой оксалиплатиновую схему химиотерапии. Также обеспечивается способ in vitro для выявления пациента, реагирующего или чувствительного к добавлению бевацизумаба в целях лечения к схеме химиотерапии. Использование группы изобретений позволяет повысить выживаемость пациента с метастатическим раком ободочной и прямой кишок без прогрессирования у него заболевания. 5 н. и 10 з.п. ф-лы, 8 ил., 4 табл., 1 пр.
1. Способ повышения выживаемости без прогрессирования заболевания у пациента, страдающего метастатическим раком ободочной и прямой кишок, с помощью добавления бевацизумаба к схеме химиотерапии, где указанный способ включает:
(а) получение образцов ткани от указанного пациента;
(б) определение уровня экспрессии VEGFA и/или CD31; и
(в) введение бевацизумаба в комбинации со схемой химиотерапии пациенту, имеющему повышенный уровень VEGFA и/или CD31 относительно контрольных уровней, определенных у пациентов с диагнозом метастатического рака ободочной и прямой кишок,
где указанная схема химиотерапии представляет собой оксалиплатиновую схему химиотерапии.
2. Способ in vitro для выявления пациента, реагирующего или чувствительного к добавлению бевацизумаба в целях лечения к схеме химиотерапии, где указанный способ включает:
(а) получение образцов ткани от пациента, предположительно страдающего или предрасположенного к метастатическому раку ободочной и прямой кишок; и
(б) определение уровня экспрессии VEGFA и/или CD31;
где повышенный уровень VEGFA и/или CD31 относительно контрольных уровней, определенных у пациентов, страдающих метастатическим раком ободочной и прямой кишок, указывает на чувствительность пациентов к добавлению бевацизумаба к указанной схеме,
где указанная схема химиотерапии представляет собой оксалиплатиновую схему химиотерапии.
3. Способ по любому из пп. 1, 2, где указанный уровень экспрессии белка определяют с помощью иммуногистохимического метода (ИГХ).
4. Способ по любому из пп. 1, 2, где указанные образцы выбраны из группы, включающей образцы, полученные при резекции желудочной ткани, биоптаты желудочной ткани или из метастатических поражений тканей.
5. Способ по любому из пп. 1, 2, где вышеупомянутая схема оксалиплатиновой химиотерапии представляет схему оксалиплатиновой терапии в комбинации с капецитабином или схему оксалиплатиновой терапии в комбинации с лейковорином и 5-фторурацилом.
6. Способ по п. 5, где схема оксалиплатиновой химиотерапии в комбинации с капецитабином представляет собой схему XELOX.
7. Способ по п. 5, где схема оксалиплатиновой химиотерапии в комбинации с лейковорином и 5-фторурацилом представляет собой схему FOLFOX4.
8. Способ по любому из пп. 1, 2, где указанный пациент дополнительно подвергнется одной или несколькими противораковым терапиям.
9. Способ по п. 8, где указанная противораковая терапия представляет собой лучевую терапию.
10. Способ по любому из пп. 1, 2, где указанный образец получен перед неоадъювантной или адъювантной терапией.
11. Набор, применимый для осуществления любого из способов по пп. 1-10, включающий олигонуклеотиды или полипептиды, с помощью которых можно определить уровень экспрессии одного или более из VEGFA и CD31.
12. Набор по п. 11, включающий полипептид, с помощью которого можно определить уровень экспрессии одного или более из VEGFA и CD31, где указанный полипептид можно применять в иммуногистохимическом методе и/или он представляет собой специфичное антитело для VEGFA или CD31.
13. Применение олигонуклеотида или полипептида для определения уровня экспрессии одного или более из VEGFA и CD31 по любому из пп. 1-10.
14. Применение по п. 13, включающее полипептид, с помощью которого можно определить уровень экспрессии одного или более из VEGFA и CD31, где указанный полипептид можно применять в иммуногистохимическом методе и/или он представляет собой специфичное антитело для VEGFA или CD31.
15. Применение бевацизумаба для повышения выживаемости без прогрессирования болезни пациента, страдающего метастатическим раком ободочной и прямой кишок, включающее следующие этапы:
(а) получение образцов ткани от указанного пациента;
(б) определение уровня экспрессии VEGFA и/или CD31; и
(в) введение бевацизумаба в комбинации со схемой химиотерапии пациенту, имеющему повышенный уровень VEGFA и/или CD31 относительно контрольных уровней, определенных у пациентов с диагнозом метастатического рака ободочной и прямой кишок,
где указанная схема химиотерапии представляет собой оксалиплатиновую схему химиотерапии.
| KABBINAVAR FF et al | |||
| Combined analysis of efficacy: the addition of bevacizumab to fluorouracil/leucovorin improves survival for patients with metastatic colorectal cancer | |||
| J Clin Oncol., 2005, 23(16), р | |||
| ТОПОЧНАЯ АРМАТУРА ДЛЯ УСТАНОВКИ БЕСПАРОВЫХ ФОРСУНОК | 1924 |
|
SU3706A1 |
| US 2009275057 A1, 05.11.2009 | |||
| NINOMIYA S et al | |||
| Effect of bevacizumab, a humanized monoclonal antibody to vascular endothelial growth | |||
Авторы
Даты
2016-12-20—Публикация
2011-01-18—Подача