Изобретение относится к разделу общей и медицинской вирусологии и касается вируса гриппа (ВГ) А.
Вирус гриппа вызывает ежегодные эпидемии и случайные пандемии, которые унесли миллионы людских жизней по всей планете. Пандемия XXI века была вызвана ВГ A(H1N1)pdm09, который быстро распространился по всему земному шару, был зарегистрирован более чем в 214 странах и стал причиной около 151,700-575,400 смертей по всему миру {Pandemic (H1N1) 2009-update 102. [Электронный ресурс]. Режим доступа: http://www.who.int/csr/don/2010_05_28/en/index.html (Дата обращения: 09.02.2015); Dawood, F.S., Luliano A.D., Reed С. et al. // Lancet Infect. Dis. 2012. №12(9). P. 687-695).
Данный ВГ отличает высокая скорость трансмиссии, однако до сих пор остаются сравнительно умеренными его вирулентные и летальные свойства. После сообщения ВОЗ о начале постпандемического периода с 10 августа 2010 года циркуляция ВГ A(H1N1)pdm09 продолжилась, став сезонной (H1N1 in Post-pandemic Period) [Электронный ресурс]. Режим доступа: http://www.who.int/mediacentre/news/statements/2010/h1n1_vpc_20100810/en/index.html (Дата обращения: 09.02.2015).
В период 2012-2014 гг. пандемический вирус 2009 года вновь преобладал среди циркулирующих вирусов гриппа А (Лабораторная диагностика гриппа и ОРВИ [Электронный ресурс]. Режим доступа: http://www.influenza.spb.ru/systern/epidemiological_situation/laboratory_diagnostics (Дата обращения: 09.02.2015; Global circulation of influenza viruses [Электронный ресурс]. Режим доступа: http://www.who.int/influenza/gisrs_laboratory/updates/summaryreport/en/ (Дата обращения: 09.02.2015).
В настоящий момент существует опасение, что в случае, если ВГ A(H1N1)pdm09 сохранит способность эффективно передаваться от человека к человеку и при этом усилит свои вирулентные свойства благодаря адаптации к организму людей, то новый адаптированный вариант, возможно, будет обладать более значительным эффектом на здоровье населения планеты, что, в свою очередь, увеличит число смертельных исходов.
ВГ А постоянно эволюционирует, и не исключено, что в будущем появятся новые пандемичные варианты. Одной из актуальнейших проблем современной вирусологии является изучение адаптации ВГ как опаснейшего инфекционного заболевания к новым хозяевам, в том числе к человеку. Вирусная адаптация является важной приспособительной задачей, цели которой заключаются в подавлении или избегании противовирусного иммунитета хозяина. Известно, что ВГ А способны преодолевать межвидовой барьер и вызывать заболевания среди людей, птиц и млекопитающих (Webstek, R.G. // Microbiol. Rev. 1992. №56(1). P. 152-179). И потому данный патоген является удобной моделью для изучения круга хозяев и механизма преодоления межвидового барьера, поскольку его геном имеет фрагментарное строение, и вклад отдельных генов можно определить используя метод реассортации или адаптации к различным экспериментальным животным {Киселев О.К., Львов Д.К. // Вопросы вирусологии. 2012. Приложение 1: Специальный выпуск, посвященный 120-й годовщине со дня открытия вирусов русским ученым Д.И. Ивановским. - С. 137-147; Ilyushina N.A. Does Pandemic A/H1N1 Virus Have the Potential To Become More Pathogenic? N.A. Ilyushina et al. // MBio [electronic resource]. - 2010. - №1(5). pii: e00249-10. doi: 10.1128/mBio.00249-10).
В настоящий момент во всем мире широко распространились и продолжают циркулировать штаммы пандемического ВГ A(H1N1)pdm09, закрепившие в своем геноме нуклеотидные последовательности характерные концу пандемического периода (http://www.euroflu.org/index.php). Известно, что в эпидемиологическом сезоне 2013-2014 гг. среди сезонных ВГ доминировал A(H1N1)pdm09 (Лабораторная диагностика гриппа и ОРВИ [Электронный ресурс]. Режим доступа: http://www.influenza.spb.ru/system/epidemiological_situation/laboratory_diagnostics (Дата обращения: 09.02.2015; Global circulation of influenza viruses [Электронный ресурс]. Режим доступа: http://www.who.int/influenza/gisrs_laboratory/updates/sunmiaryreport/en/ (Дата обращения: 09.02.2015). И потому сохраняется необходимость использования актуальных адаптированных вариантов пандемических штаммов ВГ A(H1N1)pdm09 для проверки эффективности современных противогриппозных препаратов in vivo и in vitro, имеющих важное значение в эпидемиологической и клинической практике.
Анализ известных аналогов показал, что близкими адаптированными вариантами пандемичного ВГ A(H1N1)pdm09 являются два штамма - A/Russia/01/09-ma (H1N1) и A/IIV-Anadyr/177-ma/2009 (H1N1), которые изначально были выделены из гомогенатов умерших людей в 2009 году на территории РФ, а затем адаптированы к организмам лабораторных животных (Романовская А.А., Шаршов К.А., Зайковская А.В. и д.р. // Патент на изобретение РФ 2451072 18.10.2010; Львов Д.К., Щелканов М.Ю., Федякина И.Т., Дерябин П.Г., Прошина Е.С., Пономаренко Р.А. // Патент на изобретение РФ №2487936).
Недостатки аналогов
По сравнению с предлагаемыми штаммами аналоги были выделены в более ранний период пандемии - в 2009 году, в то время как использованный нами родительский штамм - A/Tomsk/273/2010(H1N1pdm09) - был выделен в конце пандемии в январе 2010 года, что, в свою очередь, говорит о качественно разном составе геномов изучаемых патогенов. Поскольку известно, что благодаря громадной изменчивости пандемических вирусов гриппа те варианты, что циркулировали в конце пандемического периода, достаточно различались по молекулярно-генетическим характеристикам от предшествующих вариантов. Известно, что в настоящее время циркулируют пандемические ВГ A(H1N1)pdm09, закрепившие в своем геноме нуклеотидные последовательности, характерные концу пандемического периода (http://www.euroflu.org/index.php). Потому изучение адаптации штаммов ВГ A(H1N1)pdm09, выделенных в 2010 году, является необходимым в связи с опасением вероятного возникновения новых высоколетальных патогенов.
Кроме того, анализ методик получения штаммов A/Russia/01/09-ma (H1N1) и A/IIV-Anadyr/177-ma/2009 (H1N1) pdm09 показал, что предлагаемый штамм A/Tomsk/273/2010-MAl(H1N1pdm09) был получен за более короткое время - 7 пассажей через легкие мышей линии BALB/c и обладает 100% летальностью не только для мышей, к организмам которых он адаптирован, но также для мышей оппозитной линии C57BL/6z. Подобного анализа патогенности адаптированного варианта ВГ A(H1N1)pdm09 на другой генетической линии лабораторных животных ранее не проводилось.
Задача изобретения состоит в:
- создании адаптированных вариантов пандемического вируса гриппа A(H1N1)pdm09 к организмам генетически различных лабораторных мышей для формирования адекватных моделей изучения активности противовирусных препаратов против пандемического вируса гриппа A(H1N1)pdm09 in vitro и in vivo;
- создании высокопатогенных штаммов, способных вызывать летальную инфекцию среди генетически различных мышей;
- дополнении базы данных молекулярных маркеров патогенности.
Техническим результатом предлагаемого изобретения являются три штамма:
- A/Tomsk/273-MAl/2010(H1N1pdm09) (MA-BALB/c), полученный путем адаптации к организмам мышей линии BALB/c и прошедший 7 пассажей через легкие;
- A/Tomsk/273-MA2/2010(H1N1pdm09) (MA-C57Bl/6z), полученный путем адаптации к организмам мышей линии C57BL/6z прошедший 12 пассажей через легкие;
- A/Tomsk/273-MA3/2010(H1N1pdm09) (MA-CD1), полученный путем адаптации к организмам мышей CD1 и прошедший 10 пассажей через легкие.
Получены полные геномные последовательности вирусных РНК (Приложение 1), благодаря которым дополнена база данных молекулярных маркеров патогенности вируса гриппа А на примере субтипа A(H1N1)pdm09. Проведена оценка противовирусного действия химиопрепаратов в отношении полученных нами адаптированных вариантов пандемичного ВГ A(H1N1)pdm09. Полученные штаммы могут быть использованы для изучения механизмов адаптации вирусных патогенов к новым хозяевам с оценкой действия противовирусных химиопрепаратов при лечении гриппозного заболевания, вызванного пандемичным ВГ A(H1N1)pdm09.
В предлагаемом изобретении получены адаптированные варианты пандемического вируса гриппа A/Tomsk/273/2010(H1N1pdm09) к организмам инбредных мышей линий BALB/c, C57BL/6z и аутбредных мышей CD1. Данный спектр адаптированных вариантов пандемического вируса гриппа к организмам генетически различных лабораторных животных расширяет возможности оценки эффективности противогриппозных препаратов. Впервые в мире проведено перекрестное инфицирование, при котором мышей линии BALB/c заражали штаммом A/Tomsk/273/2010-MA2(H1N1pdm09), адаптированным к организму мышей линии C57BL/6Z, а мышей линии C57BL/6z - штаммом A/Tomsk/273/2010-MAl(H1N1pdm09), адаптированным к организму мышей линии BALB/c. Отмечено, что на другой экспериментальной модели животных адаптированный вариант A/Tomsk/273/2010-MA2(H1N1pdm09) не во всех случаях может проявлять свои высоколетальные свойства.
Все три штамма при интраназальном пути введения вызывают интерстициальную пневмонию с летальным исходом среди мышей, к организмам которых они адаптированы. При этом следует отметить стабильное, закономерное проявление клинических признаков заболевания как у инбредных, так и у аутбредных мышей.
Впервые проведено перекрестное инфицирование мышей оппозитных линий адаптированными вариантами пандемического вируса гриппа A(H1N1)pdm09 с выявлением особенностей патогенных свойств новых штаммов.
Показано, что штамм A/Tomsk/273/2010-MAl(H1N1pdm09), адаптированный к организму мышей линии BALB/c, проявляет более высокие вирусологические и патологические свойства по сравнению с двумя другими штаммами.
Таким образом, заявляемый объект изобретения обладает критериями новизна, изобретательский уровень и промышленная применимость.
Характеристики заявляемых штаммов
Штамм A/Tomsk/273/2010-MAl(H1N1pdm09) был адаптирован к организму мышей линии BALB/c, штамм A/Tomsk/273/2010-MA2(H1N1pdm09) был адаптирован к организму мышей линии C57B1/6Z, а штамм A/Tomsk/273/2010-MA3(H1N1pdm09) был адаптирован к организму мышей CD1. Все полученные адаптированные варианты относятся к вирусу гриппа род Influenzavirus А семейство Orthomyxoviridae. Перечень нуклеотидных последовательностей (Приложение 1).
Изначальный штамм, из которого в последствии были получены адаптированные варианты, называется A/Tomsk/273/2010(H1N1pdm09). Он был выделен по стандартной методике из носоглоточного смыва человека в январе 2010 г. (2-й пассаж на культуре клеток MDCK (Madin-Darby canine kidney) с титром вируса 5,625±0,6 lgTCID50/ml) ("Руководящие принципы ВОЗ по взятию образцов у людей для лабораторной диагностики инфекции птичьего гриппа" [Электронный ресурс]. Режим доступа: http://apps.who.int/csr/disease/avian_influenza/guidelines/humanspecimens/ru/index.html (Дата обращения: 09.02.2015). Исход заболевания благополучный. Выделенный штамм был адаптирован к организму экспериментальных мышей линии BALB/c и линии C57BL/6z, а также аутбредных мышей CD1. Полученные в ходе эксперимента адаптированные к организму мышей варианты пандемического вируса гриппа A(H1N1)pdm09 депонированы в Музей вирусов гриппа и ОРЗ ФГБУ «НИИ гриппа» МЗ РФ (г. Санкт-Петербург) под названиями A/Tomsk/273/2010-MA1(H1N1pdm09) (КМ277585-КМ277592) (MA-BALB/c) рег. номер 5410, A/Tomsk/273/2010-MA2(H1N1pdm09) (КМ277593-КМ277600) (МА-C57Bl/6z) рег. номер 5411 и A/Tomsk/273/2010-MA3(H1N1pdm09) (КМ277601-КМ277608) (MA-CD1) рег. номер 5412.
Идентификация вируса
Первичная идентификация изолированного вируса гриппа А штамма A/Tomsk/273/2010(H1N1pdm09) осуществлялась методом ОТ-ПЦР с использованием праймеров, специфичных к консервативным участкам NP-гена вируса гриппа А согласно, а также с помощью ПЦР тест-системы «АмплиСенс Influenza virus A/H1-swine-FL» (ФГУН ЦНИИЭ) (CDC Protocol of Realtime RTPCR for Influenza A (H1N1) [Электронный ресурс]. Режим доступа: http://www.who.int/csr/resources/publications/swineflu/en/ (Дата обращения: 09.02.2015).
Адаптация родительского штамма вируса гриппа A/Tomsk/273/2010(H1N1pdm09) к мышам различных генетических линий с получением заявляемых адаптированных вариантов
С целью увеличения вирулентности дикого типа пандемичного штамма A/Tomsk/273/2010(H1N1pdm09) была проведена адаптация путем пассирования через легкие лабораторных животных (инбредные мыши линии BALB/c и C57BL/6z, аутбредные мыши CD1). Были использованы мыши 6-8-недельного возраста линии BALB/c (n=145), линии C57BL/6Z (n=245) и беспородные мыши CD1 (n=205). По 10 шт. мышей каждой линии заражали интраназально 50 мкл физиологического раствора, содержащего 103 TCID50/ml штамма A/Tomsk/273/2010(H1N1pdm09). Всех животных содержали на стандартном рационе с достаточным количеством воды. По 7 шт. мышей из каждой группы были случайным образом выбраны для ежедневного мониторинга признаков болезни, потери веса и летальности в течение 14 суток со дня инфицирования (д.и.) (табл. 1). На третьи сутки после д.и. из каждой группы по 3 шт. мышей с наиболее выраженными симптомами заболевания умерщвляли путем дислокации шейных позвонков. Из их легких готовили 10%-ные гомогенаты на физиологическом растворе. После этого проводили интраназальное заражение новых групп мышей 10%-ными гомогенатами легких в объеме 50 мкл. Параллельно репликацию вируса в легких инфицированных мышей определяли титрованием 10%-ного гомогената на культуре клеток MDCK (табл. 2). После получения 100% летальности в исследуемых группах были получены адаптированные варианты пандемичного ВГ A(H1N1)pdm09 и определены значения LD50 (табл. 3) (WHO Manual on Animal Influenza Diagnosis and Surveillance, 2010). Группа отрицательного контроля каждой линии мышей (n=5) интраназально получала фосфатно-солевой буфер (ФСБ) (рН 7.2) в объеме 50 мкл. Величину 50% летальной дозы для мышей рассчитывали по методу Кербера в модификации И.П. Ашмарина и А.А. Воробьева по формуле: lgTCID50/ml=lgДн- δ(ΣLi -0,5) (И.П. Ашмарин, А.А. Воробьев, 1962).
Таким образом, были получены три адаптированных варианта пандемичного ВГ A(H1N1)pdm09 путем последовательных слепых пассажей через легкие экспериментально инфицированных животных:
- A/Tomsk/273-MAl/2010(H1N1pdm09) (MA-BALB/c), полученный путем адаптации к организмам мышей линии BALB/c и прошедший 7 пассажей через легкие;
- A/Tomsk/273-MA2/2010(H1N1pdm09) (MA-C57Bl/6z), полученный путем адаптации к организмам мышей линии C57BL/6z прошедший 12 пассажей через легкие;
- A/Tomsk/273-MA3/2010(H1N1pdm09) (MA-CD1), полученный путем адаптации к организмам мышей CD1 и прошедший 10 пассажей через легкие.
Пример 1. Моделирование летальной гриппозной инфекции у инбредных мышей линии BALB/c и линии C57BI/6z, а также у аутбредных мышей CD1 в сравнении с родительским штаммом A/Tomsk/273/2010(H1N1pdm09).
Поскольку доклинические испытания противогриппозных лекарственных препаратов проводят, главным образом, на мышах, при этом используются как чистые линии, так и беспородные мыши, в проведенных экспериментах нами были тщательно исследованы механизмы адаптации и патогенные свойства адаптированных вариантов пандемического гриппа на инбредных и аутбредных мышах.
Все три адаптированных варианта пандемического вируса гриппа получены из родительского штамма A/Tomsk/273/2010(H1N1pdm09) путем многократного пассирования через легкие экспериментальных мышей.
Штамм MA-BALB/c прошел 7 пассажей через легкие мышей линии BALB/c, штамм MA-C57Bl/6z прошел 12 пассажей через легкие мышей линии C57BL/6z, а штамм MA-CD1 прошел 10 пассажей через легкие мышей CD1. Все полученные новые штаммы вызывают 100% летальность среди мышей, к организмам которых они адаптированы. Средняя продолжительность жизни (СПЖ) у мышей линии BALB/c, инфицированных штаммом MA-BALB/c, составила 4,0 суток; у мышей линии C57BL/6z, инфицированных штаммом МА-C57Bl/6z, составила 8,5 суток; у мышей CD1, инфицированных штаммом MA-CD1, составила 5,3 суток. Значение 50% летальной дозы (LD50) для мышей линии BALB/c, инфицированных штаммом MA-BALB/c, составило 10-3,0 мл/г; для мышей линии C57BL/6z, инфицированных штаммом MA-C57Bl/6z, составило 10-1,1мл/г; у мышей CD1, инфицированных штаммом MA-CD1, составило 10-1,3 мл/г (табл. 1).
Обозначения в таблице 1: 1 - титры вирусов выражены в lgTCID50 на 1 мл исследуемого образца в виде М±2σ, где М - средняя арифметическая величина, а σ - ошибка среднего значения; 2 - гемагглютинирующая единица в 1 мл исследуемого образца; 3 - 50%-ная летальная доза для мышей в 1 мл на 1 г веса животного.
Клинические симптомы гриппозной инфекции в виде снижения аппетита и веса тела, взъерошенности шерсти, сгорбленной осанки стали регистрироваться в группе мышей линии BALB/c с 2-го пассажа, в группе мышей линии C57BL/6z с 5-го пассажа, в группе мышей CD1 - с 3-го пассажа (табл. 2).
Обозначения в таблице 2: МА - адаптированный к организму мышей штамм A/Tomsk/273/2010(H1N1pdm09), прошедший через легкие мышей линии BALB/c 7 пассажей, через легкие мышей линии C57Bl/6z 12 пассажей, а через легкие мышей CD1. Знаки, обозначающие состояния животных: "+" - взъерошенная шерсть; "++" взъерошенная шерсть, сгорбленная осанка; "+++" взъерошенная шерсть, сгорбленная осанка, снижение аппетита; "++++" взъерошенная шерсть, сгорбленная осанка, снижение аппетита, животные сбиваются в кучу; "+++++" взъерошенная шерсть, сгорбленная осанка, животные сбиваются в кучу, снижение аппетита и веса тела, усиленное брюшное дыхание, у некоторых мышей отмечается коньюктивит.
Первые летальные случаи были зарегистрированы в 4-м пассаже среди мышей линии BALB/c, в 8-м - среди мышей линии C57BL/6z и в 5-м пассаже - среди мышей CD1 (табл. 2). 100%-летальность была получена к 7-му пассажу в группе мышей линии BALB/c, к 12 пассажу в группе мышей линии C57BL/6z и в группе мышей CD1 - к 10-му пассажу (табл. 2, 3).
Обозначения к таблице 3: 1-титры вируса в легких инбредных мышей линии BALB/c и C57B16/z, а также аутбредных мышей CD1 были определены с помощью культуры клеток MDCK и выражены в lgTCID50 на 1 мл исследуемого образца, в виде М±2σ, где М - средняя арифметическая величина, а σ - ошибка среднего значения. * - Р<0,05 при сравнение титра вируса в экспериментальной группе по отношению к группе контроля (t-критерий Стьюдента).
Значения вирусных титров составили: для родительского штамма A/Tomsk/273/2010(H1N1pdm09) - 5,625±0,6 lgTCID50/ml, для штамма MA-BALB/c - 5,0±0,5 lgTCID50/ml, для штамма MA-C57Bl/6z - 5,375±0,5 lgTCID50/ml, для штамма MA-CD1 - 4,125±0,5 lgTCID50/ml (табл. 3). В процессе вирусной адаптации во всех группах экспериментальных животных отмечается нарастание инфекционного титра вируса с третьего пассажа, что говорит об увеличении вирусной продукции в легких экспериментальных животных. Достоверные отличия вирусных титров по сравнению с контролем зарегистрированы в группе мышей линии BALB/c в пятом пассаже (5,25±0,4 lgTCID50/ml), в группе мышей линии C57BL/6z во втором (4,75±0,6 lgTCID50/ml) - четвертом (4,875±0,4 lgTCID50/ml), пятом (5,5±0,4 lgTCID50/ml), шестом (4,6±0,2 lgTCID50/ml), седьмом (5,75±0,4 lgTCID50/ml) и в одиннадцатом (4,625±0,2 lgTCID50/ml) пассажах, а группе мышей CD1 достоверных отличий обнаружено не было (табл. 3). Значения 50% летальной дозы (LD50) для мышей линии BALB/c оказались наименьшими по сравнению со значением LD50 для мышей линии C57BL/6z и мышей CD1, что свидетельствует о большей степени патогенности штамма MA-BALB/c (табл. 1). Результаты реакции гемагглютинации значимых различий в группах по отношению с контролем не выявили (табл. 1).
Пример 2. Создание высокопатогенного штамма, способного вызывать летальную инфекцию среди генетически различных мышей.
При перекрестном инфицировании мыши линии BALB/c (n=10) были интраназально заражены штаммом MA-C57BL/6z в дозе 103 TCID50 титр вируса 5,0±0,6 lgTCID50/ml, а мыши линии C57BL/6Z (n=10) - штаммом MA-BALB/c в дозе 5±102 TCID50 титр вируса 5,375±0,6 lgTCID50/ml. Группа отрицательного контроля каждой линии мышей (n=5) интраназально получала ФСБ (рН 7.2) в объеме 50 мкл.
Перекрестное инфицирование, при котором мышей линии BALB/c заражали штаммом, адаптированным к организму мышей линии C57Bl/6z, а мышей линии C57Bl/6z заражали штаммом, адаптированным к организму мышей линии BALB/c, показало четкие различия в патологических свойствах двух адаптированных вариантов пандемического ВГ A(H1N1)pdm09 (рис. 1). На рисунке: выживаемость и изменения веса мышей линии BALB/c и C57B1/6z при перекрестном инфицировании штаммами A/Tomsk/273/2010-MA2(H1N1pdm09) и A/Tomsk/273/2010-MAl(H1N1pdm09) соответственно.
Вес инфицированных животных выражен как М±m, где M - средняя арифметическая величина, a m - стандартная ошибка средней величины. Так штамм MA-BALB/c оказался высоколетальным не только для мышей, к организму которых он был адаптирован (мыши линии BALB/c), но для мышей оппозитной линии C57Bl/6z, вызывая среди последних 100% летальность. А штамм MA-C57BL/6z оказался летальным только для мышей, к организму которых был адаптирован (мыши линии C57Bl/6z).
Анализ аминокислотных последовательностей штамма
A/Tomsk/273/2010(H1N1pdm09) и его адаптированных вариантов показал различия по шести белкам НА (гемагглютинине), NA (нейраминидазе), NP (нуклеокапсидном белке), NS2 (неструктурном белке), РВ2 (полимеразном белке 2), РВ1 (полимеразном белке 1) и наличие потенциальной экспрессии факультативного неструктурного белка PB1-F2 (табл.4). Аминокислотные (ам.к.) замены в белке НА отмечены в антигенных сайтах: (Sa) E172G, (Са2) G239D; в белке NA: I357V, L443I, T367I, при этом во всех исследуемых штаммах обнаружено закрепление главных несинонимичных замен - 1061, 248D (не показано в таблице), характерных для A(H1N1)pdm09, циркулирующих во второй половине пандемии. Замены в белках NP (N375D), NS2 (M235V) и в белках полимеразного комплекса: РВ1 (L50S, S233R, R586K, Р605Н), РВ2 (G158E, S279F, S317L, R482K, Т689А, I690V) также, вероятно, способствовали увеличению патогенности во время адаптации пандемического штамма A/Tomsk/273/2010(H1N1pdm09). Кроме того, во всех адаптированных вариантах отмечена возможность экспрессии белка PB1-F2, который является факультативным неструктурным белком и обнаруживается не у всех ВГА. Он играет роль в увеличении патогенности, вызывая апоптоз клеток-хозяина и разрушая альвеолярные макрофаги. Также данный белок опосредованно регулирует полимеразную активность, находясь в комплексе с белком РВ1, и влияет на иммунный ответ (Hale, B.G. Inefficient control of host gene expretion be the 2009 pandemic H1N1 influenza A virus NS1 protein / B.G.Hale [et al.] // Journal of virology. - 2010. - №84(14). - P. 6909-6922; Varga, Z.T. The influenza A virus protein PB1-F2: killing two birds with one stone? / Z.T. Varga, P. Palese // Virulence. - 2011. - №2(6). - P. 542-546). Между штаммами сравнения имеются только 2 аминокислотные замены и обе в полимеразном белке РВ2: 158E/G и 279S/F (табл. 4, Приложение 2). Возможно, наличие аминокислоты S в положении 279 белка РВ2, а также комплекс других замен в структурных и факультативном белках, у штамма A/Tomsk/273/2010-MAl(H1N1pdm09) совокупно отвечают за высокопатогенные свойства адаптированного варианта пандемического вируса гриппа, которые проявляются на различных линиях мышей.
Пример 3. Изучение аминокислотных последовательностей у родительского штамма пандемического вируса гриппа A(H1N1)pdm09 и его адаптированных вариантов - штаммов A/Tomsk/273/2010-MA1(H1N1pdm09), A/Tomsk/273/2010-MA2(H1N1pdm09) и A/Tomsk/273/2010-MA3(H1N1pdm09).
С помощью литературных источников были выявлены аминокислотные замены у адаптированных вариантов пандемического ВГ A(H1N1)pdm09, отвечающие за лекарственную устойчивость, усиление патогенности и за адаптацию к животным.
Обнаруженные аминокислотные замены: 1. вбелкеРВ2:
- G158E обнаружена у двух штаммов - MA-BALB/c и MA-C57Bl/6z. По данным литературы мутация E158G значительно увеличивает транскрипционную и репликативную активность у адаптированного варианта вируса гриппа A(H1N1)pdm09 к мышам (Ilyushina N.A. Does pandemic A/H1N1 virus have the potential to become more pathogenic? / N.A. Ilyushina et al. // MBio [electronic resource]. - 2010. - №1(5). pii: e00249-10. doi: 10.1128/mBio.00249-10.);
- T271A (у всех исследуемых штаммов) увеличивает полимеразную активность в клетках животных (Liu, Y. Altered receptor specificity and cell tropism of D222G hemagglutinin mutants isolated from fatal cases of pandemic A(H1N1) 2009 influenza virus / Y. Liu [et al.] // Journal virology. - 2010. - V. 84. - P. 12069-12074);
- T271A+590S/591R (у всех исследуемых штаммов) - данное сочетание ам.к. замен отвечает за эффективную репликацию и адаптацию ВГ A(H1N1)pdm09 у млекопитающих (Liu, Y. Altered receptor specificity and cell tropism of D222G hemagglutinin mutants isolated from fatal cases of pandemic A(H1N1) 2009 influenza virus / Y. Liu [et al.] // Journal virology. - 2010. - V. 84. - P. 12069-12074);
- S317L+R482K+T689A+I690V - ам.к. замены, обнаруженные у всех адаптированных вариантов пандемического ВГ по отношению к дикому штамму. Литературных данных по перечисленным мутациям не найдено.
2. в белке РА:
- 295Р - (у всех исследуемых штаммов) известно, что данная аминокислота в сочетании с НА (K154Q) была результатом селекции вируса с улучшенной репликацией и вирулентностью при изучении адаптации пандемического вируса A(H1N1)pdm09 на хорьковой модели (Ilyushina N.A. Does pandemic A/HINI virus have the potential to become more pathogenic? / N.A. Ilyushina et al. // MBio [electronic resource]. - 2010. - №1(5). pii: e00249-10. doi: 10.1128/mBio.00249-10).
3. в белке HA:
- 1001 - увеличивает вирусную трансмиссию (Giria, М.Т. Genomic signatures and antiviral drug susceptibility profile of A(H1N1)pdm09 / M.T. Giria et al. // Journal of vlinical virology. - 2012. - №53. -P. 140-144; Ye, J. Variations in the hemagglutinin of the 2009 H1N1 pandemic virus: potential for strains with altered virulence phenotype? / J. Ye [et al.] // PLoS Pathogens. - 2010. - V. 6 - I. 10 - e1001145);
- Ε172G и G239D - обнаружены у двух штаммов - MA-BALB/c и MA-C57Bl/6z. Литературных данных по перечисленным мутациям не найдено.
4. в белке NP:
- E119V (у всех исследуемых штаммов) отвечает за лекарственную устойчивость к занамивиру (Giria, М.Т. Genomic signatures and antiviral drug susceptibility profile of A(H1N1)pdm09 / Μ.T. Giria et al. // Journal of vlinical virology. - 2012. - №53. - P. 140-144; Song M.S. Increased virulence of neuram-inidase inhibitor-resistant pandemic H1N1 virus in mice: potential emergence of drug-resistant and virulent variants / M.S. Song [et al.] // Virulence. - 2013. - №4(6). - P. 489-93. doi: 10.4161/viru.25952);
- N375D - обнаружена у двух штаммов - MA-BALB/c и MA-C57Bl/6z. Литературных данных о данной мутации не найдено.
5. в белке NA:
- V106I - (у всех исследуемых штаммов) чувствительность ВГА к озельтамивиру (Giria, М.Т. Genomic signatures and antiviral drug susceptibility profile of A(H1N1)pdm09 / M.T. Giria et al. // Journal of vlinical virology. - 2012. - №53. - P. 140-144);
- N248D - одна из главных несинонимичных замен, характерных для ВГ A(H1N1)pdm09. Отмечена чувствительность к озельтамивиру (Morlighem, J.E. Mutation analysis of 2009 pandemic influenza A(H1N1) viruses collected in Japan during the peak phase of the pandemic / J.E. Morlighem [et al.] // PLoS One. - 2011. - №6(4). - e18956; Giria, M.T. Genomic signatures and antiviral drug susceptibility profile of A(H1N1)pdm09 / M.T. Giria et al. // Journal of vlinical virology. - 2012. - №53. - P. 140-144);
- I357V+L443I+T467I - ам.к. замены, обнаруженные у всех адаптированных вариантов пандемического ВГ по отношению к родительскому штамму. Литературных данных по перечисленным мутациям не найдено.
6. в белке NS:
- I123V - (у всех исследуемых штаммов) предполагается играет роль в адаптации ВГ A(H1N1)pdm09 к человеку и усилении вирулентности. Данная ам.к. расположена в эффекторном домене и функциональном районе, регулирующем апоптоз клеток хозяина (Pan, С.Genomic signature and mutation trend analysis of pandemic (H1N1) 2009 influenza A virus / C. Pan [et al.] // PLoS One. - 2010. - V.5. - №3. - e9594).
7. в белке NS2:
- M235V и A236V ам.к. замены, обнаруженные у всех адаптированных вариантов пандемического ВГ по отношению к дикому штамму. Литературных данных по перечисленным мутациям не найдено.
При сравнении дикого штамма и его адаптированных вариантов не было выявлено различий по аминокислотному составу белков М2, M1, РА и РА-Х.
Сравнительный анализ аминокислотного состава адаптированных вариантов пандемического ВГ A(H1N1)pdm09 выявил различия между тремя штаммами, которые являются вероятной причиной функциональных различий патогенов:
1. в белке РВ2:
- E158G - выявлена только у штамма MA-CD1. По-мнению N.A. Ilyushina и др. данная мутация значительно увеличивает транскрипционную и репликативную активность у адаптированного варианта вируса гриппа A(H1N1)pdm09 к мышам (Ilyushina N.A. Does pandemic A/H1N1 virus have the potential to become more pathogenic? / N.A. Ilyushina et al. // MBio [electronic resource]. - 2010. - №1(5). pii: e00249-10. doi: 10.1128/mBio.00249-10). Однако данная ам.к. замена изначально была у дикого штамма и, вероятно, в нашем эксперименте существенного влияния на скорость адаптаци штамма MA-CD1 к животным не повлияла;
- S279F - данная ам.к. замена выявлена только у штамма MA-C57Bl/6z и является единственным различием со штаммом MA-BALB/c. По данным международной базы FLUSURVER обнаруженная мутация является крайне редкой, ее функциональное значение не выявлено (http://flusurver.bii.a-star.edu.sg);
2. в белке НА:
- G155E+D222G данное сочетание мутаций также выявлено только у штамма MA-CD1, и по данным литературы возникает в результате адаптации ВГ A(H1N1)pdm09 к мышам (Ilyushina N.A. Does pandemic A/HINI virus have the potential to become more pathogenic? / N.A. Ilyushina et al. // MBio [electronic resource]. - 2010. - №1(5). pii: e00249-10. doi: 10.1128/mBio.00249-10.);
- D239G - выявлена только у штамма MA-CD1. Однако данная ам.к. замена изначально была у дикого штамма и, вероятно, в нашем эксперименте существенного влияния на скорость адаптации данного патогена к животным не повлияла;
3. в белке NP:
- D375N - выявлена только у штамма MA-CD1. Однако данная ам.к. замена изначально была у дикого штамма и, вероятно, в нашем эксперименте существенного влияния на скорость адаптации патогена к животным не повлияла. В международной базе данных информации о такой мутации на настоящий момент нет.
Таким образом, мы обнаружили, что увеличение патогенности адаптированных вариантов сопровождалось 19 аминокислотными заменами в белках НА, NA, NS2 и в белках рибонуклепротеинового комплекса РВ1, РВ2, NP, а также возникновением факультативного неструктурного белка PB1-F2(Q19). Наиболее близкими по аминокислотному составу оказались штаммы MA-BALB/c и MA-C57Bl/6z.
Нами было обнаружено, что во всех исследуемых штаммах отмечается лекарственная устойчивость к занамивиру благодаря мутации в белке NP (E119V) и к озельтамивиру за счет мутаций в белке NA (V106I, N248D). Данный спектр, полученных нами адаптированных вариантов пандемического вируса гриппа A(H1N1)pdm09 к генетически различных лабораторных животных, расширяет возможности оценки эффективности противогриппозных препаратов.
Кроме того, во всех адаптированных вариантах пандемического ВГ A(H1N1)pdm09 были обнаружены одинаковые мутации, которые, вероятно, также отвечают за усиление патогенности во время адаптации к экспериментальным животным. Мы предполагаем, что такими ам.к. заменами являются: в белке РВ2 (S317L; R482K; Т689А; I690V), в белке НА (E172G, G239D), в белке NP (N375D), в белке NA (I357V; L443I; T467I), в белке NS2 (M235V, A236V). Однако среди опубликованной литературы нами не было обнаружено подтверждающей или опровергающей данный факт информации. На настоящий момент известно ограниченное количество работ, посвященных изучению адаптации пандемического вируса гриппа (О.И. Киселев, Д.К. Львов 2012; Т. Rolling et al., 2009; Ν.Α. Ilyushina et al., 2010; L. Xu et al., 2011; S. Sakabe et al, 2011; M. Garigliany et al., 2010; K.J. McHugh et al., 2013). В большинстве экспериментов используются мыши линии BALB/c и пандемические штаммы, близкие по аминокислотному составу таким штаммам, как A/California/01/2009(H1N1)pdm09 и A/California/07/2009(H1N1)pdm09, однако во всех случаях в результате адаптации регистрируются новые мутации, приводящие к летальному исходу (Т. Rolling et al., 2009; N.A. Ilyushina et al., 2010; L. Xu et al., 2011), что, в свою очередь, говорит о стахостическом накоплении аминокислотных замен пандемическим вирусом гриппа A(H1N1)pdm09 во время его адаптации к млекопитающим.
Молекулярные механизмы, с помощью которых пандемический вирус гриппа 2009 года смог адаптироваться к популяции человека и быстро распространится среди людей, до сих пор остаются неизвестными. Однако лабораторные эксперименты, посвященные изучению адаптации пандемического ВГ A(H1N1)pdm09, позволяют подойти к решению актуальной фундаментальной задачи - определению генетических маркеров вирулентности, роли отдельных генов в патогенезе гриппозного заболевания, а также выявлению молекулярных основ преодоления межвидового барьера. Таким образом, полученные нами данные в ходе эксперимента по адаптации предоставляют дополнительную информацию о молекулярных маркерах патогенности вируса гриппа А на примере субтипа A(H1N1)pdm09.
Пример 4. Моделирование интерстициальной пневмонии у мышей линии BALB/c и C57Bl/6z при интраназальном инфицировании адаптированными вариантами пандемического вируса гриппа
Гистологический анализ ткани легких мышей линии BALB/c и C57Bl/6z приведен на рис. 2. Обозначения к рисунку 2: А и В - участки ткани легких мышей линии BALB/c и C57Bl/6z, соответственно, получавших интраназально ФСБ (рН 7.2) в объеме 50 мкл; С и D - участки ткани легких мышей линии BALB/c и C57Bl/6z, соответственно, от первого пассажа; Е и F - участки ткани легких мышей линии BALB/c от 7-го пассажа и C57Bl/6z от 12-го пассажа соответственно. Окраска гематоксилином и эозином. Увеличение ×10.
Гистологический анализ показал, что несмотря на отсутствие клинических признаков проявления гриппозной болезни на стадии первого пассажа адаптации вирусов к организмам мышей линии BALB/c и C57Bl/6z, в тканях легких отмечено наличие дистрофических изменений в виде десквамации бронхиального эпителия, утолщения межальвеолярных перегородок, а также полнокровия венозных сосудов (рис. 2С, D).
Наиболее выражены патологические изменения в легких мышей линии BALB/c, у которых в сосудистом русле выявлены сладж эритроцитов и плазматическое пропитывание кровеносных сосудов с формированием гиалиноподобных (фибриновых) мембран, что снижает кровооснабжение легкого и способствует развитию синдрома диссеминированного внутрисосудистого свертывания (ДВС-синдром) (рис. 2С). В седьмом пассаже под воздействием штамма MA-BALB/c в легких мышей линии BALB/c регистрируется резкое снижение воздушности респираторной ткани на фоне развития интерстициальной пневмонии (рис. 2Е). В ткани легких мышей линии C57Bl/6z под воздействием штамма MA-C57Bl/6z, полученного к 12 пассажу, не обнаружено резкого снижения воздушности респираторной ткани, однако отмечается генерализация инфекции возле крупных и средних бронхов, а также плазматическое пропитывание кровеносных сосудов и выпотевание белков плазмы крови (рис. 2F).
Пример 5. Оценка действия противовирусного препарата "Озельтамивира" при использовании адаптированных пандемических штаммов вируса гриппа A/Tomsk/273/2010-MA1(H1N1pdm09), A/Tomsk/273/2010-MA2(H1N1pdm09) и AAomsk/273/2010-MA3(H1N1pdm09)
Известно, что в настоящее время среди циркулирующих сезонных вирусов гриппа А типа сохранились и вирусы, вызвавшие пандемию в 2009 году. Именно данные пандемические
штаммы за осенне-зимний периоды 2012-2013 гг. и 2015-2016 гг. вызывали наибольшее число заболевших вирусом гриппа (Лабораторная диагностика гриппа и ОРВИ [Электронный ресурс]. Режим доступа: http://www.influenza.spb.ru/system/epidemiological_situation/laboratory_diagnostics (Дата обращения: 09.07.2016). Поэтому изучение лекарственного действия уже существующих, а также создание новых противогриппозных препаратов, способных направленно бороться с гриппозным заболеванием, вызванным пандемическим вирусом гриппа A(H1N1)pdm09, является необходимым в связи с опасением вероятного возникновения новых высоколетальных патогенов.
В связи с вышеизложенным было проведено изучение терапевтического действия противогриппозного препарата "Осельтамивир" при лечении гриппозной инфекции у экспериментальных животных, вызванной адаптированными вариантами пандемического вируса гриппа A(H1N1)pdm09. В экспериментах использовали субстанцию препарата "Осельтамивир" (Roche, Швейцария), мышей линии BALB/c, C57Bl/6z и аутбредных мышей CD1, а также три штамма MA-BALB/c, MA-C57Bl/6z и MA-CD1.
Перед началом эксперимента всех мышей взвешивали (самцы линии BALB/c (n=30), средний вес 22,95±0,23 г; самцы линии C57Bl/6z (n=30), средний вес 19,5±0,32 г; самцы CD1 (n=30), средний вес 20,73±0,28 г), а затем инфицировали интраназально под легким эфирным наркозом штаммом MA-BALB/c, MA-C57Bl/6z и MA-CD1 соответственно. Доза вируса составляла 10 ЛД50 в 50 мкл.
Лечебная схема заключалась в следующем: "Осельтамивир" (Roche, Швейцария) в дозе 20 мг/кг/сут вводили спустя 1 час после инфицирования, далее - через каждые 24 часа после инфицирования в течение 4 дней. Препарат вводили per os в объеме 200 мкл. За леченными и контрольными животными велось ежедневное наблюдение в течение 14 дней. Химиотерапевтическую активность соединений на модели гриппозной пневмонии мышей оценивали по следующим критериям: показатель защиты от смертельной вирусной инфекции - увеличение выживаемости, средней продолжительности жизни и уменьшение снижения веса в группах животных, леченных препаратом по сравнению с контрольной группой. Взвешивание мышей проводилось ежедневно. Среднее уменьшение или увеличение массы тела животных представляет собой среднее арифметическое уменьшения или увеличения веса животных в исследуемой группе.
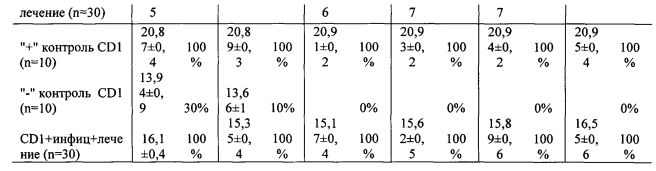
Оценка действия противогриппозного препарата "Озельтамивира" во время лечения экспериментально инфицированных лабораторных мышей BALB/c, C57Bl/6z и CD1, инфицированных штаммами MA-BALB/c, MA-C57Bl/6z, MA-CD 1 с приведением данных по средней продолжительности жизни, а также по изменению массы тела мышей, зараженных
адаптированными вариантами пандемического вируса гриппа A(H1N1)pdm09 и леченых "Осельтамивир" представлена в Таблице 5.
Обозначения к таблице 5: "+" контроль - положительный контроль соответствующей группы, получавший однократно интраназально ФСБ (рН=7,4). "-" контроль BALB/c - отрицательный контроль соответствующей группы, интраназально инфицированный адаптированным вариантом пандемического вируса гриппа A(H1N1)pdm09 в дозе 10 ЛД50 в объеме 50 мкл. BALB/c+инфиц+лечение - означает, что мышей линии BALB/c сперва инфицировали штаммом MA-BALB/c, а затем лечили "Озельтамивиром" в дозе 20 мг/кг/сут в течение 5 дней. По аналогичной схеме проводились манипуляции с мышами C57B1/6zhCD1.
В отрицательных контрольных группах (мыши, зараженные адаптированным вариантом вируса гриппа A(H1N1)pdm09 в дозе 10 ЛД50, и нелеченые препаратом) все мыши погибли в течение 10 дней после инфицирования. В положительных контрольных группах (мыши получали однократно интраназально ФСБ (рН=7,4) в объеме 50 мкл) все мыши были здоровыми. "Осельтамивир" в дозе 20 мг/кг/сут влиял на выживаемость животных, увеличивая среднюю продолжительность жизни мышей по сравнению с отрицательным контролем во всех исследуемых группах.
Однако отмечена различная продолжительность жизни экспериментально инфицированных мышей: наилучший ответ на лекарственную терапию отмечен в группе мышей CD1, инфицированных штаммом MA-CD1 (выживаемость 93,3%), наихудший ответ на лекарственную терапию отмечен в группе мышей линии C57B1/6Z, инфицированных штаммом MA-C57Bl/6z (выживаемость 80%), среднее значение между сравниваемыми группами отмечено у мышей линии BALB/c, которые были инфицированы штаммом MA-BALB/c (выживаемость 83,3%).
Таким образом, оценка действия противовирусного препарата "Озельтамивира" при использовании адаптированных пандемических штаммов вируса гриппа A/Tomsk/273/2010-MA1(H1N1pdm09), A/Tomsk/273/2010-MA2(H1N1pdm09) и A/Tomsk/273/2010-MA3(H1N1pdm09) показала его высокую эффективность при введении лабораторным мышам per os в дозе 20 мг/кг/сут в течение первых 5 суток с момента инфицирования.
Полученные данные о различиях в ответе на лечение противогриппозным препаратом "Озельтамивир" у трех групп инфицированных лабораторных мышей, вероятно, вызвано влиянием на инфекционный процесс адаптированных вариантов пандемического вируса гриппа. Благодаря молекулярно-биологическому исследованию выявлено, что наиболее близкими по аминокислотному составу оказались штаммы, полученные путем адаптации
на линейных мышах - это штамм MA-BALB и MA-C57Bl/6z. При инфицировании данными штаммами с последующим лечением показан наименьший процент выживания, по сравнению с результатами, полученными на примере действия штамма MA-CD1. Данный факт доказывает целесообразность использования штаммов MA-BALB, MA-C57Bl/6z и MA-CD1 при изучении и создании современных противогриппозных препаратов, а также при уточнении терапевтического действия существующих лекарств, способных направленно бороться с гриппозным заболеванием, вызванным пандемическим вирусом гриппа A(H1N1)pdm09.
Кроме того, выявленные в трех адаптированных штаммах вируса гриппа аминокислотные замены, отвечающие за усиление патогенности и адаптацию к животным: в белке РВ2 (G158E, T271A + 590S/591R), в белке PA (295Р), в белке НА (100I), в белке NS1 (I123V). Замены в белках NP (N375D), NS2 (M235V) и в белках полимеразного комплекса: РВ1 (L50S, S233R, R586K, Р605Н), РВ2 (G158E, S279F, S317L, R482K, Т689А, I690V), вероятно, могут возникнуть в пандемических вирусах гриппа A(H1N1)pdm09, циркулирующих в настоящее время среди сезонных вирусов, что, в свою очередь, может способствовать увеличению вирулентных свойств у патогенов по отношению к организму человека.
Благодаря выполненному анализу полных геномов адаптированных вариантов вируса гриппа A(H1N1)pdm09 и развернутому обзору литературы создана база данных маркеров патогенности, которая может найти свое применение для тестирования и разработки лекарственных препаратов, основным механизмом действия которых может быть блокировка проникновения вируса в клетку или нарушение работы полимеразного комплекса.
Полученные адаптированные варианты вируса гриппа A(H1N1)pdm09 могут быть использованы для изучения механизмов адаптации вирусных патогенов к новым хозяевам с оценкой действия противовирусных химиопрепаратов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ ВИРУСА ГРИППА А/Russia/01/2009-ma СУБТИПА H1N1 ДЛЯ ИССЛЕДОВАНИЯ ЛЕЧЕБНОЙ И ПРОФИЛАКТИЧЕСКОЙ АКТИВНОСТИ ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ in vitro И in vivo | 2010 |
|
RU2451072C1 |
| ШТАММ ВИРУСА ГРИППА A/pochard/Siberia/249/08-MA H10N7-СУБТИПА ДЛЯ ПОЛУЧЕНИЯ АНТИГЕН-СОДЕРЖАЩЕГО ДИАГНОСТИЧЕСКОГО ПРЕПАРАТА И ДИАГНОСТИЧЕСКОЙ ПОЛИКЛОНАЛЬНОЙ СЫВОРОТКИ, ПРИМЕНЕНИЯ В КАЧЕСТВЕ КОНТРОЛЬНОГО РЕФЕРЕНС-ОБРАЗЦА ПРИ ОЦЕНКЕ СПЕЦИФИЧНОСТИ ТЕСТ-СИСТЕМ НА ОСНОВЕ ПЦР И ДЛЯ ИЗУЧЕНИЯ ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ in vitro И in vivo | 2013 |
|
RU2522813C1 |
| ШТАММ ВИРУСА ГРИППА СВИНЕЙ A/SWINE/SIBERIA/1SW/2016 H1N1-СУБТИПА ДЛЯ ИСПОЛЬЗОВАНИЯ В ДИАГНОСТИКЕ ВИРУСА ГРИППА МЕТОДАМИ РТГА И ПЦР И ИССЛЕДОВАНИЯ ЭФФЕКТИВНОСТИ ВАКЦИН И ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ IN VITRO И IN VIVO | 2016 |
|
RU2631938C1 |
| ШТАММ ВИРУСА ГРИППА A/IIV-Anadyr/177-ma/2009 (H1N1) pdm09, АДАПТИРОВАННЫЙ К ТКАНЯМ ЛЕГКИХ ЛАБОРАТОРНЫХ МЫШЕЙ | 2012 |
|
RU2487936C1 |
| Метод диагностики вирусов и вирусных инфекций | 2021 |
|
RU2759906C1 |
| Вакцинный штамм вируса гриппа А/17/Южная Африка/2013/01 (H1N1)pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2016 |
|
RU2627188C1 |
| РЕКОМБИНАНТНАЯ ПРОТИВОГРИППОЗНАЯ ВАКЦИНА С ШИРОКИМ СПЕКТРОМ ЗАЩИТЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2017 |
|
RU2757013C2 |
| Вакцинный штамм вируса гриппа А/17/СЛОВЕНИЯ/2015/1121 (H1N1)pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2724706C1 |
| Реассортантный штамм вируса гриппа А/17/Виктория/2019/276 (H1N1) pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2022 |
|
RU2783878C1 |
| СПОСОБ ЗАЩИТЫ ОРГАНИЗМА ОТ ИНФЕКЦИИ, ВЫЗВАННОЙ ШТАММАМИ СУБТИПА H1N1 ВИРУСА ГРИППА А ПРЕПАРАТОМ НА ОСНОВЕ АЛЬФА-2 ИНТЕРФЕРОНА ЧЕЛОВЕКА | 2013 |
|
RU2523554C1 |















Изобретение относится к разделу общей и медицинской вирусологии и касается вируса гриппа А. Получены новые адаптированные варианты пандемического вируса гриппа A(H1N1)pdm09 к организмам различных лабораторных животных, представленные три адаптированных варианта пандемического вируса гриппа получены из штамма дикого типа A/Tomsk/273/2010(HlNlpdm09) путем многократного пассирования через легкие экспериментальных мышей. Штамм A/Tomsk/273/2010-MAl(H1N1pdm09) прошел 7 пассажей через легкие мышей линии BALB/c, штамм A/Tomsk/273/2010-MA2(H1N1pdm09) - 12 пассажей через легкие мышей линии C57BL/6z, а штамм A/Tomsk/273/2010-MA3(H1N1pdm09) - 10 пассажей через легкие мышей CD1. Все описанные штаммы вызывают 100% летальность среди мышей, к организмам которых они адаптированы. Штамм A/Tomsk/273/2010-MAl(H1N1pdm09) является высоколетальным не только для мышей, к организму которых он был адаптирован (мыши линии BALB/c), но и для мышей оппозитной линии C57Bl/6z, вызывая среди последних 100% летальность. Полученные штаммы могут быть использованы для изучения механизмов адаптации вирусных патогенов к новым хозяевам с оценкой действия противовирусных химиопрепаратов при лечении гриппозного заболевания, вызванного пандемичным ВГ A(H1N1)pdm09. 3 н.п. ф-лы, 2 ил., 5 табл., 5 пр.
1. Адаптированный пандемический штамм вируса гриппа A/Tomsk/273/2010-MA1(H1N1pdm09), депонированный в Музей вирусов гриппа и ОРЗ ФГБУ «НИИ гриппа» МЗ РФ, под номером 5410 для оценки действия противовирусных препаратов.
2. Адаптированный пандемический штамм вируса гриппа A/Tomsk/273/2010-MA2(H1N1pdm09), депонированный в Музей вирусов гриппа и ОРЗ ФГБУ «НИИ гриппа» МЗ РФ, под номером 5411 для оценки действия противовирусных препаратов.
3. Адаптированный пандемический штамм вируса гриппа A/Tomsk/273/2010-MA3(H1N1pdm09), депонированный в Музей вирусов гриппа и ОРЗ ФГБУ «НИИ гриппа» МЗ РФ, под номером 5412 для оценки действия противовирусных препаратов.
| ШТАММ ВИРУСА ГРИППА A/IIV-Anadyr/177-ma/2009 (H1N1) pdm09, АДАПТИРОВАННЫЙ К ТКАНЯМ ЛЕГКИХ ЛАБОРАТОРНЫХ МЫШЕЙ | 2012 |
|
RU2487936C1 |
| ШТАММ ВИРУСА ГРИППА А/Russia/01/2009-ma СУБТИПА H1N1 ДЛЯ ИССЛЕДОВАНИЯ ЛЕЧЕБНОЙ И ПРОФИЛАКТИЧЕСКОЙ АКТИВНОСТИ ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ in vitro И in vivo | 2010 |
|
RU2451072C1 |
| WO 2013087945 A2, 20.06.2013 | |||
| МЕТАЛЛИЧЕСКОЕ СТЕКЛО И СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛИЧЕСКОГО СТЕКЛА | 1994 |
|
RU2121011C1 |
Авторы
Даты
2016-12-20—Публикация
2015-06-04—Подача