Область техники, к которой относится изобретение
Настоящее изобретение относится к соединениям общей формулы (I), действующим и как антагонисты мускариновых рецепторов, и как агонисты бета2-адренорецепторов, к способам их получения, к содержащим их композициям, к терапевтическому применению и комбинациям с другими фармацевтически активными ингредиентами.
Предшествующая область техники
Легочные заболевания, такие как астма и хроническая обструктивная болезнь легких (COPD), как правило, лечат бронходилататорами. Хорошо известный класс бронходилататоров включает агонисты бета2-адренорецепторов, такие как сальбутамол, фенотерол, формотерол и сальметерол. Данные соединения обычно вводят путем ингаляции.
Другой известный класс бронходилататоров включает антагонисты мускариновых рецепторов (антихолинергические соединения), такие как ипратропий и тиотропий. Данные соединения также обычно вводят путем ингаляции.
Ингаляционные препараты как агонистов бета2-адренорецепторов, так и антагонистов мускариновых рецепторов представляют собой ценные препараты для лечения астмы и COPD, при этом оба класса препаратов предоставляют симптоматическое облегчение благодаря своей способности расслаблять суженные дыхательные пути. Данные о том, что бронходилатирующие эффекты двух данных классов препаратов являлись аддитивными, привели к исследованиям с использованием комбинации двух данных средств. В 1975 г. было показано, что благоприятных эффектов можно достигнуть, комбинируя в одном аэрозоле два ингредиента, такие как фенотерол и бромид ипратропия. Это привело к разработке комбинированных препаратов с фиксированной дозой бромида ипратропия сначала с фенотеролом (беродуал, введенный в 1980 г.), а затем с сальбутамолом (комбивент, введенный в 1994 г.).
Недавно доступность как антагонистов мускариновых рецепторов длительного действия, так и бета2-агонистов длительного действия привели к исследованиям комбинаций данных агентов. Например, в WO 00/69468 раскрыты лекарственные композиции, включающие антагонисты мускариновых рецепторов, такие как бромид тиотропия, и агонисты бета2-адренорецепторов, такие как фумарат формотерола или сальметерол, а в WO 2005/115467 раскрыта комбинация, включающая агонист бета2-адренорецептора и антагонист мускаринового М3-рецептора, представляющий собой соль 3(R)-(2-гидрокси-2,2-дитиен-2-илацетокси)-1-(3-феноксипропил)-1-азонийбицикло[2.2.2]октана.
Альтернативный подход к разработке комбинированных препаратов с фиксированной дозой заключается в идентификации молекул, соединяющих действие как антагонизма в отношении мускариновых рецеторов, так и агонизма в отношении бета2- адренорецепторов. Фактически, соединения, обладающие и агонистической активностью в отношении бета2-адренорецепторов, и антагонистической активностью в отношении мускариновых рецепторов, являются в высшей степени желательными, поскольку подобные бифункциональные соединения могли бы оказывать бронходилатирующее действие по двум независимым механизмам, имея при этом одинаковую молекулярную фармакокинетику.
Соединения подобного типа были описаны в некоторых патентных заявках, таких как WO 2004/074246, WO 2004/074812, WO 2005/051946, WO 2006/023457, WO 2006/023460, WO 2010/123766 и WO 2011/048409.
Было найдено, что некоторые конкретные сложноэфирные или тиоэфирные производные, помимо того, что они обладают как агонистической активностью в отношении бета2-адренорецепторов, так и антагонистической активностью в отношении мускариновых рецепторов, имеют также повышенное сродство к мускариновым М3-рецепторам и бронходилатирующую активность длительного действия.
Краткое описание изобретения
Настоящее изобретение относится к соединениям общей формулы (I), действующим и как антагонисты мускариновых рецепторов, и как агонисты бета2-адренорецепторов, к способам их получения, к содержащим их композициям, к терапевтическому применению и комбинации с другими фармацевтически активными ингредиентами, в число которых входят, например, ингредиенты, используемые в настоящее время для лечения респираторных заболеваний, например, кортикостероиды, ингибиторы Р38 МАР-киназы, IKK2, ингибиторы HNE, ингибиторы PDE4, модуляторы лейкотриенов, NSAID и регуляторы выработки слизи.
Подробное описание изобретения
В частности, данное изобретение направлено на соединения общей формулы (I)
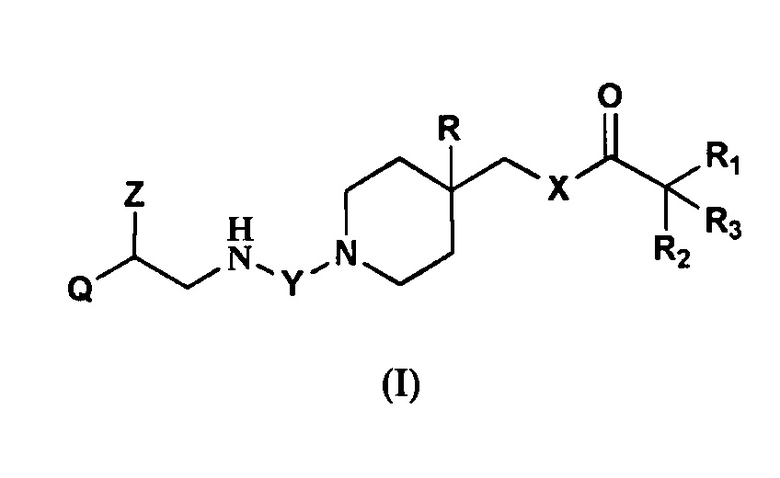
в которой
Q представляет собой группу формулы Q1, Q2, Q3, Q4, Q5 или Q6
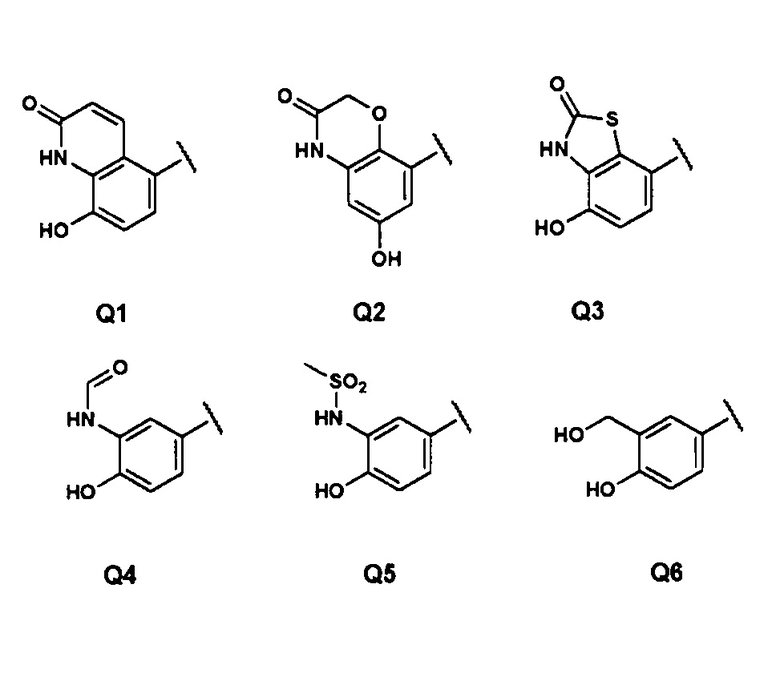
Z представляет собой Н или ОН;
Y представляет собой -(СН2)n-, где n является целым числом от 1 до 12, или представляет собой двухвалентную группу формулы Y1
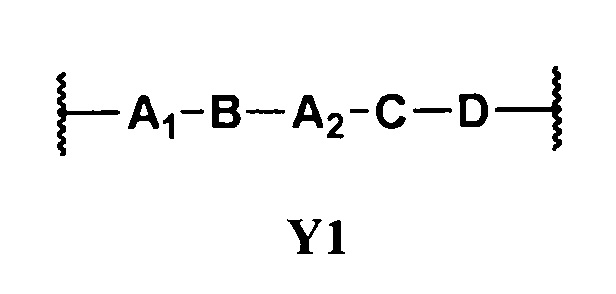
в которой
каждый из А1 и А2 независимо отсутствует или выбран из группы, включающей (С1-С6)алкилен, (С3-С8)циклоалкилен и (С3-С8)гетероциклоалкилен;
В отсутствует или выбран из группы, включающей (С3-С8)циклоалкилен, (С3-С8)гетероциклоалкилен, арилен и гетероарилен, или представляет собой группу формулы В1
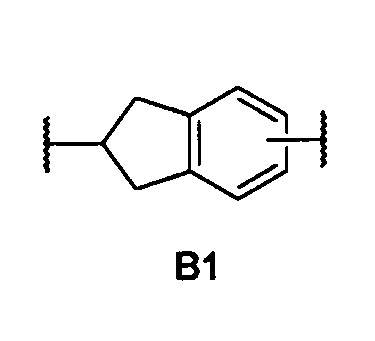
С отсутствует или выбран из группы, включающей -О-, -ОСО-, -С(О)О-, -S-, -S(O)-, -S(O)2- и -N(R4)-, или представляет собой одну из следующих групп С1-С10
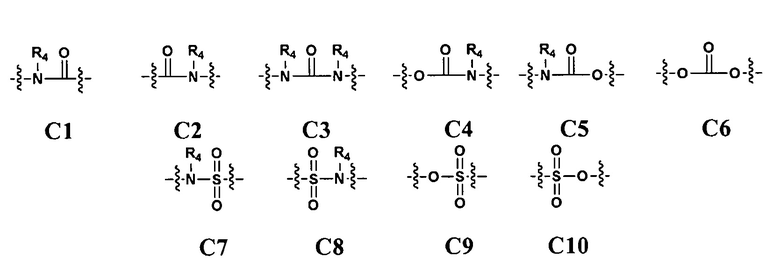
где R4 представляет собой Н или выбран из группы, включающей (С1-С8)алкил, (С3-С8)циклоалкил, (С3-С8)гетероциклоалкил, арил и гетероарил;
D выбирают из группы, включающей (С1-С12)алкилен, (С2-С12)алкенилен и (С2-С6)алкинилен, необязательно замещенных одним или более (С1-С6)алкилами;
R представляет собой Н или (С1-С4)алкил;
Х представляет собой -О- или -S-;
R1 представляет собой Н или выбран из группы, включающей (С3-С8)циклоалкил, арил, гетероарил, арил(С1-С6)алкил, гетероарил(С1-С6)алкил и (С3-С8)циклоалкил(С1-С6)алкил, необязательно замещенные одним или более (С1-С4)алкокси;
R2 выбирают из группы, включающей (С3-С8)циклоалкил, арил, гетероарил, арил(С1-С6)алкил, гетероарил(С1-С6)алкил и (С3-С8)циклоалкил(С1-С6)алкил, необязательно замещенные одним или более атомами галогена или (С1-С4)алкокси;
R3 представляет собой Н или выбран из группы, включающей -ОН, гидрокси(С1-С6)алкил, -N(R5R6) и -N(R5)CO(R6);
R5 и R6 независимо представляют собой Н или (С1-С6)алкил,
и их фармацевтически приемлемые соли или сольваты.
Выражение «(С1-С6)алкил» относится к линейным или разветвленным алкильным группам, в которых число атомов углерода составляет от 1 до 6. Примерами групп являются метил, этил, н-пропил, изопропил, трет-бутил, пентил, гексил и так далее.
Аналогичным образом, выражение «(С1-Сх)алкилен» относится к двухвалентным группам, в которых число атомов углерода составляет от 1 до х, таким как метилен, этилен, н-пропилен, изопропилен, трет-бутилен, пентилен, гексилен, октилен, нонилен, децилен, ундецилен, додецилен и так далее.
Выражение «гидрокси(С1-С6)алкил» относится к -алкилу-, замещенному гидроксильными группами.
Выражение «(С2-С6)алкенил» относится к линейным или разветвленным углеродным цепям, содержащим одну или более двойных связей, в которых число атомов углерода составляет от 2 до 6. Примеры указанных групп включают этенил, пропенил, бутенил, пентенил, гексенил и так далее.
Аналогичным образом, выражение «(С2-Сх)алкенилен» относится к двухвалентным группам, в которых число атомов углерода составляет от 2 до х, таким как этенилен, пропенилен, бутенилен, пентенилен, гексенилен, гептенилен, октенилен, ноненилен, деценилен, ундеценилен, додеценилен и так далее.
Выражение «(С2-С6)алкинил» относится к линейным или разветвленным углеродным цепям, содержащим одну или более тройных связей, в которых число атомов углерода составляет от 2 до 6. Примеры указанных групп включают этинил, пропинил, бутинил, пентинил, гексинил и так далее.
Аналогичным образом, выражение «(С2-Сх)алкинилен» относится к двухвалентным группам, в которых число атомов углерода составляет от 2 до х, таким как этинилен, пропинилен, бутинилен, пентинилен, гексинилен и так далее.
Выражение «(С1-С6)алкокси» относится к алкилокси (например, алкокси) группам, в которых алкильная часть определена выше. Примеры указанных групп включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, пентокси, гексокси и так далее.
Выражение «(С3-С8)циклоалкил» относится к моно- или бициклоалифатическим углеводородным группам, содержащим от 3 до 8 атомов углерода. Примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бицикло[2.2.1]гепт-2-ил и так далее.
Выражение «(С3-С8)гетероциклоалкил» относится к (С3-С3)циклоалкильным группам, в которых по меньшей мере один атом углерода цикла замещен гетероатомом или гетероароматической группой (например, N, NH, S или О). Примеры включают хинуклидинил, пирролидинил, пиперидинил и так далее.
Аналогичным образом, выражение «(С3-С8)циклоалкилен» и «(С3-С8)гетероциклоалкилен» относится к двухвалентным группам, таким как, соответственно, циклопропилен, циклобутилен, циклопентилен, циклогексилен, циклогептилен, бицикло[2.2.1]гепт-2-илен и хинуклидинилен, пирролидинилен, пиперидинилен, азабицикло[3.2.1]октан-3-илен и азонийбицикло[2.2.2]октанилен.
Выражение «арил» относится к моно-, би- или трициклическим циклическим системам, содержащим от 5 до 20, предпочтительно от 5 до 15 атомов цикла, и в которых по меньшей мере один цикл является ароматическим.
Выражение «гетероарил» относится к моно-, би- или трициклическим циклическим системам, содержащим от 5 до 20 атомов цикла, предпочтительно, от 5 до 15, в которых по меньшей мере один цикл является ароматическим, и в которых по меньшей мере один атом углерода цикла представляет собой гетероатом или гетероароматическую группу (например, N, NH, S или О).
Примеры подходящих арильных или гетероарильных моноциклических систем включают, например, тиофеновый, бензольный, пиррольный, пиразольный, имидазольный, изоксазольный, оксазольный, изотиазольный, тиазольный, пиридиновый, имидазолидиновый, фурановый радикалы и так далее.
Примеры подходящих арильных или гетероарильных бициклических систем включают нафталиновый, дифенильный, пуриновый, птеридиновый, бензотриазольный, хинолиновый, изохинолиновый, индольный, изоиндольный, бензотиофеновый, дигидробензодиоксиновый, дигидробензодиоксепиновый, бензооксазиновый радикалы и так далее.
Примеры подходящих арильных или гетероарильных триклических систем включают флуореновые радикалы, а также бензоконденсированные производные упомянутых выше гетероарильных бициклических систем.
Аналогичным образом, выражения «арилен» и «гетероарилен» относятся к двухвалентным группам, таким как фенилен и тиенилен.
Выражения «арил(С1-С6)алкил», «гетероарил(С1-С6)алкил» и «(С3-С8)циклоалкил(С1-С6)алкил» относятся к «(С1-С6)алкилу», соответственно замещенному одной или более арильной, гетероарильной или (С3-С8)циклоалкильной группами, определенными выше.
Примеры арил(С1-С6)алкила включают бензил, трифенилметил и так далее.
Каждый раз, когда в соединениях формулы (I) присутствуют основные аминогруппы, могут также присутствовать физиологически приемлемые анионы, выбранные из хлорида, бромида, фторида, йодида, трифторацетата, формиата, сульфата, фосфата, метансульфоната, нитрата, малеата, ацетата, цитрата, фумарата, тартрата, оксалата, сукцината, бензоата и п-толуолсульфоната. Аналогичным образом, в присутствии кислотных групп, таких как СООН группы, могут также присутствовать соли соответствующих физиологически приемлемых катионов, например, включая соли щелочных, щелочноземельных ионов металлов или соли аммония.
Будет понятно, что соединения общей формулы (I) могут содержать асимметрические центры. Поэтому данное изобретение также включает любые оптические стереоизомеры, диастереоизомеры и их смеси, в любой пропорции.
В частности, атом углерода, связанный с R1, R2 и R3 группами, в зависимости от значений, установленных для R1, R2 и R3 в ряду значений, приведенных ранее, может представлять собой хиральный центр.
В первом предпочтительном варианте осуществления данный хиральный центр может иметь абсолютную конфигурацию (R).
В другом варианте осуществления предпочтительной конфигурацией может быть (S).
В предпочтительном варианте осуществления соединения общей формулы (I), описанные в настоящем изобретении, присутствуют в виде смеси диастереоизомеров.
В другом варианте осуществления, в случае, когда в соединениях общей формулы (I) Z является -ОН, атом углерода связан с Q, а Z представляет собой хиральный центр, предпочтительной конфигурацией которого является (R).
Первой предпочтительной группой соединений является группа соединений общей формулы (I), в которой R1 представляет собой Н или выбран из группы, включающей (С3-С8)циклоалкил, арил, гетероарил и арил(С1-С6)алкил; R2 выбирают из группы, включающей (С3-С8)циклоалкил, арил, гетероарил, арил(С1-С6)алкил, гетероарил(С1-С6)алкил и (С3-С8)циклоалкил(С1-С6)алкил; R3 представляет собой Н или выбран из группы, включающей -ОН, гидрокси(С1-С6)алкил, -N(R5R6) и -N(R5)CO(R6); Х представляет собой -О- или –S; R представляет собой Н или (С1-С4)алкил; Y, Z и Q такие, как описаны выше.
В данном классе еще более предпочтительными являются соединения общей формулы (I), в которой R1 представляет собой Н или выбран из группы, включающей циклобутил, циклопентил, фенил, бензил, циклогептил, тиенил и циклогексил; R2 выбирают из группы, включающей фенил, тиенил, циклогексил, трифенилметил, хлорфенил, метоксифенил и фторфенил; R3 представляет собой Н или выбран из группы, включающей -ОН, -NH2, -CH2OH, -NHCOCH3; Х представляет собой -О-; R представляет собой Н или -СН3.
Второй предпочтительной группой соединений общей формулы (I) является группа, в которой R1, R2, R3, Х и R определены выше, Y представляет собой -(СН2)n-, где n является целым числом от 1 до 12, или представляет собой группу формулы Y1
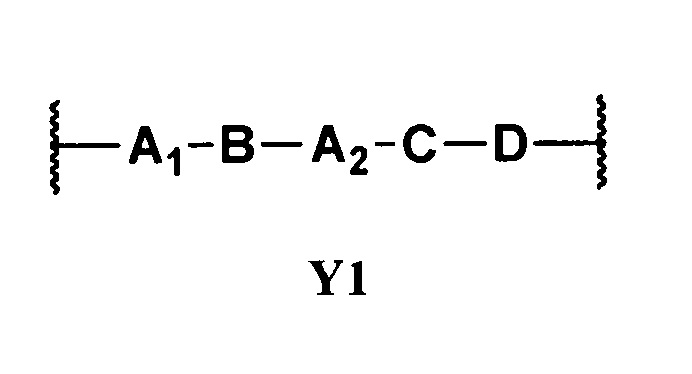
в которой
каждый из А1 и А2 независимо отсутствует или выбран из группы, включающей (С1-С6)алкилен, (С3-С8)циклоалкилен и (С1-С6)гетероциклоалкилен;
В отсутствует или выбран из группы, включающей (С3-С8)циклоалкилен, (С3-С8)гетероциклоалкилен, арилен и гетероарилен, или представляет собой группу формулы В1
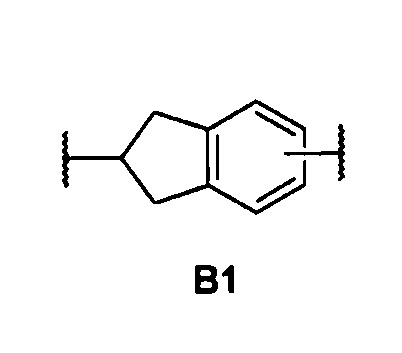
С отсутствует или выбран из группы, включающей -О-, -ОСО-, -С(О)О-, -S-, N(R4)-, или является членом одной из следующих групп С1-С10
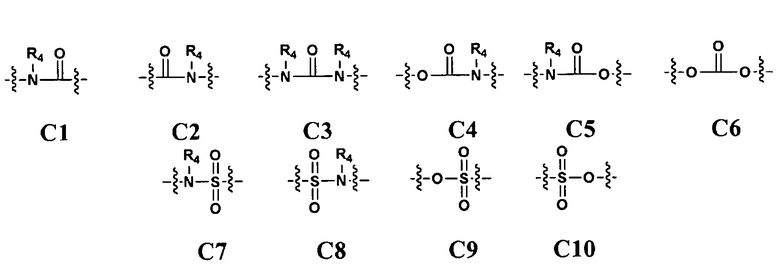
где R4 представляет собой Н или выбран из группы, включающей (С1-С8)алкил, (С3-С8)циклоалкил, (С3-С8)гетероциклоалкил, арил и гетероарил; D выбран из группы, включающей (С1-С12)алкилен, (С2-С12)алкенилен и (С2-С6)алкинилен, необязательно замещенные одним или более (С1-С6)алкилом;
Z представляет собой -Н или -ОН, а Q представляет собой группу формулы Q1, Q2, Q3, Q4, Q5 или Q6
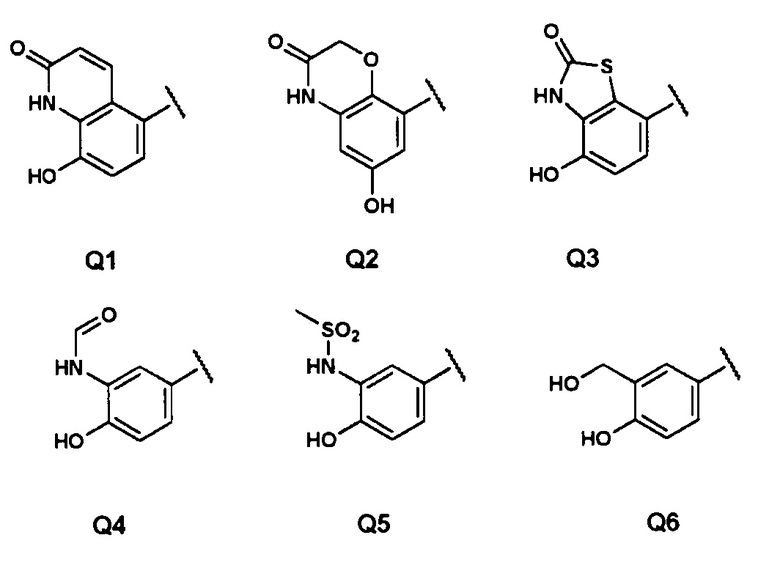
Еще более предпочтительными в данном классе являются соединения общей формулы (I), в которых Y представляет собой -(СН2)n, Z представляет собой ОН, а Q представляет собой группу формулы Q1

в соответствии с общей формулой (IA)
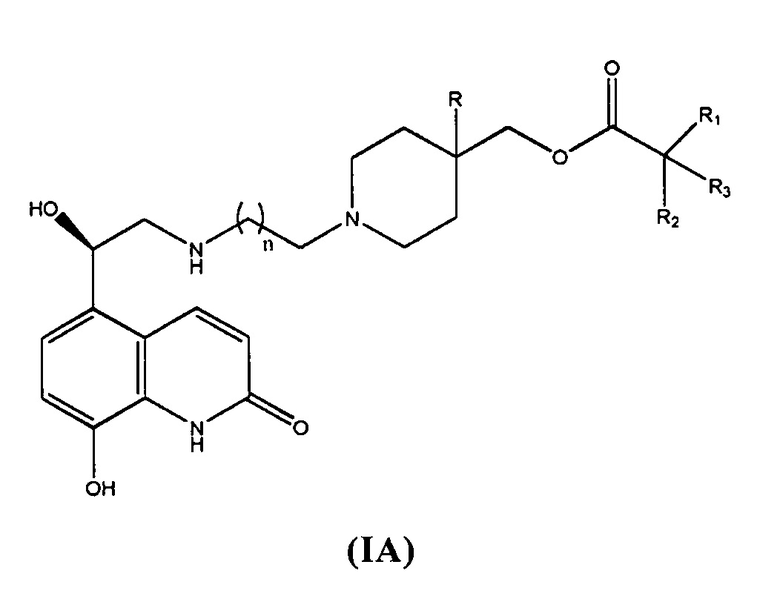
Еще более предпочтительными являются соединения общей формулы (IA), в которых n равно 4, 5, 6, 7 или 8.
Следующим классом предпочтительных соединений общей формулы (I) является класс соединений, в которых Y представляет собой двухвалентную группу формулы Y1
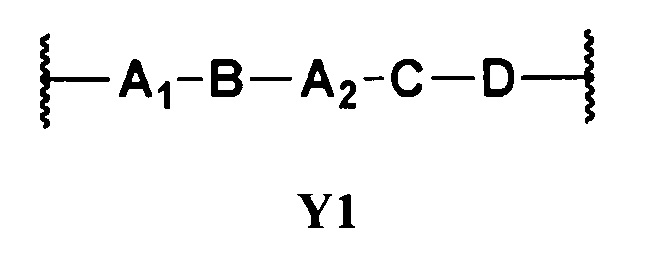
в которой А1 представляет собой (С3-С8)циклоалкилен, В и С отсутствуют, D представляет собой (С1-С12)алкилен, Z представляет собой ОН, а Q представляет собой группу формулы Q1
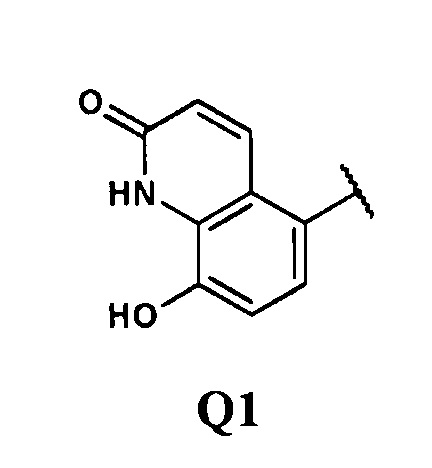
в соответствии с общей формулой (IB), в которой (С3-С8)циклоалкилен представлен как «cy»
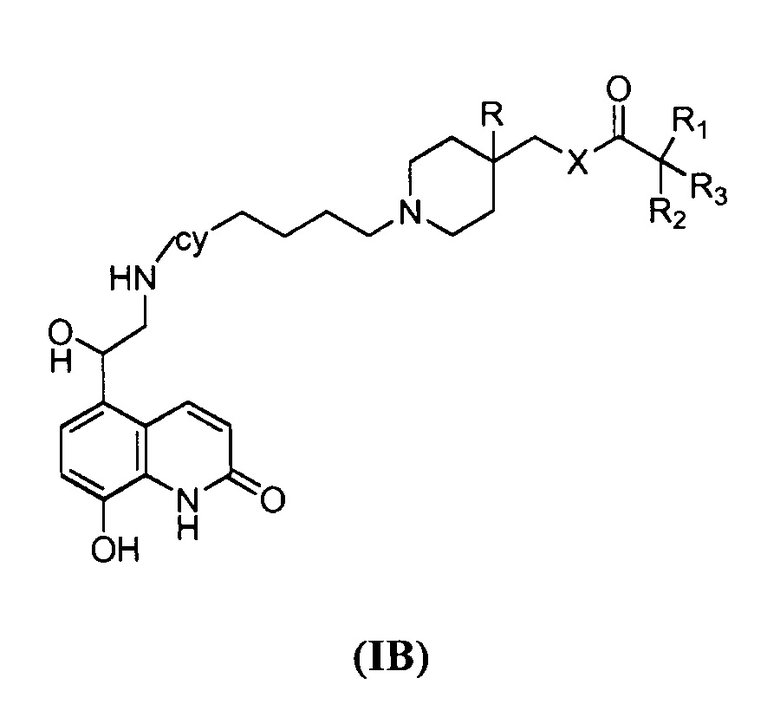
Еще более предпочтительными являются соединения общей формулы (I), в которых Y представляет собой двухвалентную группу формулы Y1, где А1 представляет собой пиперидинил, D представляет собой гексилен, Z представляет собой ОН, а Q представляет собой группу формулы Q1
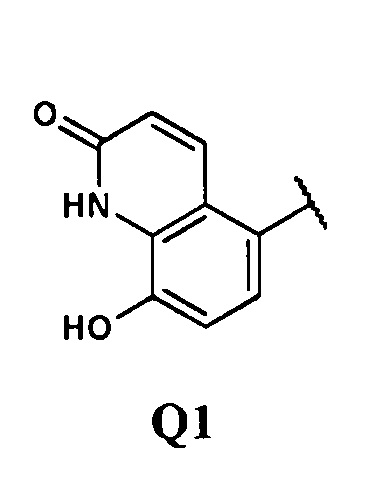
Следующий предпочтительный класс представлен соединениями общей формулы (I), в которых Y представляет собой -(СН2)n, Z представляет собой Н, а Q представляет собой группу формулы Q3
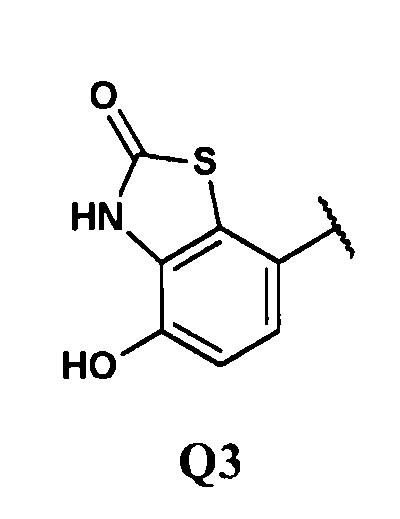
в соответствии с общей формулой (IC)
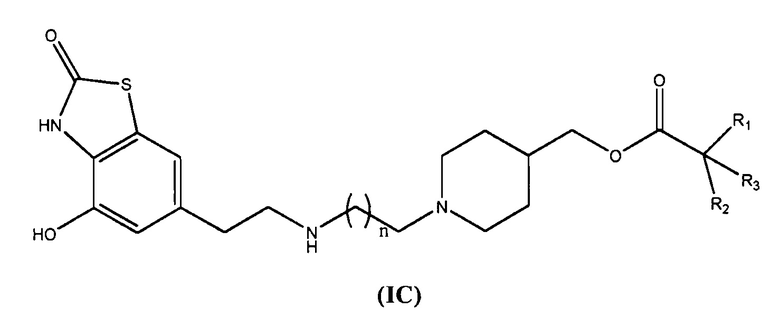
Еще более предпочтительными являются соединения общей формулы (IC), в которых n равно 8.
Следует понять, что все предпочтительные группы вариантов осуществления, описанные выше для соединений формулы (I), можно объединять друг с другом и применять также к соединениям формулы (IA), (IB) и (IC), с необходимыми изменениями.
В настоящем изобретении предоставлены также фармацевтические композиции соединений формулы (I), содержащие данные соединения индивидуально, или в комбинации, или в смеси с одним или более фармацевтически приемлемыми носителями и/или эксципиентами.
В настоящем изобретении также предоставлено применение соединений формулы (I) для получения лекарственного препарата.
В следующем аспекте, в данном изобретении предоставлено применение соединений формулы (I) для предупреждения и/или лечения любого бронхообструктивного или воспалительного заболевания, предпочтительно астмы, или хронического бронхита, или хронической обструктивной болезни легких (COPD).
В следующем аспекте, в данном изобретении предоставлено применение соединений формулы (I) для получения лекарственного препарата для предупреждения и/или лечения любого бронхообструктивного или воспалительного заболевания, предпочтительно астмы, или хронического бронхита, или хронической обструктивной болезни легких (COPD).
Кроме того, в настоящем изобретении предоставлен способ предупреждения и/или лечения любого бронхообструктивного или воспалительного заболевания, предпочтительно астмы, или хронического бронхита, или хронической обструктивной болезни легких (COPD), который включает введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения общей формулы (I).
В настоящем изобретении также предоставлены фармацевтические композиции, подходящие для введения путем ингаляции.
Ингалируемые препараты включают ингалируемые порошки, дозированные аэрозоли, содержащие пропеллент, или ингалируемые препараты, не содержащие пропеллента.
Данное изобретение также направлено на устройство, которое может представлять собой однозарядный или многозарядный сухой порошковый ингалятор, ингалятор отмеренных доз и жидкостные небулайзеры, содержащие соединения формулы (I).
Данное изобретение также направлено на набор, включающий фармацевтические композиции соединений формулы (I), содержащие данные соединения индивидуально, или в комбинации, или в смеси с одним или более фармацевтически приемлемыми носителями и/или эксципиентами, и устройство, которое может представлять собой одно- или многозарядный сухой порошковый ингалятор, ингалятор отмеренных доз и жидкостные небулайзеры, содержащие соединения общей формулы (I).
Данное изобретение также направлено на способ получения соединений общей формулы (I), при этом данный способ включает взаимодействие промежуточного соединения 7
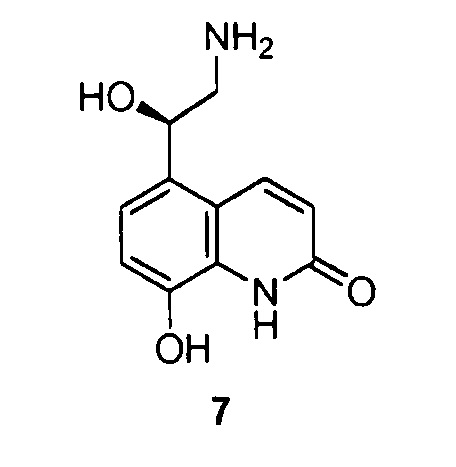
с соединением общей формулы 6
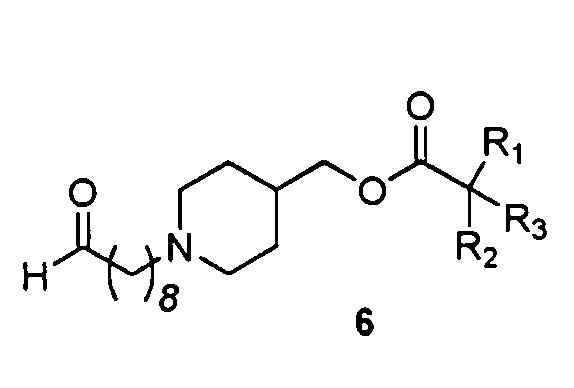
в котором R1, R2 и R3 имеют значения, приведенные выше.
Данное изобретение также направлено на способ получения соединений общей формулы (I), включающий алкилирование соединения формулы 7 соединением общей формулы 8
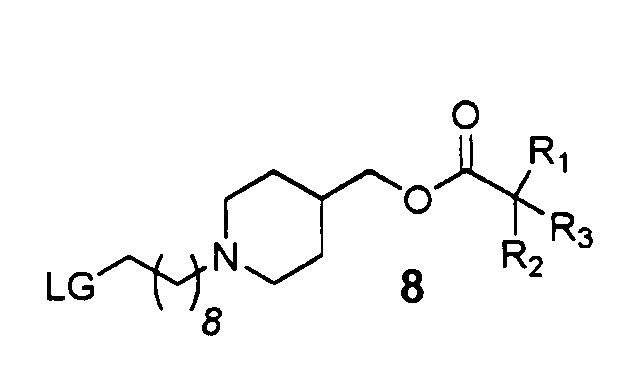
где LG является уходящей группой, подходящей для взаимодействия с амином.
Согласно конкретным вариантам осуществления, в настоящем изобретении предоставлены соединения, приведенные далее:
Соединения данного изобретения можно получить из легкодоступных исходных веществ, используя следующие общие способы и методики, или используя другие легкодоступные способы, известные в данной области. Хотя в настоящем описании можно показать или описать конкретный вариант осуществления настоящего изобретения, специалистам в данной области будет понятно, что все варианты осуществления или аспекты настоящего изобретения можно получить описанными здесь способами, или используя другие известные способы, реагенты и исходные вещества. Кроме того, будет понятно, что в случае, когда даны стандартные или предпочтительные условия способа (то есть температура реакции, продолжительность, молярные соотношения реагентов, растворители, давление и так далее), можно также применять другие условия способа, если не установлено иначе. Несмотря на то, что оптимальные условия реакции могут изменяться в зависимости от конкретных используемых реагентов или растворителя, специалист в данной области может легко определить такие условия при помощи обычных методов оптимизации.
Соединения общей формулы (I) можно получить по следующей схеме синтеза, в которой Bn обозначает бензильную группу.
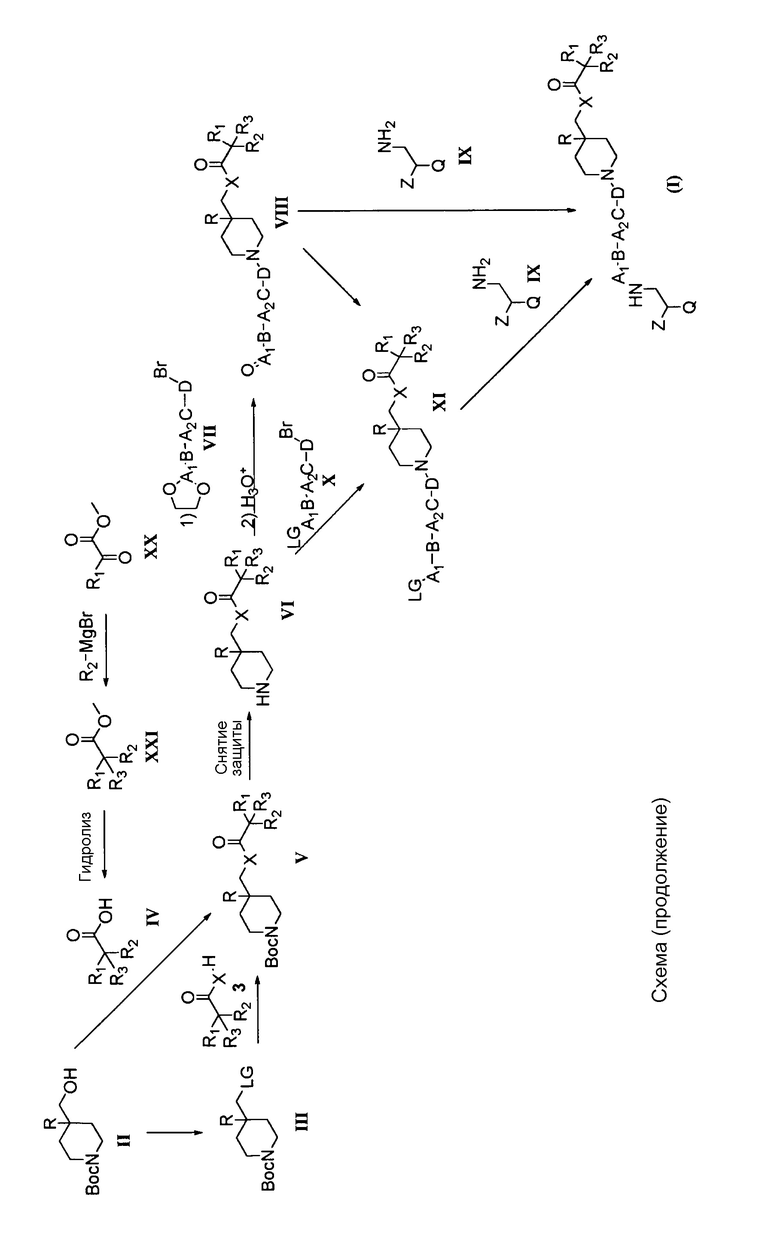
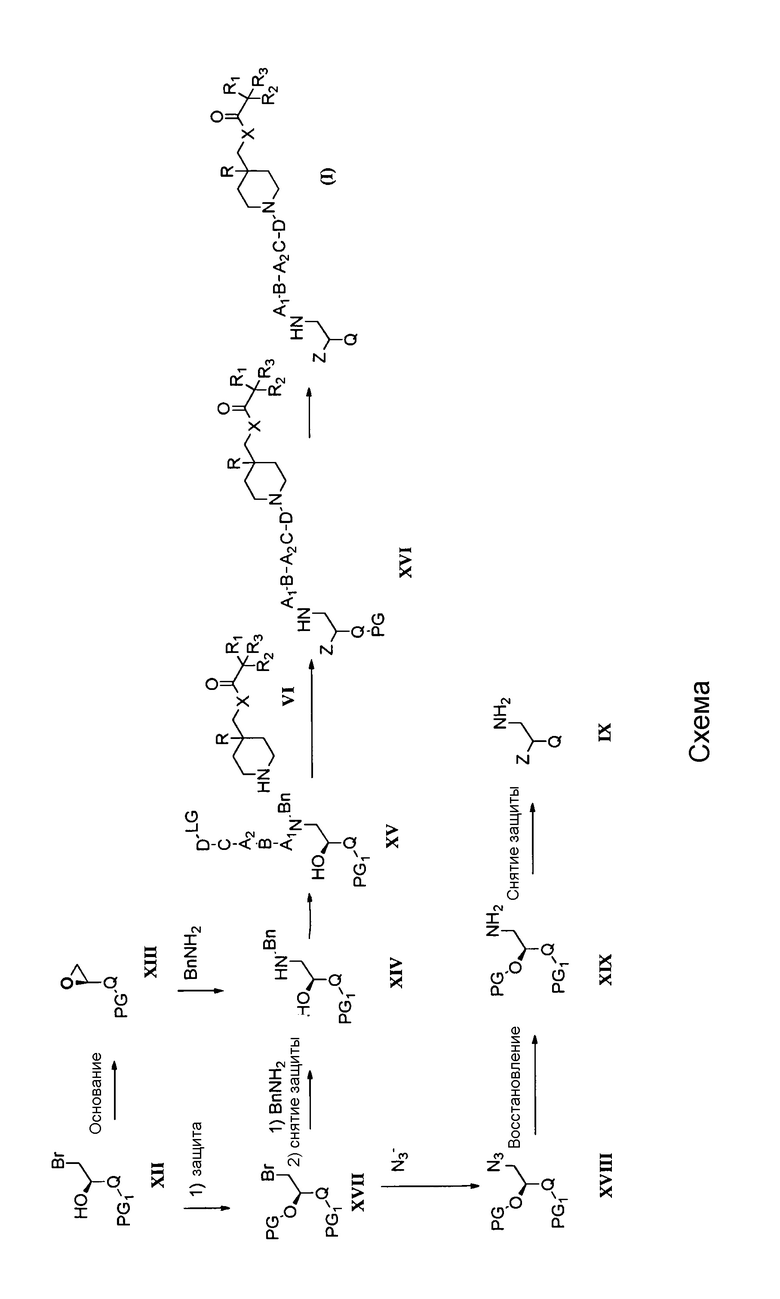
Общая методика получения соединений формулы (I)
Соединения общей формулы (I) можно получить несколькими различными способами, некоторые из которых представлены на схеме и применяются, например, для получения соединения общей формулы (I), в котором Y представляет собой группу формулы Y1 и в котором А1 представляет собой (С1-С6)алкилен, А2, В и С отсутствуют, а D представляет собой (С1-С6)алкилен. Это лишь неограничивающий пример. Аналогичный подход можно использовать для получения соединений общей формулы (I), в которых А1, А2, В, С и D имеют значения, приведенные выше, используя хорошо известные методики, описанные в литературе для введения определенных групп в органические соединения.
Соединения общей формулы VII обозначают соединение, в котором А1 представляет собой (С1-С6)алкилен, циклоалкилен или гетероциклоалкилен, замещенные оксогруппой, приводящие к альдегиду или кетону, имеющему защиту в виде циклического ацеталя. Данную циклическую ацетальную защитную группу можно удалить, получая соединение общей формулы VIII. В случае, когда А1 отсутствует, а В представляет собой циклоалкилен, гетероциклоалкилен или группу формулы В1, карбонильная группа, как таковая или защищенная, должна располагаться у группы В.
Для синтеза соединений общей формулы (I) может потребоваться защита потенциально реакционноспособной функциональной группы в дополнение к уже описанным способам. В этом случае примеры совместимых защитных групп и конкретные способы защиты и снятия защиты описаны в “Protective Groups in Organic Synthesis” T.W. Green and P. Wutz (Wiley-Interscience publication, 1999).
Соединения общей формулы (I), в которых Y представляет собой -(СН2)9-, можно получить, вводя во взаимодействие промежуточное соединение формулы IX с альдегидом формулы VIII (в котором R, R1, R2, R3, A1, A2, B, C, D, Z и Q имеют значения, приведенные выше) в условиях восстановительного аминирования. Данную реакцию можно провести в растворителе, таком как метанол, этанол, тетрагидрофуран (ТГФ) или дихлорметан (DCM). Методика проведения реакции зависит от используемого восстановителя. Например, в случае NaBH4 требуется предварительное получение имина, тогда как NaBCNH3 при рН=5, или NaAc3BH можно применять в «one-pot» реакции. Во всех случаях реакция завершается в течение промежутка времени от 1 до 12 ч при комнатной температуре (кт).
Промежуточные соединения формулы VIII можно легко получить алкилированием промежуточных соединений формулы VI подходящим защищенным альдегидом с последующим снятием защиты. Реакция алкилирования протекает в полярном апротонном растворителе, таком как ацетонитрил или диметилформамид (ДМФА), при температуре в интервале от кт до 100°С, и завершается в течение от 1 до 24 ч. Для инициирования реакции можно применять традиционное термическое или микроволновое нагревание.
Альтернативным образом, соединения формулы (I) можно получить алкилированием промежуточных соединений формулы IX соединениями формулы XI, в которых уходящая группа (LG) может представлять собой хлор, бром, мезил, тозил или другую известную уходящую группу, которая подходит для взаимодействия с амином. Реакция протекает в растворителе, таком как DCM, ТГФ, ацетонитрил или ДМФА при кт или более высокой температуре, и завершается в присутствии органического или неорганического основания в течение промежутка времени от 0,5 до 12 ч.
Промежуточные соединения формулы XI можно получить из соединений формулы VIII восстановлением альдегида с последующим превращением полученного спирта в соединения формулы XI под действием толуолсульфонилхлорида, метансульфонилхлорида, CBr4 и PPh3 или SOCl2. Все реакции должны проводиться в апротонном растворителе, таком как DCM или ТГФ. Промежуточные соединения формулы XI можно получить алкилированием соединения формулы VI бифункциональным реагентом формулы Х, таким как 1,9-дибромнонан в условиях реакции, аналогичных описанным для алкилирования соединения формулы VI соединением VII.
Промежуточные сложноэфирные соединения формулы VI можно легко получить стандартным синтезом сложных эфиров, исходя из кислоты IV и спирта II, с последующим снятием защиты с полученного соединения формулы V (для ссылки см. Protective Groups in Organic Synthesis Fourth Editions, Wiley-Interscience Publication). Реакцию получения сложного эфира можно провести в нескольких различных условиях в присутствии кислого активирующего агента, такого как дициклогексилкарбодиимид (DCC), гидрохлорид 1-этил-3-[3-диметиламинопропил]карбодиимида (EDC), гексафторфосфат 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (HBTU), или переводя сначала кислоту в соответствующий ацилхлорид действием SOCl2 или оксалилхлорида. Альтернативным образом, гидроксильную группу спирта II можно превратить в LG, как описано выше для получения промежуточного соединения XI из VIII, а затем вводя во взаимодействие с кислотой VI в полярном апротонном растворителе (например, ацетонитриле или ДМФА) в присутствии основания, например, такого как карбонат натрия, калия или цезия.
Альтернативный способ получения соединений общей формулы (I) включает алкилирование промежуточного соединения амина VI соединением XIV с последующим снятием ранее введенных защитных групп. Данную реакцию алкилирования можно осуществить в классических условиях реакции, уже описанных для получения промежуточного соединения VIII, исходя из VI.
Получение соединений формулы XIV можно осуществить реакцией промежуточного соединения XIII с бифункциональным реагентом, таким как, в случае данного примера, 1,9-дибромнонаном (как описано выше для получения промежуточного соединения VIII из VI), и можно легко распространить на получение других аналогов.
Промежуточные соединения формулы XIII можно получить обработкой эпоксида общей формулы XII бензиламинами. Данную реакцию можно провести в отсутствие растворителя или в высококипящем растворителе, таком как толуол, диоксан или бутанол. Реакция протекает гладко под действием термического или микроволнового нагревания и завершается в течение промежутка времени от 1 до 24 ч при температуре от 80 до 120°С. Другим образом данное промежуточное соединение можно получить алкилированием промежуточного соединения XVI в уже описанных условиях алкилирования амина алкилбромидами. Синтез промежуточных соединений общей формулы XI и XVI, в которых Q представляет собой группу формулы Q1, а PG1 представляет собой бензильную группу, защищающую фенольную гидроксильную группу, описан в патенте США 2004224982.
Промежуточные соединения общей формулы XII, в которых Q представляет собой группу формулы Q1, а PG1 представляет собой бензильную группу, защищающую фенольную гидроксильную группу, можно легко получить из промежуточного соединения XI, как описано в WO 2008/104781.
Получение промежуточного соединения IX, в котором Q представляет собой группу формулы Q1, а Z представляет собой ОН, можно осуществить из промежуточного соединения XVI реакцией с азидной солью щелочного металла в полярном растворителе, таком как ДМФА или ДМСО при 80°С или более высокой температуре с последующим хорошо известным восстановлением азида в условиях каталитического гидрирования или с использованием другого восстановителя, такого как PPh3, и удалением введенной защитной группы.
Соединения общей формулы IV являются коммерчески доступными, или, в случае, когда R1 и R2 имеют значения, приведенные выше, а R3 представляет собой гидроксил, могут быть получены реакцией подходящего α-кето эфира формулы ХХ с соответствующим реактивом Гриньяра формулы XXI. Реакцию осуществляют в апротонном растворителе, таком как ТГФ, при -20°С или более низкой температуре, и получают в результате кислоту общей формулы IV, где R1 и R2 имеют значения, приведенные выше, а R3 представляет собой гидроксильную группу.
Методы ХЖМС А и В, использованные для характеризации соединений настоящего изобретения, описаны далее:
Метод А (IS 10 см_ ESCI_Муравьиная кислота_MeCN)
Установка ВЭЖХ
Растворители: Ацетонитрил (качество Far UV grade) c добавкой 0,1% (об./об.) муравьиной кислоты
Вода (Высокой чистоты при помощи установки PureLab Option) с добавкой 0,1% муравьиной кислоты
Колонка: Phenomenex Luna 5 мкм С18 (2), 100×4,6 мм (Plus guard cartridge)
Скорость потока: 2 мл/мин
Градиент: А: вода/муравьиная кислота В: MeCN/муравьиная кислота
Ионизация представляет собой либо ионизацию электрораспыления (ESI), либо химическую ионизацию при атмосферном давлении (APCI).
УФ-детектирование с использованием HP или Waters DAD
Начальный интервал (нм) 210 Конечный интервал (нм) 400 Диапазон интервала (нм) 4,0
МС-детектирование
Micromass ZQ, одноквадрупольный прибор
Интервал сканирования для МС данных (m/z)
Начало (m/z) 100
Конец 650 или 1000 при необходимости
При +ve/-ve переключении
Метод В (IS 15 см_Муравьиная кислота_ASCENTIS_ВЭЖХ_CH3CN)
Установка ВЭЖХ
Растворители: Ацетонитрил (качество Far UV grade) c добавкой 0,1% (об./об.) муравьиной кислоты
Вода (Высокой чистоты с использованием установки PureLab Ultra) с добавкой 0,1% муравьиной кислоты
Колонка: Supelco, Ascentis® Express C18 или Hichrom Halo C18, 2,7 мкм С18, 150×4,6 мм.
Скорость потока: 1 мл/мин
Градиент: А: вода/муравьиная кислота В: MeCN/муравьиная кислота
Прибор: Agilent 1100, бинарный насос, пробоотборник Agilent и DAD детектор Agilent
Диодно-матричный детектор: (300 нм, ширина полосы 200 нм, этал. 450 нм, ширина полосы 100 нм)
В данном изобретении предоставлена также фармацевтическая композиция, содержащая соединения формулы (I) в смеси с одним или более фармацевтически приемлемыми носителями, например, носителями, описанными в Remington’s Pharmaceutical Sciences Handbook, XVII Ed., Mack Pub., N.Y., USA.
Введение соединений настоящего изобретения можно осуществлять в соответствии с потребностями пациента, например, перорально, назально, парентерально (подкожно, внутривенно, внутримышечно, интрастернально или путем инфузии), путем ингаляции, ректально, вагинально, местно, локально, чрескожно и путем глазного введения.
Для введения соединений данного изобретения можно применять различные твердые пероральные лекарственные формы, включая такие твердые формы, как таблетки, желатиновые капсулы, капсулы, капсуловидные таблетки, гранулы, пастилки и нерасфасованные порошки. Соединения настоящего изобретения можно вводить индивидуально или соединять с различными фармацевтически приемлемыми носителями, разбавителями (такими как сахароза, маннит, лактоза, крахмалы) и известными эксципиентами, включая суспендирующие агенты, солюбилизаторы, буферные вещества, связывающие вещества, разрыхлители, консерванты, красители, вкусовые вещества, смазывающие вещества и так далее. При введении соединений настоящего изобретения предпочтительны также капсулы с замедленным высвобождением, таблетки и гели.
Для введения соединений данного изобретения можно также использовать различные жидкие пероральные лекарственные формы, включая водные и неводные растворы, эмульсии, суспензии, сиропы и эликсиры. Подобные лекарственные формы могут также включать подходящие известные инертные разбавители, такие как вода, и подходящие известные эксципиенты, такие как консерванты, увлажняющие агенты, подсластители, вкусовые вещества, а также вещества для эмульгирования и/или суспендирования соединений данного изобретения. Соединения настоящего изобретения можно вводить в виде инъекций, например, внутривенно, в виде изотонического стерильного раствора. Возможны также другие препараты.
Суппозитории для ректального введения соединений можно получить, смешивая соединение с подходящим эксципиентом, таким как масло какао, салицилаты и полиэтиленгликоли.
Известны также препараты для вагинального введения, которые могут находиться в форме крема, геля, пасты, пены или спреевого состава, содержащие, помимо активного ингредиента, дополнительные ингредиенты, такие как подходящие носители.
Для местного применения фармацевтическая композиция может находиться в форме кремов, мазей, линиментов, лосьонов, эмульсий, суспензий, гелей, растворов, паст, порошков, спреев и капель, подходящих для введения на кожу, глаз, ухо или нос. Местное введение может также включать чрескожное введение с помощи таких средств, как чрескожные пластыри.
Для лечения заболеваний дыхательных путей соединения согласно данному изобретению предпочтительно вводят ингаляцией.
Ингалируемые препараты включают ингалируемые порошки, дозированные аэрозоли, содержащие пропеллент, или ингалируемые препараты, не содержащие пропеллента.
Для введения в виде сухого порошка можно применять однодозовые или многодозовые ингаляторы, известные из предшествующей области техники. В таком случае порошок можно помещать в желатиновые, пластиковые или другие капсулы, картриджи или блистерные упаковки, или в резервуар.
К порошкообразным соединениям данного изобретения можно добавить разбавитель или носитель, как правило, нетоксичный и химически инертный к соединениям изобретения, например, лактозу или другую добавку, подходящую для улучшения респирабельной фракции.
Ингалируемые аэрозоли, содержащие препеллент, такой как гидрофторалканы, могут включать соединения изобретения либо в виде раствора, либо в диспергированной форме. Доставляемые при помощи пропеллента препараты могут также содержать другие ингредиенты, такие как сорастворители, стабилизаторы и, необязательно, другие эксципиенты.
Не содержащие пропеллента ингалируемые препараты, включающие соединения данного изобретения, могут находиться в форме растворов или суспензий в водной, спиртовой или водно-спиртовой среде, и их можно доставлять при помощи компрессорных или ультразвуковых небулайзеров, известных из предшествующей области техники, или при помощи жидкостных небулайзеров, таких как Respimat®.
Соединения данного изобретения можно вводить в виде индивидуального активного вещества или в комбинации с другими фармацевтически активными ингредиентами, включая ингредиенты, применяемые в настоящее время при лечении респираторных заболеваний, например, кортикостероиды, ингибиторы МАР-киназ р38, IKK2, ингибиторы HNE, ингибиторы PDE4, модуляторы лейкотриена, NSAID и регуляторы муковисцидоза.
Дозировки соединений данного изобретения зависят от ряда факторов, включая конкретное заболевание, подлежащее лечению, тяжесть симптомов, способ введения, интервал между дозами, конкретное применяемое соединение, эффективность, токсикологический профиль и фармакокинетический профиль соединения.
Предпочтительно, соединения формулы (I) можно вводить, например, в дозе от 0,001 до 1000 мг/день, предпочтительно от 0,1 до 500 мг/день.
В случае введения соединений формулы (I) ингаляционным способом, их предпочтительно дают в дозе, находящейся в интервале от 0,001 до 500 мг/день, предпочтительно от 0,1 до 200 мг/день.
Соединения формулы (I) можно вводить для предупреждения и/или лечения бронхообструктивных или воспалительных заболеваний, таких как астма, хронический бронхит, хроническая обструктивная болезнь легких (COPD), бронхиальная гиперреактивность, кашель, эмфизема или ринит; урологических нарушений, таких как недержание мочи, поллакиурия, цистоспазм, хронический цистит и гиперактивный мочевой пузырь (ОАВ); нарушений деятельности желудочно-кишечного тракта, таких как синдром раздраженного кишечника, спастический колит, дивертикулит, пептическая язва, нарушение моторики желудочно-кишечного тракта, или секреции желудочного сока; сухость во рту; мидриаз, тахикардия; сердечно-сосудистые нарушения, вызванные офтальмологическими вмешательствами, такие как синусная брадикардия, обусловленная блуждающим нервом.
Далее настоящее изобретение будет дополнительно описано при помощи следующих примеров.
Промежуточные соединения для синтеза конечных соединений общей формулы (I) получали по описанным далее методикам.
Получение промежуточного соединения 1
9-Бромнонаналь
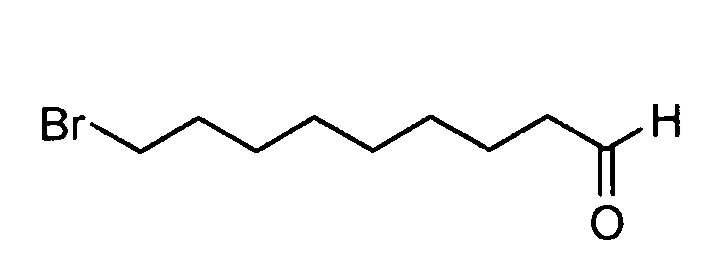
Хлорформиат пиридиния (38,7 г, 180 ммоль) и силикагель 60А (39 г, размер частиц 35-70 микрон), суспендированные в дихлорметане (250 мл), перемешивали при кт в течение 45 мин. Прибавляли 9-бромнонанол (26,7 г, 120 ммоль) в виде одной порции, и перемешивали суспензию при кт в течение 18 ч. Реакционную смесь фильтровали через колонку с целлитом, и концентрировали полученный фильтрат в вакууме, получая указанное в заголовке соединение (28,0 г, >100%).
Вещество использовали без дополнительной очистки на следующей стадии.
1H ЯМР (400 МГц, CHCl3-d): δ 9,77 (с, 1Н), 3,41 (т, 2Н), 2,43 (т, 2Н), 1,90-1,80 (м, 2Н), 1,63 (с, 2Н), 1,43 (с, 2Н), 1,32 (с, 6Н).
Получение промежуточного соединения 2
2-(8-Бромоктил)-1,3-диоксолан
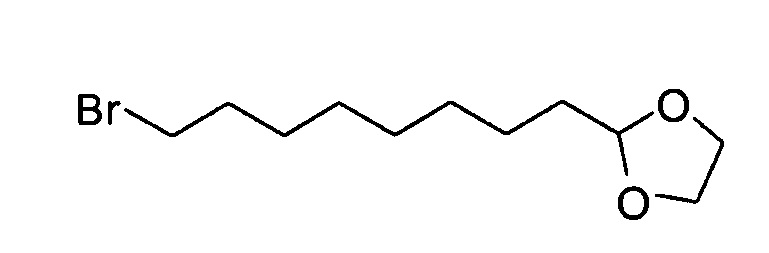
9-Бромнонаналь (28,0 г, предположительно 120 ммоль), этиленгликоль (33,6 мл, 600 ммоль) и паратолуолсульфоновую кислоту (2,7 г, 13 ммоль) в толуоле (210 мл) нагревали с обратным холодильником в течение 20 ч. Реакционную смесь охлаждали до кт и гасили насыщенным водным раствором бикарбоната натрия (300 мл). Полученную смесь экстрагировали диэтиловым эфиром (×2). Объединенные органические экстракты промывали насыщенным водным раствором бикарбоната натрия, водой и насыщенным раствором соли (100 мл). Органическую фазу сушили (сульфат магния), фильтровали и упаривали при пониженном давлении, получая указанное в заголовке соединение (25,2 г, 79%).
1H ЯМР (400 МГц, CHCl3-d): δ 4,84 (т, 1Н), 3,95-3,78 (м, 4Н), 3,43-3,37 (м, 2Н), 1,90-1,79 (м, 2Н), 1,69-1,54 (м, 2Н), 1,42 (с, 3Н), 1,32 (с, 7Н).
Все остальные 1,3-диоксоланы (т.е. 2-(7-бромгептил)-1,3-диоксолан, 2-(6-бромгексил)-1,3-диоксолан, 2-(5-бромпентил)-1,3-диоксолан и 2-(4-бромбутил)-1,3-диоксолан) получали таким же способом.
Получение промежуточного соединения 3
8-(Бензилокси)-5-(2-бромацетил)хинолин-2(1Н)-он
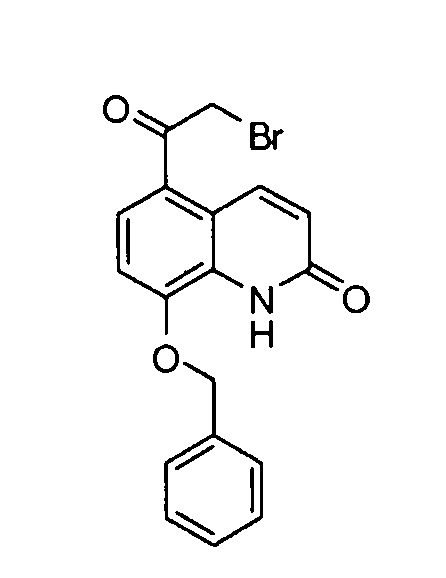
К суспензии 5-ацетил-8-(бензилокси)хинолин-2(1Н)-она (19,4 г, 66,4 ммоль) в безводном ТГФ (240 мл) и безводном метаноле (165 мл) прибавляли по каплям раствор трибромида тетра-н-бутиламмония (54,5 г, 113,0 ммоль) в безводном ТГФ (130 мл) в течение 1,5 ч. Полученный раствор перемешивали при кт в течение ночи перед концентрированием его при пониженном давлении без нагревания. Остаток повторно растворяли в метаноле (200 мл). Прибавляли насыщенный водный раствор хлорида аммония (390 мл) при охлаждении льдом. Полученную суспензию фильтровали, и осадок промывали водой и сушили в вакууме. Твердое вещество суспендировали в дихлорметане и метаноле (1:1 об./об., 100 мл) в течение 90 мин. Осадок выделяли фильтрованием, промывали дихлорметаном и сушили на воздухе, получая указанное в заголовке соединение (18,0 г, 73%).
1H ЯМР (400 МГц, CDCl3-d): δ 9,23 (уш.с, 1Н), 8,78 (д, 1Н), 7,67 (д, 1Н), 7,40 (с, 5Н), 7,03 (д, 1Н), 6,75 (д, 1Н), 5,25 (с, 2Н), 4,42 (с, 2Н).
Получение промежуточного соединения 4
(R)-8-(Бензилокси)-5-(2-бром-1-гидроксиэтил)хинолин-2(1Н)-он
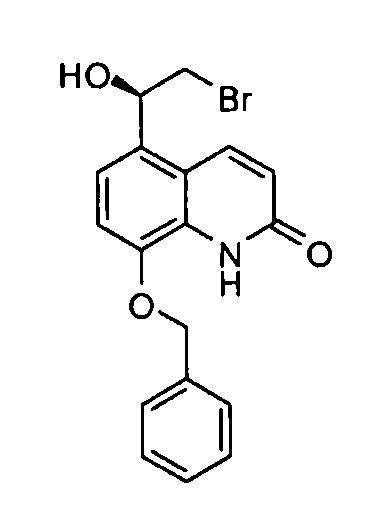
8-(Бензилокси)-5-(2-бромацетил)хинолин-2(1Н)-он (26,0 г, 69,9 ммоль) и (R)-3,3-дифенил-1-метилтетрагидро-3Н-пирроло[1,2-c][1,3,2]оксазаборол (21,3 г, 76,8 ммоль) подвергали азеотропной сушке с толуолом (×3), затем суспендировали в безводном ТГФ (400 мл) в атмосфере азота. Суспензию охлаждали до -20°С (внешняя температура) и прибавляли раствор комплекса борана с диметилсульфидом (45,4 мл, 90,8 ммоль, 2,0 М раствор в ТГФ) при помощи шприцевого насоса в течение 3 ч. По окончании прибавления реакционную смесь перемешивали в течение часа перед гашением метанолом (25 мл). Реакционную смесь нагревали до кт в течение 20 мин. Смесь концентрировали в вакууме и суспендировали остаток в водной соляной кислоте (500 мл, 1 М раствор) и перемешивали при кт в течение 18 ч. После этого осадок выделяли фильтрованием и промывали водой (×3). Твердое вещество частично растворяли в этилацетате и нагревали с обратным холодильником в течение 2 ч. Оставшееся твердое вещество удаляли горячим фильтрованием, и упаривали фильтрат, получая указанное в заголовке соединение. Твердое вещество, выделенное из горячего этилацетата, снова частично растворяли в этилацетате и нагревали с обратным холодильником в течение 2 ч, затем фильтровали, получая фильтрат, содержащий чистый продукт. Этот процесс повторяли еще четыре раза. Объединенный осадок перекристаллизовывали из этилацетата и петролейного эфира, получая указанное в заголовке соединение (20,0 г, 76%).
1H ЯМР (400 МГц, ДМСО): δ 10,68 (с, 1Н), 8,19 (д, J=9,9 Гц, 1Н), 7,58 (д, J=7,5 Гц, 2Н), 7,41-7,36 (м, 2Н), 7,34-7,29 (м, 1Н), 7,23-7,19 (м, 2Н), 6,57 (д, J=9,8 Гц, 1Н), 5,94 (д, J=4,7 Гц, 1Н), 5,31 (с, 2Н), 5,25-5,19 (м, 1Н), 3,71-3,58 (м, 2Н).
Получение промежуточного соединения 5
(R)-8-(Бензилокси)-5-(2-бром-1-(трет-бутилдиметилсилилокси)этил)хинолин-2(1Н)-он
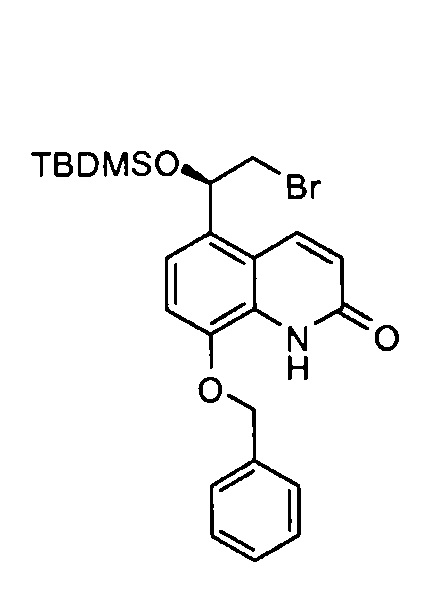
К раствору (R)-8-(бензилокси)-5-(2-бром-1-гидроксиэтил)хинолин-2(1Н)-она (10,1 г, 27 ммоль) в дихлорметане (100 мл) прибавляли 2,6-лутидин (6,9 мл, 59,5 ммоль) при 0°С. Реакционную смесь перемешивали в течение 5 мин, затем прибавляли по каплям трет-бутилдиметилсилил трифторметансульфонат (13,0 мл, 56,8 ммоль) в течение 15 мин. Смесь перемешивали при 0°С в течение 30 мин, затем при кт в течение ночи. После этого реакционную смесь гасили насыщенным водным раствором бикарбоната натрия и экстрагировали дихлорметаном (×3). Объединенные органические экстракты сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. К сырому веществу прибавляли изогексан (500 мл) и выделяли полученный осадок фильтрованием. Твердое вещество перекристаллизовывали из этилацетата и петролейного эфира (40:60), получая указанное в заголовке соединение (11,3 г, 85%).
1H ЯМР (400 МГц, CHCl3-d): δ 9,19 (с, 1Н), 8,23 (дд, J=9,9, 4,4 Гц, 1Н), 7,43 (д, J=4,6 Гц, 5Н), 7,17 (дд, J=8,3, 4,5 Гц, 1Н), 7,03 (дд, J=8,2, 4,4 Гц, 1Н), 6,71 (дд, J=9,9, 3,7 Гц, 1Н), 5,18 (д, J=4,5 Гц, 3Н), 3,63-3,56 (м, 1Н), 3,49 (дд, J=10,4, 4,8 Гц, 1Н), 0,88 (т, J=4,4 Гц, 9Н), 0,14 (д, J=4,4 Гц, 3H), -0,11 (д, J=4,4 Гц, 3Н).
Получение промежуточного соединения 6
(R)-5-(2-Азидо-1-(трет-бутилдиметилсилилокси)этил)-8-(бензилокси)хинолин-2(1Н)-он

(R)-8-(Бензилокси)-5-(2-бром-1-(трет-бутилдиметилсилилокси)этил)хинолин-2(1Н)-он (5,0 г, 10,2 ммоль) растворяли в диметилформамиде (90 мл) и воде (10 мл). Последовательно прибавляли йодид натрия (1,7 г, 11,3 ммоль) и азид натрия (0,7 г, 11,3 ммоль). Реакционную смесь перемешивали при кт до растворения всех твердых веществ. Раствор нагревали при 80°С в течение 40 ч, затем охлаждали до кт и разбавляли водой (300 мл). Водный слой экстрагировали дихлорметаном, а объединенные органические экстракты сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. Сырой остаток перекристаллизовывали из этилацетата и изогексана, получая требуемое соединение (3,6 г, 78%), использованное на следующей стадии без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3-d): δ 9,19 (с, 1Н), 8,18 (д, J=9,9 Гц, 1Н), 7,45-7,36 (м, 4Н), 7,20 (д, J=8,3 Гц, 1Н), 7,04 (д, J=8,3 Гц, 1Н), 6,70 (дд, J=9,9, 2,2 Гц, 1Н), 5,19-5,13 (м, 3Н), 3,48 (дд, J=12,7, 8,1 Гц, 1Н), 3,26 (дд, J=12,7, 3,8 Гц, 1Н), 0,89 (с, 9Н), 0,14 (с, 3Н), -0,11 (с, 3Н).
Получение промежуточного соединения 7
(R)-5-(2-Амино-1-(трет-бутилдиметилсилилокси)этил)-8-гидроксихинолин-2(1Н)-он формиат
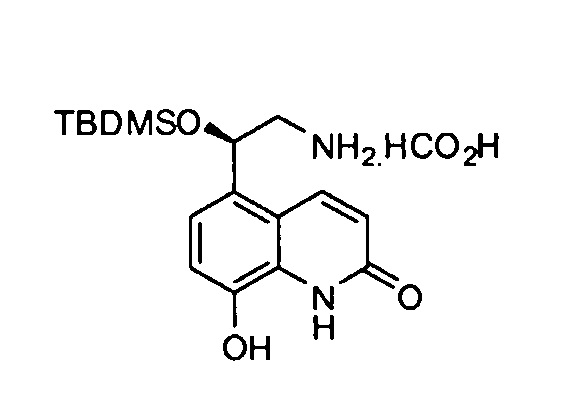
К суспензии (R)-5-(2-азидо-1-(трет-бутилдиметилсилилокси)этил)-8-(бензилокси)хинолин-2(1Н)-она (2,05 г, 4,60 ммоль) и формиата аммония (2,87 г, 63 ммоль) в метаноле (50 мл) прибавляли палладий на активированном угле (0,4 г, 10% мас./мас.). Реакционную смесь нагревали при 80°С в течение 1 ч, а затем фильтровали через целит, промывая водой. Реакционную смесь концентрировали при пониженном давлении. Полученное твердое вещество промывали водой, растирали в этилацетате и выделяли фильтрованием, получая указанное в заголовке соединение (1,32 г, 86%).
1H ЯМР (400 МГц, ДМСО): δ 8,34 (с, 1Н), 8,31-8,22 (м, 1Н), 7,03 (д, J=8,1 Гц, 1Н), 6,98-6,90 (м, 1Н), 6,53 (д, J=9,9 Гц, 1Н), 5,13 (т, J=6,0 Гц, 1Н), 3,18 (с, 1Н), 2,84-2,73 (м, 2Н), 0,83 (с, 9Н), 0,06 (с, 3Н), -0,17 (с, 3Н).
(R)-5-(2-Амино-1-(трет-бутилдиметилсилилокси)этил)-8-гидроксихинолин-2(1Н)-он
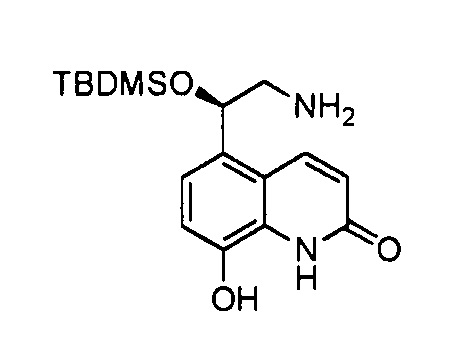
К охлажденной льдом суспензии палладия на активированном угле (4,50 г, 10% мас./мас.) и (R)-5-(2-азидо-1-(трет-бутилдиметилсилилокси)этил)-8-(бензилокси)хинолин-2(1Н)-она (4,50 г, 10,0 ммоль) в этаноле (50 мл) прибавляли по каплям 1-метил-1,4-циклогексадиен (11,0 мл, 97,9 ммоль). Охлаждающую среду отставляли и перемешивали суспензию при температуре окружающей среды в течение 10 мин, а затем нагревали при 50°С в течение одного часа. Реакционной смеси давали остыть и фильтровали суспензию через целит. Остаток на фильтре промывали дополнительным количеством этанола и концентрировали объединенные фильтраты при пониженном давлении. Остаток растирали с ацетонитрилом, получая указанное в заголовке соединение (3,03 г, 90%).
Получение промежуточного соединения 8
Гидрохлорид (R)-5-(2-амино-1-гидроксиэтил)-8-гидроксихинолин-2(1Н)-она
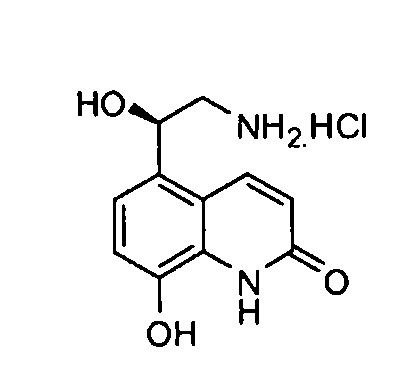
(R)-5-(2-Амино-1-(трет-бутилдиметилсилилокси)этил)-8-гидроксихинолин-2(1Н)-он формиат (0,23 г, 0,61 ммоль) растворяли в соляной кислоте (5 мл, 4 М раствор в диоксане) и метаноле (5 мл). Реакционную смесь перемешивали при кт в течение 16 ч перед концентрированием в вакууме. Полученный остаток промывали этилацетатом и сушили в вакуумной печи в течение 18 ч, получая указанное в заголовке соединение (0,15 г, 99%).
1H ЯМР (400 МГц, CD3OD): δ 7,71 (д, J=9,8 Гц, 1Н), 6,57 (д, J=8,2 Гц, 1Н), 6,31 (д, J=8,2 Гц, 1Н), 6,02 (дд, J=9,8, 6,5 Гц, 1Н), 4,58 (дд, J=9,6, 3,5 Гц, 1Н), 2,47-2,31 (м, 2Н).
Получение промежуточного соединения 9
Этил 2-гидрокси-2-фенил-2-(тиофен-3-ил)ацетат
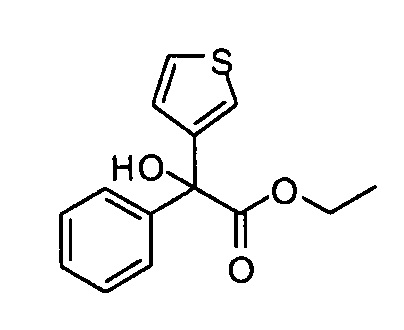
К перемешиваемому раствору этилбензоилформиата (1,30 г, 7,30 ммоль) в ТГФ (5 мл) при -78°С в атмосфере азота прибавляли 3-тиенилмагниййодид (29,2 мл, 8,76 ммоль) в течение 10 мин. После перемешивания при -78°С в течение 1 ч, реакционную смесь оставляли нагреваться до кт и перемешивали в течение ночи. Реакционную смесь гасили насыщенным водным раствором хлорида аммония и экстрагировали этилацетатом (×3). Объединенные органические экстракты промывали насыщенным раствором соли, сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. Сырое вещество очищали колоночной хроматографией на силикагеле, элюируя 0-10% этилацетата в изогексане, получая указанное в заголовке соединение (1,06 г, 55%).
1H ЯМР (400 МГц, CDCl3-d): δ 7,45-7,39 (м, 2Н), 7,37-7,28 (м, 5Н), 7,12-7,09 (м, 1Н), 4,38-4,28 (м, 2Н), 4,30-4,25 (м, 1Н), 1,32-1,24 (м, 3Н).
Получение промежуточного соединения 10
2-Гидрокси-2-фенил-2-(тиофен-3-ил)уксусная кислота
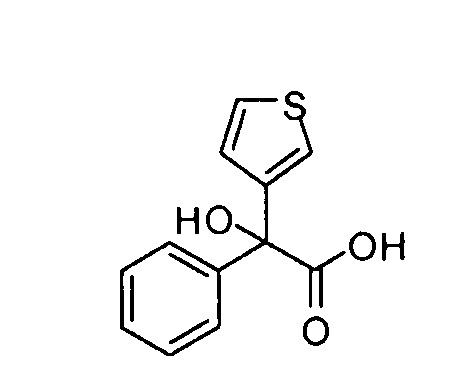
К перемешиваемому раствору этил 2-гидрокси-2-фенил-2-(тиофен-3-ил)ацетата (1,06 г, 4,02 ммоль) в ТГФ (10 мл) прибавляли гидроксид натрия (10 мл, 2,0 М водный раствор). Реакционную смесь нагревали при 60°С в течение 24 ч. Реакционной смеси давали остыть до кт и удаляли ТГФ при пониженном давлении. Полученный остаток промывали диэтиловым эфиром (×3). Водный слой подкисляли до рН 1 2,0 М водной соляной кислотой и экстрагировали этилацетатом (×3). Объединенные этилацетатные слои промывали насыщенным раствором хлорида натрия, сушили (сульфат магния), фильтровали и концентрировали в вакууме, получая указанное в заголовке соединение (0,75 г, 79%).
1H ЯМР (400 МГц, CDCl3-d): δ 13,20 (уш.с, 1H), 7,52 (д, J=2 Гц, 1H), 7,49-7,28 (м, 6Н), 7,05 (д, J=2 Гц, 1Н), 6,56 (уш.с, 1Н).
Конечные соединения получали, как описано далее, используя соответствующую кислоту (1) и соответствующие бром-1,3-диоксоланы.
Получение промежуточного соединения 11
Трет-бутил 4-(тозилоксиметил)пиперидин-1-карбоксилат
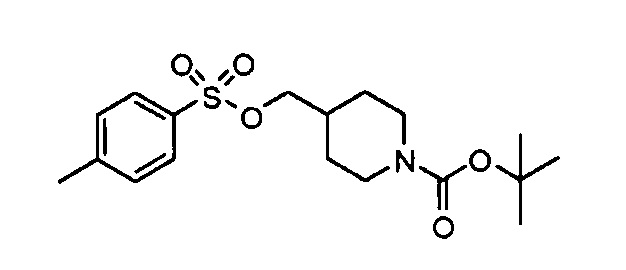
К перемешиваемому раствору трет-бутил 4-(гидроксиметил)пиперидин-1-карбоксилата (5,0 г, 23,2 ммоль) в безводном пиридине (18,5 мл) при 0°С в атмосфере азота прибавляли п-толуолсульфонилхлорид (4,87 г, 25,55 ммоль) в виде одной порции. Реакционную смесь перемешивали при 0°С в течение 100 мин перед нагреванием до кт. Через 18 ч реакционную смесь выливали в воду (100 мл) и экстрагировали этилацетатом (3×50 мл). Объединенные органические экстракты промывали водной соляной кислотой (2×100 мл, 1,0 М раствор), насыщенным раствором хлорида натрия, сушили (сульфат магния), фильтровали и концентрировали в вакууме, получая указанное в заголовке соединение (7,87 г, 91%).
1H ЯМР (400 МГц, CDCl3-d): δ 7,77-7,70 (м, 2Н), 7,31 (д, J=8,0 Гц, 2Н), 3,80 (д, J=6,5 Гц, 2Н), 2,61 (д, J=13,1 Гц, 2Н), 2,41 (с, 3Н), 1,84-1,72 (м, 1Н), 1,60 (д, J=13,1 Гц, 2Н), 1,46-1,36 (м, 9Н), 1,05 (ддд, J=24,9, 12,5, 4,4 Гц, 2Н), -0,05 (т, J=3,3 Гц, 2Н).
Получение промежуточного соединения 12
Трет-бутил 4-((2-циклогексил-2-гидрокси-2-фенилацетокси)метил)пиперидин-1-карбоксилат
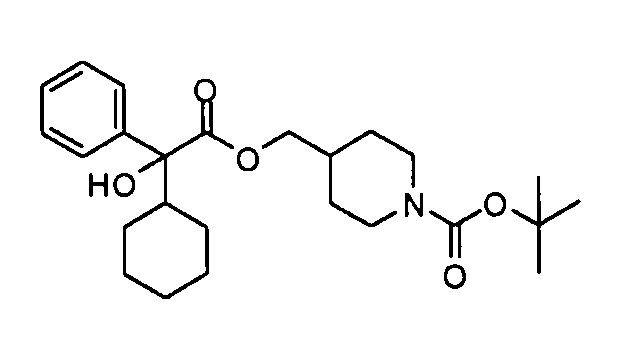
К трет-бутил 4-(бромметил)пиперидин-1-карбоксилату (957 мг, 3,44 ммоль) и карбонату калия (713 мг) в диметилформамиде (10 мл) прибавляли циклогексилминдальную кислоту (885 мг, 3,78 ммоль) при кт при перемешивании. Через 72 ч реакционную смесь разбавляли этилацетатом и водой. Органические экстракты промывали насыщенным раствором хлорида натрия, сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. Сырую реакционную смесь очищали колоночной хроматографией на силикагеле, элюируя 0-30% этилацетата в изогексане, получая указанное в заголовке соединение (1,10 г, 75%).
1H ЯМР (400 МГц, CDCl3-d): δ 7,64-7,59 (м, 2Н), 7,37-7,30 (м, 2Н), 7,31-7,25 (м, 1Н), 4,15-4,04 (м, 2Н), 4,05-3,97 (м, 2Н), 3,68 (с, 1Н), 2,73-2,60 (м, 2Н), 2,28-2,17 (м, 1Н), 1,83-1,76 (м, 2Н), 1,70-1,53 (м, 4Н), 1,46 (с, 9Н), 1,42 (дд, J=8,3, 3,4 Гц, 2H), 1,32-1,03 (м, 7Н).
Получение промежуточного соединения 13
Гидрохлорид пиперидин-4-илметил 2-циклогексил-2-гидрокси-2-фенилацетата
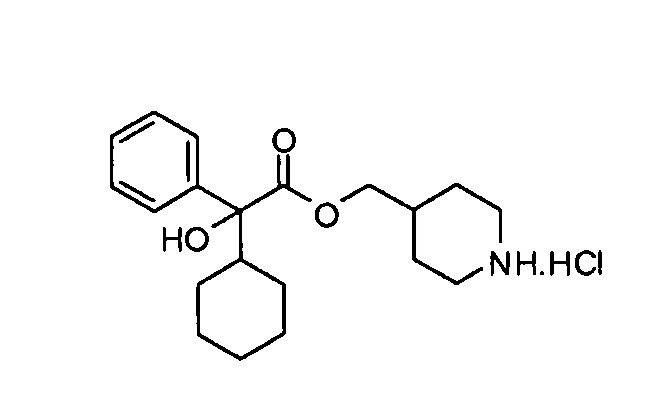
Трет-бутил 4-((2-циклогексил-2-гидрокси-2-фенилацетокси)метил)пиперидин-1-карбоксилат (1,10 г, 2,55 ммоль) растворяли в соляной кислоте (5 мл, 4 М раствор в диоксане) и дихлорметане (5 мл). Реакционную смесь перемешивали при кт в течение 3 ч и концентрировали при пониженном давлении, получая указанное в заголовке соединение (970 мг, >100%), которое использовали на следующей стадии без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3-d): δ 9,79-9,64 (уш.с, 1Н), 9,58-9,40 (уш.с, 1Н), 7,63-7,59 (м, 2Н), 7,37-7,30 (м, 2Н), 7,29-7,25 (м, 1Н), 4,10 (дд, J=11,0, 6,3 Гц, 1Н), 4,03-3,97 (м, 1Н), 3,65 (с, 1Н), 3,47 (д, J=13,0 Гц, 2Н), 2,79 (с, 2Н), 2,29-2,22 (м, 1Н), 1,92-1,61 (м, 8Н), 1,51-1,23 (м, 4Н), 1,21-1,05 (м, 3Н).
Получение промежуточного соединения 14
(1-(9-(1,3-Диоксолан-2-ил)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат
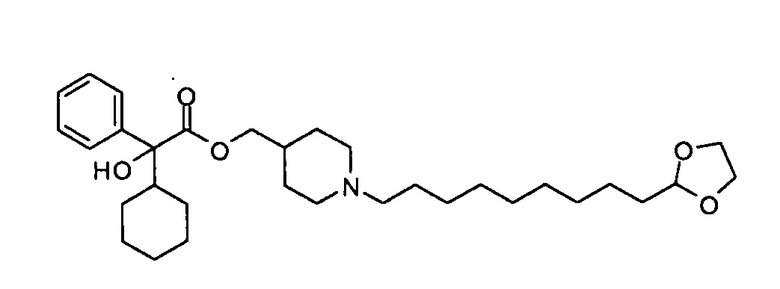
К раствору гидрохлорида пиперидин-4-илметил 2-циклогексил-2-гидрокси-2-фенилацетата (252 мг, 0,69 ммоль) в ацетонитриле (4 мл) прибавляли 2-(8-бромоктил)-1,3-диоксолан (218 мг, 0,82 ммоль), затем диизопропилэтиламин (361 мкл, 2,07 ммоль). Реакционную смесь нагревали при 60°С в течение 17 ч. После этого реакционную смесь охлаждали до кт и разбавляли дихлорметаном. Органические экстракты промывали водой, фильтровали через гидрофобный фильтрующий элемент и концентрировали при пониженном давлении. Сырое вещество очищали колоночной хроматографией на силикагеле, элюируя от 100% дихлорметана до смеси дихлорметан:метанол 40:1, получая указанное в заголовке соединение, которое использовали на следующей стадии без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3-d): δ 7,63 (д, J=7,8 Гц, 2Н), 7,33 (т, J=7,7 Гц, 2Н), 4,84 (т, J=4,8 Гц, 1Н), 4,03-3,93 (м, 3Н), 3,87-3,82 (м, 2Н), 3,69 (с, 1Н), 2,94 (с, 2Н), 2,37-2,20 (м, 3Н), 1,96-1,72 (м, 3Н), 1,70-1,06 (м, 32Н).
Получение промежуточного соединения 15
(1-(10-Оксодецил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат
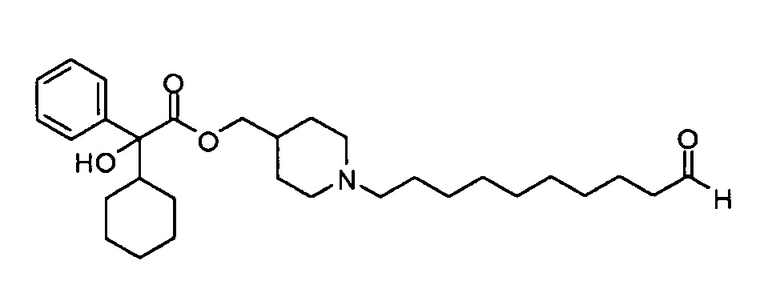
(1-(9-(1,3-Диоксолан-2-ил)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат (200 мг, 0,39 ммоль) растворяли в ТГФ (2 мл) и прибавляли соляную кислоту (4 мл, 2 М водный раствор) при перемешивании при кт. Через 3 ч реакционную смесь разбавляли этилацетатом, промывали 10%-ным водным раствором карбоната калия. Слои разделяли, и пропускали органические экстракты через гидрофобный фильтрующий элемент. Растворители удаляли в вакууме. Указанное в заголовке соединение выделяли (190 мг, >100%) и использовали его на следующей стадии без дополнительной очистки.
Получение промежуточного соединения 16
Трет-бутил 4-((2-гидрокси-2-фенил-2-(тиофен-3-ил)ацетилокси)метил)пиперидин-1-карбоксилат
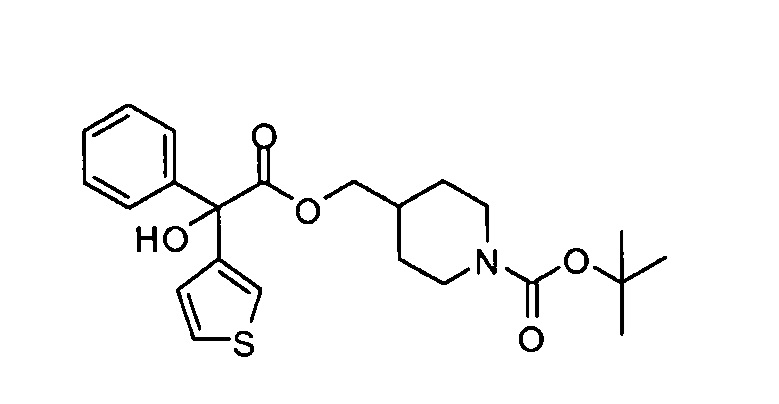
К перемешиваемому раствору 2-гидрокси-2-фенил-2-(тиофен-3-ил)уксусной кислоты (0,75 г, 3,197 ммоль) в толуоле (4 мл) и диметилформамиде (0,4 мл) прибавляли 1,8-диазабицикло[5.4.0]ундец-7-ен (735 мкл, 4,919 ммоль), затем трет-бутил 4-(тозилоксиметил)пиперидин-1-карбоксилат (0,909 г, 2,459 ммоль) в толуоле (3,5 мл) и диметилформамиде (0,35 мл). Реакционную смесь нагревали при 100°С в течение ночи. После этого реакционную смесь охлаждали до кт и концентрировали в вакууме. Сырое вещество очищали колоночной хроматографией на силикагеле, при элюировании с градиентом изогексан:этилацетат (от 1:0 до 3:1), получая указанное в заголовке соединение (0,84 г, 79%).
1H ЯМР (400 МГц, CDCl3-d): δ 7,44-7,38 (м, 2Н), 7,37-7,28 (м, 5Н), 7,08 (дд, J=5,0, 1,4 Гц, 1Н), 4,24 (с, 1Н), 4,13-4,05 (м, 2Н), 2,76-2,44 (м, 3Н), 1,82-1,69 (м, 1Н), 1,64-1,26 (м, 12Н); 1,11-0,98 (м, 2Н).
Получение промежуточного соединения 17
Пиперидин-4-илметил 2-циклогексил-2-гидрокси-2-фенилацетат тозилат
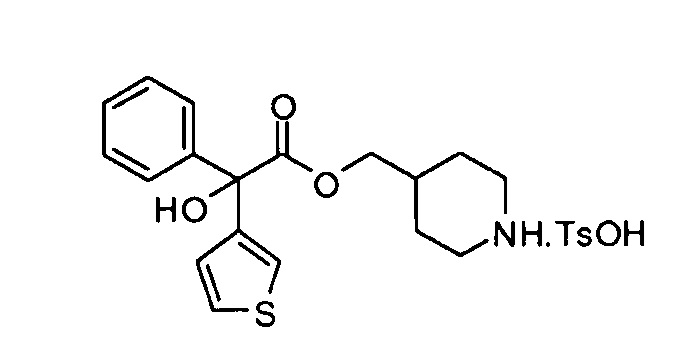
К перемешиваемому раствору трет-бутил 4-((2-гидрокси-2-фенил-2-(тиофен-3-ил)ацетилокси)метил)пиперидин-1-карбоксилата (0,84 г, 1,94 ммоль) в ацетонитриле (10 мл) прибавляли моногидрат п-толуолсульфоновой кислоты (0,55 г, 2,91 ммоль). Реакционную смесь перемешивали при 30°С в течение ночи, а затем концентрировали при пониженном давлении, получая указанное в заголовке соединение (1,17 г, >100%), которое использовали на следующей стадии без дополнительной очистки.
Получение промежуточного соединения 18
Трет-бутил 4-((3-гидрокси-2,2-дифенилпропаноилокси)метил)пиперидин-1-карбоксилат использовали для получения соединения примера 20
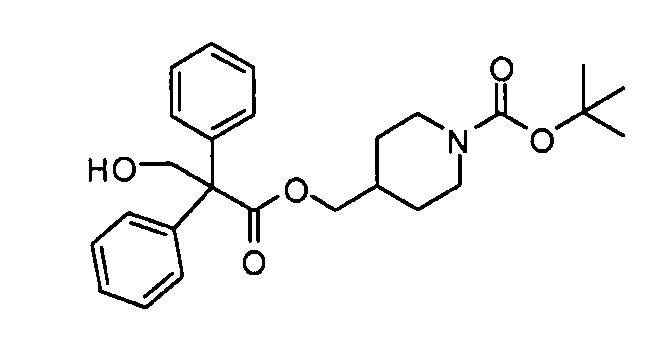
Трет-бутил 4-((2,2-дифенилацетилокси)метил)пиперидин-1-карбоксилат (полученный, как в случае получения промежуточного соединения 12, заменяя циклогексилминдальную кислоту 2,2-дифенилуксусной кислотой) (0,40 г, 0,98 ммоль) в ТГФ (5 мл) обрабатывали гексаметилдисилазидом лития (1,17 мл, 1,17 ммоль, 1,0 М раствор в ТГФ), затем формальдегидом (0,20 г, 50% мас./мас.). Реакционную смесь перемешивали при кт в течение 16 ч, затем гасили насыщенным водным раствором хлорида аммония. Водный слой экстрагировали дихлорметаном. Объединенные органические экстракты сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. Сырой продукт очищали колоночной хроматографией на силикагеле, элюируя 30-60% этилацетата в петролейном эфире (40:60), получая указанное в заголовке соединение (0,10 г, 23%).
1H ЯМР (400 МГц, CDCl3-d): δ 7,35-7,24 (м, 10Н), 4,34 (д, J=7,2 Гц, 2Н), 4,12-3,96 (м, 3Н), 2,75-2,66 (м, 1Н), 2,59 (с, 2Н), 1,78-1,65 (м, 1Н), 1,50-1,41 (м, 11Н), 1,03 (ддд, J=24,9, 12,4, 4,4 Гц, 2Н).
Получение промежуточного соединения 19
Трет-бутил 4-((2-ацетамидо-2,2-дифенилацетилокси)метил)пиперидин-1-карбоксилат использовали для получения соединения примера 23
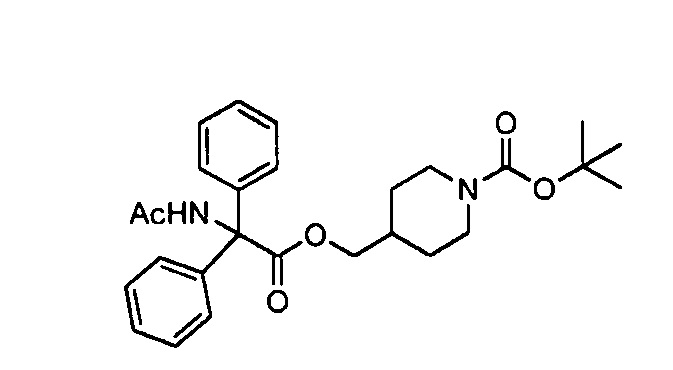
К раствору трет-бутил 4-((2-амино-2,2-дифенилацетилокси)метил)пиперидин-1-карбоксилата (полученного, как в случае получения промежуточного соединения 12, заменяя циклогексилминдальную кислоту дифенилглицином) (0,50 г, 1,18 ммоль) в DCM (1,5 мл) добавляли раствор уксусного ангидрида (0,122 мл, 1,30 ммоль) в DCM (0,5 мл). Реакционную смесь нагревали при 40°С в течение 18 ч. Реакционной смеси давали остыть до кт и добавляли еще уксусного ангидрида (0,06 мл, 0,65 ммоль). Реакционную смесь нагревали при 40°С еще в течение 18 ч. Реакционную смесь оставляли остывать до кт, гасили водой и перемешивали реакционную смесь при кт в течение 1 ч. После этого реакционную смесь распределяли между насыщенным водным раствором гидрокарбоната натрия и DCM. Органическую фазу отделяли, а водную фазу экстрагировали дополнительным количеством DCM. Объединенные DCM экстракты промывали насыщенным раствором соли, сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. Продукт выделяли (0,541 г, >100%). Сырой продукт использовали на следующей стадии без дополнительной очистки.
Получение промежуточного соединения 20
(1-(6-(4-Оксопиперидин-1-ил)гексил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат использовали для получения соединения примера 28
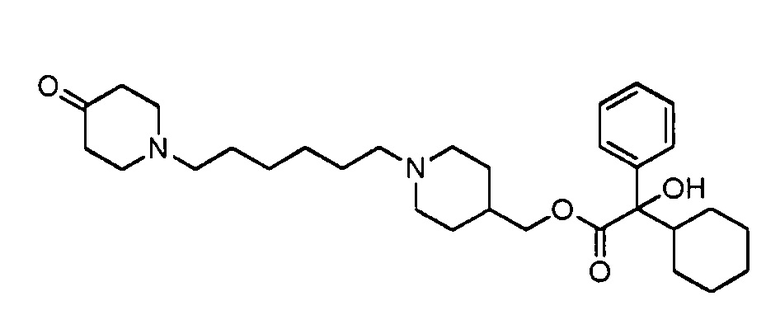
К перемешиваемому раствору (1-(6-оксогексил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетата (полученного в качестве промежуточного соединения 15, но с использованием (1-(5-(1,3-диоксолан-2-ил)пентил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетата (0,20 г, 0,47 ммоль) и 1,4-диокса-8-азаспиро[4.5]декана (0,133 г, 0,93 ммоль) в ТГФ (5 мл) прибавляли триацетоксиборгидрид натрия (0,294 г, 1,39 ммоль). Реакционную смесь перемешивали при кт в течение 18 ч. Реакционную смесь распределяли между DCM и насыщенным водным раствором гидрокарбоната натрия. Органическую фазу отделяли, а водную экстрагировали дополнительным количеством DCM. Объединенные органические экстракты сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. Сырой продукт растворяли в ТГФ (2 мл) и 2М водной HCl и нагревали при 60°С в течение 18 ч. Реакционной смеси давали остыть до кт, а затем гасили насыщенным водным раствором гидрокарбоната натрия. Смесь дважды экстрагировали этилацетатом. Органические фазы сушили (сульфат магния), фильтровали и концентрировали при пониженном давлении. Продукт выделяли (0,193 г, 80%).
Пример 1
(1-(9-((R)-2-Гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат (соединение 1)
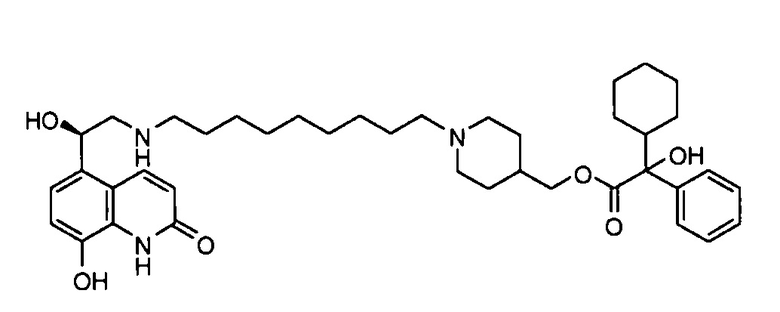
К раствору (1-(10-оксодецил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетата (182 мг, 0,39 ммоль) и гидрохлорида (R)-5-(2-амино-1-гидроксиэтил)-8-гидроксихинолин-2(1Н)-она (100 мг, 0,39 ммоль) в метаноле (4 мл) прибавляли триэтиламин (90 мкл, 0,65 ммоль). Реакционную смесь перемешивали при кт в течение 1 ч. Прибавляли триацетоксиборгидрид натрия (154 мг, 0,73 ммоль), затем уксусную кислоту (74 мкл, 1,29 ммоль), и перемешивали реакционную смесь при кт в течение 72 ч. Реакционную смесь гасили водой (500 мкл) и упаривали при пониженном давлении. Остаток растворяли в диметилсульфоксиде и подвергали препаративной ВЭЖХ с обращенной фазой для окончательной очистки. Выделяли указанное в заголовке соединение (42,3 мг, 16%).
1H ЯМР (400 МГц, CD3OD): δ 8,58 (с, 2Н), 8,40 (д, J=9,8 Гц, 1Н), 7,66-7,61 (м, 2Н), 7,37-7,22 (м, 4Н), 7,03 (д, J=8,1 Гц, 1Н), 6,69 (д, J=9,8 Гц, 1Н), 5,43-5,35 (м, 1Н), 4,02 (д, J=6,2 Гц, 2Н), 3,28-3,13 (м, 4Н), 3,06-2,97 (м, 2Н), 2,73-2,65 (м, 2Н), 2,49-2,36 (м, 2Н), 2,38-2,28 (м, 1Н), 1,87-1,59 (м, 10Н), 1,54-1,03 (м, 20H).
Следующие соединения общей формулы (IA)
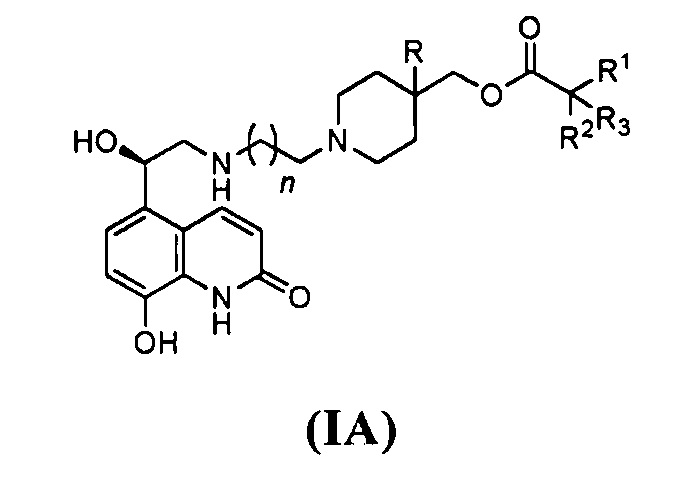
и соединения с 28 по 31 получали по методике, использованной для получения соединения 1 (в значениях R1, приведенных ниже, «с» относится к циклу):
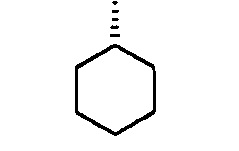
с-С6Н11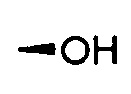
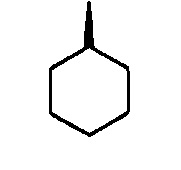
с-С6Н11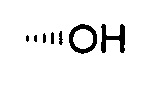
Пример 28
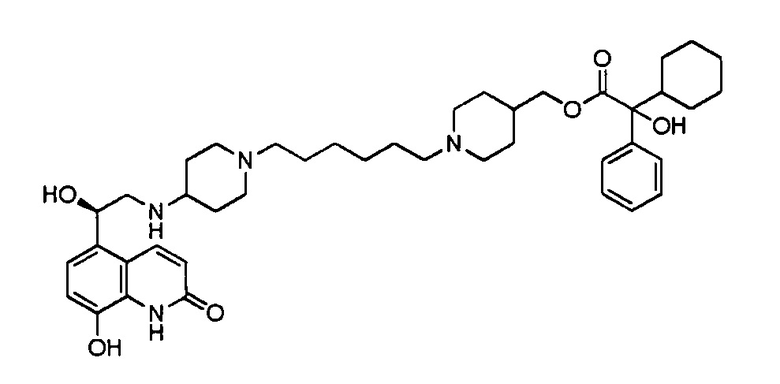
Соединение примера 28 получали по методике, описанной для получения соединения 1, заменяя (1-(10-оксодецил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат на (1-(6-(4-оксопиперидин-1-ил)гексил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат, синтез которого описан в получении 20.
Пример 29
Соединение примера 29 получали по методике, описанной для получения соединения 1, заменяя гидрохлорид (R)-5-(2-амино-1-гидроксиэтил)-8-гидроксихинолин-2(1Н)-она на гидробромид 7-(2-аминоэтил)-4-гидроксибензо[d]тиазол-2(3Н)-она (полученный, как описано в Organic Process Research & Development 2004, 8, 628-642) в примере 1.
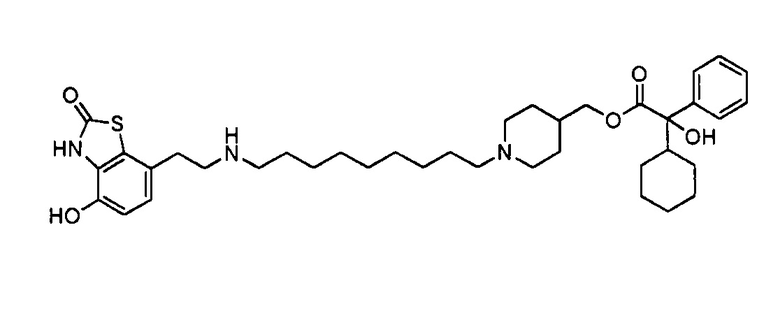
Пример 30
(1-((Е)-5-(3-(((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)пропокси)-4-метилпент-3-ен-1-ил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат
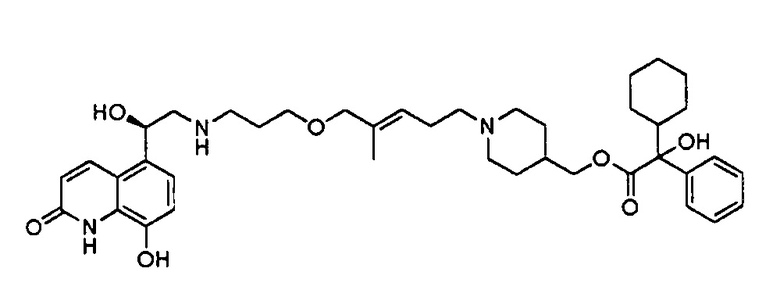
Для получения соединения примера 30 необходим синтез (Е)-5-бром-1-(3,3-диэтоксипропокси)-2-метилпент-2-ена для замены 2-(8-бромоктил)-1,3-диоксолана на стадии 4 примера 1.
Стадия 1: 3-(3,3-Диэтоксипропокси)-2-метилпроп-1-ен
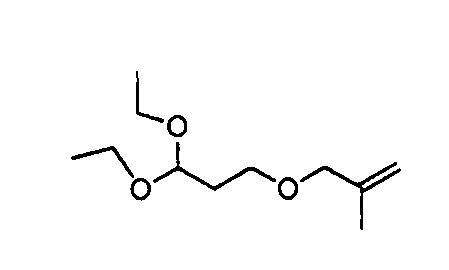
К перемешиваемому раствору 3,3-диэтокси-1-пропанола (3,0 г, 22,2 ммоль) в безводном ТГФ (50 мл) прибавляли гидрид натрия (60%-ную дисперсию в минеральном масле, 1,07 г, 26,6 ммоль). Реакционную смесь перемешивали в течение 30 мин, а затем добавляли 3-бром-2-метил-1-пропен (3,63 г, 24,5 ммоль). После этого реакционную смесь перемешивали еще в течение 18 0447. Реакционную смесь гасили насыщенным раствором гидрокарбоната натрия и экстрагировали этилацетатом (×3). Объединенные органические экстракты промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным раствором соли, сушили (сульфат натрия), фильтровали и концентрировали при пониженном давлении, получая масло (2,25 г, 50%). Вещество использовали на следующей стадии без дополнительной очистки.
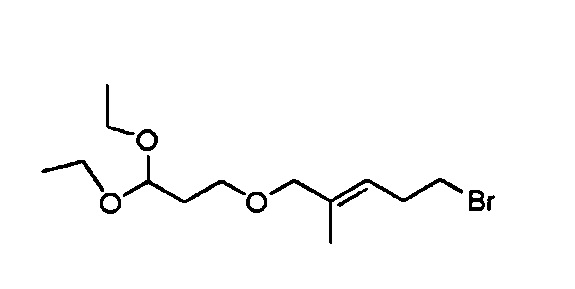
Стадия 2: (Е)-5-бром-1-(3,3-диэтоксипропокси)-2-метилпент-2-ен
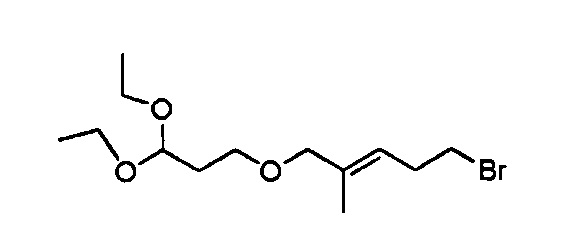
К предварительно дегазированному азотом DCM (18 мл) прибавляли катализатор Граббса второго поколения (0,225 г, 0,30 ммоль), затем 3-бромбутен (2,03 г, 15,0 ммоль) и 3-(3,3-диэтоксипропокси)-2-метилпроп-1-ен (1,52 г, 7,52 ммоль). Реакционную смесь дополнительно дегазировали в течение 5 мин, а затем кипятили в течение 2 ч. Растворитель концентрировали при пониженном давлении, и очищали остаток колоночной хроматографией на силикагеле, элюируя 0-100% этилацетата в изогексане, получая указанное в заголовке соединение (0,208 г, 9%).
1H ЯМР (400 МГц, CDCl3): δ 5,47-5,32 (м, 1Н); 4,69-4,62 (м, 1Н); 3,85 (с, 2Н); 3,72-3,61 (м, 2Н); 3,58-3,32 (м, 6Н); 2,63 (дд, J=14,3, 7,2 Гц, 2Н); 1,94-1,85 (м, 2Н); 1,66 (с, 3Н); 1,28-1,15 (м, 6Н).
Пример 31
(R)-(1-(4-((6-((2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)гексил)окси)бензил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетат (соединение 31)
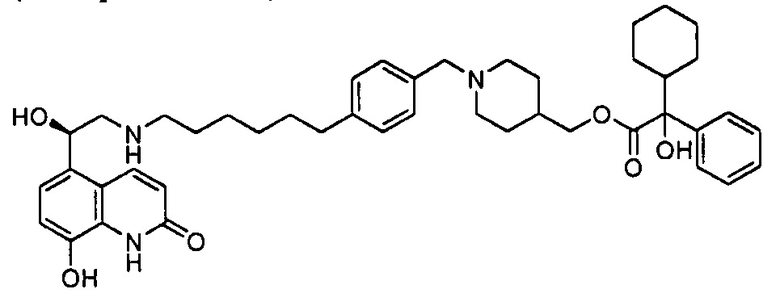
Для получения соединения 31 необходим синтез (1-(4-((5-(1,3-диоксолан-2-ил)пентил)окси)бензил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетата.
Стадия 1: 4-((5-(1,3-Диоксолан-2-ил)пентил)окси)бензальдегид
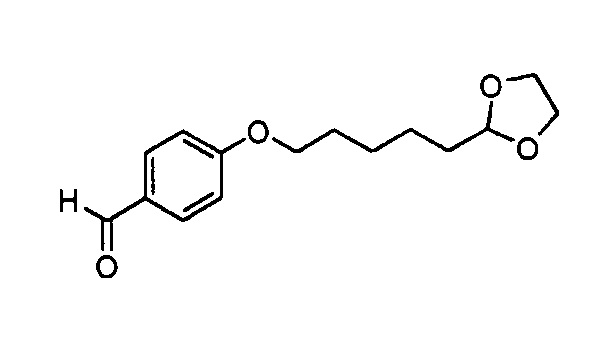
К перемешиваемому раствору 2-(5-бромпентил)-1,3-диоксолана (4,38 г, 19,6 ммоль) в диметилформамиде (30 мл) прибавляли 4-гидроксибензальдегида (3,00 г, 24,4 ммоль) и карбонат калия (4,52 г, 32,8 ммоль). Реакционную смесь перемешивали при 50°С в течение 16 ч. Реакционную смесь разбавляли водой и экстрагировали этилацетатом (×3). Объединенные органические экстракты промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным раствором соли, сушили (сульфат натрия), фильтровали и концентрировали при пониженном давлении, получая масло. Сырое вещество очищали колоночной хроматографией на силикагеле, элюируя 0-100% этилацетата в изогексане, получая указанное в заголовке вещество (1,92 г, 36%).
1H ЯМР (400 МГц, CDCl3): δ 9,92-9,86 (м, 1Н); 7,85-7,80 (м, 2Н); 7,03-6,95 (м, 2Н); 4,87 (т, J=4,7 Гц, 1Н); 4,07-3,80 (м, 6Н); 1,89-1,79 (м, 2Н); 1,75-1,67 (м, 2Н), 1,58-1,46 (м, 4Н).
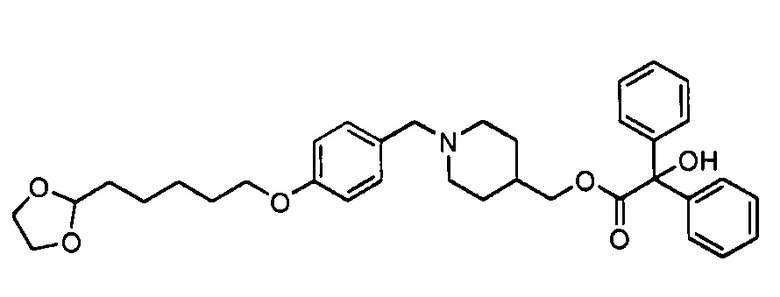
Стадия 2: (1-(4-((5-(1,3-Диоксолан-2-ил)пентил)окси)бензил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетат
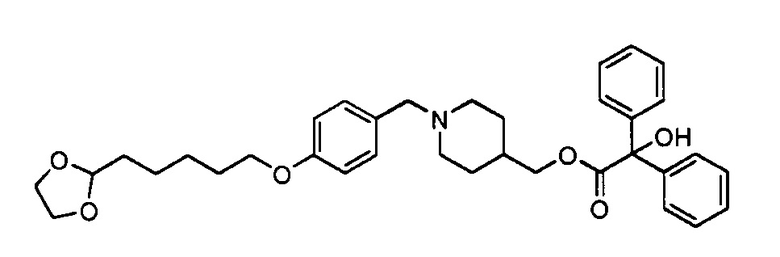
К перемешиваемому раствору пиперидин-4-илметил 2-гидрокси-2,2-дифенилацетата (0,4 г, 1,23 ммоль) и 4-((5-(1,3-диоксолан-2-ил)пентил)окси)бензальдегида (0,38 г, 1,44 ммоль) в DCM (5 мл) прибавляли триацетоксиборгидрид натрия (0,388 г, 1,83 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 ч. Реакционную смесь распределяли между EtOAc и насыщенным водным раствором гидрокарбоната натрия. Органическую фазу сушили (сульфат натрия), фильтровали и концентрировали при пониженном давлении. Сырое вещество очищали колоночной хроматографией на силикагеле, элюируя от 1 до 10% метанола в этилацетате, получая указанное в заголовке вещество в виде бесцветного масла (0,50 г, 26%).
1H ЯМР (400 МГц, CDCl3): δ 7,43-7,37 (м, 5Н); 7,35-7,29 (м, 5Н); 7,23-7,08 (м, 2Н); 6,92-6,78 (м, 2Н); 4,86 (т, J=4,8 Гц, 1Н); 4,25 (с, 1Н); 4,13-3,79 (м, 10Н); 3,44-3,30 (м, 2Н); 2,80 (д, J=11,3 Гц, 2Н); 1,92-1,65 (м, 7Н); 1,57-1,42 (м, 4Н); 1,28-1,11 (м, 2Н).
Соединения с 32 по 37 получали так же, как соединение 31 с соответствующим бромидом (2-(5-бромпентил)-1,3-диоксоланом и 2-(4-бромбутил)-1,3-диоксоланом), используемым на стадии 1, и соответствующим амином, используемым на стадии 2 (пиперидин-4-илметил 2-гидрокси-2,2-дифенилацетат или пиперидин-4-илметил 2-циклогексил-2-гидрокси-2-фенилацетат).
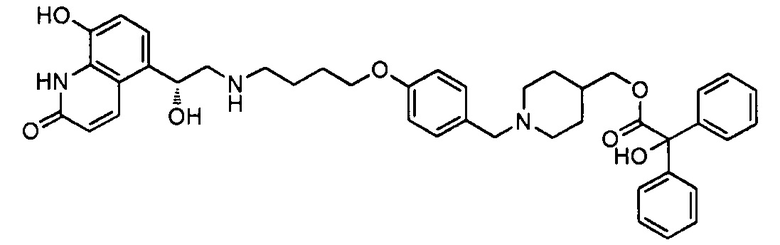
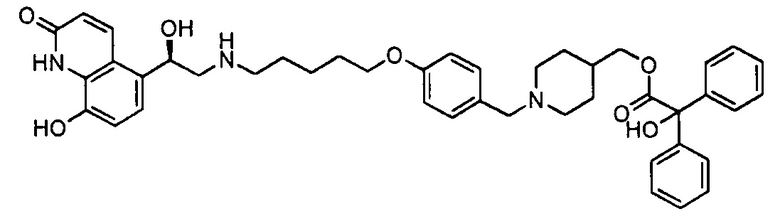
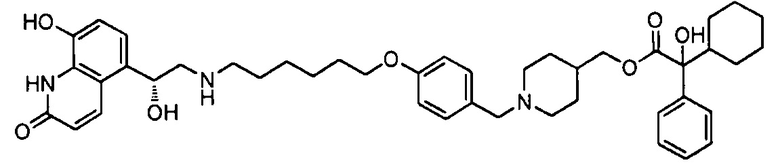
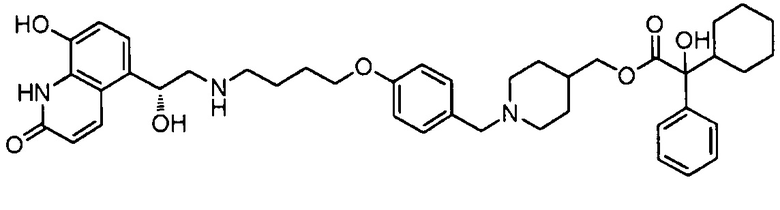
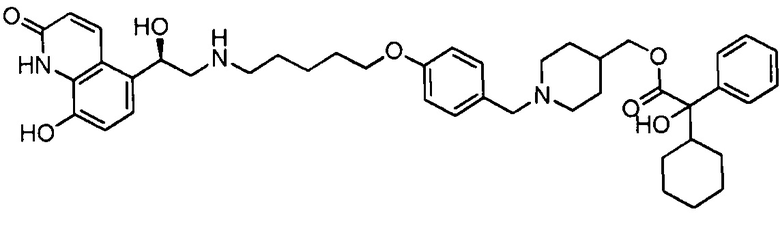
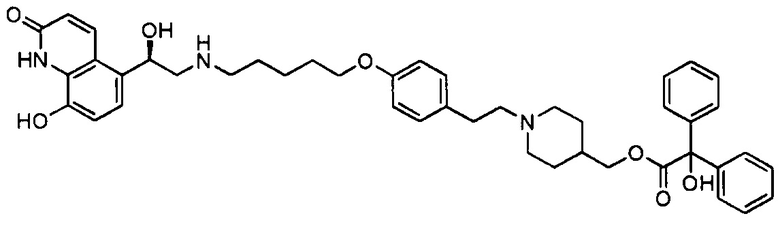
В следующей таблице приведена аналитическая характеристика соединений с 1 по 37.
Что касается данных ЯМР в CD3OD, все обменивающиеся протоны не видны.
пример
время (мин)
Данные ВЭЖХ
Метод:
А IS 10 см_ESCI_Муравьиная кислота_MeCN
В IS 15 см_Муравьиная кислота_ASCENTIS_ВЭЖХ_CH3CN
Подписи к рисункам
*ЯМР
с = синглет
д = дублет
т = триплет
кв = квадруплет
дд = дублет дублетов
м = мультиплет
уш = уширенный
Биологическая характеризация
Пример 38
Анализ связывания радиоактивного лиганда с М3-рецепторами
Мембраны человеческого М3-рецептора (15 мкг/лунку) от Perkin Elmer инкубировали с 0,52 нМ [N-метил-3Н]скополаминметилхлорида в присутствии или в отсутствие тестируемых соединений, или при насыщающей концентрации атропина (5 мкМ) для определения неспецифического связывания. Анализ проводили в 96-луночных планшетах из полипропилена в объеме 250 мкл. Используемый для анализа буфер включал 50 мМ Tris-HCl, 154 мМ NaCl (рН 7,4). Конечная концентрация ДМСО в анализе составляла 0,5% (об./об.). Планшеты герметизировали и инкубировали в течение 2 ч при комнатной температуре на круговой качалке (малая скорость). Мембраны собирали на 96-луночные фильтрующие планшеты Unifilter GF/C, предварительно обработанные 0,5% полиэтиленимина (об./об.), при помощи фильтра, промывали четыре раза 200 мкл буфера для анализа. Планшеты сушили перед добавлением 50 мкл microscint-0, герметизировали, затем считывали в счетчике сцинтилляций Trilux Microbeta. Величины IC50 определяли из сравнения кривых при помощи программы нелинейной подгонки кривых. Величины Ki рассчитывали из значений IC50 по уравнению Ченга-Прусова.
Значения Ki тестируемых соединений составляют менее 10 нМ.
Пример 39
Анализ связывания радиолиганда с β2-адренорецепторами
Мембраны человеческого β2-адренорецептора (7,5 мкг/лунку) от Perkin Elmer инкубировали с 0,3 нМ 125-I цианопиндолола в присутствии или в отсутствие тестируемых соединений, или насыщающей концентрации (S)-пропранолола (2 мкМ) для определения неспецифического связывания. Данный анализ проводили в 96-луночных планшетах из полипропилена в объеме 200 мкл. Использованный буфер для анализа включал 25 мМ HEPES, 0,5% BSA (мас./об.), 1 мМ ЭДТУ, 0,02% аскорбиновой кислоты (об./об.), (рН 7,4). Конечная концентрация ДМСО в анализе составляла 0,5% (об./об.). Планшеты герметизировали и инкубировали в течение 1 ч при комнатной температуре на круговой мешалке (малая скорость). Мембраны собирали на 96-луночные фильтрующие планшеты Unifilter GF/C, предварительно обработанные 0,5% полиэтиленимина (об./об.), при помощи фильтра, промывали шесть раз 200 мкл промывного буфера, содержащего 10 мМ HEPES и 500 мМ NaCl. Планшеты сушили перед добавлением 50 мкл microscint-0, герметизировали, затем считывали в счетчике сцинтилляций Trilux Microbeta. Величины IC50 определяли из сравнения кривых при помощи программы нелинейной подгонки кривых. Величины Ki рассчитывали из значений IC50 по уравнению Ченга-Прусова.
Значения Ki тестируемых соединений составляют менее 10 нМ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ АНТАГОНИСТОВ МУСКАРИНОВЫХ РЕЦЕПТОРОВ И АГОНИСТОВ БЕТА-2-АДРЕНЕРГИЧЕСКИХ РЕЦЕПТОРОВ | 2013 |
|
RU2661877C2 |
| Соединения, обладающие активностью антагонистов мускариновых рецепторов и агонистов бета-2-адренергических рецепторов | 2016 |
|
RU2709777C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛ-3-АМИНОМЕТИЛ-ХИНОЛОНА-2 В КАЧЕСТВЕ ИНГИБИТОРОВ NO-СИНТЕТАЗЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, БИОЛОГИЧЕСКИ АКТИВНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2003 |
|
RU2284325C2 |
| КОМПОЗИЦИИ ТЕТРАГИДРОХИНОЛИНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ БРОМОДОМЕНА ВЕТ | 2014 |
|
RU2727169C2 |
| ИМИДАЗОПИРАЗИНЫ | 2012 |
|
RU2600327C2 |
| Соединения, активные по отношению к бромодоменам | 2015 |
|
RU2743074C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ МОДУЛЯТОРЫ АКТИВНОСТИ HIF ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2698197C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ ПРОТИВООПУХОЛЕВЫХ ЦЕЛЕВЫХ ФЕРМЕНТОВ | 2002 |
|
RU2319482C2 |
| Новые соединения пиридопиримидинона для модулирования каталитической активности гистонлизиндеметилаз (KDMS) | 2015 |
|
RU2684396C2 |
| ЗАМЕЩЕННЫЕ АЗОЛЫ, ПРОТИВОВИРУСНЫЙ АКТИВНЫЙ КОМПОНЕНТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2452735C1 |
Настоящее изобретение относится к соединениям общей формулы (I), 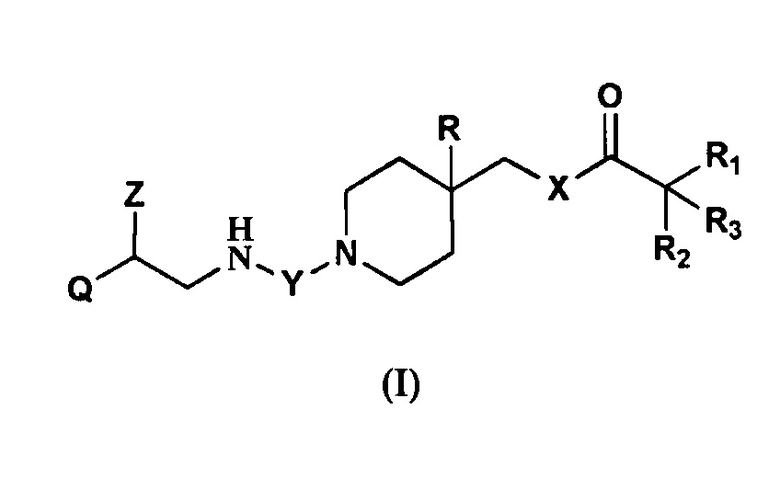 , действующим как антагонисты мускариновых рецепторов или агонисты бета2-адренорецепторов, а также к фармацевтическим композициям на их основе и к терапевтическим применениям для получения лекарственного средства для предупреждения и лечения заболеваний, таких как астма, хронический бронхит и т.д. Технический результат: получены новые соединения формулы (I), обладающие активностью в отношении мускариновых рецепторов или бета2-адренорецепторов. 5 н. и 8 з.п. ф-лы, 5 табл., 2 сх., 39 прим.
, действующим как антагонисты мускариновых рецепторов или агонисты бета2-адренорецепторов, а также к фармацевтическим композициям на их основе и к терапевтическим применениям для получения лекарственного средства для предупреждения и лечения заболеваний, таких как астма, хронический бронхит и т.д. Технический результат: получены новые соединения формулы (I), обладающие активностью в отношении мускариновых рецепторов или бета2-адренорецепторов. 5 н. и 8 з.п. ф-лы, 5 табл., 2 сх., 39 прим.
1. Соединение общей формулы (I)
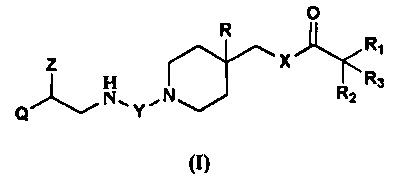
в которой Q представляет собой группу формулы Q1 или Q3
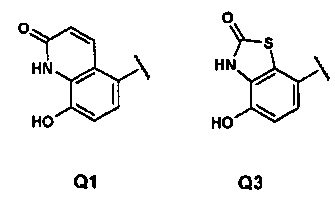
Z представляет собой Н или ОН;
Y представляет собой -(СН2)n-, где n является целым числом от 1 до 8, или представляет собой двухвалентную группу формулы Y1
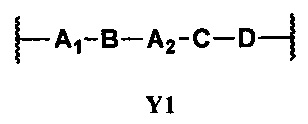
в которой
каждый из А1 и А2 независимо отсутствует или выбран из группы, включающей (C1-C6) алкилен,;
В отсутствует;
С представляет собой -О-,;
D выбирают из группы, включающей (С1-С12)алкилен и (С2-C12)алкенилен, необязательно замещенные одним или более (C1-С6) алкилами;
R представляет собой Н;
X представляет собой -О-;
R1 выбран из группы, включающей (С3-С8)циклоалкил, С6арил, гетероарил, такой как тиенил, С6арил (C1-C6) алкил;
R2 выбирают из группы, включающей (С3-С8)циклоалкил, С6арил, гетероарил, такой как тиенил, необязательно замещенные одним атомом галогена или (C1-C4)алкокси;
R3 представляет собой Н или выбран из группы, включающей -ОН, гидрокси (C1-C6) алкил и -N(R5)СО(R6);
R5 и R6 независимо представляют собой Н или (C1-C6) алкил,
и их фармацевтически приемлемые соли или сольваты.
2. Соединение по п. 1, в котором R2 выбирают из группы, включающей (С3-С8)циклоалкил, С6арил, гетероарил, такой как тиенил.
3. Соединение по п. 1, в котором R1 представляет собой Н или выбран из группы, включающей циклобутил, циклопентил, фенил, бензил, циклогептил, тиенил и циклогексил; R2 выбирают из группы, включающей фенил, тиенил, циклогексил, трифенилметил, хлорфенил, метоксифенил и фторфенил; R3 представляет собой Н или выбран из группы, включающей -ОН, -NH2, -СН2ОН, -NHCOCH3; X представляет собой -O-; R представляет собой Н.
4. Соединение по п. 1, в котором Rl, R2, R3, X и R такие, как определено в п. 1; Y представляет собой -(СН2)n, где n является целым числом от 1 до 8, или представляет собой группу формулы Y1
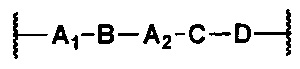
в которой
каждый из А1 и А2 независимо отсутствует или выбран из группы, включающей (C1-C6)алкилен,
В отсутствует,
С представляет собой -О-, a Q представляет собой группу формулы Q1 или Q3
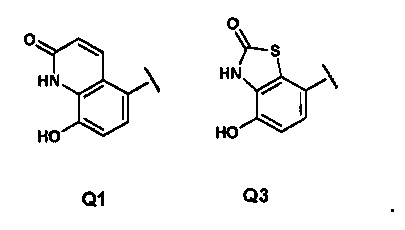
5. Соединение по п. 4, в котором Y представляет собой -(СН2)n, Z представляет собой ОН, a Q представляет собой группу формулы Q1
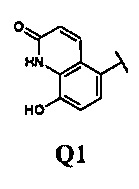
в соответствии с общей формулой (IA)
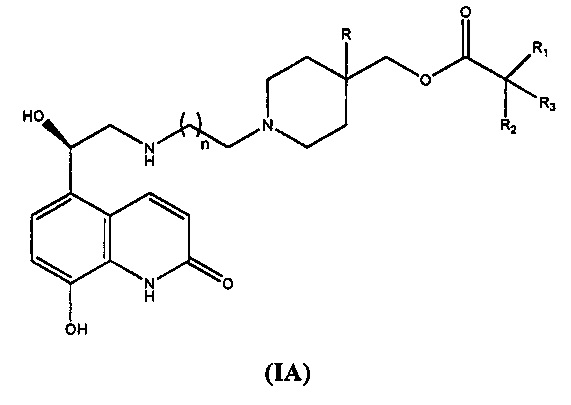
6. Соединение по п. 5, в котором n равно 4, 5, 6, 7 или 8.
7. Соединение по п. 1, в котором Y представляет собой -(CH2)n, Z представляет собой Н, a Q представляет собой группу формулы Q3
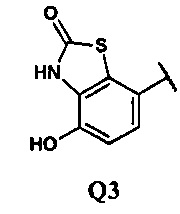
в соответствии с общей формулой (IC)
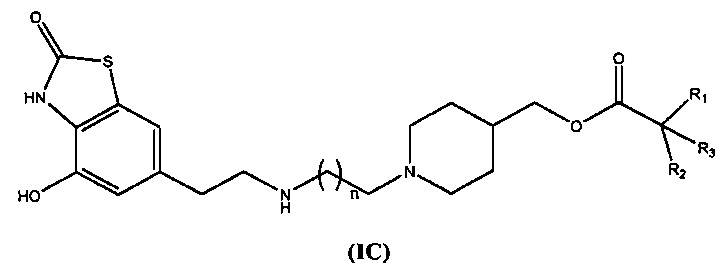
8. Соединение по п. 7, в котором n равно 8.
9. Фармацевтическая композиция, действующая как антагонист мускаринового рецептора или агонист бета2-адренорецептора, содержащая эффективное количество соединения формулы (I), определенное в любом из пп. 1-8, в присутствии одного или более фармацевтически приемлемых носителей и/или эксципиентов.
10. Применение соединения формулы (I) по любому из пп. 1-8 для получения лекарственного средства для предупреждения и/или лечения бронхообструктивных или воспалительных заболеваний, предпочтительно астмы, или хронического бронхита, или хронической обструктивной болезни легких (COPD).
11. Фармацевтическая композиция по п. 9 для введения путем ингаляции, такая как ингалируемые порошки, дозированные аэрозоли, содержащие пропеллент, или ингалируемые препараты, не содержащие пропеллента.
12. Устройство, содержащее фармацевтическую композицию по п. 11, которое может представлять собой однодозовый или многодозовый порошковый ингалятор, ингалятор для введения отмеренной дозы и жидкостный небулайзер.
13. Соединение, выбранное из группы, включающей
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклобутил-2-гидрокси-2-фенилацетат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклопентил-2-гидрокси-2-фенилацетат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-гидрокси-2,3-дифенилпропаноат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогептил-2-гидрокси-2-фенилацетат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)-4-метилпиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-фенилацетат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-(тиофен-2-ил)ацетат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-гидрокси-2-фенил-2-(тиофен-3-ил)ацетат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-амино-2,2-дифенилацетат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-гидрокси-2,2-ди(тиофен-2-ил)ацетат,
(S)-(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(R)-(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-гидрокси-2-фенил-2-(тиофен-2-ил)ацетат,
(1-(8-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)октил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(1-(7-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)гептил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(1-(5-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)пентил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(1-(6-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)гексил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилпропаноат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-дициклогексил-2-гидроксиацетат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-трифенилпропаноат,
(R)-(1-(9-(2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-ацетамидо-2,2-дифенилацетат,
1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-хлорфенил)-2-гидрокси-2-фенилацетат,
1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-(тиофен-3-ил)ацетат,
1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-гидрокси-2-(3-метоксифенил)-2-фенилацетат,
1-(9-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)нонил)пиперидин-4-ил)метил 2-(4-фторфенил)-2-гидрокси-2-фенилацетат,
1-(6-(4-((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этиламино)пиперидин-1-ил)гексил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
1-(9-(2-(4-гидрокси-2-оксо-2,3-дигидробензо[d]тиазол-7-ил)этиламино)нонил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
1-((Е)-5-(3-(((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)пропокси)-4-метилпент-3-ен-1-ил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(R)-(1-(4-((6)-((2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)гексил)окси)бензил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетат,
(R)-(1-(4-((6)-((2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)бутил)окси)бензил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетат,
(R)-(1-(4-((6)-((2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)пентил)окси)бензил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетат,
1-(4-((6)-(((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)гексил)окси)бензил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
l-(4-((6)-(((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)бутил)окси)бензил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
l-(4-((6)-(((R)-2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)пентил)окси)бензил)пиперидин-4-ил)метил 2-циклогексил-2-гидрокси-2-фенилацетат,
(R)-(1-(4-((5)-((2-гидрокси-2-(8-гидрокси-2-оксо-1,2-дигидрохинолин-5-ил)этил)амино)пентил)окси)фенетил)пиперидин-4-ил)метил 2-гидрокси-2,2-дифенилацетат,
и его фармацевтически приемлемые соли или сольваты.
| WO2004106333 A1, 09.12.2004 | |||
| RAY NICHOLAS C, Muscarinic antagonist-beta-adrenergic agonist dual pharmacology molecules as bronchodilators: a patent review, EXPERT OPINION ON THERAPEUTIC PATENTS, 19, 1, стр.:1 - 12 | |||
| ПРОИЗВОДНЫЕ БИФЕНИЛА | 2004 |
|
RU2330841C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ ХЕМОКИН-ОПОСРЕДОВАННОГО БОЛЕЗНЕННОГО СОСТОЯНИЯ С ИХ ИСПОЛЬЗОВАНИЕМ | 2003 |
|
RU2330019C2 |
Авторы
Даты
2017-01-10—Публикация
2012-06-07—Подача