Область изобретения
Настоящее изобретение относится к корму для животных, дополненному гипертермостабильной и гипертермофильной ксиланазой.
Предшествующий уровень техники и состояние уровня техники
Ксиланазы на протяжении нескольких лет используются в качестве кормовых добавок. Действительно, показано, что некоторые, но не все ксиланазы улучшают один или оба из показателей: абсолютную прибавку в весе животного (BWG) и коэффициент кормоотдачи (FCR) для данного корма.
Ксиланазы, используемые в корме, например, могут дать возможность специалистам по кормлению уменьшить энергетические потребности в диетах, не влияя на зоотехнические показатели животных.
Ксиланазы увеличивают метаболизируемую или чистую энергию сырых ингредиентов и, таким образом, увеличивают долю общей метаболизируемой или чистой энергии в диетах. Таким образом, зоотехнические показатели могут поддерживаться при меньшем содержании сырьевой энергии в менее дорогостоящих диетах (меньше жира/масла; больше волокон).
Возможная польза, связанная с использованием ксиланазы, заключается в более хорошем высвобождении (микро)питательных веществ, заключенных в клеточных стенках корма. Такое включение является следствием присутствия некрахмальных полисахаридов, резистентных к перевариванию у животных.
Для того чтобы оказаться эффективными, ксиланазы, используемые в качестве кормовых добавок, должны быть как стабильными, так и активными при рН и температуре, близкой к условиям, обнаруживаемым в желудочно-кишечном тракте животного.
В WO 95/29997 описаны термостабильные ксиланазы и упомянуто их включение в корм для животных. Термостабильность определяется как устойчивость в течение одной минуты к воздействию 95°С, связанная со способностью к последующему гидролизу раствора пшеничного арабиноксилана при 40°С. Тем не менее, после термической обработки в течение пяти минут раскрытые ксиланазы значительно утрачивали свою активность.
Описаны несколько видов и штаммов Thermotoga, которые продуцируют одну или более чем одну гипертермофильную и термостабильную эндоксиланазу(ы). Thermotoga maritima продуцирует две термостабильные эндоксиланазы, обозначенные XynA и XynB. XynA и XynB представляют собой белки с предполагаемыми молекулярными массами приблизительно 120 и 40 кДа. Максимальная активность при оптимальном рН (рН 6,2 и рН 5,4 для XynA и XynB соответственно) измерена при приблизительно 92°С для XynA и при приблизительно 105°С для XynB (Winterhalter and Liebl, 1995, Appl. Env. Microbiol., 61, 1810-1815).
Краткое изложение сущности изобретения
Первый аспект настоящего изобретения представляет собой корм для животных, дополненный композицией, содержащей гипертермофильную и гипертермостабильную ксиланазу.
Предпочтительно оптимальная температура ксиланолитической активности указанной композиции составляет выше 80°С, более предпочтительно выше 85°С, еще более предпочтительно выше 90°С.
Предпочтительно отношение ксиланолитической активности данной композиции, при оптимальной температуре и при 40°С составляет больше 10, более предпочтительно больше 20.
Является преимуществом, что более чем 70% ксиланолитической активности данной композиции устойчиво к нагреванию в течение 30 минут при 90°С.
Более предпочтительно гипертермофильная и гипертермостабильная ксиланаза обладает более чем 80% идентичностью и/или более чем 90% сходством с ксиланазой, выбранной из группы, состоящей из SEQ.ID.NO:1, SEQ.ID.NO:2, SEQ.ID.NO:3, SEQ.ID.NO:4, SEQ.ID.NO:5, аминокислот 21-332 в SEQ.ID.NO:1, в SEQ.ID.NO:2, в SEQ.ID.NO:3, в SEQ.ID.NO:4 и в SEQ.ID.NO:5, и возможно указанный корм для животных содержит от 0,08 до 40 мг/кг указанной гипертермофильной и гипертермостабильной (чистой) ксиланазы.
Возможно, данный корм для животных является жидким и предпочтительно содержит от 0,08 до 40 мг/л гипертермофильной и гипертермостабильной (чистой) ксиланазы.
В качестве альтернативы данный корм для животных выбран из группы, состоящей из силоса, гранулированного корма и мешанки.
Предпочтительно корм для животных содержит по меньшей мере 50% (от сухой массы) растительного материала, более предпочтительно выбранного из группы, состоящей из зерновых, бобовых, свекловичной мелассы, картофельной массы и арахисовой муки.
Предпочтительно корм для животных содержит по меньшей мере 5% (сухая масса) белков и/или по меньшей мере 2% (сухая масса) жира.
Связанный аспект представляет собой корм для животных, содержащий от 0,08 до 40 мг/кг (от сухой массы) полипептида, обладающего более чем 80% идентичностью и/или более чем 90% сходством с полипептидом, выбранным из группы, состоящей из SEQ.ID.NO:1, SEQ.ID.NO:2, SEQ.ID.NO:3, SEQ.ID.NO:4, SEQ.ID.NO:5, аминокислот 21-332 в SEQ.ID.NO:1, в SEQ.ID.NO:2, в SEQ.ID.NO:3, в SEQ.ID.NO:4 и в SEQ.ID.NO:5.
Еще один связанный аспект представляет собой (не терапевтическое) использование корма для животных для улучшения прибавки в весе и/или коэффициента кормоотдачи у животного, предпочтительно представляющего собой позвоночное нежвачное животное или ракообразное и более предпочтительно рыбу, свинью или домашнюю птицу.
Еще один связанный аспект представляет собой способ приготовления корма для животных, при котором осуществляют стадии:
а) выбора корма, содержащего гемицеллюлозу;
б) добавления композиции, содержащей гипертермофильную и гипертермостабильную ксиланазу.
Предпочтительно более чем 70% ксиланолитической активности композиции, добавляемой на стадии б) настоящего способа, устойчиво в течение 30 минут нагревания указанной композиции при 90°С, и/или оптимальная температура ксиланолитической активности данной композиции, составляет больше чем 80°С (предпочтительно больше чем 85°С, более предпочтительно больше чем 90°С).
Подробное описание изобретения
Авторы изобретения обнаружили, что добавление в корм гипертермофильной (и гипертермостабильной) ксиланазы приводило в результате к улучшенному коэффициенту кормоотдачи у животных.
Хотя оптимальная рабочая температура гипертермофильных (эндо)ксиланаз больше, чем температура кишечника животного, авторы изобретения обнаружили, что данные ферменты улучшали прибавку в весе и/или коэффициент кормоотдачи, даже по сравнению с обычно используемыми кормовыми (эндо)ксиланазами. Конкретней, авторы изобретения обнаружили, что ксиланазы, которые являются гипертермофильными (и гипертермостабильными) продемонстрировали лучшие результаты по сравнению с термофильными (и термостабильными) ксиланазами.
Как абсолютная прибавка в весе животного (BWG), так и коэффициент кормоотдачи (FCR) улучшались в случае животных, которых кормили мешанкой, дополненной гипертермофильной и гипертермостабильной ксиланазой, по сравнению с животными, которых кормили мешанкой без добавок, и с животными, для которых мешанка была дополнена ксиланазой, обладающей наибольшей активностью при 37-50°С.
FCR указывает на отношение количества корма, потребляемого животным, к прибавке в весе. Меньшее отношение FCR является показателем более эффективного усваивания корма.
Эти результаты противоречат, в случае использования гипертермофильной и гипертермостабильной ксиланазы, чрезвычайно низкой ксиланазной активности, измеренной при 37°С.
Первый аспект настоящего изобретения представляет собой корм (корм для животных), дополненный (и/или содержащий) композицией, содержащей гипертермофильную (т.е. температурный оптимум (общей) ксиланолитической активности составляет выше 80°С, предпочтительно выше 90°С или 95°С, и/или отношение активности при оптимальной температуре и при 40°С составляет больше 10 или даже больше 15 или 20) и гипертермостабильную ксиланазу (т.е. (общая) ксиланолитическая активность этой композиции весьма устойчива к термической инактивации (денатурации), а именно более чем 70% активности сохраняется по истечении 30 минут нагревания при 90°С в масляной бане добавки, содержащей ксиланазу).
Корм может содержать от 0,08 мг/кг корма до 40 мг/кг корма гипертермофильной и гипертермостабильной ксиланазы, более предпочтительно от 0,2 мг/кг корма до 20 мг/кг корма, еще более предпочтительно от 0,4 мг/кг корма до 16 мг/кг корма (чистого) фермента.
Предпочтительно корм содержит от 10 DXU/кг корма до 5000 DXU/кг корма гипертермофильной и гипертермостабильной ксиланазы, более предпочтительно от 25 DXU/кг корма до 2500 DXU/кг корма, еще более предпочтительно от 50 DXU/кг корма до 2000 DXU/кг корма.
В контексте настоящего изобретения одна единица ксиланазы (DXU) определяется как количество фермента, требующееся для высвобождения 1 мкмоль редуцирующего сахара (в виде ксилозы) в минуту из раствора 3% ксилана березовой древесины при рН 6 и при 70°С, если ясно не упомянуты другие величины.
Связанный аспект представляет собой кормовую добавку (добавка в корм для животных), содержащую гипертермофильную и гипертермостабильную ксиланазу.
В контексте настоящего изобретения "гипертермостабильная ксиланаза" относится к ксиланазе, где более чем 70% (общей) ксиланолитической активности (данной композиции) устойчиво к (способно выдерживать и/или способно сохраняться после) 30 минутам нагревания (данной композиции) при 90°С. Термин "общая ксиланолитическая активность" относится к ксиланолитической активности гипертермофильной и гипертермостабильной ксиланазы, и также к активности других (посторонних) ксиланаз, которые в менее предпочтительной степени представлены в композиции, добавляемой в корм для животных, как раскрыто в настоящем изобретении.
Предпочтительно по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или даже до 100% (общей) ксиланолитической активности этого корма, и/или в данной кормовой добавке, способно поддерживаться после 30 минут (или 45 минут или 1 часа) нагревания (данного корма и/или данной кормовой добавки) при 90°С (или при 95°С).
Предпочтительно оптимальная температура (температурный оптимум) для (общей) ксиланолитической активности композиции, добавляемой в корм по настоящему изобретению, составляет больше чем 80°С, более предпочтительно больше чем 85°С, 90°С или даже больше чем 95°С.
Предпочтительно отношение (общей) ксиланолитической активности композиции, добавляемой в корм по настоящему изобретению (содержащей гипертермофильную и гипертермостабильную ксиланазу), при оптимальной температуре (например 80°С, 85°С, 90°С, 95°С или даже приблизительно 100°С) и при 40°С (или 37°С) составляет больше чем 10, более предпочтительно больше чем 20.
В контексте настоящего изобретения термин "фермент, обладающий ксиланолитической активностью", "эндоксиланаза" или "ксиланаза" относится к ферменту (например рекомбинантной, по меньшей мере частично очищенной ксиланазе или, менее предпочтительно к смеси ферментов), способному (-ыми) гидролизовать внутренние гликозильные связи, связывающие остатки ксилозы в содержащих ксилозу полисахаридах. Такие гликозильные связи могут представлять собой, например бета-1,4-гликозильную связь в бета-D-ксилопиранозил-1,4-бета-D-ксилопиранозильных единицах таких полисахаридов.
Предпочтительные ферменты, обладающие ксиланолитической активностью, представляют собой эндоксиланазы (КФ 3.2.1.8. (код фермента)).
Предпочтительные ферменты, обладающие ксиланолитической активностью, представляют собой эндоксиланазы из семейства гликозидгидролаз 10.
Среди наиболее предпочтительных ферментов, обладающих ксиланолитической активностью (гипертермофильная и гипертермостабильная ксиланаза), находятся ферменты, полученные из штамма Thermotoga maritime, и еще более предпочтительно XynB (SEQ.ID.NO: 1) или близкие к нему варианты (например SEQ.ID.NO: 2-5), или содержат наиболее консервативную область тех же самых последовательностей (SEQ.ID.NOs: 1-5), предпочтительно где указанная наиболее консервативная область охватывает ксиланазный мотив семейства 10 гликозидгидролаз (консервативная часть ксиланазного мотива семейства 10 гликозидгидролаз простирается на области 21-332 в SEQ.ID.NO: 1-5, или от аминокислоты 21 до последней аминокислоты 344, 346 или 347 в этих SEQ.ID.NO: 1-5) или обладают значительной идентичностью (или сходством) с этими SEQ.ID.NO.1-5 или областями 21-332 (или с 21 до последней аминокислоты 344, 346 или 347) в этих SEQ.ID.NO: 1-5. Добавляемый(е) фермент(ы), обладающий(е) ксиланолитической активностью (гипертермофильная и гипертермостабильная ксиланаза) также может представлять собой гибридный белок, содержащий SEQ.ID.NO: 1-5, или гибридный белок, содержащий пептид, обладающий значительной идентичностью (или сходством) с SEQ.ID.NO: 1-5 или с областями 21-332 в этих SEQ.ID.NO: 1-5.
"Значительная идентичность" в контексте настоящего изобретения относится по меньшей мере к 75% идентичности, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или даже по меньшей мере 99%. Предпочтительно идентичность измеряют вдоль всей длины (изложенной) последовательности (или фрагмента), а именно вдоль всей длины SEQ.ID.NO: 1-5 или вдоль всей длины пептида, состоящего из аминокислот 21-332 (или аминокислот с 21 до последней аминокислоты) в SEQ.ID.NO: 1-5. "Значительное сходство" в контексте настоящего изобретения относится по меньшей мере к 85% сходству, предпочтительно по меньшей мере 90%, более предпочтительно по меньшей мере 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или даже по меньшей мере 99%. Предпочтительно сходство измеряют вдоль всей длины (изложенной) последовательности (или фрагмента), а именно вдоль всей длины SEQ.ID.NO: 1-5 или вдоль всей длины пептида, состоящего из аминокислот 21-332 (или аминокислот с 21 до последней аминокислоты) в SEQ.ID.NO: 1-5.
Родство между двумя аминокислотными последовательностями или между двумя нуклеотидными последовательностями описывается параметром "идентичность" или "сходство". Для целей настоящего изобретения степень сходства (и идентичности) между двумя аминокислотными последовательностями определяют как в WO 2010/0142697 с использованием алгоритма Нидлмана-Вунша, внедренного в программу Needle пакета EMBOSS, предпочтительно версии 3.0.0 или более поздней. Вспомогательные используемые параметры представляют собой штраф за пропуск 10, штраф за удлинение пропуска 0,5, и матрицу замен EBLOSUM62 (EMBOSS версия BLOSUM62). Выходные данные Needle, обозначенные как "самая длинная идентичность" (получено с использованием опции -nobrief) используются в качестве процента идентичности и рассчитываются следующим образом: (Идентичные остатки × 100)/(Длина выравнивания - Общее количество пропусков в выравнивании). Выходные данные Needle, обозначенные как "самое длинное сходство" (получено с использованием опции -nobrief) используют в качестве процента сходства и рассчитывают следующим образом: (Похожие остатки × 100)/(Длина выравнивания - Общее количество пропусков в выравнивании).
Ксиланазы (и/или композиция, содержащая гипертермофильную и гипертермостабильную ксиланазу) преимущественно добавляют во время приготовления корма, представляющего собой твердый препарат, такой как кормовая смесь или гранулят, или представляющего собой жидкость.
Способ гранулирования обычно включает стадии при высокой температуре, такие как закачивание пара.
С другой стороны, корм для животных может быть приготовлен без использования стадий нагревания (например ниже 50°С), например для корма, который не гранулирован.
Связанный аспект настоящего изобретения представляет собой корм (для животного) (и/или (кормовая) предварительная смесь), содержащий на кг от 0,08 мг до 400 мг (предпочтительно от 0,2 мг/кг до 40 мг/кг, более предпочтительно от 0,4 мг/кг до 20 мг/кг) полипептида, имеющего более чем 75% (предпочтительно более чем 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или даже 100%) идентичности (или сходства) с полипептидом, выбранным из группы, состоящей из SEQ.ID.NO: 1, SEQ.ID.NO: 2, SEQ.ID.NO: 3, SEQ.ID.NO: 4, SEQ.ID.NO: 5, аминокислот 21-332 (или с аминокислоты 21 до последней аминокислоты 344, 346 или 347) в SEQ.ID.NO: 1, в SEQ.ID.NO: 2, в SEQ.ID.NO: 3, в SEQ.ID.NO: 4 и в SEQ.ID.NO: 5, где указанный полипептид предпочтительно является гипертермостабильным и обладает предпочтительно гипертермофильной ксиланазной активностью.
Предпочтительно корм (для животного) по настоящему изобретению содержит по меньшей мере 50% (от сухой массы) растительного материала, наиболее предпочтительно по меньшей мере 55% или даже по меньшей мере 60%.
Предпочтительно указанный растительный материал выбран из группы, состоящей из зерновых, бобовых, свекловичной мелассы, картофельной массы и арахисовой муки, и также может включать их смесь, такую как смесь зерновых и бобовых.
Предпочтительно (или дополнительно) корм по настоящему изобретению (содержащий по меньшей мере 50% растительного материала) содержит по меньшей мере 5% (сухая масса) белков, более предпочтительно по меньшей мере 10%, по меньшей мере 15% или даже по меньшей мере 20% белков.
Предпочтительно (или дополнительно), корм по настоящему изобретению (содержащий по меньшей мере 50% растительного материала и/или по меньшей мере 5% белков) содержит по меньшей мере 2% (сухая масса) жира, более предпочтительно по меньшей мере 5% или даже по меньшей мере 8% жира.
Предпочтительно корм по настоящему изобретению выбран из группы, состоящей из силоса, гранулированного корма и мешанки.
Еще один связанный аспект настоящего изобретения представляет собой (нетерапевтическое) применение корма (и/или применение (кормовой) предварительной смеси, и/или применение кормовой добавки), дополненной гипертермофильной и гипертермостабильной ксиланазой (и/или применение кормовой добавки для животных по настоящему изобретению, и/или применение гипертермофильной и гипертермостабильной ксиланазы по настоящему изобретению) для улучшения прибавки в весе и/или коэффициента кормоотдачи у (растущего) животного (и наиболее предпочтительно для того, чтобы не приводить к избыточной патологической прибавки в весе).
Предпочтительная (гипертермофильная и гипертермостабильная) ксиланаза для (нетерапевтического) улучшения прибавки в весе (BWG) и/или коэффициента кормоотдачи (FCR) у (растущего) животного обладает более чем 70%, 75%, 80%, 85% 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или даже более чем 99% (общей) ксиланолитической активности, которая устойчива к нагреванию в течение 1 часа при 90°С (или 95°С).
В качестве альтернативы или дополнительно предпочтительная (гипертермофильная и гипертермостабильная) ксиланаза, используемая для (нетерапевтического) улучшения прибавки в весе (BWG) и/или коэффициента кормоотдачи (FCR) у (растущего) животного, происходит из семейства 10 гликозидгидролаз.
Наиболее предпочтительные ксиланазы, используемые для (нетерапевтического) улучшения прибавки в весе (BWG) и/или коэффициента кормоотдачи (FCR) у (растущего) животного, происходят из Thermotoga, и еще более предпочтительно обладают значительной гомологией (сходством) с SEQ.ID.NO 1-5, или с фрагментами 21-332 в SEQ.ID.NO 1-5, или содержат (в виде гибридного белка) пептид, обладающий значительной гомологией (сходством) с фрагментами 21-332 в SEQ.ID.NO 1-5.
В контексте настоящего изобретения "животные" относятся предпочтительно к животным, отличающимся от человека, и/или к животным, не имеющим (видимых) патологий, и/или не имеющим патологий, связанных с дефицитом веса.
Животные по настоящему изобретению предпочтительно представляют собой нежвачных животных и/или представляют собой животных с однокамерным желудком.
Более предпочтительно животные выбраны из группы, состоящей из свиней, домашней птицы, рыб и ракообразных, еще более предпочтительно представляют собой свиней и/или домашнюю птицу.
Происхождение и получение Фермента
Описано, что несколько видов и штаммов Thermotoga продуцируют одну или более чем одну гипертермофильную и термостабильную эндоксиланазу. Thermotoga maritima продуцирует две термостабильные эндоксиланазы, обозначенные XynA и XynB. XynA и XynB продуцируются в виде белков с предполагаемыми молекулярными массами приблизительно 120 и 40 кДа. Максимальная активность при оптимальном рН (рН 6,2 и рН 5,4 для XynA и XynB соответственно) измерена при приблизительно 92°С для XynA и при приблизительно 105°С для XynB (Winterhalter and Liebl, 1995, Appl. Env. Microbiol., 61, 1810-1815).
В WO 93/19171 описан способ получения ксиланаз из Thermotoga maritima, T. neapolitana и T. thermarum.
Опубликованы последовательности ДНК и белковые последовательности эндоксиланаз из нескольких штаммов и видов Thermotoga. Эти ксиланазы могут быть сгруппированы в два типа в соответствии с гомологией последовательности с Т. maritima XynA и XynB.
Ни в одной из ссылок, по меньшей мере ни в одной из ссылок, раскрывающих очень высокий температурный оптимум и почти отсутствие активности при 40°С, не описано применение выделенной ксиланазы Thermotoga, такой как XynB, в качестве кормовой добавки.
Ксиланазы могут быть получены из различных источников. Ксиланазы могут быть выделены/очищены после выращивания выбранного штамма Thermotoga в подходящей среде для выращивания.
Ксиланазы могут быть получены путем выращивания рекомбинантного штамма, экспрессирующего ген, кодирующий соответствующий белок (например XynB).
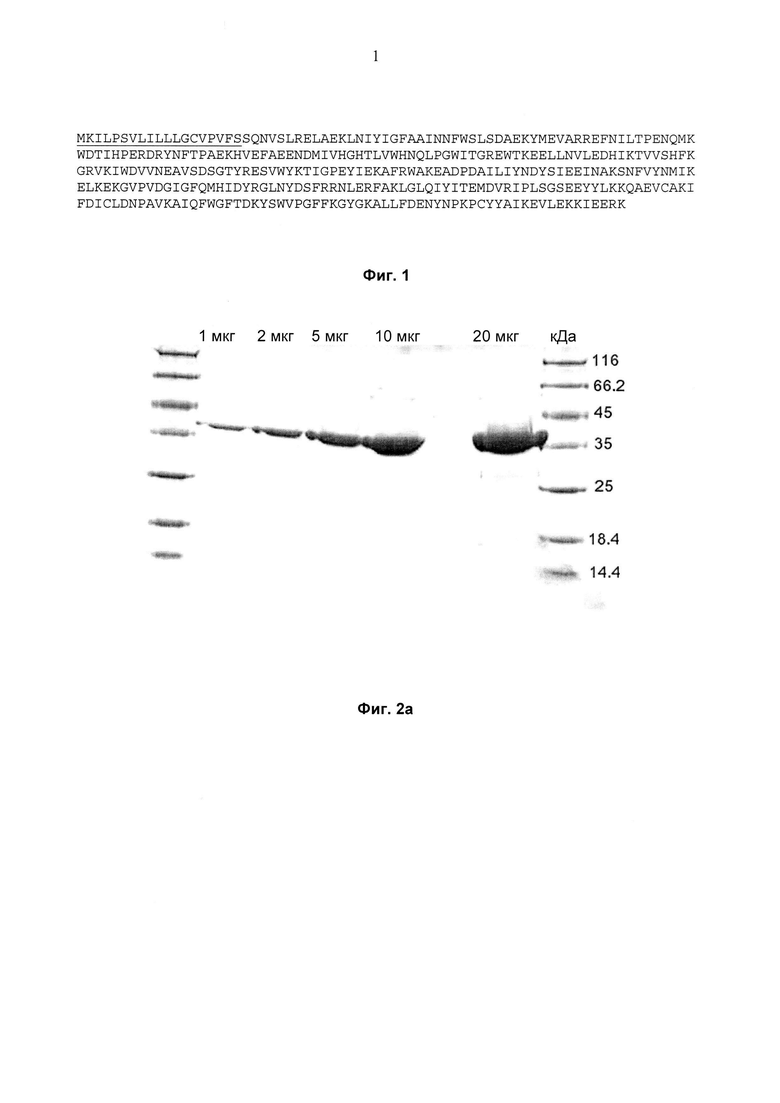
Подходящие гены могут быть выбраны среди генов, кодирующих эндо-1,4-бета-ксиланазу из Thermotoga sp. RQ2 (GenBank: АСВ09229.1), эндо-1,4-бета-ксиланазу из Thermotoga naphthophila RKU-10 (GenBank: ADA66795.1), ксиланазу из Thermotoga neapolitana (GenBank: CAA90235.1), эндо-1,4-бета-ксиланазу из Thermotoga sp. FjSS3-B.1 (GenBank: AAA90913.1) или эндо-1,4-бета-ксиланазу В из Thermotoga maritima MSB8 (GenBank: AAD35164.1 - фиг. 1 -SEQ ID NO 1).
Кроме того, варианты этих ферментов, которые демонстрируют активность при оптимальной температуре (термоактивность) и термостабильность, которые находятся в пределах диапазонов, описанных выше, могут быть получены путем модификации кодирующей последовательности этих генов.
Модификации последовательности могут включать без ограничения аминокислотную(ые) замену(ы), делецию(и) и/или вставку(и). Предпочтительные модификации последовательности представляют собой консервативные замены (например, обозначенные как положительные после анализа BLASTp).
Предпочтительно варианты ферментов имеют по меньшей мере 80% идентичности аминокислотной последовательности с Thermotoga maritima MSB8 XynB, более предпочтительно по меньшей мере 90%, еще более предпочтительно по меньшей мере 95%, или имеют по меньшей мере 90% сходство аминокислотной последовательности с Thermotoga maritima MSB8 XynB, более предпочтительно по меньшей мере 93%, 94%, 95%, еще более предпочтительно по меньшей мере 98%.
Рекомбинантная ксиланаза может быть экспрессирована в любом подходящем организме-хозяине. Особенно подходящие хозяева представляют собой бактерии, дрожжи и грибы. Предпочтительные бактериальные хозяева представляют собой штаммы Escherichia coli и Bacillus (subtilis, licheniformis, amyloliquefaciens, megaterium…) или Streptomyces (coelicolor, lividans,…).
Предпочтительные дрожжевые хозяева представляют собой штаммы Saccharomyces cerevisiae, Pichia pastoris или Yarrowia lipolytica. Предпочтительные грибковые хозяева представляют собой штаммы Aspergillus (nidulans, niger,…), Penicillium и Trichoderma.
Ксиланазы дополнительно могут быть получены в форме трансгенного растения и/или семени, экспрессирующего соответствующий фермент, или из трансгенного животного.
Ксиланаза может быть получена путем выращивания Thermotoga или рекомбинантного микробного штамма в подходящей среде для выращивания и экспрессии ксиланазы. Предпочтительно штаммы выращивают в ферментаторах.
После выращивания ксиланаза может быть выделена в виде культурального супернатанта или клеточного экстракта. Супернатант или клеточный экстракт предпочтительно дополнительно очищают с получением полуочищенного или очищенного препарата. Подходящие способы очистки включают без ограничения центрифугирование, микрофильтрацию, ультрафильтрацию, осаждение, хроматографию,…
Ксиланазы могут быть получены в виде жидкого или сухого (порошкообразного) препарата. Жидкие препараты предпочтительно стабилизуют путем добавления подходящего компонента, такого как соль (NaCl) или глицерин. Порошкообразные препараты могут быть получены, например, путем распылительной сушки или лиофилизации. Ксиланазы могут быть покрыты оболочкой.
Определение ферментативной активности
Существуют несколько способов определения ферментативной активности эндоксиланаз в жидких препаратах. Особенно подходящим является способ применения свойства эндоксиланаз гидролизовать ксилан в качестве субстрата. Реакция гидролиза высвобождает редуцирующие сахара, которые приводят к развитию типичного окрашивания вследствие реакции с динитросалициловой кислотой (DNS). Интенсивность окрашивания при 570 нм прямо пропорциональна ксиланазной активности в образце, при условии того, что концентрация субстрата остается достаточной (т.е. не более чем 10% деградация, и/или насыщающая концентрация субстрата поддерживается в тесте).
Одну DXU ксиланазы определяют как количество фермента, которое высвобождает 1 мкмоль редуцирующих сахаров (в виде ксилозного эквивалента) в минуту из раствора 3 масс./об.% ксилана березовой древесины и в 100 мМ цитратно-фосфатном буфере при рН 6 при 70°С. Реакцию осуществляют в течение 15 минут в объеме 0,8 мл (0,7 мл субстрата + 0,1 мл разбавленной ксиланазы). После инкубации реакцию останавливают путем добавления 1 мл реагента DNS (композиция: NaOH 400 мМ, 3,5-динитросалициловая кислота 40 мМ, тартрат калия-натрия 1 М). Смесь затем поддерживают при 95°С в течение 15 мин, и затем охлаждают при 25°С в течение 5 мин. Наконец, поглощение при 570 нм измеряют по сравнению с контролем.
Для оценки ксиланазной активности (DXU/мл) с точки зрения образования редуцирующего сахара строят кривую для ксилозного стандарта с ксилозой вместо препарата разведенного фермента. Все инкубации с субстратом и последующие измерения осуществляют в трех повторах.
Определение оптимальной температуры для активности эндоксиланазы и термостабильности
Температурную зависимость ксиланазной активности анализируют с использованием варианта вышеописанного способа редуцирующего сахара с динитросалициловой кислотой (DNS). Способ DNS осуществляют на смесях фермент/субстрат, инкубируемых в масляной бане при температурах, находящихся в диапазоне от 20 до 100°С. Все другие параметры способа сохраняют неизменными.
Температурную стабильность контролируют путем предварительной инкубации препаратов фермента в бане при температурах, находящихся в диапазоне от 50 до 100°С. Образцы отбирают через 0, 10, 30, 60 (и 90) минут и охлаждают в ледяной бане в течение 10 мин. Остаточную активность измеряют в трех повторах при помощи вышеописанного способа.
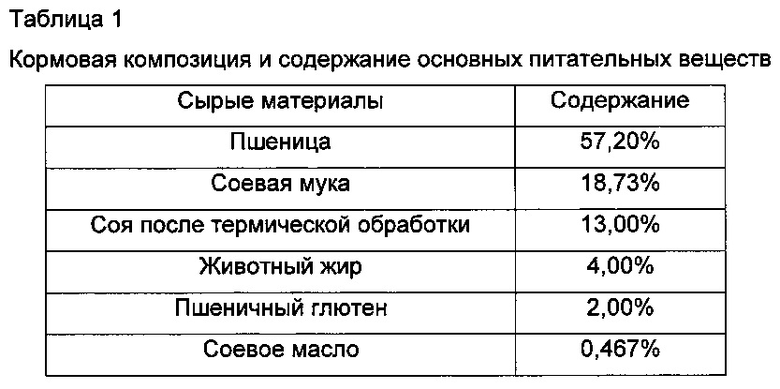
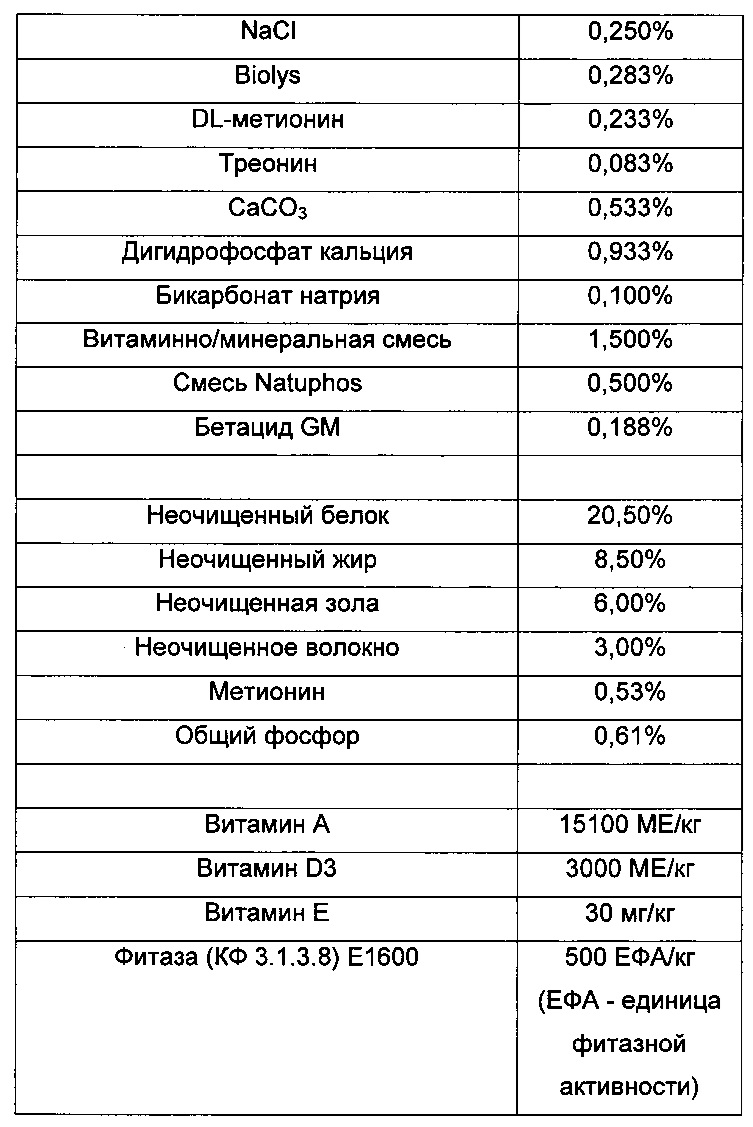
Кормовая композиция
Корма для животных (включающие силос) могут содержать зерновые, такие как пшеница, ячмень, рожь, кукуруза, рис, сорго, пшеница спельта, тритикале или овес, или побочные продукты зерновых, такие как пшеничные отруби, ячменная солома, стержни кукурузных початков, овсяный помол, пшеничные отруби, пшеничный глютен, рисовые проростки или кукурузные отруби, или другие растительные материалы, такие как соевые бобы или другие бобовые, семена рапса, люпин, горох, мука тапиоки, свекловичные мелассы, картофельная масса, арахисовая мука. Предпочтительные зерновые представляют собой пшеницу, ячмень и рожь.
Предпочтительно кормовая композиция для животных по изобретению содержит по меньшей мере один растительный белок или источник белка. Примеры растительного белка или источников белка представляют собой соевые бобы и зерновые, такие как ячмень, кукуруза, овес, рис, рожь, сорго и пшеница.
Кормовая композиция для животных по изобретению преимущественно содержит 0-80% кукурузы; и/или 0-80% сорго; и/или 0-70% пшеницы; и/или 0-70% ячменя; и/или 0-30% овса; и/или 0-40% соевой муки; и/или 0-10% рыбной муки; и/или 0-20% молочной сыворотки.
Кормовая композиция для животных по изобретению преимущественно содержит дополнительные кормовые ингредиенты или добавки, такие как ферменты, пребиотики, пробиотики, минеральные соединения и следовые элементы, витамины и провитамины, растительные, микробные или животные белки, аминокислоты, их соли и аналоги, крахмал, волокна, углеводы и сахара или подсластители, масла и мука из масличных жмыхов, растительные или животные жиры, краски и другие красители, эмульгаторы и стабилизаторы, загустители и гелеобразователи, связывающие вещества, антикомкователи и коагулянты, консерванты, регуляторы кислотности, каротиноиды и ксантофиллы, мочевина и ее производные, усилители усвояемости, стабилизаторы кишечной флоры, кокцидиостатики и другие медицинские вещества.
Предпочтительные дополнительные ферменты выбраны из группы, состоящей из фитаз, амилаз, целлюлаз, глюканаз, протеаз, маннаназ, пектиназ, гемицеллюлаз и (менее предпочтительно) (других) ксиланаз.
Предпочтительные минеральные вещества выбраны из группы, состоящей из солей (хлориды, сульфаты, фториды, карбонаты, оксиды,…), кальция, фосфора, магния, калия, натрия, марганца, цинка, никеля, молибдена, меди, железа, селена, кобальта и йода.
Предпочтительные витамины выбраны из группы, состоящей из витамина А, каротина, аскорбиновой кислоты, витамина D, D3, Ε, К, В1 тиамина, В6 пиридоксина, биотина, холина, фолиевой кислоты, ниацина, пантотеновой кислоты, В2 рибофлавина, цианокобаламина,…
Подходящие белки выбраны из группы, состоящей из растительных, микробных или животных белков.
Подходящие аминокислоты выбраны из группы, состоящей из метионина, цистеина, лизина, треонина, триптофана, изолейцина, лейцина, валина, гистидина, аргинина, глицина, серина, фенилаланина, тирозина, аспарагиновой кислоты, глутаминовой кислоты, пролина.
Подходящие микроорганизмы относятся к Aspergillus, Bacillus, Bifidobacterium, Enterococcus, Lactobacillus, Lactococcus, Leuconostoc, Pediococcus, Saccharomyces, Streptococcus, но не ограничиваются ими.
Могут быть использованы возможные другие добавки, и их можно найти, например, в Community Register of Feed Additives pursuant to Regulation (EC) №1831/2003 - Appendixes 3a&4 - Annex: List of additives, и его обновлениях.
Приготовление корма
Животная диета может быть приготовлена в виде мешанки (не гранулированной) или гранулированного корма. Как правило, измельченные комбикорма смешивают, и достаточное количество незаменимых витаминов и минеральных веществ добавляют в соответствии со стандартами для интересующих видов животных.
Композиция по изобретению может быть добавлена в форме твердого или жидкого ферментного состава или в форме кормовой добавки, такой как предварительная смесь.
Твердую композицию как правило добавляют до или во время стадии смешивания; и жидкую композицию как правило добавляют после стадии гранулирования.
Тем не менее, гипертермостабильная и гипертермоактивная жидкая композиция фермента также может быть добавлена до стадии гранулирования.
Доза ксиланазы по изобретению в корме может быть оптимизирована с использованием эмпирических методов, известных в области техники. Различные ксиланазы могут обладать отличающимися диапазонами оптимума дозы.
Краткое описание графических материалов
Фиг. 1 демонстрирует аминокислотную последовательность ксиланазы XynB из Thermotoga maritima MSB8. Сигнальный пептид подчеркнут.
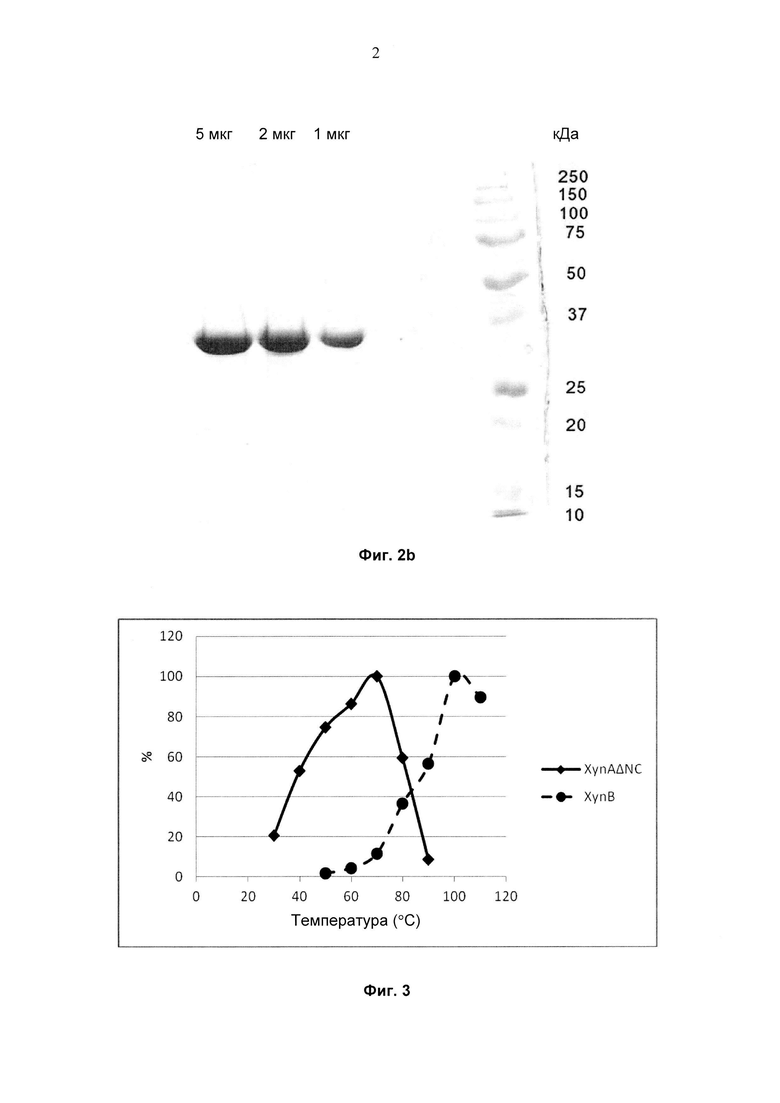
Фиг. 2а и 2b демонстрируют окрашенные кумасси голубым полиакриламидные гели с додецилсульфатом натрия (SDS) после анализа эндоксиланаз, выделенных в результате последовательных стадий очистки. Фиг. 2а: ксиланаза XynAΔNC; фиг. 2b: ксиланаза XynB.
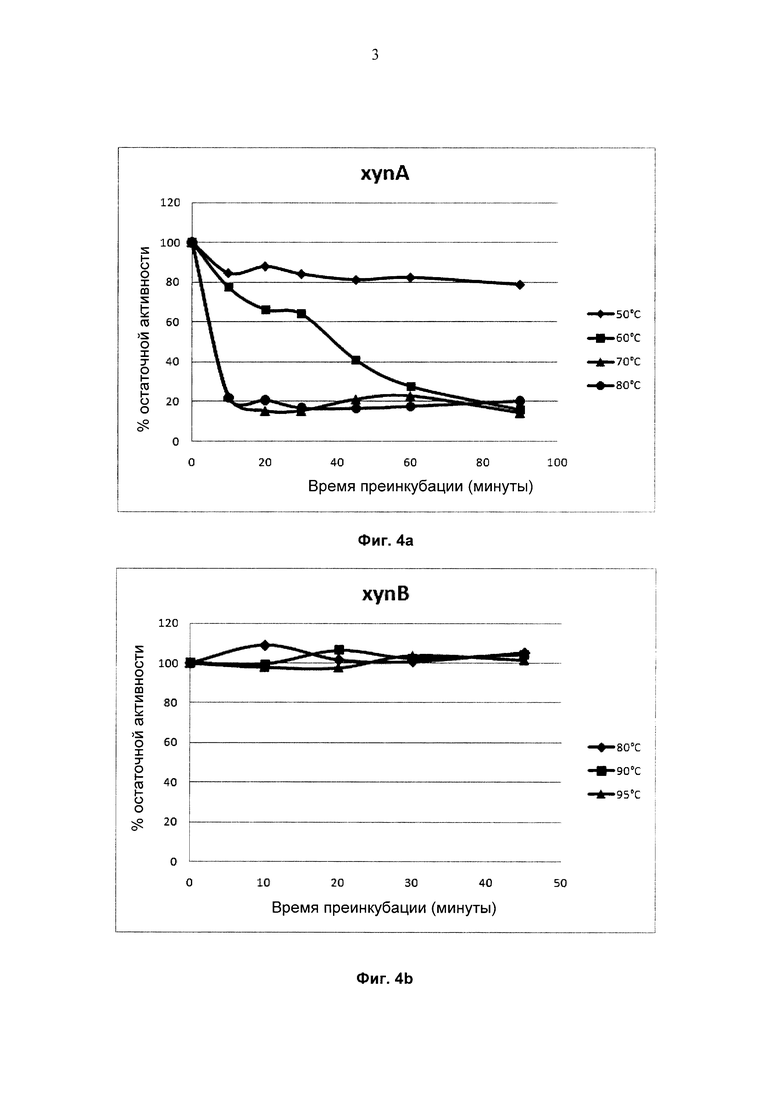
Фиг. 3 демонстрирует влияние температуры на активность эндоксиланаз XynAΔNC и XynB. Максимальная активность соответствует 100%.
Фиг. 4 демонстрирует остаточную активность эндоксиланаз после предварительной инкубации при различных температурах.
Примеры
Пример 1: получение эндоксиланазы Thermotoga.
Клонирование каталитических доменов ксиланаз XynA и XynB из Thermotoga maritima
На основе опубликованных последовательностей генов Thermotoga xynA (GenBank/GenPept™ №Z46264) и xynB (GenBank/GenPept™ №AAD35164) полноразмерный ген xynB и фрагмент ДНК, соответствующий каталитическому домену гена xynA (xynAΔNC) подвергали амплификации при помощи ПЦР (полимеразной цепной реакции) из геномной ДНК Thermotoga maritima MSB8 (DSM3109/ATCC43589) в соответствии с классическими протоколами.
Продукты ПЦР клонировали в pGEM-T Vector System I (Promega) с использованием процедуры, рекомендованной поставщиком, и использовали для трансформации ультракомпетентных клеток Е. coli DH5α®. Отбор по принципу голубой-белый дал возможность для отбора белых колоний, несущих фрагмент ПЦР. Очищенные плазмидные препараты (плазмида Nucleospin, Macherey-Nagel) секвенировали на ДНК-секвенаторе ALF (Pharmacia Biotech). Секвенирование встроенного фрагмента осуществляли с использованием универсальных праймеров Т7 и RP, а также праймеров, соответствующих внутренним последовательностям ДНК. Полученные последовательности были идентичны опубликованным последовательностям (GenBank/genPept™ №Z46264 для xynA и №AAD35164 для xynB).
Фрагмент ДНК, соответствующий производному каталитического домена модуля XynA (XynAΔNC), и полноразмерный ген XynB субклонировали в клонирующий вектор рЕТ 22b(+) (Novagen). Образующиеся в результате рекомбинантные плазмиды трансформировали в клетки Е. coli BL21 (DE3) (Stratagene).
Выращивание рекомбинантных штаммов и продукция ксиланаз XynAΔNC и XynB из Thermotoga maritima
15 мл предварительной 5-часовой культуры (37°С) клеток Е. coli BL21 (DE3), несущих гены ксиланазы, центрифугировали при 10000 g в течение 1 минуты, и осадок ресуспендировали в 900 мл питательной среды Terrific (12 г/л бактотриптона (Difco), 24 г/л дрожжевого экстракта (Difco), 4 мл/л глицерина, 12,54 г/л К2НРО4, 2,31 г/л КН2РО4), содержащего 200 мкг/мл ампициллина, в колбе для встряхивания объемом 3 литра. Культуры инкубировали при 37°С и 250 об./мин до тех пор, пока не достигали поглощения при 550 нм от 3 до 4, после чего индуцировали экспрессию фермента при помощи 1 мМ изопропил-1-тио-β-галактопиранозида.
После инкубации в течение 15 часов при 37°С клетки собирали путем центрифугирования при 18000 g в течение 30 минут при 4°С, ресуспендировали в 50 мМ BICINE, содержащем 10 мМ NaCl, разрушали в предварительно охлажденном устройстве для разрушения клеток (Constant Systems Ltd., Warwick, UK) при 28 кПси (193100 кПа) и центрифугировали при 40000 g в течение 30 минут. Хромосомную ДНК извлекали из неочищенных клеточных лизатов путем обработки 0,2% протаминсульфатом (Calbiochem) и центрифугирования при 40000 g в течение 30 минут. Затем к раствору добавляли 25 единиц бензоназы (Merck, Darmstadt, Germany).
Выделение рекомбинантных ксиланаз XynAΔNC и XynB
Неочищенные ферментативные препараты XynAΔNC и XynB из Thermotoga maritime, экспрессированные в Escherichia coli, концентрировали при помощи ультрафильтрации (UF) путем рециркуляции жидких препаратов на UF полиэфирсульфоновой мембране Biomax (отсечение = 5 кДа) на системе Proflux (Millipore). Концентрированные растворы фермента фильтровали через систему для стерильной фильтрации, включающей несколько стадий с различными отсечениями и, наконец, абсолютным фильтром (отсечение = 0,22 мкм) (Millipore).
Концентрированые жидкие ферменты сушили с использованием сушки с псевдокипящим слоем ProCell LabSystem (Glatt), где они наносились путем распыления на носитель (пшеничная мука) с получением малопыльного гранулированного препарата фермента.
Очистка рекомбинантных ксиланаз XynAΔNC и XynB
XynAΔNC очищали с использованием трехстадийной процедуры. Неочищенный экстракт подвергали диализу 2500× против хроматографического буфера (Tris-HCl 20 мМ рН 8,0) и наносили на анионообменную колонку с высокой аффинностью Q HP ХК 16/20 (GE Healthcare), и вымывали линейным градиентом (0-1 M NaCl). Полуочищенный препарат затем подвергали диализу 2500× против хроматографического буфера (Tris-HCl 20 мМ рН 8,0) и наносили на колонку для гель-фильтрации Sephacryl S-100 HR 120 мл ХК 16/70 (GE Healthcare). Активные фракции объединяли, подвергали диализу 2500× против хроматографического буфера (Tris-HCl 20 мМ рН 8,0) и наносили на анионообменную колонку с высокой аффинностью Mono-Q GL 5/50 (GE Healthcare) и вымывали линейным градиентом (0-1 M NaCl). Очищенные фракции объединяли и их чистоту проверяли при помощи электрофореза в полиакриламидном геле с додецилсульфатом натрия (SDS-PAGE) (фиг. 2а).
XynB очищали с использованием двухстадийной процедуры. Большую часть хозяйских белков удаляли при помощи тепловой обработки ферментативного препарата (30 мин при 75°С) с последующим центрифугированием (12000× g при 4°С). Супернатант подвергали диализу 2500× против хроматографического буфера (Bis-Tris 20 мМ рН 6,2, наносили на ионообменную колонку Q-Sepharose FF (GE Healthcare) и вымывали линейным градиентом (0-1 M NaCl). Чистоту рекомбинантной ксиланазы оценивали при помощи SDS-PAGE (фиг. 2b).
Характеристика рекомбинантных ферментов
Ксиланазную активность XynAΔNC и XynВ определяли при различных температурах с использованием описанных условий тестирования. Максимальные активности обнаружены при 70°С и 90-95°С, соответственно (фиг. 3).
Стабильность рекомбинантных ферментов оценивали с использованием описанного выше протокола. Результаты (фиг. 4) продемонстрировали, что XynAΔNC сохраняет 30% своей активности после инкубации при 60°С в течение 60 мин. XynB сохраняет 100% своей активности после инкубации при 90°С в течение 60 мин.
Пример 2: Использование ксиланаз Thermotoga maritima (XynAΔNC и XynB) в кормлении животных
Исследование проводили с использованием самцов или самок бройлеров (Belgabroed). В возрасте от 1 до 42 суток их содержали в закрытых напольных пеналах и давали им имеющийся в продаже корм для бройлеров, дополненный или не дополненный экзогенными ксиланазами. В возрасте 1 сутки животных (768 птиц - 384 самцов/384 самок) произвольным образом распределяли по 24 пеналам (4 обработки × 2 пола × 3 повтора) по 32 птицы/пенал, 0,8 м3/пенал. В возрасте 14 суток животных распределяли по 48 пеналам (4 обработки × 2 пола × 6 повторов) по 16 птиц. Каждый пенал оборудован 2 сосками для питья и лотком для подачи корма. Температура составила 35°С в начале и затем снижалась на 0,5°С в сутки; на 22 сутки температуру поддерживали на уровне 22°С. Световая схема составила 23 ч 30 мин световой период и 30 мин темновой период для первого периода, и 18 ч световой период и 6 ч темновой период для второго периода. Птиц вакцинировали против болезни Ньюкасла на 1 сутки (в инкубаторно-птицеводческой станции) и против болезни Гамборо + Ньюкасла на 14 сутки (через питьевую воду).
В данное исследование были включены четыре обработки. В диету, основанную на пшенице (Таблица 1), фермент не добавляли (контроль) или добавляли количество, эквивалентное 500 DXU Thermotoga maritime XynAΔNC/кг корма, или количество, эквивалентное 400 DXU Thermotoga maritima XynB/кг корма, или ксиланазу Bacillus subtilis (Belfeed™ В1100МР (Е1606), эндо-1,4-бета-ксиланазу, имеющуюся в продаже от Beldem - подразделение Puratos, Groot-Bijgaarden, Belgium), дополненную в рекомендованной дозе 10 МЕ/кг корма (положительный контроль) (ME - международная единица).
Авторы изобретения сравнивали различные уровни положительного контроля (имеющаяся в продаже ксиланаза Belfeed), такие как 50 МЕ/кг корма, и обнаружили, что оба параметра (BWG и FCR) достигали плато при 10 МЕ/кг корма. Таким образом, авторы изобретения использовали это количество для положительного контроля.
Ферменты добавляли в корм в виде жидкостей (XynAΔNC и XynB) или порошка (Belfeed), включенного в смесь до ее подмешивания в диету. Диеты животным обеспечивали ad libitum в форме комбикорма. Вода также была в свободном доступе.
Массы тела регистрировали на 1 сутки, 14 сутки и 42 сутки. Регистрировали подачу корма, и количество оставшегося корма в лотке измеряли немедленно после взвешиваний 2 и 3.
Прибавку в весе (BWG) и коэффициент кормоотдачи (FCR) определяли для возрастов 1-14 сутки, 14-42 сутки и 1-42 сутки.
Результаты данного исследования представлены в таблице 2, в которой показаны средние BWG и FCR для бройлеров в течение двух периодов.
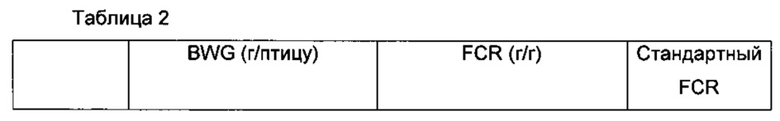
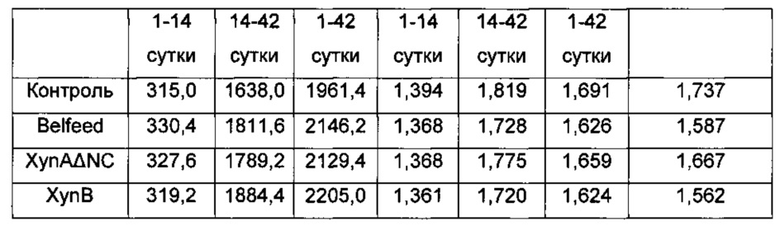
Как рост, так и FCR улучшались для диет, содержащих XynAΔNC и XynB, после 14 суток стартового периода или после общих 42 суток периода откорма. XynB демонстрировала лучшую эффективность по сравнению с XynAΔNC.
Пример 3: Применение ксиланаз Thermotoga maritina (XynB) в кормлении животных
Исследование проводили с использованием самцов или самок бройлеров (Belgabroed). В возрасте от 1 до 42 суток их содержали в закрытых напольных пеналах и давали им имеющийся в продаже корм для бройлеров, дополненный или не дополненный экзогенными ксиланазами. В возрасте 1 сутки животных (768 птиц - 384 самцов/384 самок) произвольным образом распределяли по 24 пеналам (4 обработки × 2 пола × 3 повтора) по 32 птицы/пенал, 0,8 м3/пенал. В возрасте 14 суток животных распределяли по 48 пеналам (4 обработки × 2 пола × 6 повторов) по 16 птиц. Каждый пенал оборудован 2 сосками для питья и лотком для подачи корма. Температура составила 35°С в начале и затем снижалась на 0,5°С в сутки; на 22 сутки температуру поддерживали на уровне 22°С. Световая схема составила 23 ч 30 мин световой период и 30 мин темновой период для первого периода, и 18 ч световой период и 6 ч темновой период для второго периода. Птиц вакцинировали против болезни Ньюкасла на 1 сутки (в инкубаторно-птицеводческой станции) и против болезни Гамборо + Ньюкасла на 14 сутки (через питьевую воду).
В данное исследование были включены четыре обработки. В диету, основанную на пшенице (Таблица 3), добавляли количество, эквивалентное 200 DXU XynB/кг корма, или количество, эквивалентное 400 DXU XynB/кг корма, или имеющуюся в продаже грибковую ксиланазу Hostazym® X (Huvepharma; КФ №Е1617), дополненную в рекомендованной дозе 100 млн-1, или ксиланазу Bacillus subtilis (Belfeed™ В1100МР (Е1606), эндо-1,4-бета-ксиланазу, имеющуюся в продаже от Beldem - подразделение Puratos, Groot-Bijgaarden, Belgium), дополненную в рекомендованной дозе 10 МЕ/кг корма или 100 млн-1.
Ферменты добавляли в корм в виде порошков, включенных в смесь до ее подмешивания в диету. Диеты животным обеспечивали ad libitum в форме комбикорма. Вода также была в свободном доступе.
Массы тела регистрировали на 1 сутки, 14 сутки и 42 сутки. Регистрировали подачу корма, и количество оставшегося корма в лотке измеряли немедленно после взвешиваний 2 и 3.
Прибавку в весе (BWG) и коэффициент кормоотдачи (FCR) определяли для возрастов 1-14 сутки, 14-42 сутки и 1-42 сутки.

Результаты данного исследования представлены в таблице 4, в которой представлены средние BWG и FCR для бройлеров в течение двух периодов.
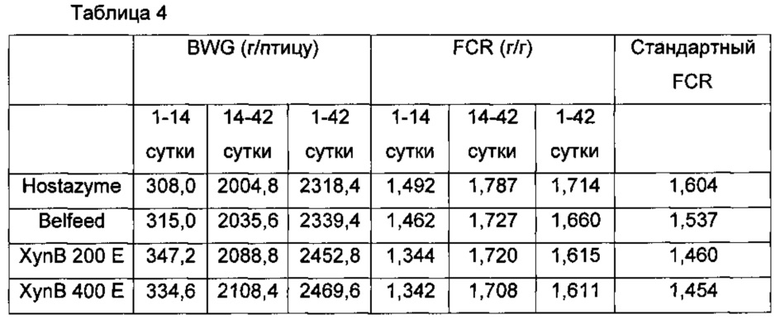
Как рост, так и FCR улучшались для диет, содержащих ферменты XynB, после 14 суток стартового периода или после общих 42 суток периода откорма. XynB демонстрировала лучшие BWG и FCR по сравнению с имеющимися в продаже ксиланазами.








Изобретение относится к области кормопроизводства. Корм для животных выбран из группы, состоящей из силоса, гранулированного корма и мешанки. Указанный корм для животных дополнен композицией, содержащей ксиланазу. Указанная ксиланаза является гипертермофильной и гипертермостабильной. Оптимальная температура ксиланолитической активности указанной композиции составляет больше чем 80°С, где более чем 70% ксиланолитической активности указанной композиции устойчиво к 30 минутам нагревания при 90°С. Отношение ксиланолитической активности указанной композиции при оптимальной температуре и при 40°С составляет больше чем 10. Применение гипертермофильной и гипертермостабильной ксиланазы для улучшения прибавки в весе и/или коэффициента кормоотдачи у животного. Способ получения корма для животных включает стадии выбора корма, содержащего гемицеллюлозу; и добавление композиции, содержащей гипертермофильную и гипертермостабильную ксиланазу. 4 н. и 15 з.п. ф-лы, 6 ил., 4 табл., 3 пр.
1. Корм для животных, выбранный из группы, состоящей из силоса, гранулированного корма и мешанки, где указанный корм для животных дополнен композицией, содержащей ксиланазу, где указанная ксиланаза является гипертермофильной и гипертермостабильной, где оптимальная температура ксиланолитической активности указанной композиции составляет больше чем 80°С, где более чем 70% ксиланолитической активности указанной композиции устойчиво к 30 минутам нагревания при 90°С, и где отношение ксиланолитической активности указанной композиции при оптимальной температуре и при 40°С составляет больше чем 10.
2. Корм для животных по п. 1, где оптимальная температура ксиланолитической активности указанной композиции составляет больше чем 85°С, предпочтительно больше чем 90°С.
3. Корм для животных по п. 1 или 2, где отношение ксиланолитической активности указанной композиции при оптимальной температуре и при 40°С составляет больше чем 20.
4. Корм для животных по п. 1, где ксиланазную активность указанной композиции измеряют с использованием 3 масс./об.% ксилана, предпочтительно с использованием 3 масс./об.% ксилана березовой древесины в качестве субстрата.
5. Корм для животных по п. 1, где ксиланазную активность указанной композиции измеряют после 15-минутной реакции.
6. Корм для животных по п. 1, где гипертермофильная и гипертермостабильная ксиланаза обладает более чем 80% идентичностью и/или 95% сходством с ксиланазой, выбранной из группы, состоящей из SEQ.ID.NO:1, SEQ.ID.NO:2, SEQ.ID.NO:3, SEQ.ID.NO:4, SEQ.ID.NO:5, аминокислот 21-332 в SEQ.ID.NO:1, в SEQ.ID.NO:2, в SEQ.ID.NO:3, в SEQ.ID.NO:4 и в SEQ.ID.NO:5.
7. Корм для животных по п. 1, где гипертермофильная и гипертермостабильная ксиланаза обладает более чем 99% идентичностью с ксиланазой, выбранной из группы, состоящей из SEQ.ID.NO:1, SEQ.ID.NO:2, SEQ.ID.NO:3, SEQ.ID.NO:4, SEQ.ID.NO:5, аминокислот 21-332 в SEQ.ID.NO:1, в SEQ.ID.NO:2, в SEQ.ID.NO:3, в SEQ.ID.NO:4 и в SEQ.ID.NO:5.
8. Корм для животных по п. 1, содержащий от 0,08 до 40 мг/кг указанной гипертермофильной и гипертермостабильной ксиланазы.
9. Корм для животных по п. 1, содержащий по меньшей мере 50% (от сухой массы) растительного материала.
10. Корм для животных по п. 9, где растительный материал выбран из группы, состоящей из зерновых, бобовых, свекловичной мелассы, картофельной массы и арахисовой муки.
11. Корм для животных по п. 1, содержащий по меньшей мере 5% (сухая масса) белков и/или по меньшей мере 2% (сухая масса) жира.
12. Применение гипертермофильной и гипертермостабильной ксиланазы для улучшения прибавки в весе и/или коэффициента кормоотдачи у животного, где указанная гипертермофильная и гипертермостабильная ксиланаза обладает температурным оптимумом больше чем 80°С, где более чем 70% ксиланолитической активности указанной гипертермофильной и гипертермостабильной ксиланазы устойчиво к 30-минутному нагреванию при 90°С, и где отношение активности при оптимальной температуре и при 40°С указанной гипертермофильной и гипертермостабильной ксиланазы составляет больше чем 10.
13. Применение по п. 12, где ксиланазную активность измеряют с использованием 3 масс./об.% ксилана, предпочтительно с использованием 3 масс./об.% ксилана березовой древесины в качестве субстрата.
14. Применение по п. 12 или 13, где ксиланазную активность измеряют после 15-минутной реакции.
15. Применение корма для животных по любому из пп. 1-11 для улучшения прибавки в весе и/или коэффициента кормоотдачи у животного.
16. Применение по пп. 12, 15, где животное представляет собой нежвачное позвоночное животное или ракообразное, и предпочтительно представляет собой рыбу, свинью или домашнюю птицу, более предпочтительно свинью или домашнюю птицу.
17. Способ получения корма для животных по любому из пп. 1-11, при котором осуществляют стадии:
а) выбора корма, содержащего гемицеллюлозу;
б) добавления композиции, содержащей гипертермофильную и гипертермостабильную ксиланазу, где более чем 70% ксиланолитической активности указанной композиции устойчиво к 30-минутному нагреванию указанной композиции при 90°С, где оптимальная температура ксиланолитической активности указанной композиции составляет больше чем 80°С, и где отношение ксиланолитической активности указанной композиции при оптимальной температуре и при 40°С составляет больше чем 10.
18. Способ по п. 17, где ксиланазную активность указанной композиции измеряют с использованием 3 масс./об.% ксилана, предпочтительно с использованием 3 масс./об.% ксилана березовой древесины в качестве субстрата.
19. Способ по п. 17 или 18, где ксиланазную активность, представленную в указанной композиции, измеряют после 15-минутной реакции.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 5902581 A, 11.05.1999 | |||
| DE 19531944 A1, 20.02.1997. | |||
Авторы
Даты
2017-01-12—Публикация
2012-11-09—Подача