Изобретение относится к области физико-химических методов анализа, в частности к анализу растворов на предмет количественного определения антиоксидантной активности веществ.
Известен способ спектрофотометрического определения антиоксидантной активности (АОА) основанный на способности ингибирования стабильного свободного радикала дифенилпикрилгидразила (ДФПГ) веществами с АО свойствами [Tuanjai N., Supalax S., Thawatchai Т., Wittaya N. New approach for evaluation of the antioxidant capacity based on scavenging DPPH free radical in micelle systems // J. Food Research International. 04/2011; 44(3): 798-806]. Сущность способа заключается в измерении снижения оптической плотности раствора ДФПГ в результате реакции с антиоксидантом при длине волны 528 нм. Значения АОА рассчитываются по концентрации анализируемого вещества, необходимого для реагирования с 50% ДФПГ.
Недостаток данного способа заключается в том, что результаты измерений выражаются не в стандартизированных единицах, а в относительных, точнее в эквивалентах галловой кислоты. Значения зависят от эталонного вещества, что не позволяет сравнивать АОА веществ, свойства которых определены в сравнении с разными эталонными веществами. Также к недостаткам данного метода можно отнести ограничения при исследовании окрашенных объектов.
Известен способ электронно-парамагнитной резонансной спектроскопии (ЭПР-спектроскопии) количественного определения АОА растворимого и молотого кофе [ V.,
V.,  A.,
A.,  F. Coffee as a source of antioxidants: An EPR study // J. Food Chemistry. 114 (2009) 859-868], основанный на использовании в качестве окислителей ряда стабильных свободных радикалов, в т.ч. ДФПГ, ЭПР-спектры которых, после смешения с веществами, обладающими АОА, снижают свою интенсивность. Количественную оценку АОА исследуемых образцов приводят в эквивалентах тролокса.
F. Coffee as a source of antioxidants: An EPR study // J. Food Chemistry. 114 (2009) 859-868], основанный на использовании в качестве окислителей ряда стабильных свободных радикалов, в т.ч. ДФПГ, ЭПР-спектры которых, после смешения с веществами, обладающими АОА, снижают свою интенсивность. Количественную оценку АОА исследуемых образцов приводят в эквивалентах тролокса.
Недостаток способа заключается в том, что количественные значения АОА представляются в относительных единицах (эквивалентах тролокса), что не позволяет сравнить результат со значениями других методов. Также исходя из результатов данного способа, нельзя описать механизм протекания реакций между свободным радикалом и веществом, обладающим АОА.
Наиболее близким решением служит способ определения АОА растительных экстрактов и соков [Sanna D., Delogu G., Mulas M., Schirra M., Fadda A. Determination of free radical scavenging activity of plant extracts through DPPH assay: an EPR and UV-Vis study // J. Food Analytical Methods. 5 (2012) 759-766], заключающийся в том, что раствор ДФПГ смешивают с образцами (растительные экстракты, соки) обладающими АОА. Количественную оценку АОА проводят по изменению интенсивности ЭПР-спектров раствора ДФПГ, установленных до и после взаимодействия с анализируемыми образцами.
К недостаткам способа относится выражение значения АОА в относительных единицах ЕС50, то есть концентрации экстракта, необходимой для снижения начальной концентрации ДФПГ на 50%. Результаты данного способа не несут информацию о возможных механизмах протекания реакции между свободным радикалом и анализируемым веществом.
Задача настоящего изобретения состоит в преодолении недостатков известных способов и в создании нового способа, позволяющего повысить точность и экспрессность определения, а также позволяющего количественно в стандартизированных единицах установить антиоксидантную активность определяемого вещества в исследуемом образце и механизм взаимодействия АО со свободными радикалами ДФПГ.
Задача решается тем, что в способе определения антиоксидантной активности веществ методом ЭПР-спектроскопии спиртовой раствор стабильного радикала ДФПГ смешивают с раствором, содержащим вещество, обладающее антиоксидантной активностью (АОА), оценку антиоксидантной активности проводят по уменьшению числа парамагнитных центров стабильного радикала, рассчитанных из ЭПР-спектров до реакции и после полного прохождения химической реакции между радикалом и анализируемым веществом, в качестве меры антиоксидантной активности вещества используют моль эквиваленты в литре, полученные из разности количества парамагнитных частиц радикала до и после взаимодействия с АО, а значение АОА рассчитывают по формуле:
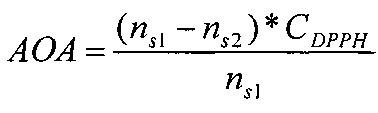 ,
,
где АОА - антиоксидантная активность, М-экв;
CDPPH - концентрация ДФПГ в исходном растворе, М;
ns1 - начальное количество парамагнитных частиц ДФПГ, ед.
ns2 - количество парамагнитных частиц ДФПГ после взаимодействия с анализируемым веществом, ед.
Сущность заявляемого способа заключается в том, что спиртовой раствор ДФПГ имеет длительный стабильный сигнал в виде ЭПР-спектра, из которого можно выразить количество парамагнитных частиц. Число парамагнитных частиц свободного радикала ДФПГ снижается после добавления вещества обладающего АОА в результате протекания химических реакций в соответствии с концентрацией и количеством функциональных групп:
1. n DPPH +m Ar-OH→Ar-О
+m Ar-OH→Ar-О +DPPH-H
+DPPH-H
2. Ar-О +DPPH
+DPPH →Ar-O-DPPH
→Ar-O-DPPH
3. Ar-О +Ar-О
+Ar-О →Ar-О-О-Ar
→Ar-О-О-Ar
где DPPH - стабильный радикал ДФПГ,
- стабильный радикал ДФПГ,
Ar-ОН - вещество с антиоксидантными свойствами,
Ar-О - промежуточный радикальный продукт взаимодействия АО с ДФПГ,
- промежуточный радикальный продукт взаимодействия АО с ДФПГ,
DPPH-H - восстановленная форма ДФПГ,
Ar-O-DPPH - молекулярный продукт взаимодействия АО с ДФПГ,
Ar-O-O-Ar - молекулярный продукт рекомбинации радикалов АО.
Определение антиоксидантной активности проводят по разности количества парамагнитных частиц стабильного свободного радикала, измеряемых до и после полного прохождения химических реакций (1-2) между свободным радикалом и анализируемым веществом. Определение проводят после завершения химической реакции, которое сопровождается снижением количества парамагнитных частиц свободного радикала после добавления анализируемого вещества. АОА в этом случае рассчитывают по формуле:
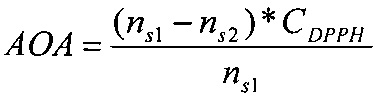 ,
,
где АОА - антиоксидантная активность, М-экв;
CDPPH - концентрация ДФПГ в исходном растворе, М;
ns1 - начальное количество парамагнитных частиц ДФПГ, ед.;
ns2 - количество парамагнитных частиц ДФПГ после взаимодействия с анализируемым веществом, ед.
В качестве реагентов могут быть использованы стабильные катион радикалы, например 2,2'-дифенил-1-пикрилгидразил (ДФПГ). В качестве веществ, обладающих АОА, могут быть использованы индивидуальные антиоксиданты, биодобавки, соки, лекарственные экстракты, экстракты различных сортов чая и кофе.
В качестве протонных растворителей могут быть использованы метиловый и этиловый спирты. Также может быть использована смесь растворителей.
Емкость для измерений должна быть изготовлена из кварца или стекла. Указанные отличия существенны. В предложенном способе измеряется на прямую содержание свободного радикала в виде количества парамагнитных частиц. Использование в качестве единиц измерения антиоксидантной активности моль эквивалентов в литре позволяет сравнивать результаты, полученные различными методами. Концентрация исходного раствора стабильного радикала значительно больше концентрации вещества обладающего АОА в исследуемом образце, поэтому химическая реакция протекает быстро, что увеличивает экспрессность метода. Прямой расчет парамагнитных частиц позволяет устанавливать механизм взаимодействия радикала ДФПГ с АО.
В настоящее время из патентной и научно-технической литературы неизвестен способ определения антиоксидантной активности в заявляемой совокупности признаков.
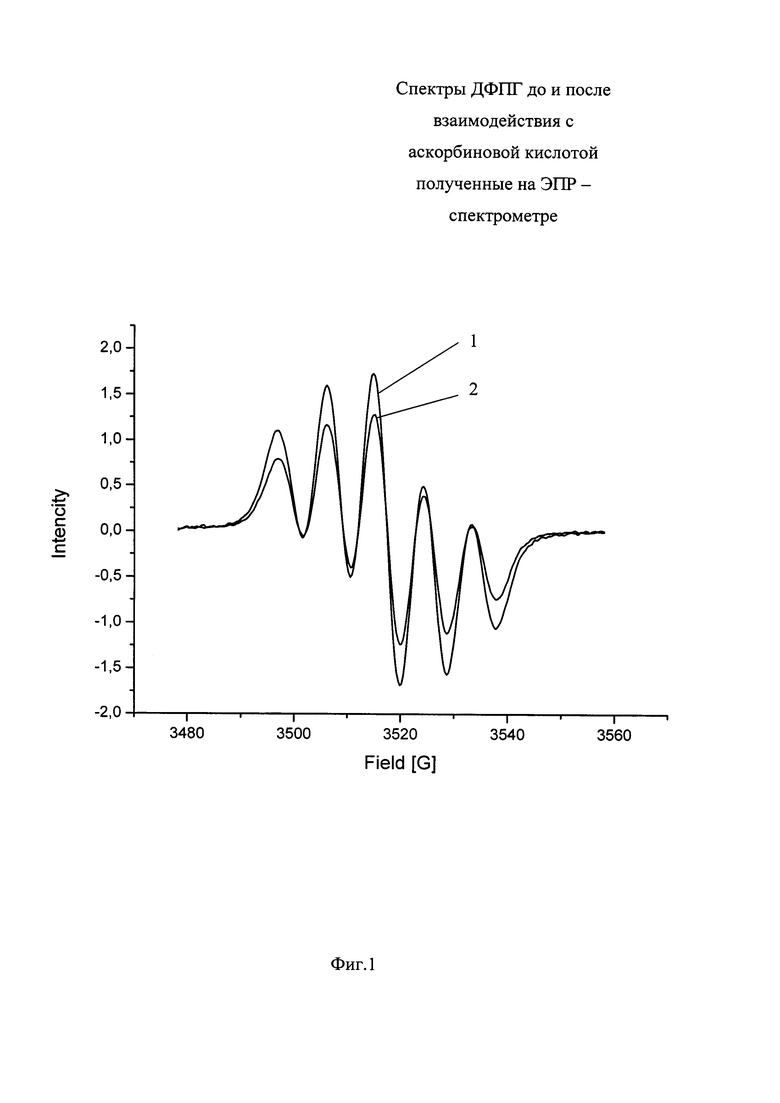
На фиг. 1 представлена зависимость поглощаемой мощности переменного поля от напряженности внешнего магнитного поля. ЭПР-спектры ДФПГ: 1 - до взаимодействия с аскорбиновой кислотой; 2 - после взаимодействия с аскорбиновой кислотой.
На фиг. 2 представлена зависимость поглощаемой мощности переменного поля от напряженности внешнего магнитного поля. ЭПР-спектры ДФПГ: 3 - до взаимодействия с пирокатехином; 4 - после взаимодействия с пирокатехином.
На фиг. 3 представлена зависимость поглощаемой мощности переменного поля от напряженности внешнего магнитного поля. ЭПР-спектры ДФПГ: 5 - до взаимодействия с зеленым чаем; 6 - после взаимодействия с зеленым чаем.
На фиг. 4 представлена зависимость поглощаемой мощности переменного поля от напряженности внешнего магнитного поля. ЭПР-спектры ДФПГ: 7 - до взаимодействия с черным чаем; 8 - после взаимодействия с черным чаем.
Способ иллюстрируется следующими примерами.
Пример 1
Навеску ДФПГ растворили в этаноле с итоговой концентрацией 0,001М. Получили ЭПР-спектр приготовленного раствора ДФПГ. После математической обработки ЭПР-спектра получили значения количества парамагнитных частиц (ns1=1,95*1016 ед.) и концентрации свободного радикала ДФПГ (CDPPH=1,03*10-3 М).
Далее в 1 мл приготовленного раствора ДФПГ внесли 1*10-4 М спиртового раствора аскорбиновой кислоты. Получили ЭПР-спектр приготовленной смеси. Установившееся значение количества парамагнитных частиц после протекания реакции между свободным радикалом ДФПГ и аскорбиновой кислотой составляет ns2=1,38*1016 ед.
ЭПР-спектры свободного радикала ДФПГ до и после взаимодействия с аскорбиновой кислотой приведены на фиг. 1.
Антиоксидантную активность аскорбиновой кислоты рассчитывали по формуле:
 ,
,
где АОА - антиоксидантная активность аскорбиновой кислоты, М-экв;
CDPPH - концентрация свободного радикала ДФПГ в исходном растворе, М;
ns1 - начальное количество парамагнитных частиц свободного радикала ДФПГ;
ns2 - количество парамагнитных частиц свободного радикала ДФПГ после взаимодействия с аскорбиновой кислотой.
Расчет показал, что с учетом разбавления АОА аскорбиновой кислоты равна 3,01*10-4 М-экв, что свидетельствует протеканию предполагаемых реакций (1 и 2):
2 DPPH +АК→АК*+DPPH-H
+АК→АК*+DPPH-H
АК +DPPH
+DPPH →АК-O-DPPH
→АК-O-DPPH
где АК - аскорбиновая кислота,
АК - промежуточный радикальный продукт окисления аскорбиновой кислоты.
- промежуточный радикальный продукт окисления аскорбиновой кислоты.
Получившееся значение АОА объясняется наличием двух функциональных групп в молекуле аскорбиновой кислоты, которые нейтрализуют две молекулы свободного радикала ДФПГ, а также протеканием реакции между продуктом окисления аскорбиновой кислоты и одной молекулой свободного радикала ДФПГ с образованием стабильного молекулярного продукта.
Пример 2
Навеску ДФПГ растворили в этаноле с итоговой концентрацией 0,001М. Получили ЭПР-спектр приготовленного раствора ДФПГ. После математической обработки ЭПР-спектра получили значения количества парамагнитных частиц (ns1=1,85*1016 ед.) и концентрации свободного радикала ДФПГ (CDPPH=0,98*10-3 М).
Далее в 1 мл приготовленного раствора ДФПГ внесли 1*10-4 М водного раствора пирокатехина. Получили ЭПР-спектр приготовленной смеси. Установившееся значение количества парамагнитных частиц после протекания реакции между свободным радикалом ДФПГ и пирокатехином составляет ns2=1,09*1016 ед.
ЭПР-спектры свободного радикала ДФПГ до и после взаимодействия пирокатехином приведены на фиг. 2.
Антиоксидантную активность пирокатехина рассчитывали по формуле:
 ,
,
где АОА - антиоксидантная активность пирокатехина, М-экв;
CDPPH - концентрация свободного радикала ДФПГ в исходном растворе, М;
ns1 - начальное количество парамагнитных частиц свободного радикала ДФПГ;
ns2 - количество парамагнитных частиц свободного радикала ДФПГ после взаимодействия с пирокатехином.
Расчет показал, что с учетом разбавления значение АОА пирокатехина составляет 4,03*10-4 М-экв, что свидетельствует о протекании предполагаемых реакций (1 и 2):
2 DPPH +ПК→ПК
+ПК→ПК +2DPPH-H
+2DPPH-H
ПК +DPPH
+DPPH →ПК-O-DPPH
→ПК-O-DPPH
где ПК - пирокатехин,
ПК - промежуточный радикальный продукт окисления пирокатехина.
- промежуточный радикальный продукт окисления пирокатехина.
Получившееся значение АОА объясняется наличием двух функциональных групп в молекуле пирокатехина, которые нейтрализуют две молекулы ДФПГ, а также протеканием реакции между продуктом окисления пирокатехина и двумя молекулами ДФПГ с образованием стабильных молекулярных продуктов.
Пример 3
Чайный пакетик Greenfield® (зеленый чай с мелиссой) заливали 100 мл кипятка, настаивали 6-8 мин. Пакетик вынимали, раствор доводили дистиллированной водой до метки (100 мл).
Навеску ДФПГ растворили в метаноле с итоговой концентрацией 0,001М. Полученный раствор измерили на ЭПР-спектрометре. После математической обработки ЭПР-спектра получили значения количества спинов (ns1=1,90*1016 ед.) и концентрации ДФПГ (CDPPH=1,00*10-3 М).
Далее в 1 мл раствора ДФПГ внесли водный раствор зеленого чая. Полученный раствор измерили на ЭПР-спектрометре. Установившееся значение количества спинов после протекания реакции между ДФПГ и зеленым чаем составляет ns2=1,15*1016 ед.
Спектры ДФПГ до и после взаимодействия с зеленым чаем, полученные на ЭПР-спектрометре, приведены на фиг. 3.
Антирадикальную активность зеленого чая рассчитывали по формуле:
 ,
,
где АОА - антиоксидантная активность зеленого чая, М-экв;
CDPPH - концентрация стабильного радикала ДФПГ в исходном растворе, М;
ns1 - начальное количество парамагнитных частиц ДФПГ;
ns2 - количество парамагнитных частиц ДФПГ после взаимодействия с зеленым чаем.
Расчет показал, что с учетом разбавления АОА зеленого чая составляет 3,97*10-4 М-экв.
Пример 4
Чайный пакетик Принцесса Нури® (черный чай классический) заливали 100 мл кипятка, настаивали 6-8 мин. Пакетик вынимали, раствор доводили дистиллированной водой до метки (100 мл).
Навеску ДФПГ растворили в метаноле с итоговой концентрацией 0,001М. Полученный раствор измерили на ЭПР-спектрометре. После математической обработки ЭПР-спектра получили значения количества спинов (ns1=1,85*1016 ед.) и концентрации ДФПГ (CDPPH=0,98*10-3 М).
Далее в 1 мл раствора ДФПГ внесли водный раствора черного чая. Полученный раствор измерили на ЭПР-спектрометре. Установившееся значение количества спинов после протекания реакции между ДФПГ и черным чаем составляет ns2=0,97*1016 ед.
Спектры ДФПГ до и после взаимодействия с зеленым чаем полученные на ЭПР-спектрометре приведены на фиг. 4.
Антиоксидантную активность черного чая рассчитывали по формуле:
 ,
,
где АОА - антиоксидантная активность черного чая, М-экв;
CDPPH - концентрация стабильного радикала ДФПГ в исходном растворе, М;
ns1 - начальное количество спинов ДФПГ;
ns2 - количество спинов ДФПГ после взаимодействия с черным чаем.
Расчет показал, что с учетом разбавления АОА черного чая равна 4,53*10-4 М-экв.
Таким образом, технический результат заключается в повышении точности, сокращении измерительных стадий, что приводит к повышению экспрессности определения, введения универсальных единиц измерения, возможности установления механизма реакции взаимодействия АО со свободным радикалом ДФПГ.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения антиокислительной активности лекарственного растительного сырья и фитопрепаратов методом дифференциальной спектрофотометрии | 2018 |
|
RU2712069C2 |
| ПОТЕНЦИОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ ЕМКОСТИ С ИСПОЛЬЗОВАНИЕМ 2,2'-ДИФЕНИЛ-1-ПИКРИЛГИДРАЗИЛА | 2022 |
|
RU2791901C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНТЕГРАЛЬНОЙ АНТИОКСИДАНТНОЙ АКТИВНОСТИ С ИСПОЛЬЗОВАНИЕМ ПОЛИМЕТАКРИЛАТНОЙ МАТРИЦЫ | 2009 |
|
RU2391660C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ ЕМКОСТИ ВЕЩЕСТВ | 2023 |
|
RU2825002C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ АКТИВНОСТИ ПРИРОДНЫХ СОЕДИНЕНИЙ В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2801864C1 |
| АНТИОКСИДАНТНЫЕ КОМПОЗИЦИИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2654804C2 |
| Сухой экстракт из фукусовых водорослей, обладающий антиоксидантным действием, и способ его получения | 2016 |
|
RU2650808C1 |
| СПЕКТРОФОТОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ АНТИРАДИКАЛЬНОЙ АКТИВНОСТИ НИЗКОМОЛЕКУЛЯРНЫХ АНТИОКСИДАНТОВ В ЭКСТРАКТАХ ПИЩЕВЫХ И ЛЕКАРСТВЕННЫХ РАСТЕНИЙ | 2009 |
|
RU2423691C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ АНТИОКСИДАНТОВ | 2010 |
|
RU2426109C1 |
| АНТИОКСИДАНТНОЕ И АНТИРАДИКАЛЬНОЕ СРЕДСТВО | 2000 |
|
RU2178303C1 |



Изобретение относится к области физико-химических методов анализа, в частности к анализу растворов на предмет количественного определения антиоксидантной активности (АОА). Сущность заявляемого способа заключается в том, что определение АОА проводят по разности количества парамагнитных частиц стабильного радикала, измеряемых до и после прохождения химической реакции частиц радикала с антиоксидантами (АО). Задача настоящего изобретения состоит в преодолении недостатков известных способов и в создании нового способа, позволяющего повысить точность и экспрессность определения, а также позволяющего количественно в стандартизированных единицах установить АОА определяемого вещества в исследуемом образце и механизм взаимодействия АО со свободными радикалами дифенилпикрилгидразила (ДФПГ). 4 ил., 4 пр.
Способ определения антиоксидантной активности веществ методом ЭПР-спектроскопии, заключающийся в том, что спиртовой раствор стабильного радикала ДФПГ смешивают с раствором, содержащим вещество, обладающее антиоксидантной активностью (АОА), количественную оценку АОА проводят из ЭПР-спектров спиртового раствора ДФПГ, отличающийся тем, что оценку антиоксидантной активности проводят по уменьшению числа парамагнитных центров стабильного радикала, рассчитанных из ЭПР-спектров до реакции и после полного прохождения химической реакции между радикалом и анализируемым веществом, в качестве меры антиоксидантной активности вещества используют моль эквиваленты в литре, полученные из разности количества парамагнитных частиц радикала до и после взаимодействия с АО, а значение АОА рассчитывают по формуле:
 ,
,
где
AOA - антиоксидантная активность, М-экв;
CDPPH - концентрация ДФПГ в исходном растворе, M;
ns1 - начальное количество парамагнитных частиц ДФПГ, ед.;
ns2 - количество парамагнитных частиц ДФПГ после взаимодействия с анализируемым веществом, ед.
| A | |||
| POPA et al | |||
| Antioxidant activity of medicinal tea evidenced by electron spin resonance / Rom | |||
| Journ | |||
| Phys., Bucharest, 2015, Vol | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Приспособление для перевода трамвайных стрелок с вагона | 1924 |
|
SU1501A1 |
| A.B | |||
| dos Santos et al | |||
| Antioxidant Properties of Plant Extracts: an EPR and DFT Comparative Study of the Reaction with DPPH, TEMPOL and Spin Trap DMPO / J | |||
| Braz | |||
| Chem | |||
| Soc., 2009, Vol | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| А.А | |||
| Федосеева и др | |||
| Антиоксидантная активность настоев чая / Химия растительного сырья, 2008, No | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Устройство для разметки подлежащих сортированию и резанию лесных материалов | 1922 |
|
SU123A1 |
Авторы
Даты
2017-03-24—Публикация
2015-12-31—Подача