Изобретение относится к медицине, а именно к экспериментальной медицине и андрологии, и предназначено для моделирования первичного мужского гипогонадизма у лабораторных животных.
Мужской гипогонадизм - патологическое состояние, обусловленное уменьшением уровня андрогенов в организме или снижением чувствительности к ним. Первичный гипогонадизм вызван нарушением функции половых желез (Дедов И.И. и др., Эндокринология, М., Гэотар-Медиа, 2007 г.). Андрогены играют ключевую роль не только в поддержании репродуктивной и сексуальной функций мужского организма. Прослеживается взаимосвязь между снижением уровня андрогенов и деминерализацией костей, саркопенией, нарушением метаболизма жиров, депрессией, повышенной утомляемостью, угасанием когнитивных функций и пр. (Dohle GR et al., Guidelines on male hypogonadism, Arnhem (The Netherlands), Europian Assotiation of Urology, 2012). Имеются данные о том, что снижение уровня тестостерона и увеличение 17β-эстрадиола коррелируют с повышенным риском сердечно-сосудистых заболеваний и сердечно-сосудистой смертности (Corona G. et al., Hypogonadism as a risk factor for cardiovascular mortality in men: a meta-analytic study. Eur J Endocrinol., 2011; 165(5):687-701).
На сегодняшний день основным методом лечения первичного мужского гипогонадизма остается заместительная терапия андрогенами, которая имеет ряд противопоказаний и побочных эффектов. Успешно устраняя некоторые симптомы андрогенодефицита, экзогенный тестостерон подавляет сперматогенез и лишь усугубляет такое значимое проявление гипогонадизма, как мужская инфертильность (Kliesch S. Testosterone and infertility. Urologe A, 2010; 49(1):32-6). Согласно европейским рекомендациям в рамках лечения мужского бесплодия заместительная терапия тестостероном строго противопоказана (Jungwirth A., Guidelines on male infertility, Arnhem (The Netherlands), European Association of Urology; 2013).
Таким образом, существует потребность в поиске новых подходов к лечению первичного мужского гипогонадизма, нацеленных на восстановление собственного андрогенпродуцирующего аппарата. Для исследований в этой области необходимо использование удобной экспериментальной модели первичного гипогонадизма.
Так, из уровня техники известен способ моделирования первичного мужского гипогонадизма, заключающийся в введении животным водного раствора 0,1% хлорида кадмия интраперитонеально из расчета 3 мг/кг веса животного (Пахомов А.В., Коррекция нарушений полового поведения самцов крыс при экспериментальном гипогонадизме, вызванном введением хлорида кадмия, путем гормонотерапии и трансплантации суспензии интерстициальных клеток, Вестник Харьковского национального университета им. В.Н. Каразина. Серия: биология, Вып. 17, №1056, 2013 г., с. 173). Недостатком данного способа является высокая токсичность для всего организма экспериментального животного.
Известен также способ моделирования первичного мужского гипогонадизма, заключающийся в фиксации яичек животных в районе латеральных каналов брюшной полости в течение 3 недель и последующем низведении их в мошонку, с рассечением сформированных спаек (Камалов А.А. и др., Особенности регенерации тестикулярной ткани и восстановление фертильности у крыс на фоне ксенотрансплантации обогащенных фетальных клеточных культур при двухстороннем абдоминальном крипторхизме, Урология, №6, 2008 г., с. 7-11). Недостатком данного способа является частое самопроизвольное восстановление половой функции у животного.
Наиболее близким к предлагаемому способу является способ моделирования первичного мужского гипогонадизма, заключающийся в ишемическом воздействии на тестикулы путем временного наложения лигатуры (Куликова П.А. и др., Экспериментальная модель первичного мужского гипогонадизма, Альманах клинической медицины, №31, 2014 г., с. 22-24). Лигатуру накладывали на дистальную часть семенного канатика (funiculus spermaticus) обоих яичек, что приводило к частичной окклюзии яичковой артерии (arteria testicularis). Данную манипуляцию проводили при помощи хирургической иглы и нити. Модель характеризуется стойким снижением гормонпродуцирующей функции, инфертильностью, отсутствием токсического воздействия на организм экспериментальных животных, технической доступностью. Однако данный способ имеет и ряд недостатков - наличие погрешности за счет двустороннего воздействия, существует риск некроза тестикула за счет неконтролируемого давления наложенной лигатурой в дистальной части семенного канатика, одновременная перевязка семявыносящего протока приводит к риску экскреторного бесплодия.
Таким образом, существует потребность в способе моделирования первичного мужского гипогонадизма, лишенном всех вышеуказанных недостатков.
Техническим результатом настоящего изобретения является простота, снижение погрешности в эксперименте, снижение риска некроза тестикула за счет контролируемого воздействия и исключение риска развития экскреторного бесплодия.
Этот технический результат достигается тем, что в предлагаемом способе моделирования первичного мужского гипогонадизма, включающем ишемическое воздействие на тестикулы путем временного наложения лигатуры, лигатуру накладывают в одностороннем порядке с одновременным удалением контралатерального тестикула путем открытой селективной перевязки семенной вены и артерии в проксимальной части семенного канатика с сохранением коллатерального кровотока, при этом накладывают лигатуру с силой деформирующего воздействия 3-4 Ньютон (Н).
Способ осуществляют следующим образом.
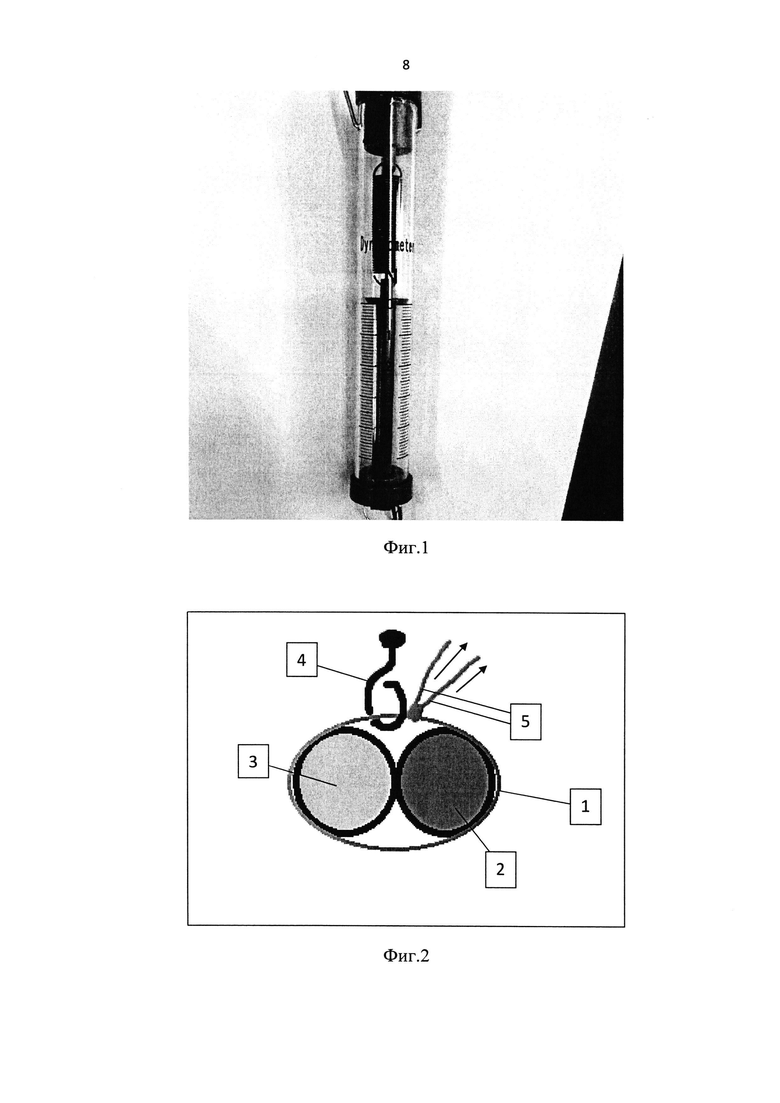
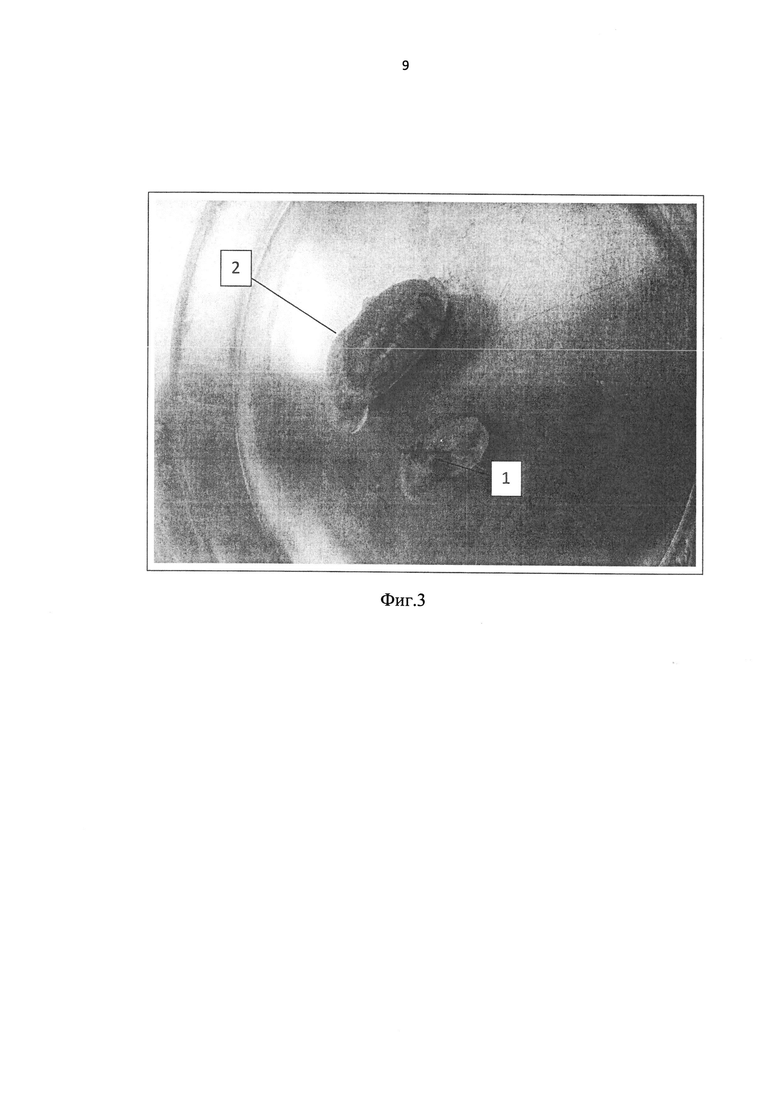
Исследование проводили на крысах-самцах Wistar (n=164), возраст два месяца (соответствует массе 200-220 г). Ишемическое воздействие на тестикулы осуществляли путем временного наложения лигатуры в одностороннем порядке. Лигатуру накладывали путем открытой селективной перевязки семенной вены и артерии в проксимальной части семенного канатика с сохранением коллатерального кровотока. Лигатуру накладывали и затягивали под контролем портативного миниатюрного динамометра (Фиг. 1) таким образом, чтобы сила ее воздействия составила 3-4 Н. Под петлю лигатуры (1), полностью охватывающую семенные вену (2) и артерию (3) без сдавливания, заводили крючок (4) неподвижно зафиксированного динамометра и затягивали концы лигатуры (5) до достижения значения в диапазоне 3-4 Н, после чего фиксировали лигатуру вторым узлом (Фиг. 2). Данную манипуляцию проводили при помощи хирургической иглы и нити (Vicryl Plus, Johnson & Johnson).
Минимальный срок окклюзии, после которого не отмечалось восстановления массы и размеров тестикул на отдаленных сроках после инициации гипогонадизма (два месяца и более), - трое суток.
Одномоментно с наложением лигатуры проводили удаление контрлатерального тестикула. Исследовали массу, линейные размеры семенников и уровень тестостерона через 48, 120, 134, 263 суток после инициации гипогонадизма. Также проводили тест на фертильность, для чего одного самца через 48 суток после инициации гипогонадизма подсаживали к пяти половозрелым самкам (всего исследовали 20 самцов и 100 самок). Оценивали количество покрытых самок.
Измерение тестостерона проводили на иммуноферментном автоматическом анализаторе HTI BioChem Analette. Все хирургические манипуляции выполняли под общей анестезией (Золетил и Ксилазин). Для забора крови и выделения семенников с целью взвешивания осуществляли эвтаназию экспериментальных животных путем введения летальной дозы анестетика - 200 мг/кг массы тела.
Животных содержали в стандартных условиях вивария при температуре 21-23°C. Они получали сбалансированный гранулированный корм, свободный доступ к питьевой воде. Исследования проводили по протоколам, одобренным Комиссией по этике Института теоретической и экспериментальной биофизики РАН. Работа выполнена с соблюдением принципов Хельсинкской декларации о гуманном отношении к животным, принципов гуманности, изложенных в директиве Европейского сообщества (86/609/ЕС), в Приказе Минздрава СССР №755 от 12 августа 1977 г. «О мерах по дальнейшему совершенствованию организационных форм работы с использованием экспериментальных животных». Статистическую обработку данных проводили с помощью программ Statistica 6.0, Microsoft Office Excel 2010.
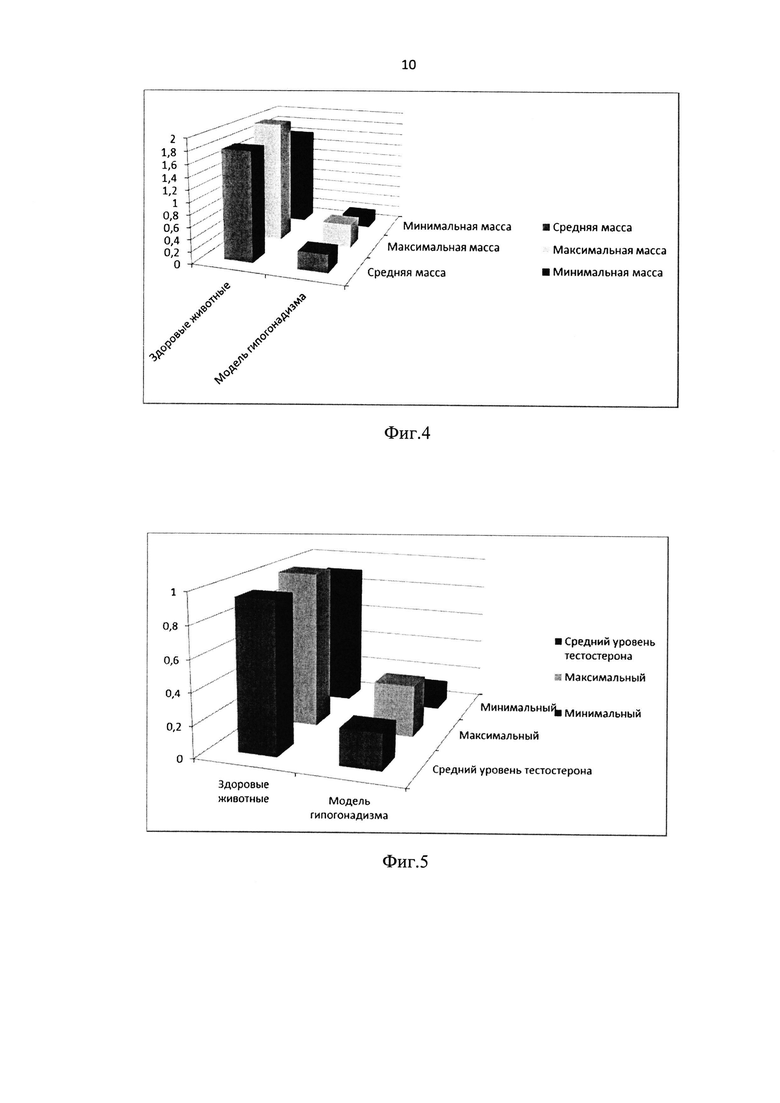
Было показано, что линейные размеры семенников крыс, перенесших инициацию гипогонадизма с помощью предлагаемого способа, в 4-5 раз меньше, чем у интактных самцов того же возраста (контроль), на всех исследуемых сроках - через 48, 120, 134, 263 суток (Фиг. 3, (1) - тестикул животного на 48-е сутки после инициации первичного гипогонадизма по предлагаемому способу, (2) - тестикул контрольного животного на аналогичном сроке) (р<0,05). Измерение массы тестикул показало, что данная масса у экспериментальных животных значимо ниже таковой у группы интактного контроля (р<0,05) (Фиг. 4, измерения массы тестикул через 8 мес. после инициации гипогонадизма). Однако очевидно, что масса семенников при изучении гипогонадизма является косвенным параметром, и основной интерес представляет уровень тестостерона исследуемых животных. Измерение общего тестостерона показало, что уровень этого гормона у экспериментальных животных значимо ниже такового у группы интактного контроля (р<0,05) (Фиг. 5, измерение уровня тестостерона через 8 мес. после инициации гипогонадизма). Тест на фертильность был отрицательным - ни одна из самок, подсаженных к экспериментальным животным, не дала потомства.
Среди существенных признаков, характеризующих способ, отличительными являются:
- наложение лигатуры в одностороннем порядке с одновременным удалением контралатерального тестикула;
- открытая селективная перевязка семенной вены и артерии в проксимальной части семенного канатика с сохранением коллатерального кровотока;
- сила деформирующего воздействия лигатуры составляет 3-4 Н.
Между совокупностью существенных признаков и заявляемым техническим результатом существует причинно-следственная связь. Так, наложение лигатуры в одностороннем порядке с одновременным удалением контралатерального тестикула позволяет повысить точность исследования за счет воздействия на конкретный тестикул. Открытая селективная перевязка семенной вены и артерии в проксимальной части семенного канатика с сохранением коллатерального кровотока и определенный диапазон силы деформирующего воздействия лигатуры позволяют снизить и практически исключить риск некроза тестикула, подвергающегося воздействию, при этом максимально точно смоделировать первичный гипогонадизм у лабораторного животного.
Таким образом, предлагаемый способ прост, доступен, обладает высокой точностью и позволяет избежать развития таких побочных эффектов, как некроз тестикула или развитие экскреторного бесплодия.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения первичного мужского гипогонадизма в эксперименте | 2016 |
|
RU2618197C1 |
| Способ моделирования мужского гипогонадотропного гипогонадизма | 2020 |
|
RU2749477C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ОСЛОЖНЕННЫХ ФОРМ ВАРИКОЦЕЛЕ | 2008 |
|
RU2367363C1 |
| Способ лечения подросткового гипогонадотропного гипогонадизма в эксперименте | 2020 |
|
RU2750713C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ АНАЛЬНОЙ ТРЕЩИНЫ | 2005 |
|
RU2300813C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФЕРТИЛЬНОСТИ ПРИ ВАРИКОЦЕЛЕ | 2010 |
|
RU2419453C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ СТИМУЛЯЦИИ СПЕРМАТОГЕНЕЗА ПРИ ОЛИГОСПЕРМИЧЕСКОМ БЕСПЛОДИИ (СЕКРЕТОРНОЙ ОЛИГО- И АЗООСПЕРМИИ) | 2004 |
|
RU2302641C2 |
| СПОСОБ ЛЕЧЕНИЯ СЕКРЕТОРНЫХ ФОРМ МУЖСКОГО БЕСПЛОДИЯ | 2001 |
|
RU2205040C2 |
| Способ формирования артериовенозной фистулы | 2017 |
|
RU2669995C1 |
| СПОСОБ ПРОТЕКЦИИ И ВОССТАНОВЛЕНИЯ СПЕРМАТОГЕНЕЗА ПРИ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВАХ НА СЕМЕННОМ КАНАТИКЕ, ЯИЧКЕ, ПРИДАТКЕ ЯИЧКА | 2020 |
|
RU2735888C2 |
Изобретение относится к области медицины, а именно к экспериментальной медицине и андрологии. Для моделирования первичного мужского гипогонадизма осуществляют ишемическое воздействие на тестикулы путем временного наложения лигатуры сроком на 3 суток. Лигатуру накладывают с силой деформирующего воздействия 3-4 Н в одностороннем порядке путем открытой селективной перевязки семенной вены и артерии в проксимальной части семенного канатика с сохранением коллатерального кровотока. Одновременно с наложением лигатуры удаляют контралатеральный тестикул. Способ позволяет избежать развития таких побочных эффектов, как некроз тестикула или развитие экскреторного бесплодия, за счет контролируемого деформирующего воздействия и сохранения коллатерального кровотока. 5 ил.
Способ моделирования первичного мужского гипогонадизма, включающий ишемическое воздействие на тестикулы путем временного наложения лигатуры сроком на 3 суток, отличающийся тем, что лигатуру накладывают с силой деформирующего воздействия 3-4 Н в одностороннем порядке путем открытой селективной перевязки семенной вены и артерии в проксимальной части семенного канатика с сохранением коллатерального кровотока, одновременно с наложением лигатуры удаляют контралатеральный тестикул.
| КУЛИКОВА П.А | |||
| и др | |||
| Экспериментальная модель первичного мужского гипогонадизма, Альманах клинической медицины, N31, 2014, с.21-24 | |||
| Способ моделирования мужского гипогонадизма | 1990 |
|
SU1720079A1 |
| Устройство для пополнения недостатка и регулирования температуры охлаждающей воды в конденсационных установках | 1928 |
|
SU17287A1 |
| 0 |
|
SU153897A1 | |
| КУЛИКОВ А.В | |||
| и др | |||
| Новая модель и способ компенсации первичного мужского гипогонадизма | |||
| Материалы симпозиума "Новейшие методы клеточных технологий в медицине", 2-6 сентября 2014 г., Новосибирск, с | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
Авторы
Даты
2017-05-02—Публикация
2016-05-05—Подача