Изобретение относится к области медицины, а именно к экспериментальной медицине, эндокринологии и андрологии, и предназначено для лечения центрального мужского гипогонадизма в эксперименте.
Гипогонадотропный гипогонадизм возникает в результате пониженной секреции гонадотропных гормонов, из-за чего продуцирование андрогенов значительно снижается. Гипогонадотропный гипогонадизм - патологическое состояние, обусловленное снижением выработки гонадотропинов гипофизом и соответственно уменьшением уровня андрогенов в организме. Старт патологии происходит в возрасте спонтанного пубертата и клинически презентируется отсутствием признаков полового созревания, что оказывает существенное негативное влияние на прогноз фертильности и другие расстройства, в том числе соматического характера. Андрогены играют ключевую роль не только в поддержании репродуктивной и сексуальной функций мужского организма. Прослеживается взаимосвязь между снижением уровня андрогенов и рядом патологий - деминерализацией костей, саркопенией, нарушением метаболизма жиров, депрессией, повышенной утомляемостью, угасанием когнитивных функций, а также с повышенным риском сердечно-сосудистых заболеваний и сердечнососудистой смертности (Corona G. et al. Hypogonadism as a risk factor for cardiovascular mortality in men: a meta-analytic study. Eur J Endocrinol. 2011; 165(5):687-701).
На сегодняшний день основным методом лечения мужского гипогонадотропного гипогонадизма в подростковом возрасте остается заместительная терапия в основном эфирами тестостерона (ТС), редко - аналогами гонадотропинов, что не всегда имеет достаточную эффективность. Успешно устраняя некоторые симптомы андрогенодефицита, экзогенные гонадотропины при продолжительном лечении или применении в больших дозах у подростков мужского пола вызывают дегенерацию половых желез, атрофию семенных канальцев (вследствие торможения продукции фолликулостимулирующего гормона (ФСГ) в результате стимуляции продукции андрогенов и эстрогенов, уменьшение количества сперматозоидов в эякуляте. (Jungwirth A., Guidelines on male infertility, Arnhem (The Netherlands), European Association of Urology; 2013).
Известен способ лечения гипогонадизма мужчин путем внутримышечного введения тестостерон-пропионата (ТП), до и через 2-2,5 ч после очередного введения 10, 25, 50 мг ТП определяют процентное содержание иодофильных клеток и мазка со щеки после обработки их в парах иода и лечение повторяют дозой ТП, при которой иодофильность находится в пределах 60-100%.
Известен способ лечения больных с нарушениями мужской половой функции методом трансплантации клеток Лейдига в органы мошонки (пат. РФ №2200010, опубл. 10.03.2003), В известном способе в толщу мошоночного отдела семенного канатика вводят 1,0 мл 2,5%-ной суспензии гидрокортизона ацетата, затем туда же трансплантируют клетки Лейдига.
Известен способ коррекции гипогонадизма у животных при моделировании острого повреждения спинного мозга (пат. РФ №2689114, опубл. 24.05.2019), включающий внутривенное однократное ежедневное введение в курсовой дозе 21,7 мг/кг водного раствора 0,5%-ного препарата D-аспарагина с 3 по 5 сутки от начала моделирования острого повреждения спинного мозга.
Известен также способ лечения первичного мужского гипогонадизма в эксперименте (пат. РФ №2618197, опул. 02.05.2017), включающий трансплантацию аллогенной ткани костного мозга лабораторному животному с первичным мужским гипогонадизмом, смоделированным на основании временной ишемии тестикул, при этом трансплантацию аллогенной ткани костного мозга осуществляют путем инъекции под белочную оболочку тестикула клеточно-гелевого комплекса, состоящего из клеточной массы аллогенного костного мозга и биодеградируемого гетерогенного гидрогеля Сферо®ГЕЛЬ медиум, причем соотношение объема вносимой клеточной массы к объему гидрогеля Сферо®ГЕЛЬ составляет 1:1-1,5:1..
Таким образом, остается актуальным потребность в поиске новых подходов к лечению мужского гипогонадотропного гипогонадизма, нацеленных на восстановление собственной андроген продуцирующей системы, а именно на активацию гипоталамо-гипофизарно-гонадной оси.
Техническим результатом заявляемого изобретения является, высокая эффективность лечения гипогонадизма, основанная на точной и контролируемой экспериментальной модели данной патологии, практически лишенной побочных и искажающих чистоту эксперимента эффектов.
Этот технический результат достигается тем, что в предлагаемом способе лечения подросткового гипогонадотропного гипогонадизма в эксперименте, осуществляют внутримышечное введение 0,1% раствора препарата кисспептина Kiss 10 в дозе 500 мкг в течение 7 дней лабораторным животным 2-х месячного пубертатного возраста с центральным гипогонадотропным гипогонадизмом, смоделированным путем оперативного удаления одной гонады у новорожденных самцов крыс на 1-3 день постнатальной жизни.
В отличие от известных аналогов, в заявляемом способе лечения подросткового гипогонадотропного гипогонадизма в эксперименте, гонадэктомию проводят у новорожденных самцов лабораторных крыс, получая эксериментальную модель данной патологии, практически лишенной побочных и искажающих чистоту эксперимента эффектов. Это объясняется тем, что в последнем триместре беременности за неделю до рождения в организме крыс наблюдается большой пик выброса тестостерона, который продолжается до 5-7 дней после родов. Этот последний период отвечает за дифференциацию, маскулинизацию и дефеминизацию развивающегося мозга Процесс половой дифференциации происходит от генетического пола, который определяет гонадный пол. Последний, в свою очередь, через половые стероиды воздействует на эмбрион, новорожденный плод, подростковый и взрослый организм крыс, и определяет фенотип самцов. Половая дифференциация головного мозга является следствием прямого гормонального воздействия, когда наличие или отсутствие тестостерона во время внутриутробного и неонатального периода будет определять степень развития дифференциации мозга и выраженности фенотипа. Превращение тестостерона в эстрадиол, который происходит в мозге и особенно активен в гипоталамусе, является ключевым событием, ведущим к дифференциации и дефеминизации. Снижение организующего действия андрогенов на головной мозг ведет к нарушению формирования центров регуляции гонадной оси. Группа клеток в гипоталамусе ЦНС программируется так, чтобы воспринимать текущий уровень андрогенов за норму, и не реагировать на низкий уровень тестостерона в пубертатном периоде по фидбэк механизму. Следовательно, воздействие на секреторную функцию яичка в раннем постнатальном возрасте оказывает постоянное влияние на ЦНС, такие эффекты являются организующими, необратимыми и определяющими, а не временными или обратимыми, такими как эффекты активации, вызываемые низким уровнем тестостероном у взрослых крыс.
Таким образом, гонадостат или гормональный статус развивающегося плода после гонадэктомии характеризуется отсутствием гипофизарного ответа на низкий уровень тестостерона увеличением синтеза и выброса гонадотропинов в кровь в постнатальном периоде жизни животных, что приводит к развитию гипогонадотропного варианта гипогонадизма в противоположность гипергонадотропному гипогонадизму в обычных условиях у взрослых самцов крыс.
Валидацию метода гипогонадотропного гипогонадизма проводили измерением в сыворотке крови гормонов ТС, лютеинизирующего гормона (ЛГ) и ФСГ в 2-х месячном возрасте методом ИФА анализа наборами Cloud-Clone Corp.(Китай). На этапах исследования производили забор андрогензависимых тканей на разных сроках полового развития. В эксперимент включали крыс с уровнем гонадотропинов в пределах референсных значений, характерных для интактных самцов аналогичного возраста из контрольной группы или же ниже этих значений. При этом уровень тестостерона у неонатально кастрированных самцов 2-х месячного возраста был значимо ниже по сравнению с интактными самцами крыс контрольной группы аналогичного возраста.
Планирование и проведение всей экспериментальной работы осуществлялось в строгом соответствии с требованиями Минздрава РФ и международными стандартами в области доклинического изучения свойства и безопасности новых фармакологических средств (ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики» (стандарта GLP- Good Laboratory Practic; Guide for the care and use of laboratory animals 8th edition. Copyright 2011 by the National Academy of Sciences. - Washington, D.C. 2010). Это позволило всесторонне исследовать функциональные системы и органы подопытных животных.
Исследование выполнено на базе Института экспериментальной медицины и Центра доклинических и токсикологических исследований (ИДТИ) ФГБУ «Национального медицинского исследовательского центра им. В.А. Алмазова» Минздрава РФ (Санкт-Петербург) и ФГБНУ «Института экспериментальной медицины» РАН (Санкт-Петербург).
Всего в эксперимент было включено 72 особей самцов крыс в возрасте 2 месяца.
Животные содержались в условиях 12/12-часового свето-темнового режима и получали стандартный корм и питьевую воду ad libitum. Животные были разделены случайным образом на 3 группы. Деление экспериментальных животных на группы проводилось на основании проводимого исследования и стадии полового развития (возраст 2 месяца соответствовал пубертатному периоду, возраст 4 месяца - половозрелым особям). Данные представлены в таблице 1.

Кроме оперированных крыс выращивали также интактных самцов крыс для контроля. Животным опытных групп назначали препарат кисспептина Kiss 10 в течение 7 дней. После завершения опыта, запланированные в соответствии с дизайном исследования сроки были взяты материалы андрогензависимых тканей (гонады, мышечная ткань, головной мозг) и кровь). Данные представлены в таблице 2.

На взятых материалах были выполнены следующие методы исследования: 1. Биохимия крови для оценки уровня тестостерона, ЛГ, ФСГ иммуноферментным методом; 2. Морфологический анализ нейронов гипоталамических ядер, участвующих регуляции гонадной оси; 3. Иммуногистохимический анализ динамики изменения рецепции кисспептина и андрогенов в гипоталамических ядрах, а также рецепции андрогенов в гонадах.
Результаты исследования.
Концентрацию лютеинизирующего гормона, фолликулостимулирующего гормона и тестостерона в плазме крови определяли у интактных и оперированных крыс в различные возрастные периоды полового созревания, Полученные данные были проанализированы, сделаны заключения. Абсолютные значения концентрации ЛГ, ФСГ в плазме крови самцов крыс различных групп представлены в таблице 3.


Динамика концентраций гонадотропинов в сыворотке крови у гонадэктомированных крыс существенно отличается по сравнению с интактными животными (таблица 3). Так, уровень ЛГ в сыворотке крови у гонадэктомированных 2-месячных крыс достоверно ниже по сравнению интактными крысами аналогичного возраста. Уровень ФСГ в крови 2-месячных гонадэктомированных крыс не отличается от таковых у интактных самцов крыс.
Таким образом, в результате ранней постнатальной гонадэктомии у самцов крыс в пубертатном возрасте отмечается низкий уровень лютеинизирующего гормона и уровень ФСГ, сравнимый с данными интактных крыс аналогичного возраста.
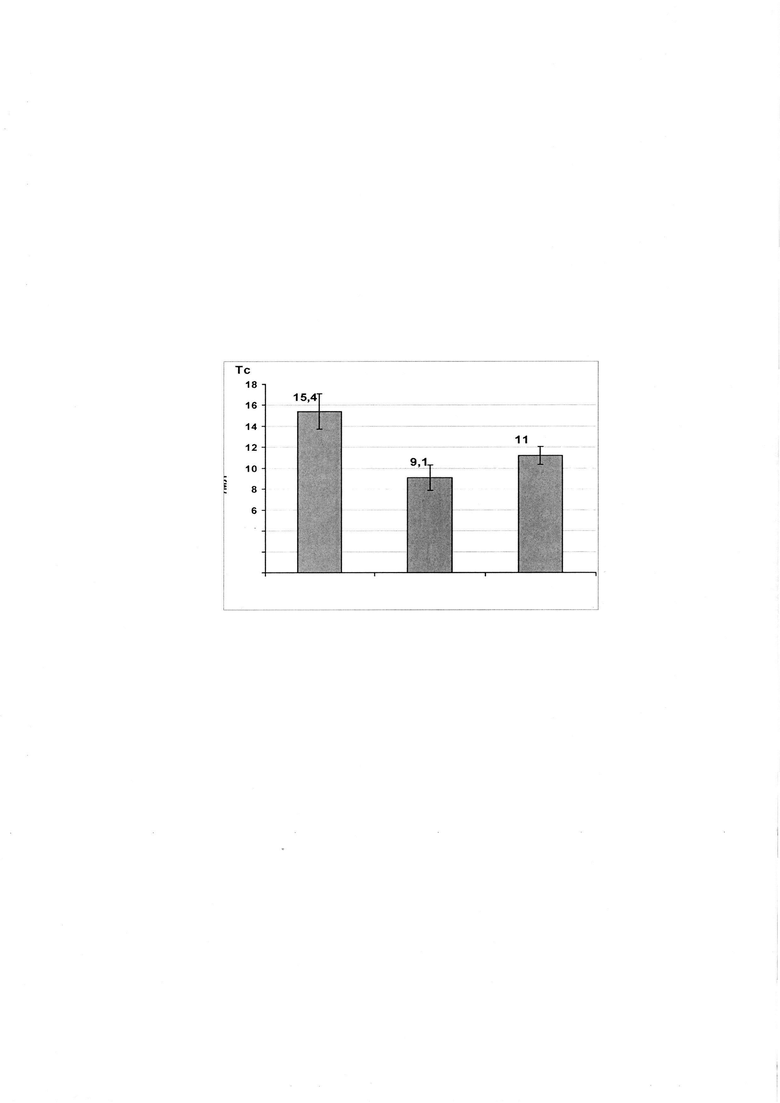
Описываемый гормональный фон соответствует модели гипогонадотропного гипогонадизма, как антитеза гипергонадотропному гипогонадизму. Тогда как, односторонняя гонадэктомия у взрослых самцов крыс по принципу обратной связи приводит к выработке гонадотропинов в гипофизе и росту их значений в периферической крови. То есть, низкое значение концентрации тестостерона у оперированных самцов коррелирует с высоким уровнем ЛГ и ФСГ в сыворотке крови. Данная гормональная ситуация характеризуется как состояние гипергонадотропного гипогонадизма. Уровень тестостерона (нг/мл) в плазме крови самцов крыс 2-х месячного возраста до и после терапии препаратом кисспептина KISS 10 представлен на диаграмме (фиг.).
Анализ полученных данных показал, что терапия экспериментально индуцированного гипогонадотропного гипогонадизма препаратом кисспептина KISS 10 приводит к значимым изменениям гормонального фона у гипогонадных самцов крыс. Так, после терапии кисспептином уровень ЛГ увеличился на 90,5% (р<0,01) по сравнению с контрольной гипогонадной группой без терапии. Так же отмечали достоверное увеличение концентрации ФСГ в плазме крови (18,8%, р<0,05). Рост абсолютных значений гонадотропинов в плазме крови приводит к закономерному увеличению концентрации андрогенов в организме. У опытной группы с терапией кисспептина отмечали рост концентрации тестостерона на 23,1% (р<0,05). К сожалению, специфика экспериментальной модели гипогонадизма, а именно наличие у самцов крыс только одной гонады не позволяет в полной мере оценить эффект проводимой терапии на уровень тестостерона.
Таким образом, в результате ранней пренатальной односторонней гонадэктомии у самцов крыс пубертатного возраста наблюдается низкий уровень гонадотропинов - лютеинизирующего и фолликулостимулирующего гормонов по сравнению с интактными крысами аналогичного возраста. Отсутствие гипофизарного ответа на низкий тестостерона увеличением выброса гонадотропинов в кровь в постнатальном периоде жизни животных, приводит к развитию гипогонадотропного варианта гипогонадизма в противоположность гипергонадотропному гипогонадизму в обычных условиях у взрослых самцов крыс
Назначение препарата кисспептина KISS 10 лабораторным животным пубертатного возраста с гипогонадотропным гипогонадизмом, приводит к восстановлению собственной андроген продуцирующей системы, а именно активацию гипоталамо-гипофизарно-гонадной оси, результатом чего является увеличение выработки ЛГ и ФСГ и повышение синтеза тестостерона в организме.
Полученные в эксперименте результаты могут быть транслированы в клиническую практику и стать основой разработки новых подходов к лечению гипогонадотропного гипогонадизма у юношей-подростков, своевременно моделируя стадии андрогензависимого полового развития и прогноза фертильности.
Заявитель просит рассмотреть представленные материалы заявки «Способ лечения подросткового гипогонадотропного гипогонадизма в эксперименте» на предмет выдачи патента РФ на изобретение.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ моделирования мужского гипогонадотропного гипогонадизма | 2020 |
|
RU2749477C1 |
| Способ прогнозирования репродуктивных нарушений у мальчиков с ожирением | 2019 |
|
RU2706360C1 |
| Способ коррекции гипогонадизма у животных при моделировании острого повреждения спинного мозга | 2017 |
|
RU2689114C2 |
| СПОСОБ СТИМУЛЯЦИИ СПЕРМАТОГЕННОЙ И АНДРОГЕНПРОДУЦИРУЮЩЕЙ ФУНКЦИИ МУЖСКИХ ПОЛОВЫХ ЖЕЛЕЗ | 1991 |
|
RU2040258C1 |
| Способ лечения гипогонадотропного гипогонадизма, назальный спрей как способ введения гонадорелина ацетата при лечении гипогонадотропного гипогонадизма | 2019 |
|
RU2733465C1 |
| Способ лечения гипогонадотронного гипогонадизма, назальный спрей как способ введения пептидного комплекса "MH-GNDR-19-21" при лечении гипогонадотронного гипогонадизма | 2023 |
|
RU2829548C1 |
| БИСАМИДНОЕ ПРОИЗВОДНОЕ ДИКАРБОНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ СРЕДСТВА, СТИМУЛИРУЮЩЕГО РЕГЕНЕРАЦИЮ ТКАНЕЙ И ВОССТАНОВЛЕНИЕ СНИЖЕННЫХ ФУНКЦИЙ ТКАНЕЙ | 2015 |
|
RU2647438C2 |
| БИСАМИДНОЕ ПРОИЗВОДНОЕ ДИКАРБОНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ СРЕДСТВА, СТИМУЛИРУЮЩЕГО РЕГЕНЕРАЦИЮ ТКАНЕЙ И ВОССТАНОВЛЕНИЕ СНИЖЕННЫХ ФУНКЦИЙ ТКАНЕЙ | 2016 |
|
RU2727142C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ХОРИОНИЧЕСКИМ ГОНАДОТРОПИНОМ У МУЖЧИН С ГИПОГОНАДИЗМОМ | 2015 |
|
RU2604681C1 |
| СПОСОБ ЛЕЧЕНИЯ ВТОРИЧНОГО ГИПОГОНАДИЗМА У МУЖЧИН | 1995 |
|
RU2117446C1 |
Изобретение относится к области медицины, а именно к экспериментальной медицине, эндокринологии и андрологии. Способ лечения подросткового гипогонадотропного гипогонадизма в эксперименте включает внутримышечное введение 0,1%-ного раствора препарата кисспептина Kiss 10 в дозе 500 мкг в течение 7 дней лабораторным животным 2-месячного пубертатного возраста с гипогонадотропным гипогонадизмом, смоделированным путем оперативного удаления одной гонады у новорожденных самцов крыс на 1-3 день постнатальной жизни. Изобретение обеспечивает высокую эффективность лечения гипогонадизма, основанную на точной и контролируемой экспериментальной модели данной патологии. 3 табл., 1 ил.
Способ лечения подросткового гипогонадотропного гипогонадизма в эксперименте, включающий внутримышечное введение 0,1%-ного раствора препарата кисспептина Kiss 10 в дозе 500 мкг в течение 7 дней лабораторным животным 2-месячного пубертатного возраста с гипогонадотропным гипогонадизмом, смоделированным путем оперативного удаления одной гонады у новорожденных самцов крыс на 1-3 день постнатальной жизни.
| Способ лечения первичного мужского гипогонадизма в эксперименте | 2016 |
|
RU2618197C1 |
| НИКИТИНА И.Л | |||
| Кисспептиновые механизмы регуляции полового развития мальчиков: потенциал диагностики и терапии при задержке старта пубертата и гипогонадотропном гипогонадизме / Проблемы эндокринологии, 2018, т | |||
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЧИСТОГО ГЛИНОЗЕМА И ЕГО СОЛЕЙ ИЗ СИЛИКАТОВ ГЛИНОЗЕМА, ПРОСТЫХ ГЛИН И. Т.П. | 1915 |
|
SU280A1 |
| THOMPSON E.L | |||
| et al | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2021-07-01—Публикация
2020-10-20—Подача