Изобретение относится к медицине, а именно к эндокринологии и экспериментальной биологии и предназначено для моделирования мужского гипогонадотропного гипогонадизма.
Известны способы моделирования первичного мужского гипогонадизма, например, «Способ моделирования мужского гипогонадизма» (авт. свид. СССР №1720079, опубл. 15.03.1992 г.), в котором животному с третьего дня постнатальной жизни в течение 3 дней ежедневно вводят пиридоксин гидрохлорид в дозе 10 мг/кг, а в.половозрелом возрасте осуществляют гонадэктомию.
Однако такой способ позволяет моделировать только тестостеронрезистентные формы гипогонадизма.
Известен «Способ моделирования гипогонадизма, вызванного метаболическими нарушениями» (пат. РФ №2611936, опубл. 01.03.2017 г.) в котором мышам-самцам линии C57Bl/6 через сутки после рождения вводят стрептозотоцин однократно, подкожно в дозе 200 мг/кг. Затем с 28-х суток после рождения переводят животных на рацион, обогащенный насыщенными жирами. Поддерживают этот рацион до достижения гипергликемии, гиперинсулинемии, нарушений глюкозотолерантности, а также угнетения сперматогенеза и нарушения фертильности. Известный способ обеспечивает создание модели гипогонадизма, вызванного метаболическими нарушениями.
Известен также «Способ моделирования первичного мужского гипогонадизма» (пат. РФ №2618196, опубл. 02.05.2017 г.), в котором осуществляют ишемическое воздействие на тестикулы путем временного наложения лигатуры сроком на 3 суток. Лигатуру накладывают с силой деформирующего воздействия 3-4 Н в одностороннем порядке путем открытой селективной перевязки семенной вены и артерии в проксимальной части семенного канатика с сохранением коллатерального кровотока. Одновременно с наложением лигатуры удаляют контралатеральный тестикул. Известный способ позволяет избежать развития таких побочных эффектов, как некроз тестикула или развитие экскреторного бесплодия, за счет контролируемого деформирующего воздействия и сохранения коллатерального кровотока.
Однако общим недостатком указанных известных способов, является то, что выполнение гонадэктомии происходит в более поздние сроки роста и развития животных или взрослых особей. Это объясняется тем, что в последнем триместре беременности за неделю до рождения в организме крыс наблюдается большой пик выброса тестостерона, который продолжается до 5-7 дней после родов. Этот последний период отвечает за дифференциацию, маскулинизацию и дефеминизацию развивающегося мозга. Процесс половой дифференциации происходит от генетического пола, который определяет гонадный пол. Последний, в свою очередь, через половые стероиды воздействует на эмбрион, новорожденный плод, подростковый и взрослый организм крыс, и определяет фенотип самцов. Половая дифференциация головного мозга является следствием прямого гормонального воздействия, когда наличие или отсутствие тестостерона во время внутриутробного и неонатального периода будет определять степень развития дифференциации мозга и выраженности фенотипа. Превращение тестостерона в эстрадиол, который происходит в мозге и особенно активен в гипоталамусе, является ключевым событием, ведущим к дифференциации и дефеминизации. Снижение организующего действия андрогенов на головной мозг ведет к нарушению формирования центров регуляции гонадной оси Группа клеток в гипроталамусе центральной нервной системы (ЦНС) программируется так, чтобы воспринимать текущий уровень андрогенов за норму, и не реагировать на низкий уровень тестостерона в пубертатном периоде по фидбэк механизму. Следовательно, воздействие на секреторную функцию тестикулы в раннем постнатальном возрасте оказывает постоянное влияние на ЦНС, такие эффекты являются организационными, необратимыми и определяющими, а не временными или обратимыми, такими как эффекты активации, вызываемые низким уровнем тестостероном у взрослых крыс.
Таким образом,. гонадостат или гормональный статус развивающегося плода после гонадэктомии характеризуется отсутствием гипофизарного ответа на низкий уровень тетстостерона увеличением синтеза и выброса гонадотропинов в кровь в нос шатал ном периоде жизни животных, что приводит к развитию гипогонадотропного варианта гипогонадизма в противоположность гипергонадотропому гипогонадизму в обычных условиях у взрослых самцов крыс. (1-11)
Целью изобретения является моделирование мужского гипогонадотропного гипогонадизма.
Технический результат изобретения заключается в получении модели мужского гипогонадизма гипогонадотропной формы.
Технический результат достигается тем, что у новорожденных самцов крыс на 1-3 день постнатальной жизни под общей ингаляционной анестезией изофлураном в асептических условиях проводят лапаротомию с односторонней гонадэктомией путем извлечения тестикула из внутрибрюшной полости перевязки и отсечения семенного канатика с последующим удалением гонады.
Применение заявленного способа путем проведения односторонней гонадэктомии в ранний постнатаольный период жизни позволяет, в отличие от аналогов моделировать гипогонадотропную форму гипогонадизма у самцов крыс.
Валидацию способа моделирования мужского гипогонадотропного гипогонадизма проводили измерением в сыворотке крови гормонов Тс, ЛГ и ФСГ в 2- и 4-месячном возрасте методом ИФА анализа наборами Cloud-Clone Corp. (Китай). На этапах исследования производили забор андрогензависимых тканей на разных сроках полового развития. Уровень гонадотропинов у всех крыс из опытной группы в эксперименте были в пределах референсных значений, характерных для интактных самцов аналогичного возраста из контрольной группы или же ниже этих значений. При этом уровень тестостерона у неонатально кастрированных самцов 2-х месячного возраста был значимо ниже по сравнению с интактными самцами крыс контрольной группы аналогичного возраста.
Планирование и проведение всей экспериментальной работы осуществлялось в строгом соответствии с требованиями Минздрава РФ и международными стандартами в области доклинического изучения свойства и безопасности новых фармакологических средств (ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики» (стандарта GLP - Good Laboratory Practic; Guide for the care and use of laboratory animals 8th edition. Copyright 2011 by the National Academy of Sciences. - Washington, D.C. 2010). Это позволило всесторонне исследовать функциональные системы и органы подопытных животных.
Исследование выполнено на базе института экспериментальной медицины ФГБУ «Национального Медицинского Исследовательского Центра им. В.А. Алмазова» Минздрава РФ (Санкт-Петербург) и ФГБНУ «Института экспериментальной медицины» РАН (Санкт-Петербург).
Исследование проводилось на лабораторных крысах линии Wistar мужского пола 1-3 дня рождения, 2- и 4-месячного возраста. Создание модели гипогонадных самцов крыс предусматривало закупку беременных самок в последней декаде гестации. Новорожденных потомств обоих полов от этих самок крыс группировали по половому признаку и по дате рождения. Новорожденные детеныши-самцы были включены в дальнейшее исследование. Всего было включено 96 особей крыс в возрасте 1-3 дней.
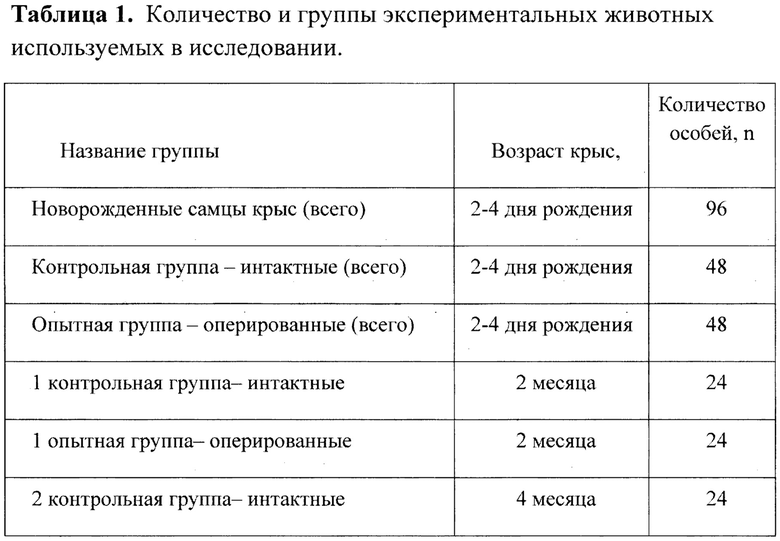
Животные содержались в условиях 12/12-часового свето-темнового режима и получали стандартный корм и питьевую воду ad libitum. Животные были разделены случайным образом на 4 группы. Деление экспериментальных животных на группы проводилось на основании проводимого исследования и стадии полового развития (возраст 2 месяца соответствовал пубертатному периоду, возраст 4 месяца - половозрелым особям). Данные представлены в таблице 1.

Проводимые исследования подтверждаются иллюстрациями, где:
на фиг. 1 - представлены этапы проведения односторонней гонадэктомии: поз. 1 - фиксация липкой лентой к термостатируемому столу; поз. 2 - разрез брюшины, выделение тестикулы; поз. 3 - перевязка семенного канатика и удаление гонады; поз. 4 - наложение шва и медицинского клея;
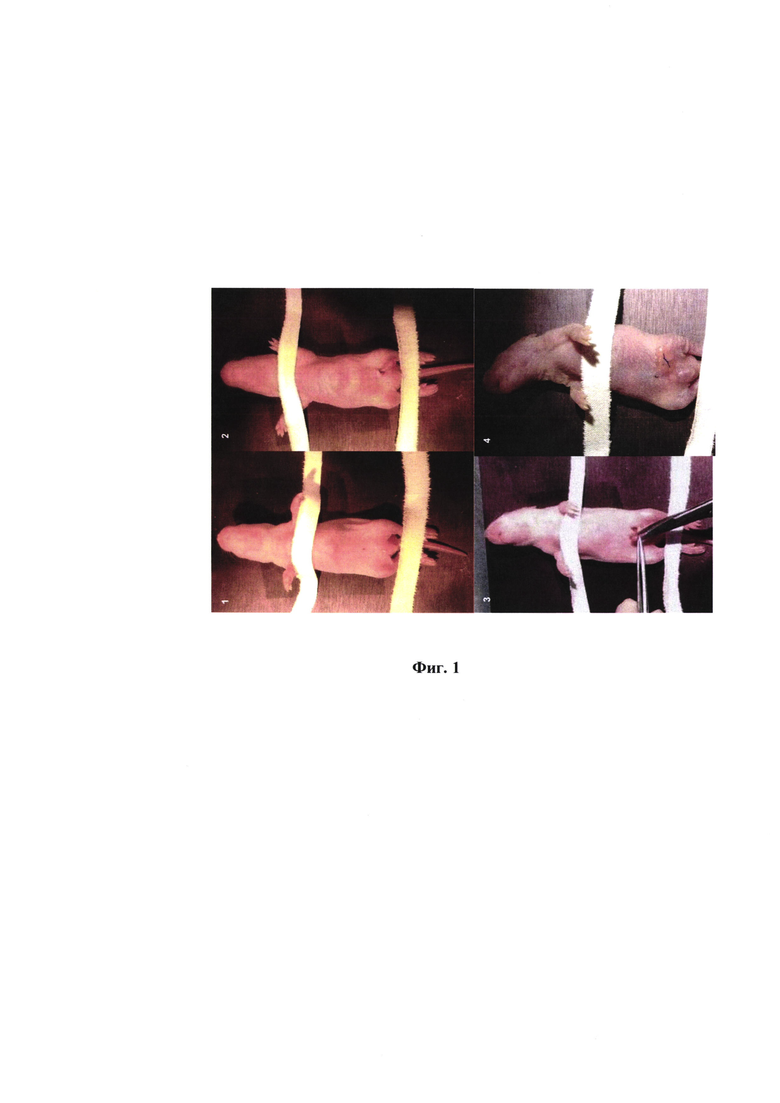
на фиг. 2 - представлен график регрессионного анализа абсолютных значений концентраций тестостерона в плазме крови самцов крыс различных групп (нг/мл);
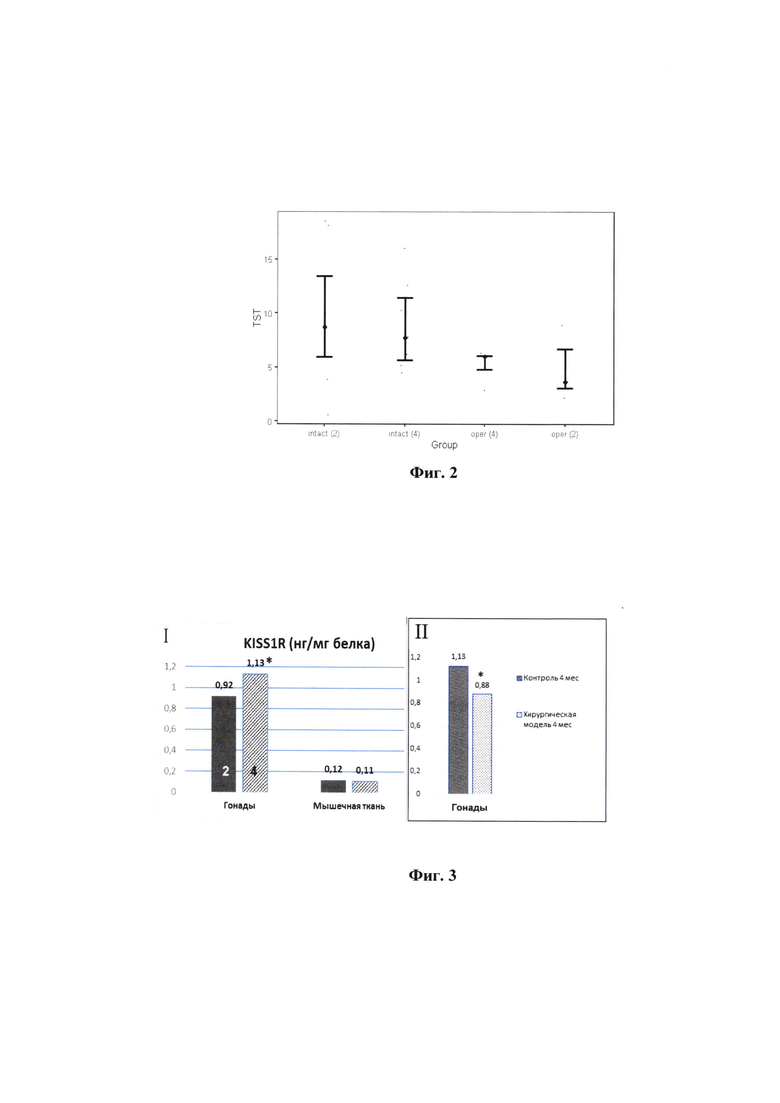
на фиг. 3 - сравнительный анализ концентрации KISS 1R в гонадах и мышечной ткани различных возрастных групп (2 и 4 месяца) здоровых самцов крыс (I) и при гипогонадотропном гипогонадизме в возрасте 4 месяца (II). Концентрация KISS1R в нг/мгбелка; * - р<0,01 достоверность между группами сравнения;
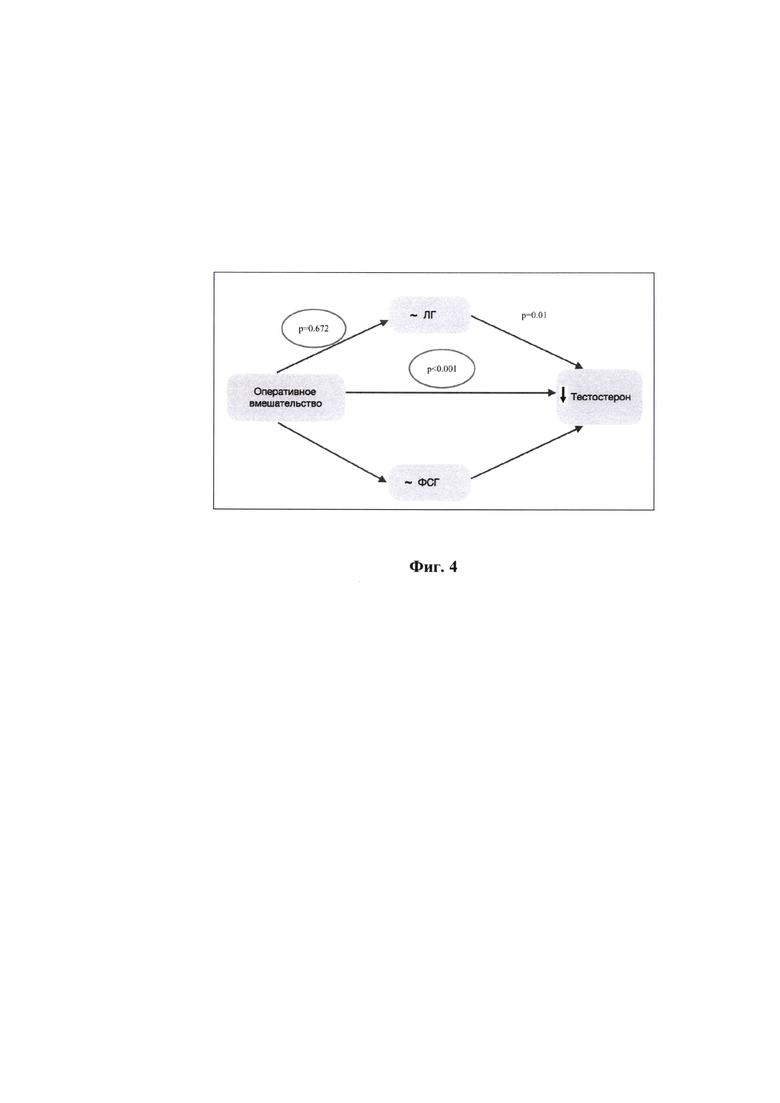
на фиг. 4 - структурное моделирование статистически значимых ассоциаций между исследуемыми показателями (факт операции, уровень тестостерона, уровень гонадотропных гормонов) с точки зрения как прямого, так и опосредованного (медиаторного) эффекта.
Выполнение хирургического метода кастрации
Новорожденные самцы крыс были подвергнуты односторонней гонадэктомии на первый-третий дни постнатальной жизни (фиг. 1). Все животные подвергались общей анестезии путем вдыхания изофлурана. Ингаляционную анестезию проводили в следующем режиме: вначале эксперимента подача кислородно-воздушной смеси с 5% содержанием изофлурана, далее в течение эксперимента подача наркоза в поддерживающем режиме. Подтверждение анестезии устанавливали по отсутствию рефлекса на раздражители.
Этапы операции
С помощью полоски лейкопластыря новорожденных крыс иммобилизировали в положении лежа на спине на термостатируемом столе под увеличительным стеклом с увеличением в 2-2,5 раза (поз. 1 фиг. 1). Местная антисептика проводилась с раствором хлоргексидина. На операционном поле, на брюшине малого таза с левой стороны делали разрез приблизительно 0,3 см. После разреза мышц и брюшины тестикула была идентифицирована, выделена и лигирована с нитью кетгута 3,0 и разрезана (поз. 2-3 фиг. 1). Разрез брюшины ушивали кетгутом с наложением одного шва, после которой на шов накладывали каплю медицинского клея (поз. 4 фиг. 1). Крыс держали в руке (в тепле) до полного отхода от анестезии, крыс возвращали в клетки к матери. Затем их содержали там до 21 дня жизни, после которого они были отделены от своей матери и помещены в клетки с пятью животными.
На следующем этапе согласно дизайну исследования, самцов крыс выращивали до достижения пубертатного (2 месяца) и половозрелого возраста (4 месяца). Из этих крыс сформировывали опытные группы (таблица 1). Кроме оперированных крыс выращивали также интактных самцов крыс для контроля. Все крысы были одного помета.
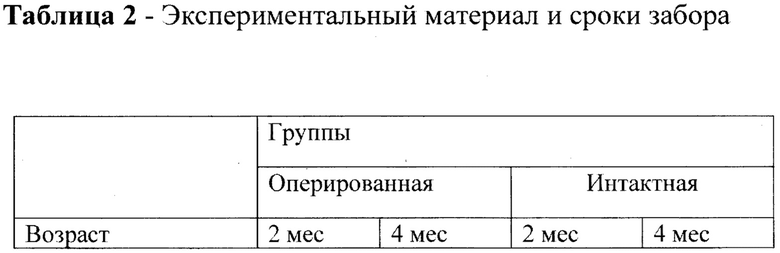
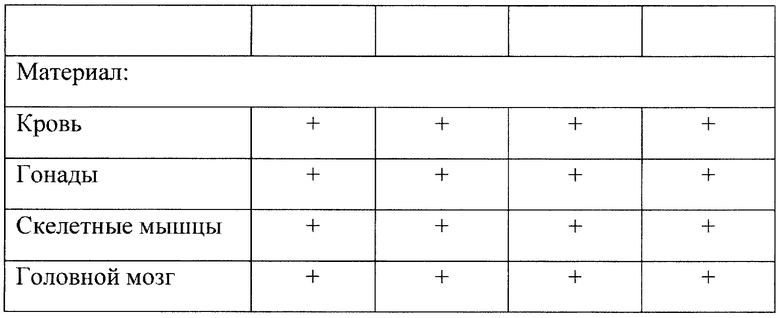
В запланированные в соответствии с дизайном исследования сроки были взяты материалы андрогензависимых тканей (гонады, мышечная ткань, головной мозг) и кровь на разных сроках полового развития (2 и 4 месяца). Данные представлены в таблице 2.
На взятых материалах были выполнены следующие методы исследования:
1. Биохимия крови для оценки уровня тестостерона, ЛГ, ФСГ иммуноферментным методом;
2. Морфологический анализ нейронов гипоталамических ядер, участвующих регуляции гонадной оси;
3. Иммуногистохимический анализ динамики изменения рецепции кисспептина и андрогенов в гипоталамических ядрах, а также рецепции андрогенов в гонадах.
Результаты исследования
Концентрацию лютеинизирующего гормона, фолликулостимулирующего гормона и тестостерона в плазме крови определяли у интактных и оперированных крыс в различные возрастные периоды полового созревания, Полученные данные были проанализированы, сделаны заключения. Абсолютные значения концентрации ЛГ, ФСГ в плазме крови самцов крыс различных групп представлены в таблице 3.
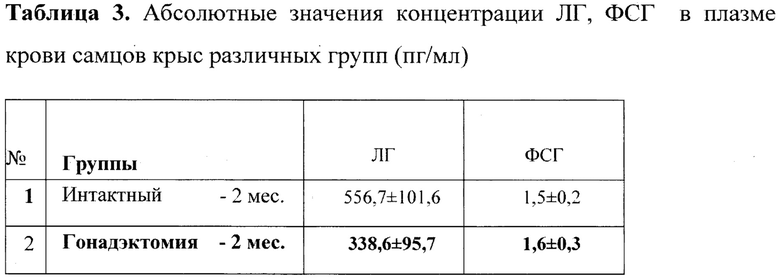

Динамика концентраций гонадотропинов в сыворотке крови эмбриона существенно отличается у гондэктомированных крыс по сравнению с интактными животными (таблица 3). Так, уровень ЛГ в сыворотке крови у гонадэктомированных 2-месячных крыс достоверно ниже по сравнению интактными крысам аналогичного возраста. Существенная разница в уровне ЛГ сохраняется также у 4-месячных крыс. Уровень ФСГ в крови 2-месячных гонадэктомированных крыс не отличается от таковых по сравнению с интактными самцами, но у половозрелых гонадэктомированных самцов 4-месячного возраста отмечается достоверное и значительное снижение уровня фолликулостимулирующего гормона по сравнению интактными крысами аналогичного возраста. Таким образом, в результате ранней постнатальной гонадэктомии у самцов крыс в течение пубертатного и половозрелого возрастов отмечается низкий уровень гонадотропинов - лютеинизирующего и фолликулостимулирующего гормонов по сравнению с интактными крысами аналогичного возраста.
Низкие значения концентраций ЛГ и ФСГ у оперированных плодов мужского пола коррелирует с низкой концентрацией тестостерона у этих же самцов крыс, как результат гонадэктомии (фиг. 2). В отличие от данной модели, у взрослых самцов односторонняя гонадэктомия по принципу обратной связи приводит к выработке гонадотропинов в гипофизе и росту их значений в периферической крови. То есть, низкое значение концентрации тестостерона у оперированных самцов коррелирует с высоким уровнем ЛГ и ФСГ в сыворотке крови. Данная гормональная ситуация характеризуется как состояние гипергонадотропного гипогонадизма.
Список литературы
1. Мыслицкий В.Ф. Половая дифференциация некоторых структур лимбической системы головного мозга крыс в онтогенезе, Автореферат диссертации на соискание ученой степени доктора биологических наук, Москва, 1990.
2. Никитина И.Л., Байрамов А.А. Формирование пола и репродуктивной системы человека - прошлое, настоящее, будущее, лечение и профилактика, 2014, №2 (10), с. 76-85.
3. Резников А.Г. Функциональная тератология нейроэндокринной системы: этиология, патогенез, профилактика // Здоров'я 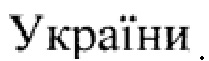 - 2007. - №22/1. - С. 19-21.
- 2007. - №22/1. - С. 19-21.
4. Шишкина И.В. Рецепторы к половым гормонам в гипоталамусе и их роль в половой дифференцировке мозга у крыс. Автореферат диссертации на соискание ученой степени кандидат биологических наук. Москва, 1984.
5. Chowen JA, Argente J, Gonzalez-Parra S, Garcia-Segura LM. Differential effects of the neonatal and adult sex steroid environments on the organization and activation of hypothalamic growth hormone - releasing hormone and somatostatin neurons. Endocrinology. 1993; 133(6): 2792-802.
6. Corbier P, Roffi J, Rhoda J. Female sexual behavior in male rats: effect of hour of castration at birth. Physiol Behav. 1983; 30(4): 613-6.
7. Dorner G, Staudt J. Structural changes in the preoptic anterior hypothalamic area of the male rat, following neonatal castration and androgen substitution. Neuroendocrinology. 1968; 3(3): 136-40
8. Handa R.J., Corbier P., Shryne J.E., Schoonmaker J.N., Gorski R.A. Differential effects of the perinatal steroid environment on three sexually dimorphic parameters of the rat brain. Biol. Repord. 1985; 32(4): 855-64.
9. Madeira MD, Lieberman AR. Sexual dimorphism in the mammalian limbic system. Prog Neurobiol. 1995; 45(4): 275-333
10. McEwen BS. Protective and damaging effects of stress mediators: central role of the brain. Prog Brain Res. 2000; 122: 25-34.
11. Patchev VK, Hayashi S, Orikasa C, Almeida OF. Implications of estrogen-dependent brain organization for gender differences in hypothalamo-pituitary-adrenal regulation. Faseb J. 1995; 9(5): 419-23.
Стандарты GLP:
1. Межгосударственный стандарт ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики» (GLP).
2 Директива 2010/63/EU Европейского Парламента и Совета Европейского Союза по охране животных, используемых в научных целях. СПб., 2012, 48 с.
4. Guide for the care and use of laboratory animals 8th edition. Copyright 2011 by the National Academy of Sciences. - Washington, D.C. 2010.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения подросткового гипогонадотропного гипогонадизма в эксперименте | 2020 |
|
RU2750713C1 |
| Способ моделирования первичного мужского гипогонадизма | 2016 |
|
RU2618196C1 |
| Способ лечения первичного мужского гипогонадизма в эксперименте | 2016 |
|
RU2618197C1 |
| Способ лечения гипогонадотропного гипогонадизма, назальный спрей как способ введения гонадорелина ацетата при лечении гипогонадотропного гипогонадизма | 2019 |
|
RU2733465C1 |
| Способ коррекции гипогонадизма у животных при моделировании острого повреждения спинного мозга | 2017 |
|
RU2689114C2 |
| Способ лечения гипогонадотронного гипогонадизма, назальный спрей как способ введения пептидного комплекса "MH-GNDR-19-21" при лечении гипогонадотронного гипогонадизма | 2023 |
|
RU2829548C1 |
| ПЕПТИДНОЕ СОЕДИНЕНИЕ, СТИМУЛИРУЮЩЕЕ ФУНКЦИЮ ПОЛОВОЙ СИСТЕМЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2006 |
|
RU2324703C1 |
| СПОСОБ ПРЕНАТАЛЬНОГО ПРОГНОЗИРОВАНИЯ ПАТОЛОГИЧЕСКОГО ТЕЧЕНИЯ МИНИ-ПУБЕРТАТА У МАЛЬЧИКОВ | 2013 |
|
RU2526268C1 |
| Способ прогнозирования репродуктивных нарушений у мальчиков с ожирением | 2019 |
|
RU2706360C1 |
| БИСАМИДНОЕ ПРОИЗВОДНОЕ ДИКАРБОНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ СРЕДСТВА, СТИМУЛИРУЮЩЕГО РЕГЕНЕРАЦИЮ ТКАНЕЙ И ВОССТАНОВЛЕНИЕ СНИЖЕННЫХ ФУНКЦИЙ ТКАНЕЙ | 2016 |
|
RU2727142C2 |
Изобретение относится к медицине, а именно к эндокринологии и экспериментальной биологии, и может быть использовано для моделирования мужского гипогонадотропного гипогонадизма. У новорожденных самцов крыс выполняют одностороннюю гонадэктомию путем извлечения тестикулы из внутрибрюшной полости, перевязки, отсечения семенного канатика с последующим удалением гонады. Одностороннюю гонадэктомию выполняют не позднее 4-го дня постнатальной жизни. Способ обеспечивает возможность получения модели мужского гипогонадизма гипогонадотропной формы за счет проведения односторонней гонадэктомии в ранний постнатальный период жизни, что позволяет в отличие от гипергонадотропной формы гипогонадизма аналогов моделировать гипогонадотропную форму гипогонадизма у самцов крыс. 3 табл., 4 ил.
Способ моделирования мужского гипогонадотропного гипогонадизма, включающий выполнение односторонней гонадэктомии у новорожденных самцов крыс путем извлечения тестикулы из внутрибрюшной полости, перевязки, отсечения семенного канатика с последующим удалением гонады, отличающийся тем, что одностороннюю гонадэктомию выполняют не позднее 4-го дня постнатальной жизни.
| ЮХЛИНА Ю.В | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Автореф | |||
| диссер | |||
| С-Пб, 2019, стр.1-22 | |||
| ДРОБЛЕНКОВ А.В | |||
| и др | |||
| Тестостерон-зависимые изменения нейронов аркуатного ядра гипоталамуса и их обратимость при моделировании мужского | |||
Авторы
Даты
2021-06-11—Публикация
2020-04-03—Подача