Изобретение относится к области медицины и касается создания средств растительного происхождения для лечения хламидиоза.
Хронический мочеполовой хламидиоз, кроме эпидемиологической актуальности, считается своеобразным маркером вторичной иммунной недостаточности, проявлением которой является достаточно частое развитие у таких больных других заболеваний вирусной и бактериальной природы. Для 95% пациентов один курс антибиотиков будет достаточен для полного излечения. При наличии осложнений, как правило только у женщин, может потребоваться лечение, дополняющее антибиотики (иммунотерапия, общеукрепляющие препараты, физиотерапия и т.д.), но эта терапия носит ситуационный характер. Длительно нелеченый хламидиоз с течением времени приводит к возникновению различного типа осложнений, обусловленных распространением микробов на другие органы и ткани (Якубович А.И., Корепанов А.Р., 2007). Автором также отмечено, что с каждым годом возрастает частота резистентности инфекции к проводимой терапии.
Известны попытки повысить результативность лечения за счет препаратов растительного происхождения. Например, назначают травы для уменьшения инфекционно-воспалительного процесса (Корсун В.Ф., Корсун Е.В., Суворова К.Н., 2004). Применяют фитотерапию для устранения микробиоценоза (Маричереда В.Г., Перминова Т.И., 2005). Был создан оригинальный травяной сбор для индукции интерферона (Погорельская Л.В., 2001).
Но ни одно из известных средств, при использовании фитопрепаратов, не воздействовало на внутриклеточное паразитирование хламидий.
Задачей изобретения является повышение эффективности терапии за счет этиологического и патогенетического лечения путем расширения ассортимента лекарственных средств растительного происхождения для лечения бактериально-вирусных хронических инфекций, а именно хламидиоза.
Для достижения поставленной задачи предложено средство, содержащее порошки хитозана пищевого, травы кипрея узколистного, душицы, зверобоя, клубни топинамбура, корни лопуха, цветки календулы, зизифоры, листья мяты, шалфея и коры осины в соотношении 1:2:1:1:3:2:1:2:1:2:3.
Заявленное средство условно названо «Ахлакор».
Изобретение иллюстрируется следующим примером
Пример 1. Наблюдалось 18 больных (больше мужчин) трудоспособного возраста с хроническим урогенитальным хламидиозом. Длительность заболевания от 3 месяцев до 7 лет, ранее лечившихся антибиотиками. Диагноз был подтвержден клинически и исследованием ПЦР. После окончания курса лечения заявляемым средством по 2 таблетки 3 раза в день в течение 3-4 недель, делают перерыв в течение 7-10 дней, а затем курс лечения обязательно повторяют. Подобных курсов следует проводить 2-3. Проведенные клинические наблюдения 18 больных с хроническим течением урогенитального хламидиоза приводили к значительному снижению проявлений заболевания. Не отмечено побочных явлений от изучаемого препарата.
На базе лаборатории хламидиоза Белорусского НИЦ эпидемиологии и микробиологии МЗ РБ изучена гемагглютинирующая активность (Корсун В.Ф., Лахтин В.М., Корсун Е.В., Мицконас А., 2007) растительного средства «Ахлакор», содержащего хитозан пищевой, траву кипрея узколистного, душицы, зверобоя, клубни топинамбура, корни лопуха, цветки календулы, зизифоры, листья мяты, шалфея, кору осины для последующего создания препарата (парафармацевтика) для вспомогательного лечения хламидиоза.
Материалы и методы исследований
Выделение лектинов из препарата «Ахлакор» проводили в следующей последовательности: 3 таблетки весом по 0,5 граммов тщательно растирали в фарфоровой ступке со стеклянным песком в ацетатном буфере рН 3,4 с 0,3 М NaCl. Гомогенат помещали в центрифужные стаканы, экстракцию проводили на холоду в течение 12 часов при периодическом перемешивании. Супернатант, содержащий суммарный экстракт лектинов, отделяли центрифугированием при 5 тыс.об/мин. При выделении лектиновых белков важен рН экстрагента. Он не должен превышать рН 4, т.к. при более высоких и тем более нейтральных рН выход лектинов очень низкий. В наших опытах белки, выделенные 0,14-0,6М NaCl без ацетатного буфера, проявляли очень низкую агглютинирующую активность, хотя концентрация белка была весьма высокой. Вероятно, в этих условиях выделяются альбумины, глобулины, ферментативные водо- и солерастворимые белки нелектиновой природы. Выделение препаратов лектинов из экстрактов осуществляли осаждением их холодным абсолютным этанолом. Осадок перерастворяли в фосфатном буфере рН 4,8 с 0,03М NaCl. Реакцию гемагглютинации ставили на иммунологических планшетах Такачи по общепринятой методике М.Д. Луцика и др.[7]. В работе мы использовали эритроциты крови различных типов животных и птиц: кролика, быка, барана, голубя, гуся, петуха и все группы крови человека системы АВО. Для контрастирования реакции агглютинации использовали трипсинизированные в 1% растворе трипсина эритроциты. Наиболее удачным тест-объектом в наших экспериментах оказались петушиные эритроциты. Титр агглютинации здесь составил 1:256. Из эритроцитов крови человека наибольшую активность с лектинами Ахлакора проявили эритроциты группы 0(I). Дальнейшую очистку лектиновых экстрактов проводили, пропуская через колонку Sephadex G-25, элюируя их раствором 0,01 н НСl рН 4,0. Элюенты с сефадекса G-25 концентрировали упариванием и наносили на колонку с сефадексом G-75 для эксклюзионного фракционирования лектинов. После гель-фильтрации были выделены 3 хроматографических фракции белков, отличающиеся по молекулярной массе и гемагглютинирующей активности.
Первый пик элюировался с 12-40 пробирки, объем его составлял 60 мл. Второй пик с 41-70 пробирки, объем его составлял 93 мл. Третий пик элюировался 71-92 пробирки объем его составил 63 мл. Пики осаждали холодным абсолютным этанолом, перерастворяли 0,14 М NaCl и ставили реакции гемагглютинации.
Результаты исследований
Реакции гемагглютинации с хроматографическими пиками позволили выявить, что максимальную активность проявили лектины второго пика, где титр агглютинации составил 1:512 единиц. Первый и третий пики осаждали с титром 1:256. Интересно отметить, что лектины пика номер 2 проявляют большее сродство к эритроцитам крови группы АВ (IV), титр активности здесь составляет 1:1024 единиц. Интенсивность реакции лектинов прямо пропорциональна количеству связываемого белка и зависит от сродства лектинов к рецепторам локализованных на поверхности эритроцитарных мембран. Различная активность в связывании лектинами лекарственных трав с эритроцитами определенных групп крови свидетельствует, что организм человека нуждается в лектинах определенной специфичности, подобно тому, что скорость протекания обменных реакции, генетические факторы, патологические процессы влияют и меняют соотносительную потребность организма в биологически активных соединениях.
Таким образом, была доказано, что заявляемая фитокомпозиция содержит фитолектины, проявляющие выраженную гемагглютинирующую активность. Вторая часть подтверждения ее положительного эффекта при хламидийной инфекции касалась изучения противохламидийной активности препарата «Ахлакор» в модельной системе in vitro.
Материалы и методы
В работе использованы штаммы Национальной коллекции вирусов и бактерий Республики Беларусь: штаммы Chlamydia trachomatis СТ-866, СТ-867, СТ-869 (депоненты В-02/2012, В-03/2012, В-04/2012 от 22.10.2012). Штамм Chlamydia trachomatis СТ-866 (титр 5,5 lg), СТ-867 (титр 6,0 lg), СТ-869 (титр 6,5 lg) пассировали в перевиваемой культуре клеток McCoy. Модельной системой являлись интактная и инфицированная хламидиями перевиваемая культура клеток McCoy. Для исследования противохламидийной активности был отобран препарат «Ахлакор» (серия №021112013) таблетки 0,5 г производства ООО «В-МИН», г. Сергиев Посад, Московская область, срок годности до 31.05.2015. Таблетку препарата предварительно растворяли в стерильной дистиллированной воде и далее делали десятикратные разведения 1:10, 1:100, 1:1000 в специальной питательной среде для изоляции хламидий. Заражение 2-суточной культуры клеток McCoy хламидиями проводили по стандартной методике. После контакта возбудителя с клетками культуральную жидкость удаляли и вносили изолирующую среду, содержащую препарат в необходимой концентрации. Учет реакции производили через 72 часа инкубации по цитопатическому действию или с помощью обработки клеток видоспецифическими противохламидийными флуоресцирующими антителами. Все процедуры проводили в трехкратной повторности.
Средство в реакции гемагглютинации с хроматографическими пиками имеет максимальную активность лектинов второго пика, где титр агглютинации составил 1:512 единиц.
Средство в культуре клеток хламидий in vitro приводит к снижению титра возбудителя в группе штамм + «Ахлакор» в сравнении с положительным контролем (штамм хламидий) на 1,25 lg ТЦИД 50/мл и более свидетельствует о противохламидийной активности препарата.
Исходя из представленных данных средняя эффективная концентрация исследуемого препарата в отношении штаммов СТ-866 и СТ-867 Chlamydia trachomatis составила 5,64 мг/мл.
Результаты исследования:
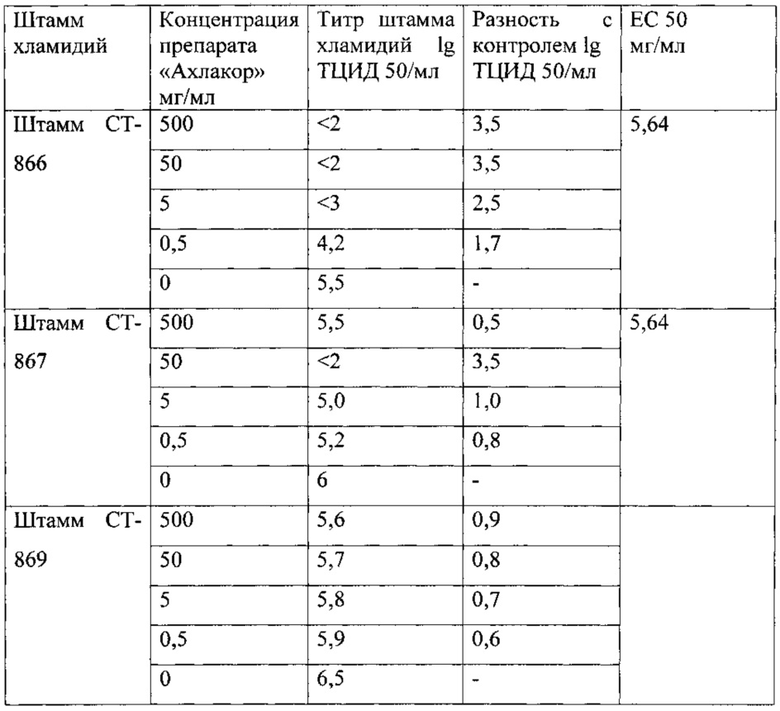
Снижение титра возбудителя в группе штамм + «Ахлакор» в сравнении с положительным контролем (штамм хламидий) на 1,25 lg ТЦИД 50/мл и более свидетельствует о противохламидийной активности препарата. Исходя из представленных данных средняя эффективная концентрация исследуемого препарата в отношении штаммов СТ-866 и СТ-867 Chlamydia trachomatis составила 5,64 мг/мл. В отношении штамма СТ-869 Chlamydia trachomatis отмечена слабая противохламидийная активность исследуемых концентраций препарата, что возможно связано с биологическими особенностями штамма.
Средство было апробировано на добровольцах.
Предложенное средство позволяет эффективно воздействовать на причину заболевания, устранить патологические симптомы болезни, предупредить развитие тяжелых осложнений в костно-мышечной системе, нивелировать циркуляцию возбудителя в организме и увеличить ремиссию заболевания. Средство позволяет использовать для амбулаторного, превентивного лечения широкого круга больных различных возрастных групп. Средство просто при использовании и экономично в применении.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО "ХИТОКОР" ДЛЯ ЛЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА B И C И СПОСОБ ЛЕЧЕНИЯ | 2001 |
|
RU2185185C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ ДЛЯ ПРОФИЛАКТИКИ И ВСПОМОГАТЕЛЬНОЙ ТЕРАПИИ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2004 |
|
RU2270585C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2004 |
|
RU2273484C2 |
| СПОСОБ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА | 1999 |
|
RU2145231C1 |
| СРЕДСТВО "РЕКТОФИТ 1" | 2011 |
|
RU2470659C1 |
| Противохламидийная вакцина и способ ее получения | 2016 |
|
RU2676768C2 |
| Штамм рекомбинантной псевдоаденовирусной частицы, экспрессирующий химерный ген MBL-CT666 Chlamydia trachomatis, способ его получения, иммуногенная композиция для защиты от урогенитального хламидиоза человека | 2019 |
|
RU2721123C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА В И С И СПОСОБ ЕГО ЛЕЧЕНИЯ | 2000 |
|
RU2171684C1 |
| СРЕДСТВО "ХИТОЭПИФИТ" ДЛЯ ЛЕЧЕНИЯ ЭПИЛЕПСИИ И СУДОРОЖНОГО СИНДРОМА | 2002 |
|
RU2204407C1 |
| СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ ПОСТИНФАРКТНОГО КАРДИОСКЛЕРОЗА | 2002 |
|
RU2204403C1 |
Изобретение относится к фармацевтической промышленности, в частности к средству для лечения хламидиоза. Средство для лечения хламидиоза, которое включает: смесь порошков хитозана пищевого, травы кипрея узколистного, душицы, зверобоя, клубней топинамбура, корней лопуха, цветков календулы, зизифоры, листьев мяты, шалфея и коры осины в определенном соотношении. Вышеописанное средство эффективно для лечения хламидиоза. 1 з.п. ф-лы, 1 пр., 1 табл.
1. Средство для лечения хламидиоза, характеризующееся тем, что оно включает: смесь порошков хитозана пищевого, травы кипрея узколистного, душицы, зверобоя, клубней топинамбура, корней лопуха, цветков календулы, зизифоры, листьев мяты, шалфея и коры осины в соотношении 1:2:1:1:3:2:1:2:1:2:3.
2. Средство по п. 1, выполненное в форме таблеток.
| Хламидиоз | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2004 |
|
RU2273484C2 |
| US 2006018984 A1, 26.01.2006. | |||
Авторы
Даты
2017-08-30—Публикация
2016-09-29—Подача