ПЕРЕКРЕСТНЫЕ ССЫЛКИ
[0001] Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США №61/544471, поданной 7 октября 2011 г., содержание которой явным образом включено в настоящую заявку посредством ссылки во всей полноте.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к лечению злокачественных и незлокачественных (т.е. доброкачественных) заболеваний, нарушений или патологических состояний с помощью антагонистов Ras.
УРОВЕНЬ ТЕХНИКИ
[0003] Ras представляет собой мембранно-связанный белок, связывающий гуанин-нуклеотид, который играет ключевую роль во многих клеточных процессах, включая пролиферацию клеток, апоптоз, дифференцировку, старение и выживание. Ras является переключателем по типу «включено-выключено» для этих клеточных процессов. В то время как в норме он находится в покое («выключен») и связан с нуклеотидом гуанозиндифосфатом (ГДФ), Ras может стать активированным («включенным») после связывания с нуклеотидом гуанозинтрифосфатом (ГТФ) под действием внеклеточных сигнальных молекул, воздействующих на различные мишени.
[0004] Белки Ras играют ключевую роль в передаче сигналов через рецептор тирозинкиназного фактора роста (Egan, S.Е. and Weinberg, R.A. Nature 365, 781-782 (1993); McCormick, F., Nature, 363, 15-16 (1993)). При активации в ГТФ-связанной форме белки Ras распространяют сигнал от фактора роста к каскаду MAP киназ. Белки Ras связаны с плазматической мембраной, где активация Raf киназы происходит в результате прямого взаимодействия Ras/Raf (Zheng, X.F. et al., Nature, 364, 308-313 (1993); Warne, P.H., Nature, 364, 352-353 (1993)).
[0005] Терминация передачи сигналов от фактора роста включает гидролиз активной ГТФ-связанной с формы Ras до неактивной, ГДФ-связанной формы Ras. Однако мутировавшие или онкогенные белки Ras не гидролизуют ГТФ и вследствие этого находятся в постоянно активном («включенном») состоянии. Неспособность гидролизовать ГТФ может приводить к различным неконтролируемым клеточным функциям.
[0006] Активированный Ras может инициировать и поддерживать злокачественный рост клеток опухоли, включая клетки опухоли, которые экспрессируют активированные белки Ras. Мутировавшие белки Ras находят с большой частотой в образцах рака человека (Bos, J.L. Cancer Res., 49, 682-4689 (1989); Barbacid, M., An. Rev. Biochem, 56, 779-829 (1987)). В некоторых типах опухолей, таких как рак толстой кишки или поджелудочной железы, частота возникновения активированного Ras составляет более 50%. Кроме опухолей, появление которых является следствием нерегулируемых действий мутировавшего или онкогенного Ras, также существуют опухоли, появление которых вызвано постоянно активными рецепторами фактора роста (например, рецептором эпидермального фактора роста, рецептором фактора роста фибробластов и рецептором фактора роста тромбоцитов), которые поддерживают Ras в активном («включенном») состоянии. Вследствие этого фармакологические способы влияния на активность Ras могут быть эффективными для лечения определенных типов рака человека.
[0007] Кроме злокачественного онкологического заболевания активированный Ras может инициировать и поддерживать незлокачественную пролиферацию клеток. Примером Ras-индуцированной незлокачественной пролиферации клеток являются псориатические поражения. Увеличенный уровень активированного Ras был обнаружен в псориатических повреждениях пациентов. (Lin F., Baldassare, J.J., Voorhees, J.J., Fisher, G.J. Increased activation of Ras in psoriatic lesions. Skin Pharmacol Appl Skin Physiol 1999 Jan-Apr; 12(1 -2):90-7). Также было установлено, что передача сигналов от рецепторов через каскад Ras/MAPK играет ключевую роль при псориатических повреждениях (Mark, Е.В., Jonsson, М., Asp, J., Wennberg, A.M., Molne, L., Lindahl, A. Expression of genes involved in the regulation of p 16 in psoriatic involved skin. Arch Dermatol Res 2006 Apr; 297(10): 459-67. Epub 2006 Mar 22).
[0008] Другие примеры Ras-индуцированной незлокачественной пролиферации клеток были обнаружены при различных наследственных заболеваниях (например, при нейрофиброматозе 1 типа (НФ 1) и поликистозе почек (ПКП)) и при различных спорадических проблемах, таких как фиброз печени, почек и сердца. Например, нейрофибромин представляет собой белок, который «выключает» Ras и является вследствие этого супрессором опухоли. Генетическая мутация, приводящая к отсутствию или потере нейрофибромина, приводит к возникновению НФ 1 - состояния, при котором в нервной ткани образуются опухоли. Эти опухоли могут быть незлокачественными (т.е., доброкачественными), но в зависимости от своего расположения они могут вызывать серьезные повреждения окружающих тканей. К тому же, эти опухоли могут трансформироваться в злокачественные состояния, такие как нейрофибросаркома или лейкоз. Другим примером является аутосомальный доминантный ПКП, который представляет собой пролиферацию эпителиальных клеток почек с последующим образованием кисты. Ингибирование Ras останавливает неконтролируемый рост этих клеток. (Parker, Е., Newby, L.J., Shaprpe, С.С., Rossetti, S., Streets, A.J., Harris, P.C., O'Hare, M.J., Ong, A.C. Hyperproliferation of PKD-1 cystic cells is induced by insulin-like growth factor-1 activation of the Ras/Raf signaling system. Kidney Int 2007 Jul:72(2): 157-65. Epub 2007 Mar 28).
[0009] Еще один пример Ras-индуцированной незлокачественной пролиферации клеток был обнаружен при патологическом состоянии постангиопластического рестеноза, который возникает после размещения стента в артериях и является следствием пролиферации клеток сосудистого эндотелия. Такая пролиферация клеток может быть вызвана травмой или повреждением ткани (например, повреждением, вызванным введением стента) или, например, локальным воспалением сосудов.
[0010] Помимо поддержания пролиферации клеток и онкогенеза активация Ras опосредует множество иммунных феноменов и аномалий иммунных функций, например, наблюдаемых при аутоиммунных заболеваниях. Такие аутоиммунные заболевания могут быть зависимыми от Ras. Аутоиммунные заболевания характеризуются самопричиненным повреждением тканей. Любой орган может подвергнуться таким процессам в результате преципитации иммунных комплексов, клеточного иммунитета или несоответствующего образования или действия провоспалительных иммунных гормонов, таких как цитокины. Аутоиммунные заболевания являются серьезной общественной проблемой здравоохранения в связи с количеством пораженных пациентов и вызываемыми ими заболеваемостью и смертностью. Распространенные хронические системные заболевания этой группы включают сахарный диабет 1 типа, тиреоидит Хашимото, ревматоидный артрит, системную красную волчанку (СКВ), первичный антифосфолипидный синдром (АФС) и множество заболеваний, которые поражают центральную и периферическую нервные системы, включая миастению гравис, миастенический синдром Ламберта-Итона, синдром Гийена-Барре, полимиозит и множественный склероз. Кроме того, при системных аутоиммунных заболеваниях существуют неврологические осложнения. Их примером является сенсорная невропатия, ассоциированная с диабетом 1 типа. Факторы, приводящие к аутоиммунным заболеваниям, включают генетическую предрасположенность и агенты окружающей среды (например, некоторые инфекции и фармацевтические продукты). Отторжение клеток и тканей, возникающее после трансплантации органов, является другим опосредованным иммунной системой феноменом, в который вовлечен Ras (Trujillo, J.I., Expert Ipin Ther Pat. 21, 1045-1069 (2011)), как, например, хроническое заболевание «трансплантат против хозяина» (Svegliati S, Olivieri A, Campelli N, Luchetti M, Poloni A, Trappolini S, Moroncini G, Bacigalupo A, Leoni P, Avvedimento EV, and Gabrielli A. Blood 110, 237-241 (2007).
[0011] Точно так же, как аномалии в передаче сигналов через Ras приводят к патологическим иммунным ответам, активированный Ras может приводить к нарушению регуляции других систем организма, таких как эндокринная и сосудистая системы. Примером этого является нарушение контроля чувствительности к инсулину в периферических тканях и в конечном счете нарушение функции поджелудочной железы при диабете 2 типа. Антагонисты Ras могут изменять резистентность к инсулину в моделях этого заболевания на животных. (Mor, A., Aizman, Е., George, J., Kloog, Y. Ras Inhibition induces insulin sensitivity and glucose uptake. PLoS One 2011 6(6):e21712. Epub 2011 Jun 29). Другим примером является воспаление сосудов, которое поддерживается провоспалительными адипокинами у животных и людей, страдающих ожирением, и которое приводит к патологии при диабете и атеросклерозе. (George, J., Afek, A., Keren, P., Herz, I., Goldberg, I., Haklai, R., Kloog, Y., Keren, G. Functional inhibition of Ras by a Ras antagonist attenuates atherosclerosis in apolipoprotein E knockout mice. Circulation 2002, 105(20): 2416-2422).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0012] В настоящем изобретении описаны новые ингибиторы или антагонисты Ras, подходящие для лечения состояний, которые являются следствием клеточных процессов, индуцированных или опосредованных Ras, включая пролиферацию клеток, дифференцировку, апоптоз, старение и выживание. Эти клеточные процессы могут быть связаны с незлокачественным или злокачественным заболеванием, нарушением или патологическим состоянием.
[0013] В настоящем изобретении также описан способ ингибирования таких клеточных процессов, индуцированных или опосредованных Ras. Способ подразумевает введение антагониста Ras в количестве, эффективном для ингибирования таких клеточных процессов.
[0014] Семейство онкогенов Ras является важным компонентом многих путей клеточной передачи сигналов. Ингибиторы такой клеточной передачи сигналов будут влиять как на вышестоящую передачу сигналов, так и на нижестоящие эффекторные пути, обеспечивая функциональный контроль над такими клеточными процессами.
[0015] Помимо злокачественных онкологических заболеваний, таких как рак поджелудочной железы, лейкоз, карцинома Меркеля и глиобластома, настоящее изобретении в особенности применимо к разнообразным незлокачественным заболеваниям, которые характеризуются пролиферацией клеток, включая цирроз печени, рестеноз сосудов после размещения стентов, ПКП и псориаз. Поскольку активация Ras поддерживает нарушение функции иммунной системы, антагонисты согласно настоящему изобретению могут быть также использованы для лечения аутоиммунных заболеваний, таких как диабет 1 типа, волчанка, ревматоидный артрит и множественный склероз, и патологических состояний, таких как отторжение трансплантата, вызванное презентацией чужеродного антигена (например, трансплантата) как реакцией на состояние болезни (например, почечной недостаточности). Аналогично, антагонисты согласно настоящему изобретению могут быть применены для лечения опосредованных Ras аномалий в эндокринных органах (например, диабет 2 типа) и кровеносных сосудах (например, артериосклероз).
[0016] В соответствии с типичным вариантом реализации настоящего изобретения предложен антагонист Ras согласно Формуле (I):

где R3 представляет собой S, О, N, SO, SO2 или Se, и R4 представляет собой фарнезил или геранил-геранил, и где по меньшей мере один из R2 представляет собой 5-членное гетероциклическое кольцо, содержащее по меньшей мере один гетероатом, и R1 представляет собой 5- или 6-членное гетероциклическое кольцо, содержащее по меньшей мере один гетероатом. Гетероатомы R2 или R1 выбирают из группы, состоящей из О, N, S, SO и SO2.
[0017] В вариантах реализации, в которых R2 представляет собой 5-членное гетероциклическое кольцо, содержащее один или два гетероатома, R1 может представлять собой CN, C(=O)R5, S(=O)(=O)R5, CO2M, SO3M, или N(R8)-замещенный тетразол, где: R5 представляет собой водород, гидроксил, С1-С4 алкилокси, С2-С4 алкенилокси, С1-С4 гидроксиалкилокси, С1-С4 аминоалкилокси или NR6R7; R6 представляет собой водород, гидроксил, С1-С4 алкил, С2-С4 алкенил, С1-С4 аминоалкил, С1-С4 гидроксиалкил, С1-С4 алкилокси или С1-С4 алкиламино, и R7 представляет собой водород, С1-С4 алкил, С2-С4 алкенил, С1-С4 аминоалкил, С1-С4 гидроксиалкил, С1-С4 алкилокси или С1-С4 алкиламино или R6 и R7 совместно образуют кольцо, включающее морфолин, пиперазин или пиперидин; М представляет собой соль, образующую органический или неорганический противоион; и R8 представляет собой водород или С1-С4 алкил. Типичный антагонист Ras включает соединение (3) ниже и его аналоги.
[0018] В вариантах реализации, в которых R1 представляет собой 5- или 6-членное гетероциклическое кольцо, содержащее по меньшей мере один гетероатом, R2 может представлять собой фенильное кольцо или возможно замещенное фенильное кольцо. R1 может представлять собой имидазолин, имидазол, пиразол, пиррол, оксазол, тиазол, 1,4,5,6-тетрагидропиримидин, триазол или N(R9)-замещенный тетразол, где R9 представляет собой водород или С1-С4 алкил; возможно замещенное фенильное кольцо замещено Cl, Br, F, I, С1-С4 алкилом или С1-С4 алкокси, амино, одно- или двузамещенным амино; и заместитель азота в фенильном кольце представляет собой С1-С4 алкил. Типичные антагонисты Ras включают соединения (1), (5) и (9) ниже и их аналоги.
[0019] В вариантах реализации, в которых R2 представляет собой 5-членное гетероциклическое кольцо, содержащее по меньшей мере три гетероатома, R1 может представлять собой C(=O)R10, где R10 представляет собой водород, гидроксил или С1-С4 алкилокси. R2 может представлять собой, например, тиадиазольную группу или оксадиазольную группу. Типичный антагонист Ras включает соединение (4) ниже и его аналоги.
[0020] Согласно другому типичному варианту реализации настоящего изобретения предложен способ ингибирования индуцированной Ras пролиферации клеток, связанной со злокачественным или незлокачественным заболеванием или патологическим состоянием. Способ включает введение пациенту антагониста Ras согласно Формуле (I) в количестве, эффективном для ингибирования пролиферации. Этап введения можно осуществить парентерально, перорально, местно, интраназально, назально, буккально или трансдермально. В одном варианте реализации пациент страдает от нарушения регуляции иммунной системы, следствием чего является по меньшей мере одно заболевание из системной красной волчанки (СКВ), множественного склероза (МС), антифосфолипидного синдрома (АФС), ревматоидного артрита, диабета 1 типа, отторжения органа и хронического заболевания «трансплантат против хозяина». В другом варианте реализации пациент страдает от нарушения регуляции по меньшей мере одного элемента из эндокринной системы и мишеней эндокринных гормонов, следствием чего является диабет 2 типа. В другом варианте реализации пациент страдает от по меньшей мере одного фактора из травмы ткани, повреждения ткани и локального воспаления сосудов, следствием чего является атеросклероз.
[0021] В соответствии с еще одним типичным вариантом реализации настоящего изобретения предложен способ ингибирования Ras-индуцированной пролиферации клеток, связанной со злокачественным заболеванием или патологическим состоянием. Способ включает приведение клеток в контакт с антагонистом Ras согласно Формуле (I) в количестве, эффективном для ингибирования пролиферации. Злокачественное заболевание может включать глиобластому, аденокарциному, саркому мягких тканей и/или лейкоз.
[0022] В соответствии с еще одним типичным вариантом реализации настоящего изобретения предложен способ ингибирования Ras-индуцированной пролиферации клеток, связанной с незлокачественным заболеванием или патологическим состоянием. Способ включаетприведение клеток в контакт с антагонистом Ras Формулы (I) в количестве, эффективном для ингибирования пролиферации. Незлокачественное заболевание может включать псориаз, нейрофиброматоз 1 типа (НФ 1), злокачественные опухоли, ассоциированные с НФ 1, поликистоз почек (ПКП), постангиопластический рестеноз, фиброз ткани и/или мышечную дистрофию.
[0023] В соответствии с еще одним типичным вариантом реализации настоящего изобретения предложен способ ингибирования Ras-индуцированной пролиферации клеток. Способ включает приведение клеток в контакт с антагонистом Ras Формулы (I) в количестве, эффективном для ингибирования пролиферации, где пролиферация индуцируется в результате травмы ткани или повреждения ткани.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
[0024] Вышеупомянутые и другие признаки и преимущества настоящего изобретения и способ их достижения станут более очевидными, и изобретение само по себе будет более понятным на основании следующего описания вариантов реализации настоящего изобретения, взятых во взаимосвязи с сопроводительными чертежами, причем:
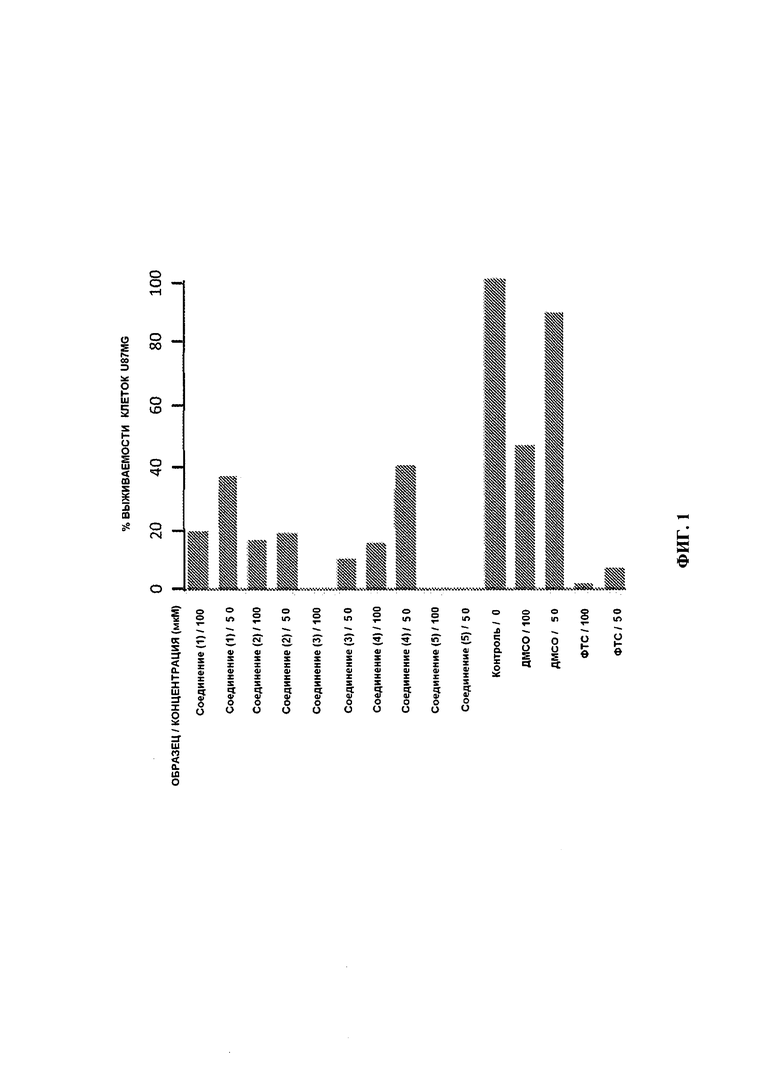
[0025] ФИГ. 1 представляет собой график, иллюстрирующий ингибирование пролиферации клеток U87MG относительно контрольного образца под действием различных доз некоторых соединений согласно настоящему изобретению;
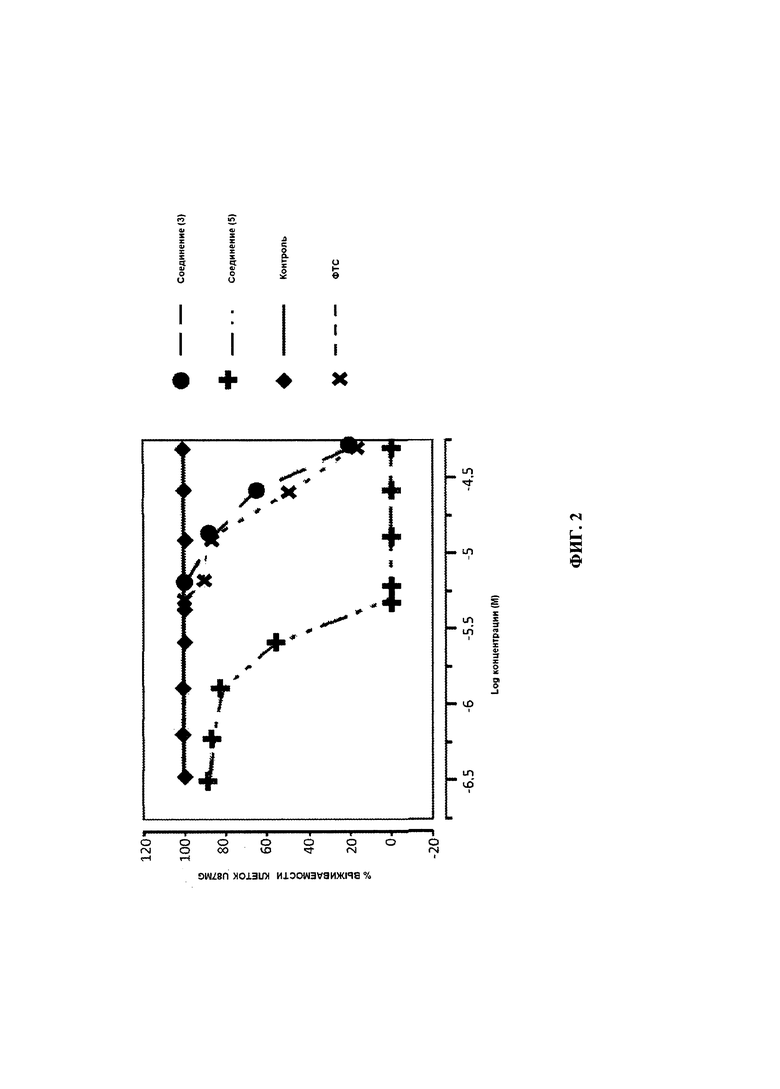
[0026] ФИГ. 2 представляет собой график, иллюстрирующий ингибирование пролиферации клеток U87MG относительно контрольного образца под действием некоторых соединений согласно настоящему изобретению в различных дозах, меньших, чем дозы, представленные на ФИГ. 1;
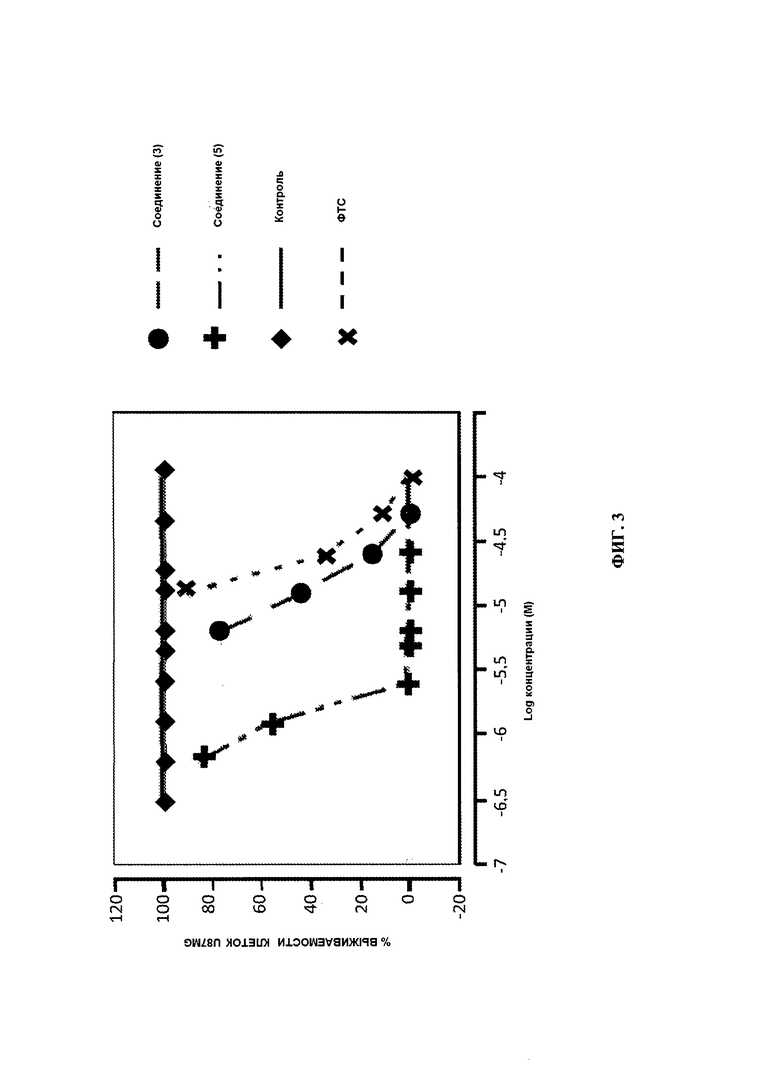
[0027] ФИГ. 3 представляет собой график, иллюстрирующий ингибирование пролиферации клеток PANC-1 относительно контрольного образца под действием различных доз некоторых соединений согласно настоящему изобретению;
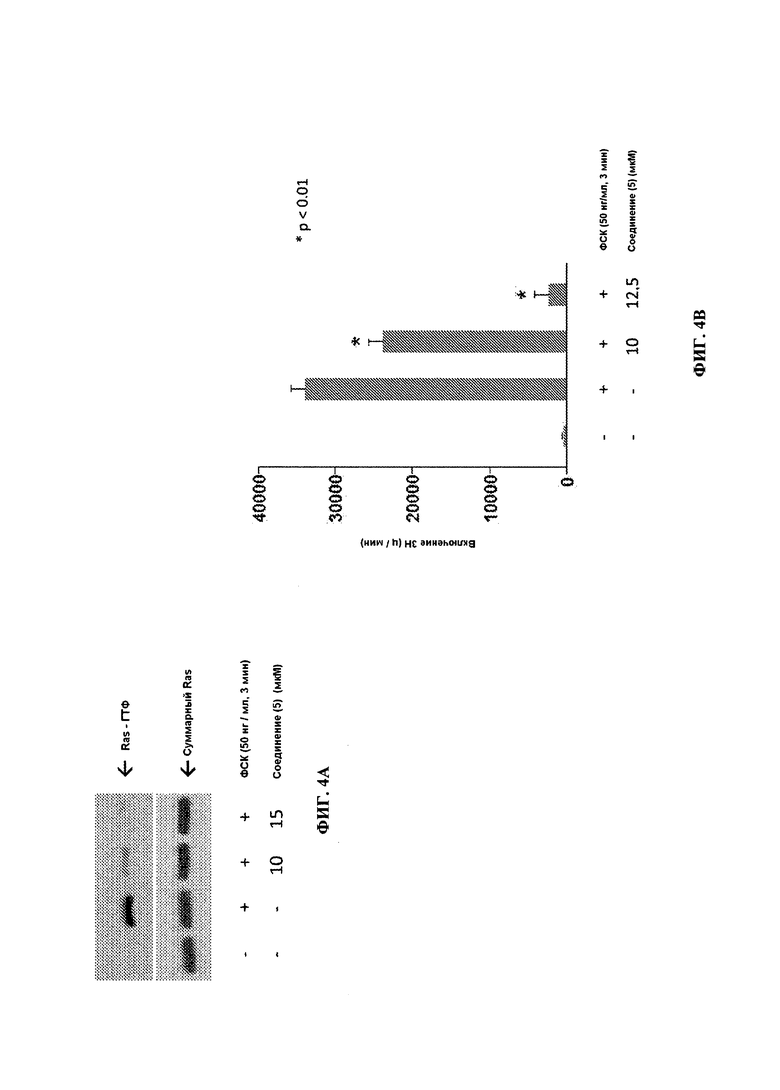
[0028] ФИГ. 4А представляет собой результат анализа методом вестерн блоттинга, иллюстрирующий ингибирование активированного Ras в тучных клетках относительно контрольного образца под действием различных доз соединения согласно настоящему изобретению;
[0029] ФИГ. 4В представляет собой график, иллюстрирующий ингибирование пролиферации тучных клеток относительно контрольного образца под действием различных доз соединения согласно настоящему изобретению;
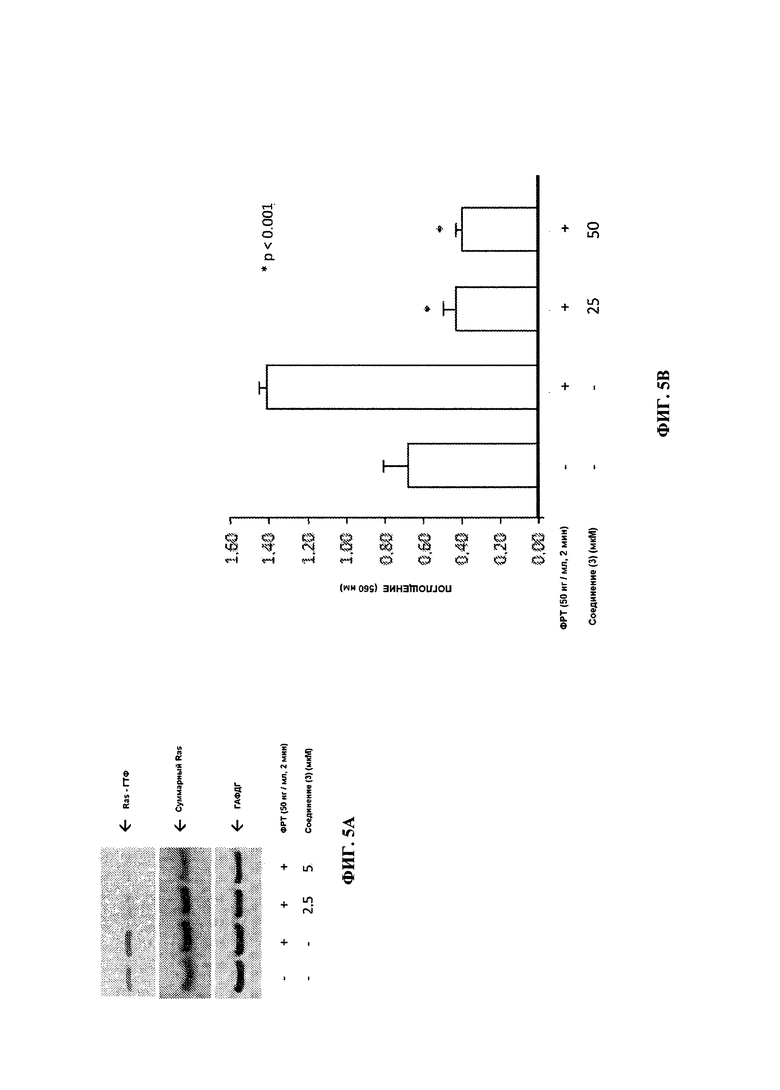
[0030] ФИГ. 5А представляет собой результат анализа методом вестерн блоттинга, иллюстрирующий ингибирование активированного Ras в шванновских клетках относительно контрольного образца под действием различных доз соединения согласно настоящему изобретению; и
[0031] ФИГ. 5В представляет собой график, иллюстрирующий ингибирование пролиферации шванновских клеток относительно контрольного образца под действием различных доз соединения согласно настоящему изобретению.
[0032] Соответствующие условные обозначения обозначают соответствующие части в рамках нескольких точек зрения. Пояснения к примерам, изложенные в настоящей заявке, иллюстрируют типичные варианты реализации настоящего изобретения, и такие пояснения к примерам не должны подразумеваться как ограничивающие каким-либо образом объем изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0033] Общие химические термины, используемые в описываемой формуле, имеют свое общепринятое значение. Например, термин «С1-С4 алкил» включает метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил и трет-бутил. Термин «С1-С4 алкилокси» используется для обозначения С1-С4 алкильной группы, связанной с первичной молекулой через атом кислорода, и включает группы метокси, этокси, изопропокси и тому подобные. Термин «С2-С4 алкенил» включает винил, аллил и кротил. Термин «С1-С4 аминоалкил» используется для обозначения С1-С4 алкильной группы, присоединенной к первичной молекуле посредством одного атома углерода и атома азота, присоединенного к одному дистальному атому углерода, и включает группы аминометилен, аминоэтилен, аминопропилен, альфа-аминоэтилен, бета-аминоэтилен и тому подобные. Термин «С1-С4 гидроксиалкил» используется для обозначения С1-С4 алкильной группы, присоединенной к первичной молекуле посредством одного атома углерода и атома кислорода, присоединенного к одному дистальному атому углерода, и включает группы гидроксиметил, гидроксиэтил, гидроксипропил, альфа-гидроксиэтил, бета-гидроксиэтил и тому подобные. Термин «амино» относится к атому азота, присоединенному к первичной структуре и возможно замещенному одной дополнительной химической группой (обозначается термином «одно-») или двумя дополнительными химическими группами (обозначается термином «дву-»), которые, взятые в совокупности, могут образовать кольцо, такое как морфолин или пиперидин, или пиперазин. Термин «С1-С4 алкиламино» используется для обозначения С1-С4 алкильной группы, связанной с первичной молекулой через атом азота, и включает группы метиламин, этиламин, изопропиламин, бутиламин, изобутиламин, втор-бутиламин и трет-бутиламин. Термин «С2-С4 алкенилокси» используется для обозначения С2-С4 алкенильной группы, связанной с первичной молекулой через атом кислорода, и включает группы винилокси, аллилокси и кротилокси. Термин «С1-С4 гидроксиалкилокси» используется для обозначения С1-С4 алкильной группы, связанной с первичной молекулой посредством атома кислорода и атома кислорода, присоединенного к одному дистальному атому углерода, и включает группы гидроксиметокси, гидроксиэтокси, гидроксипропокси, бета-гидроксиэтокси и тому подобные. Термин «С1-С4 аминоалкилокси» используется для обозначения С1-С4 алкильной группы, связанной с первичной молекулой посредством атома кислорода и атома азота, присоединенного к одному дистальному атому углерода, и включает группы альфа-гидроксиметиламин, бета-гидроксиметиламин, гамма-гидроксиметиламин, бета-гидроксиэтиламин и тому подобные.
[0034] Специалисту в данной области техники очевидно, что некоторые соединения согласно Формуле I могут существовать в виде геометрических цис- и транс- изомеров. Настоящее изобретение рассматривает все отдельные изомеры, а также смеси геометрических изомеров указанных соединений. Предпочтительно, что соединения Формулы I существуют в виде отдельных геометрических изомеров. Специалист в данной области техники понимает, что отдельные изомеры могут быть селективно приготовлены с помощью известных способов или смеси изомеров могут быть разделены с помощью, например, стандартных методик хроматографии или кристаллизации.
[0035] Специалисту в данной области техники очевидно, что могут существовать некоторые соединения Формулы I, которые содержат по меньшей мере один хиральный центр. Настоящее изобретение рассматривает все отдельные энантиомеры или диастереомеры, а также смеси энантиомеров и диастереомеров указанных соединений, включая рацематы. Предпочтительно соединения Формулы I, содержащие по меньшей мере один хиральный центр, существуют в виде отдельных энантиомеров или диастереомеров. Отдельные энантиомеры или диастереомеры могут быть приготовлены с использованием хиральных реагентов или с помощью методик стереоселективного или стереоспецифичного синтеза. В качестве альтернативы отдельные энантиомеры или диастереомеры могут быть выделены из смесей с помощью стандартных хроматографических методик или методик кристаллизации.
[0036] Специалисту в данной области техники очевидно, что некоторые соединения Формулы I могут существовать в виде таутомеров. Настоящее изобретение рассматривает все таутомерные формы.
[0037] Специалисту в данной области техники очевидно, что некоторые соединения Формулы I могут образовывать соли. Во всех случаях рассматриваются фармацевтически приемлемые соли всех соединений. Если соединения согласно настоящему изобретению включают, например, амины, соединения могут реагировать с любым количеством неорганических или органических кислот с образованием фармацевтически приемлемых солей присоединения.
[0038] Специалисту в данной области техники очевидно, что фармацевтически приемлемые сольваты соединений Формулы I рассматриваются как часть настоящего изобретения и могут быть приготовлены соответствующими способами, такими как растворение соединения Формулы I в подходящем растворителе (например, воде, метаноле, этаноле и т.д.) и перекристаллизация растворенного вещества с использованием различных методик кристаллизации. В качестве альтернативы для получения сольватов избыток растворителя можно удалить выпариванием.
[0039] Термин «Ras» используется для обозначения трех продуктов гена суперсемейства белков Ras, обозначаемых как hRas, kRas и nRas.
[0040] Термин «антагонист Ras» используется для обозначения соединения или агента, который направлен на один или более клеточных процессов, включающих пролиферацию клеток, дифференцировку, апоптоз, старение и выживание, для уменьшения, подавления или ингибирования таких клеточных процессов (Satoh Т and Kaziro Y. (1992). Cancer Biol., 3, 169±177; Khosravi-Far R and Der CJ. (1994). Cancer Metastasis Rev. 13, 67-89). Белки Ras являются переключателями (по типу «включено/выключено») между рецепторами гормона/фактора роста и регуляторными каскадами, стимулирующими деление клеток. Для того чтобы Ras был активирован («включен»), он должен быть присоединен к внутренней стороне клеточной мембраны. Вследствие этого, согласно одному варианту реализации антагонист Ras согласно настоящему изобретению препятствует взаимодействию Ras с мембраной клетки, тем самым блокируя активацию Ras или ингибируя активированный Ras (Kloog, et al., Exp. Opin. Invest. Drugs 8(12): 2121-2140 (1999)).
[0041] Настоящее изобретение направлено на лечение злокачественных заболеваний, нарушений или патологических состояний, характерной чертой которых являются, или которые каким-либо другим способом включают Ras-индуцированные клеточные функции,. Мутации в генах Ras были выявлены в приблизительно 30% всех опухолей человека. Примеры таких злокачественных состояний включают, например: аденокарциномы, включая карциномы поджелудочной железы, шейки матки, толстой кишки, предстательной железы и желудка; карциномы, включая карциномы мочевого пузыря, груди, печени, легких, кожи (например, карцинома Меркеля) и щитовидной железы; лейкоз, включая острый миелоидный лейкоз (ОМЛ), хронический миелоидный лейкоз (ХМЛ), хронический миеломоноцитарный лейкоз (ХММЛ) и ювенильный миеломоноцитарный лейкоз (ЮММЛ); саркомы мягких тканей, включая ангиосаркому, лейомиосаркому, липосаркому, радбомиосаркому и миксому; и бластомы, включая бластомы почек, печени и мозга (например, глиобластому).
[0042] Дополнительно настоящее изобретение направлено на лечение незлокачественных заболеваний, нарушений или патологических состояний, характерной чертой которых являются, или которые каким-либо другим способом включают Ras-индуцированные клеточные функции. Активированный Ras может инициировать и поддерживать незлокачественную клеточную пролиферацию, что наблюдается, например, при псориазе. Активированный Ras обнаружен при различных наследственных заболеваниях, таких как НФ 1 и ПКП. Ингибиторы Ras могут быть также подходящими для лечения различных семейных синдромов развития, при которых возникают мутации в путях передачи сигналов от Ras. Дополнительные примеры этих нарушений включают, например, синдром Леопарда, синдром Нунан, синдром Легиуса, синдром Костелло, кардио-фацио-кожный синдром, наследственный десенный фиброматоз типа 1, аутоиммунный лимфопролиферативный синдром и капиллярную мальформативную артериовенозную мальформацию. При постангиопластическом рестенозе введение внутриартериального стента вызывает повреждение, высвобождение факторов роста и пролиферацию нормальных гладкомышечных клеток. Дополнительные примеры включают цирроз печени, который включает пролиферацию нормальных гепатоцитов, звездчатых клеток и клеток соединительной ткани. Дополнительные примеры пролиферации клеток, активированной Ras, включают различные спорадические проблемы, такие как фиброз тканей, включая фиброз печени, почек и сердца (например, фиброз миокарда), которые могут наблюдаться, например, на последних стадиях заболевания почек, цирроза печени и мышечной дистрофии.
[0043] Более того, настоящее изобретение направлено на лечение активированных или опосредованных Ras иммунных феноменов и аномалий иммунной функции, таких как, например, наблюдаемые при аутоиммунных заболеваниях. Распространенные хронические системные заболевания этой группы включают сахарный диабет 1 типа, тиреоидит Хашимото, ревматоидный артрит, системную красную волчанку (СКВ), первичный антифосфолипидный синдром (АФС) и множество заболеваний, которые поражают центральную и периферическую нервные системы, включая миастению гравис, миастенический синдром Ламберта-Итона, синдром Гийена-Барре, полимиозит и множественный склероз (МС). Кроме того, при системных аутоиммунных заболеваниях существуют неврологические осложнения. Примером является сенсорная невропатия, ассоциированная с диабетом 1 типа. Факторы, приводящие к аутоиммунным заболеваниям, включают генетическую предрасположенность и агенты окружающей среды (например, некоторые инфекции и фармацевтические продукты). Хроническое отторжение клеток и тканей после трансплантации органов является другим феноменом, опосредованным иммунной системой. Отторжение трансплантата представляет собой нарушение, которое включает распознавание чужеродных клеток иммунной системой реципиента («хозяина») и которое также известно как заболевание «трансплантат против хозяина». Атака этих клеток является соответствующим иммунным ответом, но при трансплантации органов она является действительно вредной для хозяина.
[0044] Дополнительно настоящее изобретение направлено на лечение активированного или опосредованного Ras феномена и нарушения регуляции эндокринной функции, таких как наблюдаемые при диабете 2 типа. При диабете 2 типа существует нарушение контроля чувствительности к инсулину в периферических тканях и, в конечном счете, нарушение функции поджелудочной железы.
[0045] Более того, настоящее изобретение направлено на лечение категории заболеваний, вызываемых опосредованным Ras воспалением и повреждением тканей, таких как локальное воспаление сосудов и их повреждение. Воспаление сосудов, которое поддерживается провоспалительными адипокинами у животных и людей, страдающих ожирением, приводит к патологии при диабете и атеросклерозе.
[0046] Антагонист Ras согласно настоящему изобретению представлен Формулой (I) ниже:

где:
R3 представляет собой S, О, N, SO, SO2 или Se; и
R4 представляет собой фарнезил или геранил-геранил.
[0047] Формула (I) может быть описана как пренильное производное карбоксильных кислот и молекулярных структур, схожих с карбоксиконцевым фарнезилцистеином, общим для онкогенных белков Ras. Такие агенты конкурентно блокируют внутриклеточную передачу сигналов через каскад Ras и являются вследствие этого подходящими для лечения, например, онкологического заболевания. Настоящее изобретение описывает, в частности, применение и приготовление аналогов на основе фарнезила, геранил-геранил-арила и геранил-геранил-гетероарила общей Формулы (I). Известно, что эти типы агентов конкурентно блокируют внутриклеточную передачу сигналов через каскад Ras и являются вследствие этого подходящими для лечения, например, онкологического заболевания.
[0048] Согласно первому типичному варианту реализации настоящего изобретения Формула (I) также определена, как изложено ниже:
R2 представляет собой 5-членное гетероциклическое кольцо, содержащее один или два гетероатома, таких как О, N, S, SO и SO2; и
R1 представляет собой CN или одну из групп: C(=O)R5, S(=O)(=O)R5, CO2M, SO3M, и N(R8)-замещенный тетразол:
где:
R5 представляет собой водород, гидроксил, С1-С4 алкилокси, С2-С4 алкенилокси, С1-С4 гидроксиалкилокси, С1-С4 аминоалкилокси или NR6R7;
R6 представляет собой водород, гидроксил, С1-С4 алкил, С2-С4 алкенил, С1-С4 аминоалкил, С1-С4 гидроксиалкил, С1-С4 алкилокси или С1-С4 алкиламино, и R7 представляет собой водород, С1-С4 алкил, С2-С4 алкенил, С1-С4 аминоалкил, С1-С4 гидроксиалкил, С1-С4 алкилокси или С1-С4 алкиламино, или где R6 и R7 совместно образуют кольцо, такое как морфолин, пиперазин или пиперидин;
М представляет собой соль, образующую органический или неорганический противоион, такой как, но не ограничиваясь ими, натрий, калий, органический амин или солюбилизирующее органическое вещество, такое как N-алкилированные глутамины, полученные из глюкозы и алкиламина, например, N-метилглюкамин, где алкиламин представляет собой С1-С4; и
R8 представляет собой водород или С1-С4 алкил.
[0049] Согласно указанному первому типичному варианту реализации Формула (I) может включать, например, 3-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}тиофен-2-карбоновую кислоту (3) (показана ниже) и ее аналоги, где R1 представляет собой карбоновую кислоту, R2 представляет собой тиофеновое кольцо, R3 представляет собой S и R4 представляет собой фарнезил.
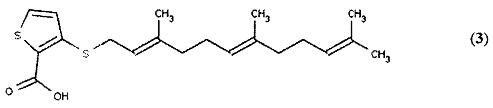
[0050] Предпочтительный аналог данного класса представлен N-метил-3-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}тиофен-2-карбоксамидом (8) (показан ниже), который подобен соединению (3) выше за исключением того, что R1 представляет собой N-метил-амид карбоновой кислоты.
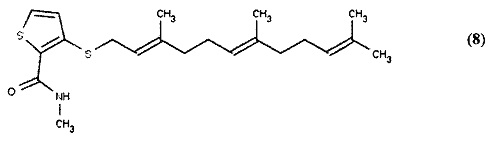
[0051] Согласно второму типичному варианту реализации настоящего изобретения Формула (I) также определена, как изложено ниже:
R2 представляет собой фенильное кольцо или возможно замещенное фенильное кольцо; и
R1 представляет собой 5- или 6-членное гетероциклическое кольцо, содержащее по меньшей мере один гетероатом, такое как имидазолин, имидазол, пиразол, пиррол, оксазол, тиазол или 1,4,5,6-тетрагидропиримидин, или 5-членное гетероциклическое кольцо, содержащее несколько атомов азота, такое как триазол или N(R9)-замещенный тетразол
где:
R9 представляет собой водород или С1-С4 алкил;
возможно замещенное фенильное кольцо может быть замещено Cl, Br, F, I, С1-С4 алкилом или С1-С4 алкокси, амино, одно- или двузамещенным амино; и
заместитель азота в фенильном кольце представляет собой С1-С4 алкил.
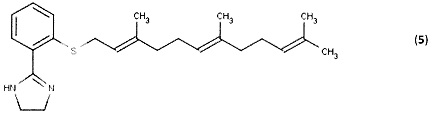
[0052] Согласно данному второму типичному варианту реализации Формула (I) может включать, например, 2-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-4,5-дигидро-1Н-имидазол (5) (показан ниже) и его аналоги, где R1 представляет собой 4,5-дигидро-1Н-имидазольную группу, R2 представляет собой фенильное кольцо, R3 представляет собой S и R4 представляет собой фарнезил.
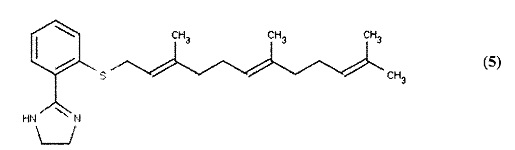
[0053] Структуры двух предпочтительных аналогов данного класса описываются следующим образом:
(i) 1-метил-2-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-4,5-дигидро-1Н-имидазол (6) (показан ниже), который подобен соединению (5) выше за исключением того, что R1 4,5-дигидро-1Н-имидазольная группа замещена метильной группой.
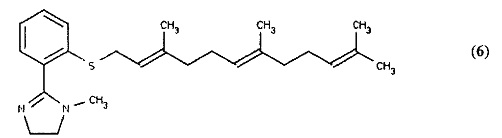
(ii) 1-(пропан-2-ил)-2-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-4,5-дигидро-1Н-имидазол (7) (показан ниже), который подобен соединению (5) выше за исключением того, что R1 4,5-дигидро-1Н-имидазольная группа замещена изопропильной группой.
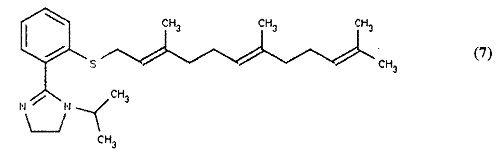
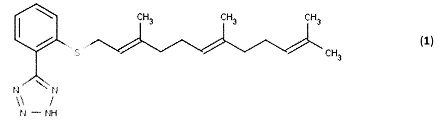
[0054] Согласно данному второму типичному варианту реализации Формула (I) может также включать, например, 5-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-2Н-1,2,3,4-тетразол (1) (показан ниже) и его аналоги, где R1 представляет собой тетразольную группу, R2 представляет собой фенильное кольцо, R3 представляет собой S и R4 представляет собой фарнезил.
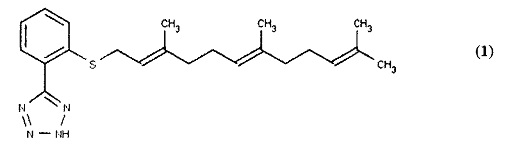
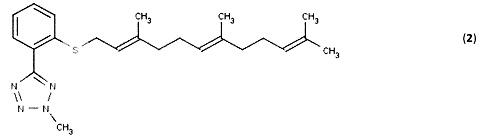
[0055] Предпочтительные аналоги данного класса представлены 2-метил-5-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-2Н-1,2,3,4-тетразолом и 1-метил-5-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1ил]сульфанил}фенил)-1Н-1,2,3,4-тетразолом (2) (показан ниже), которые подобны соединению (1) выше за исключением того, что R1 представляет собой метил-замещенную тетразольную группу.
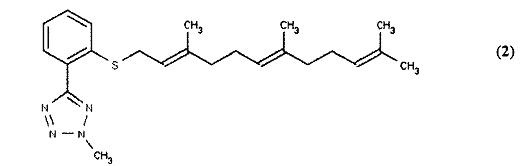
[0056] Согласно второму типичному варианту реализации Формула (I) может также включать, например, 2-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-1,4,5,6-тетрагидропиримидин (9) (показан ниже) и его аналоги, где R1 представляет собой 1,4,5,6-тетрагидропиримидин, R2 представляет собой фенильное кольцо, R3 представляет собой S и R4 представляет собой фарнезил.
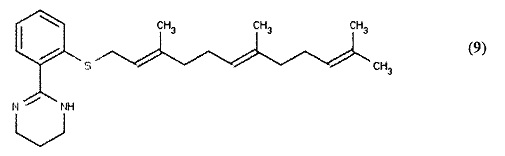
[0057] Предпочтительный аналог данного класса представлен 1-метил-2-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-1,4,5,6-тетрагидропиримидином (10) (показан ниже), который подобен соединению (9) выше за исключением того, что 1,4,5,6-тетрагидропиримидин в положении R1 замещен метальной группой.
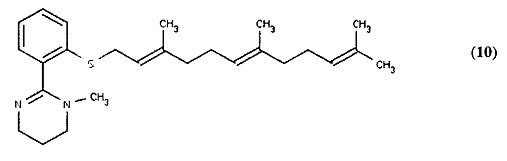
[0058] Согласно третьему типичному варианту реализации настоящего изобретения Формула (I) также определена, как изложено ниже:
R2 представляет собой 5-членное гетероциклическое кольцо, содержащее по меньшей мере три гетероатома, которые выбирают из О, N и S, такое как тиадиазольная группа или оксадиазольная группа; и
R1 представляет собой C(=O)R10,
где R10 представляет собой водород, гидроксил или С1-С4 алкилокси.
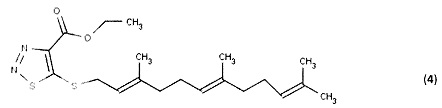
[0059] Согласно данному третьему типичному варианту реализации Формула (I) может включать, например, этил 5-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}-1,2,3-тиадиазол-4-карбоксилат (4) (показан ниже) и его аналоги, где R1 представляет собой этил-замещенную карбоксилатную группу, R2 представляет собой 1,2,3-тиадиазол, R3 представляет собой S и R4 представляет собой фарнезил.
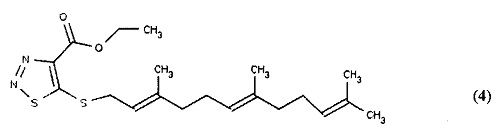
[0060] Согласно данному третьему типичному варианту реализации R1 согласно Формуле (I) может включать карбоновую кислоту и R2 согласно Формуле (I) может включать, например, 1,2,3-оксадиазол или 1,2,5-оксадиазол.
[0061] Согласно четвертому типичному варианту реализации настоящего изобретения R1 и R2 совместно представляют собой гетероциклические кольца с по меньшей мере одним гетероатомом. Например, R1 может представлять собой 5- или 6-членное гетероциклическое кольцо, содержащее по меньшей мере один гетероатом и R2 может представлять собой 5-членное гетероциклическое кольцо, содержащее по меньшей мере один гетероатом.
[0062] Специалист в данной области техники понимает, что некоторые соединения согласно настоящему изобретению являются подходящими не только в качестве ингибиторов Ras, но также являются подходящими промежуточными продуктами для приготовления дополнительных соединений согласно настоящему изобретению. Способы преобразования одной химической группы в другую понятны специалистам в данной области техники. Специалисту в данной области техники очевидно, что не все заместители соединения Формулы (I) выдержат определенные условия реакции, применяемые для синтеза соединений. Эти группы могут быть введены на подходящем этапе синтеза или могут быть защищены с последующим снятием защиты при необходимости или желании. Специалист в данной области техники понимает, что защитные группы можно удалить на любом подходящем этапе синтеза соединений согласно настоящему изобретению. Такие способы введения и удаления этих групп хорошо известны в данной области техники. Специалист в данной области техники понимает, что во многих случаях порядок, в котором вводятся группы, может быть некритичным. Конкретный порядок этапов, требуемых для получения соединения Формулы (I), зависит от конкретного синтезируемого соединения, исходного соединения и относительной лабильности или стабильности замещаемой группы.
[0063] В настоящей заявке рассматривается пероральное введение соединений согласно настоящему изобретению. Однако пероральное введение не является единственным путем или даже предпочтительным путем введения. Например, трансдермальное введение, такое как введение через трансдермальный пластырь, может быть желательным для пациентов, страдающих от заболевания, подобного псориазу. Трансдермальный путь введения может быть также предпочтительным в случаях, когда пациент может забывать или быть неспособным принимать средство для перорального введения. Внутривенный путь может быть предпочтительным для удобства в условиях стационара или для предотвращения потенциальных осложнений, связанных с дозированной формой для перорального введения. Соединения, описанные в настоящем изобретении, могут быть введены трансдермальный, внутримышечным, интраназальным, назальным, буккальным или интраректальным путем в конкретных обстоятельствах. В любом случае путь введения может варьировать в зависимости от физических свойств соединений, удобства пациента и лица, за ним ухаживающего, и других соответствующих обстоятельств (Remington's Pharmaceutical Sciences, 18th Edition, Mack Publishing Co. (1990)).
[0064] Фармацевтические композиции согласно настоящему изобретению готовят способом, хорошо известным в фармацевтической области техники. Носитель или вспомогательное вещество может представлять собой твердое, полужидкое или жидкое вещество, которое может выступать в качестве наполнителя или среды для активного компонента. Подходящие носители или вспомогательные вещества хорошо известны в данной области техники. Фармацевтическая композиция может быть адаптирована для перорального применения, ингаляции, парентерального или местного применения и может вводиться пациенту в форме таблеток, капсул, аэрозолей, средства для ингаляции, суппозиториев, растворов, суспензий и тому подобное.
[0065] Соединения согласно настоящему изобретению могут быть введены перорально, например, с инертным растворителем или в виде капсул или быть сперессованными в таблетки. С целью перорального введения соединение можно объединить со вспомогательными веществами и использовать в форме таблеток, пастилок, капсул, эликсиров, суспензий, сиропов, вафель, жевательных резинок и тому подобное. Препараты могут содержать широкое разнообразие активных компонентов в зависимости от конкретной формы, которые в целях удобства могут составлять от 4% до приблизительно 70% от веса единицы. Количество активного компонента, присутствующего в композиции, должно быть достаточным для получения подходящей дозированной формы. Предпочтительные композиции и препараты согласно настоящему изобретению могут быть определены способами, хорошо известными специалисту в данной области техники.
[0066] Таблетки, пилюли, капсулы, пастилки и тому подобное могут также содержать один или более из следующих адъювантов: связывающие вещества, такие как повидон, гидроксипропилцеллюлоза, микрокристаллическая целлюлоза или желатин; вспомогательные вещества или растворители, такие как: крахмал, лактоза, микрокристаллическая целлюлоза или дикальция фосфат, дезинтегрирующие агенты, такие как: кроскармеллоза, кросповидон, натрия крахмал гликолат, кукурузный крахмал и тому подобное; смазывающие вещества, такие как стеарат магния, стеариновая кислота, тальк или гидрогенезированное растительное масло; вещества, способствующие скольжению, такие как коллоидный диоксид кремния; увлажняющие агенты, такие как: лаурилсульфат натрия и полисорбат 80; могут быть добавлены и подсластители, такие как сахароза, аспартам или сахарин; или ароматизаторы, такие как: перечная мята, метилсалицилат или апельсиновая отдушка. Когда единица дозированной формы представляет собой капсулу, она может содержать дополнительно к веществам описанного выше типа жидкий носитель, такой как полиэтиленгликоль или жирная кислота. Другие единицы дозированной формы могут содержать другие различные вещества, которые изменяют физическую форму единицы дозирования, такие как, например, покрытие. Таким образом, таблетки или масла могут быть покрыты сахаром, гидроксипропилметилцеллюлозой, полиметакрилатом или другими веществами для покрытия. Сиропы могут содержать в дополнение к настоящим соединениям сахарозу как подсластитель и некоторые консерванты, красители, красящие вещества и ароматизаторы. Вещества, используемые при приготовлении указанных различных композиций, должны быть фармацевтически чистыми и нетоксичными в используемом количестве.
[0067] Соединения согласно настоящему изобретению обычно являются эффективными в широком диапазоне доз. Например, ежедневные дозы находятся в диапазоне от приблизительно 0,0001 до приблизительно 30 мг/кг веса тела. В некоторых случаях уровень дозы ниже нижней границы вышеуказанного диапазона может быть более чем достаточным, тогда как в других случаях еще большие дозы могут применяться без причинения любого вредного побочного действия, и вследствие этого вышеуказанный диапазон доз никоем образом не призван ограничить объем настоящего изобретения. Понятно, что количество соединения, вводимого в конкретном случае, будет определено терапевтом в свете соответствующих обстоятельств, включая состояние, требующее лечения, выбранный путь введения, фактически введенные соединение или соединения, возраст, вес, ответ конкретного пациента и степень тяжести симптомов пациента.
[0068] Специалисту в данной области техники очевидно, что существуют многочисленные варианты лечения заболеваний, охватываемых настоящим изобретением. Например, противораковая терапия включает химиотерапию, радиационную терапию, иммунотерапию или генную терапию и их комбинации. Химиотерапия относится к существующему медикаментозному лечению, вводимому пациентам с конкретным заболеванием. Специалист в данной области техники понимает объем добавления соединений, описанных в настоящем изобретении, к существующим вариантам лечения. Комбинация существующих вариантов лечения и соединений, описанных в настоящем изобретении, будет иметь особенное значение при заболеваниях, поддерживаемых Ras, описанных в настоящей заявке. Примеры химиотерапевтических агентов включают, но не ограничиваются ими, паклитаксел (Таксол®), доцетаксел (Таксотер®), цисплатин, карбоплатин (Параплатин®), гемцитабина гидрохлорид (Гемзар®), доксорубицина гидрохлорид, этопозид (Этопофос®, Вепезид®), пеметрексед (Алимта®), топотекан (Гикамтин®), винбластин (Велбе®), Виндезин (Элдизин®), винорелбин (Навелбин®), ифосфамид (Митоксана®) и Митомицин. Примеры химиотерапевтических агентов для незлокачественных заболеваний, описанных в настоящей заявке, включают, но не ограничиваются ими, глатирамера ацетат (Копаксон), метформин (Глюкофаг), хлорохин, 2-деокси-глюкозу, вальпроат натрия, холестерол, статины и клопидогрел (Плавикс®).
ПРИМЕРЫ
[0069] Следующие примеры иллюстрируют способы получения и применения антагонистов Ras согласно настоящему изобретению.
1. Пример 1: Приготовление 5-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-2Н-1,2,3,4-тетразола (1).
А. Этап 1 (A): Приготовление 2-(бензилтио)бензонитрила.
[0070] Смесь, состоящую из 2-нитробензонитрила (5,0 г, 33,75 ммоль) и 30 мл безводного диметилформамида (ДМФ), охлаждали на ледяной водяной бане (0°С) и помещали в атмосферу N2. Добавляли бензилмеркаптан (4,0 мл, 33,75 ммоль), затем добавляли по каплям водный раствор гидроксида калия (3,40 г, 60,75 ммоль в 10 мл воды). Реакционную смесь перемешивали при 0°С в течение тридцати минут, затем смесь нагревали до комнатной температуры. Через четыре часа подтверждали окончание реакции методом тонкослойной хроматографии (ТСХ). К реакционной смеси добавляли ледяную воду (100 мл). Раствор экстрагировали дихлорметаном (200 мл) и промывали солевым раствором (100 мл). Органический слой высушивали над сульфатом натрия (Na2SO4) и концентрировали при пониженном давлении до получения красного масла. Продукт очищали с помощью флэш-хроматографии на кремниевой колонке. В результате элюирования через кремниевый флэш-картридж 80-g Silicycle® с 5% этилацетатом в гептане получали целевое соединение в виде ярко-желтого твердого вещества (6,08 г, 80%) Rf 0,24ʺ с 95:5 об/об гептан: этилацетат; 1Н- ЯМР (400 МГц; CDCl3) δ 7,62 (дд, 1H), 7,47-7,42 (дт, 1Н), 7,38 (дд, 1Н), 7,32-7,25 (м, 6Н); МС (ионизация распылением в электрическом поле-) m/z 224,1 (Mz-1).
B. Этап 1(B): Приготовление 2-меркаптобензонитрила.
[0071] В трехгорлую круглодонную колбу с капельной воронкой добавляли бензол (40 мл). Колбу помещали в атмосферу N2 и охлаждали на ледяной водяной бане (0°С). К раствору бензола добавляли хлорид алюминия (4,88 г, 36,61 ммоль). В капельную воронку добавляли раствор 2-(бензилтио)бензонитрила (5,0 г, 22,19 ммоль) с этапа 1(A) в бензоле (40 мл). Раствор добавляли по каплям в течение сорока минут, реакционную смесь перемешивали при 0°С в течение одного часа и затем перемешивали при комнатной температуре в течение 48 часов. Реакцию активировали путем вливания неочищенной смеси на ледяную воду (200 мл) и перемешивания в течение 30 минут. Добавляли 10% раствор NaOH (100 мл), смесь перемешивали в течение 10 минут. Раствор подкисляли (рН=2) добавлением 6 н хлористоводородной кислоты (HCl). Раствор помещали в делительную воронку и экстрагировали дихлорметаном (3×100 мл). Объединенную органику высушивали над Na2SO4 и затем концентрировали при пониженном давлении до получения коричневого масла. Продукт очищали с помощью флэш-хроматографии на кремниевой колонке. В результате элюирования через кремниевый флэш-картридж 80-g Silicycle® с 5% этилацетатом в гептане получали целевое соединение в виде коричневого масла (2,55 г, 85%); Rf 0,56ʺ с 70:30 об/об гептан: этилацетат; 1Н-ЯМР (400 МГц; CDCl3) δ 7,52 (д, 1Н), 7,39-7,32 (м, 2Н), 7,19-7,14 (м, 1Н), 4,01 (с, 1Н); МС (ионизация распылением в электрическом поле) m/z 134,05 (Mz-1).
C. Этап 1(C): Приготовление 2-(2Н-тетразол-5-ил)бензолтиола.
[0072] В круглодонную колбу объемом 250 мл добавляли 2-меркаптобензонитрил (2,0 г, 14,8 ммоль) с этапа 1(B), затем добавляли безводный ДМФ (30 мл). В реакционную колбу добавляли хлорид аммония (1,42 г, 26,64 ммоль) и азид натрия (1,73 г, 26,64 ммоль), затем добавляли еще 10 мл ДМФ. Реакционную смесь нагревали до 105°С при потоке N2 и перемешивали в течение ночи. Реакцию активировали при первом охлаждении до комнатной температуры. Затем раствор закисляли добавлением 50 мл 1 н HCl. Раствор экстрагировали этилацетатом (2×100 мл) и затем промывали солевым раствором (100 мл). Объединенную органику высушивали над Na2SO4 и концентрировали при пониженном давлении до получения белого твердого вещества. Твердое вещество собирали фильтрацией при обработке гептаном/этилацетатом (7:3, 10 мл), в результате чего получали целевое соединение в виде белого твердого вещества (1,21 г, 46%); Rf 0,05ʺ с 95:5 об/об дихлорметан: метанол; 1Н-ЯМР (400 МГц; ДМСО-d6) δ 7,91 (д, 1Н), 7,78 (д, 1Н), 7,64-7,50 (м, 2Н), 2,90 (с, 1Н), 2,78 (с., 1Н); МС (ионизация распылением в электрическом поле-) m/z 177,1 (Mz-1).
D. Этап 1(D): Завершающее приготовление 5-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-2Н-1,2,3,4-тетразола (1).
[0073] В сцинтилляционный флакон взвешивали 2-(2Н-тетразол-5-ил)бензолтиол (0,150 г, 0,842 ммоль) с этапа 1(C). Твердое вещество растворяли в 10 мл ацетона и 1 мл безводного ДМФ. В реакционную колбу добавляли гуанидина карбонат (0,379 г, 2,105 ммоль) и транс, транс-фарнезилбромид (0,24 мл, 0,884 ммоль). Реакционную смесь нагревали до 40°С при потоке N2 и перемешивали в течение ночи. Реакцию активировали первым охлаждением до комнатной температуры. Реакционную смесь разводили дихлорметаном (100 мл) и затем промывали 1 н HCl (50 мл). Органику промывали солевым раствором (100 мл), затем высушивали над Na2SO4 и концентрировали при пониженном давлении до получения неочищенного масла. Продукт очищали с помощью флэш-хроматографии на кремниевой колонке. В результате элюирования через кремниевый флэш-картридж 80-g Silicycle® с (5-15%) этилацетатом в гептане получали целевое соединение в виде масла (32,5 мг, 10%); Rf 0,64ʺ с 50:50 об/об гептан: этилацетат; C22H30N4S1 мол. масса 382,57 г/моль; 1Н-ЯМР (400 МГц; CDCl3) δ 7,72 (д, 1Н), 7,55 (т, 1Н), 7,40 (т, 1Н), 7,30 (д, 1Н), 5,20 (т, 1Н), 5,10 (т, 1Н), 5,05 (т, 1Н), 4,81 (д, 2Н), 2,10-1,95 (м, 8Н), 1,71 (с, 3Н), 1,62-1,55 (м, 6Н), 1,43 (с, 3Н); МС (химическая ионизация при атмосферном давлении +) m/z 383,2, 765,4 (Mz+1, 2Mz+1).
2. Пример 2: Приготовление 2-метил-5-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-2Н-1,2,3,4-тетразола и 1-метил-5-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1 ил]сульфанил}фенил)-1Н-1,2,3,4-тетразола (2).
[0074] В сцинтилляционный флакон взвешивали гидрид натрия (60% дисперсия в минеральном масле, 5,0 мг). Добавляли безводный ДМФ (1 мл), затем добавляли иодметан (0,01 мл). Реакционную смесь перемешивали в течение пяти минут, затем добавляли по каплям соединение (1) (0,040 г, 0,105 ммоль) с этапа 1(D) в виде раствора в ДМФ (2 мл). Реакционную смесь перемешивали при комнатной температуре в течение 1 часа, завершение реакции подтверждали методом ТСХ. Реакцию активировали добавлением воды (6 мл). Раствор экстрагировали этилацетатом (50 мл), затем высушивали над сульфатом магния (MgSO4), фильтровали и концентрировали до получения неочищенного масла. Продукт очищали с помощью флэш-хроматографии на кремниевой колонке. В результате элюирования через кремниевый флэш-картридж 12-g Silicycle® с градиентом (2-20%) этилацетата в гептане получали целевое соединение в виде бесцветного масла (15,6 мг, 38%). C23H33N4S1 мол. масса 397,60 г/моль, Rf 0,68ʺ с 50:50 об/об гептан: этилацетат; МС (химическая ионизация при атмосферном давлении +) m/z 397,1 (Mz). Получали спектр 1Н-ЯМР смешанной фракции, который демонстрировал образование продукта (N-CH3). 1Н-ЯМР (400 МГц; CDCl3) δ 3,85 (с, 3Н).
3. Пример 3: Приготовление 3-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}тиофен-2-карбоновой кислоты (3).
[0075] 3-Сульфенил-2-тиофен карбоновую кислоту (50 мг, 0,31 ммоль) растворяли в ацетоне (5 мл). Добавляли гуанидина карбонат (66 мг, 0,38 ммоль), затем добавляли по капле транс,дранс-фарнезилбромид (88,5 мг, 0,31 ммоль) при комнатной температуре. Смесь перемешивали в течение ночи. Реакционную смесь выпаривали, суспендировали в хлороформе (20 мл) и закисляли 2 н HCl. Реакционную смесь промывали водой (10 мл), затем промывали солевым раствором. Реакционную смесь высушивали над 5 г насыщенного Na2SO4, фильтровали, фильтрат выпаривали при пониженном давлении. Неочищенную реакционную смесь очищали на колонке с прямой фазой с силикагелем (2 см × 31 см) с использованием 30:70 этилацетат:гексан. Первую фракцию объемом 100 мл собирали в колбу Эрленмейера, после чего собирали фракции объемом 7 мл. Все фракции анализировали методом ТСХ. Фракции с чистым продуктом объединяли и выпаривали. Выход составил 58 мг (50,9%), Rf 0,47ʺ в 40:60 этилацетат:гексан; C20H28O2S2, мол. масса 364,6 г/моль, МС с электрораспылением/М-Н+363, УФ λмакс 268, 314 нм.
4. Пример 4: Приготовление этил 5-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}-1,2,3-тиадиазол-4-карбоксилата(4).
[0076] Этил-5-меркапто-1,2,3-тиаздазол-4-карбоксилат (50 мг, 0,26 ммоль) растворяли в ацетоне (5 мл). Добавляли гуанидина карбонат (56 мг, 0,31 ммоль), затем добавляли по капле транс,транс-фарнезилбромид (71 мг, 0,31 ммоль) при комнатной температуре, смесь перемешивали в течение ночи. Реакционную смесь выпаривали, суспендировали в хлороформе (20 мл) и закисляли 2 н HCl. Реакционную смесь промывали водой (10 мл), затем промывали солевым раствором (20 мл). Реакционную смесь высушивали над 5 г насыщенного Na2SO4, фильтровали, фильтрат выпаривали при пониженном давлении. Неочищенную реакционную смесь очищали на колонке с прямой фазой с силикагелем (2 см × 31 см) с использованием 5:95 ацетон:гексан. Первую фракцию объемом 100 мл собирали в колбу Эрленмейера, после чего собирали фракции объемом 7 мл. Все фракции анализировали методом ТСХ. Фракции с чистым продуктом объединяли и выпаривали. Выход составил 41 мг (39,4%), Rf 0,51ʺ в 10:90 этилацетат:гексан; C20H30N2O2S2 мол. масса 394,6 г/моль, МС, химическая ионизация при атмосферном давлении/МН+394,9, УФ λмакс 303 нм.
5. Пример 5: Приготовление 2-(2-{[(2Е,6Е)-3,7,11-триметилдодека-2,6,10-триен-1-ил]сульфанил}фенил)-4,5-дигидро-1Н-имидазола (5).
[0077] 2-(4,5-Дигидро-1Н-имидазол-2-ил)бензолтиол (50 мг, 0,28 ммоль) растворяли в ацетоне (6 мл). Добавляли гуанидина карбонат (58,6 мг, 0,32 ммоль), затем добавляли по капле транс,транс-фарнезилбромид (75,6 мг, 0,28 ммоль) при комнатной температуре. Смесь перемешивали в течение ночи. Реакционную смесь выпаривали, суспендировали в хлороформе (20 мл) и закисляли 2 н HCl. Реакционную смесь промывали водой (10 мл), затем промывали солевым раствором (20 мл). Реакционную смесь высушивали над 5 г насыщенного Na2SO4, фильтровали, фильтрат выпаривали при пониженном давлении. Неочищенную реакционную смесь очищали на колонке с прямой фазой с силикагелем (2 см × 31 см) с использованием 10:90 этанол:этилацетат. Первую фракцию объемом 100 мл собирали в колбу Эрленмейера, после чего собирали фракции объемом 7 мл. Градиент растворителя медленно увеличивали до 50:50 этанол:этилацетат. Все фракции анализировали методом ТСХ. Фракции с чистым продуктом объединяли и выпаривали. Выход составил 40 мг (37,2%), Rf 0,4ʺ в 85:15:2 хлороформ:метанол:вода.
6. Пример 6: Ингибирование пролиферации клеток U87MG и PANC-1
[0078] Способность соединений согласно настоящему изобретению ингибировать рост клеток была продемонстрирована с помощью стандартных вариантов анализа, известных специалисту в данной области техники, и кратко описана в следующих пунктах.
А. Этап 6(A): Культура клеток
[0079] Зрелая клеточная линия глиобластомы U87MG была получена из коммерческого источника (АТСС). Клеточная линия рака поджелудочной железы PANC-1 была получена из местной лаборатории (Университет Индианы). Обе клеточные линии выращивали в среде Дульбекко, модифицированной по способу Исков, с 10% фетальной бычьей сывороткой (ФБС) при 37°С и 5% CO2.
В. Этап 6(B): Приготовление образца
[0080] Каждое из соединений (1), (2), (3), (4) и (5), показанных и описанных выше, растворяли в этаноле до концентрации 10 мг/мл. Отмерянную часть раствора переносили с помощью пипетки в пробирку для микроцентрифугирования. Затем этанол выпаривали из каждой пробирки с помощью SpeedVac® и оставляли в пробирке только соединение. В пробирку добавляли подходящее количество хлороформа для получения концентрации 0,1 М. Растворы помещали на лед в темное место так, чтобы их можно было перенести с помощью пипетки в виде аликвот объемом 10 и 20 мкл в пробирки для микроцентрифугирования объемом 1,5 мл. Растворы замораживали при 80°С с плотно закрытыми крышками, пробирки заматывали фольгой.
[0081] До обработки клеток пробирку с исследуемым соединением вынимали из морозильной камеры и помещали в ламинар, чтобы из пробирок испарился хлороформ. Затем в пробирки добавляли диметилсульфоксид (ДМСО) до получения точных концентраций, используемых в эксперименте (0,1 М сток). Пробирки перемешивали на вортексе и медленно добавляли теплую среду с 10% ФБС до получения точных рабочих концентраций, используемых в эксперименте. Соединения добавляли непосредственно в каждую лунку для обработки.
[0082] В качестве сравнения были приготовлены аналогичные образцы фарнезил-тиосалициловой кислоты (ФТС) (показана ниже). ФТС является объектом Патента США №5,705,528 автора Kloog.
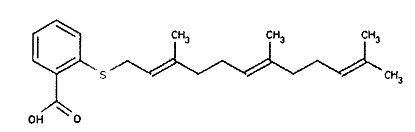
С. Этап 6(C): Анализ пролиферации клеток U87MG
[0083] Клетки U87MG выращивали в 24-луночном планшете по 5000 клеток на лунку и инкубировали в течение ночи при 37°С в бессывороточной среде. На следующий день клетки обрабатывали в трех повторах по 50 и 100 мкМ каждого из исследуемых соединений (1), (2), (3), (4) и (5) и соединением сравнения ФТС. Через пять дней клетки трипсинизировали (0,5%), окрашивали трипановым синим и подсчитывали для определения количества клеток на лунку. Рассчитывали значения IC50 с использованием программного обеспечения Multiplex Reader-Fit производства MiraiBio Group, Hitachi Solutions America, Ltd. В типичном эксперименте в контрольных лунках число клеток достигало 138000. Результаты эксперимента представлены графически на ФИГ. 1. При обработке исследуемыми соединениями в концентрации 50 мкМ наблюдалась следующая степень пролиферации клеток U87MG по сравнению с контролем: соединение (1) - 37%, соединение (2) - 18%, соединение (3) - 10%, соединение (4) - 40% и соединение (5) - 0%. При обработке соединением сравнения ФТС в концентрации 50 мкМ наблюдалось 7% пролиферации клеток по сравнению с контролем.
[0084] Для дальнейшей оценки соединений (3) и (5), которые, как видно из ФИГ. 1, в наибольшей степени ингибировали рост клеток, выращивали большее количество клеток U87MG в 24-луночных планшетах по 5000 клеток на лунку и инкубировали в течение ночи при 37°С в бессывороточной среде. На следующее утро клетки обрабатывали в среде с 5% сывороткой в трех повторах стандартными концентрациями по 6,25, 12,5, 25 и 50 мкМ каждого из исследуемых соединений (3) и (5) и соединением сравнения ФТС. Через пять дней обработки клетки трипсинизировали (0,5%) и окрашивали трипановым синим. Клетки подсчитывали для определения количества клеток на лунку. Снова рассчитывали значения IC50 с использованием программного обеспечения Multiplex Reader-Fit производства MiraiBio Group, Hitachi Solutions America, Ltd. В типичном эксперименте в контрольных лунках число клеток достигало 56000. Результаты эксперимента представлены графически на ФИГ. 2. При обработке исследуемыми соединениями в концентрации 25 мкМ наблюдалась следующая степень пролиферации клеток U87MG по сравнению с контролем: соединение (3) - 69% и соединение (5) - 0%. При обработке соединением сравнения ФТС в концентрации 25 мкМ наблюдалось более 50% пролиферации клеток по сравнению с контролем.
[0085] Поскольку дозы соединения (5), использованные выше, убивали все клетки, кривая доз была рассчитана повторно с использованием меньших доз соединения (5). Клетки U87MG выращивали в 24-луночных планшетах по 5000 клеток на лунку и инкубировали в течение ночи при 37°С в бессывороточной среде. Клетки обрабатывали в трех повторах по 6,25, 12,5, 25 и 50 мкМ соединения сравнения ФТС и по 0,3125, 0,625, 1,25, 2,5 и 5,0 мкМ исследуемого соединения (5) в среде с 5% сывороткой в течение пяти дней. Затем клетки трипсинизировали (0,5%), окрашивали трипановым синим и определяли количество клеток в каждой лунке. Снова рассчитывали значения IC50 с использованием программного обеспечения Multiplex Reader-Fit производства MiraiBio Group, Hitachi Solutions America, Ltd. В типичном эксперименте в контрольных лунках число клеток достигало 58000. Результаты эксперимента представлены графически на ФИГ. 2. При обработке исследуемым соединением (5) в концентрации 2,5 мкМ наблюдалось 56% пролиферации клеток U87MG по сравнению с контролем. При обработке соединением сравнения ФТС даже в большей дозе, 6,25 мкМ, наблюдалось более 80% пролиферации клеток по сравнению с контролем.
D. Этап 6(D): Анализ пролиферации клеток PANC-1
[0086] Для определения значения IC50 для клеток PANC-1 клетки выращивали в 24-луночных планшетах по 7500 клеток на лунку и инкубировали их в течение ночи при 37°С в бессывороточной среде. Клетки обрабатывали в трех повторах стандартными концентрациями 6,25, 12,5, 25, 50 и 100 мкМ каждого исследуемого соединения (3) и (5) и соединения сравнения ФТС и при необходимости концентрациями 0,625, 1,25, 2,5 и 5,0 мкМ в среде с 5% сывороткой в течение пяти дней. Затем клетки окрашивали трипановым синим и определяли количество клеток в каждой лунке. Снова рассчитывали значения IC50 с использованием программного обеспечения Multiplex Reader-Fit производства MiraiBio Group, Hitachi Solutions America, Ltd. В типичном эксперименте в контрольных лунках число клеток достигало 32500. Результаты эксперимента представлены графически на ФИГ. 3. При обработке исследуемым соединением (3) в концентрации 12,5 мкМ наблюдался 41% пролиферации клеток PANC-1 по сравнению с контролем и при обработке исследуемым соединением (5) в концентрации 1,25 мкМ наблюдалось 56% пролиферации клеток PANC-1 по сравнению с контролем. При обработке соединением сравнения ФТС даже в большей концентрации 12,5 мкМ наблюдалось более 80% пролиферации клеток по сравнению с контролем.
7. Пример 7: Токсичность в отношении гематопоэтических клеток-предшественников человека
[0087] Клетки низкой плотности из пуповинной крови высевали в концентрации 1×105 клеток на лунку в 1 мл полной мети л целлюлозы в присутствии каждого исследуемого соединения (3) и (5) и инкубировали в течение 12 дней в CO2 инкубаторе. В инвертированном микроскопе определяли количество гранулоцитарных колониеобразующих единиц (КОЕ-Г), эритроцитарных бурстообразующих единиц (БОЕ-Э) и смешанных колоний. Исследуемые соединения применяли в концентрациях IC50 и IC0,5, 25 и 2,5 мкМ для соединения (3) и 2,5 и 0,25 мкМ для соединения (5), значения которых определяли на клетках U87MG ранее. Исследуемые соединения были нетоксичными по отношению к гемопоэтическим клеткам-предшественникам.
8. Пример 8: Активация Ras и пролиферация тучных клеток
[0088] Очищенную популяцию тучных клеток NF-1 +/- стимулировали максимальной стимулирующей концентрацией фактора стволовых клеток (ФСК) в присутствии контроля или соединения (5) в концентрациях 10-15 мкМ. Активированную, связанную с ГТФ форму Ras (Ras-ГТФ) определяли через 3 минуты методом вестерн блоттинга. Результаты эксперимента представлены на ФИГ. 4А, которая демонстрирует, что соединение (5) существенно уменьшает уровень Ras-ГТФ относительно контроля. В параллельных экспериментах пролиферацию тучных клеток оценивали, используя включение 3Н-тимидина через 24 часа после стимуляции ФСК в присутствии контроля или соединения (5) в концентрациях 0-12,5 мкМ. Результаты эксперимента представлены на ФИГ. 4В, которая демонстрирует, что соединение (5) уменьшает пролиферацию тучных клеток относительно контроля. Каждый знак звездочки на ФИГ. 4В представляет собой статистическое различие относительно контроля, определенное с использованием дисперсионного анализа. (Yang, Feng-Chun, et. al. J Clin Invest 2003, 112(12), 1851-1861; Yang, Feng-Chun, et. al. Hum Mol Genet 2006, 15(11), 1921-1930).
9. Пример 9: Активация Ras и пролиферация шванновски клеток
[0089] Очищенную популяцию шванновских клеток NF-1 -/- S100+ выделяли из плексиформной нейрофибромы в генноинженерной мыши (Zhu, Y. et al., Science, May 2002, 3; 296(5569)):920-922) и стимулировали максимальной стимулирующей концентрацией фактора роста тромбоцитов (ФРТ) в присутствии контроля или соединения (3) в концентрациях 2,5-5 мкМ. Ras-ГТФ определяли через 3 минуты методом вестерн блоттинга. Результаты эксперимента представлены на ФИГ. 5А, которая демонстрирует, что соединение (3) существенно уменьшает уровень Ras-ГТФ относительно контроля. В параллельных экспериментах пролиферацию шванновских клеток оценивали, используя спектроскопию в видимой области через 24 часа после стимулирования ФРТ в присутствии контроля или соединения (3) в концентрациях 25-50 мкМ. Результаты эксперимента представлены на ФИГ. 5В, которая демонстрирует, что соединение (3) уменьшает пролиферацию шванновских клеток относительно контроля. Каждый знак звездочки на ФИГ. 5В представляет собой статистическое различие относительно контроля, определенное с использованием дисперсионного анализа. (Yang, Feng-Chun, et. al. J Clin Invest 2003, 112(12), 1851-1861; Yang, Feng-Chun, et. al. Hum Mol Genet 2006, 15(11), 1921-1930).
[0090] Было показано, что соединения, раскрытые в настоящей заявке, ограничивают активацию Ras и пролиферацию опухолегенных клеток, которые являются центральными в патогенезе осложнений множественного НФ 1. Путем ограничения пролиферации опухолегенных клеток соединения, раскрытые в настоящей заявке, могут ограничивать такие осложнения НФ 1.
[0091] Предпочтительные антагонисты Ras согласно настоящему изобретению включают соединения (3) и (5). Особенно предпочтительным антагонистом Ras является соединение (5). Другие антагонисты Ras, полезные в настоящем изобретении, могут быть обнаружены с использованием анализа бесклеточных мембран и вариантов клеточного анализа, описанных в заявке WO 98/38509, объект изобретения которой явным образом включен в настоящую заявку посредством ссылки во всей своей полноте. Данная публикация патента описывает несколько систем анализа, разработанных для определения способности потенциального агента вытеснять активированный Ras из мембраны. В общем виде аналитический материал, который включает конкретные мембраны, содержащие известное и обнаруживаемое количество заякоренного Ras, подвергают воздействию потенциального агента. Аналитический материал затем разделяют на мембранную фракцию, содержащую мембраны, и цитозольную фракцию, оставшуюся после удаления конкретных мембран. Измеряют фракцию известного количества меченного Ras, содержащегося в мембранной и цитозольной фракциях, что является оценкой способности потенциального агента разрушать связь Ras с мембраной. Особенно подходящим источником мембран с заякоренным активированным Ras являются мембраны, изолированный из раковых клеток, трансформированных Ras, таких как клетки PANC-1.
[0092] Хотя настоящее изобретение было описано со ссылками на типичные варианты реализации, настоящее изобретение может быть дополнительно модифицировано без выхода за рамки сущности и объема настоящего изобретения. Таким образом, предполагается, что настоящая заявка включает любые варианты, применения или адаптации настоящего изобретения на основании его общих принципов. Кроме того, предполагается, что настоящая заявка включает такие отступления от раскрытия изобретения как известные или находящиеся в рамках общепринятой практики в области техники, к которой относится настоящее изобретение, и что они находятся в пределах прилагаемой формулы изобретения.
Группа изобретений относится к химико-фармацевтической промышленности и представляет собой антагонист Ras, представленный формулой R1-R2-R3-R4, где: R3 представляет собой S; R4 представляет собой фарнезил или геранил-геранил, где геранил-геранил имеет следующую структуру
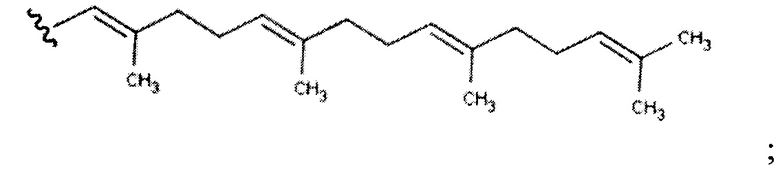
R2 представляет собой 5-членное гетероциклическое кольцо, содержащее один гетероатом S; R1 представляет собой C(=O)R5, СО2М; R5 представляет собой гидроксил; М представляет соль, образующую органический или неорганический противоион; и его фармацевтически приемлемые соли; или R1 представляет собой 5-членное гетероциклическое кольцо, содержащее 2-4 гетероатома N и R2 представляет собой фенильное кольцо; или R2 представляет собой 5-членное гетероциклическое кольцо, содержащее три гетероатома, выбранных из N и S, и R1 представляет собой C(=O)R10, и R10 представляет собой водород, гидроксил или С1-С4 алкилокси. Изобретение также относится к способу ингибирования Ras-индуцированной пролиферации клеток, связанной со злокачественным или незлокачественным заболеванием, включающему введение пациенту антагониста Ras. 7 н. и 13 з.п. ф-лы, 9 пр., 7 ил.
1. Антагонист Ras, представленный Формулой (I):

где:
R3 представляет собой S;
R4 представляет собой фарнезил или геранил-геранил, где геранил-геранил имеет следующую структуру
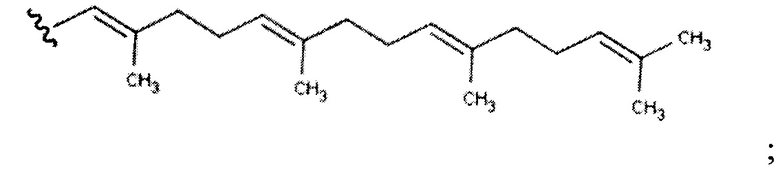
R2 представляет собой 5-членное гетероциклическое кольцо, содержащее один гетероатом S;
R1 представляет собой C(=O)R5, СО2М;
где:
R5 представляет собой гидроксил;
М представляет собой соль, образующую органический или неорганический противоион;
и его фармацевтически приемлемые соли.
2. Антагонист Ras по п. 1, имеющий формулу (3):
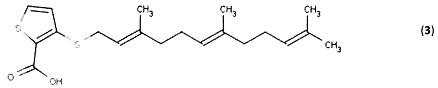
3. Антагонист Ras, представленный Формулой (I):

где:
R3 представляет собой S;
R4 представляет собой фарнезил или геранил-геранил, где геранил-геранил имеет следующую структуру
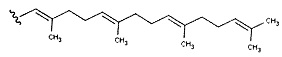 ;
;
R1 представляет собой 5-членное гетероциклическое кольцо, содержащее 2-4 гетероатома N,
R2 представляет собой фенильное кольцо; и
его фармацевтически приемлемые соли.
4. Антагонист Ras по п. 3, отличающийся тем, что R1 представляет собой имидазолин, имидазол, пиразол, триазол или N(R9)-замещенный тетразол; и
где:
R9 представляет собой водород или С1-С4 алкил.
5. Антагонист Ras по п. 3, имеющий формулу (5):
6. Антагонист Ras по п. 3, имеющий формулу (1):
7. Антагонист Ras, представленный Формулой (I):

где:
R3 представляет собой S;
R4 представляет собой фарнезил или геранил-геранил, где геранил-геранил имеет следующую структуру
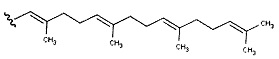 ;
;
R2 представляет собой 5-членное гетероциклическое кольцо, содержащее три гетероатома, выбранных из N и S;
R1 представляет собой C(=O)R10, и причем R10 представляет собой водород, гидроксил или С1-С4 алкилокси; и
его фармацевтически приемлемые соли.
8. Антагонист Ras по п. 7, отличающийся тем, что R2 представляет собой тиадиазольную группу.
9. Антагонист Ras по п. 7, имеющий формулу (4):
 .
.
10. Способ ингибирования Ras-индуцированной пролиферации клеток, связанной со злокачественным или незлокачественным заболеванием или патологическим состоянием, причем указанный способ включает:
введение пациенту антагониста Ras по любому из предшествующих пунктов в количестве, эффективном для ингибирования указанной пролиферации.
11. Способ по п. 10, отличающийся тем, что пациент страдает от нарушения регуляции иммунной системы, приводящего к по меньшей мере одному заболеванию из системной красной волчанки (СКВ), множественного склероза (МС), антифосфолипидного синдрома (АФС), ревматоидного артрита, диабета 1 типа, отторжения органа и хронического заболевания «трансплантат против хозяина».
12. Способ по п. 10, отличающийся тем, что пациент страдает от нарушения регуляции по меньшей мере одного из эндокринной системы и мишеней эндокринных гормонов, приводящего к диабету 2 типа.
13. Способ по п. 10, отличающийся тем, что пациент страдает от по меньшей мере одного из травмы ткани, повреждения ткани и локального воспаления сосудов, приводящего к атеросклерозу.
14. Способ по п. 10, отличающийся тем, что этап введения осуществляют парентерально, перорально, местно, интраназально, назально, буккально или трансдермально.
15. Способ ингибирования Ras-индуцированной пролиферации клеток, связанной со злокачественным заболеванием или патологическим состоянием, причем указанный способ включает:
приведение клеток в контакт с антагонистом Ras по любому из пп. 1-9 в количестве, эффективном для ингибирования указанной пролиферации.
16. Способ по п. 15, отличающийся тем, что злокачественное заболевание представляет собой по меньшей мере одно заболевание из злокачественной опухоли поджелудочной железы, глиобластомы, аденокарциномы, саркомы мягких тканей и лейкоза.
17. Способ ингибирования Ras-индуцированной пролиферации клеток, связанной с незлокачественным заболеванием или патологическим состоянием, причем указанный способ включает:
приведение клеток в контакт с антагонистом Ras по любому из пп. 1-9 в количестве, эффективном для ингибирования указанной пролиферации.
18. Способ по п. 17, отличающийся тем, что незлокачественное заболевание представляет собой по меньшей мере одно заболевание из псориаза, нейрофиброматоза 1 типа (НФ 1), злокачественных опухолей, ассоциированных с НФ 1, поликистоза почек (ПКП), постангиопластического рестеноза, фиброза ткани и мышечной дистрофии.
19. Способ ингибирования Ras-индуцированной пролиферации клеток, включающий:
приведение клеток в контакт с антагонистом Ras по любому из пп. 1-9 в количестве, эффективном для ингибирования пролиферации;
причем указанная пролиферация вызвана травмой или повреждением ткани.
20. Антагонист Ras по п. 4, имеющий формулу (2):
| US 20090226512 A1, 10.09.2009 | |||
| US 20100189781 A1, 29.07.2010 | |||
| US 6462086 B1, 08.10.2002 | |||
| КОМПЛЕКС ИНГИБИТОРА RAS-ФАРНЕЗИЛТРАНСФЕРАЗЫ, КОМПОЗИЦИЯ ИНГИБИТОРА RAS-ФАРНЕЗИЛТРАНСФЕРАЗЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1999 |
|
RU2230062C2 |
Авторы
Даты
2017-10-02—Публикация
2012-10-05—Подача