Область техники
Данное изобретение относится к соединениям, которые модулируют функцию LRRK2 и являются полезными для лечения заболеваний и состояний, опосредованных LRRK2, таких как болезнь Паркинсона.
Предшествующий уровень техники
Нейродегенеративные заболевания, такие как болезнь Паркинсона, деменция с тельцами Леви и болезнь Хантингтона поражают миллионы индивидуумов. Болезнь Паркинсона представляет собой хроническое прогрессирующее расстройство моторной системы, поражающее приблизительно одного из каждой 1000 людей, с наследственной болезнью Паркинсона, насчитывающей 5-10% всех пациентов. Болезнь Паркинсона обусловлена прогрессирующей утратой дофаминовых нейронов среднего мозга, что приводит к ослабленной способности пациентов к направленным и контролируемым движениям. Первичные симптомы болезни Паркинсона представляют собой дрожь, оцепенелость, замедленность движений и нарушение равновесия. У многих пациентов с болезнью Паркинсона также присутствуют другие симптомы, такие как эмоциональные изменения, потеря памяти, проблемы с речью и расстройства сна.
Ген, кодирующий белок богатой лейцином повторной киназы 2 (LRRK2), идентифицирован в связи с наследственной болезнью Паркинсона (Paisan-Ruiz et al., Neuron, Vol. 44(4), 2004, pp. 595-600; Zimprich et al., Neuron, Vol. 44(4), 2004, 601-607). In-vitro исследования показывают, что мутация, ассоциированная с болезнью Паркинсона, приводит к повышенной активности киназы LRRK2 и пониженной скорости гидролиза ГТФ по сравнению с диким типом (Guo et al., Experimental Cell Research, Vol. 313(16), 2007, pp. 3658-3670. Антитела к LRRK2 применяют для мечения телец Леви ствола мозга, ассоциированных с болезнью Паркинсона, и кортикальных антител, ассоциированных с деменцией с тельцами Леви, подтверждая, что LRRK2 может играть важную роль в образовании телец Леви и в патогенезе, ассоциированном с этими заболеваниями (Zhou et al., Molecular Degeneration, 2006, 1:17 doi: 10.1186/1750-1326-1-17). LRRK2 также идентифицирован в качестве гена, потенциально ассоциированного с повышенной восприимчивостью к болезни Крона и восприимчивостью к проказе (Zhang et al., New England J. Med. Vol. 361 (2009) pp. 2609-2618.
Также LRRK2 ассоциирован с переходом умеренных когнитивных нарушений в болезнь Альцгеймера (WO 2007/149789); дискинезию, индуцированную L-дигидроксифенилаланином (Hurley et al., Eur. J. Neurosci., Vol. 26, 2007, pp. 171-177; расстройства ЦНС, ассоциированные с дифференциацией предшественников нейронов (Milosevic et al., Neurodegen., Vol. 4, 2009, p. 25); рак, такой как рак почек, молочных желез, простаты, крови и легких и острый миелоидный лейкоз (WO 2011/038572); папиллярный рак почки и тиреокарциному (Looyenga et al., www.pnas.org/cgi/doi/10.1073/pnas.1012500108); множественную миелому (Chapman et al., Nature Vol. 471, 2011, pp. 467-472); амиотрофический боковой склероз (Shtilbans et al., Amyotrophic Lateral Sclerosis "Early Online 2011, pp. 1-7); ревматоидные артриты (Nakamura et al., DNA Res. Vol. 13(4), 2006, pp. 169-183); и анкилозирующий спондилит (Danoy et al., PLoS Genetics, Vol. 6(12), 2010, e1001195, pp. 1-5).
Соответственно, соединения и композиции, эффективные при модулировании активности LRRK2, могут обеспечить лечение нейродегенеративных заболеваний, таких как болезнь Паркинсона и деменция с тельцами Леви, расстройств ЦНС, таких как болезнь Альцгеймера, и дискинезии, индуцированной L-дигидроксифенилаланином, рака, такого как рак почки, молочных желез, простаты, крови, папиллярный рак и рак легких, острого миелоидного лейкоза и множественной миеломы и воспалительных заболеваний, таких как проказа, болезнь Крона, амиотрофический боковой склероз, ревматоидный артрит и анкилозирующий спондилит. В частности, существует необходимость в соединениях с аффинностью к LRRK2, которые более селективны в отношении LRRK2, чем других киназ, таких как JAK2, и которые могут обеспечить эффективные лекарственные средства для лечения нейродегенеративных расстройств, таких как болезнь Паркинсона.
Краткое описание изобретения
Изобретение предлагает соединения формулы I:

или их фармацевтически приемлемые соли,
где:
m составляет от 0 до 3;
Х представляет собой: -NRa-; -O-; или -S(O)r-, где r составляет от 0 до 2 и Ra представляет собой водород или С1-6-алкил;
R1 представляет собой: С1-6-алкил; С1-6-алкенил; С1-6-алкинил; гало-С1-6-алкил; С1-6-алкокси-С1-6-алкил; гидрокси-С1-6-алкил; амино-С1-6-алкил; С1-6-алкилсульфонил-С1-6-алкил; С3-6-циклоалкил, возможно замещенный С1-6-алкилом; С3-6-циклоалкил-С1-6-алкил, где часть С3-6-циклоалкил возможно замещена С1-6-алкилом; тетрагидрофуранил; тетрагидрофуранил-С1-6-алкил; оксиэтанил; или оксиэтан-С1-6-алкил;
или R1 и Ra вместе с двумя атомами, к которым они прикреплены могут образовывать трех-шестичленное кольцо, возможно включающее дополнительный гетероатом, выбранный из О, N и S, и замещенное оксо, гало или С1-6-алкилом;
R2 представляет собой: гало; С1-6-алкокси; циано; С1-6-алкинил; С1-6-алкенил; гало-С1-6-алкил; гало-С1-6-алкокси; С3-6-циклоалкил, где часть С3-6-циклоалкил возможно замещена С1-6-алкилом; С3-6-циклоалкил-С1-6-алкил, где часть С3-6-циклоалкил возможно замещена С1-6-алкилом; тетрагидрофуранил; тетрагидрофуранил-С1-6-алкил; ацетил; оксиэатнил; или оксиэтан-С1-6-алкил;
R3 и R4 независимо друг от друга представляют собой: гало; С1-6-алкил; С1-6-алкокси; С3-6-циклоалкилокси; гало-С1-6-алкил; или гало-С1-6-алкокси;
или R3 и R4 вместе с двумя атомами, к которым они прикреплены, могут образовывать пяти или шестичленное кольцо, возможно включающее один или два гетероатома, независимо друг от друга выбранных из О, N и S, кольцо возможно один или более раз замещено R6;
R5 представляет собой: С1-6-алкил-сульфонил; С3-6-циклоалкилсульфонил; С3-6-циклоалкил-С1-6-алкилсульфонил; циано; циано-С1-6-алкил; гетероциклил возможно замещенный один или более раз R6; гетероциклил-С1-6-алкил, где гетероциклильная группа замещена один или более раз R6; гало-С1-6-алкил; гетероциклил-сульфонил, где гетероциклильная группа возможно замещена один или более раз R6; или карбокси; и
R6 представляет собой: C1-6-алкил; гало; гало-С1-6-алкил; или оксо.
Изобретение также предлагает фармацевтические композиции, включая соединения, способы применения данных соединений и способы получения данных соединений.
Подробное описание изобретения
Определения
Если не указано иное следующие термины, примененные в данной заявке, включая описание и формулу изобретения, имеют значения, приведенные ниже. Следует отметить, что, как употреблено в описании и в прилагаемой формуле изобретения, формы единственного числа "a", "an," и "the" включают множество объектов. Если в контексте ясно не указано иное.
"Алкил" означает одновалентную линейную или разветвленную насыщенную углеводородную группу, состоящую только из атомов углерода и водорода, включающую от одного до двенадцати атомов углерода. "Низший алкил" относится к алкильной группе из одного-шести атомов углерода, т.е. С1-С6-алкилу. Примеры алкильных групп включают, но не ограничены, метил, этил, пропил, изопропил, изобутил, втор-бутил, трет-бутил, пентил, н-гексил, октил, додецил и т.п.
"Алкенил" означает линейный одновалентный углеводородный радикал из шести атомов углерода или разветвленный одновалентный углеводородный радикал из трех-шести атомов углерода, содержащий по меньшей мере одну двойную связь, например этенил, пропенил и т.п.
"Алкинил" означает линейный углеводородный радикал из двух-шести атомов углерода или разветвленный одновалентный углеводородный радикал из трех-шести атомов углерода, содержащий по меньшей мере одну тройную связь, например этенил, пропенил и т.п.
"Алкилен" означает линейный насыщенный углеводородный радикал из двух-шести атомов углерода или разветвленный насыщенный двухвалентный углеводородный радикал из трех-шести атомов углерода, например метилен, этилен, 2,2-диметилэтилен, пропилен, 2-метилпропилен, бутилен, пентилен и т.п.
"Алкокси" и "алкилокси", которые могут быть применены взаимозаменяемо, означают группу формулы -OR, где R представляет собой алкильную группу, как определено выше. Примеры алкокси групп включают, но не ограничены, метокси, этокси, изопропокси и т.п.
"Алкоксиалкил" означает группу формулы Ra-O-Rb-, где Ra представляет собой алкил и Rb представляет собой алкилен, как определено выше. Примеры алкоксиалкильных групп включают, например, 2-метоксиэтил, 3-метоксипропил, 1-метил-2-метоксиэтил, 1-(2-метоксиэтил)-3-метоксипропил, и 1-(2-метоксиэтил)-3-метоксипропил.
"Алкоксиалкокси" означает группу формулы -O-R-R', где R представляет собой алкилен и R' представляет собой алкокси, как определено в данном документе.
"Алкилкарбонил" означает группу формулы -C(O)-R, где R представляет собой алкил, как определено в данном документе.
"Алкоксикарбонил" означает группу формулы -C(O)-R, где R представляет собой алкокси, как определено в данном документе.
"Алкилкарбонилалкил" означает группу формулы -R-C(O)-R, где R представляет собой алкилен и R' представляет собой алкил, как определено в данном документе.
"Алкоксикарбонилалкил" означает группу формулы -R-C(O)-R, где R представляет собой алкилен и R' представляет собой алкокси, как определено в данном документе.
"Алкоксикарбонилалкокси" означает группу формулы -O-R-C(O)-R', где R представляет собой алкилен, и R' представляет собой алкокси, как определено в данном документе.
Тидроксикарбонилалкокси" означает группу формулы -O-R-C(O)-ОН, где R представляет собой алкилен, как определено в данном документе.
"Алкиламинокарбонилалкокси" означает группу формулы -O-R-C(O)-NHR', где R представляет собой алкилен и R' представляет собой алкил, как определено в данном документе.
"Диалкиламинокарбонилалкокси" означает группу формулы -O-R-C(O)-NR'R'', где R представляет собой алкилен и R' и R'' представляют собой алкил, как определено в данном документе.
"Алкиламиноалкокси" означает группу формулы -O-R-NHR', где R представляет собой алкилен и R' представляет собой алкил, как определено в данном документе.
"Диалкиламиноалкокси" означает группу формулы -O-R-NR'R', где R представляет собой алкилен и R' и R'' представляют собой алкил, как определено в данном документе.
"Алкилсульфонил" означает группу формулы -SO2-R, где R представляет собой алкил, как определено в данном документе.
"Алкилсульфонилалкил" означает группу формулы -R'-SO2-R'', где R' представляет собой алкилен и R'' представляет собой алкил, как определено в данном документе.
"Алкилсульфонилалкокси" означает группу формулы -O-R-SO2-R', где R представляет собой алкилен и R' представляет собой алкил, как определено в данном документе.
"Амино" означает группу формулы -NRR', где R и R' независимо представляют собой водород или алкил, как определено в данном документе. "Амино" также включает "алкиламино" (где один из R и R' представляет собой алкил, и другой представляет собой водород) и "диалкиламино (где R и R' оба представляют собой алкил).
"Аминокарбонил" означает группу формулы -C(O)-R, где R представляет собой амино, как определено в данном документе.
"Алкоксиамино" означает группу формулы -NR-OR', где R представляет собой водород или алкил и R' представляет собой алкил, как определено в данном документе.
"Алкилсульфанил" означает группу формулы -SR, где R представляет собой алкил, как определено в данном документе.
"Аминоалкил" означает группу -R-R', где R' представляет собой амино и R представляет собой алкилен, как определено в данном документе. "Аминоалкил" включает аминометил, аминоэтил, 1-аминопропил, 2-аминопропил и т.п. Аминогруппа "аминоалкила" может быть замещена один или два раза для получения "алкиламиноалкил" и "диалкиламиноалкил" соответственно. "Алкиламиноалкил" включает метиламинометил, метиламиноэтил, метиламинопропил, этиламиноэтил и т.п. "Диалкиламиноалкил" включает диметиламинометил, диметиламиноэтил, диметиламинопропил, N-метил-N-этиламиноэтил и т.п.
"Аминоалкокси" означает группу -OR-R', где R' представляет собой амино и R представляет собой алкилен, как определено в данном документе.
"Алкилсульфониламидо" означает группу формулы -NR'SO2-R, где R представляет собой алкил и R' представляет собой водород или алкил.
"Аминокарбонилоксиалкил" или "карбамилалкил" означает группу формулы -R-O-C(O)-NR'R'', где R представляет собой алкилен и R', R'' независимо друг от друга представляют собой водород или алкил, как определено в данном документе.
"Алкинилалкокси" означает группу формулы -O-R-R', где R представляет собой алкилен и R' представляет собой алкинил, как определено в данном документе.
"Арил" означает одновалентную циклическую ароматическую углеводородную группу, состоящую из моно-, би- или трициклического ароматического кольца. Арильная группа возможно может быть замещена, как определено в данном документе. Примеры арильных групп включают, но не ограничены, фенил, нафтил, фенантрил, фторенил, инденил, пенталенил, азуленил, оксидифенил, бифенил, метилендифенил, аминодифенил, дифенилсульфидил, дифенилсульфонил, дифенилизопропилиденил, бензодиоксанил. бензофуранил, бензодиоксилил, бензопиранил, бензоксазинил, бензоксазинонил, бензопиперадинил, бензопиперазинил, бензопирролидинил, бензоморфолинил, метилендиоксифенил, этилендиоксифенил и т.п., которые возможно могут быть замещены, как определено в данном документе.
"Арилалкил" и "аралкил", которые могут быть употреблены взаимозаменяемо, означают радикал-RaRb, где Ra представляет собой алкиленовую группу и Rb представляет собой арильную группу, как определено в данном документе, например, примерами арилалкила являются фенилалкилы, такие как бензил, фенилэтил, 3-(3-хлорфенил)-2-метилпентил.
"Арилсульфонил" означает группу формулы -SO2-R, где R представляет собой арил, как определено в данном документе.
"Арилокси" означает группу формулы -O-R, где R представляет собой арил, как определено в данном документе.
"Аралкилокси" означает группу формулы -O-R-R'', где R представляет собой алкилен и R' представляет собой арил, как определено в данном документе.
"Карбокси" или "гидроксикарбонил", которые могут быть употреблены взаимозаменяемо, означают группу формулы -С(O)-ОН.
"Цианоалкил" означает группу формулы -R'-R'', где R' представляет собой алкилен, как определено в данном документе, и R'' представляет собой циано или нитрил.
"Циклоалкил" означает одновалентную насыщенную карбоциклическую группу, состоящую из моно- или бициклических колец. Конкретный циклоалкил незамещен или замещен алкилом. Циклоалкил возможно может быть замещен, как употреблено в данном документе. Если не указано иное, циклоалкил возможно может быть замещен одним или более заместителем, где каждый заместитель независимо представляет собой гидрокси, алкил, алкокси, гало, галоалкил, амино, моноалкиламино или диалкиламино. Примеры циклоалкильных групп включают, но не ограничены, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.п., включая их частично ненасыщенные (циклоалкенил) производные.
"Циклоалкилалкил" означает группу формулы -R'-R'', где R' представляет собой алкилен, и R'' представляет собой циклоалкил, как определено в данном документе.
"Циклоалкилалкокси" означает группу формулы -O-R-R', где R представляет собой алкилен, и R' представляет собой циклоалкил, как определено в данном документе.
"Гетероарил" означает моноциклический или бициклический радикал из 5-12 атомного кольца, имеющий по меньшей мере одно ароматическое кольцо, содержащее один, два или три гетероатома, выбранных из N, О или S, остальные атомы кольца представляют собой С, при этом точка прикрепления гетероарильного радикала будет на ароматическом кольце. Гетероарильное кольцо может быть замещенным, как определено в данном документе. Примеры гетероарильных групп включают, но не ограничены, возможно замещенный имидазолил, оксазолил, изооксазолил, тиазолил, изотиазолил, оксадиазолил, тиадиазолил, пиразинил, тиенил, бензотиенил, тиофенил, фуранил, пиранил, пиридил, пирролил, пиразолил, пиримидил, хинолинил, изохинолинил, бензофурил, бензотиофенил, бензотиопиранил, бензимидазолил, бензооксазолил, бензооксадиазолил, бензотиазолил, бензотиадиазолил, бензопиранил, индолил, изоиндолил, триазолил, триазинил, хиноксалинил, пуринил, хиназолинил, хинолизинил, нафтиридинил, птеридинил, карбазолил, азепенил, диазепенил, акридинил и т.п., каждый из которых возможно может быть замещен, как определено в данном документе.
"Гетероариалкил" или "гетероаралкил" означает группу формулы -R-R', где R представляет собой алкилен, и R' представляет собой гетероарил, как определено в данном документе.
"Гетероарилсульфонил" означает группу формулы -SO2-R, где R представляет собой гетероарил, как определено в данном документе.
"Гетероарилокси" означает группу формулы -O-R, где R представляет собой гетероарил, как определено в данном документе.
"Гетероаралкилокси" означает группу формулы -O-R-R'', где R представляет собой алкилен и R' представляет гетероарил, как определено в данном документе.
Термины "гало", "галоген" и "галид", которые могут быть употреблены взаимозаменяемо, относятся к заместителям фтор, хлор, бром или йод.
"Галоалкил" означает алкил, как определено в данном документе, в котором один или более водород замещен таким же или другим галогеном. Примеры галоалкилов включают -CH2Cl, -CH2CF3, -CH2CCl3, перфторалкил (например, -CF3) и т.п.
"Галоалкокси" означает группу формулы -OR, где R представляет собой галоалкильную группу, как определено в данном документе. Пример галоалкокси представляет собой дифторметокси.
"Гетероциклоамино" означает насыщенное кольцо, где по меньшей мере один атом кольца представляет собой N, NH или N-алкил и остальные атомы кольца формируют алкиленовую группу.
"Гетероциклил" означает одновалентную насыщенную группу, состоящую из одного или трех колец, включающих один, два, три или четыре гетероатома (выбранных из азота, кислорода или серы). Гетероциклильное кольцо возможно может быть замещено, как определено в данном документе. Примеры гетероциклильных групп включают, но не ограничены, возможно замещенный пиперидинил, пиперазинил, морфолинил, тиоморфолинил, азепинил, пирролидинил, азетидинил, тетрагидропиранил, тетрагидрофуранил, оксэтанил и т.п. Такой гетероциклил возможно может быть замещен, как определено в данном документе.
"Гетероциклилалкил" означает группу формулы -R-R', где R представляет собой алкилен и R' представляет собой гетероциклил, как определено в данном документе.
"Гетероциклилокси" означает группу формулы -OR, где R представляет собой гетероциклил, как определено в данном документе.
"Гетероциклилалкокси" означает группу формулы -OR-R'', где R представляет собой алкилен, и R' представляет собой гетероциклил, как определено в данном документе.
"Гетероциклилсульфонил" означает группу формулы -SO2-R, где R представляет собой гетероциклил, как определено в данном документе.
"Гидроксиалкокси" означает группу формулы -OR, где R представляет собой гидроксиалкил, как определено в данном документе.
"Гидроксиалкиламино" означает группу формулы -NR-R', где R представляет собой водород или алкил, и R' представляет собой гидроксиалкил, как определено в данном документе.
"Гидроксиалкиламиноалкил" означает группу формулы -R-NR'-R'', где R представляет собой алкилен, R' представляет собой водород или алкил и R'' представляет собой гидроксиалкил, как определено в данном документе.
"Гидроксикарбонилалкил" или "карбоксиалкил" означает группу формулы -R-(CO)-OH, где R представляет собой алкилен, как определено в данном документе.
"Гидроксикарбонилалкокси" означает группу формулы -O-R-C(O)-ОН, где R представляет собой алкилен, как определено в данном документе.
"Гидроксиалкилоксикарбонилалкил" или "гидроксиалкоксикарбонилалкил" означает группу формулы -R-C(O)-O-R-ОН, где каждый R представляет собой алкилен и может быть таким же или отличным.
"Гидроксиалкил" означает алкильную группу, как определено в данном документе, замещенную на одну или более, например на одну, две или три, гидрокси группы, при условии, что атомы углерода не несут более чем одной гидрокси группы. Типичные примеры включают, но не ограничены, гидроксиметил, 2-гидроксиэтил, 2-гидроксипропил, 3-гидроксипропил, 1-(гидроксиметил)-2-метилпропил, 2-гидроксибутил, 3-гидроксибутил, 4-гидроксибутил, 2,3-дигидроксипропил, 2-гидрокси-1-гидроксиметилэтил, 2,3-дигидроксибутил, 3,4-дигидроксибутил и 2-(гидроксиметил)-3-гидроксипропил.
"Гидроксициклоалкил" означает циклоалкильную группу, как определено в данном документе, где один, два или три атома водорода в циклоалкильном радикале замещены гидроксизаместителем. Типичные примеры включают, но не ограничены, 2-, 3- или 4-гидроксициклогексил и т.п.
"Алкоксигидроксиалкил" и "гидроксиалкоксиалкил", которые могут быть употреблены взаимозаменяемо, означают алкил, как определено в данном документе, замещенный по меньшей мере один раз гидрокси и по меньшей мере один раз алкокси. "Алкоксигидроксиалкил" и "гидроксиалкоксиалкил", таким образом, охватывают, например, 2-гидрокси-3-метокси-пропан-1-ил и т.п.
"Мочевина" или "уреидо" означает группу формулы -NR'-C(O)-NR''R''', где R', R'' и R''' каждый независимо представляет собой водород или алкил.
"Карбамат" означает группу формулы -O-C(O)-NR'R'', где R' и R'' независимо друг от друга представляют собой водород или алкил.
"Карбокси" означает группу формулы -O-С(O)-ОН.
"Сульфонамидо" означает группу формулы -SO2-NR'R'', где R', R'' и R''' независимо друг от друга представляют собой водород или алкил.
"Возможно замещенный" при употреблении в связи с "арильной", "фенильной", "гетероарильной" "циклоалкильной" или "гетероциклильной" группой означает, что такая группа может быть незамещенной (т.е. все валентности заняты атомом водорода) или замещенной конкретными группами, как указано в данном документе.
"Замещаемая группа" означает группу со значением, обычно связанным с синтетической органической химией, т.е. атом или группу, замещаемую при условиях реакции замещения. Примеры замещаемых групп включают, но не ограничены, галоген, алкан- или ариленсульфонилокси, такие как метансульфонилокси, этансульфонилокси, тиометил, бензенсульфонилокси, тозилокси и тиенилокси, дигалофосфиноилокси, возможно замещенный бензилокси, изопропилокси, ациклокси и т.п.
"Модулятор" означает молекулу, которая взаимодействует с мишенью. Взаимодействия включают, но не ограничены, агонистическое, антагонистическое и т.п. взаимодействие, как определено в данном документе.
"Возможный" или "возможно" означает, что последующее описанное действие или условие может не быть необходимым и что описание включает примеры, где действие или условие требуются и примеры, в которых они не требуются.
"Болезнь" и "болезненное состояние" означает любую болезнь, состояние, симптом, расстройство или признак.
"Инертный органически растворитель" или "инертный растворитель" означает растворитель, являющийся инертным при условиях реакции, описанных в связи с ним, включая, например, бензол, толуол, ацетонитрил, тетрагидрофуран, N,N-диметилформамид, хлороформ, метиленхлорид или дихлорметан, дихлорэтан, диэтиловый эфир, этилацетат, ацетон, метилэтилкетон, метанол, этанол, пропанол, изопропанол, трет-бутанол, диоксан, пиридин и т.п. Если не указано иное, растворители, применяемые в реакциях по настоящему изобретению, представляют собой инертные растворители.
"Фармацевтически приемлемый" означает такой, который полезен при получении фармацевтической композиции, являющейся безвредной, нетоксичной и не являющейся биологически или как-либо еще нежелательной, и включает то, что является приемлемым для применения в ветеринарии, а также в фармацевтике для человека.
"Фармацевтически приемлемые соли" соединений означает соли, являющиеся фармацевтически приемлемыми, как определено в данном документе, и обладающие желаемой фармакологической активностью исходного соединения.
Следует отметить, что все ссылки на фармацевтически приемлемые соли включают формы присоединения растворителя (сольваты) или кристаллические формы (полиморфы), как определено в данном документе, таких же солей присоединения кислоты.
"Защитная группа" или "блокирующая группа" означает группу, селективно блокирующую один реакционный центр в мультифункциональном соединении, так что химическая реакция может быть проведена селективно в другом незащищенном центре в значении, обычно связанном с синтетической химией. Конкретные способы по данному изобретению основаны на защитных группах, блокирующих атомы реактивного азота и/или кислорода, присутствующие в реагентах. Например, термин "аминозащитная группа" и "азотзащитная группа" употребляют взаимозаменяемо в данном документе и они относятся к защите атомов азота от нежелательных реакций в течение процессов синтеза. Примеры азотзащитных групп включают, но не ограничены, трифторацетил, ацетамидо, бензил (Bn), бензилоксикарбонил (карбобензилокси, CBZ), п-метоксибензилоксикарбонил, п-нитробензилоксикарбонил, трет-бутоксикарбонил (ВОС) и т.п. Специалисты в области техники будут знать, как выбрать группу для легкого удаления и для способности препятствования следующим реакциям.
"Сольваты" означает формы добавления растворителя, которые содержат или стехиометрические или нестехиометрические количества растворителя. Некоторые соединения имеют тенденцию захватывать фиксированное молярное отношение молекул растворителя в кристаллическое твердое состояние, таким образом, формируя сольват. В случае, когда растворитель представляет собой воду, образуемый сольват представляет собой гидрат, в случае, когда растворитель представляет собой спирт, образуемый сольват представляет собой алкоголят. Гидраты образуют посредством комбинации одной или более молекул воды с одним из веществ, в котором вода сохраняет свое молекулярное состояние в виде H2O, такая комбинация способна образовывать один или более гидрат.
"Болезнь Паркинсона" означает дегенеративное расстройство центральной нервной системы, которое нарушает двигательную активность, речь и/или когнитивную функцию. Симптомы болезни Паркинсона могут включать, например, мышечную ригидность, тремор, замедленность физической подвижности (брадикинезию) и утрату физической подвижности (акинезию).
"Болезнь с тельцами Леви". Также называемая "деменцией с тельцами Леви", болезнь диффузных телец Леви", болезнь кортикальных телец Леви", означает нейродегенеративное расстройство, анатомически характеризующееся присутствием телец Леви в мозге.
"Субъект" означает млекопитающее или немлекопитающее. Млекопитающие означает любого члена класса млекопитающих, включая, но не ограничено, человека; приматов, не являющихся человеком, таких как шимпанзе и других видов приматов и обезьян; сельскохозяйственных животных, таких как крупный рогатый скот, лошади, овцы, козы и свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, включая грызунов, таких как крысы, мыши и морские свинки и т.п. Примеры немлекопитающих животных включают, но не ограничены, птиц и т.п. Термин "субъект" не означает конкретного возраста или пола.
"Терапевтически эффективное количество" означает количество соединения, которого при введении субъекту для лечения болезненного состояния, достаточно для достижения эффекта такого лечения болезненного состояния. "Терапевтически эффективное количество" будет зависеть от соединения, болезненного состояния, подлежащего лечению, серьезности заболевания, подлежащего лечению, возраста и относительного здоровья субъекта, пути и формы введения, решения лечащего ветеринара или терапевта и других факторов.
Термины "таковые, определенные выше" и "таковые, определенные в данном документе" при употреблении в связи параметрами, включают за счет ссылок широкое определение параметров, а также конкретные определения, если необходимо.
"Лечение" или "лечение" болезненного состояния включает в том числе ингибирование состояния заболевания, т.е. остановку развития состояния заболевания или его клинических симптомов и/или облегчение состояния заболевания, т.е. вызывание временной или постоянной регрессии состояния заболевания или его клинических симптомов.
Термины "лечение", "контактирование" и "реагирование" при употреблении в связи с химической реакцией означают добавление или смешивание двух или более реагентов при соответствующих условиях для получения указанного и/или желаемого продукта. Следует учесть, что реакция, в результате которой получают указанный и/или желаемый продукт не обязательно происходит напрямую из двух реагентов, которые добавляют изначально, т.е. может быть один или более промежуточный продукт, получаемый в смеси, которая в конечном итоге приводит к образованию указанного и/или желаемого продукта.
"C1-6" в сочетании с любым другим термином в данном документе относится к диапазону от одного до шести атомов углерода, т.е. 1, 2, 3, 4, 5 или 6 атомам углерода, "С2-6" относится к диапазону от двух до шести атомов углерода, т.е. 2, 3, 4, 5 или 6 атомам углерода, "С3-6" относится к диапазону от трех до шести атомов углерода, т.е. 3, 4, 5 или 6 атомам углерода.
Номенклатура и структуры
Обычно номенклатура и химические названия, применяемые в данной заявке, основаны на ChembioOffice™ от CambridgeSoft™. Любая открытая валентность, оказывающаяся на атоме углерода, кислорода, серы или азота, означает присутствие атома водорода, если не указано иное. В случае, если азотсодержащее гетероарильное кольцо проявляет открытую валентность на атоме азота и переменные, такие как Ra, Rb или Rc, присутствуют на гетероарильном кольце, такие переменные могут быть связаны или соединены с азотом, имеющим открытую валентность. В случае если хиральный центр существует в структуре, но конкретная стереохимия не показана для хирального центра, оба энантиомера, ассоциированных с хиральным центром охвачены структурой. В случае если структура, показанная в данном документе, может существовать в виде множественных таутомерных форм, все такие таутомеры охвачены структурой. Атомы, представленные в структурах, в данном документе предназначены для схватывания всех природных изотопов таких атомов. Таким образом, например, атомы водорода, представленные в данном документе, предназначены для включения дейтерия и трития, и атомы углерода предназначены для включения изотопов С13 и С14.
Соединения по изобретению
Изобретение предлагает соединения формулы:
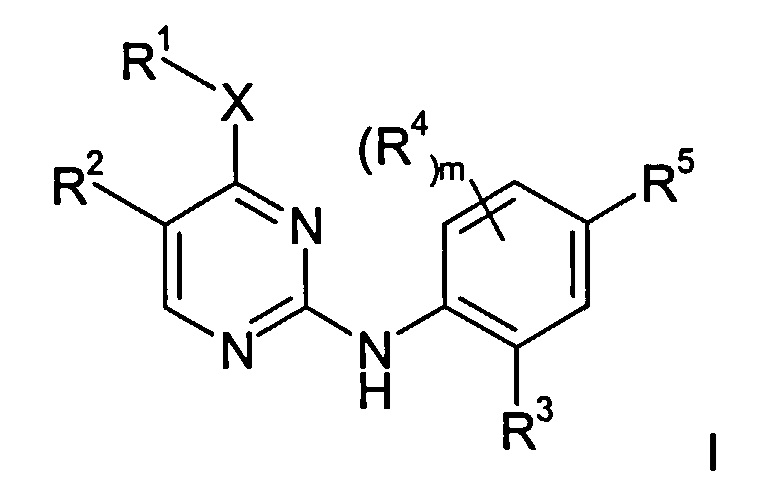
или их фармацевтически приемлемые соли,
где:
m составляет от 0 до 3;
Х представляет собой: -NRa-; -O-; или -S(O)r-, где r составляет от 0 до 2 и Ra представляет собой водород или С1-6-алкил;
R1 представляет собой: С1-6-алкил; С1-6-алкенил; C1-6-алкинил; гало-С1-6-алкил; С1-6-алкокси-С1-6алкил; гидрокси-С1-6-алкил; амино-С1-6-алкил; С1-6-алкилсульфонил-С1-6-алкил; С3-6-циклоалкил, возможно замещенный С1-6-алкилом; С3-6-циклоалкил-С1-6-алкил, где часть С3-6-циклоалкил возможно замещена C1-6-алкилом; тетрагидрофуранил; тетрагидрофуранил-С1-6-алкил; оксэтанил; или оксэтан-С1-6-алкил;
или R1 и Ra вместе с атомами, к которым они прикреплены, могут образовывать трех-шестичленное кольцо, которое возможно может включать дополнительный гетероатом, выбранный из О, N и S, и которое замещено оксо, гало или Ci-6-алкилом;
R2 представляет собой: гало; С1-6-алкокси; циано; С1-6-алкинил; С1-6-алкенил; гало-С1-6-алкил; гало-С1-6-алкокси; С3-6-циклоалкил, где часть С3-6-циклоалкил возможно замещена С1-6-алкилом; С3-6-циклоалкил-С1-6-алкил, где часть С3-6-циклоалкил возможно замещена С1-6-алкилом; тетрагидрофуранил; тетрагидрофуранил-С1-6-алкил; ацетил; оксэтанил; или оксэтан-С1-6-алкил;
R3 и R4 независимо друг от друга представляют собой: гало; С1-6-алкил; С1-6-алкокси; С3-6-циклоалкилокси; гало-С1-6-алкил; или гало-С1-6-алкокси;
или R3 и R4 вместе с атомами, к которым они прикреплены, могут образовывать пяти- или шестичленное кольцо, возможно включающее один или два гетероатома, каждый независимо выбранный из О, N и S, кольцо возможно замещено один или более раз R6;
R5 представляет собой: С1-6-алкил-сульфонил; С3-6-циклоалкилсульфонил; С3-6-циклоалкил-С1-6-алкилсульфонил; циано; циано-С1-6-алкил; гетероциклил, возможно замещенный один или более раз R6; гетероциклил-С1-6-алкил, где гетероциклильная группа возможно замещена один или более раз R6; гало-С1-6-алкил; гетероциклил-сульфонил, где гетероциклильная группа возможно замещена один или более раз R6; или карбокси; и
R6 представляет собой: С1-6-алкил; гало; гало-С1-6-алкил; или оксо.
В конкретных воплощениях формулы I,
m составляет от 0 до 1;
Х представляет собой: -NH- или -O-;
R1 представляет собой: С1-6-алкил;
R2 представляет собой: гало; циано или гало-С1-6-алкил;
R3 и R4 независимо друг от друга представляют собой: гало; С1-6-алкил или С1-6-алкокси;
R5 представляет собой: С1-6-алкил-сульфонил; циано; гетероциклил, возможно замещенный один или более раз R6; гетероциклил-С1-6-алкил, где гетероциклильная группа возможно замещена один или более раз R6; гало-С1-6-алкил; гетероциклил-сульфонил, где гетероциклильная группа возможно замещена один или более раз R6; или карбокси; и
R6 представляет собой: оксо.
В конкретных воплощениях формулы I, R1 и Ra вместе с атомами, к которым они прикреплены, могут образовывать трех-шестичленное кольцо, которое возможно может включать дополнительный гетероатом, выбранный из О, N и S, и которое возможно может быть замещено оксо, гало или С1-6-алкилом.
В конкретных воплощениях формулы I, R1 и Ra вместе с атомами, к которым они прикреплены, образуют пяти- или шестичленное кольцо.
В конкретных воплощениях формулы I, R1 и Ra вместе с атомами, к которым они прикреплены, образуют пиролидиниловую, пиперидиниловую или оксазоладиноиловую группу.
В конкретных воплощениях формулы I, R2 представляет собой ацетил.
В конкретных воплощениях формулы I, в случае, когда R1 представляет собой циклопропил, циклобутил, циклопропил-С1-6-алкил или циклобутил-С1-6-алкил, Х представляет собой -O-.
В конкретных воплощениях формулы I, m составляет от 0 до 2.
В конкретных воплощениях формулы I, m составляет 0 или 1.
В конкретных воплощениях формулы I, m составляет 0.
В конкретных воплощениях формулы I, m составляет 1.
В конкретных воплощениях формулы I, r составляет 0.
В конкретных воплощениях формулы I, r составляет 2.
В конкретных воплощениях формулы I, X составляет -NRa- или -O-.
В конкретных воплощениях формулы I, X составляет -NRa.
В конкретных воплощениях формулы I, X составляет -O-.
В конкретных воплощениях формулы I, X составляет -S(O)n-.
В конкретных воплощениях формулы I, X составляет -NH- или -O-.
В конкретных воплощениях формулы I, Ra представляет собой водород.
В конкретных воплощениях формулы I, Ra представляет собой C1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой: C1-6-алкил; гало-С1-6-алкил; С1-6-алкокси-С1-6-алкил; амино-С1-6алкил; C1-6-алкилсульфонил-С1-6-алкил; С3-6циклоалкил; или С3-6циклоалкил-С1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой: C1-6-алкил; С3-6-циклоалкил, возможно замещенный С1-6-алкилом; или С3-6-циклоалкил-С1-6-алкил, где часть С3-6-циклоалкил возможно замещена C1-6-алкилом.
В конкретных воплощениях формулы I, R1 представляет собой: C1-6-алкил; гало-С1-6-алкил; С1-6-алкокси-С1-6-алкил; амино-С1-6-алкил; C1-6-алкилсульфонил-С1-6-алкил; тетрагидрофуранил; тетрагидрофуранил-C1-6-алкил; оксэтанил; или оксэтан-С1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой: C1-6-алкил; гало-С1-6-алкил; С1-6-алкокси-С1-6-алкил; амино-С1-6-алкил; или C1-6-алкилсульфонил-С1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой C1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой гало-C1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой C1-6-алкокси-С1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой амино-С1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой C1-6-алкилсульфонил-С1-6-алкил, возможно замещенный C1-6-алкилом.
В конкретных воплощениях формулы I, R1 представляет собой С3-6-циклоалкил, возможно замещенный С1-6-алкилом.
В конкретных воплощениях формулы I, R1 представляет собой С3-6-циклоалкил-С1-6-алкил, где часть С3-6-циклоалкил возможно замещена C1-6-алкилом.
В конкретных воплощениях формулы I, R1 представляет собой тетрагидрофуранил.
В конкретных воплощениях формулы I, R1 представляет собой тетрагидрофуранил-С1-6-алкил; оксэтанил.
В конкретных воплощениях формулы I, R1 представляет собой оксэтан-С1-6-алкил.
В конкретных воплощениях формулы I, R1 представляет собой: метил; этил; н-пропил; изопропил; изобутил; 3,3-диметилпропил; циклопропил; циклобутил; циклопентил; циклогексил; циклопропилметил; циклобутилметил; циклопентилметил; циклопропилэтил; метоксиэтил; оксэтанил; или тетрагидрофуранилметил.
В конкретных воплощениях формулы I, R1 представляет собой: метил; этил; н-пропил; изопропил; изобутил; 3,3-диметилпропил; циклопентил; циклогексил; циклопропилметил; циклобутилметил; циклопентилметил; циклопропилэтил; метоксиэтил; оксэтанил; или тетрагидрофуранилметил.
В конкретных воплощениях формулы I, R1 представляет собой: метил; этил; н-пропил; изопропил; изобутил; 3,3-диметилпропил; циклопентил; циклогексил; циклопентилметил; метоксиэтил; оксэтанил или тетрагидрофуранилметил.
В конкретных воплощениях формулы I, R1 представляет собой: метил; этил; н-пропил; изопропил или изобутил.
В конкретных воплощениях формулы I, R1 представляет собой метил.
В конкретных воплощениях формулы I, R1 представляет собой метил.
В конкретных воплощениях формулы I, R1 представляет собой этил.
В конкретных воплощениях формулы I, R1 представляет собой: циклопропил; циклобутил; циклопентил; циклогексил; циклопропилметил; циклобутилметил; циклопентилметил; или циклопропилэтил.
В конкретных воплощениях формулы I, R1 представляет собой: циклопентил; циклогексил; или циклопентилметил.
В конкретных воплощениях формулы I, R2 представляет собой: гало; C1-6-алкокси; гало-С1-6-алкил; гало-С1-6-алкокси; С3-6-циклоалкил, где часть С3-6-циклоалкил возможно замещена С1-6-алкилом; С3-6-циклоалкил-С1-6-алкил, где часть С3-6-циклоалкил возможно замещена С1-6-алкилом; тетрагидрофуранил; тетрагидрофуранил-С1-6-алкил; оксэтанил; или оксэтан-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой: гало; С1-6-алкокси; гало-С1-6-алкил; циано; С1-6-алкинил; С1-6-алкенил; С3-6-циклоалкил; или С3-6-циклоалкил-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой: гало; С1-6-алкокси; гало-С1-6-алкил; циано; С3-6-циклоалкил; или С3-6-циклоалкил-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой: гало; С1-6-алкокси; гало-С1-6-алкил; С3-6-циклоалкил; или С3-6-циклоалкил-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой: гало; гало-С1-6-алкил; или циано.
В конкретных воплощениях формулы I, R2 представляет собой: гало; или гало-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой гало.
В конкретных воплощениях формулы I, R2 представляет собой C1-6-алкокси.
В конкретных воплощениях формулы I, R2 представляет собой гало-С1-6-алкокси.
В конкретных воплощениях формулы I, R2 представляет собой гало-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой С3-6-циклоалкил.
В конкретных воплощениях формулы I, R2 представляет собой С3-6-циклоалкил-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой тетрагидрофуранил.
В конкретных воплощениях формулы I, R2 представляет собой тетрагидрофуранил-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой оксэтанил.
В конкретных воплощениях формулы I, R2 представляет собой оксэтан-С1-6-алкил.
В конкретных воплощениях формулы I, R2 представляет собой гало, трифторметил или циано.
В конкретных воплощениях формулы I, R2 представляет собой хлор, трифторметил или циано.
В конкретных воплощениях формулы I, R2 представляет собой хлор или трифторметил.
В конкретных воплощениях формулы I, R2 представляет собой фтор, хлор или бром.
В конкретных воплощениях формулы I, R2 представляет собой хлор.
В конкретных воплощениях формулы I, R2 представляет собой фтор.
В конкретных воплощениях формулы I, R2 представляет собой бром.
В конкретных воплощениях формулы I, R2 представляет собой трифторметил.
В конкретных воплощениях формулы I, R2 представляет собой метокси.
В конкретных воплощениях формулы I, R2 представляет собой циано.
В конкретных воплощениях формулы I, R2 представляет собой C1-6-алкинил.
В конкретных воплощениях формулы I, R2 представляет собой C1-6-алкенил.
В конкретных воплощениях формулы I, R3 представляет собой: C1-6-алкил.
В конкретных воплощениях формулы I, R3 представляет собой гало.
В конкретных воплощениях формулы I, R3 представляет собой C1-6-алкил.
В конкретных воплощениях формулы I, R3 представляет собой C1-6-алкокси.
В конкретных воплощениях формулы I, R3 представляет собой гало или C1-6-алкокси.
В конкретных воплощениях формулы I, R3 представляет собой С3-6-циклоалкилокси.
В конкретных воплощениях формулы I, R3 представляет собой гало-С1-6-алкил.
В конкретных воплощениях формулы I, R3 представляет собой гало-С1-6-алкокси.
В конкретных воплощениях формулы I, R3 представляет собой гало или метокси.
В конкретных воплощениях формулы I, R3 представляет собой фтор, хлор или метокси.
В конкретных воплощениях формулы I, R3 представляет собой фтор или хлор.
В конкретных воплощениях формулы I, R3 представляет собой метокси.
В конкретных воплощениях формулы I, R3 представляет собой метил.
В конкретных воплощениях формулы I, R3 представляет собой хлор.
В конкретных воплощениях формулы I, R3 представляет собой фтор.
В конкретных воплощениях формулы I, R4 представляет собой: C1-6-алкил.
В конкретных воплощениях формулы I, R4 представляет собой гало.
В конкретных воплощениях формулы I, R4 представляет собой C1-6-алкил.
В конкретных воплощениях формулы I, R4 представляет собой C1-6-алкокси.
В конкретных воплощениях формулы I, R4 представляет собой гало-C1-6-алкил.
В конкретных воплощениях формулы I, R4 представляет собой гало-С1-6-алкокси.
В конкретных воплощениях формулы I, R4 представляет собой гало или метокси.
В конкретных воплощениях формулы I, R4 представляет собой фтор, хлор, метил или метокси.
В конкретных воплощениях формулы I, R4 представляет собой фтор, хлор или метокси.
В конкретных воплощениях формулы I, R4 представляет собой фтор или хлор.
В конкретных воплощениях формулы I, R4 представляет собой метокси.
В конкретных воплощениях формулы I, R4 представляет собой метил.
В конкретных воплощениях формулы I, R4 представляет собой хлор.
В конкретных воплощениях формулы I, R4 представляет собой фтор.
В конкретных воплощениях формулы I, R4 представляет собой С3-6-циклоалкилокси.
В конкретных воплощениях формулы I, R3 и R4 вместе с атомами, к которым они прикреплены, образуют пяти- или шестичленное кольцо, возможно включающее один или два гетероатома, независимо выбранных из О, N и S, кольцо возможно замещено один или более раз R6.
В конкретных воплощениях формулы I, R3 и R4 вместе с атомами, к которым они прикреплены, образуют шестичленное кольцо, которое включает два атома кислорода, разделенных этильной группой (т.е. R3 и R4 вместе образуют этилен-диокси группу).
В конкретных воплощениях формулы I, R3 и R4 вместе с атомами, к которым они прикреплены, образуют пятичленное кольцо, включающее два атома кислорода, разделенных метильной группой (т.е. R3 и R4 вместе образуют метилен-диокси группу).
В конкретных воплощениях формулы I, R5 представляет собой C1-6-алкил-сульфонил.
В конкретных воплощениях формулы I, R5 представляет собой C1-6-алкил-сульфонил или циано.
В конкретных воплощениях формулы I, R5 представляет собой С3-6-циклоалкил-сульфонил.
В конкретных воплощениях формулы I, R5 представляет собой циано.
В конкретных воплощениях формулы I, R5 представляет собой циано-С1-6-алкил.
В конкретных воплощениях формулы I, R5 представляет собой гетероциклил, возможно замещенный R6.
В конкретных воплощениях формулы I, R5 представляет собой гетероциклил-С1-6-алкил, где гетероциклильная группа возможно замещена R6.
В конкретных воплощениях формулы I, R5 представляет собой гало-С1-6-алкил.
В конкретных воплощениях формулы I, R5 представляет собой карбокси.
В конкретных воплощениях формулы I, R5 представляет собой метансульфонил.
В конкретных воплощениях формулы I, R5 представляет собой морфолин-4-ил-метил.
В конкретных воплощениях формулы I, R5 представляет собой морфолинил.
В конкретных воплощениях формулы I, R5 представляет собой морфолин-4-ил.
В конкретных воплощениях формулы I, R5 представляет собой оксэтанил.
В конкретных воплощениях формулы I, R5 представляет собой оксэтан-3-ил.
В конкретных воплощениях формулы I, R5 представляет собой пирролидинонил.
В конкретных воплощениях формулы I, R5 представляет собой пирролидин-2-он-1-ил.
В конкретных воплощениях формулы I, R5 представляет собой морфолинонил.
В конкретных воплощениях формулы I, R5 представляет собой морфолин-3-он-4-ил.
В конкретных воплощениях формулы I, R5 представляет собой пиперидинонил.
В конкретных воплощениях формулы I, R5 представляет собой пиперидин-2-он-1-ил.
В конкретных воплощениях формулы I, R5 представляет собой трифторметил.
В конкретных воплощениях формулы I, R5 представляет собой гетероциклил-сульфонил, где гетероциклильная группа возможно замещена один или более раз R6.
В конкретных воплощениях формулы I, R5 представляет собой морфолин-4-сульфонил.
В конкретных воплощениях формулы I, R5 представляет собой морфолин-сульфонил.
В воплощениях по изобретению, где R5 представляет собой гетероциклил или содержит гетероциклильную группу, такой гетероциклил может представлять собой азепинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, тетрагидрофуранил, пирролидинил, тетрагидрофуранил, азетидинил или оксэтанил, каждый возможно замещенный один или более раз R6.
В воплощениях по изобретению, где R5 представляет собой гетероциклил или содержит гетероциклильную группу, такой гетероциклил может представлять собой пиперидинил, пиперазинил, морфолинил, тиоморфолинил, тетрагидрофуранил, оксэтанил, азетидинил, азепенил, оксазепенил, или пирролидинил, каждый возможно замещенный один или более раз R6.
В воплощениях по изобретению, где R5 представляет собой гетероциклил или содержит гетероциклильную группу, такой гетероциклил может представлять собой пиперидинил, пиперазинил, морфолинил, тиоморфолинил или пирролидинил, каждый независимо замещенный один или более раз R6.
В конкретных воплощениях формулы I, R5 представляет собой: метансульфонил; циано; морфолин-4-ил-метил; морфолин-4-ил; морфолин-4-ил-сульфонил; или трифторметил.
В конкретных воплощениях формулы I, R5 представляет собой: метансульфонил; циано; или морфолин-4-ил-метил.
В конкретных воплощениях формулы I, R5 представляет собой: метансульфонил; или циано.
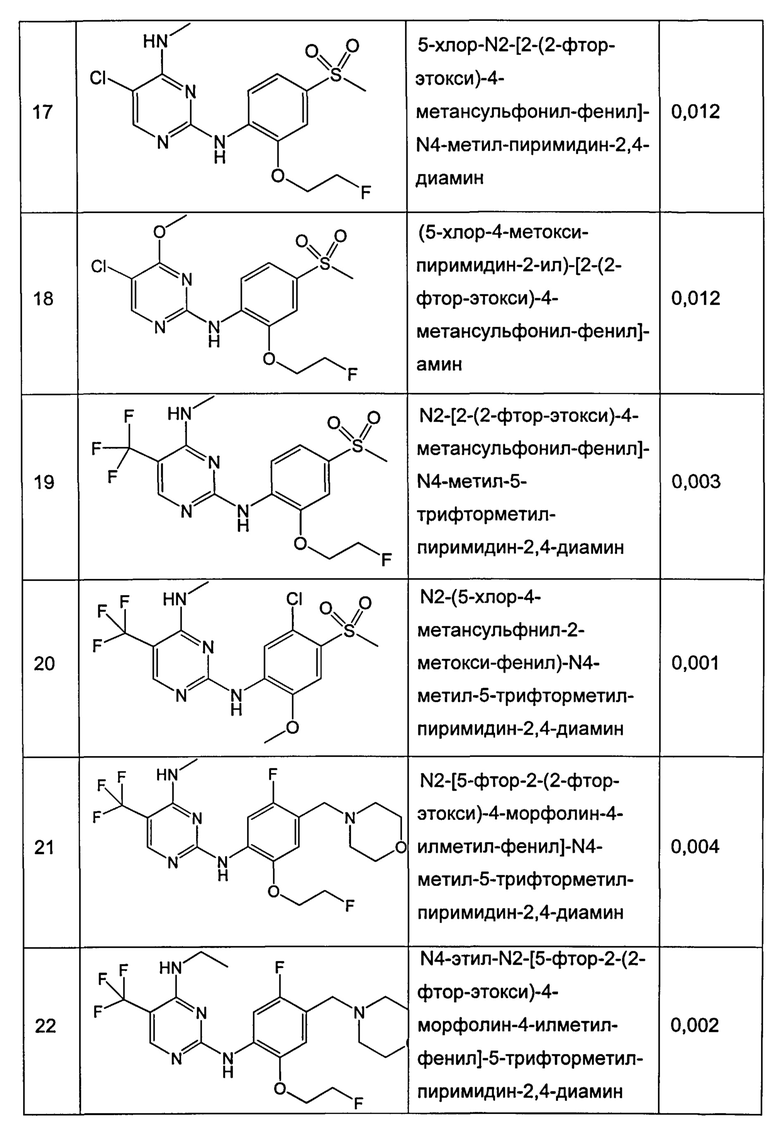
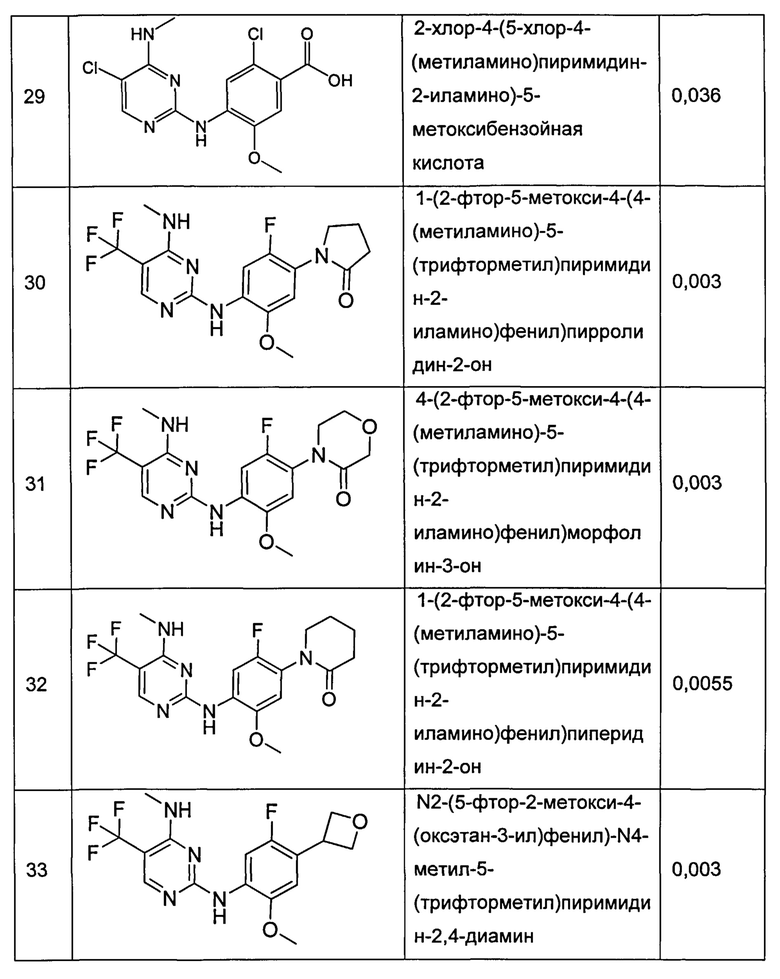
В конкретных воплощениях формулы I, соединение выбрано из группы, состоящей из:
N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин, 5-хлор-N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метилпиримидин-2,4-диамин, 2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрил, 3-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрил, 4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-3-метоксибензонитрил, (2-хлор-4-метансульфонил-фенил)-(5-хлор-4-метокси-пиримидин-2-ил)-амин, N2-(2-хлор-4-метансульфонил-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин, 5-хлор-N2-(2-хлор-4-метансульфонил-фенил)-N4-метил-пиримидин-2,4-диамин, N2-(2-метокси-4-морфолин-4-илметил-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин, 5-хлор-2-метил-4-(4-метиламино-5-трифторметил-пиримидин-2-иламино)-бензонитрил, 2-(5-фтор-2-метокси-4-морфолин-4-илметил-фениламино)-4-метиламино-пиримидин-5-карбонитрил, 4-этиламино-2-(5-фтор-2-метокси-4-морфолин-4-илметил-фениламино)-пиримидин-5-карбонитрил, 5-метокси-2-метил-4-(4-метиламино-5-трифторметил-пиримидин-2-иламино)-бензонитрил, 5-хлор-N2-[2-(2-фтор-этокси)-4-морфолин-4-илметил-фенил]-N4-метил-пиримидин-2,4-диамин, N2-(5-фтор-4-метансульфонил-2-метокси-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин, N2-(2-изопропокси-4-метансульфонил-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин, 5-хлор-N2-[2-(2-фтор-этокси)-4-метансульфонил-фенил]-N4-метил-пиримидин-2,4-диамин, (5-хлор-4-метокси-пиримидин-2-ил)-[2-(2-фтор-этокси)-4-метансульфонил-фенил]-амин, N2-[2-(2-фтор-этокси)-4-метансульфонил-фенил]-N4-метил-5-трифторметил-пиримидин-2,4-диамин, N2-(5-хлор-4-метансульфонил-2-метокси-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин, N2-[5-фтор-2-(2-фтор-этокси)-4-морфолин-4-илметил-фенил]-N4-метил-5-трифторметил-пиримидин-2,4-диамин, N4-этил-N2-[5-фтор-2-(2-фтор-этокси)-4-морфолин-4-илметил-фенил]-5-трифторметил-пиримидин-2,4-диамин, N2-(4-метансульфонил1-2-метокси-5-метил-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин, 5-хлор-N2-(2-метокси-4-морфолинофенил)-N4-метилпиримидин-2,4-диамин, 4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-3-метоксибензойная кислота, N2-(2-метокси-4-(морфолинсульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин, N2-(2-метокси-4-(трифторметил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин, 5-хлор-N2-(2-метокси-4-(трифторметил)фенил)-N4-метилпиримидин-2,4-диамин, 2-хлор-4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-5-метоксибензойная кислота, 1-(2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)фенил)пирролидин-2-он, 4-(2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)фенил)морфолин-3-он, 1-(2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)фенил)пиперидин-2-он, N2-(5-фтор-2-метокси-4-(оксэтан-3-ил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин, N4-этил-N2-(2-метокси-5-метил-4-(метилсульфонил)фенил)-5-(трифторметил)пиримидин-2,4-диамин, N2-(4-(этилсульфонил)-2-метокси-5-метилфенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин, N2-(2-метокси-5-метил-4-(метилсульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин, N2-(5-фтор-2-метокси-4-(морфолинометил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин и N4-этил-N2-(8-(метилсульфонил)-2,3-дигидробензо[b][1,4]диоксин-5-ил)-5-(трифторметил)пиримидин-2,4-диамин.
В случае когда R1, R2, R3, R4 и R5, представляет собой алкил или содержит алкильную группу, такой алкил может представлять собой низший алкил, т.е. С1-С6-алкил и во многих воплощениях может представлять собой С1-С4-алкил.
Изобретение также относится к композиции, содержащей: фармацевтически приемлемый носитель и соединение, как описано в данном документе.
Изобретение также относится к способу лечения болезни Паркинсона, предусматривающему введение субъекту, нуждающемуся в этом, эффективного количества соединения, как описано в данном документе.
Изобретение также относится к соединению формулы I, как описано в данном документе, для применения в целях предупреждения или лечения болезни Паркинсона.
Изобретение также относится к фармацевтической композиции, как описано в данном документе, где композиция полезна для предупреждения или лечения болезни Паркинсона.
Изобретение также относится к соединению формулы I, как описано в данном документе, для получения лекарственного препарата для предупреждения или лечения болезни Паркинсона.
Изобретение также предлагает способ лечения заболевания или состояния, опосредованного или иным образом связанного с рецептором LRRK2, способ, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества соединения по изобретению.
Заболевание может представлять собой нейродегенеративное заболевание, такое как болезнь Паркинсона, болезнь Хантингтона или деменция с тельцами Леви.
Заболевание может представлять собой расстройство ЦНС, такое как болезнь Альцгеймера и дискинезия, индуцированная L-дигидроксифенилаланином.
Заболевание может представлять собой рак или пролиферативное расстройство, такое как рак почек, молочных желез, простаты, крови, папиллярный или легочный рак, острую миелоидный лейкоз или множественную миелому.
Заболевание может представлять собой воспалительное заболевание, такое как проказа, болезнь Крона, амиотрофический боковой склероз, ревматоидный артрит и анкилозирующий спондилит.
Изобретение также предлагает способ улучшения когнитивной памяти, способ, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества соединения по изобретению.
Репрезентативные соединения в соответствии со способами по изобретению показаны в экспериментальных примерах, приведенных ниже.
Синтез
Соединения по настоящему изобретению могут быть получены при помощи ряда способов, изображенных на иллюстративных схемах реакции синтеза, приведенных и описанных ниже.
Исходные материалы и реагенты, применяемые при получении данных соединений обычно или доступны от коммерческих поставщиков, таких как Aldrich Chemical Co., или могут быть получены при помощи способов, хорошо известных специалистам в области техники, следующих способов, указанных в ссылках, таких как Fieser and Fieser's Reagents for Organic Synthesis; Wiley & Sons: New York, 1991, Volumes 1-15; Rodd's Chemistry of Carbon Compounds, Elsevier Science Publishers, 1989, Volumes 1-5 and Supplementals; and Organic Reactions, Wiley & Sons: New York, 1991, Volumes 1-40. Следующие схемы реакции синтеза являются лишь иллюстрацией некоторых способов, при помощи которых могут быть синтезированы соединения по изобретению, могут быть сделаны различные модификации данных схем реакции синтеза и специалисты в области техники подтвердят, что данные модификации предусмотрены раскрытием данной заявки.
Исходные материалы и промежуточные продукты схем реакции синтеза могут быть выделены и очищены при желании при помощи обычных техник, включая, но не ограниченно, фильтрование, дистилляцию, кристаллизацию, хроматографию и т.п. Такие материалы могут быть охарактеризованы при помощи обычных средств, включая физические константны и спектральные данные.
Если не указано иное, реакции, описанные в данном документе, могут быть проведены в условиях инертной атмосферы, при атмосферном давлении и температуре реакции в диапазоне от приблизительно -78°С до приблизительно 150°С, например от приблизительно 0°С до приблизительно 125°С, или просто при приблизительно комнатной температуре (или окружающей среды), например приблизительно 20°С.
Схема А, приведенная ниже, иллюстрирует один способ синтеза, применяемый для получения конкретных соединений формулы I или формулы II, где X, m, R1, R2, R3, R4 и R5 представляют собой таковые, определенные в данном документе.

На этапе 1 схемы А дихлорпиримидин (соединение а) реагирует с реагентом b с образованием соединения с. Реакция этапа 1 может протекать в условиях полярного растворителя. В воплощениях изобретения, где Х представляет собой -О- (т.е. реагент b представляет собой спирт), реакция этапа 1 может быть проведена в присутствии основания.
На этапе 2 пиримидин (соединение с} реагирует с анилином (соединение d) для получения фениламинопиридина (соединение формулы I) в соответствии с изобретением. Реакция этапа 2 может протекать в полярном протонном растворителе и в присутствии кислоты, такой как HCl. Многие анилины (соединение d) коммерчески доступны и могут быть легко получены из нитробензолов, как показано в примерах, приведенных ниже.
Многие варианты способа схемы А возможны и подтверждены специалистами в области техники. Конкретные детали получения соединений по изобретению описаны в примерах, приведенных ниже.
Введение и фармацевтическая композиция
Изобретение включает фармацевтические композиции, содержащие по меньшей мере одно соединение по настоящему изобретению или отдельный изомер, рацемическую или нерацемическую смесь изомеров или его фармацевтически приемлемую соль или сольват, вместе с по меньшей мере одним фармацевтически приемлемым носителем и возможно другими терапевтическими и/или профилактическими ингредиентами.
Обычно соединения по изобретению вводят в терапевтически эффективном количестве при помощи любого из приемлемых способов введения агентов, служащих сходным целям. Приемлемый диапазон дозирования обычно составляет 1-500 мг ежедневно, например 1-100 мг ежедневно, и наиболее предпочтительно 1-30 мг ежедневно, в зависимости от множества факторов, таких как серьезность заболевания, подлежащего лечению, возраст и относительное здоровье субъекта, эффективность применяемого соединения, путь и форма введения, показания, согласно которым назначают введение, и предпочтения и опыт лечащего врача. Специалисты в области лечения таких заболеваний будут способны без лишних экспериментов и на основании собственных знаний и раскрытия данной заявки, установить терапевтически эффективное количество соединений по настоящему изобретению для данного заболевания.
Соединения по изобретению могут быть введены в качестве фармацевтических препаратов, включающих таковые приемлемые для орального (включая буккальный и сублингвальный), ректальный, назальный, местный, пульмонарный, вагинальный или парентеральный (включая внутримышечный, внутриартериальный, интратекальный, подкожный и внутривенный) пути введения или в форме, приемлемой для введения посредством ингаляции или инсуффляции. Конкретным способом введения является оральный с обычным ежедневным режимом дозирования, который может быть применен согласно степени заболевания.
Соединение или соединения по изобретению вместе с одним или более обычных адъювантов, носителей или разбавителей, могут быть помещены в форму фармацевтических композиций и единичных дозированных форм. Фармацевтические композиции и единичные дозированные формы могут состоять из обычных ингредиентов в обычных пропорциях, с или без дополнительных активных соединений или принципов, и единичные дозированные формы могут содержать любое приемлемое эффективное количество активного ингредиента, пропорциональное ежедневному диапазону дозирования, назначенному к применению. Фармацевтические композиции могут быть применены в виде твердых веществ, таких как таблетки или наполненные капсулы, полутвердых веществ, порошков, препаратов замедленного высвобождения или жидкостей, таких как растворы, суспензии, эмульсии, эликсиры или наполненные капсулы для орального применения; или в виде свечей для ректального или вагинального введения; или в виде стерильных инъецируемых растворов для парентерального применения. Препараты, содержащие приблизительно один (1) миллиграмм активного ингредиента или, ориентировочно, от приблизительно 0,01 до приблизительно ста (100) миллиграмм, на таблетку, являются приемлемыми единичными дозированными формами.
Соединения по изобретению могут быть получены в виде большого разнообразия дозированных форм для перорального введения. Фармацевтические композиции и дозированные формы могут содержать соединение или соединения по настоящему изобретению или его фармацевтически приемлемые соли в качестве активного компонента. Фармацевтически приемлемые носители могут быть или в виде твердого вещества или в виде жидкости. Твердые формы препаратов включают порошки, таблетки, капсулы, крахмальные капсулы, свечи и диспергируемые гранулы. Твердый носитель может представлять собой одно или более веществ, которые также могут действовать в качестве разбавителей, ароматизаторов, солюбилизаторов, лубрикантов, суспендирующих агентов, связывающих веществ, консервантов, веществ для улучшения распадаемости таблеток или инкапсулирующий материал. В порошках носитель обычно представляет собой окончательно отделенное твердое вещество, являющееся смесью с окончательно отделенным активным компонентом. В таблетках активный компонент обычно смешан с носителем, обладающим необходимой связующей способностью в приемлемых пропорциях и уплотненный до желаемой формы и размера. Порошки и таблетки могут содержать от приблизительно одного (1) до приблизительно семидесяти (70) процентов активного соединения. Приемлемые носители включают, но не ограничены, карбонат магния, стеарат магния, тальк, сахар, лактозу, пектин, декстрин, крахмал, желатин, трагакант, метилцеллюлозу, натрий-карбоксиметилцелюлозу, низкоплавкие воска, масло какао и т.п. Термин «препарат» предназначен для включения препарата активного соединения с инкапсулирующим материалом в качестве носителя, обеспечивающем капсулу, в которой активный компонент с или без носителей, окружен носителем, находящимся в ассоциации с ним. Аналогично, включены крахмальные капсулы и пастилки для рассасывания. Таблетки, порошки, капсулы, пилюли, крахмальные капсулы и пастилки для рассасывания могут быть в виде твердых форм, приемлемых для перорального введения.
Другие формы, приемлемые для перорального введения, включают жидкие формы препаратов, включая эмульсии, сиропы, эликсиры, водные растворы, водные суспензии или твердые формы препаратов, которые предназначены для быстрого превращения в жидкие формы препаратов перед применением. Эмульсии могут быть получены в виде растворов, например в виде водных растворов пропиленгликоля или могут содержать эмульгирующие агенты, например, такие как лецитин, сорбитан моноолеат или акацию. Водные растворы могут быть получены за счет растворения активного компонента в воде и добавления приемлемых красителей, ароматизаторов, стабилизаторов и загустителей. Водные суспензии могут быть получены посредством диспергирования окончательно отделенного активного компонента в воде с вязким материалом, таким как естественные или синтетические камеди, смолы, метилцеллюлоза, натрий карбоксиметилцеллюлоза, и другие хорошо известные суспендирующие агенты. Твердые формы препаратов включают растворы, суспензии и эмульсии и могут содержать в дополнение к активному компоненту красители, ароматизаторы, стабилизаторы, буферы, искусственные и натуральные подсластители, дисперсанты, загустители, солюбилизаторы и т.п.
Соединения по изобретению могут быть получены для парентерального введения (например, посредством инъекции, например, болюсной инъекции или продолжительной инфузии) и могут быть представлены в единичной дозированной форме в ампулах, наполненных шприцах, инфузиях небольшого объема или многодозовых контейнерах с добавленным консервантом. Композиции могут быть в виде суспензий, растворов или эмульсий в масляной или водной среде растворения, например растворы в водном полиэтиленгликоле. Примеры масляных или неводных носителей, разбавителей, растворителей или сред растворения включают пропиленгликоль, полиэтиленгликоль, растительные масла (например, оливковое масло), и инъецируемые органические эфиры (например, этилолеат), и могут содержать вспомогательные вещества, такие как консерванты, увлажнители, эмульгаторы или суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может быть в виде порошка, полученного при помощи асептического выделения стерильного твердого вещества или при помощи лиофилизации из раствора для разбавления перед применением при помощи приемлемой среды растворения, например стерильной апирогенной воды.
Соединения по изобретению могут быть получены для местного введения в эпидермис в качестве мазей, кремов или лосьонов или в качестве трансдермального пластыря. Мази и кремы могут, например, быть получены при помощи водной или масляной основы с добавлением приемлемых загустителей и/или гелеобразующих агентов. Лосьоны могут быть получены при помощи водной или масляной основы и обычно также будут содержать один или более эмульгаторов, загустителей или красителей. Препараты приемлемые для местного введения в рот включают пастилки для рассасывания, содержащие активные агенты во вкусовой основе, обычно сахарозе и акации или трагаканте; пастилки, содержащие активный ингредиент в инертной основе, такой как желатин и глицерин или сахарозе и акации; и ополаскиватели для рта, содержащие активный ингредиент в приемлемом жидком носителе.
Соединения по изобретению могут быть получены для введения в виде свечей. Сначала расплавляют низкоплавкие воска, такие как смесь глицеридов жирных кислот или какао-масла и активный компонент диспергируют, например, при помощи перемешивания. Расплавленную гомогенную смесь затем выливают в формы соответствующего размера, дают остыть и затвердеть.
Соединения по изобретению могут быть получены для вагинального введения. Этому будут соответствовать пессарии, тампоны, кремы, гели, пасты, пены или спреи, содержащие в дополнение к активному ингредиенту такие носители, и хорошо известные в области техники.
Заявленные соединения могут быть получены для назального введения. Растворы или суспензии применяют непосредственно в носовой полости при помощи обычных средств, например при помощи капельного дозатора, пипетки или спрея. Препараты могут быть представлены в однодозовой или многодозовой форме. В последнем случае капельного дозатора или пипетки это может быть достигнуто за счет введения пациентом соответствующего предварительно определенного объема раствора или суспензии. В случае спрея это может быть достигнуто, например, за счет отмеривающего распыляющего пульвелизатора.
Соединения по изобретению могут быть получены для аэрозольного введения, в частности для введения в респираторный тракт, включая интраназальное введение. Соединение обычно будет иметь небольшой размер частиц, например порядка пяти (5) микрон или менее. Такой размер частиц может быть получен при помощи средств, известных в области техники, например микронизации. Активный ингредиент предложен в герметичном пакете с приемлемым газом-вытеснителем, таким как хлорфторкарбон (ХФК), например дихлордифторметан, трихлорфторметан или дихлортетрафторэтан или диоксид углерода или другой приемлемый газ. Аэрозоль обычно может также содержать поверхностно-активное вещество, такое как лецитин. Доза лекарственного средства может контролироваться посредством дозирующего клапана. Альтернативно активные ингредиенты могут быть предложены в виде сухого порошка, например порошковой смеси соединения в приемлемой порошковой основе, такой как лактоза, крахмал, производные крахмала, такие как гидроксипропилметилцеллюлоза и поливнилпирролидон (ПВП). Порошковый носитель будет формировать гель в носовой полости. Композиция порошка может быть представлена в единичной дозированной форме, например в капсулах или картриджах, например, из желатина, или блистерах, из которых порошок может быть введен при помощи ингалятора.
При желании могут быть получены препараты с кишечнорастворимой оболочкой, адаптированной к введению с замедленным или контролируемым высвобождением активного ингредиента. Например, соединения по настоящему изобретению могут быть получены в виде трансдермальных или подкожных систем доставки лекарственного средства. Данные системы доставки выигрышны в случае, когда необходимо замедленное высвобождение и когда крайне важно соблюдение пациентом режима лечения. Соединения в трансдермальных системах доставки часто прикреплены к твердой подложке, адгезирующей с кожей. Интересующее соединение также может быть скомбинировано с усилителем всасывания, например Азоном (1-додецилазоциклогептан-2-он). Системы замедленного высвобождения вводят подкожно в субдермальный слой посредством операции или инъекции. Субдермальные импланты инкапсулируют соединение в липидной растворимой мембране, например, силиконовом каучуке или биодеградируемом полимере, например полимолочной кислоте.
Фармацевтические препараты могут быть в единичных дозированных формах. В такой форме препарат подразделен на единичные дозы, содержащие соответствующие количества активного компонента. Единичная дозированная форма может представлять собой упакованный препарат, упаковку, содержащую дискретные количества препарата, такие как упакованные таблетки, капсулы и порошки в сосудах или ампулах. Также единичная дозированная форма может представлять собой капсулу, таблетку, крахмальную капсулу или пастилку для рассасывания, или она может представлять собой соответствующее число любой из этих упакованных форм.
Другие приемлемые фармацевтические носители и другие препараты описаны в Remington: The Science and Practice of Pharmacy 1995, edited by E.W. Martin, Mack Publishing Company, 19th edition, Easton, Pennsylvania. Репрезентативные фармацевтические препараты, содержащие соединение по настоящему изобретению, описаны ниже.
Практическое применение
Соединения по настоящему изобретению полезны для лечения заболеваний или состояний, опосредованных LRRK2, включая нейродегенеративные расстройства, такие как болезнь Паркинсона, деменция с тельцами Леви и болезнь Хантингтона, и для усиления когнитивной памяти у субъектов, нуждающихся в этом.
Примеры
Следующие получения и примеры приведены для того, чтобы специалисты в области техники могли лучше понять и внедрить в практику настоящее изобретение. Они должны рассматриваться не в качестве ограничения объема изобретения, а исключительно в качестве его иллюстрации и представления.
Если не указано иное, все температуры, включая температуры плавления (т.е. ТП) указаны в градусах Цельсия (°С). Следует понимать, что реакция, в результате которой получают указанный и/или желаемый продукт не обязательно протекает напрямую из комбинации двух изначально добавленных реагентов, т.е. может присутствовать одно или более промежуточное соединение, получаемых в смеси, которая в конечном итоге приводит к образованию указанного и/или желаемого продукта. Следующие аббревиатуры могут быть применены в Получениях и Примерах.
Список аббревиатур
Получение 1: 2-хлор-5-фтор-N-метилпиримидин-4-амин
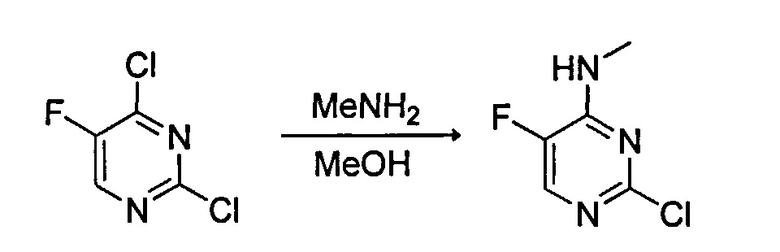
В 250 мл круглодонную колбу, оборудованную магнитной мешалкой, добавляли 9,0 г 5-фтор-2,4-дихлор-пиримидина, 40 мл метанола и 15 мл 8 М метиламина в этаноле. Реакцию нагревали (умеренно экзотермичная) и оставляли перемешиваться при комнатной температуре в течение ~30 минут. Проверка при помощи TLC (1:1 EtOAc: гептан) и LCMS показала завершение реакции. Реакцию концентрировали до получения 9,77 г неочищенного материала, который очищали при помощи пропускания через кремниевую колонку при градиенте 1%-10% MeOH в DCM свыше 35 минут для получения 6,77 г чистого 2-хлор-5-фтор-N-метилпиримидин-4-амина.
Такой же способ применяли для получения соединений, представленных в таблице 1 ниже, при применении соответствующих коммерчески доступных замещенных 2,4-дихлор-пиримидинов и аминов.

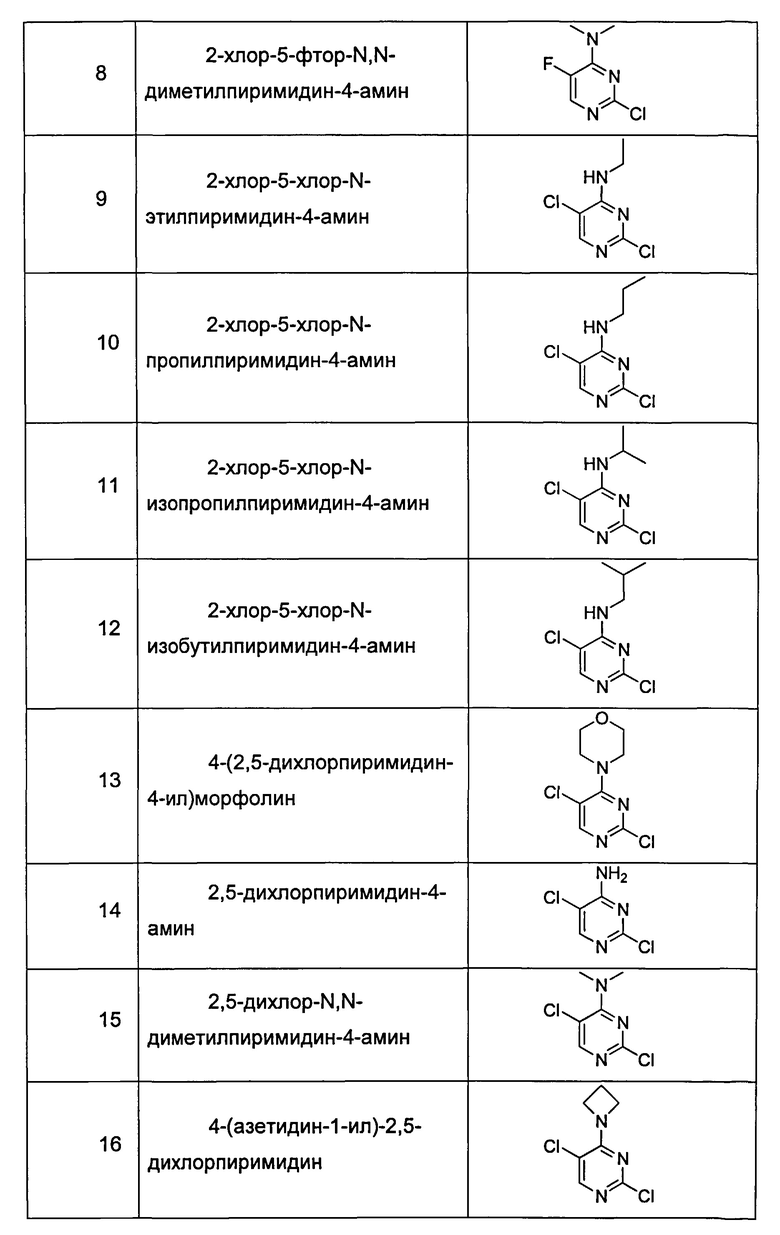

Получение 2: 2,5-дихлор-4-метоксипиримидин

В 250 мл круглодонную колбу, оборудованную магнитной мешалкой, добавляли 1 г 5-хлор-2,4-дихлор-пиримидина и 15 мл диэтилового эфира. Смесь охлаждали до 0°С в ледяной бане и затем медленно добавляли 1 эквивалент метоксида натрия в метаноле (полученного из реакции 120 мг натрия с 4 мл метанола при комнатной температуре). Реакцию перемешивали в течение ночи при комнатной температуре и проверяли при помощи LCMS. Белый осадок отфильтровывали и твердое вещество промывали холодным метанолом. После высушивания получали 0,98 г чистого 2,5-дихлор-4-метоксипиримидина и данный материал применяли без дальнейшей очистки.
Такой же способ применяли для получения соединений, представленных в таблице 2 ниже, при применении коммерчески доступных спиртов и соответственно замещенных 2,4-дихлор-пиримидинов.


Получение 3: 2-метокси-4-(метилсульфонил)анилин

Этап 1:2-метокси-4-(метилсульфонил)анилин
Смесь 4-фтор-2-метокси-1-нитробензола (1,38 г, 8,06 ммоль) и метилмеркаптида натрия (0,622 г, 8,87 ммоль) в ДМФ (25 мл) перемешивали при комнатной температуре в течение 18 часов. Реакцию разбавляли водой и экстрагировали EtOAc. Комбинированные экстракты промывали соляным раствором, высушивали над сульфатом натрия, фильтровали и концентрировали для получения (3-метокси-4-нитрофенил)(метил)сульфана (0,95 г, 59%).
Этап 2: 2-метокси-4-(метилсульфонил)-1-нитробензол
К суспензии (3-метокси-4-нитрофенил)(метил)сульфана (0,58 г, 2,9 ммоль) в ацетоне (10 мл) добавляли воду (10 мл), метанол (1,0 мл). Смесь охлаждали в ледяной бане в течение 10 минут до добавления оксона (2,90 г, 4,72 ммоль) в четырех частях через 4 минуты. Реакцию перемешивали при 0°С в течение 15 минут и затем оставляли нагреваться до комнатной температуры. Реакцию перемешивали при комнатной температуре в течение 2 часов до разбавления EtOAc (50 мл). Суспензию фильтровали, концентрировали до 1/3 ее объема и разбавляли водой (40 мл). Затем смесь экстрагировали при помощи EtOAc. Комбинированные экстракты промывали соляным раствором, высушивали над сульфатом натрия, фильтровали и концентрировали до получения 2-метокси-4-(метилсульфонил)-1-нитробензола (0,67 г, 83%).
Этап 3: 2-метокси-4-(метилсульфонил)анилин
Суспензию 2-метокси-4-(метилсульфонил)-1-нитробензола (0,175 г, 0,76 ммоль) и палладиевый катализатор на углеродном носителе (10 масс. %, 0,10 г) в этаноле (10 мл) перемешивали при водороде при давлении 1 атмосфера в течение 18 часов. Реакцию фильтровали через целит и концентрировали до получения 2-метокси-4-(метилсульфонил)анилина (0,15 г, 92%).
Аналогично получали: 2-хлор-4-(метилсульфонил)анилин; 5-фтор-2-метокси-4-(метилсульфонил)анилин; 2-изопропокси-4-(метилсульфонил)анилин; 2-(2-фторэтокси)-4-(метилсульфонил)анилин;
5-хлор-2-метокси-4-(метилсульфонил)анилин; и 2-метокси-5-метил-4-(метилсульфонил)анилин.
Получение 4: 4-амино-2-фтор-5-метоксибензонитрил

Этап 1: 1-бром-2-фтор-5-метокси-4-нитробензол
К раствору 1-бром-2,5-дифтор-4-нитробензола (2,56 г, 0.011 ммоль) в метаноле (20 мл) добавляли 25% метоксид натрия в растворе метанола (2,5 мл). Смесь перемешивали при комнатной температуре в течение 1,5 часов. Затем реакцию концентрировали, повторно растворяли в EtOAc и промывали водой. Водную промывку обратно экстрагировали EtOAc. Комбинированные органические экстракты промывали соляным раствором, высушивали над сульфатом натрия, фильтровали и концентрировали до получения 1-бром-2-фтор-5-метокси-4-нитробензола (2,65 г, 99%).
Этап 2: 4-бром-5-фтор-2-метоксианилин
К раствору 1-бром-2-фтор-5-метокси-4-нитробензола (0,998 г, 3,99 ммоль) в изопропаноле (20 мл) добавляли железо (0,7 г, 12 ммоль), хлорид аммония (0,64 г, 12 ммоль) и воду (2 мл). Реакцию перемешивали при 75°С в течение 2 часов, затем фильтровали и концентрировали. Осадок разбавляли водой и экстрагировали EtOAc. Комбинированные органические экстракты промывали соляным раствором, высушивали над сульфатом натрия. Фильтровали и концентрировали для получения 4-бром-5-фтор-2-метоксианилина (0,82 г, 93%).
Этап 3: 4-амино-2-фтор-5-метоксибензонитрил
В пробирку под давлением добавляли 4-бром-5-фтор-2-метоксианилин (0,24 г, 1,1 ммоль), цианид цинка (0,10 г, 0,87 ммоль), Pd2(dba)3 (100 мг, 0,11 ммоль), DavePhos (86 мг, 0,22 ммоль) и ДМФ (3 мл). Реакцию герметизировали и перемешивали при 100°С в течение 6 часов. Реакцию разбавляли водой и экстрагировали EtOAc. Комбинированные органические экстракты промывали соляным раствором, высушивали над сульфатом натрия, фильтровали и концентрировали. Неочищенный продукт очищали при помощи флэш-хроматографии для получения 4-амино-2-фтор-5-метоксибензонитрила (0,18 г, 77%).
Аналогично получали: 4-амино-5-хлоро-2-метилбензонитрил; 4-амино-5-метокси-2-метилбензинитрил; и 4-амино-3-метоксибензонитрил.
Пример 1: N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин
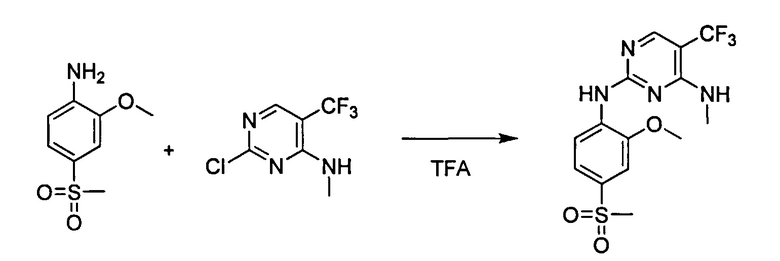
К смеси 2-метокси-4-(метилсульфонил)анилин (0,095 г, 0,47 ммоль) и 2-хлор-N-метил-5-(трифторметил)пиримидин-4-амин (0,10 г, 0,47 ммоль) в 1-бутаноле (1,5 мл) добавляли TFA (0,036 мл, 0,047 ммоль). Реакцию перемешивали в закрытой пробирке при 100°С в течение 1,5 ч. Реакцию концентрировали и продукт выделяли при помощи ВЭЖХ с обратной фазой для получения N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин (0,18 г, 20%). 1Н ЯМР (400 МГц, ДМСО) δ 8,58 (d, J=12,9, 1Н), 8,24 (d, J=5,0, 2H), 7,53 (d, J=10,1, 1Н), 7,48 (s, 1Н), 7,38 - 7,29 (m, 1Н), 3,99 (s, 3H), 3,20 (s, 3H), 2,94 (d, J=4,3, 3H); LRRK2 Ki=0,002.
Пример 2: 5-хлор-N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метилпиримидин-2,4-диамин
Аналогично при помощи 2-хлор-5-хлор-N-метилпиримидин-4-амина вместо 2-хлор-N-метил-5-(трифторметил)пиримидин-4-амина, получали 5-хлор-N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метилпиримидин-2,4-диамин; 1Н ЯМР (400 МГц, ДМСО) δ 8,64 (d, J=8,6, 1Н), 8,01 (s, 1Н), 7,86 (s, 1Н), 7,51 (d, J=8,6, 1Н), 7,45 (s, 1Н), 7,42 (d, J=4,3, 1Н), 3,99 (s, 3H), 3,18 (s, 3H), 2,93 (d, J=4,5, 3H); LRRK2 Ki=0,002.
Дополнительные соединения, полученные при помощи вышеупомянутых способов, приведены в таблице 3 ниже, вместе со значениями аффинности LRRK2 Ki (микромолярные) для выбранных соединений.
Пример 3: 2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрил

К смеси 4-амино-2-фтор-5-метоксибензонитрила (66 мг, 0,40 ммоль) и 2-хлор-N-метил-5-(трифторметил)пиримидин-4-амина (0,10 г, 0,47 ммоль) в 1-бутаноле (2 мл) добавляли TFA (0,05 мл, 0,07 ммоль). Реакцию перемешивали в закрытой пробирке при 75°С в течение 2 ч. Реакцию концентрировали и продукт выделяли при помощи ВЭЖХ с обратной фазой для получения 2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрила. 1Н ЯМР (400 МГц, ДМСО) δ 8,57 (d, J=13,4, 2H), 8,34 (s, 1Н), 8,29 (d, J=6,1, 1Н), 7,56-7,42 (m, 3H), 3,93 (s, 3H), 2,95 (s, 3H); LRRK2 Ki=0,022.
Пример 4: 3-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрил
Аналогично при помощи 4-амино-3-метоксибензонитрила вместо 4-амино-2-фтор-5-метоксибензонитрила получали 3-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрил: 1Н ЯМР (400 МГц, ДМСО) δ 8,53 (d, J=8,7, 1Н), 8,23 (d, J=8,4, 1Н), 7,49 (s, 1Н), 7,45 (d, J=8,0, 1Н), 7,35 (dd, J=12,3, 7,3, 1Н), 3,94 (s, 3H), 2,93 (d, J=4,4, 3H); LRRK2 Ki=0,008.
Пример 5: 4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-3-метоксибензонитрил
Аналогично при помощи 4-амино-3-метоксибензонитрила вместо 4-амино-2-фтор-5-метоксибензонитрила и 5-хлор-N4-метилпиримидин-2,4-диамина вместо 2-хлор-N-метил-5-(трифтоорметил)пиримидин-4-амина получали 4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-3-метоксибензонитрил: 1Н ЯМР (400 МГц, ДМСО) δ 8,59 (d, 1Н), 8,01 (s, 1Н), 7,86 (s, 1Н), 7,42 (m, 3H), 3,94 (s, 3H), 2,92 (d, 3H); LRRK2 Ki=0,008.
Дополнительные соединения, полученные при помощи вышеупомянутых способов, приведены в таблице 3 ниже вместе со значениями аффинности LRRK2 Ki (микромолярные) для выбранных соединений.




Пример 30: In Vitro LRRK2 LabChip анализ
Данное исследование применяли для определения способности соединения ингибировать активность LRRK2 за счет определения Kiapp, IC50 или значений уровня ингибирования. В полипропиленовом планшете LRRK2, флуоресцентно-меченый пептидный субстрат, АТР и тестируемое соединение инкубировали вместе. При помощи LabChip 3000 (Caliper Life Sciences), после реакции субстрат разделяли посредством капиллярного электрофореза на две части: фосфорилированную и нефосфорилированную. Относительные количества каждой вычисляли на основании интенсивности флуоресценции. LRRK2 Ki определяли согласно формуле:
Y=V0⋅(1-((x+Ki⋅(1+S/Km)+Et)/(2⋅Et)-(((x+Ki⋅(1+S/Km)+Et)^2-(4⋅Et⋅x))^0.5)/(2⋅Et))).
Ki значения в таблице 4 и где-либо еще приведены в мкМ.
Условия исследования и примененные материалы были следующими
Конечные условия исследования
LRRK2 G2019S в 5 мМ MgCl2: 5,2 нМ (Invitrogen lot # 567054А)
LRRK2 G2019S в 1 мМ MnCl2 11 нМ (Invitrogen lot # 567054А)
LRRK2 Wild type в 5 мМ MgCl2: 15 нМ (Invitrogen lot # 500607F)
LRRK2 I2020T в 5 мМ MgClz: 25 нМ (Invitrogen lot # 43594)
Субстрат: 1 мкМ АТР: 130 мкМ Время киназной реакции: 2 часа Температура: окружающей среды
Общий объем: 20 мкл
ATPapp Kms:
G2019S в 5 мМ MgCl2: 130 мкМ
G2019S в 1 мМ MnCl2: 1 мкМ
Дикий тип в 5 мМ MgCl2: 80 мкМ
I2020T в 5 мМ MgCl2: 14 мкМ
Материалы:
Твердая подложка: черный объемом 50 мкл 384-луночный полипропиленовый планшет (MatriCal cat # MP101-1-РР)
Киназа: LRRK2 G2019S (Invitrogen cat # PV4882).
LRRK2 Wild type (Invitrogen cat # PV4874).
Субстрат: 5FAM-GAGRLGRDKYKTLRQIRQ-CONH2
Несвязывающий планшет: 384-луночные прозрачные полипропиленовые планшеты с V-образным дном (Greiner cat #781280).
АТР: 10 мМ АТР (Cell Signaling cat #9804).
Triton X-100: Triton X-100.
Brij-35: Brij-35 (Pierce cat #20150).
Реагент покрытия #3: Coating Reagent #3 (Caliper).
ДМСО: ДМСО (Sigma cat #34869-100ML).
Полный реакционный буфер: H2O/25 мМ Трис, рН 8,0/5 мМ MgCl2/2 мМ DTT/0.01% Triton X-100.
Стоп-реагент: Н2О/100 мМ HEPES, рН 7,2/0,015% Brij-35/0,2% реагент покрытия #3/20 мМ ЭДТА.
Разделяющий буфер: H2O/100 мМ HEPES, рН 7,2/0,015% Brij-35/0,1% Реагент покрытия #3/1:200 Реагент покрытия #8/10 мМ ЭДТА/5% ДМСО.
Получение планшета с соединением
Для серийных разведений 34,6 мкл ДМСО добавляли в колонки 3-24. Для контроля анализа 37,5 мкл ДМСО добавляли в колонки 1 и 2 рядов А и Р. a, d и 50 мкл 25 мкМ G-028831 (Staurosporine) добавляли в колонки 1 и 2, ряд В. Для образцов: для начала добавляли 100 мкМ, 37,5 мкл ДМСО в колонки 1 и 2, затем 12,5 мкл 10 мМ соединения; для начала добавляли 10 мкМ, 78 мкл ДМСО в колонки 1 и 2, затем 2 мкл 10 мМ соединения; и для начала добавляли 1 мкМ, 25 мкМ соединения (2 мкл 10 мМ соединения + 798 мкл ДМСО) в пустые колонки 1 и 2. Точный инструмент применяли для выполнения серийных разведении 1:3.16 ("PLK_BM_serial_halflog").
Получение АТР
АТР разводили до 282,1 мкМ в полном киназном буфере (конечная концентрация составила 130 мкМ).
Общее получение и получения контроля
В полном реакционном буфере субстрат разбавляли до 4 мкМ. Эквивалентные объемы полного реакционного буфера и 4 мкМ субстрата комбинировали для получения контроля. Эквивалентные объемы полного реакционного буфера и 4 мкМ субстрата комбинировали и к комбинированному раствору добавляли 2Х конечную концентрацию LRRK2.
Процедура анализа
В 50 мкл полипропиленовый планшет 5 мкл/лунку буфера/субстрата добавляли вручную в лунки контроля. Biomek FX применяли для начала киназной реакции ("PLK SAR 23 АТР"). Следующее добавляли в соответствующие лунки:
2 мкл соединения + 23 мкл АТР;
5 мкл/лунку соединения/АТР в планшете для анализа;
5 мкл/лунку киназы/субстрата в планшете для анализа.
Планшет инкубировали в течение 2 часов в темноте. Для остановки киназной реакции ("PLK Stop") применяли Biomek FX и добавляли 10 мкл/лунку стоп-реагента в планшет для анализа. Результаты считывали на LabChip 3000.
Lab Chip 3000 протокол:
LabChip 3000 запускали при помощи задания "LRRK2 IC50" со следующими параметрами задания:
Пример 31 In Vitro анализ связывания LRRK2
Данный анализ применяли для определения способности соединения к ингибированию активности LRRK2 за счет определения Kiapp, IC50, или значений процента ингибирования. В 384-луночных черных планшетах proxiplates F с неглубокими лунками LRRK2, Еu-меченые антитела к GST, Alexa Fluor® Kinase tracer 236 и тестируемое соединение инкубировали вместе.
Связывание Alexa Fluor® "tracer" с киназой детектировали посредством добавления Eu-меченых антител к GST. Связывание меченого вещества и антитела с киназой приводило к высокой степени FRET, при этом замещение меченого вещества ингибитором киназы приводило к потере FRET.
Условия анализа и примененные материалы были следующими:
Конечные условия реакции:
Материалы:
384-луночные proxiplates F black shallow well Perkin Elmer cat #6008260
Киназа: LRRK2 G2019S Invitrogen cat # PV4882 (LOT 567054A).
Реакционный буфер: H2O/50 мМ Трис, рН 7,4/10 мМ MgCl2/1 мМ EGTA/0,01%Brij35.
Получение планшета с соединением
Серийное разведение тестируемых соединений (10 мМ сток) 1:3,16 (20 мкл + 43,2 мкл) в 100% ДМСО. Двенадцатиточечная кривая. Разведение каждой концентрации 1:33,3 (3 мкл + 97 мкл) в реакционном буфере. Наносили по 5 мкл в планшет для анализа. Конечная максимальная тестируемая концентрация 100 мкМ. Общее получение и получение контроля:
В реакционном буфере 5 мкл ДМСО (3%) добавляли в лунки контроля и в остальные лунки и 5 мкл Eu-меченых антител к GST (6 нМ) добавляли в лунки контроля.
Процедура анализа:
Добавляли 5 мкл смеси LRRK2(30 нМ)/Eu-меченые антитела к GST (6 нМ) к соединению и во все лунки. Добавляли 5 мкл киназного трейсера (25,5 нМ) в лунки. Инкубировали планшеты при комнатной температуре в течение 1 часа на планшетном шейкере (мягкое покачивание). Считывание проводили на Perkin Elmer En Vision reader, HTRF протокол.
Обработка данных:
Вычисляли соотношение: (665/620)⋅10000. Вычитали средние величины низших порядков исходя из всех данных. Вычисляли % контроля для каждого тестируемого значения. Определяли % контроля vs концентрации соединения. Вычисляли значение Ki (корректировка кривых согласно уравнению Моррисона с применением XLfit).
Результаты представляли в виде Ki в мкМ. Вычисление для Ki:
Y=V0⋅(1-((х+Ki⋅(1+S/Km)+Et)/(2⋅Et)-(((x+Ki⋅(1+S/Km)+Et)^2-(4⋅Et⋅x))^0.5)/(2⋅Et)))
где Et=4 нМ
kd (Tracer)=8,5 нМ
концентрация меченого вещества (S)=8,5 нМ.
Пример 32 животная модель болезни Паркинсона
Болезнь Паркинсонна может быть воспроизведена на мышах и приматах посредством введения 1-метил-4-фенил тетрагидропиридина (MPTP), селективного нигростриального дофаминэргического нейротоксина, который вызывает утрату стриальных дофаминовых (DA) нервных терминальных маркеров. Соединения по изобретению могут быть оценены в отношении эффективности лечения болезни Паркинсона при помощи MPTP-индуцированной нейродегенерации обычно следуя протоколу, описанному Saporito et al., J. Pharmacology (1999) Vol. 288, pp. 421-427.
Вкратце, MPTP растворяют в PBS в концентрации 2-4 мг/мл и делают мышам подкожную инъекцию (самцы С57, масса 20-25 г) 20-40 мг/кг. Соединения по изобретению солюбилизируют при помощи полиэтиленгликоль гидроксистеарата и растворяют в PBS. Мышам вводят 10 мл/кг раствора соединения при помощи подкожной инъекции 4-6 ч до введения MPTP и затем ежедневно в течение 7 дней. В день последней инъекции мышей умерщвляют и средний мозг блокируют и фиксируют в параформальдегиде. Полосатое тело иссекают, взвешивают и хранят при -70°С.
Таким образом, полосатое тело собирают и оценивают в отношении содержания дофамина и его метаболитов дигидрофенилуксусной кислоты и гомованилиновой кислоты посредством ВЭЖХ с электрохимической детекцией, как описано Sonsalla et al., J. Pharmacol. Exp. Ther. (1987) Vol. 242, pp. 850-857. Полосатое тело также может быть оценено при помощи исследования тирозингидроксилазы Okunu et al., Anal Biochem (1987) Vol. 129, pp. 405-411 посредством измерения изменения 14CO2, ассоциированного с тирозингидроксилаз-опосредованной конверсией меченого тирозина в L-дигидроксифенилаланин. В дальнейшем полосатое тело может быть оценено при помощи анализа монаминоксидазы В, как описано White et al., Life Sci. (1984), Vol. 35, pp. 827-833, и при помощи мониторинга захвата дофамина, как описано Saporito et al., (1992) Vol. 260, pp. 1400-1409.
Наряду с этим настоящее изобретение описано со ссылкой на его конкретные воплощения, специалистам в области техники следует понимать, что могут быть сделаны различные изменения и эквиваленты могут быть замещены без отхождения от сути и объема изобретения. Кроме того, многие модификации могут быть сделаны для адаптации к конкретной ситуации, материалу, композиции, способу, этапу или этапам способа, в отношении указанной сути и объема настоящего изобретения. Все такие модификации предназначены быть внутри объема формулы изобретения, прилагаемой к настоящему изобретению.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФТОР-18 И УГЛЕРОД-11 МЕЧЕНЫЕ РАДИОЛИГАНДЫ ДЛЯ ТОМОГРАФИИ С ПОЗИТРОННОЙ ЭМИССИЕЙ (РЕТ), ВИЗУАЛИЗИРУЮЩЕЙ LRRK2 | 2012 |
|
RU2650641C2 |
| ПРОИЗВОДНЫЕ 2-(ФЕНИЛ ИЛИ ПИРИД-3-ИЛ)АМИНОПИРИМИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ БОГАТОЙ ЛЕЙЦИНОМ ПОВТОРНОЙ КИНАЗЫ 2 (LRRK2) ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2012 |
|
RU2647849C2 |
| ПРОИЗВОДНЫЕ АМИНОПИРИМИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ БОГАТОЙ ЛЕЙЦИНОМ ПОВТОРНОЙ КИНАЗЫ 2 (LRRK2) | 2012 |
|
RU2651544C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛАМИНОПИРИМИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ ОБОГАЩЕННОЙ ЛЕЙЦИНОВЫМИ ПОВТОРАМИ КИНАЗЫ 2 | 2013 |
|
RU2637947C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛАМИНОПИРИМИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ ОБОГАЩЕННОЙ ЛЕЙЦИНОВЫМИ ПОВТОРАМИ КИНАЗЫ 2 (LRRK2) ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ БОЛЕЗНИ ПАРКИНСОНА | 2013 |
|
RU2637948C2 |
| ПРОИЗВОДНЫЕ 2-ФЕНИЛАМИНОПИРИМИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ БОГАТОЙ ЛЕЙЦИНОМ ПОВТОРНОЙ КИНАЗЫ 2 (LRRK2) ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2012 |
|
RU2661197C2 |
| ПИРИДОПИРИМИДИНОНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРА N-МЕТИЛ-D-АСПАРТАТА | 2016 |
|
RU2717665C2 |
| АНТАГОНИСТЫ КОРТИКОТРОПИН-РИЛИЗИНГ ФАКТОРА | 1995 |
|
RU2221799C2 |
| ГЕТЕРОЦИКЛИЛЬНЫЕ ПИРИМИДИНОВЫЕ АНАЛОГИ В КАЧЕСТВЕ ИНГИБИТОРОВ Tук2 | 2013 |
|
RU2641895C2 |
| ПРОИЗВОДНОЕ ПИРИМИДИН-4,6-ДИАМИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2022 |
|
RU2834353C2 |
Изобретение относится к новым соединениям формулы I и их фармацевтически приемлемым солям, активность которых ассоциирована с рецептором LRRK2. Соединения предназначены для лечения такого заболевания, как болезнь Паркинсона, в частности наследственной болезни Паркинсона. В формуле I

m составляет от 0 до 1; X представляет собой -NRa-; -О-; или -S(O)r-, где r составляет от 0 до 2 и Ra представляет собой водород; R1 представляет собой С1-6-алкил; R2 представляет собой галоген; циано; или гало-С1-6-алкил; R3 и R4 независимо друг от друга представляют собой галоген; C1-6-алкил; С1-6-алкокси; гало-С1-6-алкил; или гало-С1-6-алкокси; или R3 и R4 вместе с атомами, к которым они прикреплены, могут образовывать пяти- или шестичленное кольцо, которое возможно включает один или два гетероатома, независимо выбранных из О; и R5 представляет собой С1-6-алкилсульфонил; или циано. 5 н. и 12 з.п. ф-лы, 3 табл., 32 пр.
1. Соединение формулы I
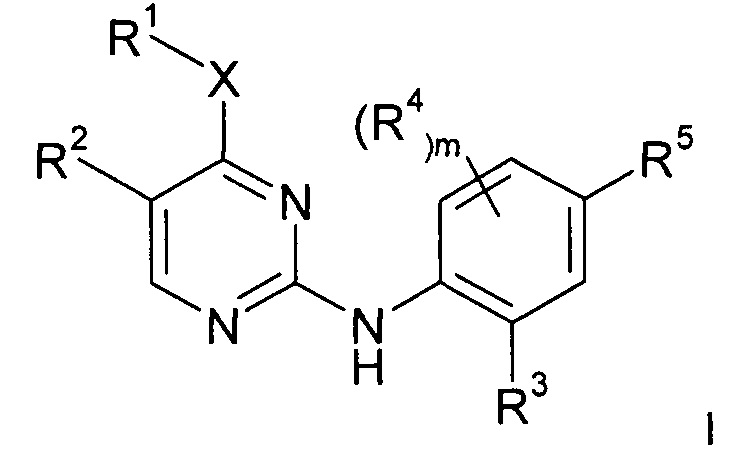
или его фармацевтически приемлемые соли,
где:
m составляет от 0 до 1;
X представляет собой -NRa-; -О-; или -S(O)r-, где r составляет от 0 до 2 и Ra представляет собой водород;
R1 представляет собой С1-6-алкил;
R2 представляет собой галоген; циано; или гало-С1-6-алкил;
R3 и R4 независимо друг от друга представляют собой галоген; C1-6-алкил; С1-6-алкокси; гало-С1-6-алкил; или гало-С1-6-алкокси;
или R3 и R4 вместе с атомами, к которым они прикреплены, могут образовывать пяти- или шестичленное кольцо, которое возможно включает один или два гетероатома, независимо выбранных из О; и
R5 представляет собой С1-6-алкилсульфонил; или циано.
2. Соединение по п. 1, где X представляет собой -NH- или -О-.
3. Соединение по п. 1, где R1 представляет собой метил.
4. Соединение по п. 1, где R2 представляет собой хлор или трифторметил.
5. Соединение по п. 1, где R3 представляет собой фтор, хлор или метокси.
6. Соединение по п. 1, где R3 представляет собой метокси.
7. Соединение по п. 1, где R4 представляет собой фтор, хлор, метил или метокси.
8. Соединение по п. 1, где R5 представляет собой C1-6-алкилсульфонил.
9. Соединение по п. 1, где R5 представляет собой метансульфонил или циано.
10. Соединение по п. 1, где R5 представляет собой циано.
11. Соединение по п. 1, где R5 представляет собой метансульфонил.
12. Соединение, выбранное из группы, состоящей из
N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин,
5-хлор-N2-(2-метокси-4-(метилсульфонил)фенил)-N4-метилпиримидин-2,4-диамин,
2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрил,
3-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)бензонитрил,
4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-3-метоксибензонитрил,
(2-хлор-4-метансульфонил-фенил)-(5-хлор-4-метокси-пиримидин-2-ил)-амин,
N2-(2-хлор-4-метансульфонил-фенил)-N4-метил-5-трифтометил-пиримидин-2,4-диамин,
5-хлор-N2-(2-хлор-4-метансульфонил-фенил)-N4-метил-пиримидин-2,4-диамин,
N2-(2-метокси-4-морфолин-4-илметил-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин,
5-хлор-2-метил-4-(4-метиламино-5-трифторметил-пиримидин-2-иламино)-бензонитрил,
2-(5-фтор-2-метокси-4-морфолин-4-илметил-фениламино)-4-метиламино-пиримидин-5-карбонитрил,
4-этиламино-2-(5-фтор-2-метокси-4-морфолин-4-илметил-фениламино)-пиримидин-5-карбонитрил,
5-метокси-2-метил-4-(4-метиламино-5-трифторметил-пиримидин-2-иламино)-бензонитрил,
5-хлор-N2-[2-(2-фтор-этокси)-4-морфолин-4-илметил-фенил]-N4-метил-пиримидин-2,4-диамин,
N2-(5-фтор-4-метансульфонил-2-метокси-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин,
N2-(2-изопропокси-4-метансульфонил-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин,
5-хлор-N2-[2-(2-фтор-этокси)-4-метансульфонил-фенил]-N4-метил-пиримидин-2,4-диамин,
(5-хлор-4-метокси-пиримидин-2-ил)-[2-(2-фтор-этокси)-4-метансульфонил-фенил]-амин,
N2-[2-(2-фтор-этокси)-4-метансульфонил-фенил]-N4-метил-5-трифторметил-пиримидин-2,4-диамин,
N2-(5-хлор-4-метансульфонил-2-метокси-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин,
N2-[5-фтор-2-(2-фтор-этокси)-4-морфолин-4-илметил-фенил]-N4-метил-5-трифторметил-пиримидин-2,4-диамин,
N4-этил-N2-[5-фтор-2-(2-фтор-этокси)-4-морфолин-4-илметил-фенил]-5-трифторметил-пиримидин-2,4-диамин,
N2-(4-метансульфонил-2-метокси-5-метил-фенил)-N4-метил-5-трифторметил-пиримидин-2,4-диамин,
5-хлор-N2-(2-метокси-4-морфолинофенил)-N4-метилпиримидин-2,4-диамин,
4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-3-метоксибензойная кислота,
N2-(2-метокси-4-(морфолиносульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин,
N2-(2-метокси-4-(трифторметил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин,
5-хлор-N2-(2-метокси-4-(трифторметил)фенил)-N4-метилпиримидин-2,4-диамин,
2-хлор-4-(5-хлор-4-(метиламино)пиримидин-2-иламино)-5-метоксибензойная кислота,
1-(2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)фенил)пирролидин-2-он,
4-(2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)фенил)морфолин-3-он,
1-(2-фтор-5-метокси-4-(4-(метиламино)-5-(трифторметил)пиримидин-2-иламино)фенил)пиперидин-2-он,
N2-(5-фтор-2-метокси-4-(оксэтан-3-ил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин,
N4-этил-N2-(2-метокси-5-метил-4-(метилсульфонил)фенил)-5-(трифторметил)пиримидин-2,4-диамин,
N2-(4-(этилсульфонил)-2-метокси-5-метилфенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин,
N2-(2-метокси-5-метил-4-(метилсульфонил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин,
N2-(5-фтор-2-метокси-4-(морфолинометил)фенил)-N4-метил-5-(трифторметил)пиримидин-2,4-диамин и
N4-этил-N2-(8-(метилсульфонил)-2,3-дигидробензо[b][1,4]диоксин-5-ил)-5-(трифторметил)пиримидин-2,4-диамин,
или его фармацевтически приемлемая соль.
13. Фармацевтическая композиция, обладающая аффинностью к LRRK2 (богатой лейцином повторной киназе 2), содержащая:
(a) фармацевтически приемлемый носитель; и
(b) терапевтически эффективное количество соединения или его фармацевтически приемлемой соли по любому из пп. 1-12.
14. Способ лечения болезни Паркинсона, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп. 1-12.
15. Соединение или его фармацевтически приемлемая соль по любому из пп. 1-12 для применения с целью предотвращения или лечения болезни Паркинсона.
16. Фармацевтическая композиция по п. 13, полезная для предотвращения или лечения болезни Паркинсона.
17. Применение соединения или его фармацевтически приемлемой соли по любому из пп. 1-12 для получения лекарственного препарата для предотвращения или лечения болезни Паркинсона.
| Anthony A Estrada et al | |||
| Discovery of Highly Potent, Selective, and Brain-Penetrable Leucine-Rich Repeat Kinase 2 (LRRK2) Small Molecule Inhibitors, Journal of Medicinal Chemistry, 17.09.2012, Vol:55, Nr:22, Page(s):9416 - 9433 | |||
| Huifen Chen; et al., Discovery of Selective LRRK2 Inhibitors Guided by Computational Analysis and Molecular Modeling Journal of Medicinal Chemistry, 14.06.2012, Vol.55, Nr.11, Page(s): 5536-5545 (таблица 3) | |||
| DE 102007010801 A1, 04.09.2008 & EA015174 B1, 30.06 | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| КЕРАМИЧЕСКАЯ МАССА | 2006 |
|
RU2309924C1 |
| WO 2010025863 А, 03.11.2010 & EA 201100438 A1, 31.10.2011 | |||
| WO 2011153553 A2, 08.12 | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| WO 2009127642 A2, 22.10.2009 | |||
| WO 2011038572 A1, 07.04.2011 & EA 021437 B1,30.06.2015 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2017-11-03—Публикация
2012-11-28—Подача