Область техники
Настоящее изобретение относится к фармацевтическим композициям, содержащим вортиоксетин и донепезил, и к применению вортиоксетина совместно с донепезилом при лечении когнитивной дисфункции.
Уровень техники
В международных патентных заявках, в том числе в WO 03/029232 и WO 2007/144005, раскрыты соединение 1-[2-(2,4-диметилфенилсульфанил)-фенил]-пиперазин и его фармацевтически приемлемые соли. WHO с тех пор опубликовала, что вортиоксетин является рекомендованным международным непатентованным наименованием (INN) для 1-[2-(2,4-диметилфенилсульфанил)-фенил]-пиперазина. Вортиоксетин в литературе ранее называли LU АА21004. В сентябре 2013 года FDA одобрило вортиоксетин для лечения депрессивного эпизода тяжелой степени под торговым наименованием Brintellix™.
Вортиоксетин является антагонистом рецепторов 5-НТ3, 5-НТ7 и 5-HT1D, агонистом рецептора 5-HT1A и частичным агонистом рецептора 5-HT1B, и ингибитором транспортера серотонина. Кроме того, было показано, что вортиоксетин повышает уровни нейромедиаторов: серотонина, норадреналина, дофамина, ацетилхолина и гистамина в конкретных областях головного мозга. Все из этих активностей считаются клинически значимыми и потенциально вовлеченными в механизм действия соединения [J.Med.Chem., 54, 3206-3221, 2011; Eur. Neuropshycopharmacol., 18 (suppl 4), S321, 2008; Eur. Neuropshycopharmacol., 21 (suppl 4), S407-408, 2011; Int. J. Psychiatry Clin Pract. 5, 47, 2012].
Как было показано в клинических испытаниях, вортиоксетин является безопасным и эффективным при лечении депрессии. Документ, в котором сообщаются результаты исследования для подтверждения концепции для оценки эффективности и переносимости соединения у пациентов с депрессивным эпизодом тяжелой степени (MDD), под авторством Alvares et al стал доступен в Интернете в Int. J. Neuropsychopharm. 18 июля 2011 года. Результаты шестинедельного рандомизированного плацебо-контролируемого исследования с приблизительно 100 пациентами в каждой группе показали, что вортиоксетин статистически значимо отличается от плацебо при лечении депрессивных симптомов и симптомов тревожного расстройства у пациентов с MDD. Также сообщается, что не наблюдалось клинически значимых изменений результатов клинических лабораторных исследований, показателей жизненно важных функций, веса или параметров ECG. Из результатов долгосрочного исследования также видно, что вортиоксетин эффективен при предупреждении рецидива у пациентов, страдающих от MDD [Eur. Neuropsychopharmacol. 21 (suppl 3), S396-397, 2011]. В исследовании на пожилых пациентах с депрессией, о котором сообщается в Int. Clin. Psychopharm., 27, 215-227, 2012, было показано, что вортиоксетин можно применять для лечения когнитивных дисфункций.
В международной заявке, опубликованной как WO 2009/062517, раскрывают, что вортиоксетин можно объединять с другими типами фармацевтически активных ингредиентов, такими как интерфероны, опиаты, ингибиторы АСЕ и ингибиторы ацетилхолинэстеразы.
Воздействие, которое могут оказывать уровни серотонина и активирование или ингибирование серотониновых рецепторов на уровни ацетилхолина, было подробно рассмотрено - см. Pharmacol Rev, 59, 360-417, 2007. Из данного обзора ясно, что влияние серотонинергической системы на высвобождение ацетилхолина является чрезвычайно сложным и далеким от понимания.
Ацетилхолин является нейромедиатором, который действует в центральной, а также периферической нервных системах. Низкий уровень ацетилхолина был связан с заболеваниями, при которых когнитивная дисфункция играет значительную роль, как например болезнь Альцгеймера. Фактически, введение ингибиторов ацетилхолинэстеразы является одной из двух основных парадигм лечения болезни Альцгеймера. Другой основной парадигмой лечения является введение мемантина, антагониста NMDA-рецептора. Три ингибитора ацетилхолинэстеразы в настоящее время одобрены для лечения болезни Альцгеймера, т.е. донепезил, ривастигмин и галантамин. Донепезил впервые был одобрен FDA в 1996 году; ривастигмин впервые был одобрен FDA в 2000 году; и галантамин впервые был одобрен FDA в 2001 году.
В дополнение к трем вышеуказанным ингибиторам ацетилхолинэстеразы, соединение такрин было предварительно одобрено FDA. Более того, в патентной литературе содержится широкий спектр документов, раскрывающих соединения, которые действуют в качестве ингибиторов ацетилхолинэстеразы, примеры которых включают WO 88/08708, WO 93/13100, WO 97/38993, WO 2003/082820, US 4914102, US 5231093, US 5246947, ЕР 268871, ЕР 298202, ЕР 409676, ЕР 477903 и ЕР 703901.
Когнитивная дисфункция играет большую роль во многих заболеваниях ЦНС (центральной нервной системы, CNS). Они включают, например, болезнь Альцгеймера, деменцию сосудистого генеза и когнитивную дисфункцию, связанную с депрессией, шизофренией, болезнью Паркинсона, злоупотреблением или болезнью Гентингтона. Когнитивная дисфункция не поддается в достаточной мере лечению при помощи существующей в настоящее время терапии, и настоящее изобретение направлено на обеспечение альтернативных и более эффективных путей лечения когнитивной дисфункции.
Краткое описание изобретения
Авторы настоящего изобретения обнаружили, что комплексное применение ингибитора ацетилхолинэстеразы донепезила и вортиоксетина вызывает синергичное увеличение внеклеточного уровня ацетилхолина в головном мозге.
Соответственно, в одном варианте осуществления настоящее изобретение относится к композиции, содержащей вортиоксетин и донепезил.
В одном варианте осуществления настоящее изобретение относится к применению вортиоксетина и донепезила для производства лекарственного препарата для лечения когнитивной дисфункции.
В одном варианте осуществления настоящее изобретение относится к способу лечения когнитивной дисфункции, при этом способ включает комбинированное введение вортиоксетина и донепезила пациенту, нуждающемуся в этом.
В одном варианте осуществления настоящее изобретение относится к вортиоксетину и донепезилу для комплексного применения в способе лечения нарушения когнитивных функций.
Фигуры
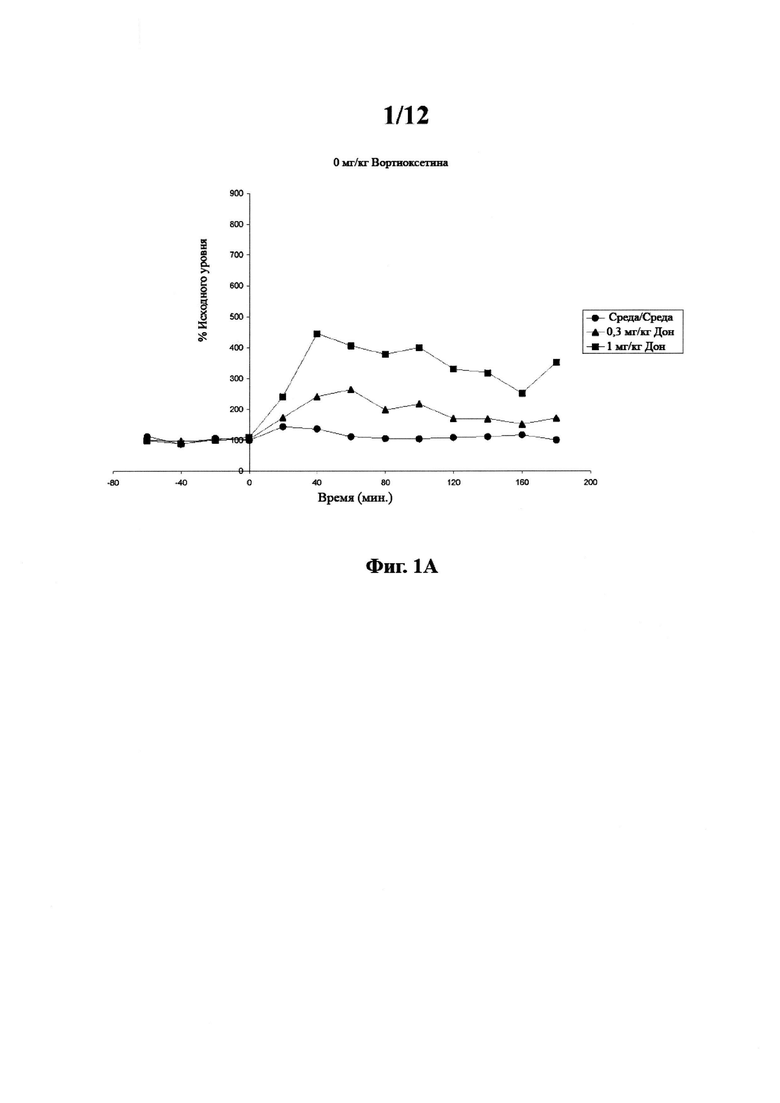
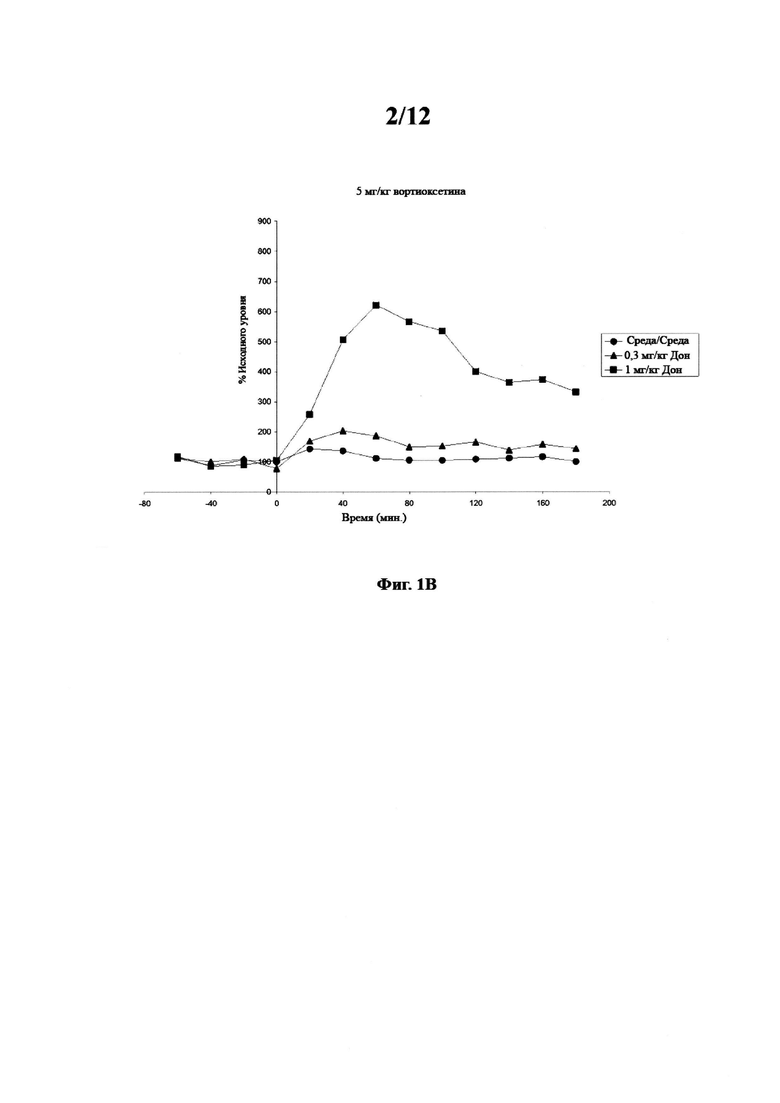
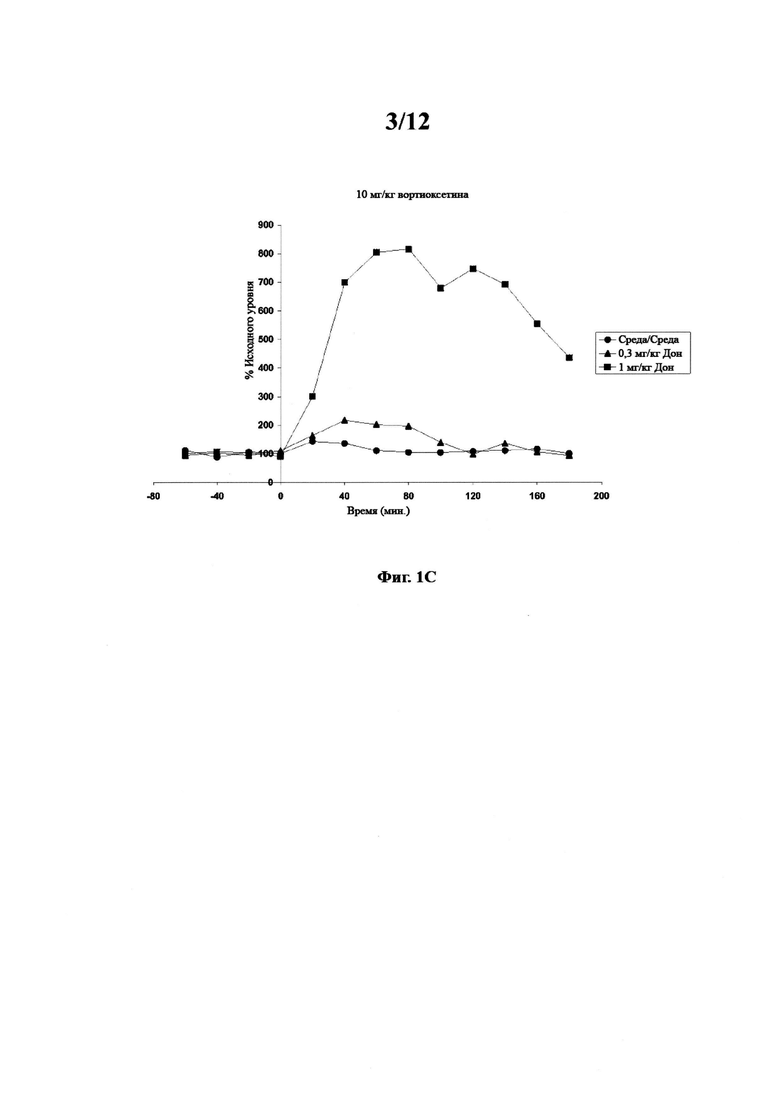
Фигура 1. Фармакодинамический ацетилхолиновый ответ в вентральном гиппокампе у свободно двигающихся крыс после комбинированного введения вортиоксетина и донепезила. Фигура 1А. Ацетилхолиновый ответ на 0 мг/кг вортиоксетина и 0 мг/кг донепезила (●); 0,3 мг/кг донепезила (▲) или 1 мг/кг донепезила (■). Фигура 1В. Ацетилхолиновый ответ на 5 мг/кг вортиоксетина и 0,3 мг/кг донепезила (▲) и 1 мг/кг донепезила (■). Среда/среда (●) включено для сравнения. Фигура 1С.
Ацетилхолиновый ответ на 10 мг/кг вортиоксетина и 0,3 мг/кг донепезила (▲) и 1 мг/кг донепезила (■). Среда/среда (●) включено для сравнения.
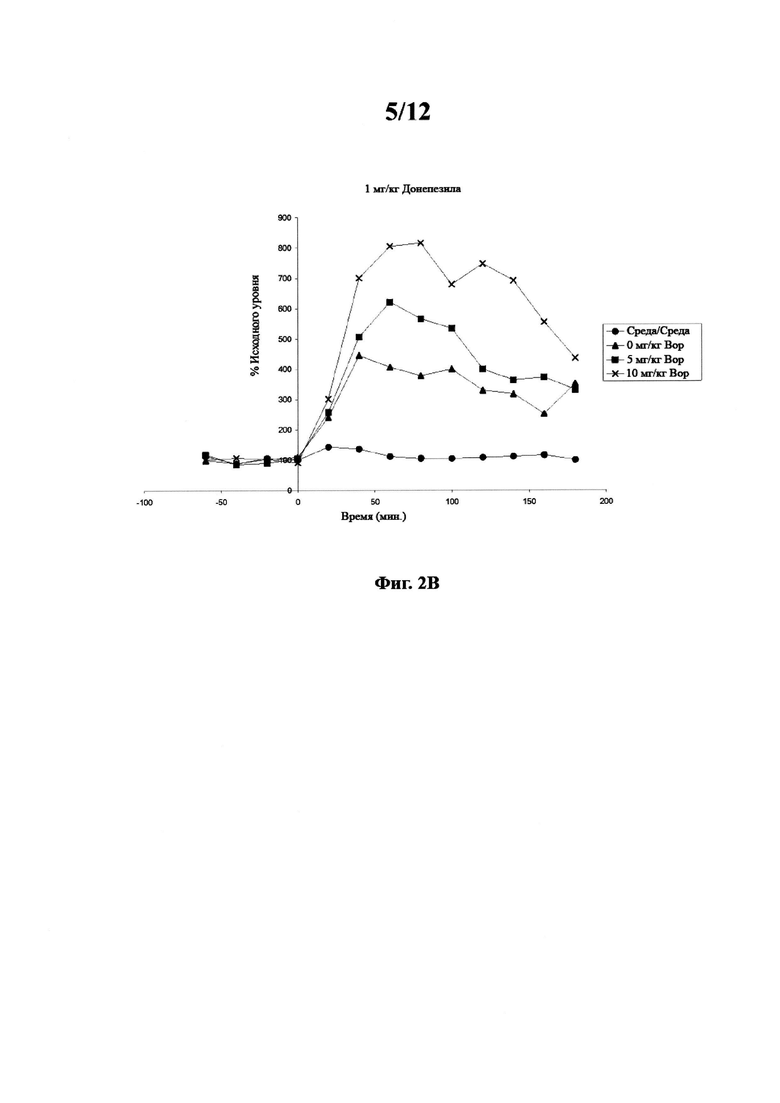
Фигура 2. Фармакодинамический ацетилхолиновый ответ в вентральном гиппокампе у свободно двигающихся крыс после комбинированного введения вортиоксетина и донепезила.
Фигура 2А. Ацетилхолиновый ответ на 0,3 мг/кг донепезила и 0 мг/кг вортиоксетина (▲); 5 мг/кг вортиоксетина (■) или 10 мг/кг вортиоксетина (✖). Среда/среда (●) включено для сравнения. Фигура 2В. Ацетилхолиновый ответ на 1 мг/кг донепезила и 0 мг/кг вортиоксетина (▲); 5 мг/кг вортиоксетина (■) или 10 мг/кг вортиоксетина (✖). Среда/среда (●) включено для сравнения.
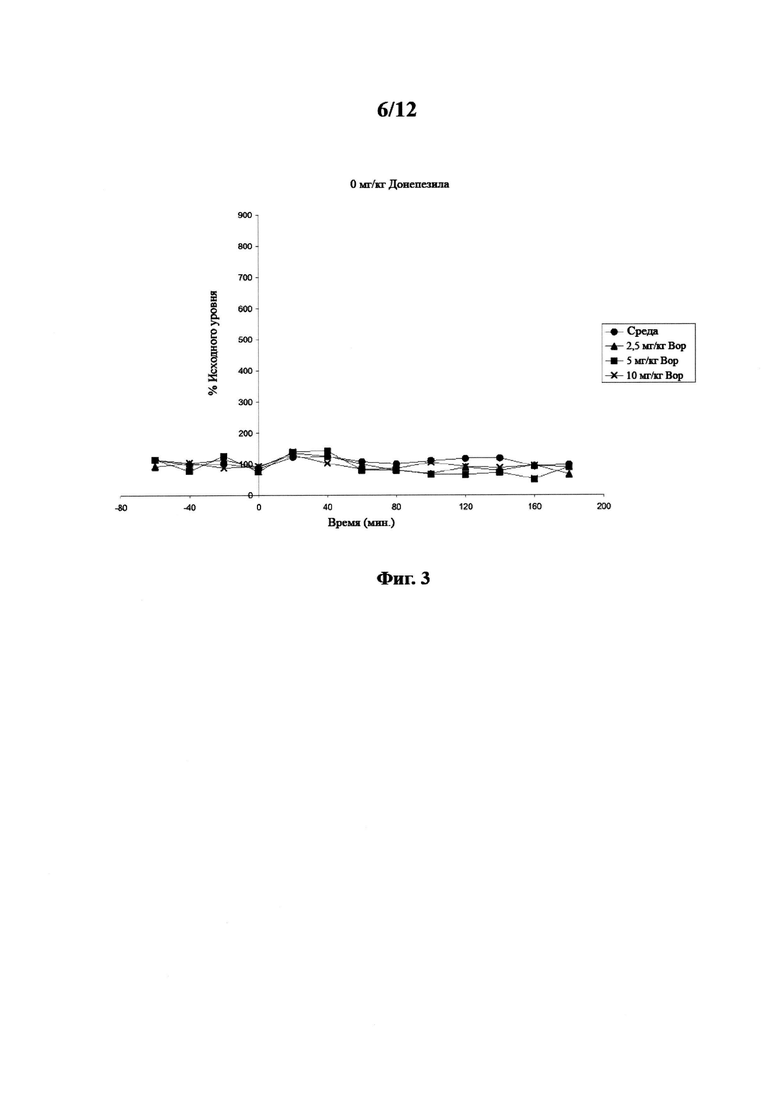
Фигура 3. Фармакодинамический ацетилхолиновый ответ в вентральном гиппокампе у свободно двигающихся крыс после введения вортиоксетина. Ацетилхолиновый ответ на 0 мг/кг (●), 2,5 мг/кг (▲), 5 мг/кг (■) и 10 мг/кг вортиоксетина (✖).
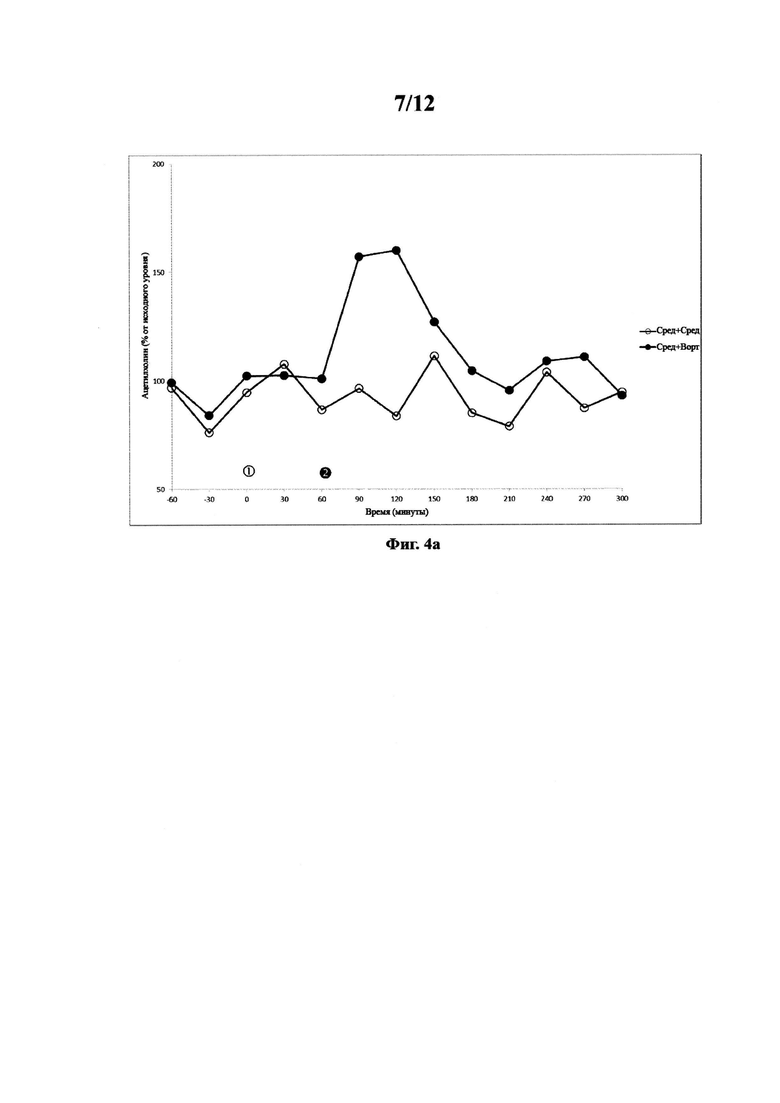
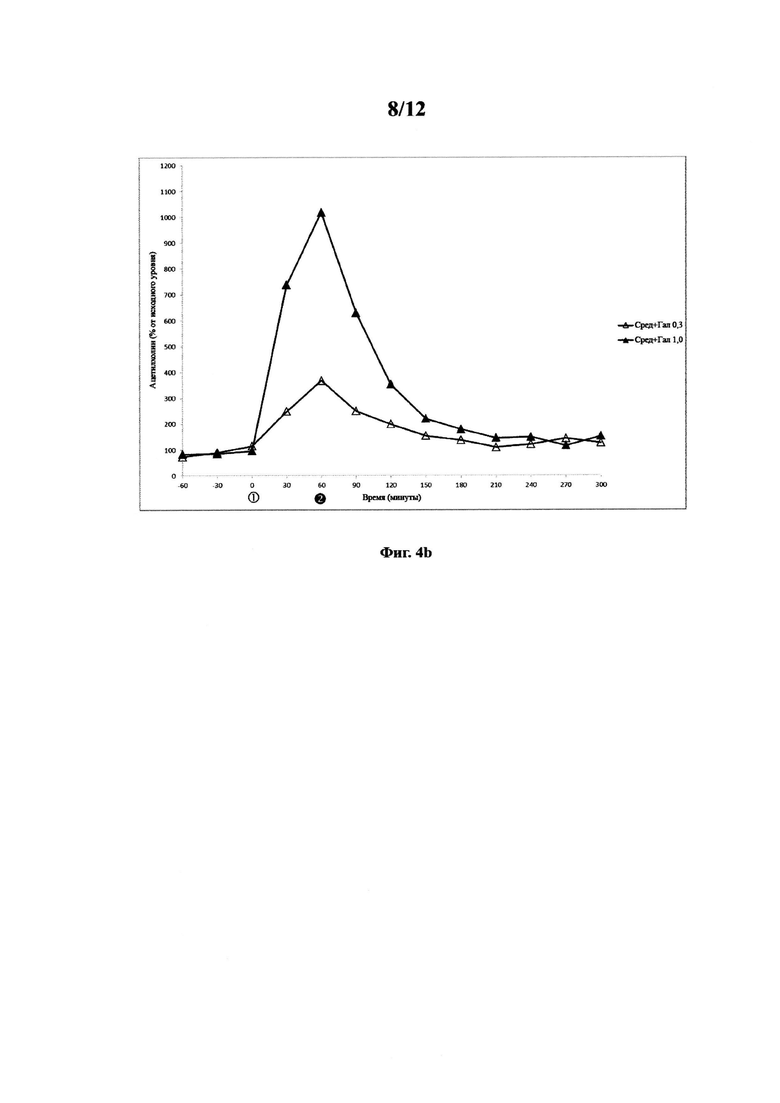
Фигура 4. Фармакодинамический ацетилхолиновый ответ в вентральном гиппокампе у свободно двигающихся крыс после комбинированного введения вортиоксетина и галантамина. Фигура 4а. Ацетилхолиновый ответ на среду (инъецируемую на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (
) ( ); и среду (инъецируемую на
); и среду (инъецируемую на  ) и вортиоксетин в дозе 10 мг/кг (инъецируемый на
) и вортиоксетин в дозе 10 мг/кг (инъецируемый на  ) (●). Фигура 4b. Ацетилхолиновый ответ на галантамин в дозе 0,3 мг/кг (инъецируемый на
) (●). Фигура 4b. Ацетилхолиновый ответ на галантамин в дозе 0,3 мг/кг (инъецируемый на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (Δ); и галантамин в дозе 1,0 мг/кг (инъецируемый на
) (Δ); и галантамин в дозе 1,0 мг/кг (инъецируемый на  ) и среду (инъецируемую на
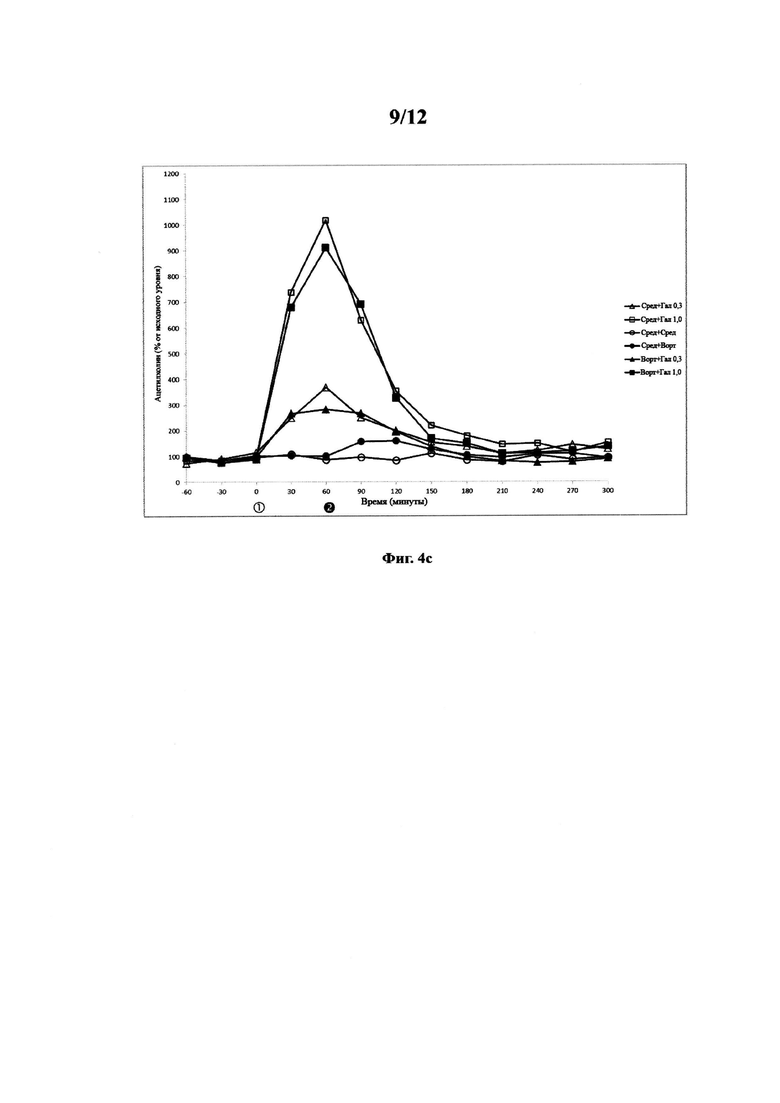
) и среду (инъецируемую на  ) (▲). Фигура 4С. Ацетилхолиновый ответ на среду (инъецируемую на
) (▲). Фигура 4С. Ацетилхолиновый ответ на среду (инъецируемую на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (
) ( ); среду (инъецируемую на
); среду (инъецируемую на  ) и вортиоксетин в дозе 10 мг/кг (инъецируемый на
) и вортиоксетин в дозе 10 мг/кг (инъецируемый на  ) (●); галантамин в дозе 0,3 мг/кг (инъецируемый на
) (●); галантамин в дозе 0,3 мг/кг (инъецируемый на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (Δ); галантамин в дозе 1,0 мг/кг (инъецируемый на
) (Δ); галантамин в дозе 1,0 мг/кг (инъецируемый на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (□); галантамин в дозе 0,3 мг/кг (инъецируемый на
) (□); галантамин в дозе 0,3 мг/кг (инъецируемый на  ) и вортиоксетин в дозе 10 мг/кг (инъецируемый на
) и вортиоксетин в дозе 10 мг/кг (инъецируемый на  ) (▲); и галантамин в дозе 1,0 мг/кг (инъецируемый на
) (▲); и галантамин в дозе 1,0 мг/кг (инъецируемый на  ) и вортиоксетин в дозе 10 мг/кг (инъецируемый на
) и вортиоксетин в дозе 10 мг/кг (инъецируемый на  ) (■).
) (■).
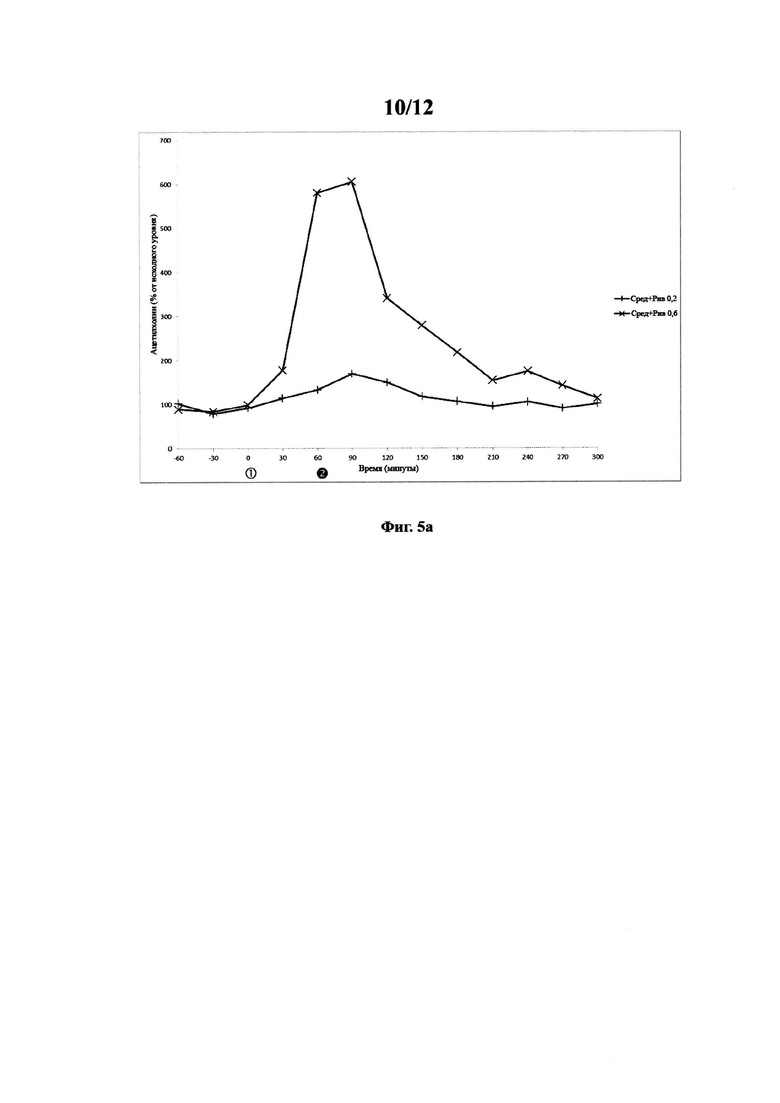
Фигура 5. Фармакодинамический ацетилхолиновый ответ в вентральном гиппокампе у свободно двигающихся крыс после комбинированного введения вортиоксетина и ривастигмина. Фигура 5а. Ацетилхолиновый ответ на ривастигмин в дозе 0,2 мг/кг (инъецируемый на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (+); и ривастигмин в дозе 0,6 мг/кг (инъецируемый на
) (+); и ривастигмин в дозе 0,6 мг/кг (инъецируемый на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (х). Фигура 5b.
) (х). Фигура 5b.
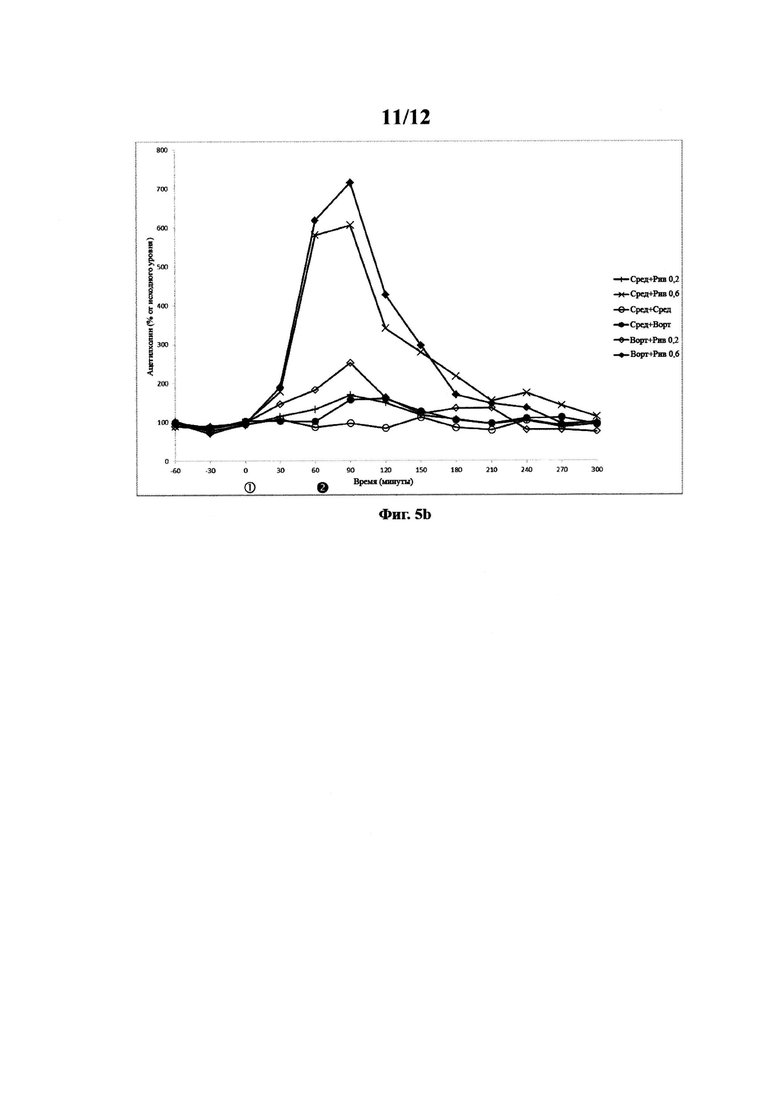
Ацетилхолиновый ответ на среду (инъецируемую на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (
) ( ); среду (инъецируемую на
); среду (инъецируемую на  ) и вортиоксетин в дозе 10 мг/кг (инъецируемый на
) и вортиоксетин в дозе 10 мг/кг (инъецируемый на  ) (●); ривастигмин в дозе 0,2 мг/кг (инъецируемый на
) (●); ривастигмин в дозе 0,2 мг/кг (инъецируемый на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (+); ривастигмин в дозе 0,6 мг/кг (инъецируемый на
) (+); ривастигмин в дозе 0,6 мг/кг (инъецируемый на  ) и среду (инъецируемую на
) и среду (инъецируемую на  ) (х); ривастигмин в дозе 0,2 мг/кг (инъецируемый на
) (х); ривастигмин в дозе 0,2 мг/кг (инъецируемый на  ) и вортиоксетин в дозе 10 мг/кг (инъецируемый на
) и вортиоксетин в дозе 10 мг/кг (инъецируемый на  ) (
) ( ); и ривастигмин в дозе 0,6 мг/кг (инъецируемый на
); и ривастигмин в дозе 0,6 мг/кг (инъецируемый на  ) и вортиоксетин в дозе 10 мг/кг (инъецируемый на
) и вортиоксетин в дозе 10 мг/кг (инъецируемый на 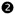 ) (
) ( ).
).
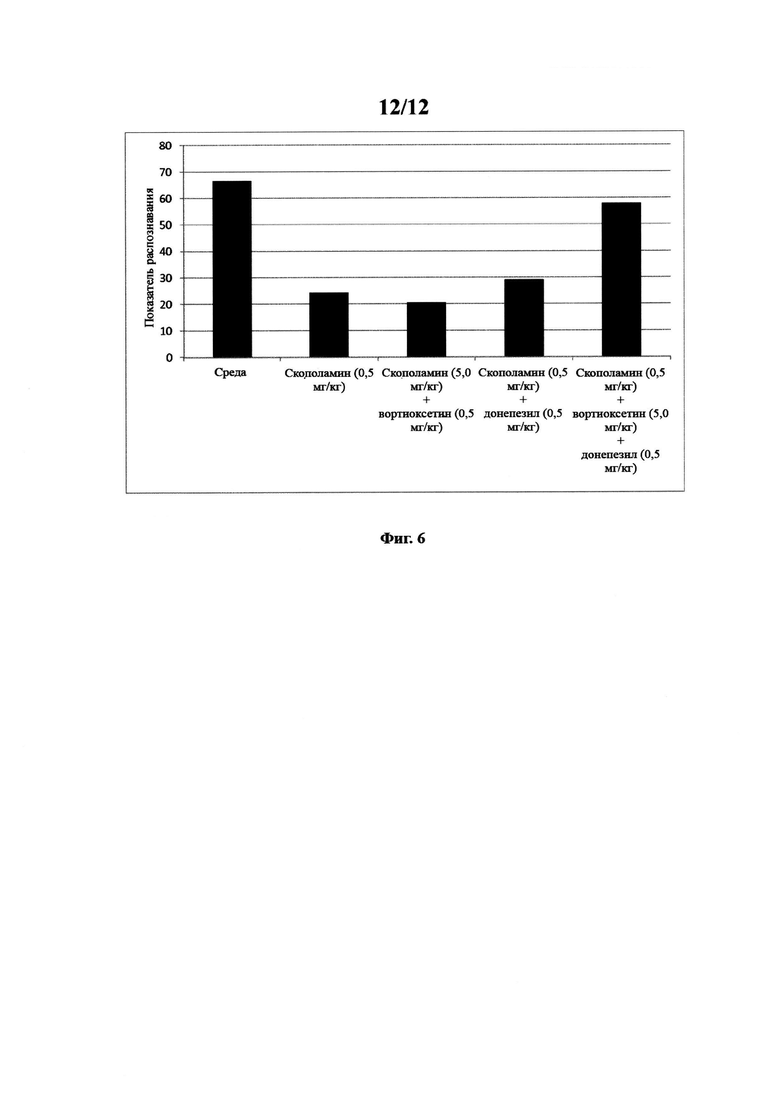
Фигура 6. Показатель распознавания, полученный при распознавании нового объекта крысами, обработанными средой: скополамином (0,5 мг/кг); скополамином (0,5 мг/кг) + вортиоксетином (5 мг/кг); скополамином (0,5 мг/кг) + донепезилом (0,5 мг/кг) или скополамином (0,5 мг/кг) + вортиоксетином (5 мг/кг) + донепезилом (0,5 мг/кг).
Подробное описание изобретения
Настоящее изобретение охватывает применение вортиоксетина для лечения когнитивной дисфункции. В контексте настоящего изобретения ʺвортиоксетинʺ включает вортиоксетин в качестве свободного основания и в качестве фармацевтически приемлемой соли. Отдельно отмечают соль, являющуюся HBr, соль, являющуюся тартратом, и соль, являющуюся (DL)-лактатом.
Молекулярная структура вортиоксетина, представляющего собой свободное основание, показана ниже.
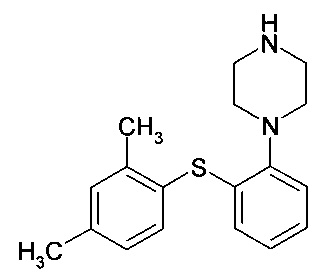
Настоящее изобретение охватывает применение донепезила для лечения когнитивной дисфункции. В контексте настоящего изобретения ʺдонепезилʺ включает донепезил в качестве свободного основания и в качестве фармацевтически приемлемой соли. Отдельно отмечают соль HCl.
Молекулярная структура донепезила, представляющего собой свободное основание, показана ниже.
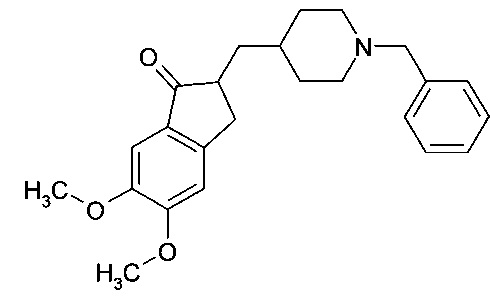
Говоря более общими терминами, указанные фармацевтически приемлемые соли являются солями присоединения кислоты нетоксичных кислот. Указанные соли включают соли органических кислот, таких как малеиновая, фумаровая, бензойная, аскорбиновая, янтарная, щавелевая, бис-метиленсалициловая, метансульфоновая, этандисульфоновая, уксусная, пропионовая, винная, салициловая, лимонная, глюконовая, молочная, оксиянтарная, миндальная, коричная, цитраконовая, аспарагиновая, стеариновая, пальмитиновая, итаконовая, гликолевая, р-аминобензойная, глутаминовая, бензолсульфоновая, теофиллинуксусная кислоты, а также 8-галогентеофиллины, например, 8-бромтеофиллин. Указанные соли также могут быть солями неорганических солей, таких как хлористоводородная, бромистоводородная, серная, сульфаминовая, фосфорная и азотная кислоты.
Способ получения вортиоксетина раскрыт в международных патентных заявках, опубликованных как WO 03/029232, WO 2007/144005 и WO 2010/094285. Донепезил легкодоступен от множества коммерческих поставщиков.
Комбинированное введение вортиоксетина и донепезила может принимать форму совместного введения. В данном варианте осуществления вортиоксетин и донепезил вводят пациенту фактически в одно и то же время либо в виде формы введения, которая содержит как вортиоксетин, так и донепезил, либо в виде отдельных форм введения, т.е. при этом первая форма введения содержит вортиоксетин, а вторая форма введения содержит донепезил.
В альтернативном случае, комбинированное введение вортиоксетина и донепезила предусматривает временной интервал между введением вортиоксетина и введением донепезила. В данном варианте осуществления можно вводить первым либо вортиоксетин, либо донепезил. Как подтверждено данными, показанными в части описания ʺПримерыʺ, между вортиоксетином и донепезилом существует синергетический эффект. Указанный синергетический эффект зависит от наличия фармакологически релевантных количеств как вортиоксетина, так и донепезила в организме в одно и то же время. Таким образом устанавливается верхний предел временного интервала, который может быть между введением вортиоксетина и введением донепезила. В практическом плане синергетический эффект возможно снизиться, если введение вортиоксетина и введение донепезила будет происходить с интервалом более чем приблизительно 2 периода полувыведения первого из двух вводимых соединений. В одном варианте осуществления введение двух соединений происходит с интервалом 0-1 период полувыведения первого вводимого соединения. В контексте настоящего изобретения ʺпериод полувыведенияʺ является временем, необходимым для того, чтобы уровень фармацевтически активного ингредиента в плазме достиг 50% от первоначального значения.
Период полувыведения донепезила у людей составляет приблизительно 70 часов [xPharm: The Comprehensive Pharmacology Reference, 1-5, Elsevier, 2007].
Период полувыведения вортиоксетина у людей составляет приблизительно 57 часов [Basic&Clin Pharm&Tox, 111, 198-205, 2012].
Вортиоксетин, как правило, вводят в количестве 1-100 мг/день, как, например, 1-50 мг/день, как например, 5, 10, 15, 20 или 30 мг/день.
Донепезил, как правило, вводят в количестве 1-100 мг/день, как, например, 1-30 мг/день, как например, 1, 5, 15 или 25 мг/день.
Данную ежедневную дозу вортиоксетина и донепезила можно вводить за один раз или за два раза, или за большее количество раз.
Как показано в части описания ʺПримерыʺ, комбинированное введение вортиоксетина и донепезила вызывает синергетический эффект в отношении уровней ацетилхолина в головном мозге. Более того, в части описания ʺПримерыʺ показано, что комбинированное введение других ингибиторов ацетилхолинэстеразы, таких как галантамин и ривастигмин, не приводит к такому синергетическому эффекту. Таким образом данные показывают, что комбинация вортиоксетина/донепезила обладает свойствами, которые являются исключительными для данной конкретной комбинации и не присущи комбинациям вортиоксетина и других ингибиторов ацетилхолинэстеразы.
Данное открытие далее подтверждается экспериментом, описанным в примере 5, в котором исследовали у крыс воздействие донепезила и вортиоксетина на память. Применяемый тест является тестом на распознавание нового объекта, который является общепризнанным способом для оценки воздействия данного лечения на память. Тест основан на естественной склонности крыс исследовать новые объекты окружающей среды, в которой они находятся, и с его помощью определяют степень, в которой крысы помнят объекты, которые им уже были доступны. При фазе ознакомления крысам позволяли исследовать окружающую среду помещения для испытания и два объекта, которые отличались по форме, цвету и текстуре. При фазе теста один из объектов меняли с тем, чтобы крысам был доступен один новый объект и один знакомый объект. Время, затраченное на исследование нового и знакомого объектов, записывали после введения тестовых соединений. По результатам в примере 5 видно, что вортиоксетин в дозе 5 мг/кг не компенсирует нарушение памяти, вызванное 0,5 мг/кг скополамина. Подобным образом, донепезил в дозе 0,5 мг/кг не компенсирует нарушение памяти, вызванное 0,5 мг/кг скополамина. Однако примечательно, что вортиоксетин и донепезил в этих дозах, ниже эффективных, при совместном введении вызывают значительное улучшение памяти крыс. По результатам данной поведенческой модели видно, что синергическое повышение уровней ацетилхолина, показанное в примерах 1-4, по-видимому отражается в поведении крыс.
Вовлечение рецепторов у крыс после введения вортиоксетина исследовали в J pharmacol Exp Ther. 340, 345-366, 2012 и Eur Neuropsychopharm, 23, 133-145, 2013. По результатам видно, что вортиоксетин в дозе 5-10 мг/кг дает фактически полное вовлечение соответствующих мишеней, как, например, транспортера серотонина, 5-НТ3-рецептора и 5-HT1B-рецептора. Вовлечение транспортера серотонина у людей исследовали в Basic & Clin Pharmacol &Тох, 110, 401-404, 2012. Было обнаружено, что 5, 10 и 20 мг/день дает вовлечение 51, 63 и 90%, соответственно. Взаимосвязь между концентрацией донепезила в плазме и ингибированием ацетилхолинэстеразы исследовали в Neurol, 50, 136-145, 1998. Было обнаружено, что концентрация в плазме равная ~20 нг/мг вызывает ~60% ингибирование и что концентрация в плазме равная ~6 нг/мл вызывает 15% ингибирование. В связи с этим также отмечают, что активные последовательности ацетилхолинэстеразы человека (Uniprot Р22303) и Ratus Norvegucus (Uniprot Р37136) обладают приблизительно 90% идентичностью. На фоне этого и помня об уровнях в плазме, описанных в примере 1, делают вывод, что исследуемый уровень вортиоксетина (5-10 мг/кг) соответствует клинической дозе 5-20 мг вортиоксетина в день для людей. Подобным образом исследуемая доза донепезила 0,3 мг/кг соответствует дозе, ниже эффективной, тогда как доза в 1 мг/кг соответствует клинической дозе в 5-25 мг в день для людей.
Одобренная поддерживающая доза (FDA) для донепезила составляет 10 или 23 мг в день с 5 мг в качестве начальной дозы. Таким образом, в одном варианте осуществления настоящее изобретение относится к введению 1 мг или более, как, например, 2 мг или более, как например, 5 мг или более, как например, 10 мг или более донепезила в день в комбинации с вортиоксетином, как правило введенного в дозе 1, 5, 15 или 20 мг в день. Отдельные примеры включают 5-10 мг донепезила в комбинации с 5-20 мг, как например, 10 или 15 мг вортиоксетина в день. Отдельные примеры включают 10-25 мг донепезила, как, например, 23 мг донепезила, в комбинации с 5-20 мг, как, например, 10 или 15 мг вортиоксетина в день.
Активные фармацевтические ингредиенты, используемые в настоящем изобретении, т.е. вортиоксетин и донепезил, можно вводить отдельно в качестве чистых соединений или в комбинации с фармацевтически приемлемыми носителями или наполнителями либо в однократных, либо многократных дозах. Фармацевтические композиции в соответствии с настоящим изобретением можно составлять с фармацевтически приемлемыми носителями или разбавителями, а также любыми другими известными вспомогательными средствами и наполнителями согласно традиционным методикам, таким как раскрытые в Remington: The Science and Practice of Pharmacy, 21 Edition, Hauber, Ed., Lippincott Williams & Wilkins, 2006.
Фармацевтические композиции можно специально составлять для введения любым подходящим путем, таким как пероральный, ректальный, назальный, легочный, местный (в том числе трансбуккальный и подъязычный), чрескожный, интрацистернальный, внутрибрюшинный, вагинальный и парентеральный (в том числе подкожный, внутримышечный, интратекальный, внутривенный и внутрикожный) путь, при этом пероральный путь является предпочтительным. Следует принять во внимание, что предпочтительный путь может зависеть от общего состояния и возраста подлежащего лечению субъекта, природы подлежащего лечению состояния и выбранного активного ингредиента.
Фармацевтические композиции для перорального введения включают твердые лекарственные формы, такие как капсулы, таблетки, драже, пилюли, таблетки для рассасывания, порошки и гранулы. При необходимости они могут быть получены с покрытиями.
Жидкие лекарственные формы для перорального введения включают растворы, эмульсии, суспензии, сиропы и эликсиры.
Фармацевтические композиции для парентерального введения включают стерильные водные и неводные инъекционные растворы, дисперсии, суспензии или эмульсии, а также стерильные порошки, подлежащие ресуспендированию в стерильных инъекционных растворах или дисперсиях перед применением.
Другие подходящие формы введения включают суппозитории, аэрозоли, мази, кремы, гели, ингаляторы, кожные пластыри, имплантаты и т.д.
Для парентерального введения можно использовать растворы соединения согласно настоящему изобретению в стерильном водном растворе, водном пропиленгликоле, водном витамине Е или кунжутном или арахисовом масле. При необходимости, такие водные растворы должны быть подходящим образом забуферены, если необходимо, а жидкий разбавитель сначала делают изотоническим с помощью достаточного количества солевого раствора или глюкозы. Водные растворы являются особенно подходящими для внутривенного, внутримышечного, подкожного и внутрибрюшинного введения. Все используемые стерильные водные среды легкодоступны при помощи стандартных методик, известных специалисту в данной области.
Подходящие фармацевтические носители включают инертные твердые разбавители или наполнители, стерильный водный раствор и различные органические растворители. Примерами твердых носителей являются лактоза, сульфат кальция, сахароза, циклодекстрин, тальк, желатин, агар, пектин, аравийская камедь, стеарат магния, стеариновая кислота и низшие алкиловые эфиры целлюлозы. Примерами жидких носителей являются сироп, арахисовое масло, оливковое масло, фосфолипиды, жирные кислоты, амины жирных кислот, полиоксиэтилен и вода. Фармацевтические композиции, образованные путем объединения соединения, используемого в настоящем изобретении, и фармацевтических приемлемых носителей, затем легко вводят при помощи множества лекарственных форм, подходящих для раскрытых путей введения.
Составы согласно настоящему изобретению, подходящие для перорального введения, могут быть представлены в виде дискретных единиц, таких как капсулы или таблетки, при этом каждая содержит заранее определенное количество активного ингредиента, и любая может включать подходящий наполнитель. Кроме того, перорально доступные составы могут иметь форму порошка или гранул, раствора или суспензии в водной или неводной жидкости или жидкой эмульсии масло-в-воде или вода-в-масле.
Если твердый носитель применяют для перорального введения, то препарат может быть в форме таблетки, например, помещенным в твердую желатиновую капсулу, в форме порошка или гранул, или в форме пастилки или таблетки для рассасывания. Количество твердого носителя может варьироваться, но, как правило, будет составлять от приблизительно 25 мг до приблизительно 1 г.
Если используют жидкий носитель, то препарат может иметь форму сиропа, эмульсии, мягкой желатиновой капсулы или стерильной инъекционной жидкости, такой как водная или неводная жидкая суспензия или раствор.
Таблетки можно получать путем смешивания активного ингредиента со стандартными вспомогательными средствами и/или разбавителями с последующим прессованием смеси в традиционной таблеточной машине. Примеры вспомогательных средств или разбавителей включают: кукурузный крахмал, картофельный крахмал, стеатит, стеарат магния, желатин, лактозу, камеди и т.п. Можно использовать любые другие вспомогательные средства или добавки, обычно применяемые для таких целей, как например, красящие вещества, ароматизирующие вещества, консерванты и т.п., при условии, что они совместимы с активными ингредиентами.
В целях удобства, соединения согласно настоящему изобретению вводят в единичной лекарственной форме, содержащей каждого, вортиоксетина и донепезила, в количестве от приблизительно 1 до 100 мг. В частности, однократная доза вортиоксетина может составлять 5, 10, 15, 20 или 25 мг. В частности, однократная доза донепезила может составлять 1, 2, 5, 10, 15, 20 или 25 мг.
Когнитивная дисфункция включает ослабление когнитивных функций или ухудшение владения когнитивными функциями, например, рабочей памяти, внимания и бдительности, вербального обучения и памяти, зрительного обучения и памяти, рассуждения и решения проблем, например, способности к целенаправленной деятельности, скорости обработки информации и/или социального познания. В частности, дисфункция может означать нарушения внимания, дезорганизованное мышление, медленное мышление, трудности в понимании, недостаточную концентрацию, нарушение функции решения проблем, слабую память, трудности при высказывании мыслей и/или трудности в сведении воедино мыслей, чувств и поведения или трудности в пресечении неподходящих мыслей. Деменция является проявлением когнитивной дисфункции. Выражения ʺкогнитивные расстройстваʺ и ʺнарушение когнитивных функцийʺ можно использовать синонимично с ʺкогнитивной дисфункциейʺ.
Как указано выше, когнитивная дисфункция составляет важную часть клинического проявления при ряде заболеваний ЦНС. В отношении некоторых заболеваний ЦНС, когнитивная дисфункция является первичным проявлением заболевания, такого как, например, болезнь Альцгеймера. В отношении других заболеваний, таких как депрессия, когнитивная дисфункция может составлять часть клинического проявления заболеваний, но она также в значительной степени не зависима от депрессии. К примеру, наблюдали, что результаты при оценке масштабов лечения когнитивной дисфункции и депрессии не шли параллельно при клинических испытаниях с антидепрессантами на пациентах, находящихся в депрессии. Часто когнитивная дисфункция сохраняется при выздоравливании от симптомов депрессии. На этом фоне полагают, что комбинированное введение вортиоксетина и донепезила полезно при лечении деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при HIV (вирусе иммунодефицита человека), деменции у злоупотребляющих лиц (алкоголем или лекарственными средствами), MCI (умеренного когнитивного нарушения), когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией.
В одном варианте осуществления настоящее изобретение относится к способу лечения заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при HIV (вирусе иммунодефицита человека), деменции у злоупотребляющих лиц (алкоголем или лекарственными средствами), MCI (умеренного когнитивного нарушения); когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией, при этом способ включает комбинированное введение терапевтически эффективного количества вортиоксетина и донепезила пациенту, нуждающемуся в этом.
В одном варианте осуществления настоящее изобретение относится к применению вортиоксетина и донепезила для производства лекарственного препарата для лечения заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при HIV (вирусе иммунодефицита человека), деменции у злоупотребляющих лиц (алкоголем или лекарственными средствами), MCI (умеренного когнитивного нарушения) когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией.
В одном варианте осуществления настоящее изобретение относится к вортиоксетину и донепезилу для комплексного применения в способе лечения заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при HIV (вирусе иммунодефицита человека), деменции у злоупотребляющих лиц (алкоголем или лекарственными средствами), MCI (умеренного когнитивного нарушения), когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией.
ʺТерапевтически эффективное количествоʺ соединений, используемое в данном документе, означает количество, достаточное для излечения, облегчения или частично угнетения клинических проявлений данного заболевания и его осложнений при терапевтическом мероприятии, включающем введение указанных соединений. Количество, достаточное для осуществления этого, определяют как ʺтерапевтически эффективное количествоʺ. Эффективные количества для каждой цели будут зависеть от тяжести заболевания или повреждения, а также от веса и общего состояния субъекта.
Выражения ʺлечениеʺ и ʺпроцесс леченияʺ, используемые в данном документе, означают ведение больного и уход за ним с целью борьбы с состоянием, таким как заболевание или расстройство. Выражения предназначены включать полный спектр мероприятий по лечению данного состояния, от которого страдает пациент, как, например, введение активных соединений для облегчения симптомов или осложнений, для отсрочки прогрессирования состояния и/или для излечения или устранения состояния. Подлежащим лечению пациентом предпочтительно является млекопитающее, в частности человек.
Все литературные источники, в том числе публикации, патентные заявки и патенты, цитируемые в данном документе, включены в данное описание посредством ссылки во всей своей полноте и в той же степени, как если бы каждый литературный источник был отдельно и конкретно обозначен как включенный посредством ссылки и приведен во всей своей полноте в данном документе (в максимальной степени, допускаемой законом), вне зависимости от любого другого отдельно сделанного в любом месте данного документа включения конкретных документов.
Использование в контексте описания настоящего изобретения форм единственного числа и аналогичных ссылок следует понимать как охватывающие как единственное, так и множественное число, если в данном документе не указано иное или это однозначно не противоречит контексту. Например, выражение ʺсоединениеʺ следует понимать как относящееся к различным ʺсоединениямʺ согласно настоящему изобретению или конкретному описываемому аспекту, если не указано иное.
Описание в данном документе любого аспекта или аспекта настоящего изобретения с использованием выражений, таких как ʺвключающийʺ, ʺимеющийʺ, ʺв том числеʺ или ʺсодержащийʺ по отношению к элементу или элементам предназначено для подтверждения аналогичного аспекта или аспекта настоящего изобретения, который ʺсостоит изʺ, ʺсостоит главным образом изʺ этого конкретного элемента или элементов или ʺпо сути содержитʺ их, если не указано иное или это однозначно не противоречит контексту (например, композиция, описанная в данном документе как содержащая определенный элемент, должна также пониматься как описывающая композицию, состоящую из этого элемента, если не указано иное или это однозначно не противоречит контексту).
Примеры
Количество вводимого соединения показано как количество соответствующего свободного основания.
Пример 1. Действия вортиоксетина и донепезила на уровни ацетилхолина в гиппокампе свободно двигающихся крыс
Для эксперимента использовали взрослых крыс Wistar мужского пола. Крысам перед операцией давали наркоз. Каждое животное помещали в стереотаксическую рамку (Kopf Instruments, США) и на верхней части черепа делали надрез. Зонд для микродиализа с подверженной воздействию поверхностью в 4 мм2 (мембрана из полиакрилонитрила, Brainlink, Нидерланды) имплантировали в вентральный гиппокамп. Координаты составляли АР=-5,3 мм (по отношению к брегме), латерально +4,8 мм (по отношению к средней линии), вентрально -8,0 мм (по отношению к твердой мозговой оболочке), зубной держатель устанавливали на -3,3 мм [Paxinos and Watson, The rat brain in stereotaxic coordinates, Academic Press, 6th edition, New York, 2008]. Зонды прикрепляли к черепу при помощи шурупов из нержавеющей стали и зубного цемента. Эксперименты начинали через один день после выздоровления.
HBr вортиоксетина готовили в 10% 2-гидроксипропил-β-циклодекстрина в дозе 0, 5 или 10 мг/мл. HCl донепезила готовили в сверхчистой воде в дозе 0, 0,3 или 1,0 мг/мл. Вортиоксетин вводили подкожно, а донепезил вводили внутрибрюшинно.
В день эксперимента зонд для микродиализа соединяли гибкой трубкой из PEEK с насосом для микроперфузии (Harvard) и перфузировали искусственной спинномозговой жидкостью, содержащей 147 мМ NaCl, 3,0 мМ KCl, 1,2 мМ CaCl2 и 1,2 мМ MgCl2, при скорости потока 1,5 мкл/мин. Через два часа предварительной стабилизации собирали образцы (30 мкл) и хранили в 20 мМ муравьиной кислоте и 0,04% аскорбиновой кислоте (10 мкл).
Концентрацию ацетилхолина в образцах определяли при помощи HLPC с тандемной масс-спектрометрией (MS/MS), при этом для выявления использовали ацетил-β-метил-холин в качестве внутреннего стандарта. Хроматографическое разделение выполняли на колонке для обращенно-фазовой хроматографии Phenomenex Synergi Max-RP (2,0×150 мм, размер частиц 4 мкм) при 50°С. Компоненты разделяли при помощи изократического потока элюента А (20 мМ ацетата аммония, 5% ацетонитрила и 0,3% трифторуксусной кислоты) при скорости потока 0,25 мл/мин.
MS-анализы выполняли при помощи системы API 3000 MS/MS, состоящей из детектора API 3000 MS/MS и интерфейса турбоэлектрического ионизатора. Регистрации осуществляли в режиме положительной ионизации с напряжением при ионораспылении установленным на 4,5 кВ и температурой зонда на 550°С. Прибором управляли в режиме мониторинга множественных реакций.
Среднее значение трех образцов, взятых перед введением, было установлено на 100%. Если образцы для сравнения составляли <50% или >150%, их считали выпавшими точками и не использовали для расчета исходного уровня. Все образцы, полученные после введения, выражали как процент от исходного уровня того же субъекта. Время и эффекты обработки сравнивали при помощи двухфакторного ANOVA для повторяющихся измерений с последующим тестом Стьюдента-Ньюмана-Кейлса по полученным результатам. Значимость определяли как p<0,05.
Группы из пяти животных подвергали воздействию комбинации вортиоксетина (среда, 5 мг/кг и 10 мг/кг sc) и донепезила (среда, 0,3 мг/г и 1 мг/кг ip), вводимых одновременно. Данные показаны на фигурах 1а-с и 2а-b.
Кроме того, образцы крови брали от каждого животного для измерения уровней в плазме активных ингредиентов. В таблице 1, ниже, показаны результаты.
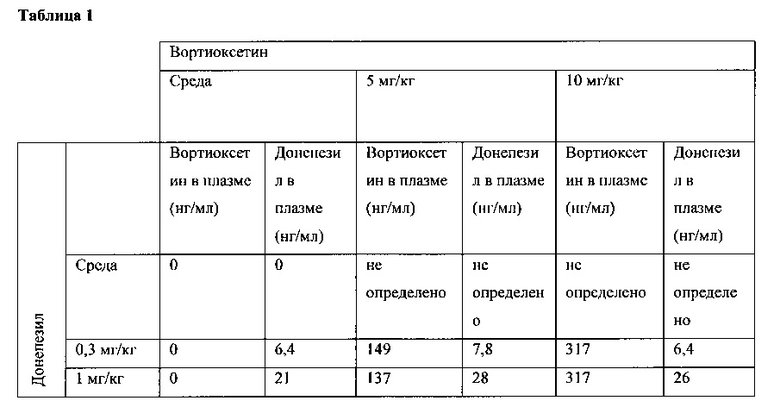
Данные в вышеупомянутой таблице показывают, что животных действительно подвергали воздействию двух активных ингредиентов и что сопоставимые уровни были обнаружены на протяжении экспериментов.
Данные, полученные для уровней ацетилхолина в вентральном гиппокампе и изображенные на фигурах 1а-с и 2а-b, показывают, что уровни ацетилхолина при 10 мг/кг вортиоксетина и 1 мг/кг донепезила были значительно повышены по сравнению с уровнями ацетилхолина при любой другой обработке. Данные также показывают, что уровни ацетилхолина при 5 мг/кг вортиоксетина и 1 мг/кг донепезила были значительно повышены по сравнению с уровнями ацетилхолина при любом уровне вортиоксетина при 0 и 0,3 мг/кг донепезила. Данные также показывают, что введение донепезила в дозе 1 мг/кг и среды значительно повышает уровни ацетилхолина по сравнению с обработкой среда + среда.
Пример 2. Действие вортиоксетина на уровни ацетилхолина в гиппокампе свободно двигающихся крыс
Данный эксперимент осуществляли, главным образом, как описано в примере 1. Аналитическую установку слегка видоизменяли как указано далее.
Хроматографическое разделение выполняли на аналитической колонке с обращенной фазой 150×2,00 мм (4 мкм) (Phenomenex Synergy MAX-RP, Bester), защищенной защитной колонкой 4×2,0 мм (Phenomenex Synergy MAX-RP AJO-6073, Bester), обе поддерживали при температуре 30°С. Подвижная фаза (изократическая) состояла из воды, ацетонитрила (ACN) и трифторуксусной (TFA) кислоты (вода: ACN:TFA=95,0:5:0,1 объем/объем/объем %) при скорости потока 0,200 мл/мин.
MS-анализы выполняли с помощью системы API 3000 MS/MS, состоящей из детектора API 3000 MS/MS и интерфейса турбоэлектрического ионизатора (оба от Applied Biosystems, Ниднрланды). Регистрацию выполняли в режиме положительной ионизации с напряжением при ионораспылении, установленным на 5,5 кВ, с температурой зонда 450°С.
Группы из пяти животных подвергали воздействию вортиоксетина (среда, 2,5 мг/кг, 5 мг/кг и 10 мг/кг sc). Данные показаны на фигуре 3.
Результаты, полученные в примерах 1 и 2 ясно устанавливают, что внеклеточные уровни ацетилхолина, полученные как результат комбинированного введения вортиоксетина и донепезила, значительно выше, чем уровни, полученные при отдельном введении вортиоксетина и донепезила. То есть, был показан синергетический эффект в отношении уровней ацетилхолина между вортиоксетином и донепезилом.
Синергетический эффект между двумя фармацевтически активными соединениями можно применять по меньшей мере двумя путями. Дозы, обычно применяемые в монолечении, использующем два фармацевтически активных соединения, можно сохранять при комплексном лечении и можно достигать эффекта более, чем ожидаемый клинический эффект. В альтернативном случае, дозы, ниже, чем обычно, применяемые в монолечении, использующем два фармацевтически активных соединения, можно применять по отношению к любому или к обоим соединениям для поддержания клинического эффекта, однако при меньшей экспозиции лекарственного средства. Меньшая экспозиция препарата может быть выгодной, поскольку можно ожидать увеличения побочных явлений с увеличением содержания лекарственного средства.
Пример 3. Действия вортиоксетина и галантамина на уровни ацетилхолина в гиппокампе свободно двигающихся крыс
Для экспериментов использовали взрослых крыс Sprague Dawley мужского пола. Крысам перед операцией давали наркоз. Животных помещали в стереотаксическую рамку (Kopf instruments, США) и имплантироавли направляющую канюлю СМА12 (СМА Microdialysis, Швеция), нацеленную на вентральный гиппокамп. Координаты для концов зондов составляли АР=-5,3 мм по отношению к брегме, латерально (ML)=-4,8 мм по отношению к средней линии и вентрально =-8,0 мм по отношению к твердой мозговой оболочке (Paxinos and Watson).
Галантамин, химическим названием которого является (4aS,6R,8aS)-4а,5,9,10,11,12-гексагидро-3-метокси-11-метил-6Н-бензофуро[3а,3,2-ef][2]бензазипин-6-ол, вводили в виде соли, представляющей собой НВr. Вортиоксетин вводили в виде соли, представляющей собой HBr. Вортиоксетин и галантамин готовили в 0,9% солевом растворе. Вортиоксетин вводили подкожно в дозе 10 мг/кг и галантамин вводили подкожно в дозе 0,3 мг/кг и 1,0 мг/кг.
За день до эксперимента зонд для микродиализа (СМА/12, 4 мм, PAES, MWKO 100 кДа) вставляли в соответствующую направляющую канюлю крыс в сознании. Зонды перфузировали при постоянной скорости потока в 1 мкл/мин. стерильной искусственной спинномозговой жидкостью, содержащей 148 мМ NaCl, 4 мМ KCl, 0,8 мМ MgCl2, 1,4 мМ CaCl2, 1,2 мМ Na2HPO4, 0,3 мМ NaH2PO4, pH 7,2. В день эксперимента образцы собирали с интервалами в 30 мин. перед введением для определения исходного уровня. Данные представлены как процент исходного уровня того же животного. Значимость определяли как p<0,05. Животные получали обработки согласно экспериментальному протоколу и образцы собирали с интервалами в 30 минут.
Концентрацию ацетилхолина в образцах определяли с помощью системы Waters Acquity HPLC, оснащенной колонкой для частиц Sunshell RP-Aqua 2,1×100 мм, 2,6 мкм с присоединенным тройным квадрупольным масс-спектрометром Waters Quattro Premier ХЕ, работающим в режиме MS/MS. Компоненты разделяли с помощью изократического потока элюента А (100 мМ ацетата аммония в воде milliQ).
Группы по 6-8 животных подвергали воздействию комбинаций вортиоксетина (среда и 10 мг/кг) и галантамина (среда, 0,3 мг/кг и 1,0 мг/кг). Инъекцию галантамина делали за 60 минут до инъекции вортиоксетина. Полученные данные показаны на фигурах 4а-4с.
Данные показывают, что введение галантамина в дозах 0,3 и 1,0 мг/кг вызывает дозозависимое значительное повышение уровней ацетилхолина в гиппокампе свободно двигающихся крыс. Результаты также показывают, что введение вортиоксетина в дозе 10 мг/кг вызывает значительное повышение уровней ацетилхолина в гиппокампе свободно двигающихся крыс. Данные результаты подтверждают полученные сведения в примере 2. Данные также показывают, что введение галантамина в дозе 0,3 или 1,0 мг/кг в комбинации с дозами вортиоксетина не вызывает значительного повышения уровней ацетилхолина по сравнению с введением галантамина при любом уровне совместно со средой. Фактически, числовые значения уровней ацетилхолина ниже для комбинированного введения галантамина на любом уровне и вортиоксетина по сравнению с введением галантамина при любом уровне и среды. Важно отметить, что результаты примера 3 показывают, что комбинированное введение вортиоксетина и галантамина не оказывает синергетического эффекта на уровни ацетилхолина.
Пример 4. Действия вортиоксетина и ривастигмина на уровни ацетилхолина в гиппокампе свободно двигающихся крыс
Пример 4 осуществляли, главным образом, подобно примеру 3, за исключением тестовых соединений. Ривастигмин готовили в 0,9% солевом растворе и вводили подкожно в дозе 0,2 мг/кг и 0,6 мг/кг. Ривастигмин, химическим названием которого является (S)-N-этил-N-метил-3[1-(диметиламино)этил]-фенилкарбамат, вводили в виде соли, представляющей собой тартрат.
Полученные данные показаны на фигурах 5а-5b и фигуре 4а для тестов среда-среда.
Данные показывают, что введение ривастигмина в дозе 0,2 и 0,6 мг/кг дозозависимо и значительно повышает уровни ацетилхолина. Данные также показывают, что комбинированное введение вортиоксетина и ривастигмина в дозе 0,6 мг/кг не вызывает повышения уровней ацетилхолина по сравнению с введением ривастигмина и среды. Данные показывают, что комбинированное введение ривастигмина в дозе 0,2 мг/кг и вортиоксетина вызывает значительно более высокие уровни ацетилхолина по сравнению с введением ривастигмина в дозе 0,2 мг/кг и среды. Данные показывают, что сумма уровней ацетилхолина после введения вортиоксетина + среда и ривастигмина в дозе 0,2 мг/кг + среда не отличается от уровней ацетилхолина после комбинированного введения ривастигмина в дозе 0,2 мг/кг и вортиоксетина. Это показывает, что комбинированное введение вортиоксетина и ривастигмина в дозе 0,2 мг/кг вызывает аддитивный эффект в отношении уровней ацетилхолина в гиппокампе свободно двигающихся крыс. Важно отметить, что данные показывают, что комбинированное введение ривастигмина и вортиоксетина не вызывает синергетического эффекта в отношении уровней ацетилхолина в гиппокампе.
Пример 5. Действие донепезила и вортиоксетина на кратковременную эпизодическую память у крыс.
Задание по распознаванию нового объекта (NOR) использовали для оценки воздействия вортиоксетина и донепезила, отдельно или в комбинации, на память крыс с вызванным скополамином нарушением памяти. Использовали крыс Sprague-Dawley
На 1 день и 2 день эксперимента крысы осуществляли два сеанса для ознакомления с окружающей средой помещения для испытания, в том числе с двумя объектами (знакомыми объектами). Каждый сеанс длился 6 минут. Крыс, которые не исследовали объекты, или крыс, которые имели природное предпочтение по отношению к одному объекту по сравнению с другим, исключали из испытания. В день проведения теста пять групп крыс выполняли третий тест для ознакомления (испытание на осваивание), после которого их удаляли из приспособления для испытаний и один из объектов заменяли новым объектом. Четыре часа спустя крыс помещали обратно в приспособление для испытания (фаза теста) и записывали время, использованное для исследования знакомого объекта и нового объекта.
Пять групп крыс обрабатывали средой, скополамином, вортиоксетином, донепезилом и вортиоксетином + донепезил внутрибрюшинно, как указано далее. Номера в скобках означают количество крыс в каждой группе.
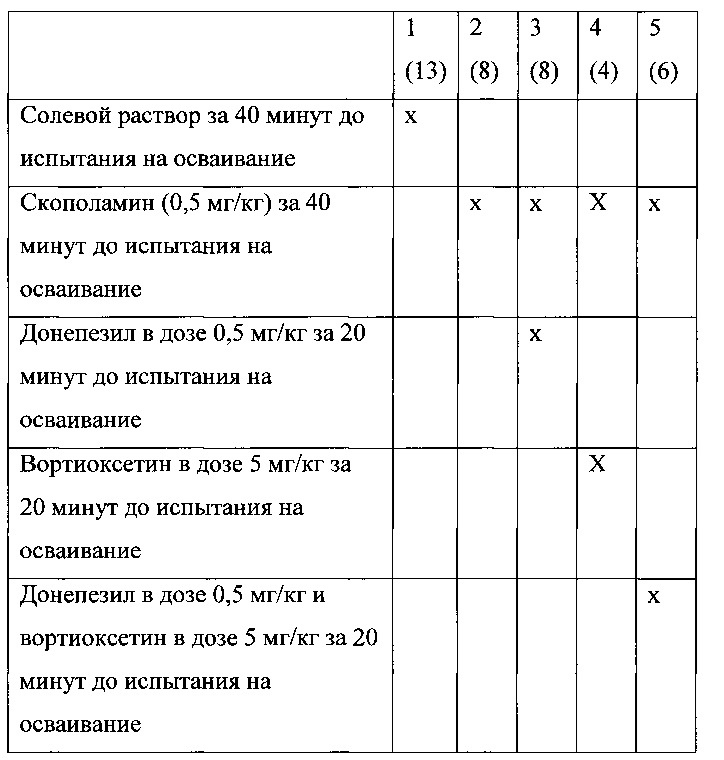
На фигуре 6 показано исследование нового объекта при помощи показателя распознавания (RI), определенного как
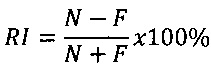
где N является временем, затраченным на новый объект, a F является временем, затраченным на знакомый объект.
Данные показывают, что RI для групп 2, 3 и 4 значительно (p<0,001) ниже, чем RI для группы 1 и что RI для группы 5 значительно (p<0,05) выше, чем RI для любой из групп 2, 3 и 4. Это показывает, что скополамин поражает кратковременную память у крыс и что ни вортиоксетин в дозе 5 мг/кг, ни донепезил в дозе 0,5 мг/кг не способны обратить данное нарушение. В отличие от этого, комбинированное действие вортиоксетина в дозе 5 мг/кг и донепезила в дозе 0,5 мг/кг обращает нарушение памяти, вызванное скополамином.

Изобретение относится к фармацевтической промышленности и представляет собой фармацевтическую композицию, содержащую вортиоксетин и донепезил совместно с фармацевтически приемлемым наполнителем, при этом композиция предназначена для лечения заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при вирусе иммунодефицита человека, деменции у лиц, злоупотребляющих алкоголем или лекарственными средствами, умеренного когнитивного нарушения, когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией. Изобретение обеспечивает синергичное увеличение внеклеточного уровня ацетилхолина в головном мозге. 4 н. и 8 з.п. ф-лы, 5 пр., 1 табл., 6 ил.
1. Фармацевтическая композиция, содержащая вортиоксетин и донепезил совместно с фармацевтически приемлемым наполнителем, при этом композиция предназначена для лечения заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при вирусе иммунодефицита человека, деменции у лиц, злоупотребляющих алкоголем или лекарственными средствами, умеренного когнитивного нарушения, когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией.
2. Композиция по п. 1, содержащая 5-25 мг донепезила.
3. Композиция по п. 1 или 2, содержащая 5-20 мг вортиоксетина.
4. Применение вортиоксетина и донепезила для производства лекарственного препарата для лечения заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при вирусе иммунодефицита человека, деменции у лиц, злоупотребляющих алкоголем или лекарственными средствами, умеренного когнитивного нарушения, когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией.
5. Применение по п. 4, где указанный лекарственный препарат содержит 5-25 мг донепезила.
6. Применение по п. 4 или 5, где указанный лекарственный препарат содержит 5-20 мг вортиоксетина.
7. Применение вортиоксетина и донепезила в лечении заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при вирусе иммунодефицита человека, деменции у лиц, злоупотребляющих алкоголем или лекарственными средствами, умеренного когнитивного нарушения, когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией.
8. Применение по п. 7, где указанный донепезил составляет от 5 до 25 мг донепезила.
9. Применение по п. 7 или 8, где указанный вортиоксетин составляет от 5 до 20 мг вортиоксетина.
10. Способ лечения заболевания, выбранного из когнитивной дисфункции, деменции при болезни Альцгеймера, деменции сосудистого генеза, деменции при болезни Пика, деменции при болезни Крейтцфельда-Якоба, деменции при болезни Гентингтона, деменции при болезни Паркинсона, деменции при вирусе иммунодефицита человека, деменции у лиц, злоупотребляющих алкоголем или лекарственными средствами, умеренного когнитивного нарушения, когнитивной дисфункции, связанной с депрессией, и когнитивной дисфункции, связанной с шизофренией, при этом способ включает комбинированное введение вортиоксетина и донепезила пациенту, нуждающемуся в этом.
11. Способ по п. 10, где указанному пациенту вводят 5-25 мг донепезила.
12. Способ по п. 10 или 11, где указанному пациенту вводят 5-20 мг вортиоксетина.
| WO 2009062517 A1, 22.05.2009 | |||
| WO 2009005519 A1, 08.01.2009 | |||
| Обдирочно-шлифовальный станок | 1987 |
|
SU1509232A1 |
| ЛЕНТОЧНОСТРОГАЛЬНАЯ МАШИНА ДЛЯ ДОБЫЧИ ТОРФА И ПРОРЫТИЯ ОСУШИТЕЛЬНЫХ КАНАЛОВ | 1928 |
|
SU12325A1 |
| ПРЕПАРАТИВНЫЕ ФОРМЫ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРОТИВ СЛАБОУМИЯ ДЛЯ ЧРЕСКОЖНОГО ВВЕДЕНИЯ | 2006 |
|
RU2428179C2 |
Авторы
Даты
2017-11-13—Публикация
2013-12-12—Подача