Область техники
[0001] Настоящее изобретение относится к терапевтическому средству для лечения деменции, представляющему собой комбинацию производного пиразолохинолина, обладающего ингибирующей активностью в отношении фосфодиэстеразы 9 (PDE9), или его фармацевтически приемлемой соли и мемантина или его фармацевтически приемлемой соли.
Уровень техники
[0002]
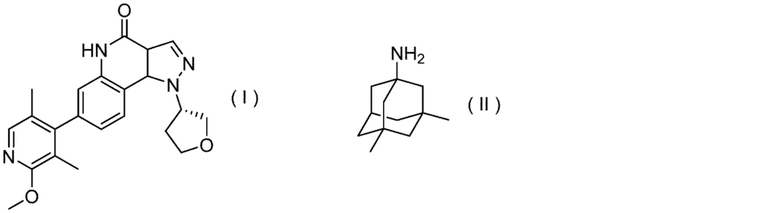
[0003] Производные пиразолохинолина, представленные формулой (I) (далее в данном документе называемые "соединением (I)"), обладают ингибирующей активностью в отношении фосфодиэстеразы 9 (PDE9), и считается, что они обладают перспективными благоприятными эффектами в отношении когнитивной функции при болезни Альцгеймера (PTL 1).
[0004] Мемантин, представленный формулой (II) (в данном документе называемый "соединением (II)"), обладает антагонистическим эффектом в отношении глутаматных рецепторов типа NMDA и, как сообщалось, обеспечивает улучшение когнитивной функции при болезни Альцгеймера со степенью тяжести от умеренной до тяжелой, при этом также проявляет эффективность в отношении второстепенных симптомов, таких как тревожное возбуждение, раздражительность, агрессия и расстройство поведения (BPSD: поведенческие и психологические симптомы деменции) (см. NPL 1 и 2).
[0005] Другие терапевтических средств для лечения болезни Альцгеймера, которые были одобрены для применения, включают ингибиторы ацетилхолинэстеразы: донепезил, галантамин и ривастигмин. Донепезил показан для лечения болезни Альцгеймера со степенью тяжести от легкой до тяжелой, и сообщалось, что в дополнение к благоприятному эффекту в отношении когнитивной функции он также обладает эффектом против BPSD, включая тревожное возбуждение, тревожность, апатию, бред, депрессию, расторможенность, галлюцинацию, раздражительность, нарушенное моторное поведение и апатию (см. NPL 3, 4, 5, 6 и 7). Галантамин и ривастигмин показаны для лечения болезни Альцгеймера со степенью тяжести от легкой до умеренной (см. NPL 8 и 9). Комбинированное применение разных ингибиторов ацетилхолинэстеразы противопоказано, но любой ингибитор ацетилхолинэстеразы можно использовать в комбинации с мемантином. В соответствии с Руководством по лечению деменции, 2010 года, ингибиторы ацетилхолинэстеразы рекомендованы для облегчения главных симптомов болезни Альцгеймера с использованием одного из донепезила, галантамина или ривастигмина, выбранного исходно, и с последующей заменой на другой ингибитор ацетилхолинэстеразы, если возникает проблема в плане эффективности или переносимости. Если эффект ингибитора ацетилхолинэстеразы является недостаточным или возникает проблема в отношении переносимости, то можно рассматривать комбинацию с мемантином или с заменой на мемантин.
[0006] Однако, ингибиторы ацетилхолинэстеразы обладают побочными эффектами в отношении пищеварительной системы. В тех случаях, где их применение исключено из-за побочных эффектов или особенностей переносимости, можно выбрать мемантин для пациентов с болезнью Альцгеймера со степенью тяжести от умеренной до тяжелой, но для пациентов с болезнью Альцгеймера легкой степени на данный момент не существует эффективного способа лечения. Комбинированное применение ингибиторов ацетилхолинэстеразы с мемантином возможно у пациентов, у которых наблюдались неудовлетворительные эффекты, но мнения разделяются, поскольку в некоторых сообщениях отмечен эффект от их комбинированного применения (см. NPL 10) в то время, как в других сообщениях отмечается отсутствие эффекта (см. NPL 11).
Список использованной литературы
Патентная литература
[0007] [PTL 1] Патент США № 8563565
Непатентные литературные источники
[0008] [NPL 1] Mecocci et al., Int J Geriatr Psychiatry, vol. 24, p. 532
[NPL 2] Grossberg et al., Dement Geriatr Cogn Disord, 2009, vol. 27, p. 164
[NPL 3] Homma et al., Dement. Geriatr. Cogn. Disord., 2000, vol. 11, p. 299
[NPL 4] Homma et al., Dement. Geriatr. Cogn. Disord., 2008, vol. 25, p. 399
[NPL 5] Mori et al., Ann. Neurol, vol. 72, p. 41 2012
[NPL 6] Holmes at al., Neurology, 2004, vol. 63, p. 214
[NPL 7] Gauthier et al., Int Psychogeriatr, 2002, vol. 14, p. 389
[NPL 8] Raskind et al., Neurology, 2000, vol. 54, p. 226
[NPL 9] Winblad et al., Neurology, 2007, vol. 69, p. S14
[NPL 10] Lopez et al., J Neurol Neurosurg Psychiatry, 2009, vol. 80, p. 600
[NPL 11] Howard et al., New Eng J. Med., 2012, vol. 366, p. 893
Краткое описание изобретения
Техническая задача
[0009] Дело обстоит так, что в настоящее время не существует удовлетворительного способа лечения болезни Альцгеймера, вместе с тем эффективное средство против деменции также еще не было разработано.
Решение задачи
[0010] С целью решения данной задачи авторы настоящего изобретения провели очень тщательное исследование с применением модели индуцированного скополамином когнитивного нарушения на крысах, в результате которого авторы настоящего изобретения завершили настоящее изобретение с выявлением, что комбинированное применение соединения (I) или его фармацевтически приемлемой соли с соединением (II) или его фармацевтически приемлемой солью неожиданно проявляет эффект ингибирования в отношении индуцированного скополамином когнитивного нарушения в дозах, каждая из которых по отдельности является неэффективной.
[0011] В частности, настоящее изобретение относится к следующим пунктам <1>-<19.3>.
<1> Терапевтическое средство для лечения болезни Альцгеймера, предназначенное для комбинированного применения (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она, представленного формулой (I):

или его фармацевтически приемлемой соли с мемантином, представленным формулой (II):
 , или его фармацевтически приемлемой солью.
, или его фармацевтически приемлемой солью.
<2> Терапевтическое средство в соответствии с <1>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<3> Терапевтическое средство в соответствии с <1> или <2>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<4> Терапевтическое средство в соответствии с любым из <1>-<3>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<5> Терапевтическое средство для лечения болезни Альцгеймера, предназначенное для одновременного или раздельного введения (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она, представленного формулой (I):
 , или его фармацевтически приемлемой соли и мемантина, представленного формулой (II):
, или его фармацевтически приемлемой соли и мемантина, представленного формулой (II):
 , или его фармацевтически приемлемой соли.
, или его фармацевтически приемлемой соли.
<6> Терапевтическое средство в соответствии с <5>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<7> Терапевтическое средство в соответствии с <5> или <6>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<8> Терапевтическое средство в соответствии с любым из <5>-<7>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<9> Терапевтическое средство для лечения болезни Альцгеймера, содержащее (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он, представленный формулой (I):
 , или его фармацевтически приемлемую соль и мемантин, представленный формулой (II):
, или его фармацевтически приемлемую соль и мемантин, представленный формулой (II):
 , или его фармацевтически приемлемую соль.
, или его фармацевтически приемлемую соль.
<10> Терапевтическое средство в соответствии с <9>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<11> Терапевтическое средство в соответствии с <9> или <10>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<12> Терапевтическое средство в соответствии с любым из <9>-<11>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<13> Мемантин, представленный формулой (II):
 , или его фармацевтически приемлемая соль для лечения болезни Альцгеймера путем применения в комбинации с (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-оном, представленным формулой (I):
, или его фармацевтически приемлемая соль для лечения болезни Альцгеймера путем применения в комбинации с (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-оном, представленным формулой (I):
 , или его фармацевтически приемлемой солью.
, или его фармацевтически приемлемой солью.
<13.1> Мемантин или его фармацевтически приемлемая соль в соответствии с <13>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<13.2> Мемантин или его фармацевтически приемлемая соль в соответствии с <13> или <13.1>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<13.3> Мемантин или его фармацевтически приемлемая соль в соответствии с любым из <13>-<13.2>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<14> (S)-7-(2-Метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он, представленный формулой (I):
 , или его фармацевтически приемлемая соль для лечения болезни Альцгеймера путем применения в комбинации с мемантином, представленным формулой (II):
, или его фармацевтически приемлемая соль для лечения болезни Альцгеймера путем применения в комбинации с мемантином, представленным формулой (II):
 , или его фармацевтически приемлемой солью.
, или его фармацевтически приемлемой солью.
<14.1> Соединение, представленное формулой (I), или его фармацевтически приемлемая соль в соответствии с <14>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<14.2> Соединение, представленное формулой (I), или его фармацевтически приемлемая соль в соответствии с <14> или <14.1>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<14.3> Соединение, представленное формулой (I), или его фармацевтически приемлемая соль в соответствии с любым из <14>-<14.2>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<15> Способ лечения болезни Альцгеймера, предусматривающий комбинированное применение (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она, представленного формулой (I):
 , или его фармацевтически приемлемой соли с мемантином, представленным формулой (II):
, или его фармацевтически приемлемой соли с мемантином, представленным формулой (II):
 , или его фармацевтически приемлемой солью.
, или его фармацевтически приемлемой солью.
<15.1> Способ в соответствии с <15>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<15.2> Способ в соответствии с <15> или <15.1>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<15.3> Способ в соответствии с любым из <15>-<15.2>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<16> Фармацевтическая композиция, содержащая (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он, представленный формулой (I):
 , или его фармацевтически приемлемую соль, мемантин, представленный формулой (II):
, или его фармацевтически приемлемую соль, мемантин, представленный формулой (II):
 , или его фармацевтически приемлемую соль и вспомогательное вещество.
, или его фармацевтически приемлемую соль и вспомогательное вещество.
<16.1> Фармацевтическая композиция в соответствии с <16>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<16.2> Фармацевтическая композиция в соответствии с <16> или <16.1>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<17> Набор, содержащий
фармацевтическую композицию, содержащую (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он, представленный формулой (I):
 , или его фармацевтически приемлемую соль и вспомогательное вещество, и
, или его фармацевтически приемлемую соль и вспомогательное вещество, и
фармацевтическую композицию, содержащую мемантин, представленный формулой (II):
 , или его фармацевтически приемлемую соль и вспомогательное вещество.
, или его фармацевтически приемлемую соль и вспомогательное вещество.
<17.1> Набор в соответствии с <17>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<17.2> Набор в соответствии с любым из <17>-<17.1>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой малеат.
<18> Применение мемантина, представленного формулой (II):
 , или его фармацевтически приемлемой соли для получения терапевтического средства для лечения болезни Альцгеймера путем применения в комбинации с (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-оном, представленным формулой (I):
, или его фармацевтически приемлемой соли для получения терапевтического средства для лечения болезни Альцгеймера путем применения в комбинации с (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-оном, представленным формулой (I):
 , или его фармацевтически приемлемой солью.
, или его фармацевтически приемлемой солью.
<18.1> Применение мемантина или его фармацевтически приемлемой соли в соответствии с <18>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<18.2> Применение мемантина или его фармацевтически приемлемой соли в соответствии с <18> или <18.1>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<18.3> Применение мемантина или его фармацевтически приемлемой соли в соответствии с любым из <18>-<18.2>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
<19> Применение (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она, представленного формулой (I):
 , или его фармацевтически приемлемой соли для получения терапевтического средства для лечения болезни Альцгеймера путем применения в комбинации с мемантином, представленным формулой (II):
, или его фармацевтически приемлемой соли для получения терапевтического средства для лечения болезни Альцгеймера путем применения в комбинации с мемантином, представленным формулой (II):
 , или его фармацевтически приемлемой солью.
, или его фармацевтически приемлемой солью.
<19.1> Применение соединения, представленного формулой (I), или его фармацевтически приемлемой соли в соответствии с <19>, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
<19.2> Применение соединения, представленного формулой (I), или его фармацевтически приемлемой соли в соответствии с <19> или <19.1>, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
<19.3> Применение соединения, представленного формулой (I), или его фармацевтически приемлемой соли в соответствии с любым из <19>-<19.2>, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразолo[4,3-c]хинолин-4(5H)-она малеат.
Полезные эффекты изобретения
[0012] Настоящее изобретение предусматривает терапевтическое средство для лечения болезни Альцгеймера, представляющее собой комбинацию производного пиразолохинолина, представленного формулой (I), или его фармацевтически приемлемой соли, которые обладают ингибирующим действием в отношении PDE9, с мемантином или его фармацевтически приемлемой солью, которые обладают антагонистическим эффектом в отношении глутаматных рецепторов типа NMDA. Терапевтическое средство, в котором задействована данная комбинация, проявляет более ощутимый благоприятный эффект в отношении когнитивной функции в животных моделях по сравнению с их применениями по отдельности, и оно обладает потенциалом для применения в качестве терапевтического средства для лечения болезни Альцгеймера.
Описание вариантов осуществления
[0013] Далее настоящее изобретение будет пояснено подробно.
[0014] "Фармацевтически приемлемая соль", как указано в данном описании, конкретно не ограничена, если она представляет собой соль, образованную соединением по настоящему изобретению, и конкретные примеры включают соли присоединения кислоты, такие как соли неорганических кислот, соли органических кислот или соли кислых аминокислот.
[0015] Если не указано иное, в контексте "фармацевтически приемлемой соли", как используется в данном документе, количество молекул кислоты на одну молекулу соединения в образованной соли конкретно не ограничено, если соль образована при соответствующем соотношении. В одном варианте осуществления количество молекул кислоты на одну молекулу соединения составляет от приблизительно 0,1 до приблизительно 5; в другом варианте осуществления количество молекул кислоты на одну молекулу соединения составляет от приблизительно 0,5 до приблизительно 2; и в еще одном варианте осуществления количество молекул кислоты на одну молекулу соединения составляет приблизительно 0,5, приблизительно 1 или приблизительно 2.
[0016] Конкретные примеры соли неорганической кислоты включают гидрохлорид, гидробромид, сульфат, нитрат и фосфат, а конкретные примеры соли органической кислоты включают ацетат, сукцинат, фумарат, малеат, тартрат, цитрат, лактат, стеарат, бензоат, метансульфонат, пара-толуолсульфонат и бензолсульфонат.
[0017] Конкретные примеры соли кислой аминокислоты включают аспартат и глутамат.
[0018]
[Состав]
Фармацевтическую композицию по настоящему изобретению можно получить путем смешивания фармацевтически приемлемой добавки с соединением (I) или его фармацевтически приемлемой солью и/или с соединением (II) или его фармацевтически приемлемой солью. Фармацевтическую композицию по настоящему изобретению можно получить с помощью известного способа, такого как способ, описанный в "Общие правила получения" в Японской фармакопее, 16-е издание.
Фармацевтическую композицию по настоящему изобретению можно соответствующим образом вводить пациенту в соответствии с лекарственной формой.
[0019] Доза соединения (I) или его фармацевтически приемлемой соли и соединения (II) или его фармацевтически приемлемой соли в соответствии с настоящим изобретением будет варьироваться в зависимости от тяжести симптомов, возраста пациента, пола и веса тела, типа введения, и типа соли, и конкретного типа заболевания и т. п.; но обычно взрослым перорально вводят в сутки от приблизительно 30 мкг до 10 г, в одном варианте осуществления от 100 мкг до 5 г, а в другом варианте осуществления от 100 мкг до 1 г в виде однократной дозы или в виде нескольких раздельных доз; или вводят посредством инъекции в сутки от приблизительно 30 мкг до 1 г, в одном варианте осуществления от 100 мкг до 500 мг, а в другом варианте осуществления от 100 мкг до 300 мг в виде однократной дозы или в виде нескольких раздельных доз.
Примеры
[0020] Соединение (I) можно получить, например, с помощью способа, описанного в PTL 1.
[0021]
(Примеры фармакологических тестов)
Авторы настоящего изобретения подтвердили эффекты, полученные при комбинированном применении соединения (I) и мемантина гидрохлорида с использованием следующей животной модели.
[0022]
[Тестовое испытание 1] Тест на распознавание новых объектов с использованием крыс с индуцированным скополамином когнитивным нарушением
Имеются сообщения о расстройстве нервной системы, обусловленном ацетилхолином, при болезни Альцгеймера (Whitehouse et al., Science, 1982, vol.215, p.1237), и при этом животные, которым вводили скополамин, являются пригодными для применения в качестве животной модели болезни Альцгеймера. Скополамин представляет собой ингибитор мускариновых рецепторов, который блокирует передачу ацетилхолина в нервной системе. Ацетилхолин в нервной системе вовлечен в функции памяти и внимания, и здоровые люди или животные, которым вводили скополамин, демонстрировали симптомы амнезии, подобной таковой при деменции, которые ослабляли с помощью лекарственных средств, используемых для лечения когнитивного нарушения при болезни Альцгеймера (Snyder et al., Alzheimer's & Dementia 1(2005)126-135, Sambeth et al., European Journal of Pharmacology, vol.572(2007), pp.151-159).
[0023]
Материалы и методы
Тестирование проводили на самцах крыс Long-Evans 6-недельного возраста (Институт репродукции животных). Процесс привыкания к экспериментальной процедуре проводили один раз в сутки в течение 2 дней перед испытанием. В процессе привыкания среду-носитель вводили крысам, а затем крыс помещали в пустой аппарат для тестирования (40 см × 30 см × высота 45 см) и оставляли их для изучения территории в течение 3 минут, а затем, после помещения в камеру ожидания (13 см × 30 см × высота 45 см) на приблизительно 1 минуту, их снова возвращали в пустой аппарат для тестирования и оставляли на 5 минут.
Испытание с обнаружением (T1) проводили в день проведения теста. Соединение (I) задавали перорально за 2 часа до T1. Мемантина гидрохлорид вводили перорально за 1 час до T1. Скополамин (Wako Pure Chemical Industries, Ltd.) вводили подкожно за 30 минут до T1 в дозе, составляющей 0,7 мг/кг. В ходе T1 крысам предоставляли возможность привыкнуть к пустому аппарату для тестирования в течение 3 минут, а затем помещали их в камеру ожидания. После расположения двух идентичных объектов в аппарате для тестирования, крыс снова возвращали в аппарат для тестирования и предоставляли им возможность свободного изучения двух идентичных объектов в течение 5 минут. Затем крыс обратно возвращали в их клетки для содержания. Через 2 часа проводили испытание на запоминание (T2). Крыс помещали в пустой аппарат для тестирования на 3 минуты для привыкания, а затем переносили в камеру ожидания. После размещения в аппарате для тестирования объекта, использованного в T1 ("знакомого" объекта), и объекта, не использованного в T1 ("нового" объекта), крыс снова возвращали в аппарат для тестирования и предоставляли им возможность свободного изучить такие объекты в течение 3 минут. Объекты протирали влажной салфеткой, пропитанной этанолом, после каждого эксперимента таким образом, чтобы не осталось следов запаха. Поведение крыс в ходе T1 и T2 регистрировали с помощью цифровой видеокамеры, а общее время исследования, затраченное на изучение каждого объекта, измеряли вручную с помощью секундомера. Исследовательское поведение определяли как поведение, при котором крыса подносила свой нос на расстояние в пределах 2 см от объекта и направляла свой нос к объекту.
В тесте распознавания нового объекта процентная доля исследования нового объекта в ходе T2 считается показателем для амнезии, отражающим различие знакомых и новых объектов. Процентную долу исследования нового объекта рассчитывали с помощью следующей формулы.
Процентная доля исследования нового объекта (%) = N/(N+F) × 100,
где F: время, затраченное на изучение знакомого объекта;
N: время, затраченное на изучение нового объекта.
Крысы, у которых общее время, затраченное на исследование объектов в ходе T1 или T2, составляло 10 секунд или меньше, или крысы, у которых процентная доля времени, затраченного на исследование одного из объектов в ходе T1, составляла не менее 70% или не более 30% от общего времени исследования, были исключены из анализа данных.
Результаты выражены в виде среднего значения ± стандартная погрешность. Различие между нормальной контрольной группой, не обработанной скополамином, и контрольной группой с заболеванием, обработанной скополамином, анализировали с помощью непарного t-критерия (значимое различие: *). Различие между контрольной группой с заболеванием и группой, обработанной одним лекарственным средством, анализировали с помощью критерия множественных сравнений Даннетта (значимое различие: #). Различие между группой, которую подвергали комбинированной обработке, и группой, обработанной одним лекарственным средством, анализировали с помощью критерия Стьюдента для одной выборки (значимое различие: 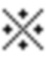 ). Значение p<0,05 оценивали как статистически значимое различие. Статистический анализ проводили с использованием GraphPad Prism версии 5.04 или 6.02. Результаты показаны в таблицах 1-4.
). Значение p<0,05 оценивали как статистически значимое различие. Статистический анализ проводили с использованием GraphPad Prism версии 5.04 или 6.02. Результаты показаны в таблицах 1-4.
[0024]
0,3 мг/кг
1 мг/кг
[0025]
3,3 мг/кг
10 мг/кг
[0026]
3 мг/кг
10 мг/кг
[0027]
1 мг/кг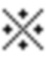
[0028]
Результаты
В ходе T2 крысы из контрольной группы с заболеванием демонстрировали в значительной степени более низкую процентную долю исследования нового объекта, чем крысы из нормальной контрольной группы. Это означает, что нарушение памяти у крыс было индуцировано скополамином.
Соединение (I) демонстрировало значительный благоприятный эффект в отношении процентной доли исследования нового объекта при 3,3 мг/кг (таблица 2), но не демонстрировало значительного эффекта при 1 мг/кг (таблица 1). Мемантина гидрохлорид демонстрировал значительный благоприятный эффект в отношении процентной доли исследования нового объекта при 3 мг/кг (таблица 3). Несмотря на то, что значительный благоприятный эффект в отношении процентной доли исследования нового объекта не демонстрировался при применении только мемантина гидрохлорида (1 мг/кг), в группе, которую подвергали комбинированной обработке соединением (I) (1 мг/кг) и мемантина гидрохлоридом (1 мг/кг), демонстрировалась значительно более высокая процентная доля исследования нового объекта, чем в группе, которую подвергали обработке только мемантина гидрохлоридом (1 мг/кг) (таблица 4). Данный результат указывает на усиливающий эффект соединения (I) в отношении когнитивной функции в случае применения в комбинации с мемантина гидрохлоридом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ТЕЛЕЦ ЛЕВИ, СОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ ПИРАЗОЛОХИНОЛИНА | 2018 |
|
RU2802212C2 |
| ПИРИДИНИЛПИРАЗОЛОХИНОЛИНОВЫЕ СОЕДИНЕНИЯ | 2014 |
|
RU2655172C2 |
| СОЛЬ ПРОИЗВОДНОГО ПИРАЗОЛОХИНОЛИНА И ЕЕ КРИСТАЛЛ | 2014 |
|
RU2655171C2 |
| ПИРАЗОЛОХИНОЛИНОВОЕ ПРОИЗВОДНОЕ | 2012 |
|
RU2605096C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2015 |
|
RU2702732C1 |
| КОНДЕНСИРОВАННОЕ ТРИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2021 |
|
RU2833338C1 |
| ЗАМЕЩЕННЫЕ 2-АМИНО-3-СУЛЬФОНИЛ-ТЕТРАГИДРО-ПИРАЗОЛО[1,5-a]ПИРИДО-ПИРИМИДИНЫ - АНТАГОНИСТЫ СЕРОТОНИНОВЫХ 5-HT РЕЦЕПТОРОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2008 |
|
RU2384581C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2015 |
|
RU2709786C2 |
| АГОНИСТЫ 5-НТ4-РЕЦЕПТОРОВ ДЛЯ ЛЕЧЕНИЯ ДЕМЕНЦИИ | 2011 |
|
RU2569733C2 |
| (3-АРИЛСУЛЬФОНИЛХИНОЛИН-8-ИЛ)-ДИАЛКИЛ-АМИНЫ - СЕЛЕКТИВНЫЕ АНТАГОНИСТЫ СЕРОТОНИНОВЫХ 5-HT РЕЦЕПТОРОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2012 |
|
RU2500672C1 |
Изобретение относится к области медицины и фармацевтики и может быть использовано для лечения болезни Альцгеймера. Терапевтическое средство для лечения болезни Альцгеймера представляет собой комбинацию (S)–7–(2–метокси–3,5–диметилпиридин–4–ил)–1–(тетрагидрофуран–3–ил)–1H–пиразолo[4,3–c]хинолин–4(5H)–она, который представлен формулой (I)

или его фармацевтически приемлемой соли и мемантинa, который представлен формулой (II)

или его фармацевтически приемлемой соли. Предложены также способ лечения болезни Альцгеймера и применение указанного терапевтического средства для лечения болезни Альцгеймера. Изобретение обеспечивает усиливающий эффект соединения (I) в отношении когнитивной функции в случае применения в комбинации с мемантином при уменьшении дозы соединений. 4 н. и 15 з.п. ф-лы, 4 табл.
1. Терапевтическое средство для лечения болезни Альцгеймера, содержащее (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он, представленный формулой (I)
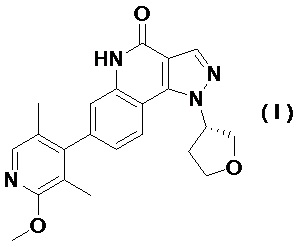 ,
,
или его фармацевтически приемлемую соль, в комбинации с мемантином, представленным формулой (II)

или его фармацевтически приемлемой солью.
2. Терапевтическое средство по п. 1, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
3. Терапевтическое средство по п. 1 или 2, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
4. Терапевтическое средство по любому из пп. 1-3, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-она малеат.
5. Терапевтическое средство по любому из пп. 1-4, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль и мемантин или его фармацевтически приемлемая соль вводятся одновременно или раздельно.
6. Способ лечения болезни Альцгеймера, включающий введение пациенту (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-она, представленного формулой (I)
 ,
,
или его фармацевтически приемлемой соли и мемантина, представленного формулой (II)

или его фармацевтически приемлемой соли.
7. Способ по п. 6, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
8. Способ по п. 6 или 7, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
9. Способ по любому из пп. 6-8, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-она малеат.
10. Способ по любому из пп. 6-9, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль и мемантин или его фармацевтически приемлемая соль вводятся одновременно или раздельно.
11. Терапевтическое средство для лечения болезни Альцгеймера, содержащее (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он, представленный формулой (I)
 ,
,
или его фармацевтически приемлемую соль и мемантин, представленный формулой (II)

или его фармацевтически приемлемую соль.
12. Терапевтическое средство по п. 11, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
13. Терапевтическое средство по п. 11 или 12, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
14. Терапевтическое средство по любому из пп. 11-13, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-она малеат.
15. Применение терапевтического средства, содержащего комбинацию (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-она, представленного формулой (I)
 ,
,
или его фармацевтически приемлемой соли и мемантина, представленного формулой (II)

или его фармацевтически приемлемой соли для лечения болезни Альцгеймера.
16. Применение по п. 15, где болезнь Альцгеймера представляет собой болезнь Альцгеймера умеренной или тяжелой степени.
17. Применение по п. 15 или 16, где мемантин или его фармацевтически приемлемая соль представляет собой мемантина гидрохлорид.
18. Применение по любому из пп. 15-17, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль представляет собой (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-она малеат.
19. Применение по любому из пп. 15-18, где (S)-7-(2-метокси-3,5-диметилпиридин-4-ил)-1-(тетрагидрофуран-3-ил)-1H-пиразоло[4,3-c]хинолин-4(5H)-он или его фармацевтически приемлемая соль и мемантин или его фармацевтически приемлемая соль вводятся одновременно или раздельно.
| US 20160046623 A1, 18.02.2016 | |||
| US 8563565 B2, 22.10.2013 | |||
| ДОЖДЕВАЛЬНЫЙ АГРЕГАТ | 1998 |
|
RU2152712C1 |
| CN 102365285 B, 06.08.2014 | |||
| AU 2008249750 A1, 20.11.2008 | |||
| HUTSON P.H | |||
| et al | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
2022-11-24—Публикация
2018-05-30—Подача