ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Область техники, к которой относится изобретение
Изобретение относится к применению специфичных соединений-агонистов рецептора 5-HT4 для лечения расстройств познавательной способности, конкретно, к применению этих соединений в сочетании с другими средствами, особенно ингибиторами ацетилхолинэстеразы, для лечения болезни Альцгеймера и других расстройств познавательной способности.
Предшествующий уровень техники
Число пожилых людей, имеющих риск развития деменции, быстро растет, по мере того как продолжительность жизни увеличивается во всем мире. Болезнь Альцгеймера является наиболее общей причиной деменции в пожилом возрасте, насчитывая 50-60% всех случаев, в соответствии с некоторыми экспертными оценками. В 2008 предположительно 5,2 миллиона людей проживали с болезнью Альцгеймера только в Соединенных Штатах, насчитывая 13% населения США в возрасте 65 лет и старше.
Болезнь Альцгеймера определяют как прогрессирующее отклонение познавательной деятельности и ослабленный функциональный статус, несовместимые с нормальным старением. Полагают, что недостатки в холинергической системе являются основным действующим фактором при когнитивных симптомах, ассоциированных с болезнью Альцгеймера. Соответственно, преобладающее фармацевтическое лечение болезни Альцгеймера предоставляет умеренное симптоматическое купирование посредством применения ингибиторов ацетилхолинэстеразы. Полагают, что эти средства действуют посредством снижения степени разрушения ацетилхолина, таким образом, приводя к увеличению концентраций ацетилхолина в мозге.
Серотонин (5-гидрокситриптамин, 5-HT) представляет собой нейромедиатор, который широко распространен по всему организму как в центральной нервной системе, так и в периферических системах. Идентифицировано, по меньшей мере, семь подтипов рецепторов серотонина, и взаимодействие серотонина с этими различными рецепторами связано с широким разнообразием физиологических функций. Показано, что серотонергическая система в мозге вовлечена в процессы распознавания. В частности, на животных моделях продемонстрировано, что рецепторы 5-HT4 играют роль в нейрональном механизме улучшения памяти и когнитивных процессах. Активация рецептора 5-HT4 усиливает высвобождение ацетилхолина из холинергических нейронов, таким образом, предоставляя еще один потенциальный подход к фармакологическому вмешательству, которое благоприятным образом увеличивает концентрации ацетилхолина в синапсах внутри мозга (Maillet et al. (2004) Current Alzheimer Research 1:79-85). Кроме того, предполагают, что некоторые соединения-агонисты рецептора 5-HT4 могут применяться при лечении расстройств центральной нервной системы, включая расстройства познавательной способности, поведенческие нарушения, расстройства настроения, такие как депрессия и тревожность, и расстройства контроля автономной функции.
Активация рецептора 5-HT4 также стимулирует активность α-секретазы, что приводит в результате к увеличенным уровням растворимого амилоидного белка-предшественника альфа (sAPPα), который обладает нейротрофными и нейропротекторными свойствами и также ассоциирован с когнитивным усилением преклинически. Бета-амилоид (Aβ) представляет собой пептид из 39-43 аминокислот, который, по-видимому, является основной составной частью амилоидных бляшек в мозге пациентов с болезнью Альцгеймера. Aβ образуется после расщепления амилоидного белка-предшественника β- и γ-секретазами. В преклинических исследованиях, индуцированная агонистом рецептора 5-HT4 активация α-секретазы и генерация sAPPα снижает уровень Aβ. Ожидают, что такое снижение уровней Aβ является благоприятным. Следовательно, агонисты рецептора 5-HT4 предлагают возможность предоставления как симптоматических, так и модифицирующих заболевание благоприятных эффектов (Lezoualc'h (2007) Experimental Neurology 205:325-329).
К настоящему времени не было одобрено никакого лечения, в котором используется потенциальная применимость механизма 5-HT4 для лечения расстройств познавательной способности. Соответственно, остается необходимость лечения дисфункции памяти у людей, страдающих от болезни Альцгеймера, благоприятный эффект которого происходит от увеличения концентраций ацетилхолина, и ожидают, что применение средства-агониста рецептора 5-HT4 будет иметь другие потенциальные благоприятные эффекты.
КРАТКОЕ СОДЕРЖАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Изобретение относится к применению специфичных соединений-агонистов рецептора 5-HT4 и к применению специфичных соединений-агонистов рецептора 5-HT4 в сочетании с ингибитором ацетилхолинэстеразы для лечения болезни Альцгеймера или расстройства познавательной способности. В частности, изобретение относится к применению соединений-агонистов рецептора 5-HT4 и ингибитора ацетилхолинэстеразы, где каждое средство применяют при концентрации ниже той концентрации, при которой может наблюдаться существенный эффект при применении по отдельности.
Агонист рецептора 5-HT4, {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты (1) и его фармацевтически приемлемые соли,

раскрыт в патенте США 7375114 B2. Соединение 1 альтернативно обозначают как 1,2-дигидро-N-[(3-эндо)-8-[(2R)-2-гидрокси-3-[метил(метилсульфонил)амино]пропил]-8-азабицикло[3.2.1]окт-3-ил]-1-(1-метилэтил)-2-оксо-3-хинолинкарбоксамид.
Агонист рецептора 5-HT4, метиловый эфир 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты (2) и его фармацевтически приемлемые соли,

раскрыт в патенте США 7256294 B2 и заявке США 2006/0270652 A1. Соединение 2 альтернативно обозначают как метиловый эфир 4-[[4-[[[[2-(1-метилэтил)-1H-бензимидазол-7-ил]карбонил]амино]метил]-1-пиперидинил]метил]-1-пиперидинкарбоновой кислоты.
Соединения 1 и 2 являются активными и селективными агонистами рецептора 5-HT4, которые демонстрируют характеристическую активность от умеренной до высокой в исследованиях in vitro. Было продемонстрировано, что каждое из соединений 1 и 2 смягчает индуцированное антагонистом мускариновых рецепторов нарушение памяти у крыс на доклинической модели распознавания водного лабиринта Морриса. Наблюдали результаты, согласующиеся с аддитивным или синергистическим эффектом, между соединением 1 и ингибитором ацетилхолинэстеразы донепезилом и между соединением 2 и донепезилом при дозах, которые сами по себе оказывали незначительный эффект или не оказывали эффекта. Было также показано, что соединения 1 и 2 вызывают зависимое от концентрации возрастание sAPPα в исследованиях in vitro. Следовательно, можно ожидать, что соединения 1 и 2 являются применимыми при лечении дисфункции памяти.
В одном аспекте, изобретение находит применение в способе лечения болезни Альцгеймера или расстройства познавательной способности у пациента, включающем введение пациенту соединения-агониста рецептора 5-HT4, где соединение выбирают из {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты и метилового эфира 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты и их фармацевтически приемлемых солей. Таким образом, в одном аспекте, изобретение предоставляет соединение-агонист рецептора 5-HT4, как описано выше, для применения в лечении болезни Альцгеймера или расстройства познавательной способности.
Настоящие соединения-агонисты 5-НТ4 благоприятным образом применяют в сочетании со средством, которое действует, чтобы ингибировать действие ацетилхолинэстеразы в организме. Применимые ингибиторы включают, но не ограничены ими, гидрохлорид донепезила (доступный для приобретения как Aricept®), гидробромид галантамина, альтернативно пишется как галантамина гидробромид (Razadyne®, Reminyl®), тартрат ривастигмина (Exelon®) и гидрохлорид такрина (Cognex®).
Изобретение находит применение в способе лечения болезни Альцгеймера или расстройства познавательной способности у пациента, включающем введение пациенту соединения-агониста рецептора 5-HT4, где соединение выбирают из {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты и метилового эфира 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты и их фармацевтически приемлемых солей и ингибитора ацетилхолинэстеразы.
В еще одном аспекте, следовательно, изобретение предоставляет настоящие соединения-агонисты рецептора 5-HT4 для применения в сочетании с ингибитором ацетилхолинэстеразы для лечения болезни Альцгеймера или расстройств познавательной способности. Изобретение дополнительно предоставляет настоящие соединения-агонисты рецептора 5-HT4 для усиления эффективности действия ингибитора ацетилхолинэстеразы для лечения болезни Альцгеймера или расстройств познавательной способности.
В одном аспекте изобретения, в вышеуказанном способе, каждое из соединения-агониста 5-HT4 и ингибитора ацетилхолинэстеразы вводят в дозе, которая является недостаточно эффективной для лечения болезни Альцгеймера или расстройств познавательной способности при введении по отдельности.
В конкретном аспекте, соединение-агонист рецептора 5-HT4 представляет собой гидрохлорид {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты, а ингибитор ацетилхолинэстеразы представляет собой донепезил.
В еще одном конкретном аспекте, соединение-агонист рецептора 5-HT4 представляет собой метиловый эфир 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты, а ингибитор ацетилхолинэстеразы представляет собой донепезил.
Изобретение дополнительно находит применение в способе улучшения памяти у пациента, испытывающего нарушение памяти, включающем введение пациенту соединения-агониста рецептора 5-HT4, где соединение выбирают из {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты и метилового эфира 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты и их фармацевтически приемлемых солей и ингибитора ацетилхолинэстеразы.
В одном аспекте, соединение-агонист 5-HT4 и ингибитор ацетилхолинэстеразы каждое вводят в дозе, которая является недостаточно эффективной для улучшения памяти у пациента, испытывающего нарушение памяти, при введении по отдельности.
Поскольку увеличение уровней sAPPα связано с усилением познавательных способностей, в еще одном другом аспекте, изобретение находит применение в способе увеличения уровней sAPPα у пациента, включающем (a) идентификацию пациента, нуждающегося в повышенной выработке sAPPα, т.е. пациента, страдающего от нарушения когнитивных функций, и (b) введение пациенту терапевтически эффективного количества соединения-агониста рецептора 5-HT4, где соединение выбирают из {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты и метилового эфира 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты и их фармацевтически приемлемых солей.
Изобретение дополнительно предоставляет фармацевтическую композицию, содержащую фармацевтически приемлемый носитель, соединение-агонист рецептора 5-HT4, где соединение выбирают из {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил} амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты и метилового эфира 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты и их фармацевтически приемлемых солей и ингибитора ацетилхолинэстеразы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Разнообразные аспекты настоящего изобретения иллюстрируют посредством ссылки на прилагаемые чертежи.
Фиг.1-6 отображают среднее значение латентности спасения в секундах на третий день тестирования животных, тестируемых на когнитивную функцию в модели водного лабиринта Морриса для крыс.
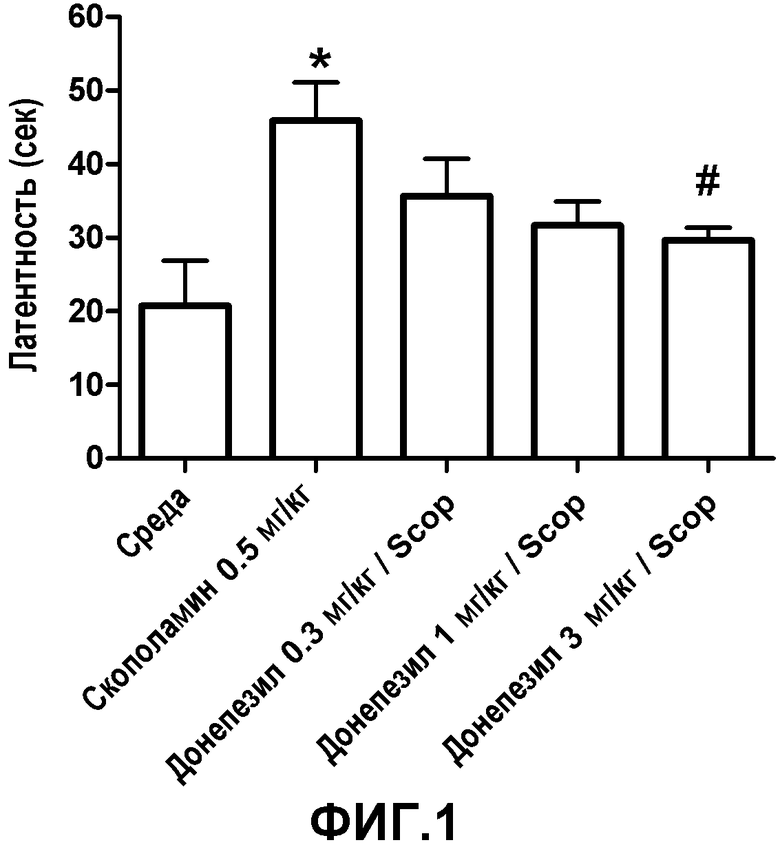
Фиг.1 показывает результаты введения среды, скополамина (Scop) (0,5 мг/кг), донепезила (0,3 мг/кг) плюс скополамин (0,5 мг/кг), донепезила (1 мг/кг) плюс скополамин (0,5 мг/кг) и донепезила (3 мг/кг) плюс скополамин (0,5 мг/кг). * статистически значимые по отношению к среде (t-тест Стьюдента с корректировкой Бонферрони p<0,025), # статистически значимые по отношению к скополамину (0,5 мг/кг) (однофакторный дисперсионный анализ ANOVA для скополамина (0,5 мг/кг) и все дозы донепезила плюс скополамин (0,5 мг/кг), тест Даннета с апостериорными множественными сравнениями p<0,05).
Фиг.2 показывает результаты введения среды, скополамина (Scop) (0,5 мг/кг), донепезила (3 мг/кг) плюс скополамин (0,5 мг/кг), соединения 1 (0,01 мг/кг) плюс скополамин (0,5 мг/кг), соединения 1 (0,03 мг/кг) плюс скополамин (0,5 мг/кг), соединения 1 (0,1 мг/кг) плюс скополамин (0,5 мг/кг) и соединения 1 (0,1 мг/кг) плюс скополамин (0,5 мг/кг). *** статистически значимые по отношению к среде (t-тест Стьюдента с корректировкой Бонферрони p<0,0005), # статистически значимые по отношению к скополамину (0,5 мг/кг) (однофакторный дисперсионный анализ ANOVA для скополамина (0,5 мг/кг) и все дозы соединения 1 плюс скополамин (0,5 мг/кг), тест Даннета с апостериорными множественными сравнениями p<0,05).
Фиг.3 показывает результаты введения среды, скополамина (Scop) (0,5 мг/кг), GR125487 (1 мг/кг), соединения 1 (0,1 мг/кг) плюс GR125487 (1 мг/кг) и скополамин (0,5 мг/кг) и соединения 1 (0,1 мг/кг) плюс скополамин (0,5 мг/кг). * статистически значимые по отношению к среде (t-тест Стьюдента с корректировкой Бонферрони p<0,025), †† статистически значимые по отношению к соединению 1 (0,1 мг/кг) плюс GR125487 (1 мг/кг) и скополамин (0,5 мг/кг) (t-тест Стьюдента с корректировкой Бонферрони p<0,005), # статистически значимые по отношению к скополамину (0,5 мг/кг) (t-тест Стьюдента с корректировкой Бонферрони p<0,025).
Фиг.4 показывает результаты введения среды, скополамина (Scop) (0,5 мг/кг), донепезила (0,1 мг/кг) плюс скополамин (0,5 мг/кг), соединения 1 (0,01 мг/кг) плюс скополамин (0,5 мг/кг) и соединения 1 (0,01 мг/кг) плюс донепезил (0,1 мг/кг) и скополамин (0,5 мг/кг). * статистически значимые по отношению к среде (t-тест Стьюдента p<0,05).
Фиг.5 показывает результаты введения среды, скополамина (Scop) (0,5 мг/кг), донепезила (3 мг/кг) плюс скополамин (0,5 мг/кг), соединения 2 (0,01 мг/кг) плюс скополамин (0,5 мг/кг), соединения 2 (0,03 мг/кг) плюс скополамин (0,5 мг/кг), соединения 2 (0,1 мг/кг) плюс скополамин (0,5 мг/кг) и соединения 2 (1 мг/кг) плюс скополамин (0,5 мг/кг). *** статистически значимые по отношению к среде (t-тест Стьюдента с корректировкой Бонферрони p<0,0005), # статистически значимые по отношению к скополамину (0,5 мг/кг) (однофакторный дисперсионный анализ ANOVA для скополамина (0,5 мг/кг) и все дозы соединения 2 плюс скополамин (0,5 мг/кг), p=0,0096 тест Даннета с апостериорными множественными сравнениями p<0,05).
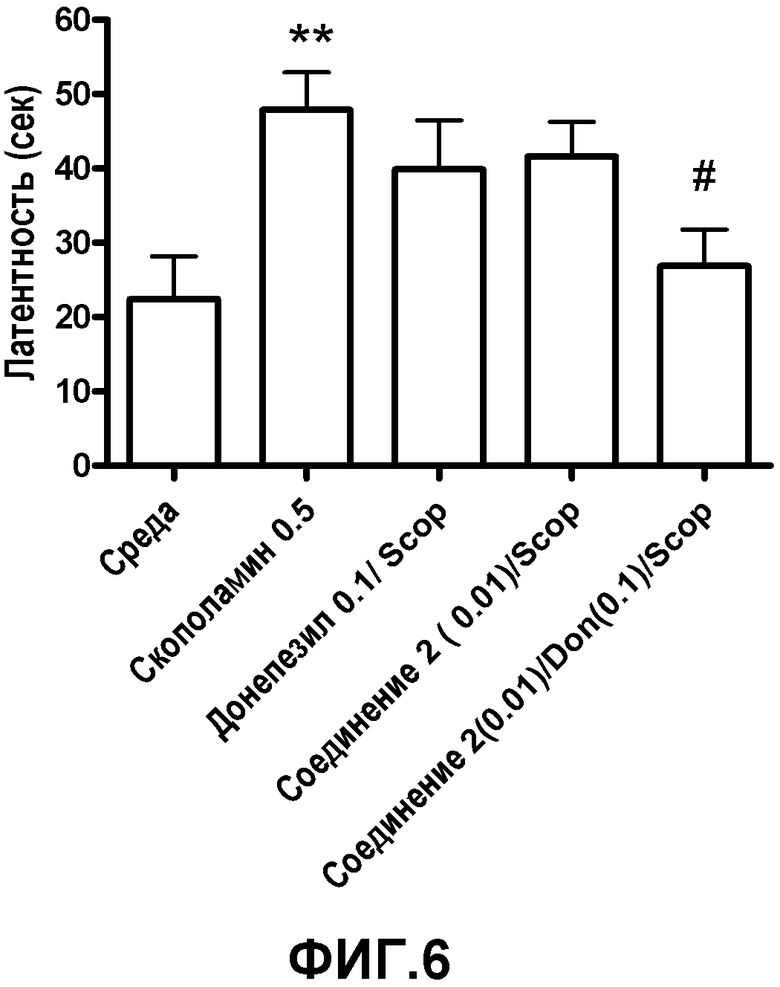
Фиг.6 показывает результаты введения среды, скополамина (Scop) (0,5 мг/кг), донепезила (0,1 мг/кг) плюс скополамин (0,5 мг/кг), соединения 2 (0,01 мг/кг) плюс скополамин (0,5 мг/кг) и соединения 2 (0,01 мг/кг) плюс донепезил (0,1 мг/кг) и скополамин (0,5 мг/кг). ** статистически значимые по отношению к среде (t-тест Стьюдента с корректировкой Бонферрони p<0,005), # статистически значимые по отношению к скополамину (0,5 мг/кг) (t-тест Стьюдента с корректировкой Бонферрони p<0,025).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
При описании композиций и способов изобретения, следующие термины имеют следующие значения, если не указано иначе.
Термин "терапевтически эффективное количество" означает количество, достаточное для проведения лечения при введении пациенту, нуждающемуся в лечении.
Термин "недостаточно эффективное количество" или эквивалентно "недостаточно эффективная доза" означает количество или дозу, более низкие, чем терапевтически эффективное количество или доза.
Термин "лечение", как используется в настоящем документе, означает лечение заболевания, расстройства или медицинского состояния у пациента, такого как млекопитающее (конкретно, человек), которое включает одно или более из следующих:
(a) предотвращение заболевания, расстройства или медицинского состояния из имеющихся, т.е. профилактическое лечение пациента;
(b) улучшение заболевания, расстройства или медицинского состояния, т.е. устранение или стимуляция регрессии заболевания, расстройства или медицинского состояния у пациента, включая противодействие эффектам других терапевтических средств;
(c) подавление заболевания, расстройства или медицинского состояния, т.е. замедление или остановку развития заболевания, расстройства или медицинского состояния у пациента; или
(d) облегчение симптомов заболевания, расстройства или медицинского состояния у пациента.
Термин "комбинированная терапия" как используется в настоящем документе, означает, введение двух или более терапевтических средств как часть протокола лечения, предназначенного для предоставления благоприятных эффектов от комбинированного действия терапевтических средств.
Термин "ингибитор ацетилхолинэстеразы", как используется в настоящем документе, означает любое средство, которое обладает эффектом ингибирования действия ацетилхолинэстеразы. Термин включает средства, именуемые ингибиторы холинэстеразы, которые могут обладать другой активностью в дополнение, например, в качестве ингибиторов бутирилхолинэстеразы.
Термин "донепезил" применяют в данном документе как эквивалент гидрохлорида донепезила.
Демонстрация усиления познавательной деятельности in vivo
Как описано далее в следующих примерах, эффективность действия агонистов 5-HT4, {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты (1) и метилового эфира 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты (2) при обращении нарушения памяти у крыс, индуцированного антагонистами мускариновых рецепторов, оценивали на модели водного лабиринта Морриса.
Соединение 1 при дозах, равных 0,03, 0,1 и 1 мг/кг, и соединение 2 при дозах, равных 0,03 и 0,1 мг/кг, ослабляли нарушение памяти, индуцированное у крыс посредством инъекции скополамина. Для обоих соединений, статистически достоверную ответную реакцию наблюдали при 0,1 мг/кг. Активность и/или эффективность действия обоих соединений-агонистов 5-НТ4, по-видимому, являются сходными с этими характеристиками для донепезила, ингибитора ацетилхолинэстеразы, представленного на рынке для симптоматического лечения болезни Альцгеймера. Эффекты усиления познавательной деятельности соединения 1 и соединения 2 предотвращались при совместном введении каждого соединения с селективным антагонистом 5-HT4, подтверждая включение рецепторов 5-HT4 в наблюдаемую ответную реакцию.
Важно, что был отмечен аддитивный или синергистический эффект между соединением 1 и донепезилом при дозах, равных 0,01 мг/кг и 0,1 мг/кг, соответственно, и между соединением 2 и донепезилом при дозах, равных 0,01 мг/кг и 0,1 мг/кг, соответственно, дозах, которые были неэффективными при обращении скополамин-индуцированного ухудшения познавательной деятельности при введении по отдельности.
Демонстрация высвобождения sAPPα in vitro
Эффекты соединений 1 и 2 на внеклеточное высвобождение sAPPα исследовали на клетках HEK293, стабильно трансфицированных человеческими 5-HT4(d) рецепторами и человеческим APP695 (амилоидным белком-предшественником). Оба соединения индуцировали концентрационно-зависимое увеличение высвобождения sAPPα. Высвобождение блокировалось селективным антагонистом 5-HT4-рецептора GR113808, указывая на то, что наблюдаемый эффект относится к агонизму рецептора 5-HT4.
Способы лечения
Ожидают, что агонисты 5-HT4 настоящего изобретения, соединения 1 и 2, будут применимыми для лечения болезни Альцгеймера или расстройств познавательной способности, включая лечение умеренного когнитивного нарушения и лечение дисфункции памяти, ассоциированное с болезнью Альцгеймера, и деменции по типу Альцгеймера. Соединения в дальнейшем могут найти применение при лечении дополнительных расстройств центральной нервной системы, включая поведенческие нарушения, расстройства настроения, такие как депрессия и тревога, и нарушения контроля автономной функции. В дополнение, было предположено, что соединения, которые увеличивают концентрации ацетилхолина, могут также применяться для лечения других форм деменции, такой как деменция, ассоциированная с болезнью Паркинсона, деменция вследствие сосудистых механизмов и деменция с тельцами Леви.
Аддитивный или синергистический эффект был отмечен в экспериментах на крысах с водным лабиринтом, когда 5-HT4-соединения настоящего изобретения совместно вводили с ингибитором ацетилхолинэстеразы при дозах, где каждое соединение было неэффективным при введении по отдельности. Соответственно, ожидают, что соединения настоящего изобретения будут применимыми для лечения болезни Альцгеймера или расстройств познавательной способности, при введении в сочетании с ингибитором ацетилхолинэстеразы, таким как гидрохлорид донепезила (Aricept®), гидробромид галантамина (Razadyne®, Reminyl®), тартрат ривастигмина (Exelon®) или гидрохлорид такрина (Cognex®). В дополнение к предоставлению благоприятного эффекта от средств, действующих посредством различных комплементарных механизмов действия, комбинированная терапия предлагает дополнительное благоприятное воздействие, позволяя применять более низкие дозировки каждого используемого средства, таким образом, ограничивая степень воздействия для любых неблагоприятных побочных эффектов.
Дополнительно, соединения 1 и 2 могут быть применимыми при совместном введении со средствами, сконструированными для обеспечения симптоматической терапии пациентов с болезнью Альцгеймера, но еще при использовании других механизмов действия. Например, соединения настоящего изобретения могут быть применимыми в сочетании с мемантином (Namenda®), антагонистом рецептора NMDA. Дополнительные средства, которые могут применяться в сочетании для лечения болезни Альцгеймера, включают антагонисты 5-HT6, такие как DMXB-анабазеин, GSK-742457, SUVN-502, PRX-07034 и SAM-531 (WAY-262531); агонисты никотинового рецептора, такие как ABT-089, SSR-180711, AZD-0328 и EVP-6124; мускариновые M1 агонисты, такие как NGX-267, AF-102B (Cevimeline) и WAL 2014 FU (талсаклидин); гистаминовые антагонисты H3, такие как GSK-189254 и PF-365474; и димебон. Также, 5-HT4 агонисты могут иметь благоприятное воздействие в сочетании с другими предполагаемыми терапиями, модифицирующими заболевание, такими как ингибиторы амилоида-бета и ингибиторы тау-аггрегации, ингибиторы бета-секретазы или ингибиторы гамма-секретазы, такие как BMS-708163.
При использовании в комбинированной терапии, 5-HT4 соединения настоящего изобретения либо физически смешивают с другим терапевтическим средством для образования композиции, содержащей оба средства; либо каждое средство присутствует в раздельных и различимых композициях, которые вводят пациенту одновременно или последовательно в любом порядке. Комбинированная терапия включает введение двух средств, при раздельном составлении, по существу в одно и то же время, а также введение каждого средства в различное время.
Например, 5-HT4 соединения настоящего изобретения могут сочетаться со вторым терапевтическим средством с использованием общепринятых методик и оборудования для образования композиции, содержащей соединение 1 или соединение 2 и второе терапевтическое средство. Дополнительно, терапевтическое средство может сочетаться с фармацевтически приемлемым носителем для образования фармацевтической композиции, содержащей соединение 1 или соединение 2, второе терапевтическое средство и фармацевтически приемлемый носитель. В этом варианте осуществления, компоненты композиции обычно смешивают или замешивают для создания физической смеси. Физическую смесь затем вводят в терапевтически эффективном количестве, используя любой из путей, описанных ниже.
Альтернативно, терапевтическое средство может оставаться отдельным и четко отличимым перед введением пациенту. В этом варианте осуществления, средства не смешивают физически вместе перед введением, но вводят одновременно или в разделенные моменты времени в виде раздельных композиций. Такие композиции могут быть упакованы раздельно или могут быть упакованы вместе в виде набора. Два терапевтических средства в наборе могут вводиться посредством одного и того же пути введения или посредством различных путей введения.
При использовании для лечения болезни Альцгеймера или расстройств познавательной способности, соединение 1 или соединение 2 будут типовым образом вводиться перорально в виде разовой суточной дозы или в виде множественных доз в день, несмотря на то что могут применяться другие формы введения. В некоторых обстоятельствах, может быть благоприятным вводить 5-HT соединения настоящего изобретения чрескожно или парентерально. Количество активного средства, вводимого в дозе, или общее количество, вводимое в день, будут обычным образом определяться терапевтом в свете имеющихся обстоятельств, включая тяжесть состояния, подлежащего лечению, выбранный путь введения, конкретное вводимое соединение и его относительную активность, возраст, массу тела и ответную реакцию индивидуального пациента и т.п.
Подходящие дозы для лечения болезни Альцгеймера или расстройств познавательной способности будут находиться в интервале от приблизительно 0,1 до приблизительно 90 мг в день средства-агониста 5-HT4 для средней массы тела человека, равной 70 кг, включая, например, от приблизительно 1 до приблизительно 50 мг в день соединения 1 и от приблизительно 0,5 до приблизительно 20 мг в день соединения 2.
Когда 5-HT4-соединения настоящего изобретения применяют в комбинированной терапии с ингибитором ацетилхолинэстеразы, ингибитор ацетилхолинэстеразы вводят в терапевтически эффективном количестве, т.е. в любом количестве, которое продуцирует терапевтически благоприятный эффект при совместном введении с соединением 1 или соединением 2. Подходящие дозы для ингибитора ацетилхолинэстеразы, вводимого в сочетании с соединениями настоящего изобретения, обычно находятся в интервале от приблизительно 1 мг/день до приблизительно 30 мг/день. Как описано прежде, при использовании в качестве части комбинированной терапии, эффективная доза каждого индивидуального средства может быть более низкой, чем эффективная доза, когда средства применяют независимо.
Фармацевтические композиции
Агонисты 5-HT4 настоящего изобретения и другие терапевтические средства, такие как ингибиторы ацетилхолинэстеразы, обычно вводят пациенту в форме фармацевтической композиции или готовой лекарственной форме. Такие фармацевтические композиции могут вводиться пациенту посредством любого приемлемого пути введения, включая, но не ограничиваясь ими, пероральный, ректальный, вагинальный, назальный, ингаляционный, местный (включая чрескожный) и парентеральные режимы введения.
Фармацевтические композиции обычно содержат терапевтически эффективное количество активных средств. Квалифицированные специалисты в данной области смогут понять, однако, что фармацевтическая композиция может содержать большее, чем терапевтически эффективное, количество, т.е. объемные композиции, или меньшее, чем терапевтически эффективное, количество, т.е. индивидуальные разовые дозы, разработанные для множественного введения, чтобы достичь терапевтически эффективного количества.
Обычно, такие фармацевтические композиции будут содержать от приблизительно 0,1 до приблизительно 95% масс активного средства; предпочтительно, от приблизительно 5 до приблизительно 70% масс активного средства.
В фармацевтических композициях изобретения может применяться любой традиционный носитель или эксципиент. Выбор конкретного носителя или эксципиента или сочетаний носителей или эксципиентов, будет зависеть от режима используемого введения для лечения конкретного пациента или типа медицинского состояния или состояния заболевания. В этом отношении, получение подходящей фармацевтической композиции для конкретного режима введения хорошо осуществлять в пределах объема квалификации специалистов в области фармацевтики. Дополнительно, носители или эксципиенты, используемые в фармацевтических композициях данного изобретения, являются доступными для приобретения. Посредством дополнительной иллюстрации, общепринятые методы получения лекарственных форм описаны в Remington: The Science and Practice of Pharmacy, 20th Edition, Lippincott Williams & White, Baltimore, Maryland (2000); и H. C. Ansel et al., Pharmaceutical Dosage Forms and Drug Delivery Systems, 7th Edition, Lippincott Williams & White, Baltimore, Maryland (1999).
Примеры веществ, которые могут служить в качестве фармацевтически приемлемых носителей, включают, но не ограничены ими, следующие: сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлоза, такая как микрокристаллическая целлюлоза, и ее производные, такие как натриевая соль карбоксиметилцеллюлозы, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; эксципиенты, такие как масло какао и суппозиторные воска; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль; полиолы, такие как глицерин, сорбит, маннитол и полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные средства, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический физиологический раствор; раствор Рингера; этиловый спирт; фосфатные буферные растворы и другие нетоксичные совместимые вещества, используемые в фармацевтических композициях.
Фармацевтические композиции обычно получают посредством тщательного и плотного смешивания или замешивания активного средства с фармацевтически-приемлемым носителем и одним или более необязательными ингредиентами. Полученная в результате однородно замешанная смесь может затем формоваться или загружаться в таблетки, капсулы, пилюли и т.п. с использованием общепринятых методик и оборудования.
Фармацевтические композиции предпочтительно упаковывают в единичную дозированную лекарственную форму. Термин "единичная дозированная лекарственная форма" относится к физически дискретной единице, пригодной для дозирования пациента, т.е. каждой единице, содержащей предварительно определенное количество активного средства, рассчитанное для получения желательного терапевтического эффекта либо по отдельности, либо в сочетании с одной или более дополнительными единицами. Например, такие единичные дозированные лекарственные формы могут представлять собой капсулы, таблетки, пилюли и т.п. или упаковки, содержащие единичную дозу, пригодную для парентерального введения.
В одном варианте осуществления, фармацевтические композиции изобретения являются подходящими для перорального введения. Подходящие фармацевтические композиции для перорального введения могут находиться в форме капсул, таблеток, пилюль, лепешек, облаток, драже, порошков, гранул; или в виде раствора или суспензии в водной или неводной жидкости; или в виде жидкой эмульсии масло-в-воде или вода-в-масле; или в виде эликсира или сиропа и т.п.; причем каждая содержит предварительно определенное количество терапевтического соединения в качестве активного ингредиента.
Когда они предназначены для перорального введения в твердой лекарственной форме (т.е. в виде капсул, таблеток, пилюль и т.п.), фармацевтические композиции будут обычно содержать активное средство и один или более фармацевтически приемлемых носителей, таких как цитрат натрия или дикальцийфосфат. Необязательно или альтернативно, такие твердые лекарственные формы могут также содержать: наполнители или расширители, такие как крахмалы, микрокристаллическая целлюлоза, лактоза, сахароза, глюкоза, маннитол и/или кремниевая кислота; связующие вещества, такие как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и/или акация; смачивающие средства, такие как глицерин; дезинтегрирующие средства, такие как агар-агар, карбонат кальция, картофельный крахмал или крахмал из тапиоки, альгиновая кислота, некоторые силикаты и/или карбонат натрия; средства, замедляющие растворение, такие как парафин; ускорители абсорбции, такие как четвертичные аммониевые соединения; увлажняющие средства, такие как цетиловый спирт и/или моностеарат глицерина; абсорбенты, такие как каолиновая и/или бентонитовая глина; смазки, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и/или их смеси; красящие средства и буферные средства.
Высвобождающие средства, увлажняющие средства, покровные средства, подсластители, ароматизаторы и отдушки, консерванты и антиоксиданты могут также присутствовать в фармацевтических композициях изобретения. Примеры фармацевтически приемлемых антиоксидантов включают: водорастворимые антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфат натрия, сульфит натрия и т.п.; растворимые в масле антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол, бутилированный гидрокситолуол, лецитин, пропилгаллат, альфа-токоферол и т.п.; и металл-хелатирующие средства, такие как лимонная кислота, этилендиаминтетрауксусная кислота, сорбит, винная кислота, фосфорная кислота и т.п. Покровные средства для таблеток, капсул, пилюль и т.п. включают средства, применяемые для энтеросолюбильных покрытий, таких как фталатацетатцеллюлоза, поливинилацетатфталат, фталат гидроксипропилметилцеллюлозы, сополимеры метакриловой кислоты-сложного эфира метакриловой кислоты, тримеллитатацетатцеллюлоза, карбоксиметилэтилцеллюлоза, сукцинат ацетата гидроксипропилметилцеллюлозы и т.п. Покровные средства также включают тальк, полиэтиленгликоль, гипомеллозу и диоксид титана.
Фармацевтические композиции могут также быть составлены для предоставления медленного или контролируемого высвобождения активного средства с использованием, например, гидроксипропилметилцеллюлозы в изменяющихся пропорциях или другие полимерные матрицы, липосомы и/или микросферы. В дополнение, фармацевтические композиции могут необязательно содержать опалесцирующие средства и могут быть составлены таким образом, что они высвобождают активный ингредиент только или, предпочтительно, в определенной части желудочно-кишечного тракта, необязательно, замедленным образом. Примеры погружающих композиций, которые могут применяться, включают полимерные вещества и воска. Активное средство может также находиться в микроинкапсулированной форме, если необходимо, с одним или более из описанных выше эксципиентов.
Подходящие жидкие дозированные лекарственные формы для перорального введения включают, для иллюстрации, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Жидкие дозированные лекарственные формы обычно содержат активное средство и инертный разбавитель, такой как, например, вода или другие растворители, солюбилизирующие средства и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (особенно, хлопковое, арахисовое, кукурузное, из ростков пшеницы, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и жирнокислотные сложные эфиры сорбитана и их смеси. Суспензии, в дополнение к активному ингредиенту, могут содержать суспендирующие средства, такие как, например, этоксилированные изостеариловые спирты, сложные эфиры полиоксиэтилен-сорбита и сорбитана, микрокристаллическую целлюлозу, метагидроксид алюминия, бентонит, агар-агар и трагакант и их смеси.
Активные средства настоящего изобретения могут также вводиться парентерально (например, посредством внутривенной, подкожной, внутримышечной или внутрибрюшинной инъекции). Для парентерального введения активное средство обычно смешивают с подходящей средой для парентерального введения, включая, например, стерильные водные растворы, физиологический раствор, спирты с низкой молекулярной массой, такие как пропиленгликоль, полиэтиленгликоль, растительные масла, желатин, сложные эфиры жирных кислот, такие как этилолеат, и т.п. Парентеральные готовые лекарственные формы могут также содержать один или более из антиоксидантов, солюбилизаторов, стабилизаторов, консервантов, увлажняющих средств, эмульгаторов, буферных средств или диспергирующих средств. Этим средам можно придать стерильность посредством применения стерильной среды для инъекций, стерилизующего средства, фильтрации, облучения или нагрева.
Альтернативно, средства составляют для введения посредством ингаляции. Подходящие фармацевтические композиции для введения посредством ингаляции будут типовым образом находиться в виде аэрозоля или порошка. Такие композиции обычно вводят, используя хорошо известные устройства для доставки, такие как дозирующий ингалятор, ингалятор сухого порошка, распылитель или аналогичное устройство для доставки.
При введении посредством ингаляции с использованием находящегося под давлением контейнера, фармацевтические композиции изобретения будут типовым образом содержать активный ингредиент и подходящий пропеллент, такой как дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, диоксид углерода или другой подходящий газ. Дополнительно, фармацевтическая композиция может находиться в форме капсулы или картриджа (сделанного, например, из желатина), содержащих соединение изобретения и порошок, подходящий для применения в порошковом ингаляторе. Подходящие порошковые основы включают, например, лактозу или крахмал.
Кроме того, активные средства могут также вводиться чрескожно с использованием известных систем чрескожной доставки и эксципиентов. Например, активное средство может быть смешано с усилителями проницаемости, такими как пропиленгликоль, монолаурат полиэтиленгликоля, азациклоалкан-2-оны и т.п., и введено в пластырь или сходную систему доставки. Дополнительные эксципиенты, включающие гелеобразующие средства, эмульгаторы и буферы, могут применяться в таких чрескожных композициях, если желательно.
Репрезентативные фармацевтические композиции, применимые для лечения болезни Альцгеймера или расстройств познавательной способности, включают, но не ограничены ими, следующие примеры, где 'соединение изобретения' представляет соединение 1 или соединение 2. Соединение 1 обычно поставляют в виде гидрохлоридной соли, а соединение 2 обычно поставляют в виде свободного основания, но будет понятным, что любая форма соединения (т.е. свободное основание или фармацевтическая соль), которые являются подходящими для конкретного режима введения, могут применяться в следующих фармацевтических композициях.
Пример готовой лекарственной формы A: Твердые желатиновые капсулы для перорального введения
Соединение изобретения (20 мг), крахмал (89 мг), микрокристаллическую целлюлозу (89 мг) и стеарат магния (2 мг) тщательно смешивают и затем пропускают через сито № 45 меш США. Полученную в результате композицию загружают в твердые желатиновые капсулы (200 мг композиции на капсулу).
Пример готовой лекарственной формы B: Желатиновые капсулы для перорального введения
Соединение изобретения (10 мг), моноолеат полиоксиэтиленсорбитана (50 мг) и порошок крахмала (250 мг) тщательно смешивают и затем загружают в желатиновую капсулу (310 мг композиции на капсулу).
Пример готовой лекарственной формы C: Таблетки для перорального введения
Соединение изобретения (5 мг), микрокристаллическую целлюлозу (400 мг), высокодисперсный диоксид кремния (10 мг) и стеариновую кислоту (5 мг) тщательно смешивают и затем прессуют с образованием таблеток (420 мг композиции на таблетку).
Пример готовой лекарственной формы D: Таблетки для перорального введения
Соединение изобретения (2 мг), микрокристаллическую целлюлозу (400 мг), высокодисперсный диоксид кремния (10 мг) и стеариновую кислоту (5 мг) тщательно смешивают и затем прессуют с образованием таблеток (417 мг композиции на таблетку).
Пример готовой лекарственной формы E: Таблетки для перорального введения
Соединение изобретения (20 мг), микрокристаллическую целлюлозу (400 мг), высокодисперсный диоксид кремния (10 мг) и стеариновую кислоту (5 мг) тщательно смешивают и затем прессуют с образованием таблеток (435 мг композиции на таблетку).
Пример готовой лекарственной формы F: Таблетки с одной риской для перорального введения
Соединение изобретения (15 мг), кукурузный крахмал (50 мг), кроскармеллозу натрия (25 мг), лактозу (120 мг) и стеарат магния (5 мг) тщательно смешивают и затем прессуют с образованием таблетки с одной риской (215 мг композиции на таблетку).
Пример готовой лекарственной формы G: Суспензия для перорального введения
Следующие ингредиенты тщательно смешивают с образованием суспензии для перорального введения, содержащей 20 мг активного ингредиента на 10 мл суспензии: соединение изобретения (200 мг), бензоат натрия, цитрат натрия, очищенная вода (q.s. до 100 мл).
Пример готовой лекарственной формы H: Готовая лекарственная форма для инъекций
Соединение изобретения (20 мг) смешивают с буферным раствором 0,1M цитрата натрия (15 мл). pH полученного в результате раствора регулируют до pH 6, используя 1N водную хлористоводородную кислоту или 1N водный гидроксид натрия. Затем добавляют стерильный нормальный физиологический раствор в цитратном буфере для обеспечения общего объема, равного 20 мл.
Пример готовой лекарственной формы I: Таблетки с одной риской для перорального введения
Соединение изобретения (5 мг), гидрохлорид донепезила (5 мг), кукурузный крахмал (50 мг), микрокристаллическую целлюлозу (15 мг), гидроксипропилцеллюлозу (10 мг), лактозу (120 мг) и стеарат магния (5 мг) тщательно смешивают и затем прессуют с образованием таблетки с одной риской (210 мг композиции на таблетку).
Пример готовой лекарственной формы J: Суспензия для перорального введения
Следующие ингредиенты тщательно смешивают с образованием суспензии для перорального введения, содержащей 5 мг каждого средства на 10 мл суспензии: соединение изобретения (50 мг), тартрат ривастигмина (50 мг), бензоат натрия, цитрат натрия, очищенная вода (q.s. до 100 мл).
ПРИМЕРЫ
Способность агонистов 5-HT4, {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты (1) и метилового эфира 4-(4-{[(2-изопропил-1H-бензимидазол-4-карбонил)амино]метил}пиперидин-1-илметил)пиперидин-1-карбоновой кислоты (2), применяемых по отдельности или в сочетании с ингибитором ацетилхолинэстеразы, донепезилом, для предотвращения нарушения пространственной памяти, индуцированного антагонистом мускаринового рецептора, скополамином, оценивали у крыс на модели водного лабиринта Морриса для животных (Morris (1984) Journal of Neuroscience Methods 11:47-60). Гидрохлоридную соль соединения 1 применяли во всех экспериментах.
Методология модели Морриса с водным лабиринтом
Взрослые самцы крыс Sprague-Dawley (диапазон массы тела 275-400 г) приручались исследователем в течение приблизительно 5 минут за один день перед каждым исследованием. В первый день исследования каждой крысе внутрибрюшинно (вн.бр.) вводили дозу, сначала тестируемого соединения или среды, с последующим немедленным введением антагониста мускаринового рецептора, скополамина (0,5 мг/кг), дозы, ранее установленной для предоставления близкого к максимальному когнитивного отклонения в данной модели, или среды. Через тридцать минут после дозирования крыс помещали индивидуально в круглую темно-синюю полиэтиленовую емкость (6 футов в диаметре), заполненную водой (поддерживаемую при 23°C±1°C). Чистую платформу Perspex® располагали в фиксированном положении на 1 см ниже поверхности воды и на 34 см от стены емкости. Четыре визуальных ключевых раздражителя (картинки формата A4 с различными черными и белыми символами) равномерно располагали по стене емкости, непосредственно над поверхностью воды. Вокруг емкости размещали черные шторы и генерировали белый шум на протяжении всего теста. Каждую крысу высвобождали в воду, обращая к стенке емкости, в обозначенной исходной точке (т.е. у северной стороны емкости) и давали 60 секунд установить местонахождение погруженной в воду платформы после каждого размещения. Латентность спасения (в секундах) между высвобождением крысы в воду и ее установлением на платформе регистрировали автоматически видеокамерой (San Diego Instrument, CA) и программным обеспечением для слежения (SMART software, San Diego Instrument, CA). Когда крысе не удавалось найти платформу за 60 секунд, ее направляли в сторону платформы и затем помещали на ней (обращая к конкретному визуальному раздражителю). Крысам позволяли оставаться на платформе в течение 30 секунд для наблюдения внешних визуальных раздражителей и ассоциирования их с относительным положением платформы. Крыс затем забирали с платформы и осторожно высушивали бумажным полотенцем перед повторением теста еще три раза (с исходных положений, соответствующих югу, затем востоку и окончательно западу). После четвертого теста каждую крысу помещали под лампу нагрева на 5 минут перед возвращением в ее клетку для содержания. Полную процедуру повторяли в дни 2 и 3. В течение трех дней тестирования крысы учились ассоциировать расположение погруженной в воду платформы (и их единственного средства для спасения из воды) с визуальными раздражителями.
Оценивали способность тестируемого средства ингибировать индуцированное скополамином когнитивное нарушение. На день 4 каждой крысе вводили дозу, как прежде, и подвергали 2-минутному "пробному испытанию", в течение которого платформу удаляли из емкости. Число пересеканий предыдущего расположения платформы и время, проведенное крысой в каждом квадранте, регистрировали. Животные, которые выучивали расположение платформы, проводили больше времени в соответствующем квадранте и повторно пересекали этот квадрант. Посредством осуществления пробного теста ложноположительные результаты могли быть исключены из анализа (т.е. крысы, которые прежде установили расположение платформы посредством стратегии, независимой от визуальных раздражителей, такой как разупорядоченное плавание до прикасания ноги к платформе). Ни одно животное не было исключено, на основании противоречий между данными трех дней тестирования и пробного теста.
Анализ данных
Среднюю латентность спасения от каждой из четырех попыток в тот же день тестирования рассчитывали для индивидуальных крыс и затем эти данные объединяли для определения средней латентности спасения для каждой группы обработки в дни 1, 2 и 3. С данными проводили следующие статистические тесты.
Используя t-тест Стьюдента, сравнивали значения латентностей спасения групп среда/среда и среда/скополамин. Значение α корректировали по Бонферрони до 0,025, поскольку группу среда/скополамин подвергали как t-тесту Стьюдента, так и тесту с однофакторным дисперсионным анализом ANOVA.
Однофакторный дисперсионный анализ ANOVA, с последующим тестом Даннета с апостериорными множественными сравнениями, применяли для сравнения латентностей спасения для групп среда/скополамин и тестируемое соединение/скополамин, с p<0,05, указывающим на статистически значимое различие.
Двухфакторный с повторными измерениями дисперсионный анализ ANOVA, с последующим тестом Бонферрони с апостериорными множественными сравнениями, применяли для сравнения средней латентности спасения для каждого из трех последовательных дней тестирования, с p<0,05, указывающим на статистически значимое различие.
Материалы
Соединения-агонисты 5-НТ4 1 и 2 получали в соответствии с методиками, описанными в патентах США №№ 7375114 B2 и 7256294 B2, соответственно, раскрытия которых включены в данный документ посредством ссылки. Гидрохлорид донепезила был приобретен от Changzhou Dahua Imp. и Exp. Corp. Ltd. (Changzhou, Jiangsu, China), в то время как скополамина гидрохлорид был приобретен от Sigma Aldrich (St. Louis, MO) или Spectrum Chemical Mfg. Corp. (Gardena, CA). GR125487 сульфамат был приобретен от Tocris (Ellisville, MO). Соединения 1 и 2 и донепезил были составлены в 5% диметилсульфоксиде и 95% стерильном физиологическом растворе, в то время как скополамин и GR125487 были получены в 100% стерильном физиологическом растворе. Дозы были выражены по отношению к массам свободного основания каждого соединения.
Обоснование модели
В каждом исследовании, дозирование (вн.бр.) крыс средой за 30 мин перед тестом приводило к постепенному снижению латентности спасения. В день 1 крысы, обработанные средой, обычно располагались на скрытой платформе со средней латентностью от четырех попыток в интервале 40-50 секунд, в то время как в день 3 это сокращалось до 10-25 секунд. Скополамин (0,5 мг/кг вн.бр.) производил статистически значимое ослабление обучения (p<0,025, t-тест Стьюдента с корректировкой Бонферрони) по сравнению с животными, обработанными средой. Ингибитор ацетилхолинэстеразы донепезил (3 мг/кг вн.бр.) и агонисты рецептора 5-HT4, соединение 1 (1 мг/кг вн.бр.) и соединение 2 (1 мг/кг вн.бр.), не оказывали эффекта, положительного или отрицательного, на способность крыс узнать расположение погруженной в воду платформы при введении по отдельности, т.е. при введении животным, которые не были подвергнуты воздействию скополамина. Донепезил (0,3-3 мг/кг вн.бр.) обращал индуцированный скополамином (0,5 мг/кг вн.бр.) дефицит распознавания дозозависимым образом, как показано на Фиг.1, где отображена средняя латентность спасения на третий день тестирования. Доза донепезила при 3 мг/кг производила статистически значимое обращение эффекта.
Пример 1: Эффект соединения 1 на индуцированное скополамином когнитивное нарушение
Соединение 1 тестировали при дозах, равных 0,01, 0,03, 0,1 и 1 мг/кг, на модели водного лабиринта Морриса для крыс. Как показано на Фиг.2, где отображена средняя латентность спасения на третий день тестирования, соединение 1 было ассоциировано с обращением нарушения памяти, продуцированным 0,5 мг/кг скополамина. Эффект соединения 1 при дозе, равной 0,1 мг/кг, достигал статистической значимости по отношению к скополамину (0,5 мг/кг). "U-образная" кривая зависимости доза-ответ была явной; наивысшая доза соединения 1, 1 мг/кг, не оказывала эффекта на индуцированную скополамином ответную реакцию в отличие от дозы 0,1 мг/кг. Соединение 1 (0,1 мг/кг вн.бр.) производило обращение эффекта, сходное с донепезилом (3 мг/кг вн.бр.), на день 3 (т.е. в интервале 50-60%, см. Фиг.1).
Пример 2: Эффект соединения 1 вместе с антагонистом рецептора 5-HT 4 на индуцированное скополамином когнитивное нарушение
Для того чтобы проверить, могут ли наблюдаемые эффекты соединения 1 быть отнесены к агонизму на рецепторе 5-HT4, соединение 1 тестировали вместе с GR125487, селективным соединением-антагонистом рецептора 5-HT4. Как показано на Фиг.3, GR125487 (1 мг/кг вн.бр.) не оказывало эффекта при введении по отдельности. Однако совместное введение антагониста GR125487 (1 мг/кг вн.бр.) отменяло способность соединения 1 (0,1 мг/кг вн.бр.) обращать индуцированное скополамином когнитивное нарушение. Следовательно, рационально заключить, что наблюдаемые эффекты соединения 1 обусловлены агонизмом рецептора 5-HT4.
Пример 3: Эффект совместного введения соединения 1 вместе с ингибитором ацетилхолинэстеразы, донепезилом, на индуцированное скополамином когнитивное нарушение
Эффект совместного введения соединения 1 и донепезила проиллюстрирован на Фиг.4. Ни соединение 1 при дозе, равной 0,01 мг/кг, ни донепезил при дозе, равной 0,1 мг/кг, не обнаруживали значительного эффекта при введении по отдельности. Однако такие же дозы соединения 1 и донепезила, при составлении вместе в 5% DMSO и 95% стерильном физиологическом растворе, приводили в результате к заметному ослаблению когнитивного ухудшения, индуцированного скополамином.
Пример 4: Эффект соединения 2 на индуцированное скополамином когнитивное нарушение
Соединение 2 тестировали, как описано в Примере 1. Как проиллюстрировано на Фиг.5, эффект соединения 2 при дозе, равной 0,1 мг/кг, достигал статистической значимости по отношению к скополамину. "U-образная" кривая зависимости доза-ответ была явной; наивысшая доза соединения 2, 1 мг/кг, не оказывала эффекта на индуцированную скополамином ответную реакцию, в отличие от доз 0,03 и 0,1 мг/кг. Соединение 2 (0,1 мг/кг вн.бр.) производило сходное обращение эффекта с обращением эффекта от донепезила (3 мг/кг вн.бр.) на день 3 (т.е. в интервале 50-60%, см. Фиг.1).
Пример 5: Эффект соединения 2 вместе с антагонистом рецептора 5-HT 4 на индуцированное скополамином когнитивное нарушение
Эффект совместного введения соединения 2 с антагонистом рецептора 5-HT4, GR125487, был проверен, как описано в Примере 2. Добавление GR125487 (1 мг/кг вн.бр.) отменяло способность соединения 2 (0,1 мг/кг вн.бр.) обращать индуцированное скополамином когнитивное нарушение, указывая на то, что наблюдаемые эффекты соединения 2 обусловлены агонизмом рецептора 5-HT4.
Пример 6: Эффект совместного введения соединения 2 вместе с ингибитором ацетилхолинэстеразы, донепезилом, на индуцированное скополамином когнитивное нарушение
Эффект совместного введения соединения 2 и донепезила проиллюстрирован на Фиг.6. Ни соединение 2 при дозе, равной 0,01 мг/кг, ни донепезил при дозе, равной 0,1 мг/кг, не обнаруживали значительного эффекта при введении по отдельности. Однако такие же дозы соединения 2 и донепезила, при составлении вместе в 5% DMSO и 95% стерильном физиологическом растворе, приводили в результате к статистически значимому обращению эффекта (t-тест Стьюдента с корректировкой Бонферрони p<0,025) индуцированного скополамином когнитивного отклонения.
Пример 7: Исследование in vitro эффектов соединения 1 и соединения 2 на внеклеточное высвобождение sAPPα в клетках HEK293-5-HT 4(d) -APP 695
Культура клеток
Клетки HEK-293 (почка эмбриона человека), устойчиво трансфицированные кДНК человеческого рецептора 5-HT4(d) и кДНК человеческого APP695 кДНК (HEK293-5-HT4(d)-APP695), выращивали в среде Игла, модифицированной Дульбекко (DMEM), содержащей D-глюкозу, дополненной 10% сывороткой зародыша теленка, 2 мМ GlutaMax-1 и 100 единицами пенициллина (100 мкг) и 100 мкг/мл стрептомицина в 5% CO2, в увлажняемом инкубаторе при 37°C. Клетки выращивали при непрерывном селекционном давлении посредством добавления антибиотика G418 (500 мкг/мл).
Высвобождение sAPPα
Клетки HEK293-5-HT4(d)-APP695 (3×105 клеток/лунка) были лишены сыворотки в течение 4-часового периода перед инкубацией с агонистами в течение 30 мин (если не установлено иначе) при 37°C. Культуральную среду аспирировали, центрифугировали для удаления продуктов распада клеток и уровень sAPPα определяли посредством Вестерн-блоттинга. sAPPα обнаруживали, используя антитела 6E10 (Signet/Covance) и козьи против-мышиных HRP-конъюгированные 2° антитела. Иммунореактивные полосы, соответствующие sAPPα, визуализировали и количественно оценивали с использованием субстрата ECL (Pierce) и системы визуализации FluorChem HD2 (Alpha Innotech). Анализ образцов методом Вестерн-блоттинга проводили в двух повторностях.
Результаты
Данные по активности приведены в виде значений pEC50, отрицательного десятичного логарифма значения EC50, где EC50 представляет собой эффективную концентрацию для 50% максимальной ответной реакции. Тестируемые соединения, проявляющие более высокое значение pEC50 в данном исследовании, имеют более высокую активность по стимуляции высвобождения sAPPα. Для определения значений EC50, данные от независимых экспериментов были нанесены одновременно на сигмоидальную кривую зависимости ответной реакции от концентрации, с использованием программного обеспечения Graph Pad Prism (ограниченный наклон до единства). Данные по активности для соединения 1 и соединения 2 вместе с выраженной в процентах ответной реакцией относительно эффекта эндогенного лиганда 5-HT при концентрации 1 мкМ приведены ниже:
(% ответа относительно 1 мкМ 5-НТ)
Эффект селективного антагониста рецептора 5-HT4, GR113808, был проверен посредством инкубации клеток в течение 10 мин с 1 мкМ GR113808 перед инкубированием с соединением 1 или соединением 2 при концентрации, равной 100 нМ, концентрации, при которой соединения индуцировали близкую к максимальной или максимальную ответную реакцию. Антагонист полностью блокировал эффект соединения 1 и соединения 2, указывая на то, что наблюдаемое высвобождение sAPPα относится к агонизму рецептора 5-HT4.
В то время как настоящее изобретение было описано со ссылками на его конкретные варианты осуществления, квалифицированные специалисты в данной области должны понимать, что могут быть сделаны разнообразные изменения и могут замещаться эквиваленты без отступления от истинной сущности и объема притязаний изобретения. В дополнение, может быть сделано множество модификаций для адаптации конкретных ситуации, материала, композиции вещества, способа, стадии или стадий способа к цели, сущности и объему притязаний настоящего изобретения. Подразумевают, что все такие модификации предназначены для включения в пределы объема притязаний формулы изобретения, приложенной к описанию. Дополнительно, все публикации, патенты и патентные документы, цитируемые здесь выше, включены в данный документ посредством ссылки полностью, как если бы они были включены посредством ссылки индивидуально.




Группа изобретений относится к медицине, а именно к неврологии, и может быть использована для лечения болезни Альцгеймера или расстройства познавательной способности у пациента. Для этого вводят агонист рецептора 5-НТ4, который представляет собой {[1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль, и гидрохлорид донепезила, где агонист рецептора 5-НТ4 и гидрохлорид донепезила каждый вводят в дозе, которая является недостаточно эффективной для лечения болезни Альцгеймера или расстройства познавательной способности при введении по отдельности. Способ позволяет усилить эффект действия ингибитора ацетилхолинэстеразы (АХЭ) при введении агониста рецептора 5-НТ4 в дозах, которые являются недостаточно эффективными при введении их по отдельности. 8 н. и 3 з.п. ф-лы, 3 ил., 1 табл., 7 пр.
1. Способ лечения болезни Альцгеймера или расстройства познавательной способности у пациента, включающий введение пациенту агониста рецептора 5-НТ4, где агонист рецептора 5-НТ4 представляет собой {[1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль, и гидрохлорида донепезила, где агонист рецептора 5-НТ4 и гидрохлорид донепезила каждый вводят в дозе, которая является недостаточно эффективной для лечения болезни Альцгеймера или расстройства познавательной способности, при введении по отдельности.
2. Способ по п. 1, где агонист рецептора 5-НТ4 представляет собой гидрохлорид {(1S, 3R, 5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты.
3. Способ улучшения памяти у пациента, испытывающего нарушение памяти, включающий введение пациенту агониста рецептора 5-НТ4, где агонист рецептора 5-НТ4 представляет собой {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль, и гидрохлорида донепезила, где агонист рецептора 5-НТ4 и гидрохлорид донепезила каждый вводят в дозе, которая является недостаточно эффективной для лечения болезни Альцгеймера или расстройства познавательной способности, при введении по отдельности.
4. Способ по п. 3, где агонист рецептора 5-НТ4 представляет собой гидрохлорид { (1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амида 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты.
5. Способ увеличения уровней sAPPα у пациента, включающий:
(a) идентификацию пациента, нуждающегося в повышенной выработке sAPPα; и
(b) введение пациенту соединения-агониста рецептора 5-НТ4, где соединение представляет собой {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль в количестве, эффективном для увеличения выработки sAPPα.
6. Применение агониста 5-НТ4, где агонистом 5-НТ4 является {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемая соль в комбинации с гидрохлоридом донепезила для лечения болезни Альцгеймера или расстройства познавательной способности у пациента, где агонист рецептора 5-НТ4 и гидрохлорид донепезила каждый вводят в дозе, которая является недостаточно эффективной для лечения болезни Альцгеймера или расстройства познавательной способности, при введении по отдельности.
7. Применение агониста 5-НТ4, который представляет собой {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль, для усиления эффективности гидрохлорида донепезила для лечения болезни Альцгеймера или расстройства познавательной способности.
8. Применение агониста 5-НТ4, который представляет собой {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль, в комбинации с гидрохлоридом донепезила для улучшения памяти у пациента, испытывающего нарушение памяти, где агонист рецептора 5-НТ4 и гидрохлорид донепезила каждый вводят в дозе, которая является недостаточно эффективной для лечения болезни Альцгеймера или расстройства познавательной способности, при введении по отдельности.
9. Фармацевтическая композиция для лечения болезни Альцгеймера или расстройства познавательной способности, содержащая ингибитор ацетилхолинэстеразы, агонист рецептора 5-НТ4, где агонист рецептора 5-НТ4 представляет собой {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль, и фармацевтически приемлемый носитель.
10. Фармацевтическая композиция по п. 9, где ингибитор ацетилхолинэстеразы представляет собой гидрохлорид донепезила.
11. Применение агониста 5-НТ4, где агонист 5-НТ4 представляет собой {(1S,3R,5R)-8-[(R)-2-гидрокси-3-(метансульфонилметиламино)пропил]-8-азабицикло[3.2.1]окт-3-ил}амид 1-изопропил-2-оксо-1,2-дигидрохинолин-3-карбоновой кислоты или его фармацевтически приемлемую соль, для изготовления лекарственного средства для применения в комбинации с гидрохлоридом донепезила для лечения болезни Альцгеймера или расстройства познавательной способности у пациента, где лекарственное средство предназначено для применения в дозе агониста рецептора 5-НТ4 и донепезила гидрохлорида, которая является недостаточно эффективной для лечения болезни Альцгеймера или расстройства познавательной способности, при введении по отдельности.
| WO2006108127 A2, 12.1.2012 | |||
| US 7375114 B2, 20.05.2008 | |||
| ДАМУЛИН И.В | |||
| "Болезнь Альцгеймера: некоторые дифференциально-диагностические и терапевтические аспекты", с.1 абзац 1// найдено[25.03.2014] найдено из Интернет: http://medi.ru/doc/a030101.htm | |||
| VAN DEN HEUVEL C | |||
| et al | |||
| Neuroprotective effects of SAAPa administration following diffuse traumatic |
Авторы
Даты
2015-11-20—Публикация
2010-04-12—Подача