ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к соединению, представленному общей формулой (I):
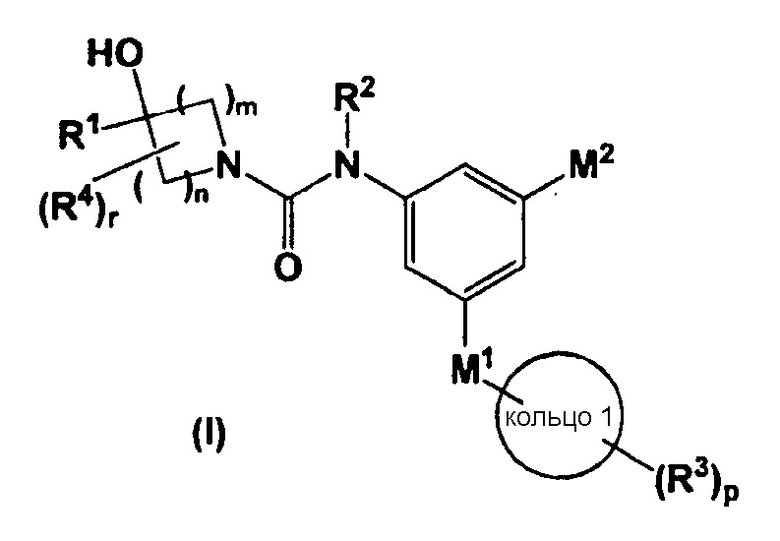 ,
,
в которой все обозначения обладают такими же значениями, как описано ниже в настоящем изобретении, и к его соли, его сольвату, его N-оксиду или его пролекарству (ниже в настоящем изобретении иногда называемому, как соединение, предлагаемое в настоящем изобретении).
УРОВЕНЬ ТЕХНИКИ
Сфингозин-1-фосфат [(2S,3R,4E)-2-амино-3-гидроксиоктадека-4-енил-1-фосфат; ниже в настоящем изобретении иногда обозначаемый как S1P] является липидом, который синтезируется с помощью метаболического обмена сфинголипидов или внеклеточного воздействия секреторных сфингозинкиназ. Предполагается, что этот липид действует как межклеточный медиатор и внутриклеточный вторичный медиатор.
Для рецепторов S1P2 (EDG-5/AGR16/H218), входящих в число рецепторов S1P, сообщают, что протекание сильной экспрессии их мРНК (матричная РНК) подтверждено в тканях сердца, легких, желудка и тонкой кишки, и что экспрессируемое количество этой мРНК в нормальных клетках интимы в модели баллонного поражения сонной артерии на мышах, которая является моделью коронарного артериосклероза, значительно уменьшено по сравнению с количеством для нормальных клеток интимы (см. Патентный документ 1).
Также сообщают, что рецепторы S1P (в частности, рецепторы S1P2) участвуют в портальной гипертензии, астме и т.п. (см. Непатентный документ 1). Также известно, что эти рецепторы участвуют в экспрессии факторов роста соединительной ткани (CTGF), связанных с началом фиброза, рака и т.п. (см. Непатентный документ 2).
Указанные ниже соединения известны, как относящиеся к области техники, к которой относится настоящее изобретение.
В качестве соединений, обладающих антагонистической активностью по отношению к S1P2, раскрыты пиразолопиридины или их фармацевтически приемлемые соли, представленные общей формулой (a)
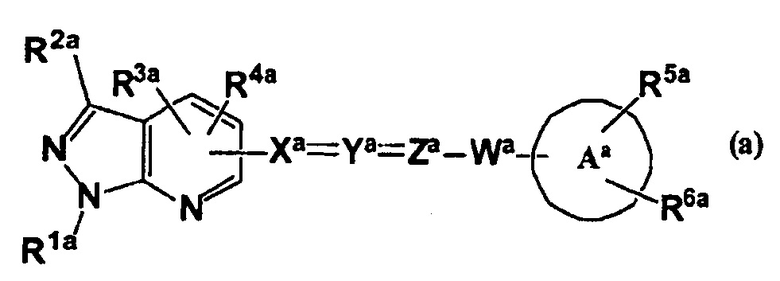 ,
,
в которой R1a, R2a и R3a означают C1-C8-алкильную группу и т.п.; R4a означает атом водорода и т.п.; R5a и R6a являются одинаковыми или разными и означают атом водорода, C1-C8-алкильную группу, C1-C6-алкоксигруппу, атом галогена и т.п.; Xa означает -NH-, -O-, -CH2- и т.п.; Ya означает -NH- и т.п.; Za означает -CO- и т.п.; Wa означает -NH- и т.п.; и кольцо Aa представляет собой арильную группу, гетероарильную группу и т.п. (определения соответствующих групп обобщены), которые специфически воздействуют на рецепторы S1P2 и применимы в качестве лекарственных средств при фиброзе (см. Патентный документ 2).
Известные соединения, обладающие антагонистической активностью по отношению к S1P2, также включают соединения, содержащие пиперидиновый каркас, представленные общей формулой (b)
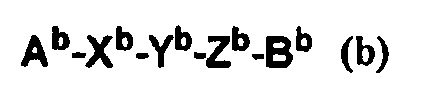 ,
,
в которой Ab означает циклическую группу, которая может содержать заместитель; Xb означает одинарную связь или мостик, содержащий в основной цепи от 1 до 3 атомов; Yb означает одинарную связь или мостик, содержащий в основной цепи от 1 до 3 атомов; Zb означает одинарную связь или мостик, содержащий в основной цепи от 1 до 3 атомов; и Bb означает циклическую группу, которая может содержать заместитель (см. Патентный документ 3), и соединения, содержащие азетидиновый каркас (см. Патентный документ 4).
В документах предшествующего уровня техники не раскрыто и не предположено, что соединение, предлагаемое в настоящем изобретении, которое содержит два особых заместителя, а именно атом галогена или галогеналкильную группу и феноксигруппу, в некоторых положениях, может значительно улучшить антагонистическую активность по отношению к S1P2 человека.
Патентный документ 1: Japanese Patent Application Laid-open No. H6-234797.
Патентный документ 2: WO 01/98301.
Патентный документ 3: WO 2004/002531.
Патентный документ 4: WO 2005/063704
Непатентный документ 1: Biochemical и Biophysical Research Communications, vol. 320, No. 3, p. 754-759, 2004.
Непатентный документ 2: Molecular Cancer Research, vol. 6, No. 10, p. 1649-1656, 2008.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Объектом настоящего изобретения является получение соединения, обладающего антагонистической активностью по отношению к S1P2 человека, которое недостаточно представлено соединениями, раскрытыми в Патентном документе 3, для улучшения растворимости соединения и получения из него медицинского продукта.
Авторы настоящего изобретения провели обширные исследования для решения указанной задачи и обнаружили соединение, обладающее улучшенной антагонистической активностью по отношению к S1P2 человека. В результате авторы настоящего изобретения неожиданно обнаружили, что соединение, обладающее особыми заместителями, в частности атомом галогена или галогеналкильной группой и феноксигруппой в некоторых положениях, обладает антагонистической активностью по отношению к S1P2 человека, значительно улучшенной по сравнению с соединением, раскрытым в Патентном документе 3, и тем самым завершили настоящее изобретение.
Таким образом, настоящее изобретение относится к:
[1] соединению, представленному общей формулой (I)
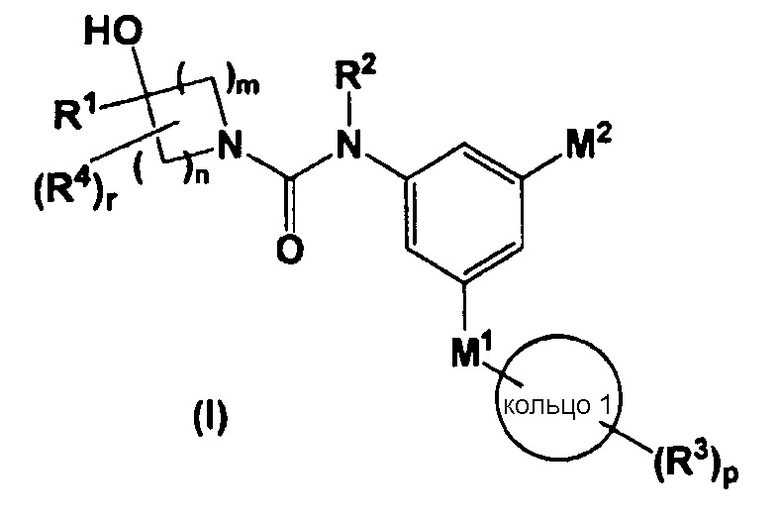 ,
,
в которой R1 означает (1) C1-C8-алкильную группу, которая может быть замещена 1-5 группами R21, (2) C2-C8-алкенильную группу, которая может быть замещена 1-5 группами R21, (3) C2-C8-алкинильную группу, которая может быть замещена 1-5 группами R21, или (4) C3-C7-карбоцикл, который может содержать от 1 до 5 заместителей, выбранных из группы, состоящей из C1-C4-алкильной группы, C1-C4-галогеналкильной группы, C1-C4-алкоксигруппы и атома галогена;
R21 означает (1) атом галогена, (2) OR22 (в этой группе R22 означает (1) атом водорода, (2) C1-C4-алкильную группу или (3) C1-C4-галогеналкильную группу), (3) -NR23R24 (в этой группе R23 и R24 соответственно и независимо означают (1) атом водорода или (2) C1-C4-алкильную группу) или (4) оксогруппу;
R2 означает (1) атом водорода, (2) C1-C4-алкильную группу или (3) C1-C4-галогеналкильную группу;
R3 означает (1) атом галогена, (2) C1-C4-алкильную группу, (3) C1-C4-галогеналкильную группу, (4) C1-C4-алкоксигруппу, (5) гидроксигруппу, (6) -L-CONR6R7, (7) -L-SO2R8 или (8) -L-COOR9;
R4 означает (1) атом галогена, (2) C1-C4-алкильную группу или (3) C1-C4-галогеналкильную группу;
L означает (1) связь, (2) группу, описываемую формулой
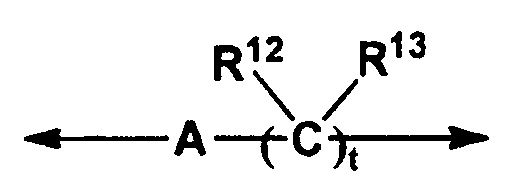 ,
,
в которой A означает (1) связь или (2) атом кислорода; R12 и R13 соответственно и независимо означают (1) атом водорода, (2) C1-C4-алкильную группу, (3) гидроксигруппу или (4) NH2 или (5) R12 и R13 вместе с атомом углерода, к которому они присоединены, могут образовать C3-C7-карбоцикл; и стрелка справа означает связь с -CONR6R7, -SO2R8 или -COOR9, (3) C2-C4-алкениленовую группу, (4) -O-C2-C4-алкениленовую группу, (5) атом кислорода или (6) атом азота, который может быть замещен C1-C4-алкильной группой;
R6 и R7 соответственно и независимо означают (1) атом водорода, (2) C1-C4-алкильную группу, (3) C1-C4-галогеналкильную группу, (4) гидроксигруппу, (5) -CONR15R16, (6) -SO2NR15R16, (7)-COR17 или (8) -SO2R17, или R6 и R7 вместе с атомом азота, к которому они присоединены, могут образовать 4- -7-членный азотсодержащий насыщенный гетероцикл, который может быть замещен гидроксигруппой;
R8 означает (1) C1-C4-алкильную группу, (2) C1-C4-галогеналкильную группу или (3) NR10R11;
R9 означает (1) атом водорода или (2) C1-C8-алкильную группу;
R10 и R11 соответственно и независимо означают (1) атом водорода, (2) C1-C4-алкильную группу, (3) -CONR15R16, (4) -SO2NR15R16, (5) -COR17 или (6) -SO2R17;
кольцо 1 представляет собой 5- - 7-членную циклическую группу;
R15 и R16 соответственно и независимо означают (1) атом водорода, (2) C1-C4-алкильную группу или (3) 5- -7-членную циклическую группу;
R17 означает (1) C1-C4-алкильную группу или (2) 5- -7-членную циклическую группу;
M1 означает (1) связь, (2) -C(O)-, (3) -O-, (4) -S-, (5) -C(O)O-, (6) -CH2O- или (7) -C(O)NH-;
M2 означает атом галогена или C1-C4-галогеналкильную группу;
n означает целое число, равное от 1 до 2;
m означает целое число, равное от 1 до 2;
p означает целое число, равное от 0 до 5;
r означает целое число, равное от 0 до 4;
t означает целое число, равное от 1 до 4;
где p равно 2 или более, множество групп R3 могут быть одинаковыми или разными;
где r равно 2 или более, множество групп R4 могут быть одинаковыми или разными; и
где t равно 2 или более, множество групп R12 и R13 соответственно могут быть одинаковыми или разными;
к его соли, его сольвату, его N-оксиду или его пролекарству;
[2] соединению, соответствующему параграфу [1], в котором R1 означает (1) C1-C8-алкильную группу, которая может быть замещена 1-5 группами R21, или (2) C3-C7-карбоцикл, который может содержать от 1 до 5 заместителей, выбранных из группы, состоящей из C1-C4-алкильной группы, C1-C4-галогеналкильной группы, C1-C4-алкоксигруппы и атома галогена;
[3] соединению, соответствующему параграфу [1] или [2], в котором M1 означает (1) -O- или (2) -C(O)O-;
[4] соединению, соответствующему параграфу [1], которое представлено общей формулой (I-1)
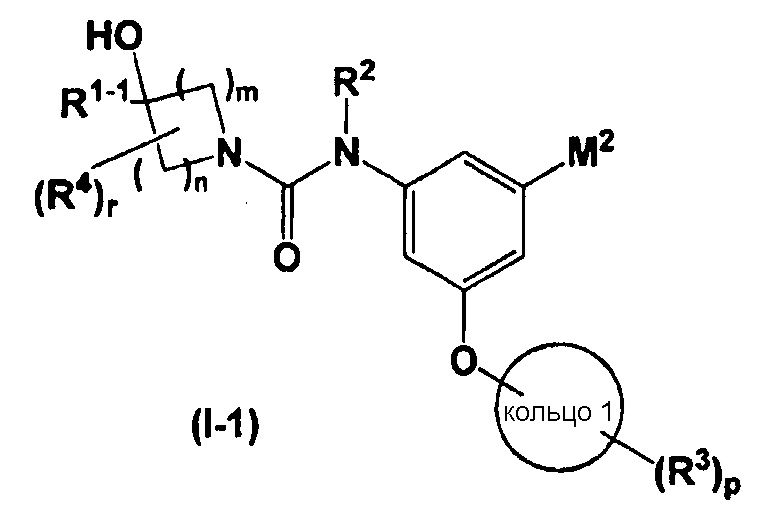 ,
,
в которой R1-1 означает (1) C1-C8-алкильную группу, которая может быть замещена 1-5 группами R21, или (2) C3-C7-карбоцикл, который может содержать от 1 до 5 заместителей, выбранных из группы, состоящей из C1-C4-алкильной группы, C1-C4-галогеналкильной группы, C1-C4-алкоксигруппы и атома галогена; и другие обозначения обладают такими же значениями, как выше;
[5] соединению, соответствующему параграфу [4], в котором R2 означает атом водорода;
[6] соединению, соответствующему параграфу [4] или [5], в котором кольцо 1 представляет собой (1) бензольное, (2) циклогексановое или (3) пиридиновое кольцо;
[7] соединению, соответствующему параграфу [4], в котором соединением, представленным общей формулой (I-1), описанной в параграфе [4], является 2-{3-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}-2-метилпропановая кислота, 4-циклопентил-4-гидрокси-N-[3-{4-[(метилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-1-пиперидинкарбоксамид, 4-циклопентил-N-[3-{4-[(этилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-4-гидрокси-1-пиперидинкарбоксамид, 1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопропанкарбоновая кислота, 2-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенокси}-2-метилпропановая кислота, 1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенокси}циклопропанкарбоновая кислота, 1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклобутанкарбоновая кислота, 1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопентанкарбоновая кислота, 3-{[(4-гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}-5-(трифторметил)бензойная кислота, 2-(4-{[3-{[(4-гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}-5-(трифторметил)бензоил]окси}фенил)-2-метилпропановая кислота, 1-{4-[3-хлор-5-({[4-(4-фторфенил)-4-гидрокси-1-пиперидинил]карбонил}амино)фенокси]фенокси}циклопропанкарбоновая кислота или 2-[4-(3-фтор-5-{[(4-гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}фенокси)фенил]-2-метилпропановая кислота;
[8] соединению, соответствующему параграфу [4], в котором соединением, представленным общей формулой (I-1), описанной в параграфе [4], является 4-циклопентил-4-гидрокси-N-[3-{4-[(метилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-1-пиперидинкарбоксамид или 1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопентанкарбоновая кислота;
[9] фармацевтической композиции, содержащей соединение, представленное общей формулой (I), его соль, его сольват, его N-оксид или его пролекарство, соответствующее параграфу [1];
[10] фармацевтической композиции, соответствующей параграфу [9], которая является антагонистом S1P2;
[11] фармацевтической композиции, соответствующей параграфу [9], которая является профилактическим и/или терапевтическим средством при заболевании, опосредованном S1P2;
[12] фармацевтической композиции, соответствующей параграфу [11], где опосредованное S1P2 заболевание представляет собой заболевание, обусловленное сужением сосудов, фиброз, респираторное заболевание, артериосклероз, окклюзионное заболевание периферической артерии, ретинопатию, глаукому, возрастную дегенерацию желтого пятна, нефрит, диабет, осложнение при диабете, дислипидемию, гепатит, цирроз печени, печеночную недостаточность, невропатию, ревматоидный артрит, рану, боль, крапивницу, системную красную волчанку (SLE) или рак;
[13] фармацевтической композиции, соответствующей параграфу [12], где заболевание, обусловленное сужением сосудов, представляет собой вазоспастическое заболевание головного мозга, вазоспастическое заболевание сердца, коронарное вазоспастическое заболевание, гипертензию, легочную гипертензию, инфаркт миокарда, стенокардию, аритмию, фибрилляцию предсердий, портальную гипертензию, варикоз, асциты, спленомегалию, печеночную энцефалопатию или ишемическое реперфузионное поражение;
[14] фармацевтической композиции, соответствующей параграфу [13], которая способна устойчиво снизить портальное давление;
[15] фармацевтической композиции, соответствующей параграфу [14], которую можно вводить один раз в сутки;
[16] фармацевтической композиции, соответствующей любому из параграфов [13] - [15], которая является профилактическим средством при первичном или вторичном кровотечении при варикозе пищевода, связанном с портальной гипертензией;
[17] способу профилактики и/или лечения опосредованного S1P2 заболевания, включающему введение млекопитающему эффективного количества соединения, представленного общей формулой (I), его соли, его сольвата, его N-оксида или его пролекарства, соответствующего параграфу [1];
[18] соединению, представленному общей формулой (I), его соли, его сольвату, его N-оксиду или его пролекарству, соответствующему параграфу [1], для профилактики и/или лечения опосредованного S1P2 заболевания; и
[19] применению соединения, представленного общей формулой (I), его соли, его сольвата, его N-оксида или его пролекарства, соответствующего параграфу [1], для приготовления профилактического и/или терапевтического средства при заболевании, опосредованном S1P2.
Соединение, предлагаемое в настоящем изобретении, обладает высокой антагонистической активностью по отношению к S1P2 человека и поэтому применимо для лечения опосредуемых с помощью S1P2 заболеваний, таких как заболевания, обусловленные сужением сосудов, и фиброз.
НАИЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение подробно описано ниже.
Атом галогена при использовании в настоящем изобретении означает фтор, хлор, бром и йод.
C1-C8-Алкильная группа при использовании в настоящем изобретении может включать линейные или разветвленные C1-C8-алкильные группы, которые могут включать, например, метильную, этильную, пропильную, бутильную, пентильную, гексильную, гептильную, октильную, изопропильную, изобутильную, втор-бутильную, трет-бутильную, 1-метилбутильную, 1-этилпропильную, 1,1-диметилпропильную, 1,2-диметилпропильную, 2-метилбутильную, 3-метилбутильную, 2,2-диметилпропильную, 1-метилпентильную, 1-этилбутильную, 2-этилбутильную, 1-этил-1-метилпропильную, 1-этил-2-метилпропильную, 1,1-диметилбутильную, 1,2-диметилбутильную, 1,3-диметилбутильную, 2-метилпентильную, 3-метилпентильную, 4-метилпентильную, 2,3-диметилбутильную, 1-метилгексильную, 1-этилпентильную, 2-этилпентильную, 1-пропилбутильную, 2-метил-3-гексильную, 1,2-диметилпентильную, 1,3-диметилпентильную, 1,4-диметилпентильную, 1-этил-1-метилбутильную, 1-метил-2-этилбутильную, 1-этил-2-метилбутильную, 1-этил-3-метилбутильную, 1,1-диметилпентильную, 1,1,3-триметилбутильную, 1,1-диэтилпропильную, 2-метилгексильную, 3-метилгексильную, 4-метилгексильную, 5-метилгексильную, 3-этилпентильную, 1-метилгептильную, 2-метилгептильную, 3-метилгептильную, 4-метилгептильную, 5-метилгептильную, 6-метилгептильную, 1-этилгексильную, 2-этилгексильную, 3-этилгексильную, 1-пропилпентильную, 2-пропилпентильную, 1,5-диметилгексильную, 1-этил-4-метилпентильную, 1-пропил-3-метилбутильную, 1,1-диметилгексильную, 1-этил-1-метилпентильную и 1,1-диэтилбутильную группы.
C1-C4-Алкильная группа при использовании в настоящем изобретении может включать линейные или разветвленные C1-C4-алкильные группы, которые могут включать, например, метильную, этильную, пропильную, бутильную, изопропильную, изобутильную, втор-бутильную и трет-бутильную группы.
C1-C4-Галогеналкильная группа при использовании в настоящем изобретении означает фторметильную группу, хлорметильную группу, бромметильную группу, йодметильную группу, дифторметильную группу, трифторметильную группу, 1-фторэтильную группу, 2-фторэтильную группу, 2-хлорэтильную группу, пентафторэтильную группу, 1-фторпропильную группу, 2-хлорпропильную группу, 3-фторпропильную группу, 3-хлорпропильную группу, 4,4,4-трифторбутильную группу и 4-бромбутильную группу.
C2-C8-Алкенильная группа при использовании в настоящем изобретении может включать линейные или разветвленные C2-C8-алкенильнные группы, которые могут включать, например, винильную, пропенильную, бутенильную, пентенильную, гексенильную, гексадиенильную, гептенильную, гептадиенильную, октенильную, октадиенильную, 2-метилпропен-1-ильную, 2-этил-1-бутен-1-ильную, 2-метилбутен-2-ильную и 2-метилпентен-2-ильную группы.
C2-C4-Алкениленовая группа при использовании в настоящем изобретении может включать этениленовую, пропениленовую и бутениленовую группы.
C2-C8-Алкинильная группа при использовании в настоящем изобретении может включать линейные или разветвленные C2-C8-алкинильные группы, которые могут включать, например, этинильную, пропинильную, бутинильную, пентинильную, гексинильную, гексадиинильную, гептинильную, гептадиинильную, октинильную, октадиинильную и 3,3-диметил-1-бутин-1-ильную группы.
C1-C4-Алкоксигруппа при использовании в настоящем изобретении может включать, например, метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу и трет-бутоксигруппу.
C3-C7-Карбоцикл при использовании в настоящем изобретении означает C3-C7-моноциклический карбоцикл или C3-C7-карбоцикл, который может быть полностью или частично насыщенным и может включать, например, циклопропановое, циклобутановое, циклопентановое, циклогексановое, циклогептановое, циклобутеновое, циклопентеновое, циклогексеновое, циклогептеновое, циклобутадиеновое, циклопентадиеновое, циклогексадиеновое, циклогептадиеновое и бензольное кольца.
C5-C7-Карбоцикл при использовании в настоящем изобретении означает C5-C7-моноциклический карбоцикл или C5-C7-карбоцикл, который может быть полностью или частично насыщенным и может включать, например, циклопентановое, циклогексановое, циклогептановое, циклопентеновое, циклогексеновое, циклогептеновое, циклопентадиеновое, циклогексадиеновое, циклогептадиеновое и бензольное кольца.
4- - 7-Членный азотсодержащий насыщенный гетероцикл при использовании в настоящем изобретении означает полностью или частично насыщенные 4- - 7-членные моноциклические гетероциклы, которые содержат от 1 до 5 гетероатомов, выбранных из группы, включающей атом кислорода, атом азота и атом серы, и обязательно содержат один или большее количество атомов азота. Например, можно отметить азетидиновое, пирролиновое, пирролидиновое, имидазолиновое, имидазолидиновое, триазолиновое, триазолидиновое, тетразолиновое, тетразолидиновое, пиразолиновое, пиразолидиновое, дигидропиридиновое, тетрагидропиридиновое, пиперидиновое, дигидропиразиновое, тетрагидропиразиновое, пиперазиновое, дигидропиримидиновое, тетрагидропиримидиновое, пергидропиримидиновое, дигидропиридазиновое, тетрагидропиридазиновое, пергидропиридазиновое, дигидроазепиновое, тетрагидроазепиновое, пергидроазепиновое, дигидродиазепиновое, тетрагидродиазепиновое, пергидродиазепиновое, дигидрооксазольное, тетрагидрооксазольное (оксазолидиновое), дигидроизооксазольное, тетрагидроизооксазольное (изооксазолидиновое), дигидротиазольное, тетрагидротиазольное (тиазолидиновое), дигидроизотиазольное, тетрагидроизотиазольное (изотиазолидиновое), дигидрофуразановое, тетрагидрофуразановое, дигидрооксадиазольное, тетрагидрооксадиазольное (оксадиазолидиновое), дигидрооксазиновое, тетрагидрооксазиновое, дигидрооксадиазиновое, тетрагидрооксадиазиновое, дигидрооксазепиновое, тетрагидрооксазепиновое, пергидрооксазепиновое, дигидрооксадиазепиновое, тетрагидрооксадиазепиновое, пергидрооксадиазепиновое, дигидротиадиазольное, тетрагидротиадиазольное (тиадиазолидиновое), дигидротиазиновое, тетрагидротиазиновое, дигидротиадиазиновое, тетрагидротиадиазиновое, дигидротиазепиновое, тетрагидротиазепиновое, пергидротиазепиновое, дигидротиадиазепиновое, тетрагидротиадиазепиновое, пергидротиадиазепиновое, морфолиновое и тиоморфолиновое кольца.
5- - 7-Членная циклическая группа при использовании в настоящем изобретении означает C5-C7-карбоцикл и 5- - 7-членный гетероцикл. C5-C7-Карбоцикл обладает таким же значением, как выше, и 5- - 7-членный гетероцикл может включать 5- - 7-членные ненасыщенные гетероциклы и 5- - 7-членные насыщенные гетероциклы. 5- - 7-Членные гетероциклы могут включать, например, пирролиновое, пирролидиновое, имидазолиновое, имидазолидиновое, триазолиновое, триазолидиновое, тетразолиновое, тетразолидиновое, пиразолиновое, пиразолидиновое, дигидропиридиновое, тетрагидропиридиновое, пиперидиновое, дигидропиразиновое, тетрагидропиразиновое, пиперазиновое, дигидропиримидиновое, тетрагидропиримидиновое, пергидропиримидиновое, дигидропиридазиновое, тетрагидропиридазиновое, пергидропиридазиновое, дигидроазепиновое, тетрагидроазепиновое, пергидроазепиновое, дигидродиазепиновое, тетрагидродиазепиновое, пергидродиазепиновое, дигидрофурановое, тетрагидрофурановое, дигидропирановое, тетрагидропирановое, дигидрооксепиновое, тетрагидрооксепиновое, пергидрооксепиновое, дигидротиофен, тетрагидротиофен, дигидротиопирановое, тетрагидротиопирановое, дигидротиепиновое, тетрагидротиепиновое, пергидротиепиновое, дигидрооксазольное, тетрагидрооксазольное (оксазолидиновое), дигидроизооксазольное, тетрагидроизооксазольное (изооксазолидиновое), дигидротиазольное, тетрагидротиазольное (тиазолидиновое), дигидроизотиазольное, тетрагидроизотиазольное (изотиазолидиновое), дигидрофуразановое, тетрагидрофуразановое, дигидрооксадиазольное, тетрагидрооксадиазольное (оксадиазолидиновое), дигидрооксазиновое, тетрагидрооксазиновое, дигидрооксадиазиновое, тетрагидрооксадиазиновое, дигидрооксазепиновое, тетрагидрооксазепиновое, пергидрооксазепиновое, дигидрооксадиазепиновое, тетрагидрооксадиазепиновое, пергидрооксадиазепиновое, дигидротиадиазольное, тетрагидротиадиазольное (тиадиазолидиновое), дигидротиазиновое, тетрагидротиазиновое, дигидротиадиазиновое, тетрагидротиадиазиновое, дигидротиазепиновое, тетрагидротиазепиновое, пергидротиазепиновое, дигидротиадиазепиновое, тетрагидротиадиазепиновое, пергидротиадиазепиновое, морфолиновое, тиоморфолиновое, оксатиановое, диоксолановое, диоксановое, дитиолановое, дитиановое, пиррольное, имидазольное, триазольное, тетразольное, пиразольное, пиридиновое, пиразиновое, пиримидиновое, пиридазиновое, азепиновое, диазепиновое, фурановое, пирановое, оксепиновое, тиофен, тиопирановое, тиепиновое, оксазольное, изооксазольное, тиазольное, изотиазольное, фуразановое, оксадиазольное, оксазиновое, оксадиазиновое, оксазепиновое, оксадиазепиновое, тиадиазольное, тиазиновое, тиадиазиновое, тиазепиновое и тиадиазепиновое кольца.
В настоящем изобретении R1 предпочтительно означает C1-C8-алкильную группу, которая может быть замещена 1-5 группами R21, или C5-C7-карбоцикл, который может содержать от 1 до 5 заместителей, выбранных из группы, включающей C1-C4-алкильную группу, C1-C4-галогеналкильную группу, C1-C4-алкоксигруппу и атом галогена, и более предпочтительно разветвленную C1-C8-алкильную группу или циклопентановое, циклогексановое или бензольное кольцо, которое содержит от 1 до 5 заместителей, выбранных из группы, включающей атом галогена и трифторметильную группу. Разветвленная C1-C8-алкильная группа предпочтительно представляет собой изопропильную, изобутильную, 2-этилбутильную, 2-метилпентильную или 3-метилпентильную группу.
В настоящем изобретении R21 предпочтительно означает атом фтора.
В настоящем изобретении R2 предпочтительно означает атом водорода.
В настоящем изобретении R3 предпочтительно означает -L-CONR6R7, -L-SO2R8 или -L-COOR9.
В настоящем изобретении M1 предпочтительно означает -O- или -C(O)O-.
В настоящем изобретении M2 предпочтительно означает атом фтора, атом хлора или C1-C4-галогеналкильную группу, более предпочтительно C1-C4-галогеналкильную группу, и C1-C4-галогеналкильная группа предпочтительно представляет собой фторметильную группу, дифторметильную группу или трифторметильную группу.
В настоящем изобретении кольцо 1 предпочтительно представляет собой бензольное, пиридазиновое, пиримидиновое, пиразиновое, пиридиновое или циклогексановое кольцо и более предпочтительно бензольное кольцо.
В настоящем изобретении соединение, представленное общей формулой (I), предпочтительно представляет собой соединение, представленное общей формулой (I-1)
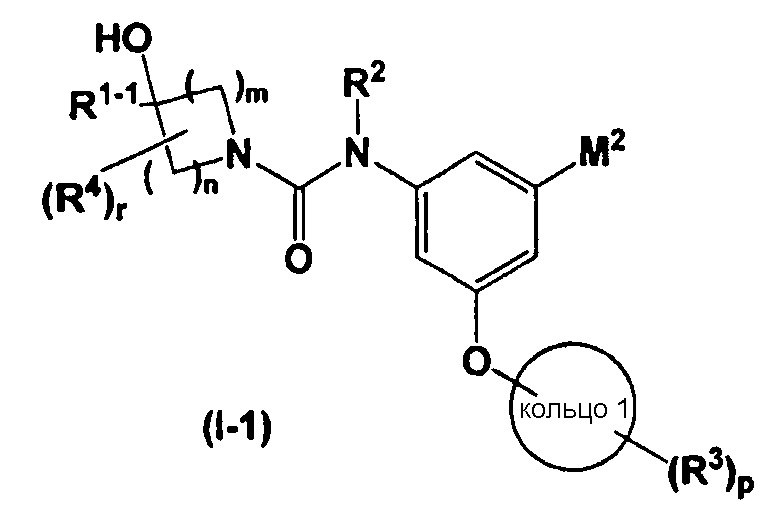 ,
,
в которой все обозначения обладают такими же значениями, как и выше. В общей формуле (I-1) R2 предпочтительно означает атом водорода; R3 предпочтительно означает -L-CONR6R7, -L-SO2R8 или -L-COOR9 и более предпочтительно -L-CONR6R7 или -L-COOR9; M2 предпочтительно означает фторметильную группу, дифторметильную группу или трифторметильную группу и более предпочтительно трифторметильную группу; кольцо 1 предпочтительно представляет собой бензольное, пиридиновое или циклогексановое кольцо и кольцо 1 более предпочтительно представляет собой бензольное кольцо.
В настоящем изобретении соединение, представленное общей формулой (I), предпочтительно представляет собой соединение, представленное общей формулой (I-1)
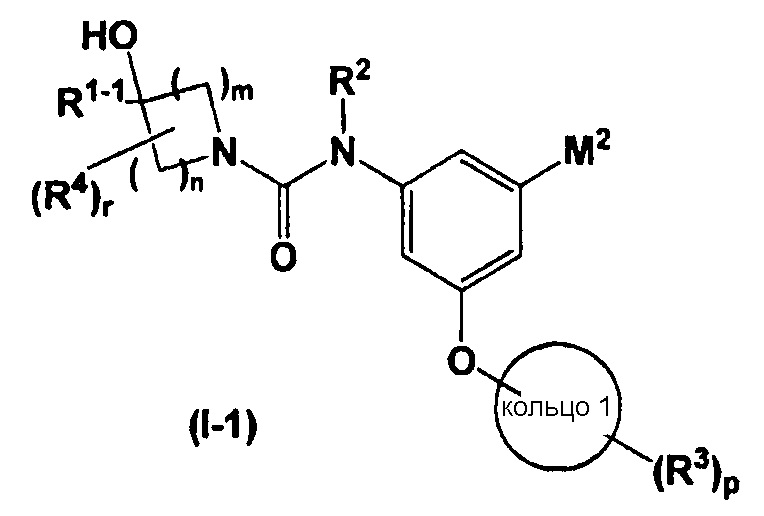 ,
,
в которой все обозначения обладают такими же значениями, как и выше. В общей формуле (I-1) R2 предпочтительно означает атом водорода; R3 предпочтительно означает -L-CONR6R7, -L-SO2R8 или -L-COOR9 и более предпочтительно -L-CONR6R7 или -L-COOR9; M2 предпочтительно означает C1-C4-галогеналкильную группу; C1-C4-галогеналкильная группа более предпочтительно представляет собой фторметильную группу, дифторметильную группу или трифторметильную группу; кольцо 1 предпочтительно представляет собой бензольное, пиридиновое или циклогексановое кольцо и более предпочтительно бензольное кольцо.
В настоящем изобретении соединения, описанные в примерах, являются более предпочтительными и 4-циклопентил-4-гидрокси-N-[3-{4-[(метилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-1-пиперидинкарбоксамид, или 1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопентанкарбоновая кислота является особенно предпочтительной.
Изомеры
В объем настоящего изобретения входят все изомеры, если специально не указано иное. Например, алкильная группа включает линейные и разветвленные группы. Кроме того, в объем настоящего изобретения входят геометрические изомеры относительно двойных связей, изомеры колец и конденсированных колец (E-формы, Z-формы, цис-формы и транс-формы), оптические изомеры, обусловленные наличием асимметрических атомов углерода (R- и S-формы, α- и β-конфигурации, энантиомеры и диастереоизомеры), оптически активные соединения, способные к оптическому вращению (D-, L-, d- и l-формы), полярные соединения, которые можно разделить с помощью хроматографии (высокополярные соединения и низкополярные соединения), равновесные соединения, поворотные изомеры, их смеси в произвольных соотношениях и рацемические смеси. В объем настоящего изобретения также входят таутомеры.
Оптические изомеры, предлагаемые в настоящем изобретении, могут включать не только обладающие чистотой, составляющей 100%, но и содержащие другие оптические изомеры при содержании, составляющем менее 50%.
В настоящем изобретении, если специально не указано иное, знак

показывает, что связь направлена вниз от плоскости бумаги (т.е. α-конфигурация), знак

показывает, что связь направлена вверх от плоскости бумаги (т.е. β-конфигурация), и знак

показывает, что связь находится в α-конфигурации, в β-конфигурации или имеется смесь этих конфигураций в произвольном соотношении, что очевидно для специалиста в данной области техники.
Соединение, представленное общей формулой (I), превращают в соль по хорошо известной методике. Соль предпочтительно является растворимой в воде. Подходящие соли могут включать соли щелочных металлов (калия, натрия и т.п.), соли щелочноземельных металлов (кальция, магния и т.п.), соли аммония, фармацевтически приемлемые соли органического амина (тетраметиламмония, триэтиламина, метиламина, диметиламина, циклопентиламина, бензиламина, фенетиламина, пиперидина, моноэтаноламина, диэтаноламина, трис(гидроксиметил)аминометана, лизина, аргинина, N-метил-D-глюкамина и т.п.), соли присоединения с кислотами (соли неорганических кислот (гидрохлориды, гидробромиды, гидройодиды, сульфаты, фосфаты, нитраты и т.п.), соли органических кислот (ацетаты, трифторацетаты, лактаты, тартраты, оксалаты, фумараты, малеаты, бензоаты, цитраты, метансульфонаты, этансульфонаты, бензолсульфонаты, толуолсульфонаты, изетионаты, глюконураты, глюконаты и т.п.) и т.п.) и т.п.
Соединение, представленное общей формулой (I), и его соль также можно превратить в сольват. Сольват предпочтительно обладает низкой токсичностью и растворим в воде. Подходящие сольваты могут включать, например, сольваты с водой и растворителями - спиртами (например, с этанолом).
N-Оксид соединения, представленного общей формулой (I), означает соединение, представленное общей формулой (I), в котором атом азота окислен. N-Оксид соединения, представленного общей формулой (I), также может представлять собой соль щелочного (щелочноземельного) металла, соль аммония, соль органического амина и соль присоединения с кислотой, описанные выше.
Пролекарство соединения, представленного общей формулой (I), означает соединение, которое in vivo превращается в соединение, представленное общей формулой (I), по реакции с ферментами, кислотой желудочного сока и т.п. Пролекарство соединения, представленного общей формулой (I), может включать, если соединение, представленное общей формулой (I), содержит гидроксигруппу, соединения, в которые гидроксигруппа ацилирована, алкилирована, фосфорилирована или превращена в борат (например, соединения, предлагаемые в настоящем изобретении, в которых гидроксигруппа превращена в ацетильную, пальмитоильную, пропаноильную, пивалоильную, сукцинильную, фумарильную, аланильную, диметиламинометилкарбонильную группу и т.п.); соединения, представленные общей формулой (I), в которых карбоксигруппа этерифицирована или амидирована (например, соединения, представленные общей формулой (I), в которых карбоксигруппа превращена в этиловый эфир, изопропиловый эфир, фениловый эфир, карбоксиметиловый эфир, диметиламинометиловый эфир, пивалоилоксиметиловый эфир, этоксикарбонилоксиэтиловый эфир, фталидиловый эфир, (5-метил-2-оксо-1,3-диоксолен-4-ил)метиловый эфир, циклогексилоксикарбонилэтиловый эфир, метиламид и т.п.) и т.п. Эти соединения можно получить по хорошо известным методикам. Пролекарством соединения, представленного общей формулой (I), могут быть гидраты или негидраты. Пролекарство соединения, представленного общей формулой (I), может представлять собой такое, которое превращается в соединение, представленное общей формулой (I), при физиологических условиях, таких как описанные в публикации "Iyakuhin no Kaihatsu", vol. 7 "Bunshi Sekkei", p. 163-198, 1990, Hirokawa Shoten Co. Соединение, представленное общей формулой (I), может быть мечено изотопом (например, 2H, 3H, 11C, 13C, 14C, 13N, 15N, 15O, 17O, 18O, 35S, 18F, 36Cl, 123I, 125I и т.п.).
Способ получения соединения, предлагаемого в настоящем изобретении.
Соединение, предлагаемое в настоящем изобретении, можно получить по хорошо известным методикам, например по методике, описанной в публикации Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition (Richard C. Larock, John Wiley & Sons Inc, 1999), или методике, описанной в примерах с соответствующими модификациями и комбинациями.
Соединение общей формулы (I), в которой R2 означает атом водорода, и M1 означает атом кислорода, а именно соединение, представленное общей формулой (I-A)
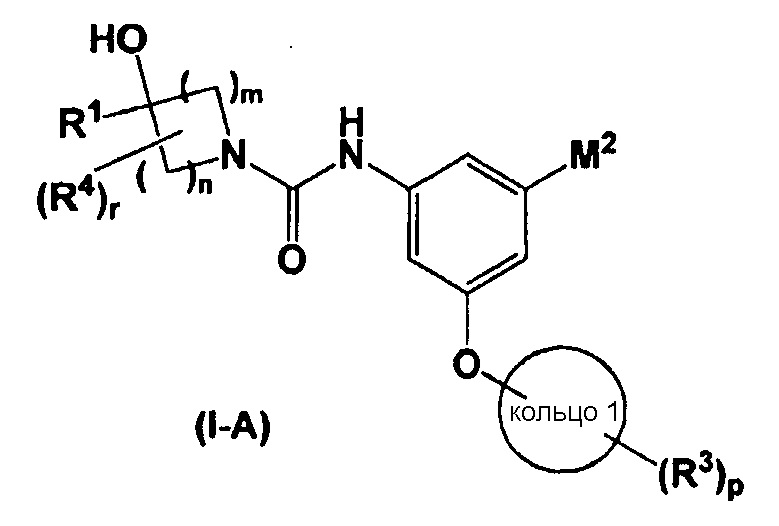 ,
,
в которой все обозначения обладают такими же значениями, как и выше, можно получить по приведенной ниже схеме реакций 1
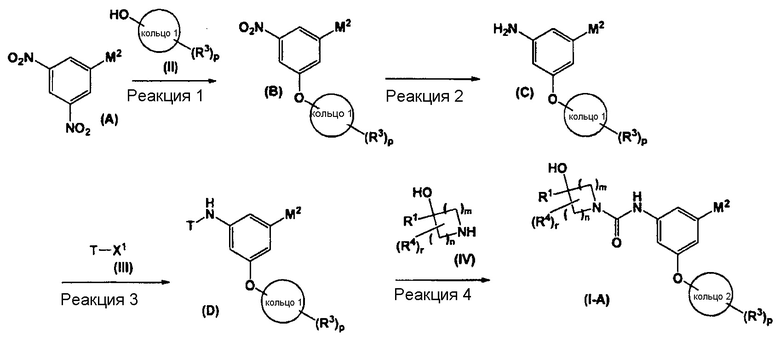


 ,
,
в которой T означает защитную группу аминогруппы, содержащую карбонильную группу (например, 2,2,2-трихлорэтоксикарбонильную (Troc) группу, феноксикарбонильную группу, п-нитрофеноксикарбонильную группу и т.п.); X1 означает атом галогена; и другие обозначения обладают такими же значениями, как выше.
На схеме реакций 1 реакцию 1 можно провести в виде реакции образования простого эфира между соединением, представленным общей формулой (A), и соединением, представленным общей формулой (II). Эта реакция образования простого эфира хорошо известна и ее проводят, например, в органическом растворителе (N,N-диметилацетамид, N,N-диметилформамид, диметилсульфоксид, хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран, метил-трет-бутиловый эфир и т.п.) в присутствии гидроксида щелочного металла (гидроксид натрия, гидроксид калия, гидроксид лития и т.п.), гидрида щелочного металла (гидрид натрия и т.п.), гидроксида щелочноземельного металла (гидроксид бария, гидроксид кальция и т.п.), фосфата (фосфат калия и т.п.) или карбоната щелочного металла (карбонат цезия, карбонат натрия, карбонат калия и т.п.) или его водного раствора или их смеси и при температуре, равной от 0 до 100°C.
На схеме реакций 1 реакцию 2 можно провести в виде реакции восстановления нитрогруппы соединения, представленного общей формулой (B). Реакция восстановления нитрогруппы хорошо известна и ее проводят, например, по методикам, описанным ниже в настоящем изобретении.
(1) Реакцию проводят, например, в растворителе [простые эфиры (тетрагидрофуран, диоксан, диметоксиэтан, диэтиловый эфир и т.п.), спирты (метанол, этанол и т.п.), бензолы (бензол, толуол и т.п.), кетоны (ацетон, метилэтилкетон и т.п.), нитрилы (ацетонитрил и т.п.), амиды (диметилформамид и т.п.), вода, этилацетат, уксусная кислота или смешанные растворители, содержащие два или большее количество из указанных выше] в присутствии катализатора гидрирования (палладий на угле, палладиевая чернь, палладий, гидроксид палладия, диоксид платины, платина на угле, никель, никель Ренея, хлорид рутения и т.п.) в присутствии или при отсутствии кислоты (хлористоводородная кислота, серная кислота, гипохлористая кислота, борная кислота, тетрафторборная кислота, уксусная кислота, п-толуолсульфоновая кислота, щавелевая кислота, трифторуксусная кислота, муравьиная кислота и т.п.), в атмосфере водорода при нормальном или повышенном давлении, в присутствии формиата аммония или гидразина и при температуре, равной от 0 до 200°C.
(2) Реакцию проводят, например, в смешивающемся с водой растворителе (этанол, метанол, тетрагидрофуран и т.п.) в присутствии или при отсутствии кислоты (хлористоводородная кислота, бромистоводородная кислота, хлорид аммония, уксусная кислота, формиат аммония и т.п.), с использованием реагента, содержащего металл (цинк, железо, олово, хлорид олова, хлорид железа, самарий, индий, борогидрид натрия-хлорид никеля и т.п.) при температуре, равной от 0 до 150°C.
На схеме реакций 1 реакция 3 хорошо известна и ее проводят с соединением, представленным общей формулой (C), и соединением, представленным общей формулой (III), например, по реакции соединения, представленного общей формулой (III), в присутствии основания (пиридин, триэтиламин, диметиланилин, диметиламинопиридин, диизопропилэтиламин и т.п.) с соединением, представленным общей формулой (C), в органическом растворителе (хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран и т.п.) при температуре, равной от 0 до 40°C. Соединение, представленное общей формулой (III), также можно ввести в реакцию с соединением, представленным общей формулой (C), в органическом растворителе (этилацетат, диоксан, тетрагидрофуран и т.п.) с использованием водного раствора щелочи (раствор гидрокарбоната натрия, раствор гидроксида натрия и т.п.) при температуре, равной от 0 до 40°C.
На схеме реакций 1 реакция 4 хорошо известна и ее проводят с соединением, представленным общей формулой (D), и соединением, представленным общей формулой (IV), например, по реакции соединения, представленного общей формулой (D), в присутствии основания (пиридин, триэтиламин, диметиланилин, диметиламинопиридин, диизопропилэтиламин и т.п.) с соединением, представленным общей формулой (IV), в органическом растворителе (N,N-диметилацетамид, хлороформ, дихлорметан, диэтиловый эфир, тетрагидрофуран и т.п.) при температуре, равной от 0°C до температуры кипения.
На схеме реакций 1, если соединение, представленное общей формулой, содержит защитную группу, например, если R3 содержит защитную группу, то при необходимости можно провести реакцию удаления защитной группы. Реакция удаления защитных групп хорошо известна и ее можно провести по указанным ниже методикам, которые могут включать, например, (1) реакцию удаления защитной группы с помощью щелочного гидролиза, (2) реакцию удаления защитной группы в кислой среде, (3) реакцию удаления защитной группы с помощью гидролиза, (4) реакцию удаления силильных защитных групп, (5) реакцию удаления защитной группы с использованием металла, (6) реакцию удаления защитной группы с использованием комплекса металла и т.п.
Эти методики специально описаны ниже в настоящем изобретении.
(1) Реакцию удаления защитной группы с помощью щелочного гидролиза проводят, например, в органическом растворителе (например, метанол, тетрагидрофуран и диоксан), с использованием гидроксида щелочного металла (например, гидроксид натрия, гидроксид калия и гидроксид лития), гидроксида щелочноземельного металла (например, гидроксид бария и гидроксид кальция) или карбоната (например, карбонат натрия и карбонат калия) или его водного раствора, или их смеси при температуре, равной от 0 до 40°C.
(2) Реакцию удаления защитной группы в кислой среде проводят, например, в органическом растворителе (например, дихлорметан, хлороформ, диоксан, этилацетат, метанол, изопропиловый спирт, тетрагидрофуран и анизол) и в органической кислоте (например, уксусная кислота, трифторуксусная кислота, метансульфоновая кислота и п-толуолсульфоновая кислота) или в неорганической кислоте (например, хлористоводородная кислота и серная кислота), или их смеси (например, бромид водорода/уксусная кислота) в присутствии или при отсутствии 2,2,2-трифторэтанола при температуре, равной от 0 до 100°C.
(3) Реакцию удаления защитной группы с помощью гидролиза проводят, например, в растворителе (например, простые эфиры (например, тетрагидрофуран, диоксан, диметоксиэтан и диэтиловый эфир), спирты (например, метанол и этанол), бензолы (например, бензол и толуол), кетоны (например, ацетон и метилэтилкетон), нитрилы (например, ацетонитрил), амиды (например, N,N-диметилформамид), вода, этилацетат, уксусная кислота или смешанные растворители, содержащие два или большее количество из указанных выше), в присутствии катализатора (например, палладий на угле, палладиевая чернь, гидроксид палладия на угле, оксид платины и никель Ренея), в атмосфере водорода при нормальном или повышенном давлении или в присутствии формиата аммония при температуре, равной от 0 до 200°C.
(4) Реакцию удаления силильных защитных групп проводят, например, в смешивающемся с водой органическом растворителе (например, тетрагидрофуран и ацетонитрил), с использованием тетрабутиламмонийфторида при температуре, равной от 0 до 40°C. Альтернативно, реакцию проводят, например, в органической кислоте (например, уксусная кислота, трифторуксусная кислота, метансульфоновая кислота и п-толуолсульфоновая кислота) или в неорганической кислоте (например, хлористоводородная кислота и серная кислота) или их смеси (например, бромид водорода/уксусная кислота) при температуре, равной от -10 до 100°C.
(5) Реакцию удаления защитной группы с использованием металла проводят, например, в кислом растворителе (например, уксусная кислота, буфер со значением pH, равным от 4,2 до 7,2, или в их смешанном растворе с органическим растворителем, таким как тетрагидрофуран) в присутствии порошкообразного цинка с обработкой ультразвуком, при необходимости при температуре, равной от 0 до 40°C.
(6) Реакцию удаления защитной группы с использованием комплекса металла проводят, например, в органическом растворителе (например, дихлорметан, N,N-диметилформамид, тетрагидрофуран, этилацетат, ацетонитрил, диоксан и этанол), вода или смешанный растворитель в присутствии улавливающего реагента (например, гидрид трибутилолова, триэтилсилан, димедон, морфолин, диэтиламин и пирролидин), в присутствии органической кислоты (например, уксусная кислота, муравьиная кислота и 2-этилгексановая кислота) и/или соли органической кислоты (например, 2-этилгексаноат натрия и 2-этилгексаноат калия), в присутствии или при отсутствии содержащего фосфин реагента (например, трифенилфосфин), с использованием комплекса металла (например, тетракистрифенилфосфинпалладия(0), дихлорид бис(трифенилфосфин)палладия(II), ацетат палладия(II) и хлорид трис(трифенилфосфин)родия(I)) при температуре, равной от 0 до 40°C.
Альтернативно, реакцию удаления защитной группы можно провести по методике, описанной, например, в публикации T. W. Greene, Protective Groups in Organic Synthesis, Wiley, New York, 1999.
Защитная группа гидроксигруппы может включать, например, метильную группу, тритильную группу, метоксиметильную (MOM) группу, 1-этоксиэтильную (EE) группу, метоксиэтоксиметильную (MEM) группу, 2-тетрагидропиранильную (THP) группу, триметилсилильную (TMS) группу, триэтилсилильную (TES) группу, трет-бутилдиметилсилильную (TBDMS) группу, трет-бутилдифенилсилильную (TBDPS) группу, ацетильную (Ac) группу, пивалоильную группу, бензоильную группу, бензильную (Bn) группу, п-метоксибензильную группу, аллилоксикарбонильную (Alloc) группу, 2,2,2-трихлорэтоксикарбонильную (Troc) группу и т.п.
Защитная группа аминогруппы может включать, например, бензилоксикарбонильную группу, трет-бутоксикарбонильную группу, аллилоксикарбонильную (Alloc) группу, 1-метил-1-(4-бифенил)этоксикарбонильную (Bpoc) группу, трифторацетильную группу, 9-флуоренилметоксикарбонильную группу, бензильную (Bn) группу, п-метоксибензильную группу, бензилоксиметильную (BOM) группу, 2-(триметилсилил)этоксиметильную (SEM) группу и т.п.
Защитная группа гидроксигруппы и аминогруппы специально не ограничивается указанными выше при условии, что ее можно легко и селективно удалить. Например, можно использовать описанные в публикации T. W. Greene, Protective Groups in Organic Synthesis, Wiley, New York, 1999.
В реакциях, описанных в настоящем изобретении, соединения, использующиеся в качестве исходных веществ, такие как соединения, представленные общими формулами (A), (II), (III) и (IV), хорошо известны или их можно легко получить по хорошо известным методикам.
В реакциях, описанных в настоящем изобретении, реакции можно провести путем нагревания, что очевидно для специалиста в данной области техники, на водяной бане, масляной бане, песчаной бане или путем нагревания микроволновым излучением.
В реакциях, описанных в настоящем изобретении, можно использовать иммобилизованный на твердой фазе реагент, который иммобилизован на высокомолекулярном полимере (например, полистироле, полиакриламиде, полипропилене и полиэтиленгликоле).
В реакциях, описанных в настоящем изобретении, продукты реакции можно очистить по обычным методикам очистки, таким как перегонка при нормальном или пониженном давлении, высокоэффективная жидкостная хроматография с использованием силикагеля или силиката магния, тонкослойная хроматография, с использованием ионообменных смол, поглощающих смол, или колоночная хроматография или промывка и перекристаллизация. Очистку можно провести после каждой реакции или после некоторых реакций.
Токсичность
Соединение, предлагаемое в настоящем изобретении, обладает достаточно низкой токсичностью и поэтому его можно безопасно использовать в качестве лекарственного средства.
Применение в фармацевтике
Соединение, предлагаемое в настоящем изобретении, обладает антагонистической активностью по отношению к S1P2 (EDG-5) и, таким образом, применимо в качестве профилактического и/или терапевтического средства при опосредованном S1P2 заболевании. Опосредованное S1P2 заболевание может включать заболевание, обусловленное сужением сосудов, фиброз, респираторное заболевание, артериосклероз, окклюзионное заболевание периферической артерии, ретинопатию, глаукому, возрастную дегенерацию желтого пятна, нефрит, диабет, осложнение при диабете (включая диабетическую ретинопатию, диабетическую нефропатию и т.п.), дислипидемию, гепатит, цирроз печени, печеночную недостаточность (включая неалкогольный стеатогепатит, алкогольный стеатогепатит, вирусный гепатит и т.п.), невропатия, ревматоидный артрит, рану, боль, крапивницу, системную красную волчанку (SLE), рак и т.п.
В настоящем изобретении заболевание, обусловленное сужением сосудов, может включать вазоспастическое заболевание головного мозга, вазоспастическое заболевание сердца, коронарное вазоспастическое заболевание, гипертензию, легочную гипертензию, инфаркт миокарда, стенокардию, аритмию, фибрилляцию предсердий, портальную гипертензию, варикоз, асциты, спленомегалию, печеночную энцефалопатию, ишемическое реперфузионное поражение и т.п.
При использовании в настоящем изобретении фиброз может включать фиброз легких, фиброз печени, фиброз почек, фиброз миокарда, фиброз кожи и т.п.
При использовании в настоящем изобретении респираторное заболевание может включать бронхиальную астму, острое поражение легких, сепсис, хроническое обструктивное заболевание легких и т.п.
В настоящем изобретении варикоз может включать варикоз пищевода, варикоз желудка, варикоз двенадцатиперстной кишки, варикоз кишечника, варикоз толстой кишки, варикоз прямой кишки и т.п.
Соединение, предлагаемое в настоящем изобретении, способно снизить портальное давление и поэтому его можно использовать в качестве профилактического и/или терапевтического средства для портальной гипертензии и в качестве профилактического средства при первичном или вторичном кровотечении при варикозе пищевода, связанном с портальной гипертензией.
Соединение, предлагаемое в настоящем изобретении, способно устойчиво снизить портальное давление и тем самым может оказать профилактическое и/или терапевтическое воздействие при портальной гипертензии при введении один раз в сутки.
Соединение, предлагаемое в настоящем изобретении, можно объединять с другим лекарственным препаратом и, таким образом, вводить в качестве дополнительного лекарственного препарата, чтобы:
1) дополнить и/или усилить профилактическое и/или терапевтическое воздействие соединения, предлагаемого в настоящем изобретении;
2) улучшить кинетику и усвоение и снизить дозу соединения, предлагаемого в настоящем изобретении; и/или
3) уменьшить побочный эффект соединения, предлагаемого в настоящем изобретении.
Дополнительный лекарственный препарат - соединение, предлагаемое в настоящем изобретении, и другой лекарственный препарат можно вводить в виде объединенного средства, содержащего оба компонента в одном составе, или вводить по отдельности. Это раздельное введение включает одновременное введение и последовательное введение. Последовательное введение может включать введение соединения, предлагаемого в настоящем изобретении, до другого лекарственного препарата и введение другого лекарственного препарата до введения соединения, предлагаемого в настоящем изобретении. Методики введения компонентов могут быть одинаковыми или разными.
Дополнительный лекарственный препарат может оказывать профилактическое и/или терапевтическое воздействие при любых заболеваниях без наложения ограничений, если дополняется и/или усиливается профилактическое и/или терапевтическое воздействие соединения, предлагаемого в настоящем изобретении.
Другой лекарственный препарат, который используют для дополнения и/или усиления профилактического и/или терапевтического воздействия соединения, предлагаемого в настоящем изобретении, на заболевание, обусловленное сужением сосудов, может включать, например, антагонисты кальция, тромболитические средства, ингибиторы тромбоксансинтазы, антагонисты эндотелина, антиоксиданты, акцепторы радикалов, ингибиторы PARP, средства, улучшающие функцию астроцитов, ингибиторы киназы Rho, антагонисты ангиотензина II, ингибиторы ангиотензинконвертирующего фермента, диуретические средства, ингибиторы фосфодиэстеразы (PDE) 4, простагландины (ниже в настоящем изобретении иногда обозначаемые, как PG или PGs), антагонисты альдостерона, антагонисты эндотелина, препараты простациклина, нитраты, β-блокаторы, сосудорасширяющие средства и т.п.
Другой лекарственный препарат, который используют для дополнения и/или усиления профилактического и/или терапевтического воздействия соединения, предлагаемого в настоящем изобретении, в случае фиброза может включать, например, стероиды, иммуносупрессанты, ингибиторы TGF-β, ингибиторы PDE5 и т.п.
Другой лекарственный препарат, который используют для дополнения и/или усиления профилактического и/или терапевтического воздействия соединения, предлагаемого в настоящем изобретении, на респираторное заболевание может включать, например, ингибиторы PDE4, стероиды, β-агонисты, антагонисты лейкотриенового рецептора, ингибиторы тромбоксансинтазы, антагонисты тромбоксанового A2 рецептора, средства, подавляющие высвобождение медиаторов, антигистамины, производные ксантина, антихолинергические средства, ингибиторы цитокина, PGs, препараты форсколина, ингибиторы эластазы, ингибиторы металлопротеазы, отхаркивающие средства, антибиотики и т.п.
Антагонисты кальция могут включать, например, нифедипин, бенидипингидрохлорид, дилтиаземгидрохлорид, верапамилгидрохлорид, нисолдипин, нитрендипин, бепридилгидрохлорид, амлодипинбезилат, ломеризингидрохлорид, эфонидипингидрохлорид и т.п. Тромболитические средства могут включать, например, алтеплазу, урокиназу, тизокиназу, назаруплазу, натеплазу, тканевый активатор плазминогена, памитеплазу, монтеплазу и т.п. Ингибиторы тромбоксансинтазы могут включать, например, озагрелгидрохлорид, имитродаст-натрий и т.п. Акцепторы радикалов могут включать, например, радикут и т.п. Ингибиторы PARP могут включать, например, 3-аминобензамид, 1,3,7-триметилксантин, PD-141076, PD-141703 и т.п.
Средства, улучшающие функцию астроцитов, могут включать, например, ONO-2506 и т.п.
Ингибиторы киназы Rho могут включать, например, фазудилгидрохлорид и т.п.
Антагонисты ангиотензина II могут включать, например, лосартан, кандесартан, валсартан, ирбесартан, олмесартан, телмисартан и т.п.
Ингибиторы ангиотензинконвертирующего фермента могут включать, например, алацеприл, имидаприлгидрохлорид, хинаприлгидрохлорид, темокаприлгидрохлорид, делаприлгидрохлорид, беназеприлгидрохлорид, каптоприл, трандолаприл, периндоприл эрбумин, эналаприлмалеат, лизиноприл и т.п.
Диуретические средства могут включать, например, маннит, фуросемид, ацетазоламид, дихлорфенамид, метазоламид, трихлорметиазид, мефрузид, спиронолактон, аминофиллин и т.п.
Ингибиторы PDE4 могут включать, например, ролипрам, циломиласт, Bay19-8004, NIK-616, рофлумиласт, ципамфиллин, атизорам, SCH-351591, YM-976, V-11294A, PD-168787, ONO-6126, D-4396, IC-485 и т.п.
Простагландины (PGs) могут включать, например, агонисты рецептора PG, антагонисты рецептора PG и т.п.
Рецептор PG может включать, например, рецепторы PGE (EP1, EP2, EP3 и EP4), рецепторы PGD (DP и CRTH2), рецептор PGF (FP), рецептор PGI (IP), тромбоксановый рецептор (TP) и т.п.
Антагонисты альдостерона могут включать, например, дроспиренон, метирапон, канреноат-калий, канренон, эплеренон, ZK-91587 и т.п.
Препараты простациклина могут включать, например, трепростинил-натрий, эпопростенол-натрий, берапрост-натрий и т.п.
Нитраты могут включать, например, амилнитрит, нитроглицерин, изосорбиддинитрат и т.п.
β-Блокаторы могут включать, например, алпренололгидрохлорид, бупранололгидрохлорид, буфетололгидрохлорид, окспренололгидрохлорид, атенолол, бисопрололфумарат, бетаксололгидрохлорид, бевантололгидрохлорид, метопрололтартрат, ацебутололгидрохлорид, целипрололгидрохлорид, нипрадилол, тилизололгидрохлорид, надорол, пропранололгидрохлорид, инденололгидрохлорид, картеололгидрохлорид, пиндолол, бунитрололгидрохлорид, ландиололгидрохлорид, эсмололгидрохлорид, аротинололгидрохлорид, карведилол, тимололмалеат и т.п.
Сосудорасширяющие средства могут включать, например, дилтиаземгидрохлорид, триметазидингидрохлорид, дипиридамол, этанофенгидрохлорид, диазепгидрохлорид, трапидил, никорандил и т.п.
Стероиды могут включать, в качестве средств для перорального введения или инъекции, например, кортизонацетат, гидрокортизон, гидрокортизон фосфат натрия, гидрокортизон-натрийсукцинат, флудрокортизонацетат, преднизолон, преднизолонацетат, преднизолон-натрийсукцинат, преднизолонбутилацетат, преднизолон-фосфат натрия, галопредонацетат, метилпреднизолон, метилпреднизолонацетат, метилпреднизолон-натрийсукцинат, триамцинолон, триамцинолондиацетат, триамцинолонацетонид, дексаметазон, дексаметазонацетат, дексаметазон-фосфат натрия, дексаметазонпальмитат, параметазонацетат, бетаметазон и т.п. Стероиды для ингаляции могут включать, например, беклометазонпропионат, флутиказонпропионат, будезонид, флунизолид, триамцинолон, ST-126P, циклезонид, дексаметазонпаломитионат, мометазонфуронат, прастеронсульфонат, дефлазакорт, метилпреднизолонслептанат, метилпреднизолон-натрийсукцинат и т.п.
Иммуносупрессанты могут включать, например, азатиоприн, мизорибин, метотрексат, микофенолят мофетил, циклофосфамид, циклоспорин A, такролимус, сиролимус, эверолимус, преднизолон, метилпреднизолон, ортоклон OKT3, антилимфоцитарный глобулин человека, дезоксиспергуалин и т.п.
Ингибиторы PDE5 могут включать, например, силденафил, тадалафил, варденафил, уденафил и т.п.
β-Агонисты могут включать, например, фенотеролгидробромид, салбутамолсульфат, тербуталинсульфат, формотеролфумарат, салметеролксинафоат, изопротеренолсульфат, орципреналинсульфат, клорпреналинсульфат, эпинефрин, триметохинолгидрохлорид, гексопреналин сульфат, прокатеролгидрохлорид, тулобутеролгидрохлорид, тулобутерол, пирбутеролгидрохлорид, кленбутеролгидрохлорид, мабутеролгидрохлорид, ритодрингидрохлорид, бамбутерол, допексамингидрохлорид, мелуадринтартрат, AR-C68397, левосалбутамол, R,R-формотерол, KUR-1246, KUL-7211, AR-C89855, S-1319 и т.п.
Антагонисты лейкотриенового рецептора могут включать, например, пранлукаст гидрат, монтелукаст, зафирлукаст, сератродаст и т.п.
Антагонисты тромбоксанового A2 рецептора могут включать, например, сератродаст, раматробан, домитробан-кальций гидрат и т.п.
Средства, подавляющие высвобождение медиаторов, могут включать, например, траниласт, кромолин-натрий, амлексанокс, репиринаст, ибудиласт, тазаноласт, пемироласт-калий и т.п.
Антигистамины могут включать, например, кетотифенфумарат, меквитазин, азеластингидрохлорид, оксатомид, терфенадин, эмедастинфумарат, эпинастингидрохлорид, астемизол, эбастин, цетиризингидрохлорид, бепотастин, фексофенадин, лоратадин, дезлоратадин, олопатадингидрохлорид, TAK-427, ZCR-2060, NIP-530, мометазон фуроат, мизоластин, BP-294, андоласт, ауранофин, акривастин и т.п.
Производные ксантина могут включать, например, аминофиллин, теофиллин, доксофиллин, ципамфиллин, дипрофиллин и т.п.
Антихолинергические средства могут включать, например, ипратропийбромид, окситропийбромид, флутропийбромид, циметропийбромид, темиверин, тиотропийбромид, реватропат и т.п.
Ингибиторы цитокина могут включать, например, суплатасттозилат и т.п.
Ингибиторы эластазы могут включать, например, ONO-5046, ONO-6818, MR-889, PBI-1101, ЭПИ-HNE-4, R-665 и т.п.
Отхаркивающие средства могут включать, например, нашатырно-анисовые капли, гидрокарбонат натрия, бромгексингидрохлорид, карбоцистеин, амброксолгидрохлорид, препарат амброксолгидрохлорида пролонгированного действия, метилцистеингидрохлорид, ацетилцистеин, L-этилцистеингидрохлорид, тилоксапол и т.п.
Антибиотики могут включать, например, цефуроксим-натрий, меропенемтригидрат, нетилмицинсульфат, сизомицинсульфат, цефтибутен, PA-1806, IB-367, тобрамицин, PA-1420, доксорубицин, астромицинсульфат, цефетаметпивоксилгидрохлорид и т.п. Антибиотики для ингаляции могут включать, например, PA-1806, IB-367, тобрамицин, PA-1420, доксорубицин, астромицинсульфат, цефетамет, пивоксилгидрохлорид и т.п.
Лекарственные препараты, которые объединяют с соединением, предлагаемым в настоящем изобретении, включают не только известные соединения, но и соединения, которые будут обнаружены в будущем.
Соединение, предлагаемое в настоящем изобретении, обычно вводят системно или местно в пероральной или парентеральной форме. Пероральные составы могут включать, например, жидкости для перорального введения (например, эликсиры, сиропы, фармацевтически приемлемые растворы, суспензии и эмульсии), твердые средства для перорального введения (например, таблетки (включая сублингвальные таблетки и распадающиеся во рту таблетки)), пилюли, капсулы (включая твердые капсулы, мягкие капсулы, желатиновые капсулы и микрокапсулы), порошки, гранулы и пастилки) и т.п. Парентеральные составы могут включать, например, жидкости (например, составы для инъекций (подкожных инъекций, внутривенных инъекций, внутримышечных инъекций, внутрибрюшинных инъекций, вливаний и т.п.), офтальмологические растворы (например, водные офтальмологические растворы (водные офтальмологические растворы, водные офтальмологические суспензии, вязкие офтальмологические растворы и солюбилизированные офтальмологические растворы)), неводные офтальмологические растворы (неводные офтальмологические растворы, неводные офтальмологические суспензии и т.п.)) и т.п.), составы для местного применения (например, мази (офтальмологические мази и т.п.)), глазные капли и т.п. Эти составы могут представлять собой препараты регулируемого высвобождения, такие как препараты немедленного высвобождения или препараты пролонгированного высвобождения. Эти составы можно получить по хорошо известным методикам, таким как методики, описанные в Фармакопее Японии, и т.п.
Жидкости для перорального введения получают, например, путем растворения, суспендирования или эмульгирования активного ингредиента в разбавителе, который обычно используют (например, очищенная вода, этанол и их смесь). Жидкости дополнительно могут содержать смачивающий агент, суспендирующий агент, эмульгирующий агент, подсластитель, вкусовой агент, отдушку, консервант, буферный реагент и т.п.
Твердые вещества для перорального введения готовят по обычным методикам, например, путем смешивания активного ингредиента с разбавителем (например, лактоза, маннит, глюкоза, микрокристаллическая целлюлоза и крахмал), связующим (например, гидроксипропилцеллюлоза, поливинилпирролидон и алюмометасиликат магния), разрыхлителем (например, кальциевая соль карбоксиметилцеллюлозы), смазывающим веществом (например, стеарат магния), стабилизатором, вспомогательным веществом для растворов (глутаминовая кислота, аспарагиновая кислота и т.п.) и т.п. На твердые вещества при желании можно нанести покрытие из агента, образующего покрытие (например, сахароза, желатин, гидроксипропилцеллюлоза и фталат гидроксипропилметилцеллюлозы) и можно нанести два или большее количество слоев покрытия.
Составы для местного применения в виде парентеральных составов получают по хорошо известным методикам или в виде обычных составов. Например, мази получают путем растирания или сплавления активного ингредиента с основанием. Основы для мази выбирают из числа хорошо известных или обычно использующихся. Одну или большее количество из них выбирают из числа указанных ниже, например, их можно использовать по отдельности или в комбинации: высшая жирная кислота или эфир высшей жирной кислоты (например, адипиновая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота, адипат, миристат, пальмитат, стеарат и олеат), воск (например, пчелиный воск, воск жировых тканей кита и церезин), поверхностно-активное вещество (например, фосфаты полиоксиэтиленалкилового эфира), высший спирт (например, цетанол, стеариловый спирт и цетостеариловый спирт), силиконовое масло (например, диметилполисилоксан), углеводород (например, гидрофильное вазелиновое масло, белое вазелиновое масло, очищенный ланолин и жидкий парафин), гликоль (например, этиленгликоль, диэтиленгликоль, пропиленгликоль, полиэтиленгликоль и макрогол), растительное масло (например, касторовое масло, оливковое масло, кунжутное масло и терпентинное масло), животный жир (например, норковый жир, масло яичного желтка, сквалан и сквален), вода, средство, улучшающее впитывание, и средство, предупреждающее образование сыпи. Составы также могут включать влагоудерживающее средство, консервант, стабилизатор, антиоксидант, средство, придающее запах, и т.п.
Составы для инъекций в виде парентеральных составов включают растворы, суспензии, эмульсии и твердые составы для инъекций, которые перед использованием растворяют или суспендируют в растворителе. Составы для инъекций используют, например, путем растворения, суспендирования или эмульгирования активного ингредиента в растворителе. Использующимся растворителем является, например, дистиллированная вода для инъекций, физиологический раствор, растительное масло, пропиленгликоль, полиэтиленгликоль, спирты, такие как этанол, или их комбинации. Составы для инъекций также могут содержать стабилизатор, вспомогательное вещество для раствора (например, глутаминовая кислота, аспарагиновая кислота и Polysolvate 80®), суспендирующий агент, эмульгирующий агент, успокаивающий агент, буферный реагент, консервант и т.п. Составы для инъекций готовят с использованием стерилизации на конечной стадии или в асептических условиях. Альтернативно, можно приготовить асептические твердые составы, например, высушенные вымораживанием составы, которые перед использованием можно растворить в стерилизованной или асептической дистиллированной воде для инъекций или в другом растворителе.
Для описанных выше целей соединение, предлагаемое в настоящем изобретении, или дополнительный лекарственный препарат - соединение, предлагаемое в настоящем изобретении, и другой лекарственный препарат обычно вводят системно или местно в пероральной или парентеральной форме. Доза может меняться в зависимости от возраста, массы тела, симптомов, терапевтического эффекта, пути введения, длительности лечения и т.п., и ее обычно можно вводить перорально в виде разовой дозы для взрослого, составляющей от 1 нг до 1000 мг, один или несколько раз в сутки, или вводить парентерально в виде разовой дозы для взрослого, составляющей от 0,1 нг до 10 мг один или несколько раз в сутки, или непрерывно вводить внутривенно в течение от 1 ч до 24 ч ежедневно. Разумеется, доза может меняться, как указано выше, в зависимости от различных условий и поэтому в некоторых случаях может быть достаточной доза, которая меньше описанного выше диапазона значений, и в некоторых случаях может потребоваться доза, которая больше описанного выше диапазона значений.
Примеры
Настоящее изобретение ниже подробно описано с помощью примеров, которые не ограничивают настоящее изобретение.
Растворители, указанные в скобках в разделах, относящихся к хроматографическому разделению и ТСХ (тонкослойная хроматография), представляют собой использующиеся элюирующие растворители или проявляющие растворители, и указанные их соотношения являются объемными.
Растворители, указанные в скобках в разделах, относящихся к ЯМР, представляют собой растворители, использующиеся для измерений.
В настоящем описании названия соединений образованы с помощью компьютерной программы ACD/Name®, выпускающейся фирмой Advanced Chemistry Development, и обычно они образуются в соответствии с правилами ИЮПАК (Международный союз теоретической и прикладной химии) или в соответствии с номенклатурой ИЮПАК.
Экспериментальные примеры
Пример 1: Бензил-2-метил-2-{3-[3-нитро-5-(трифторметил)фенокси]фенил}пропаноат
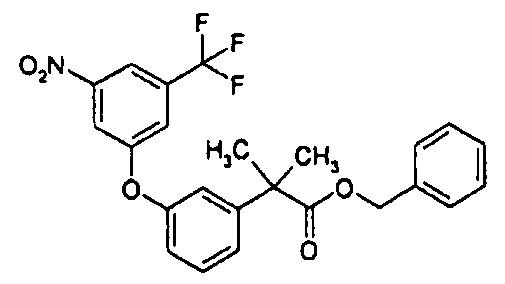
В атмосфере аргона при комнатной температуре 1,3-динитро-5-(трифторметил)бензол (1,52 г) и бензил-2-(3-гидроксифенил)-2-метилпропаноат (1,735 г) добавляли к диметилформамиду (ДМФ) (10 мл) и к смеси добавляли сульфат калия (2,04 г) и затем перемешивали при 90°C в течение 9 ч. Раствор реакционной смеси охлаждали до комнатной температуры, разбавляли этилацетатом, дважды промывали водой, промывали рассолом и сушили над безводным сульфатом магния, и растворитель отгоняли. Полученный остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 100:0→0:100), и получали искомое соединение (2,82 г), обладающее приведенными ниже физическими характеристиками.
1H-ЯМР (CDCl3): δ 8,18 - 6,80, 5,12, 1,62.
Пример 2: Бензил-2-{3-[3-амино-5-(трифторметил)фенокси]фенил}-2-метилпропаноат
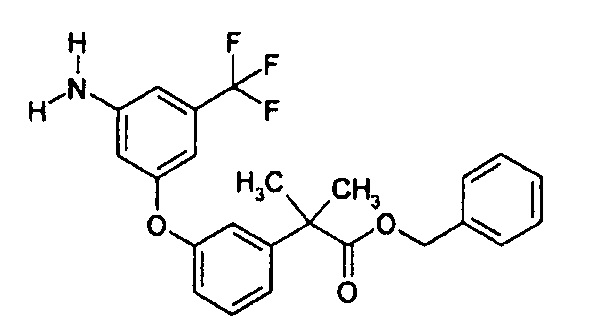
Соединение (2,82 г), полученное в примере 1, растворяли в этаноле (50 мл) и воде (10 мл) при комнатной температуре и к полученному раствору добавляли хлорид аммония (327 мг). Затем к раствору реакционной смеси добавляли железо (1,88 г) и ее перемешивали при 90°C в течение 2 ч. Раствор реакционной смеси охлаждали до комнатной температуры и фильтровали через целит. Полученный фильтрат концентрировали, разбавляли этилацетатом, промывали водой, промывали рассолом и сушили над безводным сульфатом магния, и растворитель отгоняли. Таким образом получали искомое соединение (2,63 г), обладающее приведенными ниже физическими характеристиками.
1H-ЯМР (CDCl3): δ 7,36 - 7,00, 6,89, 6,60, 6,36, 5,12, 1,62.
Пример 3: Бензил-2-метил-2-{3-[3-{[(2,2,2-трихлорэтокси)карбонил]амино}-5-(трифторметил)фенокси]фенил}пропаноат
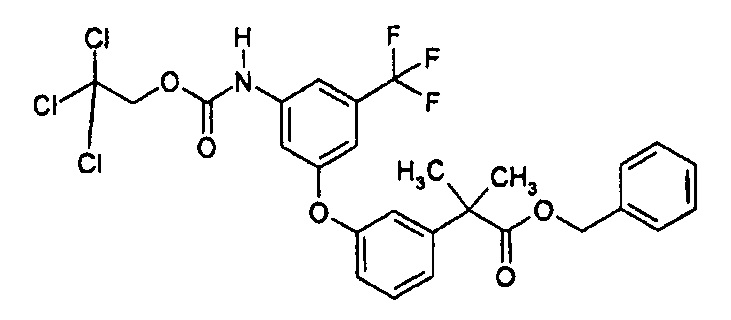
Соединение (2,63 г), полученное в примере 2, растворяли в этилацетате (50 мл) при комнатной температуре. К раствору добавляли гидрокарбонат натрия (2,57 г) и при перемешивании по каплям добавляли 2,2,2-трихлорэтилхлорформиат (0,824 мл). Раствор реакционной смеси перемешивали в течение 4 ч, дважды промывали водой, промывали рассолом и сушили над безводным сульфатом магния, и растворитель отгоняли. Полученный остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 100:0→0:100) и получали искомое соединение (3,33 г), обладающее приведенными ниже физическими характеристиками.
1H-ЯМР (CDCl3): δ 7,50 - 6,90, 5,12, 4,82, 1,61.
Пример 4: 3-Циклогексил-3-пирролидинол
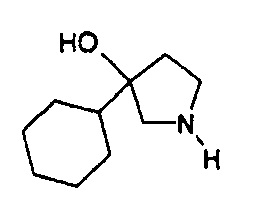
В высушенную на подставке трехгорлую колбу помещали хлорид лантана - бис(хлорид лития) (LaCl3.2LiCl) (0,6 M, 100 мл). В нее добавляли бром(циклогексил)магний (1 M, 33 мл) и в атмосфере аргона смесь перемешивали при комнатной температуре в течение 1 ч. При 0°C к раствору реакционной смеси по каплям добавляли раствор бензил-3-оксо-1-пирролидинкарбоксилата (5,00 г) в тетрагидрофуране (ТГФ) (10 мл) и затем ее постепенно нагревали и перемешивали в течение ночи при комнатной температуре. К раствору реакционной смеси добавляли 10% уксусную кислоту (100 мл) и перемешивали в течение 15 мин. Затем органический слой отделяли и растворитель отгоняли. Полученный остаток частично очищали с помощью хроматографии на силикагеле (гексан:этилацетат =9:1→0:100), и после отгонки растворителя разбавляли метанолом (50 мл) и этилацетатом (50 мл). К разбавленному раствору добавляли 5% палладий на угле (100 мг) и в атмосфере водорода перемешивали при комнатной температуре в течение 2 ч. Раствор фильтровали через целит, и растворитель отгоняли, и получали искомое соединение, обладающее приведенными ниже физическими характеристиками, в виде 1,40 г первичных кристаллов и 2,0 г остатка.
1H-ЯМР (CD3OD): δ 3,40 - 3,20, 2,00 - 1,20.
Пример 5: 2-{3-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}-2-метилпропановая кислота
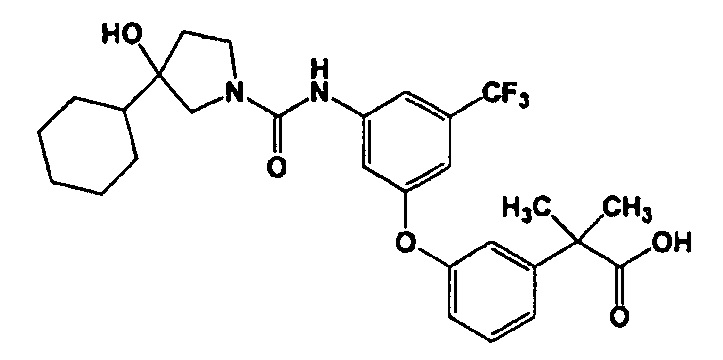
Соединение (357 мг), полученное в примере 3, и соединение (100 мг), полученное в примере 4, добавляли к ДМФ (1 мл) и перемешивали в микроволновом реакторе (CEM Corporation, DISCOVER) при нагревании микроволновым излучением при 90°C в течение 15 мин. Раствор реакционной смеси охлаждали до комнатной температуры, разбавляли этилацетатом, дважды промывали водой, промывали рассолом и сушили над безводным сульфатом магния, и растворитель отгоняли. Полученный остаток частично очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 9:1→0:100), и после отгонки растворителя разбавляли метанолом (5 мл) и этилацетатом (5 мл). К раствору добавляли 5% палладий на угле (10 мг) и перемешивали в атмосфере водорода при комнатной температуре в течение 2 ч. Раствор фильтровали через целит, и растворитель отгоняли, и получали искомое соединение (199 мг), обладающее приведенными ниже физическими характеристиками.
ТСХ: Rf 0,33 (дихлорметан:метанол = 10:1);
1H-ЯМР (CDCl3): δ 7,36 - 7,23, 7,18 - 7,15, 7,12 - 7,10, 6,95 - 6,89, 6,48, 3,65 - 3,46, 3,27, 2,00 - 1,54, 1,45 - 1,08.
Примеры 5 (1)-5 (7)
В следующем примере соединения получали путем проведения реакций при таких же условиях, как в примере 1 → примере 2 → примере 3 → примере 5, с использованием бензил-2-(3-гидроксифенил)-2-метилпропаноата или, альтернативно, соответствующего производного фенола и соединения, полученного в примере 4, или, альтернативно, соответствующего производного пиперидина.
Пример 5 (1): 4-Циклопентил-4-гидрокси-N-[3-{4-[(метилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-1-пиперидинкарбоксамид
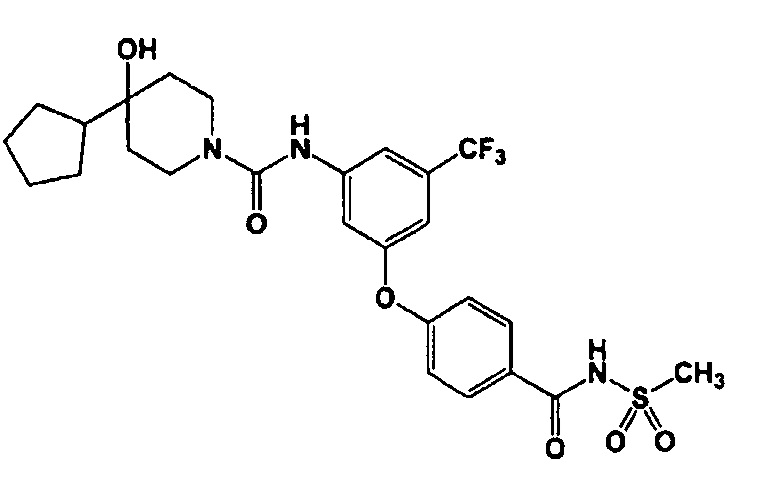
ТСХ: Rf 0,21 (дихлорметан : метанол = 10:1);
1H-ЯМР (CD3OD): δ 8,02, 7,63 - 7,53, 7,47 - 7,36, 7,13 - 7,02, 6,96 - 6,87, 4,01 - 3,78, 3,24, 3,27 - 3,16, 1,99 - 1,75, 1,72 - 1,35.
Пример 5 (2): 4-циклопентил-N-[3-{4-[(этилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-4-гидрокси-1-пиперидинкарбоксамид
ТСХ: Rf 0,26 (дихлорметан : метанол = 10:1);
1H-ЯМР (CD3OD): δ 8,02, 7,62 - 7,55, 7,46 - 7,39, 7,15 - 7,03, 6,95 - 6,88, 4,00 - 3,83, 3,41, 3,28 - 3,16, 1,98 - 1,78, 1,72 - 1,40, 1,36.
Пример 5 (3): 1-{4-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопропанкарбоновая кислота
ТСХ: Rf 0,56 (дихлорметан : метанол = 10:1);
1H-ЯМР (CDCl3):δ 7,50, 7,37 - 7,28, 7,23, 7,00 - 6,89, 6,42, 3,66 - 3,54, 3,50, 3,31, 2,02 - 1,58, 1,32 - 1,18.
Пример 5 (4): 2-{4-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенокси}-2-метилпропановая кислота
ТСХ: Rf 0,17 (дихлорметан : метанол = 10:1);
1H-ЯМР (CDCl3): δ 7,32 - 7,24, 6,96 - 6,86, 6,49, 3,66 - 3,44, 3,30, 2,01 - 1,52, 1,45 - 1,13.
Пример 5 (5): 1-{4-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенокси}циклопропанкарбоновая кислота
ТСХ: Rf 0,11 (дихлорметан : метанол = 10:1);
1H-ЯМР (CDCl3): δ 7,63 - 7,58, 7,50 - 7,46, 7,12 - 7,00, 6,93 - 6,88, 3,73 - 3,64, 3,57, 3,39, 2,10 - 1,71, 1,64 - 1,55, 1,52 - 1,26, 1,25 - 1,18.
Пример 5 (6): 1-{4-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклобутанкарбоновая кислота
ТСХ: Rf 0,69 (хлороформ : метанол = 5:1);
1H-ЯМР (CD3OD): δ 7,65, 7,41, 7,29, 6,97, 6,81, 3,60 - 3,30, 2,80, 2,40, 2,00 - 1,08.
Пример 5 (7): 1-{4-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопентанкарбоновая кислота
ТСХ: Rf 0,46 (хлороформ : метанол = 5:1);
1H-ЯМР (CD3OD): δ 7,65, 7,46, 7,28, 6,95, 6,80, 3,60 - 3,20, 2,60, 2,00 - 1,08.
Пример 6: (+)-1-{4-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклобутанкарбоновая кислота и (-)-1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклобутанкарбоновая кислота
Соединение, полученное в примере 5 (6), разделяли на оптические изомеры с помощью ВЭЖХ (используемая колонка: Daicel Corporation, CHIRALPAK AD (4,6 мм × 250 мм); проявляющий растворитель: гексан : этанол : трифторуксусная кислота = 50:50:1; скорость потока: 1 мл/мин). При указанных выше условиях разделения на оптические изомеры оптически активные соединения примера 5 (6) получали в виде первого пика (время удерживания: примерно 4,5 мин) и в виде второго пика (время удерживания: примерно 5,5 мин) соответственно. Оптическое вращение для соединения, полученного в виде первого пика, было следующим:
[α]D = -25,8 (CHCl3, c=0,33).
Поэтому было установлено, что соединение, соответствующее первому пику, было правовращающим оптически активным соединением примера 5 (6) и соединение, соответствующее второму пику, было левовращающим оптически активным соединением примера 5(6).
Пример 6 (1): (+)-2-{3-[3-{[(3-Циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}-2-метилпропановая кислота и (-)-2-{3-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}-2-метилпропановая кислота
Из соединения, полученного в примере 5, при условиях разделения на оптические изомеры, описанных в примере 6, получали правовращающее и левовращающее оптически активные соединения.
Пример 7: 3-{[(4-Гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}-5-(трифторметил)бензойная кислота
Искомое соединение (957 мг), обладающее приведенными ниже физическими характеристиками, получали путем проведения реакции при таких же условиях, как в примере 5, с использованием 4-изобутил-4-пиперидинола и соединения, полученного путем проведения реакций при таких же условиях, как в примере 2 → примере 3 с использованием метил-3-нитро-5-(трифторметил)бензоата (5,3 г) вместо соединения, полученного в примере 1.
ТСХ: Rf 0,18 (дихлорметан : метанол : уксусная кислота = 100:10:1);
ESI-MS (масс-спектрометрия с ионизацией электрораспылением) (ионизация с образованием положительных ионов при 20 В) 389 (M+H).
Пример 8: 2-(4-{[3-{[(4-Гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}-5-(трифторметил)бензоил]окси}фенил)-2-метилпропановая кислота
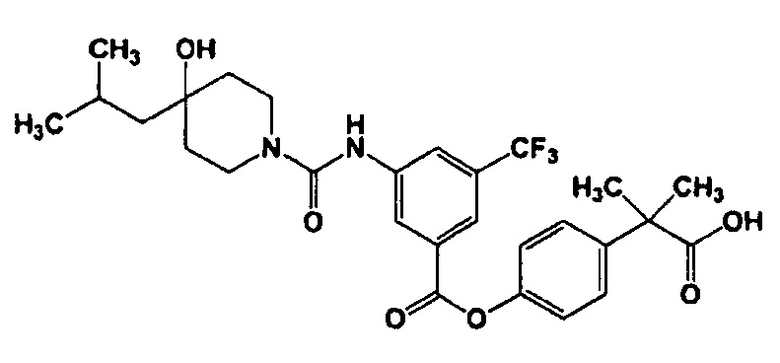
Соединение (150 мг), полученное в примере 7, растворяли в ДМФ (1 мл) и к нему добавляли бензил-2-(4-гидроксифенил)-2-метилпропаноат (125 мг), 1-этил-3-(3-диметиламинопропил)карбодиимидгидрохлорид (EDC) (111 мг), моногидрат 1-гидроксибензотриазола (HOBt) (78,2 мг) и диизопропилэтиламин (100 мкл) и перемешивали в течение ночи при комнатной температуре. Раствор реакционной смеси разбавляли этилацетатом, дважды промывали водой, промывали рассолом и сушили над безводным сульфатом магния, и растворитель отгоняли. Полученный остаток частично очищали с помощью хроматографии на силикагеле (гексан : этилацетат = 9:1→0:100), растворитель отгоняли и раствор разбавляли метанолом (1 мл) и этилацетатом (1 мл). К раствору добавляли 5% палладий на угле (10 мг) и в атмосфере водорода, перемешивали при комнатной температуре в течение 2 ч. Раствор реакционной смеси фильтровали через целит и растворитель отгоняли, и получали искомое соединение (27,5 мг), обладающее приведенными ниже физическими характеристиками.
ТСХ: Rf 0,68 (хлороформ:метанол = 5:1);
1H-ЯМР (CDCl3): δ 8,20 - 6,80, 3,90, 3,14, 1,80, 1,70 - 1,50, 1,62, 1,43, 0,99.
Пример 9: 1-{4-[3-Хлор-5-({[4-(4-фторфенил)-4-гидрокси-1-пиперидинил]карбонил}амино)фенокси]фенокси}циклопропанкарбоновая кислота
Искомое соединение, обладающее приведенными ниже физическими характеристиками, получали путем проведения реакций при таких же условиях, как в примере 1 → примере 2 → примере 3 → примере 5, с использованием 1,3-динитро-5-хлорбензола, соответствующего производного фенола вместо бензил-2-(3-гидроксифенил)-2-метилпропаноата и соответствующего производного пиперидина вместо соединения, полученного в примере 4.
ТСХ: Rf 0,14 (хлороформ : метанол = 9:1);
1H-ЯМР (CD3OD): δ 7,55, 7,25, 7,10-6,80, 6,55, 4,05, 3,29, 2,99, 1,75, 1,54, 1,20.
Пример 10: 2-[4-(3-Фтор-5-{[(4-гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}фенокси)фенил]-2-метилпропановая кислота
Искомое соединение, обладающее приведенными ниже физическими характеристиками, получали путем проведения реакций при таких же условиях, как в примере 1 → примере 2 → примере 3 → примере 5, с использованием 1,3-динитро-5-фторбензола, бензил-2-(4-гидроксифенил)-2-метилпропаноата и соответствующего производного пиперидина вместо соединения, полученного в примере 4.
ТСХ: Rf 0,49 (хлороформ : метанол = 9:1);
1H-ЯМР (CDCl3): δ 7,30, 7,00, 6,65, 6,58, 6,30, 3,74, 3,25, 1,80 - 1,50, 1,41, 0,98.
Экспериментальные примеры
Воздействие соединений, предлагаемых в настоящем изобретении, проверяли с помощью экспериментальных методик, представленных ниже в настоящем изобретении в виде биологического экспериментального примера и физического экспериментального примера.
Биологический экспериментальный пример 1: Исследование антагонистической активности по отношению к S1P2 (EDG-5) путем мониторинга изменения внутриклеточной концентрации ионов кальция
Клетки яичника китайского хомячка (CHO), сверхэкспрессирующие ген S1P2 (EDG-5) человека, выращивали в среде Ham's F12, содержащей 10% фетальную бычью сыворотку (FBS), антибиотик/фунгицидный агент и G418. Клетки CHO, сверхэкспрессирующие ген S1P2 (EDG-5) крысы, выращивали в среде Ham's F12, содержащей 10% FBS, пенициллин/стрептомицин и бластицидин S. Выращенные клетки инкубировали в растворе Fura2-AM (5 мкМ) [среда Ham's F12, содержащая FBS (10%), буфер HEPES (20 мМ, pH от 7,2 до 7,5) и пробенецид (2,5 мМ)] при 37°C в течение 60 мин. Клетки дважды промывали сбалансированным солевым раствором Хэнкса, содержащим буфер HEPES (20 мМ, pH от 7,2 до 7,5) и пробенецид (2,5 мМ), и погружали в этот же раствор. Планшет устанавливали в системе скрининга лекарственного средства на основе флуоресценции и внутриклеточную концентрацию ионов кальция измеряли в течение 30 с без стимулирования. Добавляли раствор исследуемого соединения (конечная концентрация S1P2 человека: от 0,25 нМ до 25 мкМ и конечная концентрация S1P2 крысы: от 0,25 нМ до 2,5 мкМ) или диметилсульфоксид (ДМСО) и через 3 мин добавляли S1P (конечная концентрация: 30 или 300 нМ) и увеличение внутриклеточной концентрации ионов кальция до и после добавления S1P измеряли с интервалом в 3 с (длина волны возбуждения: 340 нм и 380 нм, длина волны флуоресценции: 540 нм).
Антагонистическую активность по отношению к S1P2 (EDG-5) рассчитывали, как подавление (%) по приведенному ниже уравнению, в котором A означает контрольное значение, которым являлось максимальное значение после добавления S1P (конечная концентрация: 30 или 300 нМ) в лунках, в которые добавляли ДМСО без исследуемого соединения, и B означает увеличенное значение после добавления S1P в лунки, обработанные исследуемым соединением
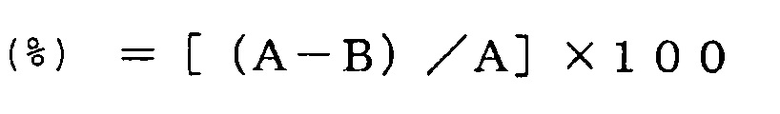
Значения IC50 рассчитывали, как концентрацию соединения, предлагаемого в настоящем изобретении, которая приводит к подавлению на 50%.
Использующимися сравнительными соединениями являлись соединения, раскрытые в примере 1(64) (ниже в настоящем изобретении называющееся сравнительным соединением A) и в примере 1(85) (ниже в настоящем изобретении называющееся сравнительным соединением B) в Патентном документе 3 (WO 2004/002531). Структурные формулы сравнительных соединений приведены ниже.
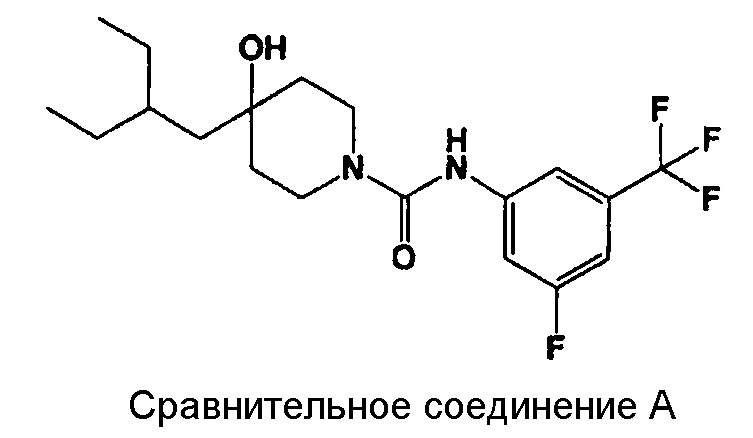
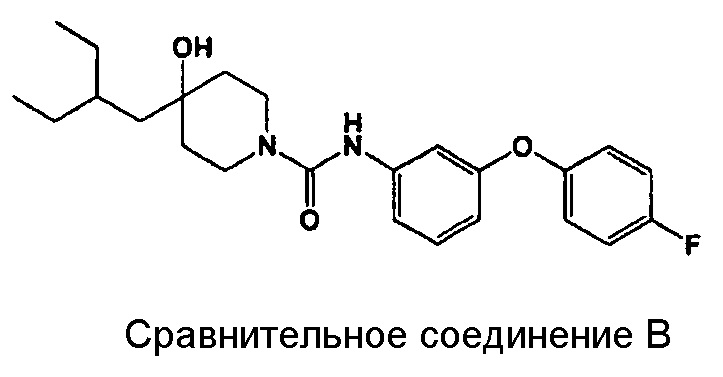
Антагонистическая активность по отношению к S1P2 человека и крысы (EDG-5) для соединений, предлагаемых в настоящем изобретении, и сравнительных соединений приведены в представленной ниже таблице 1.
В результате установлено, что соединения, предлагаемые в настоящем изобретении, обладают антагонистической активностью по отношению к S1P2 человека, значительно улучшенной по сравнению со сравнительными соединениями. Кроме того, соединения, предлагаемые в настоящем изобретении, также обладают значительно улучшенными разностями значений антагонистической активности по отношению к S1P2 для разных видов, т.е. для людей и крыс, и, таким образом, эффективность, полученную с помощью моделей патологических состояний на крысах, можно экстраполировать на людей.
Физический экспериментальный пример 2: Определение растворимости
Раствор для построения градуировочной кривой готовили путем разбавления исследуемого соединения (10 ммоль/л, раствор в ДМСО) в ацетонитриле и добавления ацетонитрила, содержащего соединение - внутренний стандарт (варфарин) до концентрации, равной 0,1, 0,4 и 2 мкмоль/л. Раствор образца готовили путем добавления к 495 мкл (pH 6,8) второго раствора, определенного в Фармакопее Японии (используемый раствор готовили путем добавления воды к 250 мл 0,2 моль/л раствора реагента - дигидрофосфата калия и 118 мл 0,2 моль/л раствора реагента - гидроксида натрия с доведением объема до 1000 мл), 5 мкл исследуемого соединения (10 ммоль/л, раствор в ДМСО), перемешивания при комнатной температуре в течение 5 ч, переноса полученного раствора в чашку с фильтром для вакуумного фильтрование, разбавления 20 мкл фильтрата ацетонитрилом и добавления ацетонитрила, содержащего внутренний стандарт. Раствор для построения градуировочной кривой и раствор образца (по 5 мкл) инжектировали в прибор LC-MS/MS (жидкостная хроматография-масс-спектрометрия/масс-спектрометрия (Discovery Max from Thermo Scientific) для количественного исследования (диапазон количественного определения: от 0,1 до 2 мкмоль/л). Растворимость рассчитывали путем умножения количественного значения на 50. Если количественное значение выходило за границы диапазона количественного определения, растворимость выражали, как равную < 5 мкмоль/л или 100 мкмоль/л.
Значения растворимости соединений, предлагаемых в настоящем изобретении, и сравнительных соединений приведены в представленной ниже таблице 2.
В результате установлено, что соединения, предлагаемые в настоящем изобретении, обладают более значительной растворимостью, чем сравнительные соединения.
Примеры составов
Пример состава 1
Указанные ниже компоненты смешивали и затем прессовали в таблетки по обычной методике и получали 10000 таблеток, содержащих 10 мг активного ингредиента в одной таблетке.
Пример состава 2
Указанные ниже компоненты смешивали по обычной методике, затем пропускали через фильтр для удаления пыли, фасовали по 5 мл в ампулы, стерилизовали путем нагревания в автоклаве и получали 10000 ампул, содержащих 20 мг активного ингредиента в одной ампуле.
ПРИМЕНЕНИЕ В ПРОМЫШЛЕННОСТИ
Соединение, предлагаемое в настоящем изобретении, обладает высокой антагонистической активностью по отношению к S1P2 человека и поэтому применимо для лечения заболеваний, опосредованных S1P2, таких как заболевания, обусловленные сужением сосудов, и фиброз.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФЕНИЛЬНОЕ ПРОИЗВОДНОЕ | 2012 |
|
RU2619105C2 |
| НОВОЕ ПИРРОЛИДИНОВОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ АГОНИСТА РЕЦЕПТОРА МЕЛАНОКОРТИНА | 2015 |
|
RU2669938C2 |
| ПРИМЕНЕНИЕ РЕЦЕПТОРА АНТАГОНИСТА ЕР4 ДЛЯ ЛЕЧЕНИЯ ХРЯЩЕВОЙ БОЛЕЗНИ | 2014 |
|
RU2663620C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ РЕЦЕПТОРА EP4 В ЛЕЧЕНИИ IL-23-ОПОСРЕДУЕМЫХ ЗАБОЛЕВАНИЙ | 2011 |
|
RU2571816C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ДВОЙНЫХ ИНГИБИТОРОВ АУТОТАКСИНА (ATX)/КАРБОАНГИДРАЗЫ (CA) | 2016 |
|
RU2725138C2 |
| ТВЕРДЫЙ СОСТАВ С УЛУЧШЕННЫМИ РАСТВОРИМОСТЬЮ И СТАБИЛЬНОСТЬЮ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2375046C2 |
| ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ИНГИБИТОР НАТРИЙЗАВИСИМОГО ПЕРЕНОСЧИКА ФОСФАТА | 2015 |
|
RU2740008C2 |
| НОВЫЕ СОЕДИНЕНИЯ | 2001 |
|
RU2261245C2 |
| ПРОФИЛАКТИЧЕСКОЕ ИЛИ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ОТ ФОТОДЕРМАТОЗА | 2021 |
|
RU2812785C1 |
| ПРОИЗВОДНЫЕ 4-АМИНОПИПЕРИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2266282C2 |
Изобретение относится к соединению общей формулы (I), обладающему высокой антагонистической активностью по отношению к S1P2 человека, и может применяться для приготовления лекарственного средства для лечения заболевания, опосредованного S1P2, такого как заболевание, обусловленное сужением сосудов, фиброз и респираторное заболевание. 4 н. и 10 з.п. ф-лы, 2 табл., 9 пр.
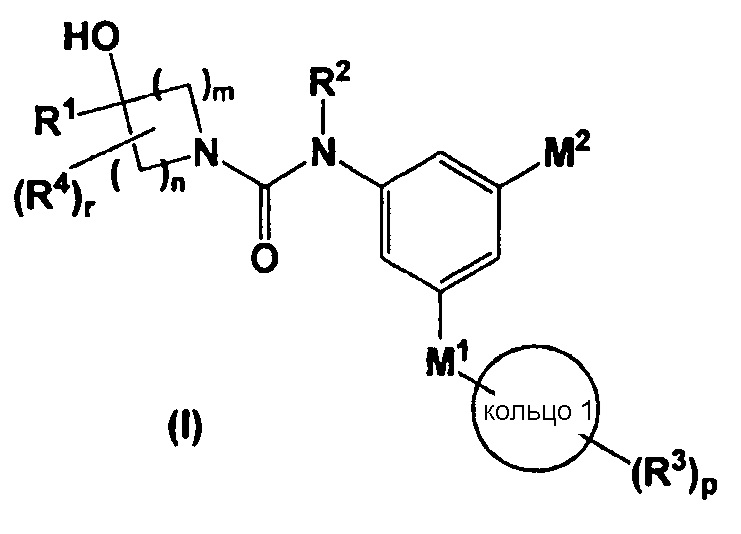
1. Соединение, представленное общей формулой (I)
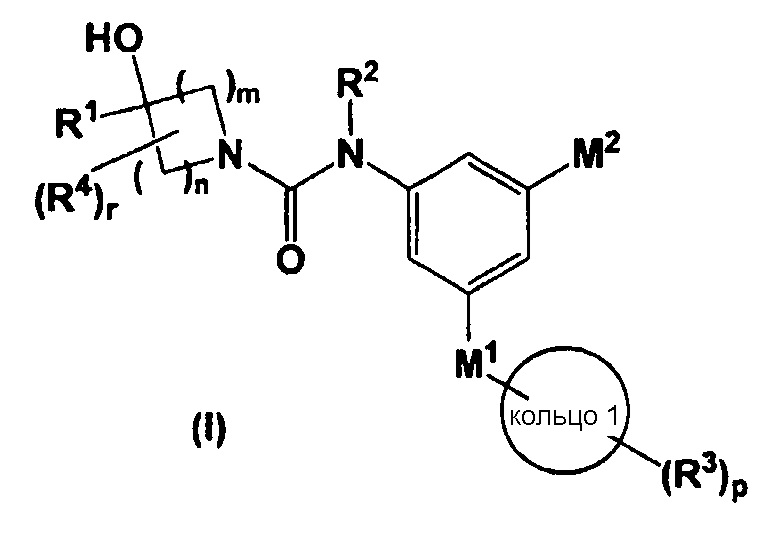 ,
,
в которой R1 означает (1) C1-C8-алкильную группу или (2) C3-C7-карбоцикл, который может содержать от 1 до 5 заместителей, представляющих собой атом галогена;
R2 означает (1) атом водорода;
R3 означает (1) -L-CONR6R7 или (2) -L-COOR9;
R4 отсутствует;
L означает (1) связь, (2) группу, описываемую формулой
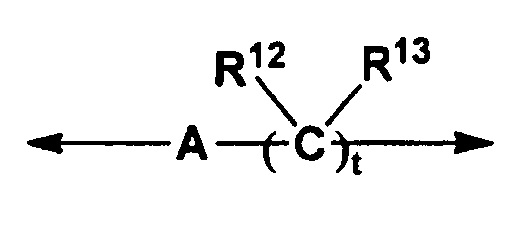 ,
,
в которой A означает (1) связь или (2) атом кислорода; R12 и R13 соответственно и независимо означают (1) C1-C4-алкильную группу или (2) R12 и R13 вместе с атомом углерода, к которому они присоединены, могут образовать C3-C7-карбоцикл; и стрелка справа означает связь с -CONR6R7 или -COOR9;
R6 и R7 соответственно и независимо означают (1) атом водорода или (2) -SO2R17;
R9 означает (1) атом водорода;
кольцо 1 представляет собой фенил;
R17 означает (1) C1-C4-алкильную группу;
M1 означает (1) -O- или (2) -C(O)O-;
M2 означает атом галогена или C1-C4-галогеналкильную группу;
n означает целое число, равное от 1 до 2;
m означает целое число, равное от 1 до 2;
p означает целое число, равное 1;
r означает целое число, равное 0;
t означает целое число, равное 1;
или его фармацевтически приемлемая соль.
2. Соединение по п. 1, которое представлено общей формулой (I-1)
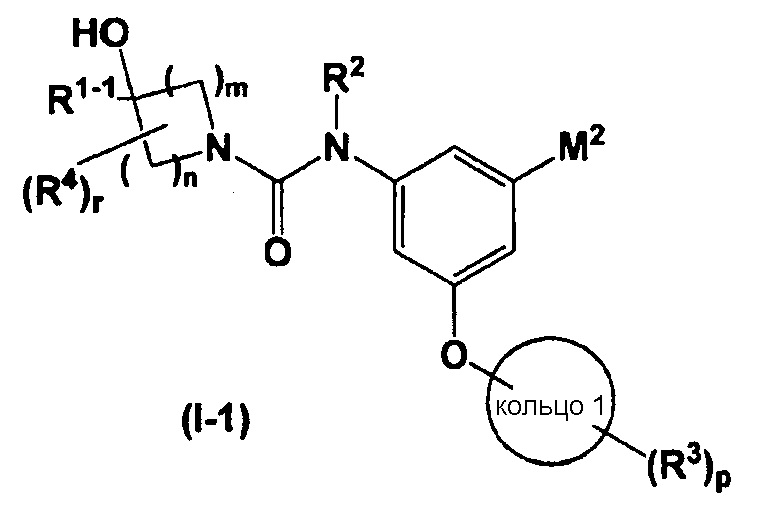 ,
,
в которой R1-1 имеет те же определения, как определено в п. 1, другие символы имеют те же определения, как определено в п. 1 формулы.
3. Соединение по п. 2, которым является
2-{3-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}-2-метилпропановая кислота,
4-циклопентил-4-гидрокси-N-[3-{4-[(метилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-1-пиперидинкарбоксамид,
4-циклопентил-N-[3-{4-[(этилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-4-гидрокси-1-пиперидинкарбоксамид,
1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопропанкарбоновая кислота,
2-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенокси}-2-метилпропановая кислота,
1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенокси}циклопропанкарбоновая кислота,
1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклобутанкарбоновая кислота,
1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопентанкарбоновая кислота,
2-(4-{[3-{[(4-гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}-5-(трифторметил)бензоил]окси}фенил)-2-метилпропановая кислота, 1-{4-[3-хлор-5-({[4-(4-фторфенил)-4-гидрокси-1-пиперидинил]карбонил}амино)фенокси]фенокси}циклопропанкарбоновая кислота,
2-[4-(3-фтор-5-{[(4-гидрокси-4-изобутил-1-пиперидинил)карбонил]амино}фенокси)фенил]-2-метилпропановая кислота,
(+)-1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклобутанкарбоновая кислота,
(-)-1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклобутанкарбоновая кислота,
(+)-2-{3-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}-2-метилпропановая кислота,
(-)-2-{3-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}-2-метилпропановая кислота
или его фармацевтически приемлемая соль.
4. Соединение по п. 2, которым является 4-циклопентил-4-гидрокси-N-[3-{4-[(метилсульфонил)карбамоил]фенокси}-5-(трифторметил)фенил]-1-пиперидинкарбоксамид или
1-{4-[3-{[(3-циклогексил-3-гидрокси-1-пирролидинил)карбонил]амино}-5-(трифторметил)фенокси]фенил}циклопентанкарбоновая кислота.
5. Фармацевтическая композиция, обладающая антагонистической активностью по отношению к S1P2, содержащая эффективное количество соединения, представленного общей формулой (I), или его фармацевтически приемлемой соли по п. 1.
6. Фармацевтическая композиция по п. 5, которая является профилактическим и/или терапевтическим средством при заболевании, опосредованном S1P2.
7. Фармацевтическая композиция по п. 6, где заболевание, опосредованное S1P2, представляет собой заболевание, обусловленное сужением сосудов, фиброз, респираторное заболевание, артериосклероз, окклюзионное заболевание периферической артерии, ретинопатию, глаукому, возрастную дегенерацию желтого пятна, нефрит, диабет, осложнение при диабете, дислипидемию, гепатит, цирроз печени, печеночную недостаточность, невропатию, ревматоидный артрит, рану, боль, крапивницу, системную красную волчанку (SLE) или рак.
8. Фармацевтическая композиция по п. 7, где заболевание, обусловленное сужением сосудов, представляет собой вазоспастическое заболевание головного мозга, вазоспастическое заболевание сердца, коронарное вазоспастическое заболевание, гипертензию, легочную гипертензию, инфаркт миокарда, стенокардию, аритмию, портальную гипертензию, варикоз, асциты, спленомегалию, печеночную энцефалопатию или ишемическое реперфузионное поражение.
9. Фармацевтическая композиция по п. 8, которая способна устойчиво снизить портальное давление.
10. Фармацевтическая композиция по п. 9, которую можно вводить один раз в сутки.
11. Фармацевтическая композиция по любому из пп. 8-10, которая является профилактическим средством при первичном или вторичном кровотечении при варикозе пищевода, связанном с портальной гипертензией.
12. Способ профилактики и/или лечения заболевания, опосредованного S1P2, включающий введение млекопитающему эффективного количества соединения, представленного общей формулой (I), или его фармацевтически приемлемой соли по п. 1.
13. Соединение, представленное общей формулой (I), или его фармацевтически приемлемая соль по п. 1 для профилактики и/или лечения заболевания, опосредованного S1P2.
14. Применение соединения, представленного общей формулой (I), или его фармацевтически приемлемой соли по п. 1 для получения профилактического и/или терапевтического средства при заболевании, опосредованном S1P2.
| ФЕНИЛЬНОЕ ПРОИЗВОДНОЕ | 2012 |
|
RU2619105C2 |
| Способ укрепления откосов | 1988 |
|
SU1698375A1 |
| Коммутатор | 1987 |
|
SU1522314A1 |
Авторы
Даты
2017-12-25—Публикация
2014-03-25—Подача