ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к натуральным синим антоцианин-содержащим красителям, включая фракции молекул антоцианина, выделенные при заданном рН из смеси соков и экстрактов антоцианин-содержащих овощей и плодов, исходя из разницы в молекулярном заряде и полярности.
УРОВЕНЬ ТЕХНИКИ
[0002] В пищевой промышленности растет интерес к замещению натуральными красителями синтетических материалов для окрашивания пищевых продуктов.
[0003] Одной из проблем замещения синтетических красителей натуральными красителями является идентификация натуральных красителей, обеспечивающих характеристики, аналогичные таковым, обеспеченным синтетическими красителями. До настоящего времени не найдены натуральные красители, обеспечивающие те же характеристики цвета, что и синтетический синий краситель FD&C Blue No. 1. Отсутствие подходящих натуральных красителей зеленовато-синего цветового оттенка также сделало проблематичным получение желаемых натуральных красителей зеленого цветового оттенка смешиванием натурального синего и желтого красителей.
[0004] В качестве натурального синего красителя используют голубую спирулину, синевато-зеленый материал, полученный из водорослей, но он не обеспечивает такие же цветовые характеристики, как у FD&C Blue No. 1.
[0005] Антоцианины представляют водорастворимые соединения, находящиеся в вакуолях клеток плодов, овощей и лепестков цветов, и иногда корней, листьев, стеблей, и коры растений. По меньшей мере отчасти в виду широкой доступности соков и экстрактов антоцианин-содержащих овощей и плодов их используют в качестве натуральных съедобных красителей и получают красители, в частности натуральные красители красного, пурпурного и синего цветов.
[0006] Антоцианин содержит антоцианидин (агликон) переэтерифицированный одной или более молекулой сахара (гликон(ы)) с получением гликозида. Молекулы сахара могут быть присоединены в С-3, С-5, С-7, С-3', С-4', и/или С-5' позициях. Примеры молекул сахара, присутствующих в структурах антоцианина, представляют арабинозу, галактозу, глюкозу, рамнозу, рутинозу, самбубиозу, софорозу и ксилозу.
[0007] Также антоцианины могут быть ацилированны, то есть они могут иметь одну или более молекулу, переэтерифицированную молекулой сахара, как правило, в 6-позиции моносахарида, но также потенциально во 2-, 3- или 4-позициях. Самые распространенные ацильные единицы включают таковые, полученные из кумариновой кислоты, феруловой кислоты, кофеиновой кислоты, синаповой кислоты, галлиевой кислоты, малоновой кислоты, уксусной кислоты, яблочной кислоты, янтарной кислоты, ванилиновой кислоты и щавелевой кислоты.
[0008] Структура антоцианидина приведена ниже в форме флавилиевых катионов, которые представляют первичную форму в кислых условиях. Антоцианидин может быть замещен водородом, гидроксильной и/или метоксильной группами в различных позициях:
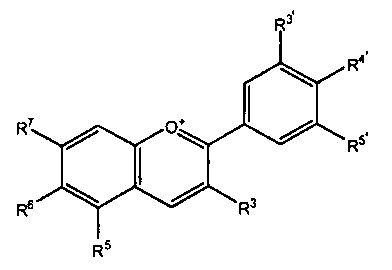
где R3 представляет Н или ОН,
R5 представляет Н, ОН или ОСН3,
R6 представляет Н или ОН,
R7 представляет ОН или ОСН3,
R3' представляет Н, ОН или ОСН3,
R4' представляет ОН или ОСН3 и
R5' представляет Н, ОН или ОСН3.
[0009] Самые распространенные в природе антоцианидины представляют следующие структуры:
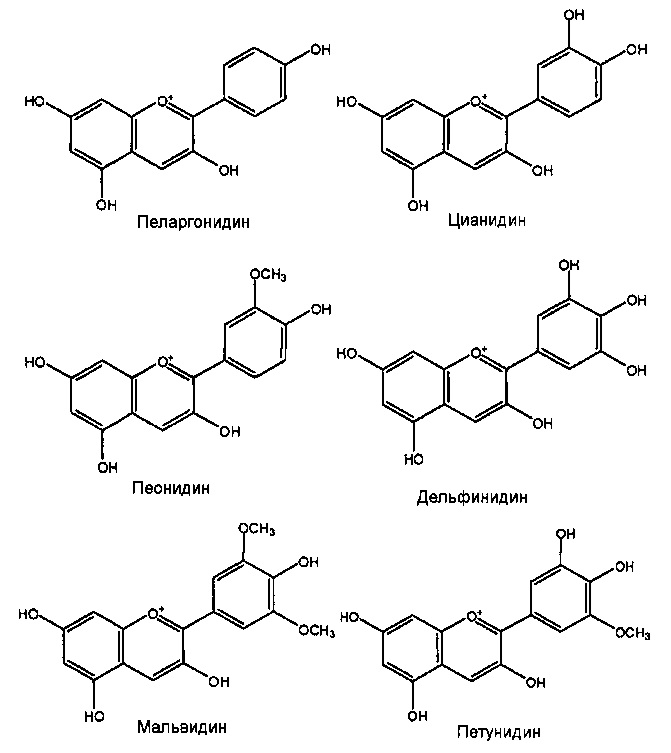
[0010] Следовательно, класс соединений, известных как антоцианины, включает огромное количество структурно различных соединений на основе различий первичной структуры, гликозилированных и ацилированных моделей.
[0011] Известные растительные источники антоцианинов включают: (1) овощи, такие как краснокочанная капуста, фиолетовый сладкий картофель, синий картофель, красный картофель, красный редис, черная морковь, фиолетовая морковь, фиолетовая кукуруза, красная кукуруза, красный лук, фиолетовая брокколи, красная брокколи, фиолетовая цветная капуста, корень ревеня, черные бобы, красный листовой салат, черный рис и баклажаны; и (2) плоды, такие как клубника, малина, клюква, брусника, красный виноград, яблоки, черная смородина, красная смородина, вишня, голубика, бузина, черника, водяника, ежевика, арония, крыжовник, асаи, нектарин, персик, слива, апельсин-королек и синие томаты. Каждый источник антоцианина содержит различные количества нескольких, отличающихся видов антоцианинов с от 15 до 30 структурно отличающихся молекул антоцианинов, являющихся обычными для данного растительного источника.
[0012] В результате изменения рН происходит изменение характеристик цвета соков и экстрактов антоцианин-содержащих овощей и плодов. Как правило, антоцианин-содержащие соки и экстракты имеют красный цветового оттенка при низком рН, и цветовой оттенок сдвигается в сторону фиолетового при повышении рН. Только несколько соков и экстрактов имеют синий цветового оттенка при дальнейшем повышении рН.
[0013] Изменение цвета антоцианин-содержащих соков и экстрактов в результате изменения рН зависит от множества вторичных структур антоцианинов, которые могут существовать в равновесии с первичной структурой флавилиевых катионов в водном растворе. В случае, когда рН изменяется, относительные количества различных равновесных структур изменяются. При данном рН может преобладать одна или более структурная форма, при этом другие присутствуют в малых количествах или не присутствуют вообще. Например, при очень низком рН, преобладает форма флавилиевых катионов. При повышении рН молекулы в форме флавилиевых катионов могут быть депротеинированы и превращены в форму карбиноловых псевдооснований, которая далее может быть превращена через потерю молекулы воды и протона в формы нейтральных и ионизированных хиноидных оснований, соответственно, и далее в форму халкона. Эти трансформации уменьшают число молекул в форме флавилиевых катионов и увеличивают количество других равновесных форм в разной степени. Следовательно, различные равновесные структуры существуют в различных относительных количествах при более высоком рН по сравнению с более низким рН. Каждая структурная форма антоцианина может по разному поглощать свет, в результате приводя к различному восприятию цвета, включая отсутствие цвета. Следовательно, при изменении рН раствора изменяются относительные количества различных структурных форм, что в результате в свою очередь может привести к изменению цвета раствора.
[0014] Каждая отдельная молекула антоцианина характеризуется своим собственным набором равновесных молекулярных структур и константой равновесия для реакции трансформации одной структуры в другую. Например, реакция трансформации одной равновесной структуры антоцианина в другую может иметь конкретную константу кислотной диссоциации Ka, связанную с ней. Реакция также может рассматриваться относительно логарифмической постоянной pKa, которая определена как - log10 Ka.
[0015] Структуры флавилиевых катионов и хиноидных оснований имеют сопряженные связи, соединяющие все три кольца молекул антоцианина. Пространственные делокализованные pi связи позволяют флавилиевым катионам и хиноидному основанию поглощать видимый свет, что в результате приводит к восприятию цветового оттенка красного флавилиевых катионов при низком рН и фиолетового или синего цветового оттенка ионизированного хиноидного основания при более высоком рН. Напротив, структуры карбинолового псевдооснования и халкона не имеют делокализованных pi связей, соединяющих все три кольца, и бесцветны или имеют желтоватый цвет.
[0016] Замещение антоцианинов также оказывает воздействие на цвет. Например, как правило, наблюдается изменение цветового тона от розового к фиолетовому, когда атомы водорода замещают гидроксильными группами. Аналогично, наблюдается воздействие на цвет количества и типа гликозильных (сахарных) единиц и ацильных единиц. Однако эти феномены в настоящее время не до конца понятны и предсказуемы.
[0017] Дополнительно, межмолекулярные и внутримолекулярные взаимодействия также оказывают воздействие на цвет антоцианина. Один и тот же антоцианин может иметь различные цветовые оттенки в зависимости от других присутствующих молекул. Например, считается, что ацильные группы на сахарах антоцианина могут увеличивать и защищать флавилиевые катионы в C-2 позиции от нуклеофильной атаки. Следовательно, это внутримолекулярное взаимодействие предотвращает образование бесцветной структуры карбинольного псевдоснования. Аналогично, считается, что молекулы антоцианина самоассоциируются, что подтверждается тем фактом, что увеличение в два раза концентрации антоцианина может вызвать 300-кратное увеличение цветности и может изменить цветовой оттенок наряду с яркость/насыщенностью. Предполагается, что эта самоассоциация аналогична внутримолекулярной упаковке и предотвращает нуклеофильную атаку и образование структуры карбинольного псевдоснования.
[0018] Хотя известно, что каждый из таких факторов, как рН, химическая структура антоцианина, схемы замещения, меж- и внутримолекулярные взаимодействия, оказывает воздействие на наблюдаемый цвет соков и экстрактов антоцианин-содержащих овощей и плодов, не до конца понятно, как эти факторы воздействуют на изменение цвета, то есть не предсказуема конкретная причина и эффект.
[0019] Например, отдельные молекулы антоцианина отделяют при использовании ВЭЖХ, но разделение проводят всегда при низком рН, и характеристики цвета отдельных антоцианинов анализируют при низком рН. Аналогично, изучалось влияние рН на характеристики цвета соков и экстрактов антоцианин-содержащих овощей и плодов, но в этих исследованиях анализировали комплексную смесь антоцианинов, естественным образом присутствующих в соках и экстрактах. Однако в настоящее время не до конца понятно и не может быть предсказано, как изменение рН влияет на характеристики цвета отдельных молекул антоцианинов или фракций антоцианинов, выделенных из натуральных источников. В предшествующем уровне техники указывается, что число и тип заместителей, например сахарные и ацильные группы, влияют на цвет; однако не указывается, как эти заместители влияют на цвет при изменении рН. Наконец, хотя в предшествующем уровне техники предполагается, что различные меж- и внутримолекулярные взаимодействия влияют на цвет, не указывается, как изменение рН влияет на эти меж- и внутримолекулярные взаимодействия и в конечном итоге на наблюдаемый цвет антоцианинов.
[0020] В WO 2009/100165 А2 описывается способ отделения антоцианинов от других фенольных молекул в соках антоцианин-содержащих плодов и овощей. В WO 2009/100165 А2 не описывается селективное отделение фракций молекул антоцианина, исходя из разницы зарядов и полярности молекул, с получением фракций с заданным цветом, который отличается от цвета антоцианин-содержащего сока.
[0021] Выделение отдельных антоцианинов при использовании аналитической шкалы описано в J. Цветность tography Α., 1148 (2007), 38-45. Отделение проводят при низком рН, то есть рН менее чем 2, при использовании ВЭЖХ, что способствует определению отдельных антоцианинов. Этот способ позволяет отделить молекулы антоцианина для определения, а не получения фракций со смесями антоцианинов.
[0022] В WO 2004/012526 описывается раствор синего красителя из антоцианинов краснокочанной капусты при рН 7,9, который используют в сахарном сиропе для покрытия ядер кондитерских изделий. Антоцианины краснокочанной капусты не выделяют во фракции.
[0023] В предшествующем уровне техники отсутствуют примеры антоцианин-содержащих красителей, содержащих фракции молекул антоцианина, выделенных из соков и экстрактов антоцианин-содержащих овощей и плодов при заданном рН, исходя из разницы в заряде и полярности молекул. Дополнительно, не описаны фракции антоцианина, обеспечивающие отличающиеся характеристики цвета, иные, чем таковые, обеспеченные источником из соков и экстрактов. В частности, в предшествующем уровне техники не описываются натуральные синие антоцианин-содержащие красители, обеспечивающие характеристики цвета, аналогичные таковым, обеспеченным синтетическим синим красителем FD&C Blue No. 1.
[0024] Продолжает существовать потребность в широкой палитре красителей, доступных для окрашивания пищевых продуктов. В частности, продолжает существовать потребность в натуральных красителях, обеспечивающих характеристики цвета, аналогичные таковым, обеспеченным синтетическими красителями, в частности FD&C Blue No. 1. Фракции антоцианина, полученные из соков и экстрактов овощей и плодов, являются потенциальным источником этих натуральных красителей.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0025] Настоящее изобретение относится к натуральным синим антоцианин-содержащим красителям, обеспечивающим характеристики цвета, аналогичные таковым синтетического синего красителя FD&C Blue No. 1. Натуральный синий антоцианин-содержащий краситель получают селективным выделением антоцианинов из соков и экстрактов антоцианин-содержащих овощей и плодов при заданном рН, исходя из разницы в заряде и полярности молекул антоцианинов.
[0026] В одном варианте выполнения настоящего изобретения натуральный синий антоцианин-содержащий краситель получают из овощей, плодов или их комбинаций, и он содержит селективно выделенную смесь антоцианинов, где краситель, когда он находится в форме водного раствора при рН 8,0, имеет максимальное поглощение от 615 нм до 635 нм. Селективно выделенная смесь антоцианинов представляет собой подсовокупность, то есть фракцию или комбинацию фракций смеси антоцианинов, которые естественным образом присутствуют в овощах или плодах и, следовательно, отличается от смесей антоцианинов, существующих в природе.
[0027] Также настоящее изобретение относится к натуральным зеленым красителям, полученным смешиванием натурального синего антоцианин-содержащего красителя с натуральным желтым красителем. Предпочтительным натуральным желтым красителем является куркума или куркумин.
[0028] Также настоящее изобретение относится к съедобному продукту, окрашенному натуральным антоцианин-содержащим синим красителем. Съедобный продукт также может включать натуральный желтый краситель с получением съедобного продукта, окрашенного в зеленый цвет.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0029] На Фиг. 1 приведены два вида в перспективе трехмерного изображения характеристик цвета, обеспеченных FD&C Blue No. 1, в CIE 1976 CIELAB L*a*b* цветовом пространстве, как функции концентрации в водном растворе.
[0030] На Фиг. 2 приведены два вида в перспективе трехмерного изображения характеристик цвета, обеспеченных FD&C Blue No. 1, в CIE 1976 CIELCH L*C*h° цветовом пространстве, как функции концентрации в водном растворе.
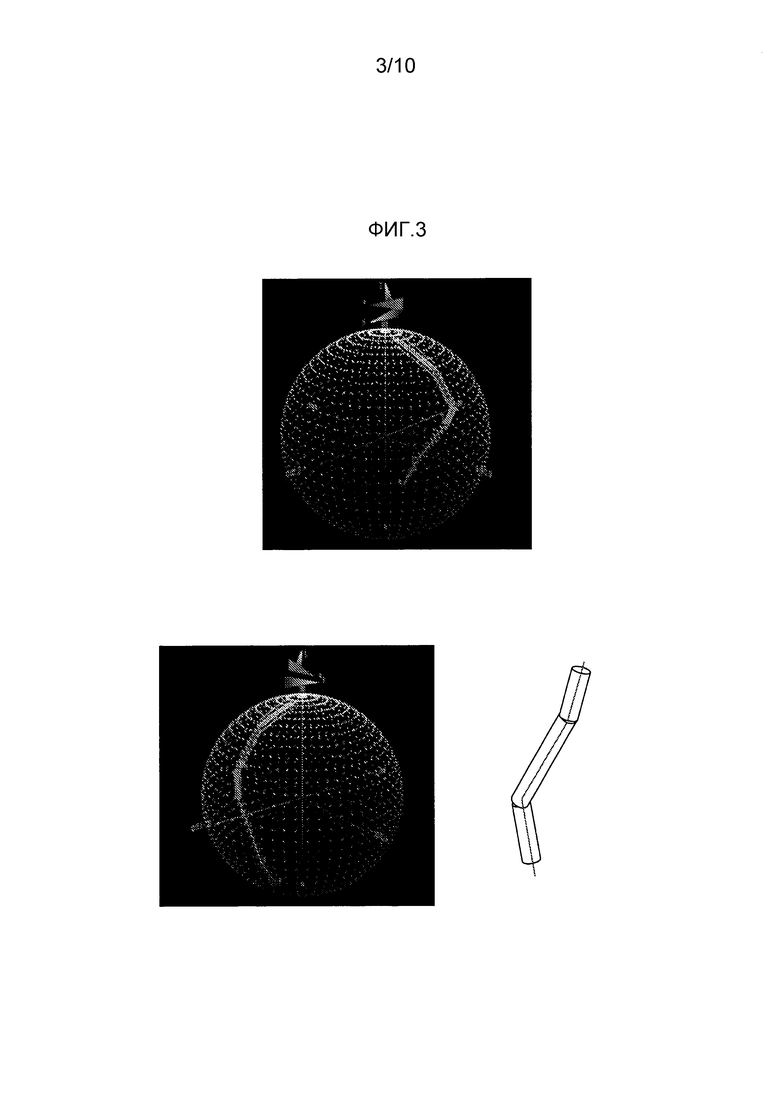
[0031] На Фиг. 3 представлены два вида в перспективе области в CIE 1976 CIELAB L*a*b* цветовом пространстве цветов, отличающихся от цветов, обеспеченных FD&C Blue No. 1, при ΔΕ 3 или менее и иллюстрация сегментированных туннелей/очерченных сегментирующей линий по данным цветового пространства.
[0032] На Фиг. 4 приведено сравнение цветов, обеспеченных экстрактами плодов и овощей, в водном растворе при различных показателях рН.
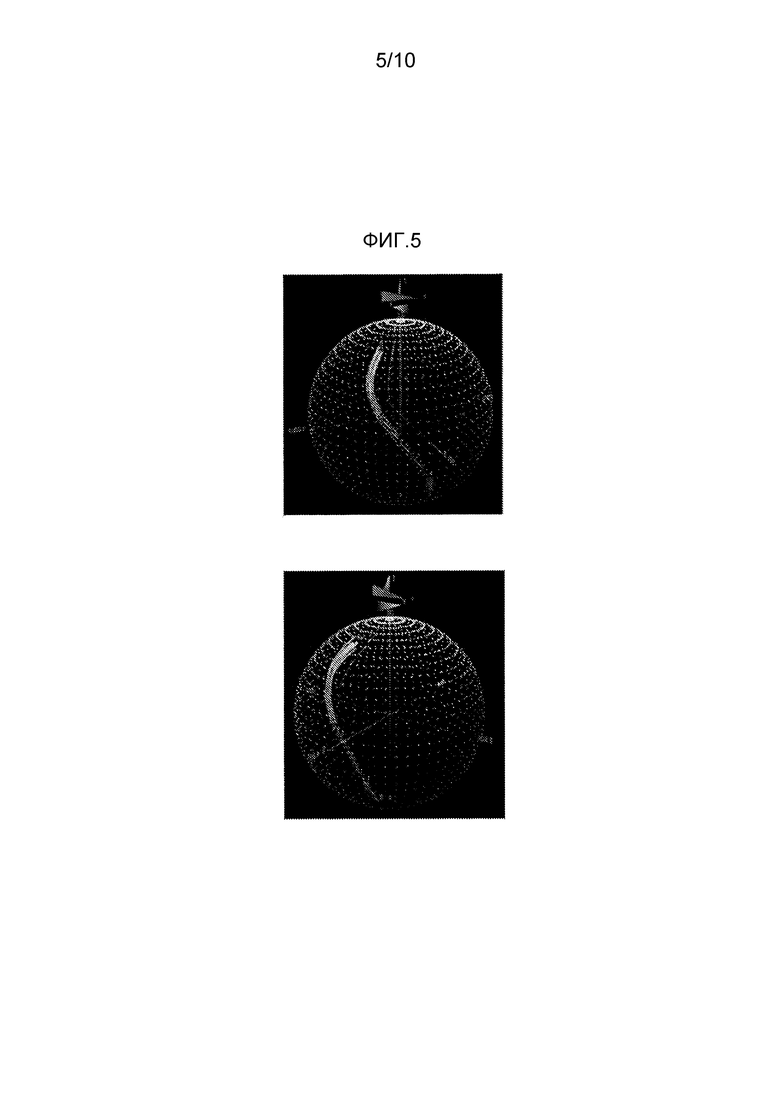
[0033] На Фиг. 5 приведены два вида в перспективе трехмерного изображения характеристик цвета, обеспеченных FD&C Blue No. 1, в CIE 1976 CIELAB L*a*b* цветовом пространстве, как функции концентрации в водном растворе наряду с областью цветов, отличающихся от цветов, обеспеченных FD&C Blue No. 1, при ΔΕ 3 или менее, и также приведены два вида в перспективе трехмерного изображения характеристик цвета, обеспеченных синим из спирулины, как функции концентрации в водном растворе (белая линия ближе к х-оси).
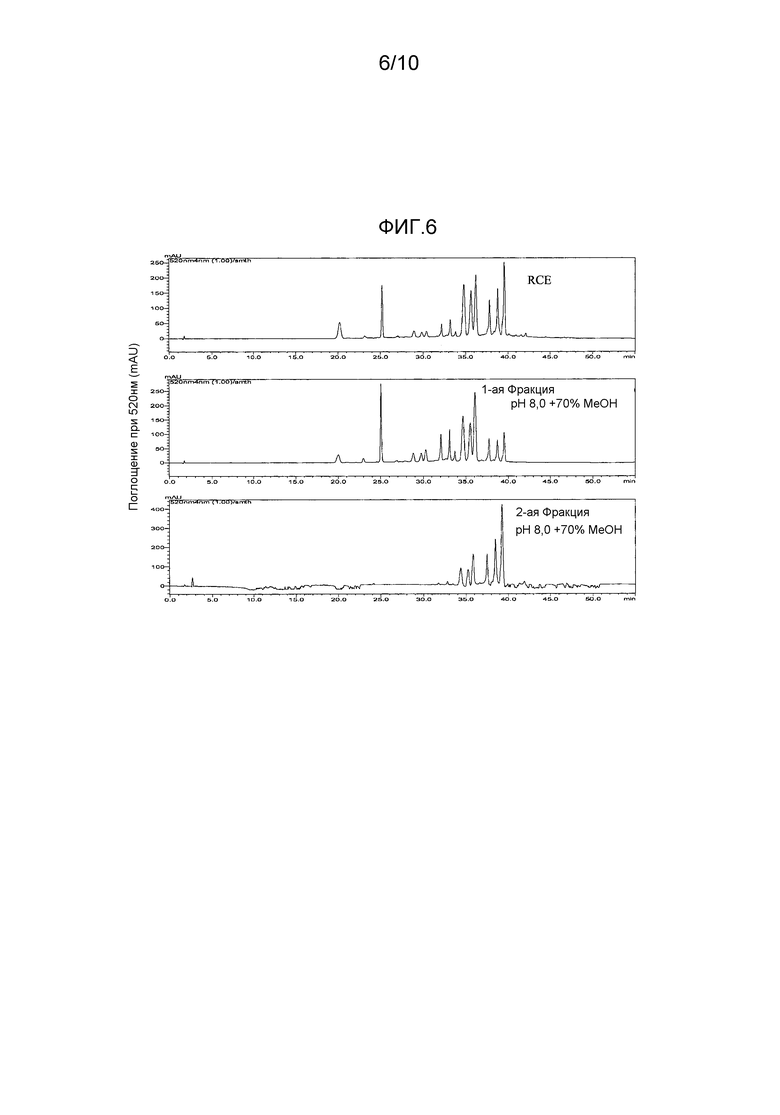
[0034] На Фиг. 6 приведены ВЭЖХ хроматограммы при 520 нм раствора экстракта краснокочанной капусты и двух фракций, выделенных из раствора экстракта краснокочанной капусты при использовании колонки с сильной катионообменной смолой.
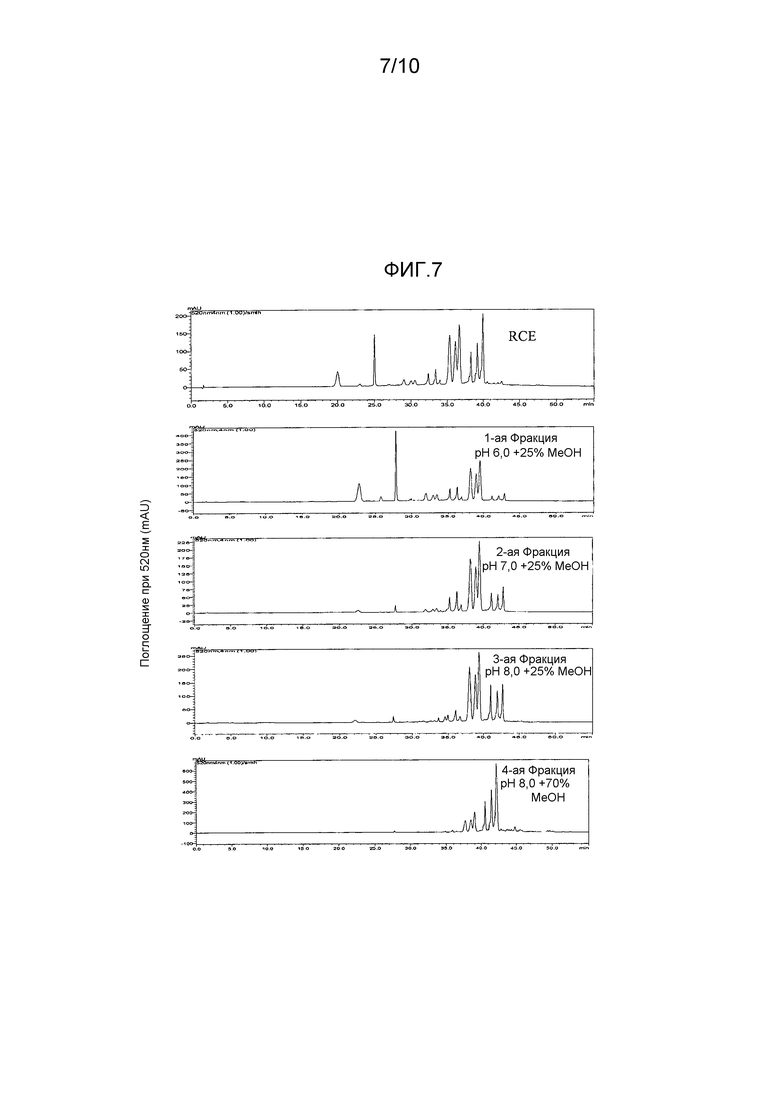
[0035] На Фиг. 7 приведены ВЭЖХ хроматограммы при 520 нм раствора экстракта краснокочанной капусты и четырех фракций, выделенных из раствора экстракта краснокочанной капусты при использовании колонки с сильной катионообменной смолой.
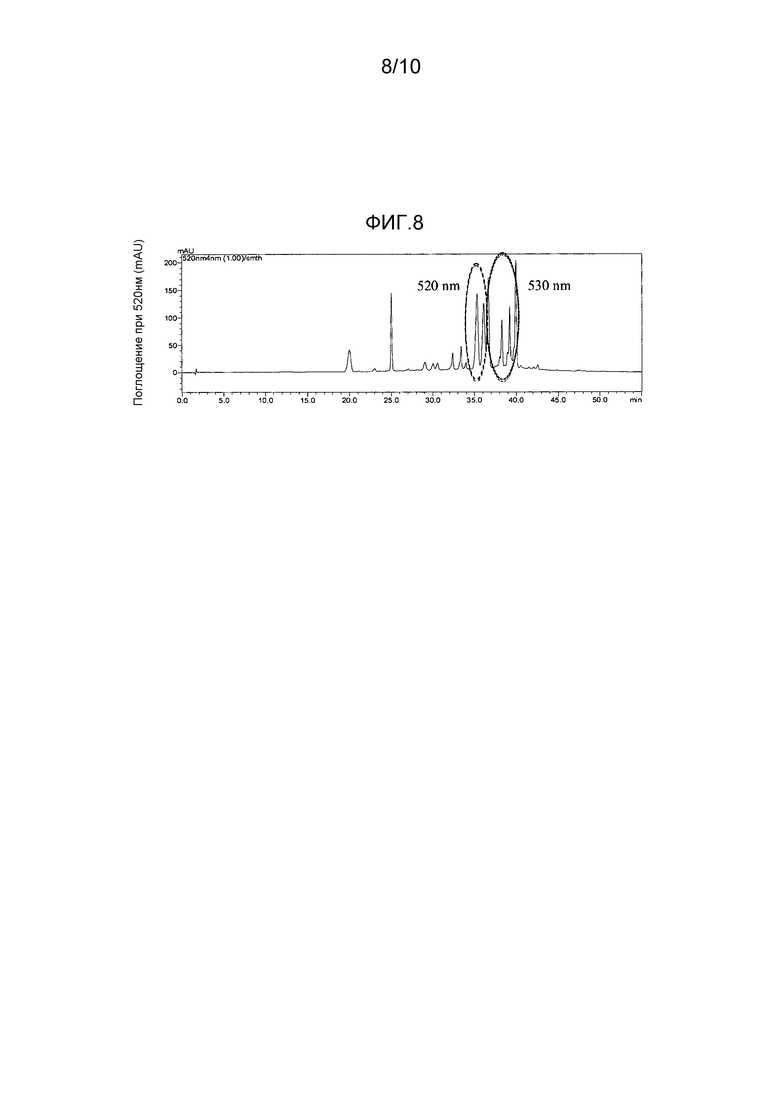
[0036] На Фиг. 8 приведены ВЭЖХ хроматограммы при 520 нм раствора экстракта краснокочанной капусты, дающие две группы пиков, как целевые для выделения. Эти две группы пиков выделили как «520-нм Фракция» и «530-нм Фракция».
[0037] На Фиг. 9 приведено визуальное сравнение цветов, обеспеченных при использовании 520-нм и 530-нм Фракций при различных показателях рН. Также Фиг. 9 позволяет провести визуальное сравнение цветов, обеспеченных при использовании 520-нм и 530-нм Фракций с цветом дражированного сахарным сиропом окрашенным FD&C Blue No. 1 кондитерского изделия.
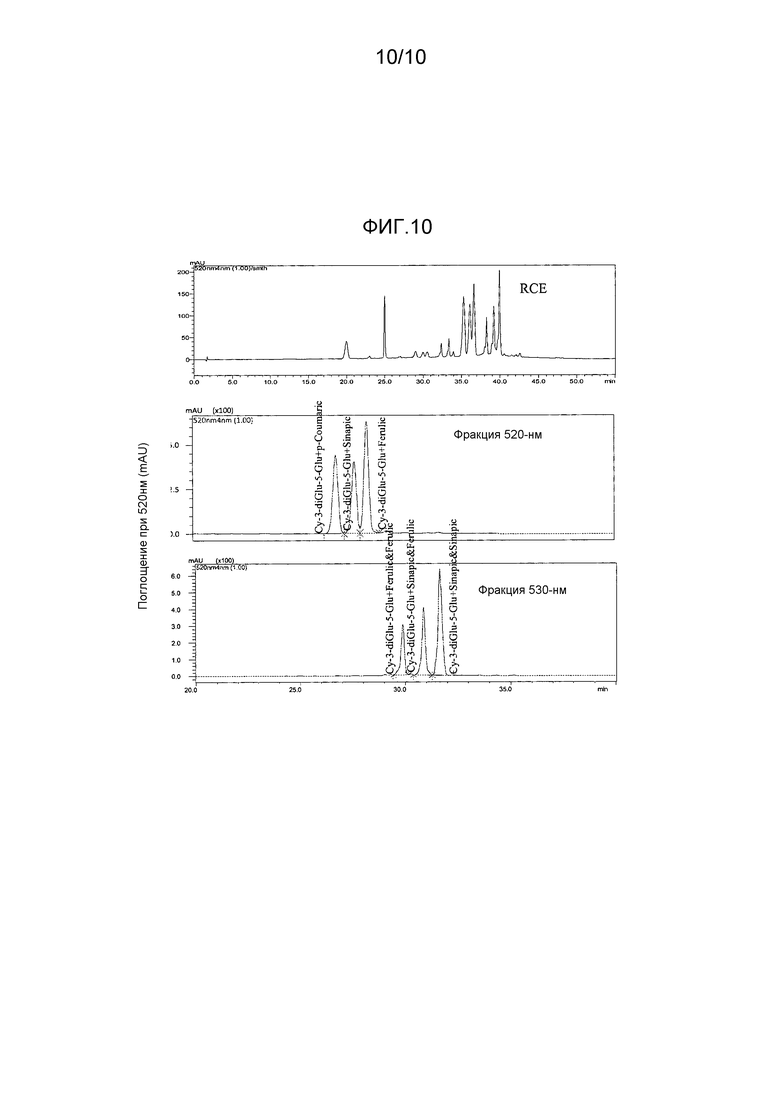
[0038] На Фиг. 10 приведены ВЭЖХ хроматограммы при 520 нм раствора экстракта краснокочанной капусты и двух фракций, выделенных из раствора экстракта краснокочанной капусты при использовании полупрепаративной ВЭЖХ. На Фиг. 10 показано, что каждая из 520-нм и 530-нм Фракций содержит три различных соединения антоцианина и определяет наличие функциональных групп и сахаров на соединениях антоцианина.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0039] В настоящее время соки и экстракты антоцианин-содержащих овощей и плодов используют в качестве натуральных съедобных красителей и для получения красителей, в частности натуральных красителей красного, фиолетового и синего цветовых оттенков. Соки и экстракты содержат смесь всех молекул антоцианинов, естественным образом присутствующих в овощных и плодовых источниках, вместе со множеством соединений других классов. Следовательно, доступные в настоящее время антоцианин-содержащие красители ограничены цветами, связанными со смесями антоцианинов, которые естественным образом присутствуют в овощных и плодовых источниках. Настоящее изобретение относится к натуральным синим антоцианин-содержащим красителям, которые содержат антоцианины, селективно выделенные из естественным образом присутствующей в природе смеси, с обеспечением, таким образом, характеристик цвета, аналогичных таковым, обеспеченным синтетическим синим красителем FD&C Blue No. 1.
[0040] В одном аспекте настоящее изобретение относится к выделению фракций молекул антоцианина из соков и экстрактов антоцианин-содержащих овощей и плодов с получением красителей, обеспечивающих специфические целевые характеристики цвета, аналогичные таковым, обеспеченным синтетическим синим красителем FD&C Blue No. 1. Используемый в описании настоящей патентной заявки термин обеспечивающий характеристики цвета «аналогичные» FD&C Blue No. 1 означает, что цвет более близок к характеристикам цвета, чем у любого другого натурального красителя, такого как, например, синий из спирулины.
[0041] Авторы настоящей патентной заявки обнаружили, что выделение антоцианинов при использовании растворителя при заданном рН и разницы в полярности молекул антоцианина позволяет получить фракции, содержащие смеси антоцианинов, обеспечивающие характеристики цвета аналогичные таковым, обеспеченным синтетическим синим красителем FD&C Blue No. 1. Каждый источник антоцианина содержит различные количества множества различных молекул антоцианинов, и каждая молекула может существовать в равновесии с одной или более вторичной структурой. Они могут отличаться по заряду и/или полярности от других молекул антоцианина и их равновесных молекулярных структур. Проводя выделение на основе разницы в заряде и полярности молекул антоцианина при заданном рН, авторы настоящего изобретения смогли выделить фракции антоцианинов с различными спектральными характеристиками из комплексной смеси антоцианинов. Спектральные характеристики фракций отличаются и не очевидны из спектральных характеристик комплексной смеси антоцианинов, присутствующих в соке или экстракте. Авторы настоящего изобретения обнаружили, что выявленные фракции антоцианина обеспечивают характеристики цвета, более близкие к таковым, обеспеченным синтетическим FD&C Blue No. 1, чем обеспеченные любым известным натуральным синим красителем, включая синий из спирулины.
[0042] Сок антоцианин-содержащих овощей или плодов может быть получен прессованием с выделением жидкости из плодов или овощей. Экстракт антоцианин-содержащих овощей или плодов может быть получен промывкой измельченных плодов или овощей растворителем (например, вода, спирт). Соки и экстракты содержат антоцианины наряду с другими естественным образом присутствующими соединениями, включая, например, углеводы, кислоты, флавоноиды, ионы металлов, фенольные кислоты, сложные эфиры фенольных кислот и витамины. Используемый в описании настоящей патентной заявки термин «сок или экстракт овощей или плодов» является эквивалентом списка терминов «овощной сок, сок плодов, экстракт овощей или экстракт плодов» и включает в объем понятия соки и экстракты, включая, например, восстановленные соки и экстракты, дезодорированные соки и экстракты, и соки и экстракты, подвергшиеся другим видам технологической обработки для удаления специфических или широких классов соединений.
[0043] Используемый в описании настоящей патентной заявки термин «Фракционирование» относится к процессу селективного отделения и выделения части антоцианинов из комплексной смеси антоцианинов в соке или экстракте антоцианин-содержащих овощей или плодов. Синий антоцианин-содержащий краситель по настоящему изобретению может быть получен из сока или экстракта антоцианин-содержащих овощей или плодов и обеспечивает синий цветовой оттенок при высоких показателях рН. В некоторых вариантах выполнения настоящего изобретения синий антоцианин-содержащий краситель может быть получен из краснокочанной капусты, фиолетового сладкого картофеля, синего картофеля, фиолетовой моркови или черной моркови или их комбинаций.
[0044] Используемый в описании настоящей патентной заявки термин «фракция» относится к фракционированию продукта. Используемый в описании настоящей патентной заявки термин «фракция антоцианина» относится к смеси антоцианинов, отличающейся от смеси антоцианинов в антоцианин-содержащем соке или экстракте, из которого была выделена фракция. Фракции антоцианина выделяют из смеси сока или экстракта при заданном рН, исходя из разницы в заряде и полярности различных присутствующих молекул антоцианина.
[0045] Используемый в описании настоящей патентной заявки термин «заданный рН» относится к рН 2 или выше, например рН от около 2 до около 9, в обоих контекстах, и в контексте выделения, и в контексте проведения оценки характеристик цвета антоцианинов. В других вариантах выполнения настоящего изобретения рН может составлять рН 3 или выше, 4 или выше, 5 или выше, 6 или выше, или 7 или выше, например рН в одном из следующих соответствующих пределах, то есть от около 3 до около 9, от около 4 до около 9, от около 5 до около 9, от около 6 до около 9 или от около 7 до около 9.
[0046] В одном варианте выполнения настоящее изобретение относится к натуральному синему красителю, содержащему антоцианин, полученный из овощей или плодов или их комбинаций, содержащий селективно выделенную смесь антоцианинов, где краситель в форме водного раствора при рН 8,0 имеет максимальное поглощение от 615 нм до 635 нм. Натуральный синий антоцианин-содержащий краситель может содержать антоцианины, селективно выделенные при использовании ионообменной колонки, исходя из разницы в заряде и полярности молекул антоцианина.
[0047] Используемый в описании настоящей патентной заявки термин «максимальное поглощение», «лямбда max» или 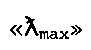 относится к длине волны в нанометрах, при которой максимальная фракция света поглощается веществом. Как правило, максимальное поглощение может быть использовано как собственное значение для сравнения веществ, прошедших измерение при использовании УФ/Видимой области спектрофотометра или колориметра.
относится к длине волны в нанометрах, при которой максимальная фракция света поглощается веществом. Как правило, максимальное поглощение может быть использовано как собственное значение для сравнения веществ, прошедших измерение при использовании УФ/Видимой области спектрофотометра или колориметра.
[0048] Ссылка на «FD&C Blue No. 1» включает различные названия, присвоенные идентичному синтетическому синему красителю, Brilliant Blue FCF и Е133 согласно Европейской Комиссии (European Commission). Лямбда max FD&C Blue No. 1 составляет 630 нм.
[0049] Используемый в описании настоящей патентной заявки термин «краситель» относится к любому веществу, придающему цвет за счет поглощения или рассеяния света при различной длине волны. Используемый в описании настоящей патентной заявки термин «натуральный краситель» относится к красителю, который существует в природе или его получают из природного источника. Используемый в описании настоящей патентной заявки термин «синий краситель» относится к красителю, отражающему свет с длиной волны в области 450-495 нанометров и имеющему максимальное поглощение от 615 до 635 нанометров. Используемый в описании настоящей патентной заявки термин «натуральный антоцианин-содержащий краситель» относится к натуральному красителю, содержащему антоцианины, полученные из растений.
[0050] Натуральный антоцианин-содержащий краситель представляет собой композицию, которая может содержать только антоцианины, которые были селективно выделены (например, выделенная смесь) или также может содержать другие растительные компоненты, носители, например воду и/или инертные наполнители, известные для применения с красителями. Композиция может быть в форме твердого вещества, например порошка, или жидкого раствора, например водного раствора.
[0051] В другом варианте выполнения настоящее изобретение относится к натуральному синему антоцианин-содержащему красителю, полученному из овощей, фруктов или их комбинаций, содержащему селективно выделенную смесь антоцианинов, где краситель в форме водного раствора при рН 8,0 в концентрации от 1 м.д. до 1000 м.д. (миллионных долей) имеет параметр h° от 209 до 290. В другом варианте выполнения настоящего изобретения параметр h° может составлять от около 225 до 250.
[0052] Используемый в описании настоящей патентной заявки термин «цветовой тон» относится к свойству цвета, которое дает название цвета, как таковое, например, красный, оранжево-красный, синий, фиолетовый и тому подобное.
[0053] Используемый в описании настоящей патентной заявки термин «цветность» относится к свойству цвета, указывающему чистоту цвета, где более высокая цветность ассоциируется с более чистым цветовым тоном и меньшим разбавлением белым, серым или черным.
[0054] Используемый в описании настоящей патентной заявки термин «насыщенность» относится к свойству цвета, указывающему на светлоту или темноту цвета, где более высокий показатель ассоциируется с более высокой светлотой.
[0055] Используемые в описании настоящей патентной заявки термины «цвет» и «характеристики цвета» взаимозаменяемы и включают такие свойства цвета, как цветовой тон, цветность и насыщенность, и для описания этих свойств используют параметры системы цветовой модели, такие как показатели Commission Internationale del'Eclairage CIE 1976 CIELAB цветового пространства L*a*b* и показатели CIELCH цветового пространства L*C*h°. Модели цвета CIELAB и CIELCH обеспечивают более равномерное восприятие цветовых пространств по сравнению с более ранними моделями цветами. Красители анализируют при использовании спектрофотометра, и показатели CIELAB L*a*b* и CIELCH L*C*h° рассчитывают по спектральным данным. Показатели L*a*b* и L*C*h° обеспечивают средства представления характеристик цвета и позволяют оценить величину разницы между двумя цветами. Приведенные в описании настоящей патентной заявки показатели CIELAB L*a*b* и CIELCH L*C*h° во всех случаях, если не указано иное, рассчитывают по спектральным данным, полученным при использовании спектрофотометра Konica Minolta Spectrophotometer CM-3500d, работающего в режиме светопропускания со стандартным источником света CIE Standard Illuminant D65 и углом обзора 10 градусов.
[0056] Показатели L*a*b* состоят из системы координат, определенных трехмерной системой координат Cartesian. L* представляет координату насыщенности или светлости. L* обеспечивает шкалу светлости от черного (0 L* единиц) до белого (100 L* единиц) на вертикальной оси, а* и b* представляют координаты, относящиеся к обоим, и цветовому тону и цветности, а* обеспечивает шкалу от зелености (- а* единиц) до красноты (+а* единиц) с нейтральным в центральной точке (0 а* единиц) на горизонтальной оси, b* обеспечивает шкалу от синевы (- b* единиц) до желтизны (+b* единиц) с нейтральным в центральной точке (0 b* единиц) на второй горизонтальной оси, перпендикулярной первой горизонтальной оси. Три оси пересекаются, где L* имеет показатель 50, и а* и b* оба равны нулю.
Показатели L*C*h° состоят из системы координат, определенных трехмерной цилиндрической системой координат. L* представляет координату насыщенности или светлости. L* обеспечивает шкалу светлости от черного (0 L* единиц) до белого (100 L* единиц) на продольной оси. h° представляет координату цветового тона. h° определяют как угол от 0° до 360°, движущийся против часовой стрелки вокруг оси L*. Чистый красный имеет угол цветового тона 0°, чистый желтый имеет угол цветового тона 90°, чистый зеленый имеет угол цветового тона 180°, и чистый синий имеет угол цветового тона 270°. Координата С* представляет цветность и определяется как расстояние по радиусу от оси L*. С* обеспечивает шкалу от ахроматического, то есть нейтрального белого, серого или черного на оси L* (0 С* единиц) до более чистого цветового тона при движении координат в направлении от оси L* (вплоть до 100 или более С* единиц). С* и h° могут быть рассчитаны из а* и b* при использовании Уравнений 1 и 2:
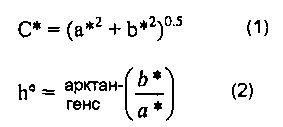
[0058] «Дельта Е», «ΔEab*» или «ΔЕ» представляют измерение величины полного цветового различия между двумя цветами, представленными в CIELAB L*a*b* цветовом пространстве. Сообщается, что наблюдатель не может различить наблюдаемый цвет при любой разнице между двумя цветами, когда ΔЕ составляет около 2,3 или менее ΔЕ двух различных цветов с показателями L*a*b*L*1a*1b*1 и L*2a*2b*2, рассчитывают при использовании Уравнения 3:
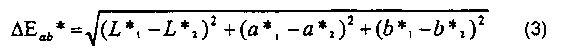
[0059] В Таблице 1 приведены показатели CIELAB L*a*b* и CIELCH L*C*h° FD&C Blue No. 1 при семи различных концентрациях в водном растворе.
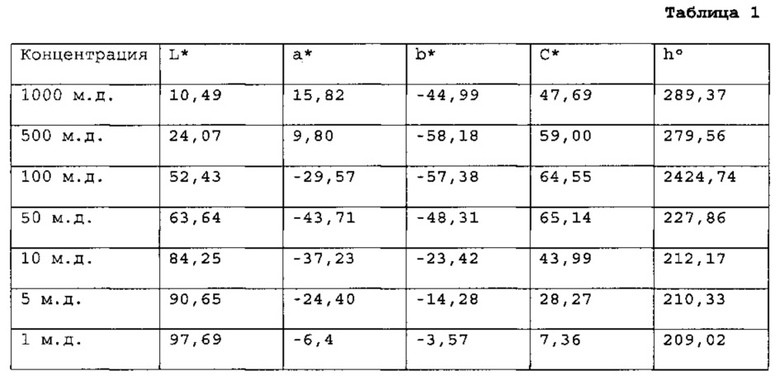
[0060] Эти показатели L*a*b* и L*С*h°°для FD&C Blue No. 1 представляют идеальные целевые показатели для альтернативного FD&C Blue No. 1 натурального синего красителя. Предполагается, что натуральные синие красители с показателями L*a*b*, которые попадают в ΔЕ 2,3 или менее от этих целевых показателей, обеспечивают характеристики цвета в достаточной степени схожие с таковыми, обеспеченными FD&C Blue No. 1, чтобы человеческий глаз не мог уловить различие в цвете, обеспеченном натуральным красителем, по сравнению с синтетическим. Очевидно, что чем ближе показатели L*a*b* натурального синего красителя к целевым показателям синтетического (то есть с получением на выходе меньшего показателя ΔЕ), тем лучше будет натуральный синий краситель заменять FD&C Blue No. 1 в пищевых применениях.
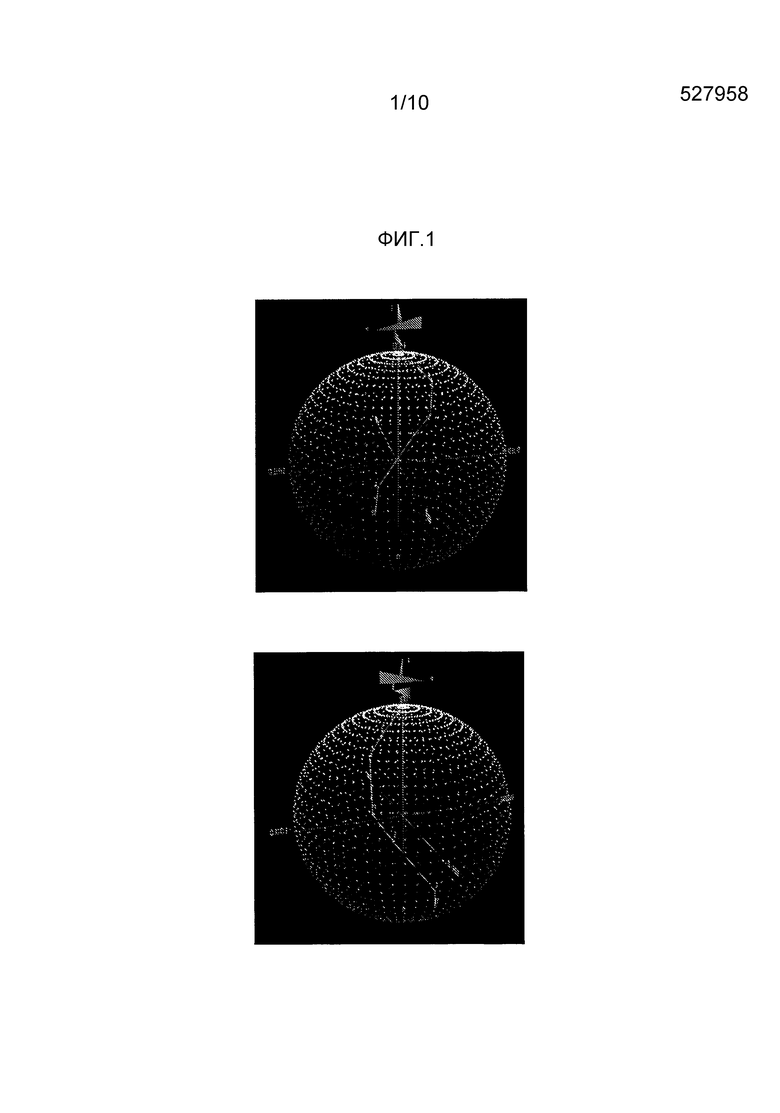
[0061] На Фиг. 1 приведены два вида в перспективе трехмерного изображения показателей L*a*b* для водных растворов FD&C Blue No. 1 в семи концентрациях, приведенных в Таблице 1, соединенных линией в сегменты. На Фиг. 2 приведены два вида в перспективе трехмерного изображения показателей L*C*h° для водных растворов FD&C Blue No. 1 в семи концентрациях, приведенных в Таблице 1, соединенных линией в сегменты.
[0062] Для получения изображения характеристик цвета, обеспеченных FD&C Blue No. 1 при любой концентрации в показателях L*a*b* и L*C*h° цветового пространства, могут быть построены математические модели. Например, характеристики цвета могут быть представлены моделью, очерченной в сегмент линией, связывающей точечные значения L*a*b* или L*C*h° Таблицы 1. Линия (L), соединяющая две точки (Р1 и Р2), представляющая две различных концентрации FD&C Blue No. 1 в L*a*b* пространстве, может быть рассчитана при использовании следующего Уравнения 4:
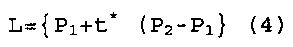
где P1 представляет (L*1, a*1, b*1); Р2 представляет (L*2, а*2, b*2); и t представляет любое неотрицательное вещественное число.
[0063] Соответственно, очерченная в сегмент линией модель для FD&C Blue No. 1 в L*a*b* цветовом пространстве может быть интерполирована, исходя из показателей L*a*b* для семи различных точек концентраций при использовании Уравнения 4, как следующее:
Для концентраций от 500 до 1000 м.д., 0<t<1:

Для концентраций от 100 до 500 м.д., 0<t<1:

Для концентраций от 50 до 100 м.д., 0<t<1:
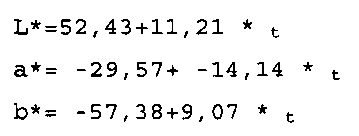
Для концентраций от 10 до 50 м.д., 0<t<1:

Для концентраций от 5 до 10 м.д., 0<t<1:
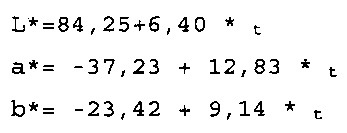
Для концентраций от 1 до 5 м.д., 0<t<1:

Очерченная в сегмент линией модель для FD&C Blue No. 1 в L*a*b* пространстве приведена на Фиг. 1.
[0064] Дополнительно, цвета с показателями L*a*b*, попадающие в специфические пределы ΔЕ FD&C Blue No. 1 модели, могут быть математически смоделированы в L*a*b* цветовом пространстве. На Фиг. 3 видно, что выбор специфического показателя ΔЕ, например 3, в отношении FD&C Blue No. 1 и построение графика ΔЕ в L*a*b* цветовом пространстве в результате приводит к получению туннелеподобной структуры вокруг FD&C Blue No. 1 модели. Следует отметить, что любой цвет с показателем ΔЕ около 2,3 или менее из любой точки на модели не будет отличим от цвета, обеспеченного FD&C Blue No. 1.
[0065] Для определения, попадает ли точка (Х0) в L*a*b* цветовом пространстве в специфический показатель ΔЕ FD&C Blue No. 1 модели, должно быть рассчитано минимальное расстояние dmin между точкой и моделью (представлено линией сегмента Х1-Х2).
[0066] Для расчета d может быть использовано Уравнение 5,
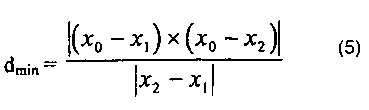
где х обозначает точку пересечения двух векторов, и вертикальные диаграммы определяют величину векторного выражения.
В случае, когда показатель dmin составляет менее чем или равное выбранному показателю ΔЕ, точка в L*a*b* цветовом пространстве попадает в специфический показатель ΔЕ FD&C Blue No. 1 модели.
[0067] Например, может быть определено, обеспечивает ли синий из спирулины цвет с ΔЕ 12 или менее сравнимый с цветом, обеспеченным FD&C Blue No. 1. В Таблице 2 приведены характеристики цвета, обеспеченные синим из спирулины - известным натуральным синим красителем при двух различных концентрациях в водном растворе:
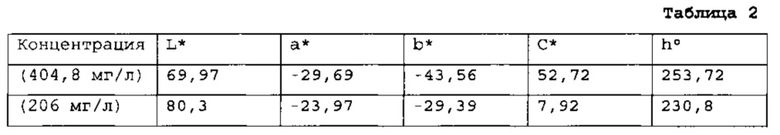
Х0 для 404,8 мг/л раствора синего из спирулины в L*a*b* цветовом пространстве составляет:
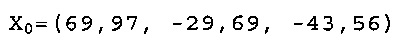
Х0 для 206 мг/л раствора синего из спирулины в L*a*b* цветовом пространстве составляет:
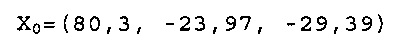
X1 и Х2 представляют две точки FD&C Blue No. 1 модели при концентрациях 10 м.д. и 50 м.д. в водном растворе соответственно:
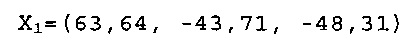
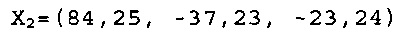
dmin, рассчитанное при использовании Уравнения 5, составляет 12,4 для 404,8 мг/л раствора синего из спирулины и 14,4 для 206 мг/л раствора синего из спирулины. Следовательно, раствор синего из спирулины не обеспечивает цвет с ΔЕ 12 или менее сравнимый с цветом, обеспеченным FD&C Blue No. 1 в водном растворе, как измерено по очерчивающей сегмент линии, определенной показателями L*a*b* для 10 м.д. и 50 м.д. FD&C Blue No. 1 в водном растворе.
[0068] Спектральные характеристики множества различных растворов синего из спирулины приведены в Таблице 3.
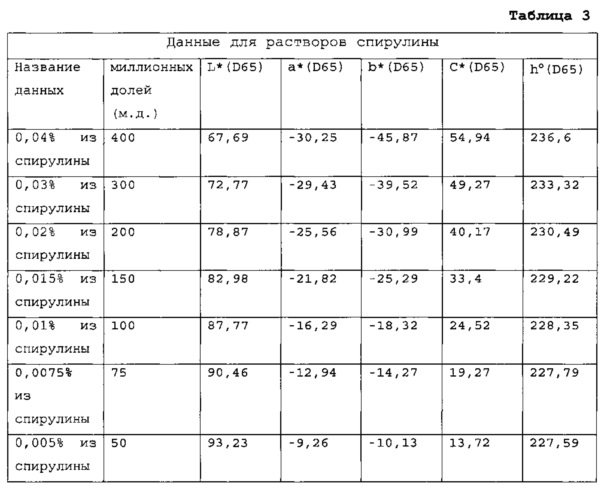
Данные для синего из спирулины приведены в виде графика цвета на Фиг. 5 по сравнению с данными для FD&C Blue No. 1.
[0069] Различия между характеристиками цвета, обеспеченными синим из спирулины и FD&C Blue No. 1, представлены на Фиг. 5. На Фиг. 5 приведена очерченная в сегмент линией модель характеристик цвета, обеспеченных FD&C Blue No. 1 в L*a*b* цветовом пространстве при концентрациях от 1 м.д. до 1000 м.д. в водном растворе, с моделью, окруженной туннелем, представляющим область цветов, которые отличаются от цветов, обеспеченных Blue No. 1, при ΔΕ 3 или менее. Также на Фиг. 5 для сравнения приведена очерченная в сегмент линией модель характеристик цвета, обеспеченных синим из спирулины в L*a*b* цветовом пространстве в концентрациях от 50 м.д. до 400 м.д. в водном растворе. Модель синего из спирулины не пересекает Blue No. 1 модель или не не связана с туннелем в какой-либо точке в L*a*b* цветовом пространстве.
[0070] Настоящее изобретение относится к натуральным синим антоцианин-содержащим красителям, полученным из овощей, плодов или их комбинаций, содержащим селективно выделенную смесь антоцианинов, где по меньшей мере одна концентрация красителя в форме водного раствора при рН 8,0 обеспечивает характеристики цвета с показателем ΔΕ 12 или менее по сравнению с характеристиками цвета, определенными очерчивающей сегмент линией, определенной показателями L*a*b* 5 м.д. и 10 м.д. FD&C Blue No. 1 в водном растворе. В других вариантах выполнения настоящего изобретения показатель ΔΕ может составлять менее чем 11, 10, 9, 8, 7, 6, 5, 4 или 3. Если требуется, также по меньшей мере одна концентрация красителя может быть измерена по множеству очерчивающих в сегмент линий, определенных различными концентрациями FD&C Blue No. L в водном растворе, например 1 и 5 м.д., 10 м.д. и 50 м.д., 50 м.д. и 100 м.д., 100 м.д. и 500 м.д., 500 м.д. и 1000 м.д., или любая комбинация, выбранная из них. Например, хотя и не требуется, по меньшей мере одна концентрация красителя может быть определена как имеющая показатель ΔΕ 12 или менее для первой очерчивающей сегмент линии при от 5 м.д. до 10 м.д., показатель ΔΕ 8 или менее для очерчивающей сегмент линии при от 1 до 5 м.д. и показатель ΔΕ 12 или менее для очерчивающей сегмент линии при от 10 м.д. до 50 м.д. Однако если показатель ΔΕ используют для описания красителя по настоящему изобретению, то для определения красителя требуется только одна очерчивающая в сегмент линия.
[0071] Хотя считается, что синий из спирулины, являющийся натуральным красителем, обеспечивает самое близкое соответствие цвета к FD&C Blue No. 1, натуральный синий антоцианин-содержащий краситель, полученный из овощей, плодов или их комбинаций, содержащий селективно выделенную смесь антоцианинов, имеет лучшее совпадение цвета. В частности, когда по меньшей мере одна концентрация красителя присутствует в водном растворе при рН 8,0, то водный раствор красителя обеспечивает характеристики цвета, совпадающие с FD&C Blue No. 1 очерчивающей сегмент линией, исходя из серий водных растворов с различными концентрациями FD&C Blue No. 1, определенными в L*a*b* цветовом пространстве, где соответствие означает, что по меньшей мере одна концентрация красителя в водном растворе при рН 8,0 имеет показатель ΔΕ, измеренный по FD&C Blue No. 1 очерчивающей сегмент линии, который по меньшей мере на одну единицу меньше, чем показатель ΔΕ для синего из спирулины очерчивающей сегмент линии, определенной в том же самом L*a*b* цветовом пространстве, исходя из серий водных растворов с различными концентрациями синего из спирулины, измеренного по FD&C Blue No. 1 очерчивающей сегмент линии. В других вариантах выполнения настоящего изобретения показатель ΔΕ по меньшей мере одной концентрации красителя в водном растворе при рН 8,0, измеренный по FD&C Blue No. 1 очерчивающей сегмент линии, составляет по меньшей мере на 2, 3, 4, 5 или 6 единиц менее, чем показатель ΔΕ для синего из спирулины очерчивающей сегмент линии, измеренный по FD&C Blue No. 1 очерчивающей сегмент линии. В другом варианте выполнения настоящего изобретения показатель ΔΕ по меньшей мере одной концентрации красителя в водном растворе при рН 8,0, измеренный по FD&C Blue No. 1 очерчивающей сегмент линии, составляет по меньшей мере на 7, 8, 9, 10 или 11 единиц менее, чем показатель ΔΕ для синего из спирулины очерчивающей сегмент линии, измеренной по FD&C Blue No. 1 очерчивающей сегмент линии.
[0072] Провели анализ экстрактов различных антоцианин-содержащих плодов и овощей для определения источника антоцианинов, который позволяет обеспечить характеристики цвета, самые близкие к таковым, обеспеченным синтетическим синим красителем FD&C Blue No. 1. На Фиг. 4 приведено сравнение шести различных коммерчески доступных экстрактов краснокочанной капусты, фиолетового сладкого картофеля, черной моркови, красной редиски, фиолетовой кукурузы и винограда в водном растворе при пяти различных показателях рН. При визуальном сравнении видно, что антоцианины из красной редиски, фиолетовой кукурузы и винограда не обеспечивают оттенки синего цвета в водном растворе при любом рН от рН 6 до рН 8. Антоцианины из краснокочанной капусты, фиолетового сладкого картофеля и черной моркови обеспечивают оттенки синего цвета в водном растворе при более высоких значениях предела.
[0073] Любой сок или экстракт антоцианин-содержащих плодов или овощей, обеспечивающий оттенки синего цвета при показателях рН 4 или выше, может быть использован в качестве источника антоцианинов. В некоторых вариантах выполнения настоящего изобретения фракцию антоцианина выделяют из экстракта краснокочанной капусты, фиолетового сладкого картофеля, синего картофеля, фиолетовой моркови или черной моркови, или их комбинаций. Краснокочанная капуста демонстрирует хорошие результаты и легко доступна.
[0074] Отобранные фракции содержащих антоцианин соков и экстрактов плодов и овощей могут быть выделены при использовании ионообменной колонки или колонки для полупрепаративной ВЭЖХ. Подходящая ионообменная среда включает катион- и ионообменную среду. Подходящие колонки для полупрепаративной ВЭЖХ включают С-18 колонки. В одном варианте выполнения настоящего изобретения ионообменную колонку активируют растворителем, подходящим для ионообменной среды, перед загрузкой в нее сока или экстракта овощей или плодов.
[0075] Антоцианин-содержащую фракцию выделяют из смеси сока или экстракта антоцианин-содержащих овощей или плодов растворителем при рН по меньшей мере около 2, предпочтительно по меньшей мере около 4. В некоторых вариантах выполнения настоящего изобретения фракцию антоцианинов выделяют растворителем при рН от около 2 до около 9. В другом варианте выполнения настоящего изобретения фракцию антоцианинов выделяют растворителем при рН от около 3 до около 9. В другом варианте выполнения настоящего изобретения фракцию антоцианинов выделяют растворителем при рН от около 4 до около 9. В другом варианте выполнения настоящего изобретения фракцию антоцианинов выделяют растворителем при рН от около 5 до около 9. В других вариантах выполнения настоящего изобретения фракцию антоцианинов выделяют растворителем при рН от около 6 до около 9. В другом варианте выполнения настоящего изобретения фракцию антоцианинов выделяют растворителем при рН от около 7 до около 9.
[0076] Подходящие растворители для элюирования выбранных фракций включают метанол, ацетонитрил, воду и их смеси, в зависимости от полярности колоночной среды и растворимости антоцианин-содержащего сока или экстракта. В некоторых вариантах выполнения настоящего изобретения растворитель представляет собой водный раствор метанола.
[0077] Подходящие агенты, которые могут быть добавлены в растворитель для регулирования рН, включают фосфат калия, гидроксид натрия и тому подобное.
[0078] Дополнительная фракция антоцианинов может быть выделена при дополнительном фракционировании фракции антоцианинов при использовании ионообменной колонки или колонки для полупрепаративной ВЭЖХ. Подходящие колонки для полупрепаративной ВЭЖХ включают С-18 колонки.
[0079] В одном варианте выполнения настоящего изобретения выделенная фракция или их комбинация обеспечивает натуральный синий антоцианин-содержащий краситель, содержащий антоцианины, селективно выделенные при использовании ионообменной колонки, исходя из разницы в полярности молекул антоцианина, полученных из антоцианин-содержащих овощей, плодов или их экстрактов.
[0080] В другом варианте выполнения настоящего изобретения натуральный синий антоцианин-содержащий краситель по настоящему изобретению выделяют из натурального овощного или плодового источника антоцианинов при использовании селективного выделения в ионообменной колонке, натуральный синий антоцианин-содержащий краситель получают способом, включающим следующие стадии:
a) загрузку активированной ионообменной колонки соком или экстрактом антоцианин-содержащих овощей или плодов, или их комбинацией;
b) промывку загруженной колонки водным раствором с рН 8;
c) элюирование первой фракции 25% объем/объем раствором метанола при рН 8; и
d) элюирование натурального синего антоцианин-содержащего красителя 70% объем/объем раствором метанола при рН 8 и необязательно очистку и концентрирование натурального синего антоцианин-содержащего красителя.
[0081] В другом варианте выполнения настоящего изобретения натуральный синий антоцианин-содержащий краситель по настоящему изобретению выделяют из натурального источника антоцианинов при использовании селективного выделения в ионообменной колонке, натуральный синий антоцианин-содержащий краситель получают способом, включающим следующие стадии:
a) загрузку активированной ионообменной колонки соком или экстрактом антоцианин-содержащих овощей или плодов, или их комбинацией;
b) промывку загруженной колонки водным раствором с рН 6;
c) элюирование первой фракции 25% объем/объем раствором метанола при рН 6;
d) промывку загруженной колонки водным раствором с рН 7;
e) элюирование второй фракции 25% объем/объем раствором метанола при рН 7;
f) промывку загруженной колонки водным раствором с рН 8;
g) элюирование третьей фракции 25% объем/объем раствором метанола при рН 8; и
h) элюирование натурального синего антоцианин-содержащего красителя 70% объем/объем раствором метанола при рН 8 и необязательно очистку и концентрирование натурального синего антоцианин-содержащего красителя.
[0082] В другом варианте выполнения настоящего изобретения натуральный синий антоцианин-содержащий краситель по настоящему изобретению содержит антоцианины краснокочанной капусты, селективно выделенные при использовании полупрепаративной ВЭЖХ, где краситель в форме водного раствора при рН 8,0 имеет максимальное поглощение от 620 нм до 635 нм.
[0083] Выделенные антоцианин-содержащие фракции могут быть использованы в качестве красителей или могут быть подвергнуты дополнительной технологической обработке, например очистке, концентрированию, дезодорированию или стабилизации цвета.
[0084] Натуральный синий антоцианин-содержащий краситель может быть нанесен на или введен во все типы съедобных продуктов, включая пищевые продукты для потребления человеком и кормовые продукты для потребления животными, напитки и фармацевтические продукты. Примеры таких продуктов включают кормовые продукты и лакомства для домашних животных, бакалейные товары (например, рис, зерновые и злаки), супы и соусы, кондитерские изделия (например, шоколад, все виды конфет с сахаром и без сахара, конфеты в виде батончиков, жевательная резинка и драже), десертные продукты (например, пудинг, фростинги, айсинги и топпинги), хлебобулочные изделия (например, торты, печенье, вафли и печенье типа галет), молочные продукты (например, йогурт, взбитые сливки и сыр), напитки (например, напитки на основе молока, воды, соки, чаи и безалкогольные тонизирующие прохладительные напитки), снэковые продукты (например, крекеры, снэки в виде бетончиков, крендельки и чипсы) и фармацевтические формы (например, таблетки, суспензии, жевательные таблетки и сиропы). Натуральный синий антоцианин-содержащий краситель также может быть введен в пищевые композиции, покрытия и краски. В одном варианте выполнения настоящего изобретения синий антоцианин-содержащий краситель вводят в покрытия или краски, наносимые на поверхность кондитерского изделия. В другом варианте выполнения настоящего изобретения синий антоцианин-содержащий краситель вводят в покрытия или краски, наносимые на поверхность кондитерского изделия, причем кондитерское изделие содержит кондитерскую сердцевину с мягким или твердым глазирующим покрытием на основе сахара. В другом варианте выполнения настоящего изобретения синий антоцианин-содержащий краситель вводят в покрытия или краски, наносимые на поверхность кондитерского изделия, причем кондитерское изделие содержит кондитерскую сердцевину с мягким или твердым глазирующим покрытием без сахара.
[0085] В одном варианте выполнения настоящего изобретения натуральный синий антоцианин-содержащий краситель получают фракционированием экстракта краснокочанной капусты при использовании колонки с сильной катионообменной смолой. Первую фракцию элюируют первым элюентом из раствора растворителя, который представляет собой смесь 75% объем/объем водного 0,1 M калий- фосфатного буфера при рН 8 и 25% объем/объем метанола. Вторую фракцию элюируют вторым элюентом из раствора растворителя, который представляет собой смесь 30% объем/объем 0,1 M калий-фосфатного буфера при рН 8 и 70% объем/объем метанола.
[0086] В другом варианте выполнения настоящего изобретения натуральный синий антоцианин-содержащий краситель получают фракционированием экстракта краснокочанной капусты при использовании колонки с сильной катионобменной смолой. Первую фракцию элюируют 75% объем/объем 0,1 M калий-фосфатным буфером при рН 6 и 25% объем/объем метанолом. Вторую фракцию элюируют 75% объем/объем 0,1 M калий-фосфатным буфером при рН рН 7 и 25% объем/объем метанолом. Третью фракцию элюируют 75% объем/объем 0,1 M калий-фосфатным буфером при рН рН 8 и 25% объем/объем метанолом. Четвертую фракцию элюируют 30% объем/объем 0,1 M калий-фосфатным буфером при рН рН 8 и 70% объем/объем метанолом.
[0087] В другом варианте выполнения настоящего изобретения натуральный синий антоцианин-содержащий краситель выделяют из экстракта краснокочанной капусты при использовании С-18 колонки для полупрепаративной ВЭЖХ.
[0088] Антоцианин-содержащие красители по настоящему изобретению отвечают давно существующей потребности в натуральных синих красителях, которые обеспечивают характеристики цвета, аналогичные таковым, обеспеченным синтетическим синим красителем FD&C Blue No. 1.
[0089] Далее будут приведены конкретные варианты выполнения настоящего изобретения со ссылкой на следующие Примеры. Следует понимать, что эти Примеры приведены только для иллюстрации настоящего изобретения и его варианты не выходят за рамки объема притязаний настоящего изобретения.
ПРИМЕР 1
ФРАКЦИОНИРОВАНИЕ ЭКСТРАКТА КРАСНОКОЧАННОЙ КАПУСТЫ ПРИ ИСПОЛЬЗОВАНИИ КАРТРИДЖА С СИЛЬНОЙ КАТИОНООБМЕННОЙ СМОЛОЙ
[0090] SCX (сильная катионообменная смола Strong Cation Exchange) картридж для твердофазной экстракции от Phenomenex® (Torrance, СА) активировали при использовании чистого метанола. Картридж промыли при использовании 0,01% объем/объем подкисленной воды. Водный раствор экстракта краснокочанной капусты загрузили в картридж и промыли 0,01% объем/объем подкисленной водой. Через картридж пропустили калий-фосфатный буфер (0,1 М) при рН 8. Фракцию 1 элюировали и собрали при использовании 25% объем/объем забуференного водного раствора метанола при рН 8. Фракцию 2 элюировали и собрали при использовании 70% объем/объем забуференного водного раствора метанола при рН 8.
[0091] Фракции 1 и 2 подкислили 2-5 мл 88% объем/объем муравьиной кислоты. Метанол удалили при использовании ротационного испарителя.
[0092] Для удаления солей Фракцию 1 загрузили в С-18 картридж и элюировали 0,01% объем/объем подкисленной водой. Элюент собрали в 0,01% объем/объем подкисленную воду и выпарили остаточный метанол. Фракцию 2 также пропустили через С-18 картридж при использовании процедуры, приведенной для Фракции 1.
[0093] Максимальное поглощение длин волн УФ/Видимой области и характеристики цвета были обеспечены раствором экстракта краснокочанной капусты (RCE), Фракции 1 и 2 были подвергнуты анализу при различных показателях рН, как приведено ниже в Таблице 4. Спектральные данные получили при использовании спектрофотометра Konica Minolta Spectrophotometer CM-3500d, работающего в режиме светопропускания со стандартным источником света CIE Standard Illuminant D65 и углом обзора 10 градусов.
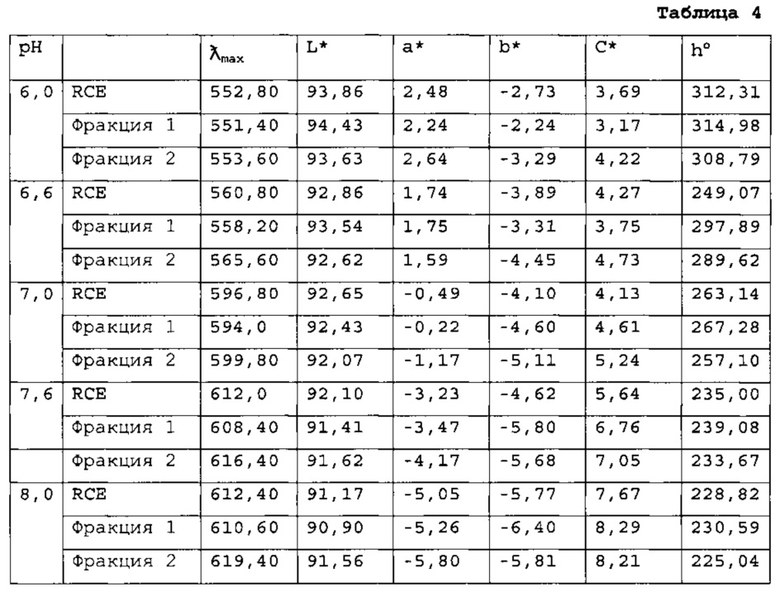
Фракция 2 при рН 7,6 и рН 8,0 обеспечила показатели 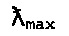 самые близкие к таковым синтетического FD&C Blue No. 1
самые близкие к таковым синтетического FD&C Blue No. 1 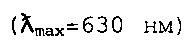 , то есть показатели
, то есть показатели 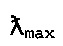 616,40 и 619,40 соответственно.
616,40 и 619,40 соответственно.
Также для сравнения характеристик цвета, обеспеченных Фракцией 2 при рН 7,6 и рН 8,0, с таковыми обеспеченными синтетическим FD&C Blue No. 1 могут быть рассчитаны показатели ΔЕ. Показатели ΔЕ представляют эквивалентные минимальным расстояниям между значениями цвета Фракции 2 в L*a*b* цветовом пространстве и FD&C Blue No. 1 модели. Следовательно, Уравнение 5 используют для расчета dmin или показателей ΔЕ по следующим данным:
Х0 для Фракции 2 при рН 7,6 в L*a*b* цветовом пространстве составляет:
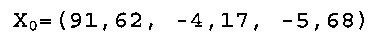
Х0 для Фракции 2 при рН 8,0 в L*a*b* цветовом пространстве составляет:
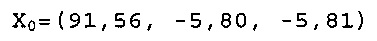
X1 и X2 представляют две точки FD&C Blue No. 1 модели:
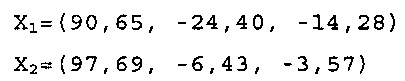
Рассчитанный dmin или ΔЕ составил 6,7 для Фракции 2 при рН 7,6, и 6,0 для Фракции 2 при рН 8,0.
[0094] На Фиг. 6 приведены хроматограммы ВЭЖХ при 520 нм раствора экстракта краснокочанной капусты (RCE) и Фракций 1 и 2. На Фиг. 6 видно, что Фракция 2 имеет более высокую концентрацию пиков последнего элюирования по сравнению с раствором экстракта краснокочанной капусты.
ПРИМЕР 2
ФРАКЦИОНИРОВАНИЕ ЭКСТРАКТА КРАСНОКОЧАННОЙ КАПУСТЫ ПРИ ИСПОЛЬЗОВАНИИ КАРТРИДЖА С СИЛЬНОЙ КАТИОНООБМЕННОЙ СМОЛОЙ И РАСТВОРИТЕЛЕЙ ПРИ РАЗЛИЧНЫХ ВЫСОКИХ ПОКАЗАТЕЛЯХ РН
[0095] SCX (сильная катионообменная смола Strong Cation Exchange) картридж для твердофазной экстракции от Phenomenex® (Torrance, СА) активировали при использовании чистого метанола. Разбавленный 0,01% объем/объем подкисленной водой (10-15 мл) экстракт краснокочанной капусты загрузили в картридж и промыли 0,01% объем/объем подкисленной водой. Через картридж пропустили калий-фосфатный буфер (0,1 М) при рН 6. Фракцию 1 элюировали и собрали при использовании 25% объем/объем раствора метанола при рН 6. Через картридж пропустили калий-фосфатный буфер (0,1 М) при рН 7. Фракцию 2 элюировали и собрали при использовании 25% объем/объем раствора метанола при рН 7. Через картридж пропустили калий-фосфатный буфер (0,1 М) при рН 8. Фракцию 3 элюировали и собрали при использовании 25% объем/объем раствора метанола при рН 8. Фракцию 4 элюировали и собрали при использовании 70% объем/объем раствора метанола при рН 8.
[0096] Фракции 1-4 подкислили 20% объем/объем муравьиной кислотой. Метанол удалили при использовании ротационного испарителя.
[0097] Для вымывания солей Фракцию 1 загрузили в С-18 картридж и элюировали 0,01% объем/объем подкисленной водой. Элюент собрали в 0,01% объем/объем подкисленную воду и выпарили остаточный метанол. Фракции 2-4 также пропустили через С-18 картридж при использовании процедуры, приведенной для Фракции 1.
[0098] Максимальное поглощение длин волн УФ/Видимой области и характеристики цвета были обеспечены раствором экстракта краснокочанной капусты (RCE), Фракции 1-4 были подвергнуты анализу при различных показателях рН, как приведено ниже в Таблице 5.
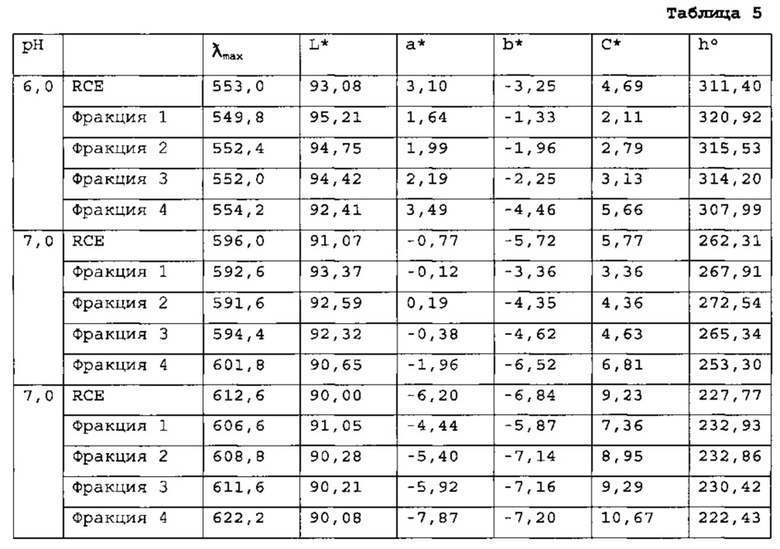
Фракция 4 при рН 8,0 обеспечила показатель 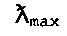 самый близкий к таковому синтетического FD&C Blue No. 1
самый близкий к таковому синтетического FD&C Blue No. 1 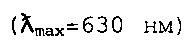 , то есть показатель
, то есть показатель 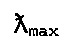 622,2.
622,2.
Также для сравнения характеристик цвета, обеспеченных Фракцией 4 при рН 8,0, с таковыми обеспеченными синтетическим FD&C Blue No. 1 может быть рассчитан показатель ΔЕ. Показатель ΔЕ представляет собой эквивалент минимального расстояния между значениями цвета Фракции 4 в L*a*b* цветовом пространстве и FD&C Blue No. 1 модели. Следовательно, Уравнение 5 используют для расчета dmin или ΔЕ по следующим данным:
Х0 для Фракции 4 при рН 8,0 в L*a*b* цветовом пространстве составляет:
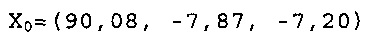
X1 и Х2 представляют две точки FD&C Blue No. 1 модели:
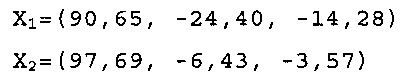
Рассчитанный dmin, или ΔЕ, составил 6,7 для Фракции 4 при рН 8,0.
На Фиг. 7 приведены хроматограммы ВЭЖХ при 520 нм водного экстракта краснокочанной капусты (RCE) и Фракций 1-4. На Фиг. 7 видно, что Фракция 4 имеет более высокую концентрацию пиков последнего элюирования по сравнению с раствором экстракта краснокочанной капусты.
ПРИМЕР 3
ВЫДЕЛЕНИЕ ГРУПП ПИКОВ ЭКСТРАКТА КРАСНОКОЧАННОЙ КАПУСТЫ ПРИ ИСПОЛЬЗОВАНИИ ПОЛУПРЕПАРАТИВНОЙ ВЭЖХ
[0099] Фракции, ассоциируемые с двумя специфическими группами пиков, как показано на хроматограммах на Фиг. 8, могут быть выделены и собраны из раствора экстракта краснокочанной капусты при использовании полупрепаративной ВЭЖХ. Раствор экстракта краснокочанной капусты загрузили в С-18 картридж для полупрепаративной ВЭЖХ и две фракции, Фракцию 520-нм 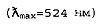 и Фракцию 530-нм
и Фракцию 530-нм 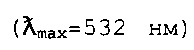 , элюировали при использовании кислого ацетонитрила и водного градиента. Остаточный ацетонитрил выпарили из каждой фракции при использовании ротационного испарителя.
, элюировали при использовании кислого ацетонитрила и водного градиента. Остаточный ацетонитрил выпарили из каждой фракции при использовании ротационного испарителя.
[0100] Оценку цветовых характеристик провели после регулирования концентраций фракций и смешивания аликвот отдельных фракций с буфером с получением пяти аликвот при рН 6, 6,6, 7, 7,6, и 8. Максимальное поглощение длин волн УФ/Видимой области и характеристики цвета аликвот Фракций 520-нм и 530-нм проанализировали, результаты приведены в Таблице 6.
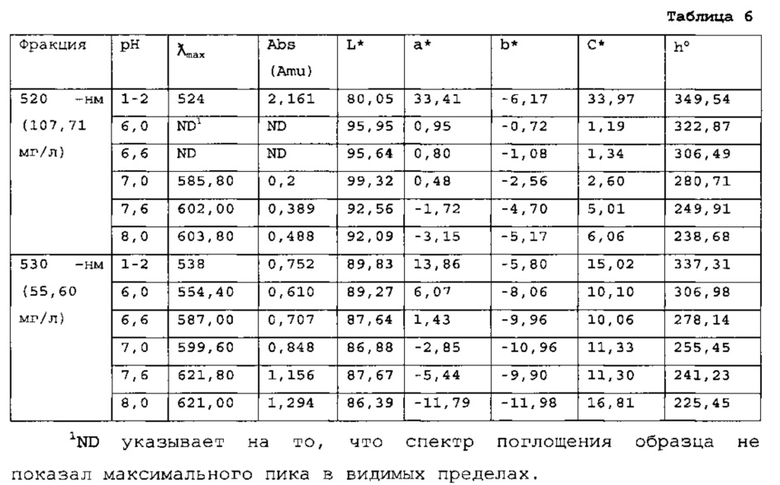
Фракция 530-нм имела максимальное поглощение около 621 нм при рН 7,6 и рН 8,0 и обеспечила самый близкий к синтетическому FD&C Blue No. 1 показатель 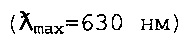 .
.
Также для сравнения характеристик цвета, обеспеченных Фракцией 530-нм при рН 7,6 и рН 8,0, с таковыми обеспеченными синтетическим FD&C Blue No. 1 могут быть рассчитаны показатели ΔЕ. Показатели ΔЕ представляют эквивалентные минимальным расстояниям между значениями цвета Фракции 530-нм в L*a*b* цветовом пространстве и FD&C Blue No. 1 модели. Следовательно, Уравнение 5 используют для расчета dmin или ΔЕ по следующим данным:
Х0 для Фракции 530-нм при рН 7,6 в L*a*b* цветовом пространстве составляет:
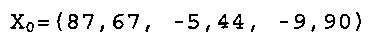
Х0 для Фракции 530-нм при рН 8,0 в L*a*b* цветовом пространстве составляет:

X1 и Х2 представляют две точки FD&C Blue No. 1 модели:
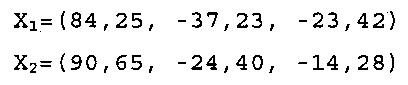
Рассчитанный dmin, или ΔΕ, составил 12,1 для Фракции 530-нм при рН 7,6, и 9,9 для Фракции 530-нм при рН 8,0.
[0101] На Фиг. 9 приведено визуальное сравнение Фракций 520-нм и 530-нм при различных показателях рН. Концентрация Фракции 520-нм составила 107,7 мг/л (Cyn-3-glu), и концентрация Фракции 530-нм составила 55,6 мг/л (Cyn-3-glu). При нейтральном и более высоком рН видно, что Фракция 530-нм обеспечила от в два до в четыре раза большую цветность (как измерено при использовании С*) по сравнению с Фракцией 520-нм при половинной концентрации красителя.
[0102] На Фиг. 10 приведены хроматограммы ВЭЖХ при 520 нм раствора экстракта краснокочанной капусты и Фракции 520-нм и 530-нм. На Фиг. 10 видно, что каждая фракция содержит три различных соединения антоцианина.
СРАВНИТЕЛЬНЫЙ ПРИМЕР 1
[0103] Получили несколько разных концентраций раствора антоцианина краснокочанной капусты, как описано в Примерах WO 2004/012526 при рН 8,0. Для выделения и сбора выделенных антоцианин-содержащих красителей фракционирование не проводили. Максимальное поглощение полученных в результате растворов составило 610 нм. Такой цвет не считается приемлемым совпадением с цветом FD&C Blue No. 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ ФРАКЦИЙ СИНИХ АНТОЦИАНИНОВ | 2014 |
|
RU2629257C2 |
| Композиции красителей на основе антоцианина и способы их применения | 2019 |
|
RU2795394C2 |
| КОМПОЗИЦИИ КРАСИТЕЛЕЙ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2016 |
|
RU2721836C2 |
| СТАБИЛИЗАЦИЯ НАТУРАЛЬНЫХ СИНИХ АНТОЦИАНСОДЕРЖАЩИХ КРАСИТЕЛЕЙ И ПРИГОТОВЛЕННЫХ ПРОДУКТОВ | 2014 |
|
RU2636761C2 |
| ОРАНЖЕВЫЕ И КРАСНЫЕ КРАСИТЕЛИ, СОДЕРЖАЩИЕ АНТОЦИАНИН | 2014 |
|
RU2652386C2 |
| КОРИЧНЕВЫЙ КРАСИТЕЛЬ, СОДЕРЖАЩИЙ АНТОЦИАНИН | 2014 |
|
RU2652141C2 |
| АНТОЦИАНОВАЯ КРАСЯЩАЯ КОМПОЗИЦИЯ | 2013 |
|
RU2628398C2 |
| Состав натуральных разноцветных антоциановых губных помад | 2023 |
|
RU2805477C1 |
| КОМПОЗИЦИИ С ЦВЕТОВОЙ ИНДИКАЦИЕЙ | 2016 |
|
RU2728204C2 |
| СВЕТОСТАБИЛЬНЫЕ ПРИРОДНЫЕ ЖЕЛТЫЕ КРАСЯЩИЕ СИСТЕМЫ В МАРИНОВАННЫХ И ФЕРМЕНТИРОВАННЫХ ОВОЩАХ | 2020 |
|
RU2830302C1 |



Изобретение относится к натуральным синим антоцианин-содержащим красителям, выделенным из смеси соков и экстрактов антоцианин-содержащих овощей и плодов. Фракцию антоцианинов выделяют при заданном pH, исходя из разницы в заряде и полярности молекул антоцианина, с использованием ионообменной колонки и растворителя, выбранного из метанола, ацетонитрила, воды и их смесей. Описывается также натуральный зеленый краситель, содержащий натуральный синий антоцианин-содержащий краситель и натуральный желтый краситель. Описывается также съедобный продукт, содержащий натуральные синие антоцианин-содержащие красители. Изобретение обеспечивает антоцианин-содержащие красители, которые в форме водного раствора при рН 8,0 имеют максимальное поглощение от 615 нм до 635 нм и характеристики цвета, аналогичные синтетическому пищевому синему красителю FD&C Blue No. 1. 4 н. и 11 з.п. ф-лы, 10 ил., 6 табл.
1. Натуральный синий антоцианин-содержащий краситель, полученный из овощей, плодов или их комбинаций, содержащий селективно выделенную смесь антоцианинов, где краситель в форме водного раствора при рН 8,0 имеет максимальное поглощение от 615 нм до 635 нм;
при этом селективное выделение указанной смеси антоцианинов основано на различиях в заряде и полярности молекул антоцианина, с использованием ионообменной колонки и растворителя, выбранного из группы, включающей метанол, ацетонитрил, воду и их смеси.
2. Краситель по п. 1, который в форме водного раствора при рН 8,0 в концентрации от 1 м.д. до 1000 м.д. имеет показатель h° от 209 до 290.
3. Краситель по п. 1, в котором по меньшей мере одна концентрация красителя в форме водного раствора при рН 8,0 обеспечивает характеристики цвета с показателем ΔЕ 12 или менее по сравнению с характеристиками цвета, определенными очерчивающей сегмент линией, определенной показателями L*a*b* 5 м.д. и 10 м.д. FD&C Blue No. 1 в водном растворе.
4. Краситель по п. 3, в котором показатель h° по меньшей мере одной концентрации красителя в водном растворе составляет от 209 до 250.
5. Краситель по пп. 1-4, в котором источник антоцианинов выбирают из группы, состоящей из краснокочанной капусты, фиолетового сладкого картофеля, синего картофеля, черной моркови, фиолетовой моркови и их комбинаций.
6. Краситель по пп. 1-4, в котором источником антоцианинов является краснокочанная капуста.
7. Натуральный синий антоцианин-содержащий краситель, полученный из овощей, плодов или их комбинации, содержащий селективно выделенную смесь антоцианинов,
при этом селективное выделение указанной смеси антоцианинов основано на различиях в заряде и полярности молекул антоцианина, с использованием ионообменной колонки и растворителя, выбранного из группы, включающей метанол, ацетонитрил, воду и их смеси,
причем по меньшей мере одна концентрация красителя в форме водного раствора при рН 8,0 обеспечивает характеристики цвета, совпадающие с FD&C Blue No. 1 очерчивающей сегмент линией, исходя из серий водных растворов с различными концентрациями FD&C Blue No. 1, определенными в L*a*b* цветовом пространстве,
при этом соответствие означает, что по меньшей мере одна концентрация красителя в водном растворе при рН 8,0 имеет показатель ΔЕ, измеренный по FD&C Blue No. 1 очерчивающей сегмент линии, который по меньшей мере на одну единицу меньше, чем показатель ΔЕ для синего из спирулины очерчивающей сегмент линии, определенной в том же самом L*a*b* цветовом пространстве, исходя из серий водных растворов с различными концентрациями синего из спирулины, измеренного по FD&C Blue No. 1 очерчивающей сегмент линии.
8. Натуральный зеленый краситель, состоящий по существу из натурального желтого красителя и натурального синего антоцианин -содержащего красителя по любому из пп. 1, 3 и 7.
9. Съедобный продукт, содержащий натуральный синий антоцианин-содержащий краситель по любому из пп. 1, 3 и 7.
10. Продукт по п. 9, дополнительно содержащий натуральный желтый краситель.
11. Продукт по п. 9, представляющий собой кондитерское изделие.
12. Продукт по п. 11, дополнительно содержащий натуральный желтый краситель.
13. Продукт по п. 11, в котором краситель входит в состав покрытия, наносимого на поверхность кондитерского изделия.
14. Продукт по п. 13, содержащий кондитерскую сердцевину с мягким или твердым глазирующим покрытием на основе сахара.
15. Продукт по п. 13, содержащий кондитерскую сердцевину с мягким или твердым глазирующим покрытием без сахара.
| WO 2009100165 A1, 13.08.2009 | |||
| WO 2004012526 A1, 12.02.2004 | |||
| RU 2010147323 A, 10.06.2012. |
Авторы
Даты
2018-01-22—Публикация
2014-03-14—Подача