В настоящем изобретении описывается ветеринарная композиция в области фармацевтической технологии, которая увеличивает биодоступность инъецируемых растворов хинолонов и цефалоспоринов.
Известный уровень техники
Хинолоны представляют собой большое семейство антибактериальных агентов. Их используют в основном для лечения инфекций мочевых путей и, кроме того, при системных инфекциях в силу наличия у них широкого спектра активности и хорошей диффузии.
Среди семейства хинолонов наиболее широко используемыми соединениями являются налидиксовая кислота, пипемидовая кислота и пиромидовая кислота. Они известны как хинолоны 1-го поколения или уросептические хинолоны из-за быстрого выведения их почками. Структурная модификация 1-го поколения хинолонов приводит ко 20-му поколению, среди которого одним из наиболее значимых является флумеквин. 3е поколение хинолонов также известно как фторхинолоны из-за наличия фтора в положении 6 кольца 3-хинолон-карбоновой кислоты и включает норфлоксацин, пефлоксацин, офлоксацин, енофлоксацин, ципрофлоксацин и энрофлоксацин в качестве основных примеров.
Далее, цефтиофур представляет собой цефалоспорин 3-го поколения, особенно активный против широкого спектра грамположительных и грамотрицательных бактерий, включая штаммы, продуцирующие р-лактамазы. Как и любые другие Р-лактамы, цефтиофур подавляет синтез клеточных стенок бактерий, придавая соединению антибактериальные свойства. Соединение было одобрено в EU (Европейский Союз) в особенности для использования у крупного рогатого скота с бронхопневмонией, вызванной Pasteurella haemolytica и P. multocida.
Помимо цефтиофура, 3-е поколение цефалоспоринов включает цефриаксон, цефсулодин, цефотаксим, цефоперазон и некоторые другие средства. Эти соединения зачастую являются способными проходить сквозь гематоэнцефалический барьер животного и поэтому часто назначаются при бактериальном менингите. Обычно эта группа соединений проявляет только умеренную активность против грамположительных бактерий, но является активной против широкого разнообразия грамотрицательных бактерий, включая в некоторых случаях Pseudomonas spp., Proteus vulgaris, Enterobacter spp. и Citrobacter spp.
Синтез клеточной стенки бактерии зависит от ферментов, представляющих собой пенициллинсвязывающие белки (РВР). Некоторые микроорганизмы способны развивать устойчивость к цефалоспоринам посредством нескольких механизмов. β-Лактамы, продуцируемые некоторыми кишечными грамотрицательными микроорганизмами, требуют высокой минимальной ингибирующей концентрации (MIC) цефалоспоринов, а также пенициллинов и комбинаций ингибиторов Р-лактамаз.
Большое количество Грам+ и Грамм- бактерий, хотя и не штаммов, продуцирующих β-лактамазы, является чувствительным к полусинтетическим пенициллинам широкого спектра. Хотя бактериальная устойчивость является широко распространенной, комбинирование ингибиторов β-лактамаз и пенициллинов широкого спектра заметно увеличивает спектр и эффективность как против грамположительных, так и против грамотрицательных патогенов. Потенциированный клавуланатом амоксициллин является превосходным примером такой синергетической ассоциации.
Цефалоспорины представляют собой более продвинутые β-лактамные антибиотики, чем пенициллины, и демонстрируют более широкий спектр активности, являясь активными против многих Грам+ и Грам- бактерий. Они имеют высокий терапевтический индекс и высокие уровни в плазме при парентеральном пути введения.
Mandal продемонстрировал определенный синергетический эффект комбинации пенициллина амоксициллина и ципрофлоксацина, который представляет собой фторхинолоновый предшественник энрофлоксацина (Mandal et al. "In vitro efficacy of ciprofloxacin alone and in combination with amoxycillin against Salmonella typhi isolates", Indian J Exp Biol. 2003, 41(4):360-2).
Синергетический эффект хинолона с цефалоспорином известен в данной области техники. Более того, цефалоны (cefalones) представляют собой лекарственные средства, состоящие из фторхинолона и цефалоспорина, связанных амидом. Однако в фармацевтической практике никогда еще не разрабатывалось какое-либо лекарственное средство на основе цефалонов.
Кроме того, проблема в данной области техники заключается в нахождении пути введения хинолона и цефалоспорина для эффективного лечения бактериальной инфекции у животного. Раствор, предлагаемый в настоящем изобретении, представляет собой комбинацию хинолона и цефалоспорина в масляной суспензии.
Описание изобретения
В изобретении предложено комбинирование бета-лактамного антибиотика с фторхинолоном для обеспечения широкого спектра терапевтического действия.
Таким образом, настоящее изобретение представляет собой инъецируемую ветеринарную композицию, содержащую хинолон, предпочтительно энрофлоксацин, и более предпочтительно в количестве от 5 до 20% (мас./мас.), и цефалоспорин, предпочтительно гидрохлорид цефтиофура, и более предпочтительно в количестве от 2,5 до 10% (мас./мас.), все количества относительно общей массы композиции, или их фармацевтически приемлемые соли, с фармацевтически приемлемыми эксципиентами в масляной суспензии для лечения бактериальной инфекции у животного.
В настоящей заявке термин "хинолон" определяется как соединение, выбранное из группы, состоящей из энрофлоксацина, марбофлоксацина, дифлоксацина, данофлоксацина, сарафлоксацина и флумеквина.
В настоящей заявке термин "цефалоспорин" определяется как соединение, выбранное из группы, состоящей из гидрохлорида цефтиофура, сульфата цефхинома и цефалексина.
В предпочтительном аспекте изобретения указанные фармацевтически приемлемые эксципиенты выбирают из группы, состоящей из сложного эфира сорбитана и жирной кислоты, пропилгаллата, пропиленгликоля дикаприлокапрата, глицерилкаприлокапрата, макрогол-(15)-гидроксистеарата, гидрогенизированного касторового масла, касторового масла РЕС-35 и полисорбата или их смесей, более предпочтительно сложного эфира сорбитана и жирной кислоты и еще более предпочтительно олеата сорбитана. Олеат сорбитана означает сложный эфир олеиновой кислоты и сорбита.
Другой предпочтительный аспект настоящего изобретения включает эксципиенты, полученные из глицерина, пропиленгликоля и полиэтиленгликоля, определенные как триглицериды, полученные этерификацией глицерина, пропиленгликоля или полиэтиленгликоля 200-1500 жирными кислотами С6-С7.
Предпочтительный аспект настоящего изобретения включает любое фармацевтически приемлемое производное касторового масла, предпочтительно полиоксил-гидрогенизированное касторовое масло.
В предпочтительном аспекте изобретения указанное животное представляет собой свинью. В более предпочтительном аспекте указанная бактериальная инфекция включает наличие по меньшей мере одного микроорганизма, выбранного из группы, состоящей из Pasteurella multocida, Actinobacillus pleuropneumoniae и Streptococcus suis.
В еще одном предпочтительном аспекте изобретения указанное животное представляет собой представителя крупного рогатого скота. В более предпочтительном аспекте указанная бактериальная инфекция включает наличие по меньшей мере одного микроорганизма, выбранного из группы, состоящей из Pasteurella multocida, Mannehimia haemolytica, Histophilus somnim, Fusobacterium necrophorum, Bacteroides melaninogenicus, Escherichia coli, Arcanobactehum pyogenes и Fusobacterium necrophorum.
Еще один аспект настоящего изобретения представляет собой инъецируемую ветеринарную композицию, содержащую хинолон и цефалоспорин или их фармацевтически приемлемые соли с фармацевтически приемлемыми эксципиентами и по меньшей мере еще один терапевтический агент в масляной суспензии, для лечения бактериальной инфекции у животного.
Поверхностно-активные вещества постулируются в качестве модуляторов всасывания у животного. Их воздействия на мембрану являются, однако, сложным и не вполне определенными. Многие из них взаимодействуют с мембранами, содействуя проницаемости и облегчая всасывание некоторых растворенных лекарственных средств; этот эффект является особенно интересным, когда содержание поверхностно-активного вещества в растворе лекарственного средства является равным или ниже критической концентрации мицеллообразования (CMC).
Цефтиофур, как и любой β-лактам, является нестабильным в водной среде. Однако фторхинолоны всегда вводят в водной среде, содействующей их растворимости и стабильности. Таким образом, добавление фторхинолона в масляную суспензию для комбинации по изобретению определяет изобретательский вклад, поскольку масляная среда неожиданно оказалась подходящей для поддержания стабильности комбинации.
В масляной суспензии по настоящему изобретению частицы энрофлоксацина и цефтиофура имеют средний размер 10 мкм. При внутримышечной инъекции изменение растворителя, обусловленное водной средой мышцы, ориентирует соответственно поверхностно-активные вещества композиции, приводя липофильную фазу в контакт с масляной средой, тогда как гидрофильная фаза ориентируется по направлению к водной среде ткани, образуя мицеллы. Эти структуры увеличивают всасывание лекарственного средства, поскольку они улучшают взаимодействие с клеточными мембранами, содействуя его биодоступности.
Композиция по настоящему изобретению является стабильной легко вводимой животному фармацевтической формой, демонстрирующей широкий терапевтический спектр.
Краткое описание графических материалов
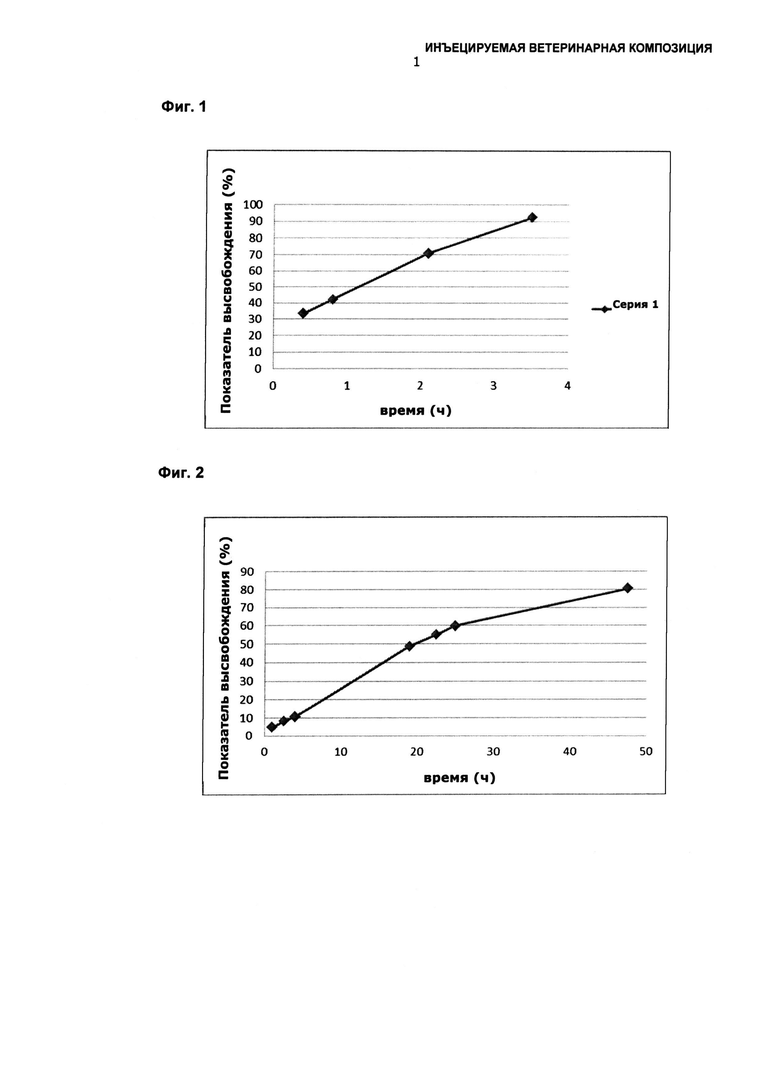
Фиг.1: Процент высвобождения энрофлоксацин + цефтиофур в композиции с 10% макрогол-(15)-гидроксистеарата, 5% олеата сорбитана и 70% пропиленгликоля дикаприлокапрата согласно Примеру 1.
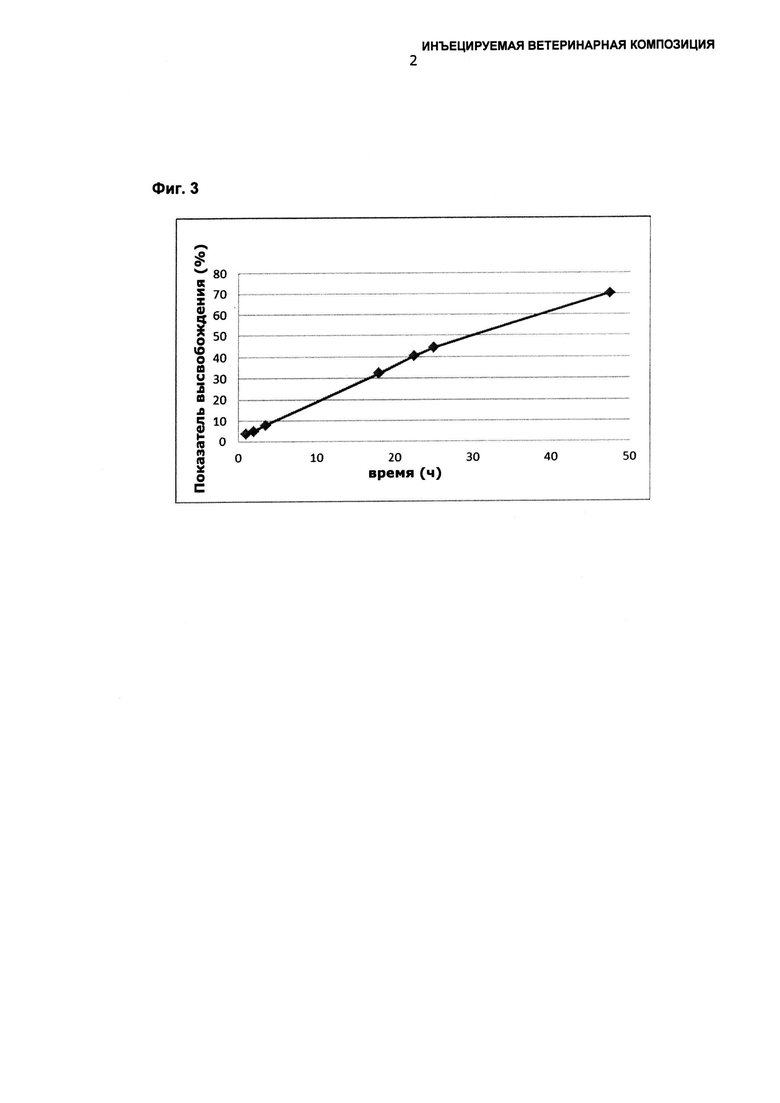
Фиг.2: Процент высвобождения энрофлоксацин + цефтиофур в композиции с 10% гидрогенизированного касторового масла - PEG(40), 5% олеата сорбитана и 70% пропиленгликоля дикаприлокапрата.
Фиг.3: Процент высвобождения энрофлоксацин + цефтиофур в композиции с 10% макрогол-(15)-гидроксистеарата, 5% олеата сорбитана и 70% глицерилкаприлокапрата согласно Примеру 2.
Предпочтительные аспекты
Следующие примеры предлагаются с целью демонстрации настоящего изобретения иллюстративным, однако не ограничивающим образом. Все количества приведены в массовых процентах соединений относительно общей массы композиции.
Пример 1
350 г дикаприлокапрата пропиленгликоля и 50 мг пропилгаллата растворяли при перемешивании. При осторожном перемешивании добавляли в этот раствор 50 г макрогол-(15)-гидроксистеарата. Как только смесь становилась гомогенной, дополнительно при перемешивании добавляли 25 г олеата сорбитана. После полного растворения этих компонентов полученный раствор фильтровали с помощью осветляющего 0,6 мкм фильтра. Затем полученный раствор нагревали при 130°С для стерилизации и оставляли охлаждаться при КТ (комнатной температуре). После охлаждения добавляли 50 г микронизированного энрофлоксацина с использованием гомогенизатора Turrax на бане 15-20°С и затем гомогенизировали в течение 10 мин. В завершение добавляли 25 г микронизированного гидрохлорида цефтиофура и также гомогенизировали в течение 10 мин.
Пример 2
350 г глицерилкаприлатакапрата и 50 мг пропилгаллата растворяли при перемешивании. При осторожном перемешивании добавляли в этот раствор 50 г макрогол-(15)-гидроксистеарата. Как только смесь становилась гомогенной, дополнительно при перемешивании добавляли 25 г олеата сорбитана. После полного растворения этих компонентов полученный раствор фильтровали с помощью осветляющего 0,6 мкм фильтра. Затем полученный раствор нагревали при 130°С для стерилизации и оставляли охлаждаться при КТ. После охлаждения добавляли 50 г микронизированного энрофлоксацина с использованием гомогенизатора Turrax на бане 15-20°С и затем гомогенизировали в течение 10 мин. В завершение добавляли 25 г микронизированного гидрохлорида цефтиофура и также гомогенизировали в течение 10 мин.
Пример 3: Тест на биодоступность. Скорость высвобождения энрофлоксацина
С целью оценки биодоступности композиции по изобретению выполняли исследование распределения, используя дисплей из диффузионных ячеек Франца, как описано в ADDICKS, W.J. "Validation of a Flow-Through Diffusion Cell for Use in Transdermal Research". Pharmaceutical Research, 4(4), 337(1987). Каждую композицию по изобретению, как представлено в Таблицах, помещали в донорный отсек, тогда как приемный отсек содержал буфер с физиологическим рН 7,4 согласно Sorensen, состоящий из раствора 250 мл абсолютного этилового спирта и 750 мл фосфатного буфера, где приемный и донорный отсеки разделены нейлоновой мембраной (ZATS, J.L. et al., "Techniques for Measuring In Vitro Release from Semisolids". Dissolution Technologies. February 1998). Настоящий дисплей соответствует условиям достаточного разбавления (DASH, S. et al. "Kinetic modeling on drug release from controlled Drug delivery systems". Acta Poloniae Pharmaceutica - Drug Research, 67(3), 217-223(2010)). Образцы из приемного контейнера отбирали в разные моменты времени с целью определения количества энрофлоксацина, проникшего через мембрану. В Таблице 1 представлены показатели проникновения композиции из Примера 1 (Фиг.1).
В Таблице 2 представлены показатели проникновения композиции с 10% гидрогенизированного касторового масла - PEG(40), 5% олеата сорбитана и 70% пропиленгликоля дикаприлокапрата (Фиг.2).
В Таблице 3 представлены показатели проникновения композиции, соответствующей Примеру 2 (Фиг.3).
Увеличение показателя высвобождения композиции из Примера 1 обнаруживает корреляцию с увеличением всасывания лекарственного средства и, следовательно, с увеличением его биодоступности.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПАРЕНТЕРАЛЬНЫЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2744987C2 |
| ДИСПЕРГИРУЕМЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2003 |
|
RU2311201C2 |
| Композиции длительного действия на основе кетопрофена | 2014 |
|
RU2646829C1 |
| КОМПОЗИЦИИ И СПОСОБ ДЛЯ ЛЕЧЕНИЯ МИКРОБНЫХ И ПАРАЗИТАРНЫХ ИНФЕКЦИЙ У КРУПНОГО РОГАТОГО СКОТА И ДРУГИХ ЖИВОТНЫХ | 2004 |
|
RU2359667C2 |
| ДИСПЕРГИРУЕМАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ МАСТИТА И ПОРАЖЕНИЙ УХА | 2004 |
|
RU2329064C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ГИГИЕНИЧНОГО ПРИМЕНЕНИЯ НА УШАХ | 2005 |
|
RU2431486C2 |
| Готовые к применению лекарственные формы для инъекций | 2020 |
|
RU2777360C1 |
| Препарат для лечения мастита у коров в период лактации | 2024 |
|
RU2827450C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБ ЛЕЧЕНИЯ МАСТИТОВ | 2013 |
|
RU2659430C2 |
| КРИСТАЛЛИЧЕСКАЯ СВОБОДНАЯ ЦЕФТИОФУРОВАЯ КИСЛОТА, КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1994 |
|
RU2136685C1 |
Группа изобретений относится к медицине и может быть использована для лечения бактериальной инфекции у животного. Для этого вводят инъецируемую ветеринарную композицию, содержащую хинолон и цефалоспорин или их фармацевтически приемлемые соли с пропиленгликоля дикаприлокапратом и/или глицерилкаприлокапратом в масляной суспензии. Также предложена инъецируемая ветеринарная композиция для лечения бактериальной инфекции у животного, содержащая по меньшей мере еще один терапевтический агент в масляной суспензии. Группа изобретений позволяет осуществлять лечение бактериальной инфекции у свиней или крупного рогатого скота. 2 н. и 11 з.п. ф-лы, 3 табл., 3 ил., 3 пр.
1. Инъецируемая ветеринарная композиция, содержащая хинолон и цефалоспорин или их фармацевтически приемлемые соли с пропиленгликоля дикаприлокапратом и/или глицерилкаприлокапратом в масляной суспензии, для лечения бактериальной инфекции у животного.
2. Инъецируемая ветеринарная композиция по п. 1, в которой указанный хинолон представляет собой энрофлоксацин.
3. Инъецируемая ветеринарная композиция по п. 2, в которой указанный энрофлоксацин присутствует в количестве от 5 до 20% (мас./мас.) относительно общей массы композиции.
4. Инъецируемая ветеринарная композиция по п. 1, в которой указанный цефалоспорин представляет собой гидрохлорид цефтиофура.
5. Инъецируемая ветеринарная композиция по п. 4, в которой указанный гидрохлорид цефтиофура присутствует в количестве от 2,5 до 10% (мас./мас.) относительно общей массы композиции.
6. Инъецируемая ветеринарная композиция по п. 1, содержащая дополнительные фармацевтически приемлемые эксципиенты.
7. Инъецируемая ветеринарная композиция по п. 6, в которой указанные эксципиенты содержат сложный эфир сорбитана и жирной кислоты.
8. Инъецируемая ветеринарная композиция по п. 7, в которой указанный сложный эфир сорбитана и жирной кислоты представляет собой олеат сорбитана.
9. Инъецируемая ветеринарная композиция по п. 1, в которой указанное животное представляет собой свинью.
10. Инъецируемая ветеринарная композиция по п. 9, в которой указанная бактериальная инфекция включает наличие по меньшей мере одного микроорганизма, выбранного из группы, состоящей из Pasteurella multocida, Actinobacillus pleuropneumoniae и Streptococcus suis.
11. Инъецируемая ветеринарная композиция по п. 1, в которой указанное животное представляет собой представителя крупного рогатого скота.
12. Инъецируемая ветеринарная композиция по п. 11, в которой указанная бактериальная инфекция включает наличие по меньшей мере одного микроорганизма, выбранного из группы, состоящей из Pasteurella multocida, Mannehimia haemolytica, Histophilus somnim, Fusobacterium necrophorum, Bacteroides melaninogenicus, Escherichia coli, Arcanobacterium pyogenes и Fusobacterium necrophorum.
13. Инъецируемая ветеринарная композиция, содержащая хинолон и цефалоспорин или их фармацевтически приемлемые соли с пропиленгликоля дикаприлокапратом и/или глицерилкаприлокапратом и по меньшей мере еще один терапевтический агент в масляной суспензии, для лечения бактериальной инфекции у животного.
| WO 9841207 A1, 24.09.1998 | |||
| КОМПОЗИЦИИ И СПОСОБ ДЛЯ ЛЕЧЕНИЯ МИКРОБНЫХ И ПАРАЗИТАРНЫХ ИНФЕКЦИЙ У КРУПНОГО РОГАТОГО СКОТА И ДРУГИХ ЖИВОТНЫХ | 2004 |
|
RU2359667C2 |
| US 5079007 B1, 07.01.1992 | |||
| CHRISTENSEN JM et al., The disposition of five therapeutically important antimicrobial agents in lamas, J.Vet | |||
| Pharmacol | |||
| Ther.,1996, 19(6) | |||
| Приспособление для удержания и защиты диафрагмы в микрофонной коробке | 1925 |
|
SU431A1 |
Авторы
Даты
2018-01-23—Публикация
2013-07-03—Подача