1. Область техники, к которой относится изобретение
Изобретение относится к области биологически активных соединений и способам их получения. Впервые синтезировано новое химическое соединение - 7-(4-метоксифенил)-5-фенил-4,5-дигидро-[1,2,4]триазоло[1,5-а]пиримидин, который может быть использован в качестве активатора глюкокиназы и ингибитора дипептидилпептидазы типа 4 при лечении сахарного диабета 2-ого типа.
2. Уровень техники
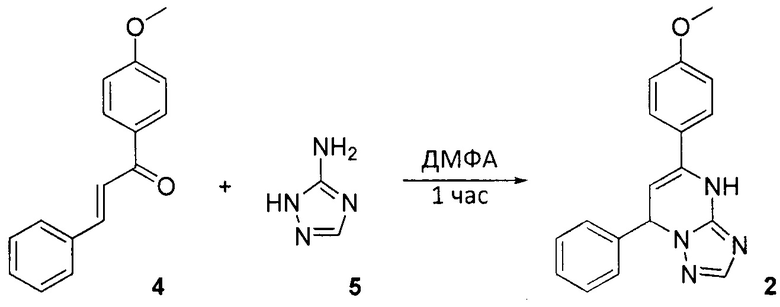
В литературе описаны структурные аналоги 7-(4-метоксифенил)-5-фенил-4,5-дигидро-[1,2,4]триазоло[1,5-а]пиримидина (1): 7-фенил-5-(4-метоксифенил)-4,7-дигидро-[1,2,4]триазоло[1,5-а]пиримидин (2) - прототип, - и 7-фенил-5-(4-метоксифенил)-6,7-дигидро-[1,2,4]триазоло[1,5-а]пиримидин (3) [Orlov V.D., Desenko S.М, Potekhin K.А., Struchkov Y.Т. // Chem. Heterocycl. Compd. 1988. Vol. 24. №2, P. 192-196], [Desenko S.M.,. Orlov V.D., Shishkin О.V., Barykin K.E., Lindenman Y.Т., Struchkov S.V. // Khimiya Geterotsiklicheskikh Soedin. 1993. №10. P. 1357-1363], которые являются таутомерными формами друг друга и отличаются от вещества 1 тем, что имеют другое расположение заместителей и атомов водорода в -[1,2,4]триазоло[1,5-а]пиримидиновом ядре. Кроме того, в литературных источниках не найдены упоминания о биологической активности соединений 2 и 3.
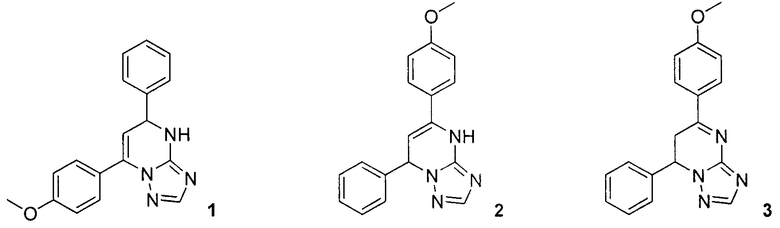
Соединение 2 получают с помощью реакции конденсации халкона (4) и 3-амино-[1,2,4]триазола (5) путем кипячения в диметилформамиде (ДМФА) в течение одного часа [Orlov V.D., Desenko S.М., Potekhin K.A., Struchkov Y. Т. // Chem. Heterocycl. Compd. 1988. Vol. 24, №2. P. 192-196]:
Аналогом по назначению является ряд соединений, вышедших на стадию клинических испытаний. Известно соединение RO4389620 (Piragliatin) (Hoffman LaRoche) [Пат. США №2003225283 Substituted-cycloalkyl and oxygenated-cycloalkyl glucokinase activators], которое было одним из первых активаторов глюкокиназы, интенсивно исследовавшихся в клинике. Препарат изучался в качестве монотерапии, а также в комбинации с метформином и симвастатином, и дошел до II фазы клинического исследования, которое, однако, было прекращено. Причины - недостаточная клиническая эффективность (снижение концентрации глюкозы в крови составило не более 30-35%), а также побочные эффекты у некоторых пациентов (гипогликемия) [J. Zhi, S. Zhai // J. Clin. Pharmacol. 2016. Vol. 56, №2. P. 231-238]. Известен аналог заявленного технического решения по назначению - соединение PF-04937319 (Pfizer), дошедшее до II фазы клинических исследований. Однако в 2015 году клинические исследования были прекращены вследствие недостаточной эффективности и нестабильности наблюдаемых эффектов [Amin N.B. // Diabetes, Obes. Metab. 2015. Vol. 17, №8. P. 751-759].
Несколько соединений в настоящее время проходит различные фазы клинических испытаний как ингибиторы ДПП4. Среди них можно выделить производное пиразолопиримидина анаглиптин (SK-0403, Sanwa Kagaku Kenkyusho), проходящий фазу III клинических испытаний. Он продемонстрировал способность эффективно ингибировать активность ДПП4, улучшать гликемический контроль, а также хорошую переносимость пациентами [Yang Н.K., Min K.W., Park S.W., Chung C.H., Park K.S., Choi S.H., Baik S.H. // Endocrine journal. 2015. Vol. 6, №. 5. P. 449-462]. Производное имидазопиридазина E-3024 (Eisai) вышло на I фазу испытаний [Yasuda N., Nagakura Т., Inoue Т., Yamazaki K., Katsutani N., Takenaka O., Clark R., Matsuura F., Emori E., Yoshikawa S., Kira K., Ikuta H., Okada Т., Saeki Т., Asano O., Tanaka I. // Eur. J. Pharm. 2006. Vol. 548. P. 181-187]. Соединение RO-0730699 (Hoffmann-LaRoche) было исключено из фазы II клинических испытаний по неизвестным причинам [Juillerat-Jeanneret L. // J. Med. Chem. 2014. Vol. 57, №6. P. 2197-2212].
Проведенный заявителем анализ уровня техники российских и зарубежных патентных баз данных, научной литературы и Интернет-ресурсов показал, что существуют аналоги заявленного технического решения по назначению, способные активировать ГК или ингибировать ДПП4, которые, однако, обладают значительными недостатками, а именно недостаточно высокой эффективностью и/или существенными побочными эффектами. Аналоги, обладающие активностью относительно обоих ферментов одновременно, неизвестны и в литературе не описаны.
3. Раскрытие изобретения
На сегодняшний день существует высокая потребность в создании и внедрении в клиническую практику новых, эффективных, безопасных препаратов для лечения сахарного диабета II типа. Одной из наиболее перспективных мишеней для создания новых противодиабетических средств является глюкокиназа (ГК) [Nauck М.А. // Diabetologia. 2016. Vol. 59, №2. P. 227-228] и дипептидилпептидаза типа 4 (ДПП4). ГК оказывает большое влияние на гомеостаз глюкозы: выступает в качестве «сенсора» глюкозы в β-клетках поджелудочной железы, регулируя уровень секреции инсулина, а также контролирует скорость гликолиза в печени. Активаторы глюкокиназы представляют собой новый класс перспективных противодиабетических препаратов, которые обладают гипогликемическим эффектом благодаря повышению активности глюкокиназы печени и поджелудочной железы, что доказано в доклинических исследованиях [Matschinsky F.M. //Nat. Rev. Drug Discov. 2009. Vol. 8, №5. P. 399-416].
Препараты группы ингибиторов ДПП4 воздействуют сразу на несколько патогенетических механизмов сахарного диабета 2 типа и характеризуются более высоким профилем безопасности, чем большинство традиционных пероральных гипогликемических средств. Существуют данные, указывающие на способность ингибиторов ДПП-4 улучшать секрецию инсулина, замедлять апоптоз островковых клеток и даже формировать инсулинпозитивные клетки, которые начинают вырабатывать инсулин [Mu J., Woods J., Zhou Y.P., Roy R.S., Li Z., Zycband E., Feng Y., Zhu L., Li C., Howard A.D. et al. // Diabetes. 2006. Vol. 55, №6. P. 1695-1704]. Применение ингибиторов ДПП4 позволяет оптимизировать фармакотерапию пациентов с сахарным диабетом 2 типа [Liu Y., Hu Y. // Future Med. Chem. 2014. Vol. 6, №7. P. 793-808].
Таким образом, задачей изобретения является поиск нового химического соединения, обладающего биологической активностью в отношении глюкокиназы и дипептидилпептидазы типа 4 одновременно и разработка способа его получения. Поставленная задача решается новым химическим соединением - 7-(4-метоксифенил)-5-фенил-4,5-дигидро-[1,2,4]триазоло[1,5-а]пиримидином (1), проявляющим свойства активатора глюкокиназы, и ингибитором дипептидилпептидазы одновременно и его синтезом через реакцию присоединения фенилмагнийбромида к 7-(4-метоксифенил)-[1,2,4]триазоло[1,5-а]пиримидину (6), с последующей нейтрализацией водным раствором хлорида аммония образовавшегося интермедиата - N-магниевой соли 7-(4-метоксифенил)-5-фенил-4,5-дигидро-[1,2,4]триазоло[1,5-а]пиримидина (7):
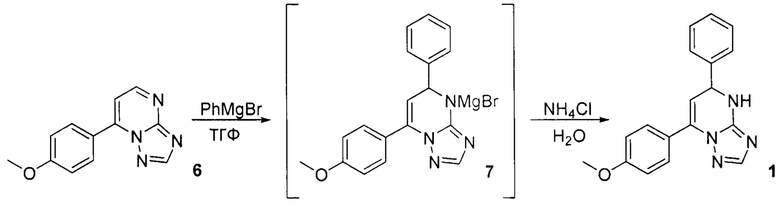
Соединение 1 синтезировано впервые, ранее в литературе не описывалось, а разработанный способ позволяет получать его в одну стадию с достаточно высоким выходом.
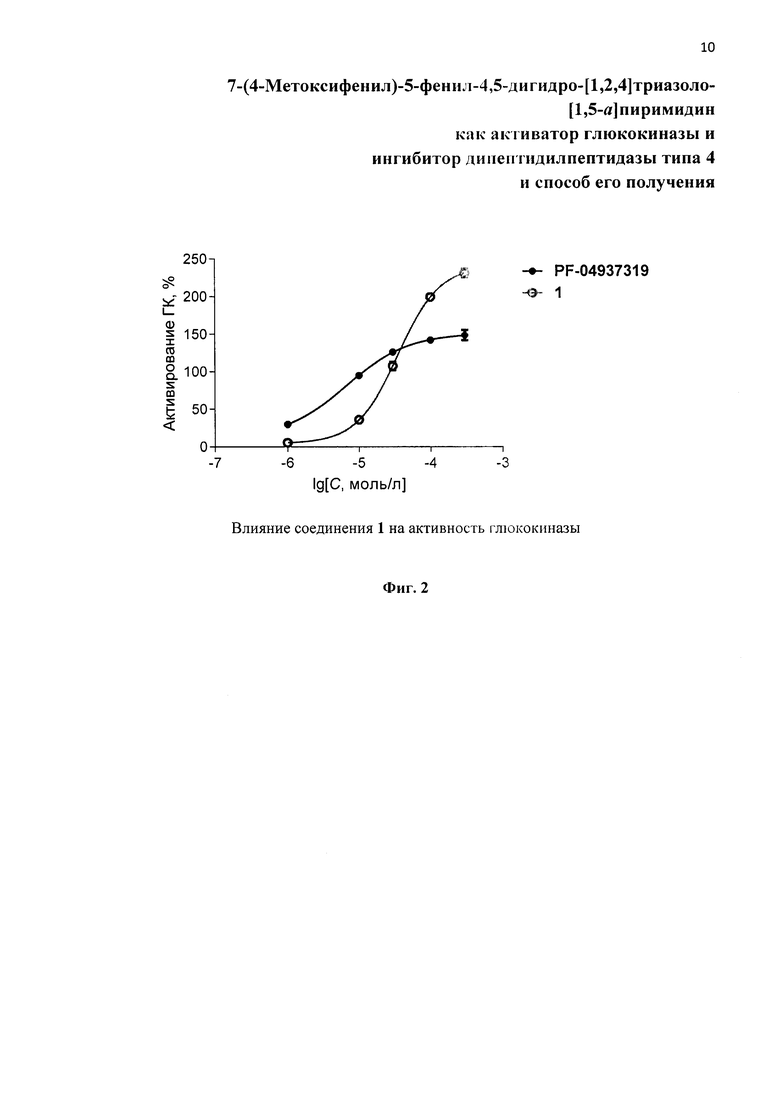
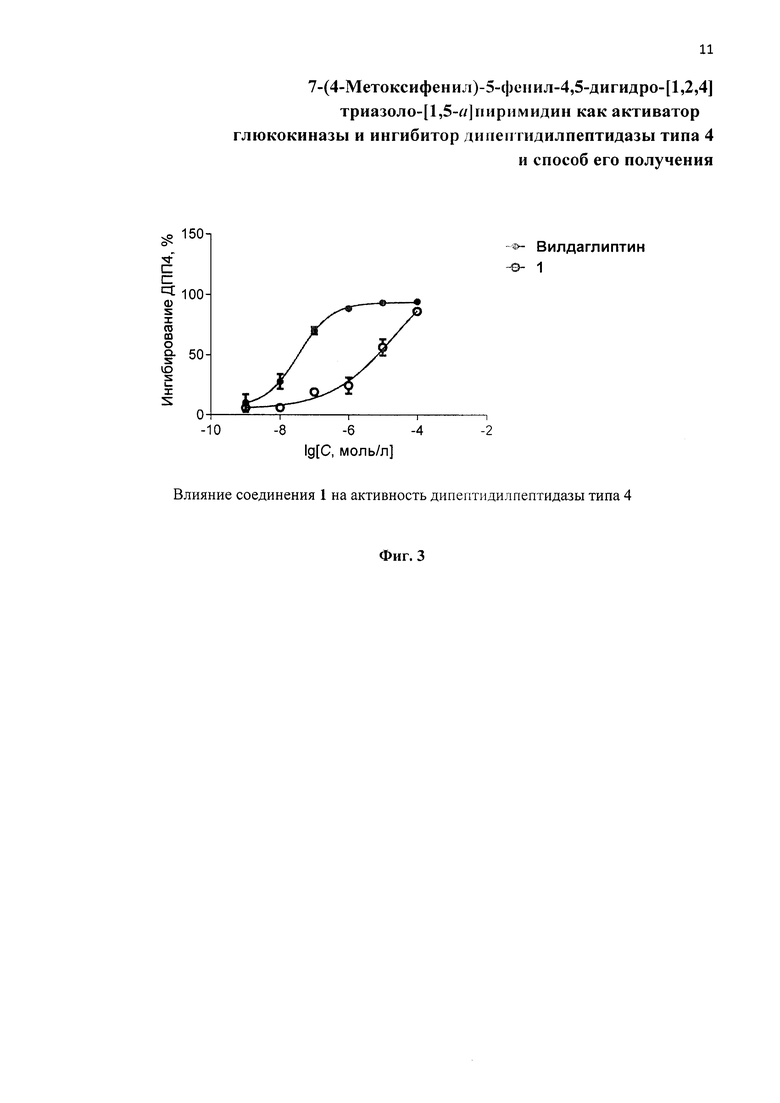
Соединение 1 статистически значимо повышает активность ГК в диапазоне концентраций 10-300 мкМ, в концентрациях более 50 мкМ превышая активность препарата сравнения PF-04937319. Также соединение 1 концентрационно-зависимо ингибирует активность дипептидилпептидазы типа 4 с величиной IC50 39,74 мкМ. Таким образом, по результатам проведенных исследований можно заключить, что производное азолоазинов 1 проявляет одновременно два вида активности - активирует глюкокиназу и ингибирует дипептидилпептидазу типа 4 - и обладает потенциальными антидиабетическими свойствами.
Заявленное техническое решение поясняется Фиг. 1, Фиг. 2. Фиг. 3.
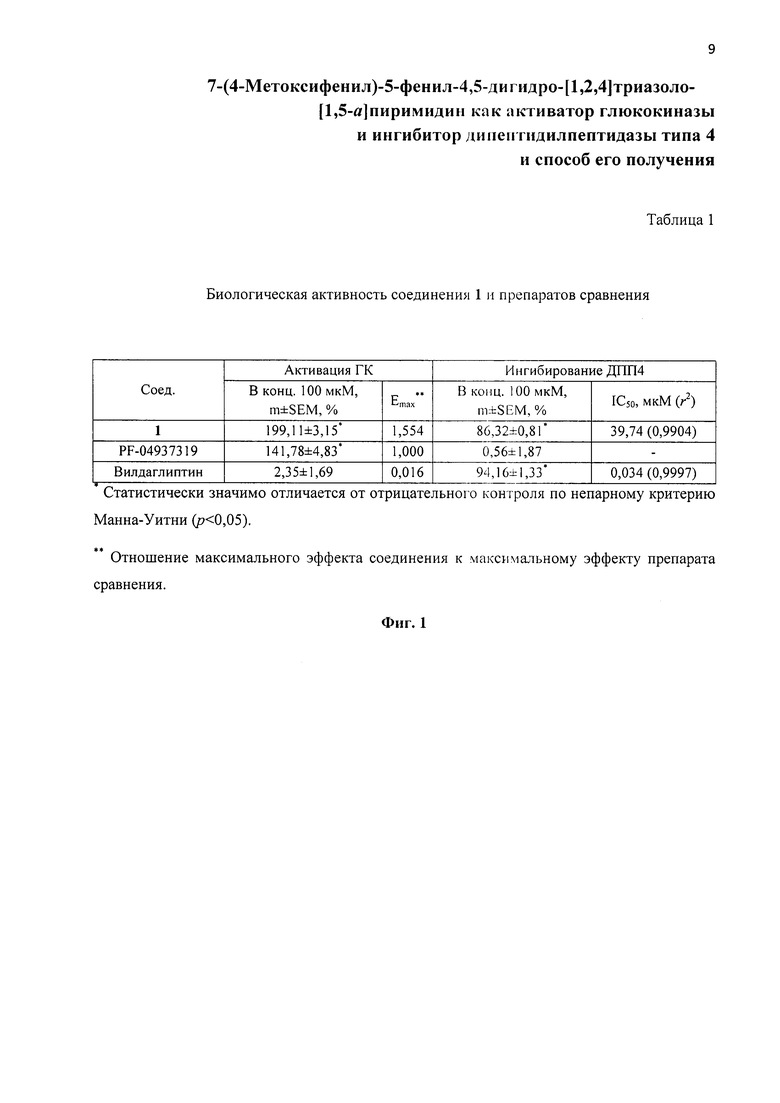
На Фиг. 1 представлена Таблица 1, в которой приведены данные о биологической активности соединения 1 относительно глюкокиназы и дипептидилпептидазы типа 4.
На Фиг. 2 представлен график, показывающий влияние соединения 1 и препарата сравнения на активность глюкокиназы. По оси ординат - активирование в %, по оси абсцисс - десятичный логарифм молярной концентрации активатора.
На Фиг. 3 представлен график, показывающий влияние соединения 1 и препарата сравнения вилдаглиптина на активность дипептидилпептидазы типа 4. По оси ординат - ингибирование в %, по оси абсцисс - десятичный логарифм молярной концентрации ингибитора.
Общее описание способа получения.
В сухой, перемешиваемой емкости, в инертной атмосфере готовят раствор фенилмагнийбромида либо используют коммерчески доступный раствор фенилмагнийбромида в диэтиловом эфире или тетрагидрофуране. охлаждают до (-50°С) - (-90°С) и вносят 7-(4-метоксифенил)-[1,2,4]триазоло[1,5-а]пиримидин, затем нагревают до (+20°С)-(+50°С) в течение 2 часов. Затем, сохраняя инертную атмосферу, реакционную смесь нейтрализуют водным раствором хлорида аммония и удаляют органический растворитель. Образовавшийся осадок соединения 1 фильтруют и перекристаллизовывают из этилового спирта. Выход 72,1-77,3%.
Пример 1.
В предварительно прогретой в сухожаровом шкафу и охлажденной в эксикаторе двугорлой колбе, снабженной магнитной мешалкой, термометром, обратным холодильником, создают инертную, сухую атмосферу и помещают 36,5 мг магния (1,5 ммоль), свежеперегнанный тетрагидрофуран (ТГФ) и 157,0 мкл бромбензола (1,5 ммоль). После растворения магния реакционную смесь охлаждают до -90°С и вносят 226,0 мг 7-(4-метоксифенил)-[1,2,4]триазоло[1,5-а]пиримидина (1 ммоль), нагревают до 50°С за 2 часа. Затем, сохраняя инертную атмосферу, реакционную смесь нейтрализуют раствором 107,0 мг (2 ммоль) хлорида аммония в 2 мл воды и удаляют ТГФ на ротационном испарителе. Образовавшийся осадок соединения 1 фильтруют и перекристаллизовывают из этилового спирта. Выход 235,0 мг (77,3%) в виде кристаллического белого осадка с температурой плавления 156°С, не растворимого в воде, растворимого в горячем этаноле и диметилсульфооксиде (ДМСО).
Заявляемое соединение - 7-(4-метоксифенил)-5-фенил-4,5-дигидро-[1,2,4]триазоло[1,5-а]пиримидин (1) имеет следующие физико-химические характеристики: 1Н NMR (400 MHz, DMSO-d6) δ 8.14 (d, J=2.5 Hz, 1H), 7.61-7.50 (m, 3H), 7.44-7.32 (m, 4H), 7.35-7.26 (m, 1H), 7.01-6.92 (m, 2H), 5.43 (d, J=1.8 Hz, 2H), 3.78 (s, 3H). 13C NMR (101 MHz, DMSO-d6) δ 159.80, 153.44, 149.14, 143.72, 134.12, 129.71, 128.67, 127.59, 126.18, 124.19, 113.45, 106.40, 55.22, 54.18. Вычислено: С, 71.04; H, 5.30; N, 18.41; О, 5.26. Найдено: С, 71.11; Н, 5.36; N, 18.35.
Физико-химические характеристики соединения 1 полностью соответствуют приписываемой структуре.
Пример 2.
Активность глюкокиназы (ГК человеческой печени рекомбинантная, экспрессированная в Е. coli, Sigma, США) определяют посредством сопряженной реакции образования глюкозо-6-фосфата с генерацией НАДН с помощью глюкозо-6-фосфатдегидрогиназы (Г6ФДГ L. mesenteroides, 550-1100 ЕД/мг, Sigma, США). Анализ проводят при 37°С в 96-луночном прозрачном полистиреновом планшете с плоским дном (Costar 9018, США) в конечном инкубируемом объеме 210 мкл. Инкубационная смесь содержит: 25 мМ HEPES (рН 7,2), 25 мМ КСl, 5 мМ D-глюкозы, 1 мМ АТФ, 1,8 мМ НАД, 2 мМ MgCl2, 1 мМ дитиотретола, тестируемое соединение или 5% ДМСО, 1,8 ед/мл Г6ФДГ и 2 мкг/мл ГК. Тестируемые соединения вносят в 5% ДМСО и предварительно инкубируют с ГК в термостатируемом шейкере PST-60HL (Biosan, Латвия) в течение 10 мин до достижения температурного равновесия, а затем инициируют реакцию введением 10 мкл раствора D-глюкозы [Sigma quality control test procedure: Enzymatic assay of glucokinase (EC 2.7.1.2) principle. 1995. P. 7-10]. За меру активности ГК принимают повышение оптической плотности при длине волны 340 нм в течение 20 мин инкубирования после начала реакции. Измерения проводят с помощью микропланшетного ридера Infinite М200 PRO (Тесаn, Австрия). В лунки, содержащие 5% ДМСО без тестируемого соединения, добавляют ГК в количестве, достаточном для того, чтобы за 20 мин инкубирования достичь повышения оптической плотности от 0,08 до 0,1 ед. Предварительными опытами установлено, что реакция ГК в течение этого периода времени остается линейной. Активность ГК в контрольных лунках сравнивают с активностью в лунках, содержащих тестируемые активаторы ГК. В качестве положительного контроля используют PF-04937319 (CAS 1245603-92-2, Sigma, США) [Amin N.B. et al. // Diabetes, Obes. Metab. 2015. Vol. 17, №8. P. 751-759].
Пример 3.
Для оценки ингибиторной активности соединений в отношении дипептидилпептидазы-4 вносят 40 мкл плазмы крови здоровых добровольцев в 50 мкл 0,1 М Трис-HCl буферного раствора (рН 8,0). В полученную смесь добавляют 10 мкл раствора исследуемого вещества заданной концентрации в Трис-буферном растворе и преинкубируют при 37°С в течение 5 мин. Затем вносят в реакционную смесь 100 мкл 1 мМ раствора субстрата дипептидилпептидазы-4 Gly-Pro-p-нитроанилида (Sigma, США). Инкубируют при 37°С в течение 15 мин и регистрируют образование п-нитроанилина по величине оптической плотности при длине волны 405 нм [Matheeussen V. et al. // Clin. Chim. Acta. 2012. Vol. 413, №3-4. P. 456-462.], используя микропланшетный ридер Infinite M200 PRO (Tecan, Австрия). В качестве положительного контроля используют вилдаглиптин (Sigma, США) [Pi-Sunyer F.X. et al. // Diabetes Res. Clin. Pract. 2007. Vol. 76, № 1. P. 132-138].
| название | год | авторы | номер документа |
|---|---|---|---|
| Энантиомеры 6-этоксикарбонил-7-(тиен-2-ил)-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 6-этоксикарбонил-7-фенил-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, обладающие туберкулостатической активностью | 2017 |
|
RU2654463C1 |
| Соединения на основе пиридоксина, обладающие способностью активировать фермент глюкокиназу | 2017 |
|
RU2644355C1 |
| 2-(5-НИТРОНИЛФУРАН-2-ИЛ)-5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-А]ПИРИМИДИН-7(4Н)-ОН И ЕГО СОЛИ | 2018 |
|
RU2716715C2 |
| БИС[1,2,4]ТРИАЗОЛО[4,3-b:3',4'-f][1,2,4,5]ТЕТРАЗИНЫ, ОБЛАДАЮЩИЕ АНТИГЛИКИРУЮЩЕЙ, АНТИГЛИКОКСИДАЦИОННОЙ И АНТИАГРЕГАНТНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2755897C1 |
| 2-ФУРИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-а]ПИРИМИДИН-7-ОН | 2016 |
|
RU2620594C1 |
| Способ получения 6-этоксикарбонил-7-(тиен-2-ил)-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, обладающего высокой туберкулостатической активностью | 2017 |
|
RU2642420C1 |
| Способ получения 6-бензилоксикарбонил-5-метил-7-(гет)арил-4,7-дигидроазоло[1,5-a]пиримидинов, в том числе активных в отношении вируса гриппа A/H1N1 | 2024 |
|
RU2836465C1 |
| ИНЪЕКЦИОННЫЙ ИЛИ ИНФУЗИОННЫЙ РАСТВОР L-АРГИНИНИЕВОЙ СОЛИ 5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-а]ПИРИМИДИН-7-ОНА МОНОГИДРАТА ДЛЯ ТЕРАПИИ ГРИППА И ДРУГИХ ВИРУСНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2586283C1 |
| СЕЛЕКТИВНЫЕ ПРОТИВОТУБЕРКУЛЕЗНЫЕ АГЕНТЫ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ ЗАМЕЩЕННЫЕ 7-АРИЛ(ГЕТЕРИЛ)-6-КАРБЭТОКСИ-4,7-ДИГИДРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНЫ ИЛИ ЗАМЕЩЕННЫЕ 7-АРИЛ(ГЕТЕРИЛ)-4,7-ДИГИДРО-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ АДДИТИВНЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 7-АРИЛ(ГЕТЕРИЛ)-6-КАРБЭТОКСИ-5-МЕТИЛ-4,7-ДИГИДРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНОВ | 2007 |
|
RU2360905C2 |
| НАТРИЕВАЯ СОЛЬ ДИЭТИЛОВОГО ЭФИРА 4-ОКСО-1,4-ДИГИДРОПИРАЗОЛО[5,1-C]-1,2,4-ТРИАЗИН-3,8-ДИКАРБОНОВОЙ КИСЛОТЫ, МОНОГИДРАТ | 2015 |
|
RU2612300C1 |
Изобретение относится к 7-(4-метоксифенил)-5-фенил-4,5-дигидро-[1,2,4]триазоло[1,5-а]пиримидину как активатору глюкокиназы и ингибитору дипептидилпептидазы типа 4:
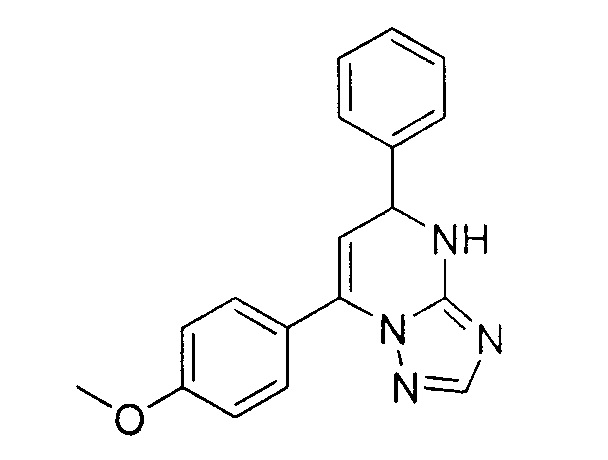 .
.
Изобретение также относится к его способу получения. Технический результат: получено новое соединение, которое может применяться в качестве активатора глюкокиназы и ингибитора дипептидилпептидазы типа 4. 2 н.п. ф-лы, 3 ил., 3 пр.
1. 7-(4-Метоксифенил)-5-фенил-4,5-дигидро-[1,2,4]триазоло[1,5-а]пиримидин как активатор глюкокиназы и ингибитор дипептидилпептидазы типа 4:
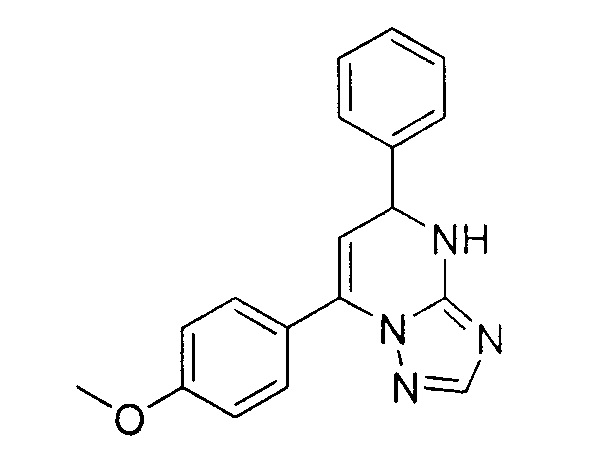
2. Способ получения соединения по п. 1, включающий взаимодействие 7-(4-метоксифенил)-[1,2,4]триазоло[1,5-а]пиримидина со свежеприготовленным фенилмагнийбромидом в диэтиловом эфире или тетрагидрофуране в инертной атмосфере при нагревании от (-90) - (-50) до (+20) - (+50) в течение 2 часов, затем нейтрализацию реакционной смеси хлоридом аммония, удаление тетрагидрофурана и перекристаллизацию целевого соединения из этилового спирта.
| В.Д | |||
| Орлов и др | |||
| "Циклоконденсация α,β-непредельных кетонов с 3-амино-1,2,4-триазолом" Химия Гетероциклических Соединений, N2, 1988, 229-233 | |||
| С.М | |||
| Десенко и др | |||
| "Имин-енаминная таутомерия дигидроазолопиримидинов | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| M | |||
| N | |||
| Shahi et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2018-01-25—Публикация
2017-06-19—Подача