Изобретение относится к медицине, в частности к иммунологии, и может применяться для лечения наркоманий, отравлений различными ядами в промышленности и быту, при техногенных катастрофах и т.п.
Изобретение представляет собой синтетический иммуноген для защиты от токсического действия наркотических и психоактивных веществ. Иммуноген выполнен в виде конъюгата макромолекулярного носителя, выбранного из ряда: природный или искусственный белок, олиго- и полипептид, углевод, липид или нуклеотид, и гаптена - наркотического или психотропного соединения, связанного с синтетическим полимером, отличающийся тем, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы I
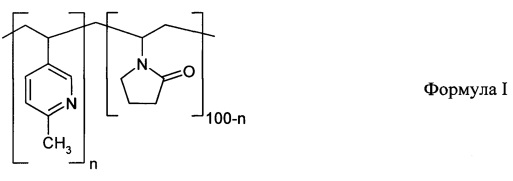
где n равно 25-50 мол. %, а средневязкостная молекулярная масса Мη равна 15-45 кДа, или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы II
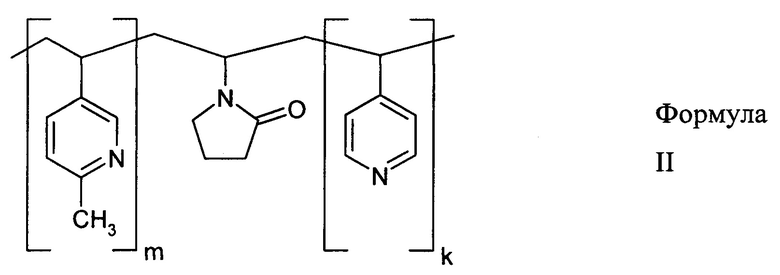
где (m+k) составляет 20-90 мол. %, при этом доля мономерных звеньев 4-винилпиридина составляет от 0,05(m+k) до 0,30(m+k), а средневязкостная молекулярная масса Мη равна 15-250 кДа. Из уровня техники известен синтетический иммуноген для терапии и профилактики злоупотреблений наркотическими веществами (в частности, опиатной зависимости), представляющий собой конъюгат в виде носителя - природного или искусственного белка и гаптена - наркотического или психотропного соединения. Причем в качестве носителя он содержит бычий сывороточный альбумин или синтетические полипептиды и гликопротеины, а в качестве гаптена - морфин, или кодеин, или героин, или метадон, или т.п. (см. Ковалев И.Е., Полевая О.Ю. Биохимические основы иммунитета к низкомолекулярным химическим соединениям. М.: Наука, 1985).
Однако этот иммуноген имеет балластные примеси, снижающие его терапевтическую (иммуностимулирующую) активность и требует применения больших доз (до 20 мг/кг). Кроме того, продолжительность иммунизации доходит до 6 месяцев, а достижение стабильного и/или пролонгированного иммунитета не всегда возможно.
Известен иммуноген, представляющий собой конъюгаты производных морфина (6-гемисукцинильного и 3-О-карбоксиметильного) с белком-носителем (столбнячный анатоксин), способный, по результатам доклинических испытаний на грызунах, запускать синтез поликлональных антител к опиатам - морфину и его структурному аналогу героину - в результате повторного введения этих препаратов при активной иммунизации (ЕР 1767221 А2, 28.03.2007; US 20080241183 А1, 10.02.2008; US 008,008,457 В2, 30.08.2011). При введении такого иммуногена в крови появляются в высоких титрах антитела к этим опиатам, способные связать поступающие в организм извне наркотики в кровяном русле и воспрепятствовать тем самым их проникновению в мозг через гематоэнцефалический барьер. В результате снижения положительного подкрепления угасает влечение к опиатам (морфину и его производным, в частности, героину), что было показано на модели внутривенного самовведения этих наркотиков грызунами.
Недостатком этого иммуногена является нестабильность такого соединения, приводящая к самопроизвольному распаду на исходные составляющие, пусть даже в незначительных количествах.
Известен синтетический иммуноген для терапии и профилактики злоупотреблений наркотическими и психоактивными веществами (патент RU 2236257 С1, 15.09.2003), который представляет собой конъюгат в виде носителя - природного или искусственного белка (яичный альбумин, человеческий гаммаглобулин, микробные токсины) и наркотического или психотропного соединения из следующих групп низкомолекулярных соединений: ароматические пропанамины, или изохинолины, или дифенилметаны, или индоламины, или производные барбитуровой кислоты, или производные замещенных пиперидинов. Конъюгат модифицирован иммунокомпетентным полиэлектролитом - полиоксидонием.
К недостаткам этого иммуногена можно отнести то, что получение предлагаемого конъюгата требует использования либо высокотоксичного и канцерогенного бензидина, либо сукцинилдихлорида, обладающего лакриматорными свойствами, высокой токсичностью и коррозионной активностью.
Известно также средство для профилактики и лечения опийной наркомании (патент RU 2264228, 20.11.2005), представляющее собой иммуноген - первичные моноклональные антитела к опиатам, в частности к конъюгату морфин-3БСА, при иммунизации которыми в организме животного или человека должны образовываться антиидиотипические (вторичные) антитела. Механизм действия такого средства, по мнению автора, связан с модификацией образуемыми антиидиотипическими антителами периферических опиоидных рецепторов, что отраженным образом может влиять на опиоидную систему мозга.
Недостатком этого средства является достаточно сложная и дорогая технология получения моноклональных антител (получение поликлональных антител проще и дешевле), а также тот факт, что эффект от иммунизации будет наблюдаться только в случае присутствия в крови определенного уровня вторичных (антиидиотипических) антител к опиатам (морфину). Употребление опиатов, которое может иметь место, несмотря на иммунизацию, не будет дополнительно стимулировать выработку вторичных (антиидиотипических) антител к опиатам (морфину).
В качестве ближайшего аналога настоящего изобретения авторы рассматривают конъюгат гаптен-носитель, который способен вызывать выработку антител против гаптена для лечения от зависимости от психоактивных веществ, представляющий собой конъюгат макромолекулярного носителя, гаптена, который выполнен в виде сополимерных частиц, нековалентно связанный с конъюгатом (европейский патент ЕР 1329226 А2, 23.07.2003).
Задачей настоящего изобретения является создание иммуногена, который не требует для своего получения использования поли(4-нитрофенил)акрилата, трудноудаляемых и огнеопасных органических растворителей и при этом позволяет вызвать в организме стабильный иммунный ответ и уменьшает токсическое действие наркотиков и психоактивных веществ за счет стойкого повышения титра специфических антител к ним.
Поставленная задача решается тем, что в известном синтетическом иммуногене для защиты от токсического действия наркотических и психоактивных веществ, представляющем собой конъюгат макромолекулярного носителя, выбранного из природного или искусственного белка, олиго- и полипептида, углевода, липида или нуклеотида, и гаптена - наркотического или психотропного соединения, новым является то, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона.
Таким образом, изобретение представляет синтетический иммуноген вызывающий выработку антител специфичных по отношению к психоактивным веществам, представляющий собой конъюгат макромолекулярного носителя, выбранного из ряда: природный или искусственный белок, олиго- или полипептид, углевод, липид или нуклеотид, и гаптена - наркотического или психотропного соединения, и связанного с коньюгатом синтетического полимера, отличающийся тем, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы I

где n равно 25-50 мол. %, а средневязкостная молекулярная масса Mη равна 15-45 кДа, или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы II

где (m+k) составляет 20-90 мол. %, при этом доля мономерных звеньев 4-винилпиридина составляет от 0,05(m+k) до 0,30(m+k), а средневязкостная молекулярная масса Мη равна 15-250 кДа.
Предпочтительно в качестве макромолекулярного носителя, выбранного из группы природных белков иммуноген содержит человеческий гамма-глобулин или альбумин.
В качестве гаптена он может содержать наркотическое или психотропное соединение, выбранное из опиатов, например морфин, героин, кодеин; антагонистов опиоидных рецепторов, например, налтрексон налоксон; каннабиноидов, например дельта-9-тетрагидроканнабинол; амфетаминов, например амфетамин, метамфетамин, экстази; бензоилэкгонина и его производных, например кокаин; барбитуратов, например барбамил, фенобарбитал; бензодиазепинов, например гидезепам; метадона, фенциклидина, трициклических антидепрессантов, котинина и их производных и метаболитов.
Предпочтительно в качестве гаптена иммуноген содержит налтрексон.
Техническим результатом изобретения является более эффективная по сравнению с ближайшим аналогом иммунная реакция, которую заявляемый синтетический иммуноген обеспечивает за счет добавления к конъюгату синтетического полимера, в качестве которого применяют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы I или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы II. Таким образом, в стандартных условиях без применения трудноудаляемых и огнеопасных веществ возможно воспроизводить структуру иммуногена в заданном диапазоне соотношений компонентов, добиваясь увеличения длительности стойкого гуморального иммунитета и повышенного содержания специфических антител. Кроме того, в результате использования изобретения наблюдается снижение токсичности иммуногена, что связано с составом применяемых при его получении химических соединений.
Диапазон соотношений от 2 до 20 молей конъюгата на моль синтетического полимера обеспечивает стандартизацию и контроль фармакологического эффекта в заданных соотношениях при формировании и укрупнении структуры иммуногена. Предпочтительным является отношение 10:1 моль/моль, которое дает максимально возможную воспроизводимость и стабильность синтетического иммуногена.
Использование в предлагаемом синтетическом иммуногене конкретных носителей и гаптенов защищает организм человека от действия широкого спектра психоактивных и наркотических веществ.
Анализ известных технических решений позволяет сделать вывод о том, что предлагаемое изобретение не известно из уровня техники, что свидетельствует о его соответствии условию патентоспособности «новизна».
По мнению авторов, специалист не способен прийти к техническому решению, предлагаемому в соответствии с настоящим изобретением, исключительно на основании общих знаний и анализа известного уровня техники, что позволяет сделать вывод о его соответствии условию патентоспособности «изобретательский уровень».
Возможность приготовления синтетического иммуногена из доступных промышленно выпускаемых компонентов на традиционном оборудовании с помощью известных методик с достижением технических результатов свидетельствует о соответствии изобретения критерию «промышленная применимость».
Далее приведены примеры осуществления изобретения, способствующие более точному и полному пониманию его сути. Специалисту в данной области очевидны возможные модификации и замены, например, относящиеся к протоколам исследований, которые не выходят за рамки объема изобретения, определяемые его формулой.
Приведенные примеры подтверждают, но не ограничивают объем заявленных притязаний по настоящему изобретению.
1. Краткое описание таблиц и терминов
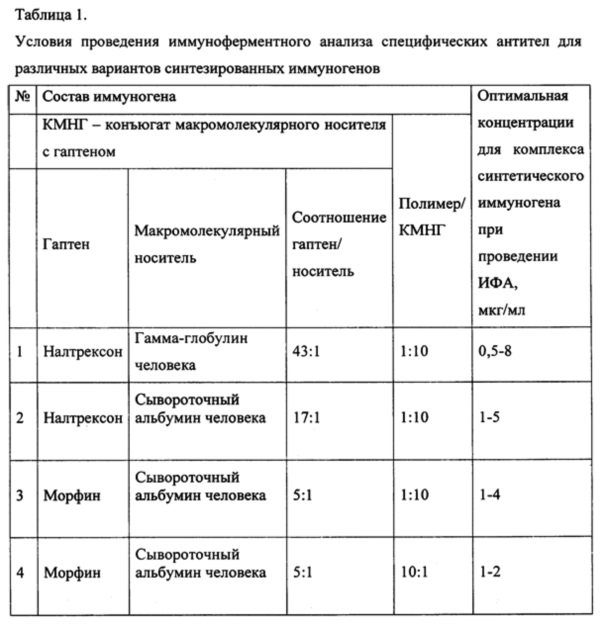
В Таблице 1 представлены данные по специфичности и доступности эпитопов иммуногена связывания с антителами в ИФА.
В Таблице 2 представлены обобщенные данные по изучению специфичности антител, полученных при иммунизации кроликов синтетическими иммуногенами.
В Таблице 3 представлены составы предлагаемого синтетического иммуногена и известного, взятого за прототип, а также данные по определению иммунологической активности и их фармакологического действия.
В настоящем изобретении под термином «ингибитор» понимается вещество, которое используют в процедуре конкурентного иммуноферментного анализа (ИФА) для оценки специфичности и аффинности антител. В качестве ингибиторов применяют соединения, структурно родственные гаптену, входящему в состав заявленного иммуногена, а также наркотические вещества и ряд психотропных лекарственных препаратов другой химической природы: это метадон, псевдоэфедрин, норэфедрин, барбамил, канабинол, морфин, героин, кодеин и др.
2. Синтез конъюгатов макромолекулярных носителей с гаптенами
Введение карбоксилсодержащих производных, способствующих проведению реакции связывания гаптена с макромолекулярным носителем, для опиатов, кокаина, барбитуратов, бензодиазепинов осуществляют их взаимодействием с ангидридом янтарной кислоты в абсолютированном растворителе.
Синтез карбоксилсодержащих производных каннабиноидов, амфетамина, метадона, фенциклидина, трициклических антидепрессантов, котинина проводят по реакции азосочетания с диазотированной 4-аминобензойной кислотой.
На основе модифицированных наркотических и психотропных веществ готовят конъюгаты, в которых эти вещества нековалентно связанны с макромолекулярными носителями.
Реакции конденсации карбоксилсодержащих производных гаптенов с макромолекулярным носителем осуществляют с использованием водорастворимого карбодиимида, глутарового альдегида или изобутилхлорформиата. Макромолекулярные носители содержат перечисленные выше гаптены.
Полученный конъюгат выделяли гель-хроматографией на колонке (2×50 см) с сефадексом G-25, уравновешенным в 0.05 М фосфатном буфере (pH 7.2). Скорость элюирования составляла 50 мл/ч, при этом отбирали белковую фракцию конъюгата, выходящую в свободном объеме колонки (250 мл). Контроль хроматографического процесса осуществляли с помощью проточной кварцевой ячейки Uvicord II фирмы «Pharmacia» (Швеция) при длине волны 280 нм с использованием регистрирующегося устройства и коллектора фракций той же фирмы. Концентрацию белка, присутствующего в элюированной фракции, определяли при длине волны 280 нм в спектрофотометре Genesys 10UV (Thermo Fisher Scientific, США).
Количество молей гаптена, связавшихся с макромолекулярным белковым носителем, определяют с помощью сравнительного спектрального анализа в ультрафиолетовой и видимой областях.
Пример 1. Синтез конъюгата морфина с человеческим сывороточным альбумином (М-ЧСА)
Раствор 65 мг (0,001 ммоль) человеческого сывороточного альбумина (ЧСА) в 5,0 мл дистиллированной воды смешивают с 3,0 мл 0,1М фосфатного буфера содержащего 15,0 мг (0,039 ммоль) 6-(3-(аминогексиламинокарбонил)-пропионат)морфина и при охлаждении по каплям прибавляют раствор 15 мг (0,055 ммоль) водорастворимого карбодиимида в 3 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.
Получают 25 мг конъюгата морфина с ЧСА (М-ЧСА), содержащего 5 молей морфина на моль белка.
Пример 2. Синтез конъюгатов амфетамина с человеческим сывороточным альбумином (А-ЧСА).
D,L-1-фенил-2-аминопропан (5 мг; 0,0369 ммоль) и (14 мг; 0,00022 ммоль) ЧСА растворяют в 3,0 мл 0,1 М фосфатного буфера. По каплям при комнатной температуре и перемешивании к реакционной смеси добавляют 50 мкл (0,4 ммоль) раствора глутарового альдегида. Постепенно реакционная смесь приобретает характерную желтую окраску, свидетельствующую об окончании реакции. Для остановки реакции к смеси добавляют 40 мкл 1М раствора лизина и инкубируют в течение 1 часа.
Полученный конъюгат диализируют против фосфатного буфера в течение ночи при температуре 4°С. Выделение конъюгата проводят колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.
Получают 5 мг конъюгата (А-ЧСА), содержащего 12 молей амфетамина на моль белка.
Пример 3. Синтез конъюгата кокаина с сывороточным альбумином человека (Кок-ЧСА)
Конъюгат кокаина с сывороточным альбумином человека (Кок-ЧСА) получают по методике примера 1 из 65 мг (0,001 ммоль) ЧСА и 4,55 мг (0,015 ммоль) бензоилэкгонина.
Выделяют 29 мг конъюгата Кок-ЧСА, содержащего 14 молей кокаина на моль белка.
Пример 4. Синтез конъюгата тетрагидроканнабинола с человеческим сывороточным альбумином (Δ9-ТГК-ЧСА).
К раствору 21 мг (3,3×10-3 ммоль) ЧСА в 3 мл дистиллированной воды прибавляют раствор 16,6 мг (0,05 ммоль) дельта-9-тетрагидроканнабинола, модифицированного реакцией азосочетания с диазотированной 4-аминобензойной кислотой в 2,0 мл 0,1 М фосфатного буфера, реакционную смесь охлаждают до 0°С и при перемешивании прибавляют 5 мг водорастворимого карбодиимида. Реакционную смесь выдерживают в течение 12 часов в холодильнике, отделяют выпавший осадок мочевины, а полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25).
Получают 10 мг конъюгата тетрагидроканнабинола с ЧСА (Δ9-ТГК-ЧСА), содержащего 15 молей гаптена на моль белка.
Пример 5. Синтез конъюгата налтрексона с человеческим сывороточным альбумином (Н-ЧСА).
Раствор 65 мг (0,001 ммоль) ЧСА в 17,0 мл дистиллированной воды смешивают с 4,0 мл 0,1 М фосфатного буфера, содержащего 12 мг (0,03 ммоль) сукцинилналтрексона, и при охлаждении по каплям прибавляют раствор 13 мг (0,04 ммоль) водорастворимого карбодиимида в 3 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.
Получают 27 мг конъюгата налтрексона с человеческим сывороточным альбумином (Н-ЧСА), содержащего 17 молей налтрексона на моль белка.
Пример 6. Получение конъюгата морфина с лизоцимом (М-Лиз).
К раствору 50 мг (3,33×10-3 ммоль) лизоцима в 2,5 мл 0,3 М раствора NaHCO3 прибавляют при охлаждении 0,3 мл раствора смешанного ангидрида 6-сукцинилморфина, полученного из 19,2 мг (0,05 ммоль) 6-сукцинилморфина и 6,0 мкл изобутилхлорформиата. Реакционную смесь инкубируют в течение 18 часов. При 4°С образовавшийся конъюгат морфина с лизоцимом выделяют гель-фильтрацией на колонке с Сефадексом G-25 и лиофильно высушивают.
Получают 30 мг конъюгата морфина с лизоцимом (М-Лиз). Количество присоединенного морфина вычисляют на основе УФ-спектров исходного белка и полученного конъюгата по изменению поглощения при 280 нм. В полученном конъюгате содержится 12 молей морфина на моль белка.
Пример 7. Получение конъюгатов морфина с полилизином (М-ПолиЛиз)
Раствор 50 мг (0,001 ммоль) полилизина (полиструктура пептидов) в 5,0 мл дистиллированной воды смешивают с 2,0 мл 0,1 М фосфатного буфера, содержащего 15,0 мг (0,039 ммоль) 6-сукцинилморфина, и при охлаждении по каплям прибавляют раствор 15 мг (0,055 ммоль) водорастворимого в 3 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.
Получают 25 мг конъюгата морфина с полилизином (М-ПолиЛиз), содержащего 10 молей морфина на моль белка.
Пример 8. Получение конъюгатов морфина с полилизином (М-ПолиЛиз)
Раствор 27 мг (0,0005 ммоль) полилизина в 30 мл 0,25 М раствора NaHCO3 добавляют к раствору смешанного ангидрида, содержащего 1,0 мг (0,003 ммоль) 3-О-карбоксиметилморфина. Смесь выдерживают при 0°С в течение ночи. Конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.
Получают 20 мг конъюгата морфина с полилизином (М-ПолиЛиз), содержащего 2 моля морфина на моль белка.
Пример 9. Получение конъюгата Δ9-тетрагидроканнабинола с гамма-глобулином (Δ9-ТГК-гамма-глобулин)
К раствору 15 мг (0,1×10-3 ммоль) гамма-глобулина в 3 мл дистиллированной воды прибавляют раствор 2,0 мг (0,006 ммоль) производного 4-карбосифенил-азо Δ9-тетрагидроканнабинола (каннабиноид) в 1,0 мл 0,1 М фосфатного буфера, охлаждают реакционную смесь до 0°С и при перемешивании добавляют 5 мг водорастворимого карбодиимида. Реакционную смесь выдерживают в течение 12 часов в холодильнике, удаляют выпавший осадок мочевины, конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.
Получают 12 мг конъюгата Δ9-тетрагидроканнабинола с гамма-глобулином (Δ9-ТГК-гамма-глобулин), содержащего 5 молей Δ9-тетрагидроканнабинола на моль белка.
Пример 10. Синтез конъюгированных антигенов амфетамина с дифтерийным токсином (А-Дт)
Аналогично примеру 2 используют D,L-1-фенил-2-аминопропан (2 мг; 0,014 ммоль) и 10 мг (0,00016 ммоль) белка дифтерийного токсина, которые растворяют в 2,0 мл 0,1 М фосфатного буфера.
Получают 7 мг конъюгата, содержащего 6 молей амфетамина на моль белка.
Пример 11. Получение конъюгата барбамила с гамма-глобулином человека (Б-ГГЧ)
Аналогично примеру 9 из раствора 15 мг (0,1×10-3 ммоль) гамма-глобулина в 3 мл дистиллированной воды, к которому прибавляют при охлаждении и перемешивании раствор 1,0 мл 0,1 М фосфатного буфера, содержащего 5,2 мг (0,02 ммоль) барбамила (производного барбитуровой кислоты) и 5 мг водорастворимого карбодиимида, получают 10 мг конъюгата барбамила с гамма-глобулином (Б-ГГЧ), содержащего 6 молей барбамила на моль белка.
Пример 12. Получение конъюгата налтрексона с гамма-глобулином человека (Н-ГГЧ)
Раствор 50 мг (0,0003 ммоль) гамма-глобулина в 40 мл дистиллированной воды смешивают с 15,0 мл 0,1 М фосфатного буфера, содержащего 30,0 мг (0,07 ммоль) сукцинилналтрексона, и при охлаждении по каплям прибавляют раствор 45 мг (0,16 ммоль) водорастворимого карбодиимида в 10 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.
Получают 35 мг конъюгата налтрексона с гамма-глобулином, содержащего 43 моля налтрексона на моль белка (Н-ГГЧ).
3. Получение синтетического иммуногена
Для получения синтетического иммуногена - комплекса, состоящего из конъюгата макромолекулярного носителя в виде природного или искусственного белка и гаптена - наркотического или психотропного соединения, нековалентно связанного с полимерной матрицей в качестве которой используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона необходимо соблюдать соотношение гаптена и макромолекулярного носителя в соответствии с предлагаемым изобретением. Коньюгат содержит указанные выше макромолекулярные носители и гаптены в различных соотношениях (Примеры 1-12).
Пример 13. Получение иммуногена, состоящего из конъюгата налтрексона с ЧСА (Н-ЧСА), связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=50 мол. % и Мη=15 кДа).
К раствору 180 мг конъюгата (Н-ЧСА), полученного в примере №5, в 30 мл 0,1 М фосфатного буфера (pH 7,2) добавляют 1600 мг синтетического полимера, представляющего сополимер 2-метил-5-винилпиридина и N-винилпирролидона, с n=50 мол. % и Mη=15 кДа. Смесь выдерживают в течение суток при 20°С. Полученный иммуноген лиофильно высушивают, в результате получают иммуноген, содержащий конъюгат гаптен/Н-ЧСА (12:1) и синтетический полимер в соотношении 1:10, структуру которого характеризуют с помощью ИФА, определяя доступность эпитопов гаптена налтрексона для связывания с антителами к опиатам (Таблица 1, №2).
Пример 14. Получение иммуногена, состоящего из конъюгата налтрексона с ГГЧ (Н-ГГЧ), связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона)
К раствору 300 мг конъюгата (Н-ГГЧ), полученного в примере 12, в 80 мл 0,1 М фосфатного буфера (pH 7,2) добавляют 2500 мг синтетического полимера, представляющего собой сополимер 2-метил-5-винил пиридина и N-винилпирролидона, с n=25 мол. % и Мη=45 кДа. Смесь выдерживают в течение суток при 20°С. Очистку иммуногена и его характеризацию осуществляют, как описано в примере 13.
Получают иммуноген, содержащий конъюгат налтрексон/Н-ГГЧ (43:1) и синтетический полимер в соотношении 1:10. Структуру иммуногена и доступность эпитопов гаптена характеризуют с помощью ИФА (Таблица 1, №1).
Пример 15. Получение иммуногена, состоящего из конъюгата ЧСА с морфином (М-ЧСА), и связанного с ним синтетическим полимером (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=20 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,05(m+k), Мη=250 кДа).
К раствору 13,5 мг синтетического полимера в 2 мл воды апирогенной добавляют 38 мг М-ЧСА, полученного в примере 1, содержащего в качестве гаптена 6-(3-(аминогексиламинокарбонил)-пропионат)морфина, в соотношении 5:1 выдерживают смесь в течение суток при 20°С. Полученный иммуноген характеризуют, как описано в примере 13.
Получают иммуноген, содержащий конъюгат налтрексон / М-ЧСА (5:1) и синтетический полимер в соотношении 1:10. Структуру иммуногена и доступность эпитопов гаптена характеризуют с помощью ИФА (Таблица 1, №3).
Пример 16. Получение иммуногена, состоящего из конъюгата ЧСА (М-ЧСА) с морфином, и связанного с ним синтетического полимера (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3(m+k), Mη=15 кДа), при соотношении 10 молей синтетического полимера на моль конъюгата.
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 6 мг синтетического полимера (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3(m+k), Мη=15 кДа) в 2 мл воды апирогенной и 2 мг М-ЧСА, полученного в примере 1, содержащего в качестве гаптена (6-(3-(аминогексиламинокарбонил)-пропионат)морфина.
Получают иммуноген, содержащий конъюгат морфин/М-ЧСА (5:1) и синтетический полимер в соотношении 1:10. Структуру иммуногена и доступность эпитопов гаптена характеризуют с помощью ИФА (Таблица 1, №4).
Пример 17. Получение иммуногена, состоящего из конъюгата полилизин (М-ПолиЛиз) с морфином, связанного с синтетическим полимером (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3 (m+k), Мη=15 кДа), при соотношении 1 моль конъюгата на 3 моля полимера.
Получение проводят аналогично примеру 14, только в качестве исходных соединений берут 5 мг синтетического полимера (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3(m+k), Мη=15 кДа), в 2 мл фосфатного буфера и 1,4 мг конъюгата М-ПолиЛиз, полученного в примере 7.
Получаемый комплекс имеет 3:1 замещение полимерной матрицы конъюгатом полилизина со спейсером (3-О-карбоксиметилморфина) по 3-му положению молекулы морфина.
Пример 18. Получение иммуногена, состоящего из конъюгата гамма-глобулина с Δ9-тетрагидроканнабинолом (Δ9-ТГК-гамма-глобулин), связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=25 мол. % и Мη=25 кДа) при соотношении 1 моль конъюгата на 2 моля полимера.
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 3,5 мг сополимера 2-метил-5-винилпиридина и N-винилпирролидона, где n=25 мол. % и Мη=25 кДа, в 1 мл фосфатного буфера и 1,2 мг конъюгата Δ9-ТГК-гамма-глобулин, полученного в примере 9. Получаемый комплекс имеет 2:1 замещение полимерной матрицы конъюгатом Δ9-ТГК-гамма-глобулин.
Пример 19. Получение иммуногена, состоящего из конъюгата дифтерийного токсина с амфетамином, связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=23 мол. % и Мη=45 кДа) при соотношении 1 моль конъюгата на 4 моля полимера.
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 3,5 мг сополимера 2-метил-5-винилпиридина и N-винилпирролидона, где n=23 мол. % и Mη=45 кДа в 1 мл фосфатного буфера и 0,9 мг конъюгата амфетамин-дифтерийный токсин, полученного в примере 10.
Получаемый комплекс имеет 4:1 замещение полимерной матрицы конъюгатом амфетамин-дифтерийный токсин.
Пример 20. Получение иммуногена, состоящего из конъюгата гамма-глобулина с барбамилом, связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=20 мол. % и Мη=35 кДа) при соотношении 1 моль конъюгата на 6 молей полимерной матрицы
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 3,5 мг сополимера 2-метил-5-винилпиридина и N-винилпирролидона, где n=20 мол. % и Мη=35 кДа в 3 мл фосфатного буфера и 0,5 мг конъюгата барбамил-гамма-глобулин, полученного в примере 11.
Получаемый комплекс имеет 6:1 замещение полимерной матрицы конъюгатом барбамил-гамма-глобулин.
4. Эксперименты in vivo
В экспериментах на животных показано, что полученные синтетические иммуногены способны индуцировать иммунные ответы с появлением антител, специфически взаимодействующих с гаптеном и нейтрализующие их активность в организме. В серии опытов была выяснена возможность нейтрализации токсического действия морфина на животных.
Пример 21. Кроличья модель интоксикации морфином
Кроликов распределяют на две группы с учетом возраста и массы тела так, чтобы средние показатели были сопоставимы. Группа контрольных животных состоит из восьми неиммунизированных кроликов, а опытная группа включает восемь кроликов, предварительно иммунизированных синтетическим иммуногеном морфин-ЧСА-синтетический полимер, полученным в примере 13. Для этого в течение месяца с интервалом 7 дней, делают инъекции по 0,2 мл в 4 точки вблизи позвоночника - в области лопаток и в области крестца из расчета в 200 мкг/кг на кролика.
Всем животным внутривенно вводят летальную дозу морфина (LD100). Все восемь кроликов контрольной группы погибают от указанной летальной дозы. Среди иммунизированных кроликов гибели не зарегистрировано ни в одном из восьми случаев, т.е. наблюдается высокая иммунологическая защита образовавшимися в процессе иммунизации специфическими антителами.
Пример 22. Крысиная модель интоксикации первитином
Аналогично примеру 21 проводят исследования в двух группах по шесть половозрелых беспородных крыс обоего пола. Животных из опытной группы иммунизируют синтетическим иммуногеном амфетамин-дифтерийный токсин-синтетический полимер из расчета 400 мкг/кг. Всем крысам вводят летальную дозу психоактивного вещества первитина.
Все животные контрольной группы, не получавшие иммуноген, погибли. Среди иммунизированных крыс гибели не зарегистрировано ни в одном из шести случаев, т.е. наблюдается высокая иммунологическая защита образовавшимися в процессе иммунизации специфическими антителами.
Пример 23. Крысиная модель интоксикации барбитуратом
Аналогично примеру 21 шесть половозрелых беспородных крыс обоего пола иммунизируют синтетическим иммуногеном барбамил-гамма-глобулин-синтетический полимер (гаптен из группы производных барбитуровой кислоты) из расчета 200 мкг/кг. Вводят летальную дозу снотворного - барбитурата.
В контрольной группе погибают все животные. Среди иммунизированных крыс гибели не зарегистрировано ни в одном из шести случаев, т.е. наблюдается полная иммунологическая защита образовавшимися в процессе иммунизации специфическими антителами.
Исследования по указанной выше схеме, выполненные для гаптенов, входящих в заявленный состав иммуногена, показали аналогичные результаты.
Пример 24. Определение специфичности антител, образующихся при иммунизации синтетическим иммуногеном
Специфичность определяют в тесте конкуренции ИФА. Для этого в твердофазном ИФА в качестве ингибиторов используют соединения, структурно родственные гаптену, входящему в состав заявленного иммуногена, а также наркотические вещества и ряд психотропных лекарственных препаратов другой химической природы.
Для каждого из этих соединений определяют концентрацию, при которой происходит 50% торможение взаимодействия антигаптеновых антител, с антигеном на твердой фазе. Специфичность вычисляют как отношение молярных концентраций исследуемого вещества и исходного гаптена и выражают в процентах. Данные о специфичности антител (в %) представлены в таблице 2.
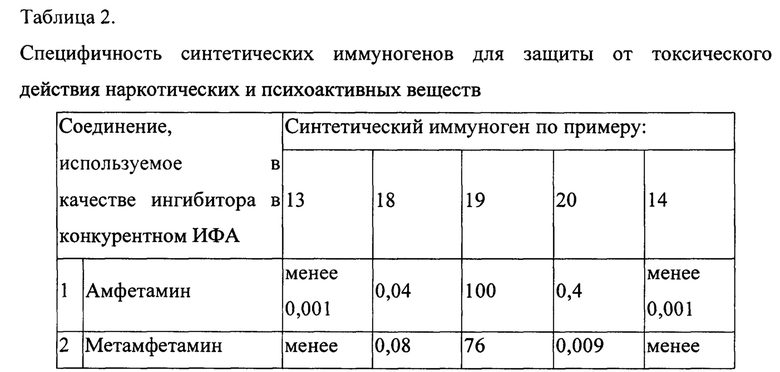
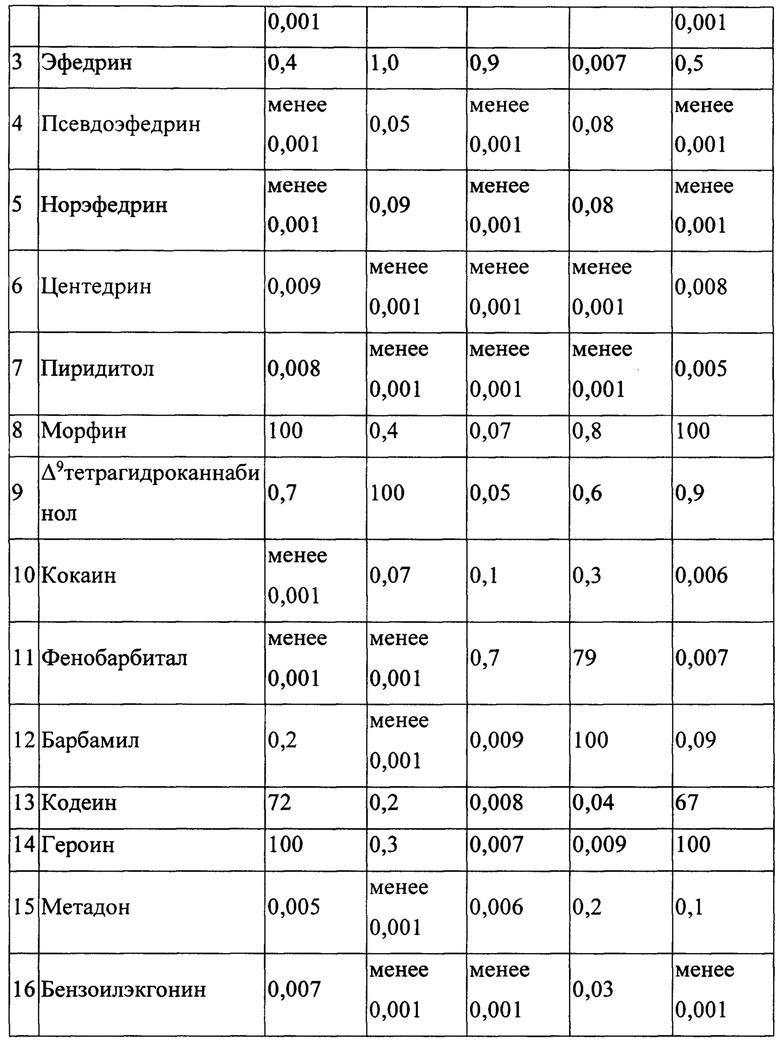
По данным таблицы 2 видно, что только иммунные кроличьи антитела к гаптенам, входящим в состав заявляемого иммуногена, не давали перекрестных реакций с соединениями других классов и в значительной степени реагировали со структурно родственными веществами. Так, для иммуногена, состоящего из конъюгата альбумина с налтрексоном (Н-ЧСА), связанного с синтетическим полимером (пример 13), образуются антитела, специфически реагирующие с морфином, героином и в чуть меньшей степени с кодеином. Перекрестные реакции отсутствуют с метадоном, амфетамином, каннабиноидами, кокаином и др. веществами, не относящимися к классу опиатов.
Аналогичные результаты получены и для иммуногена, состоящего из конъюгата гамма-глобулина (Н-ГГЧ) с налтрексоном, связанного с синтетическим полимером (пример 14).
Для иммуногена, состоящего из конъюгата гамма-глобулина с Δ9-тетрагидроканнабинолом (Δ9-ТГК-ГГЧ), связанного с синтетическим полимером, специфическая реакция антител наблюдается только для каннабиноидов (пример 18). Для иммуногена, состоящего из конъюгата альбумина с амфетамином (пример 19), связанного с синтетическим полимером антитела реагируют с амфетамином и в меньшей степени с метамфетамином при отсутствии реакции со структурами эфедрина, а также с соединениями других классов.
Для иммуногена, состоящего из конъюгата гамма-глобулина с барбамилом Б-ГГЧ), связанного с синтетическим полимером, полученные антитела взаимодействуют с барбамилом и в меньшей степени с фенобарбиталом, не давая перекрестных реакций с соединениями других классов (пример 20).
Таким образом, антитела, полученные иммунизацией животных искусственными синтетическими иммуногенами, могут быть использованы для нейтрализации вредного воздействия психоактивного вещества, что в свою очередь может быть использовано для защиты от токсического действия при злоупотреблениях наркотическими и психоактивными веществами.
Для подтверждения полученных данных в таблице 3 приведены дополнительные сведения об иммуногенах.

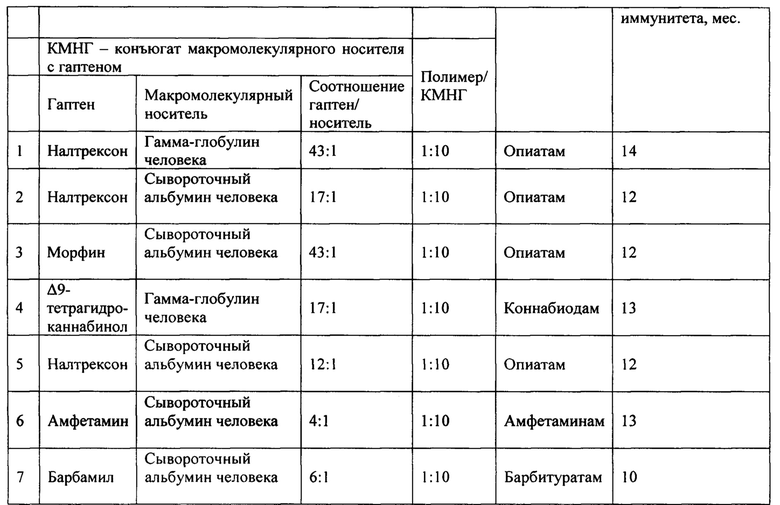
СП - синтетический полимер
КМНГ - конъюгат макромолекулярного носителя с гаптеном.
6. Иммунный ответ в крысиной модели
Пример 25. Интоксикация первитином
Шесть половозрелых крыс обоего пола иммунизируют синтетическим иммуногеном комплекс с конъюгатом : дифтерийный токсин : амфетамин и синтетическим полимером, полученным в примере 19, из расчета 400 мкг/кг.
Лабораторные данные: ИФА 1 мл - 75000 пмоль (через 5 недель после начала иммунизации). Вводили летальную дозу психоактивного вещества первитина.
Контрольные лабораторные данные: ИФА 1 мл - 54000 пмоль. Синтез антител, отсутствие аллергических реакций.
Пример 26. Интоксикация барбитуратом
Шесть половозрелых крыс обоего пола иммунизируют синтетическим иммуногеном комплекса с конъюгатом гамма-глобулин : барбамил : синтетическим полимером, полученным в примере 20, из расчета 500 мкг/кг.
Лабораторные данные: ИФА 1 мл - 76000 пмоль (через 5 недель после начала иммунизации). Вводили летальную дозу снотворного - барбитурата.
Контрольные лабораторные данные: ИФА 1 мл - 57000 пмоль. Синтез антител; отсутствие аллергических реакций.
Пример 27. Интоксикация героином
Шесть половозрелых крыс обоего пола иммунизируют синтетическим иммуногеном комплекс с конъюгатом овальбумин : морфин : синтетическим полимером, полученным в примере 15, из расчета 300 мкг/кг.
Лабораторные данные: ИФА 1 мл - 85000 пмоль специфических антител к героину (через 4 недели после начала иммунизации). Вводили летальную дозу наркотического вещества героина 100 мг/кг.
Контрольные лабораторные данные: ИФА 1 мл - 60000 пмоль. Синтез антител; отсутствие аллергических реакций.
Как видно из приведенных примеров и данных таблицы 3, введение заявляемого синтетического иммуногена позволяет вызывать образование в организме антител и стабильный иммунный ответ, что приводит к детоксикации организма в отношении соответствующих психоактивных и наркотических веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИНТЕТИЧЕСКИЙ ИММУНОГЕН ДЛЯ ЗАЩИТЫ И ЛЕЧЕНИЯ ОТ ЗАВИСИМОСТИ ОТ ПСИХОАКТИВНЫХ ВЕЩЕСТВ | 2016 |
|
RU2635517C1 |
| СИНТЕТИЧЕСКИЙ ИММУНОГЕН ДЛЯ ЗАЩИТЫ ОТ ТОКСИЧЕСКОГО ДЕЙСТВИЯ НАРКОТИЧЕСКИХ И ПСИХОАКТИВНЫХ ВЕЩЕСТВ | 2012 |
|
RU2526807C2 |
| СИНТЕТИЧЕСКИЙ ИММУНОГЕН ДЛЯ ТЕРАПИИ И ПРОФИЛАКТИКИ ЗЛОУПОТРЕБЛЕНИЙ НАРКОТИЧЕСКИМИ И ПСИХОАКТИВНЫМИ ВЕЩЕСТВАМИ | 2003 |
|
RU2236257C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАРКОТИЧЕСКИХ СРЕДСТВ В РОТОВОЙ ЖИДКОСТИ ЧЕЛОВЕКА МЕТОДОМ ИММУНОХРОМАТОГРАФИИ | 2010 |
|
RU2442988C1 |
| СПОСОБ ДИАГНОСТИКИ ПОТРЕБЛЕНИЯ НАРКОТИЧЕСКИХ ВЕЩЕСТВ | 2005 |
|
RU2291436C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ФАКТА ПОТРЕБЛЕНИЯ НАРКОТИЧЕСКИХ ВЕЩЕСТВ В ОТСУТСТВИЕ КЛИНИЧЕСКИХ ПРИЗНАКОВ СОСТОЯНИЯ ЗАВИСИМОСТИ ОТ НАРКОТИКОВ | 2005 |
|
RU2296332C1 |
| Способ определения наркотических средств в ротовой жидкости человека методом иммунохроматографии | 2010 |
|
RU2746467C1 |
| СПОСОБ ДИАГНОСТИКИ ФАКТА ПОТРЕБЛЕНИЯ НАРКОТИЧЕСКИХ ВЕЩЕСТВ | 2003 |
|
RU2250467C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К ЗАБОЛЕВАНИЯМ ЗАВИСИМОСТИ | 2008 |
|
RU2369872C1 |
| ИМПЛАНТИРУЕМОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ НАЛТРЕКСОНА ДЛЯ ЛЕЧЕНИЯ ПАЦИЕНТОВ, ЗАВИСИМЫХ ОТ АЛКОГОЛЯ ИЛИ ОПИАТОВ | 2012 |
|
RU2476209C1 |
Изобретение относится к медицине, в частности к иммунологии, и может применяться для защиты и лечения от зависимости от психоактивных веществ. Изобретение представляет собой синтетический иммуноген, выполненный в виде конъюгата макромолекулярного носителя, гаптена и синтетического полимера, нековалентно связанного с коньюгатом, отличающийся тем, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы I, где n равно 25-50 мол. %, а средневязкостная молекулярная масса Mη равна 15-45 кДа. Или представляет собой сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы II, где (m+k) составляет 20-90 мол. %, при этом доля мономерных звеньев 4-винилпиридина составляет от 0,05(m+k) до 0,30(m+k), а средневязкостная молекулярная масса Mη равна 15-250 кДа. Использование данного синтетического иммуногена позволяет вызвать в организме образование антител и стабильный иммунный ответ, что приводит к детоксикации организма в отношении психоактивных и наркотических веществ за счет добавления к конъюгату синтетического полимера. 3 з.п. ф-лы, 27 пр., 3 табл.
1. Синтетический иммуноген для защиты и лечения от зависимости от психоактивных веществ, представляющий собой конъюгат макромолекулярного носителя, гаптена и синтетического полимера, нековалентно связанного с коньюгатом, отличающийся тем, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы I
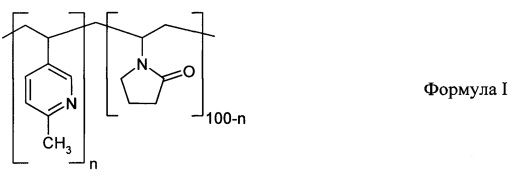
где n равно 25-50 мол. %, а средневязкостная молекулярная масса Mη равна 15-45 кДа, или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы II
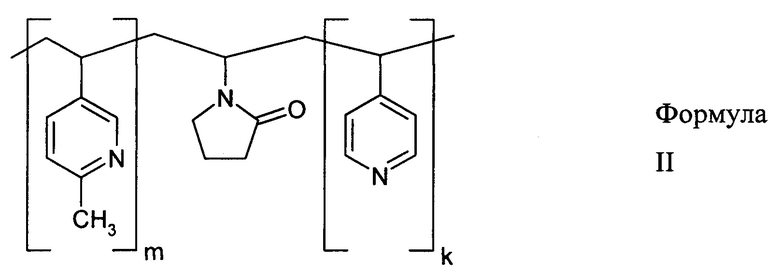
где (m+k) составляет 20-90 мол. %, при этом доля мономерных звеньев 4-винилпиридина составляет от 0,05(m+k) до 0,30(m+k), а средневязкостная молекулярная масса Mη равна 15-250 кДа.
2. Синтетический иммуноген для защиты и лечения от зависимости от психоактивных веществ по п. 1, отличающийся тем, что в качестве конъюгата макромолекулярного носителя, можно применить природный белок, или искусственный белок, или олигопептид, или полипептид, или углевод, или липид, или нуклеотид.
3. Синтетический иммуноген для защиты и лечения от зависимости от психоактивных веществ по п. 1, отличающийся тем, что в качестве макромолекулярного носителя можно применить человеческий гамма-глобулин или альбумин.
4. Синтетический иммуноген для защиты и лечения от зависимости от психоактивных веществ по п. 1, отличающийся тем, что в качестве гаптена можно применить налтрексон.
| EP 1329226 A2, 23.07.2003 | |||
| СИНТЕТИЧЕСКИЙ ИММУНОГЕН ДЛЯ ЗАЩИТЫ ОТ ТОКСИЧЕСКОГО ДЕЙСТВИЯ НАРКОТИЧЕСКИХ И ПСИХОАКТИВНЫХ ВЕЩЕСТВ | 2012 |
|
RU2526807C2 |
| СОПОЛИМЕР, СОДЕРЖАЩИЙ ЗВЕНЬЯ N-ВИНИЛПИРРОЛИДОНА, 2-МЕТИЛ-5-ВИНИЛПИРИДИНА И 4-ВИНИЛПИРИДИНА | 2011 |
|
RU2459838C1 |
| RU 2000004 C1, 15.02.1993 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ АЛКОГОЛИЗМА, НАРКОМАНИИ И ТОКСИКОМАНИИ С УЛУЧШЕННЫМ ПРОФИЛЕМ ВЫСВОБОЖДЕНИЯ НАЛТРЕКСОНА | 2011 |
|
RU2471478C1 |
Авторы
Даты
2018-01-31—Публикация
2016-09-14—Подача