Изобретение относится к области химической технологии, а именно к получению металлоорганического каркасного соединения с люминесцентными свойствами, которое можно использовать в качестве фотоактивного материала для преобразования инфракрасного излучения в видимый свет, а также в качестве материала для хранения и транспортировки газов и микропористых катализаторов различных процессов.
Металлоорганические каркасные соединения - это кристаллические пористые материалы, которые состоят из металл-оксидных нанокластеров, связанных между собой органическими лигандами-линкерами. Последние двадцать лет этот новый класс гибридных соединений привлекает к себе все большее и большее внимание благодаря своей необычной структуре и большой адсорбционной емкости и, как следствие, многообразием потенциальных путей применения этих соединений. Однако до сих пор существуют трудности при синтезе подобных соединений сложной структуры, с одной стороны. С другой стороны, происходит поиск путей создания металлоорганических каркасных соединений с определенными функциональными свойствами. Отдельным классом можно выделить металлоорганические соединения, содержащие ионы редкоземельных металлов и карбоксилатные органические лиганды. Такие системы замечательны своими фотофизическими и оптическими свойствами.
Известен способ [1 - Патент Китая CN 103965230 "Functional metal-organic framework based on rare earth metal cluster and preparation method thereof. Опубликован 06.08.2014] получения функционального металлоорганического каркасного соединения на основе редкоземельных металлических кластеров с формулой Ln4(μ3-OH)4(bpdc)3(ox)(H2O)5⋅nH2O, где Ln - ионы редкоземельных металлов Dy, Er, Но или Yb; bpdc - 2,2'-бипиридин-3,3'-дикарбоксилат; ох - оксалат ион, который реализуется следующим образом. Оксид редкоземельного металла Ln2O3 (источник иона металла), бипиридин-3,3'-дикарбоновую кислоту (источник органического лиганда) и щавелевую кислоту (источник дополнительного органического лиганда) в мольном соотношении между собой (2:1:1)-(2:10:7) растворяют в одном или нескольких следующих растворителях: вода, этанол, метанол и диметилформамид, с перемешиванием в течение 0.5-2 часов. Концентрация ионов редкоземельных металлов в смеси равна 0.01-0.05 М. Далее реакционную смесь переносят в тефлоновый реактор, закрывают реактор и проводят гидротермальный синтез в печи при 80-200°С в течение 12-120 часов. Далее реакционную смесь охлаждают до комнатной температуры со скоростью 1-20°С/ч. Полученные материалы обладают флуоресцентными свойствами, пригодными для определения с помощью люминесценции различных малых молекул органических растворителей. Однако известный способ имеет плохую воспроизводимость сложной структуры продукта из-за одновременного использования нескольких типов органических лигандов, что также приводит к низкой термостабильности полученного соединения. Большая длительность процесса, осуществляемого при высокой температуре, обуславливает высокую энергоемкость. Величина выхода продукта завышена за счет большого количества остающегося в его порах растворителя в связи с недостаточностью только промывания продукта и необходимостью его сушки в вакууме.
Известен способ [2 - Патент Китая CN 104672260 "Fluorescent probe material prepared from Ln-MOFs (rare earth metal-organic frameworks) and application of fluorescent probe material". Опубликован 03.06.2015] получения материала для флуоресцентной пробы на основе лантанидсодержащих металл-органических каркасных структур с формулой Ln(DHBDC)2, где Ln - ионы редкоземельных металлов Eu или Tb; DHBDC - 2,5-дигидрокси-терефталат (2,5-дигидрокси-бензол-1,4-дикарбоксилат), для количественного и качественного определения ионов бария в водных растворах. Способ реализуется следующим образом. Гексагидрат ацетата редкоземельного металла и 2,5-дигидрокси-терефталиевую кислоту смешивают с ионной жидкости на основе имидазола в мольном соотношении 1:2:n, где n≥1. Реакцию проводят при температуре 140-160°С в течение 10 минут (при микроволновом способе получения) и в течение 5 дней (при гидротермальном способе получения). После охлаждения реактора промывку готового продукта осуществляют этанолом и водой 2-3 раза, затем сушат. Однако следует отметить, что рассматриваемый способ имеет такие же недостатки, как и предыдущий рассматриваемый способ [1 - Патент Китая CN 103965230 "Functional metal-organic framework based on rare earth metal cluster and preparation method thereof. Опубликован 06.08.2014], а именно использование высокомощного микроволнового нагрева до высоких температур и большая длительность процесса получения продукта путем гидротермального синтеза усложняют процесс и обуславливают его высокую энергоемкость. Использование терефталевой кислоты ведет к низкой термической стабильности получаемого металлоорганического каркасного соединения, а оставшийся растворитель в порах продукта в связи с необходимостью вакуумирования при сушке (сушки в вакууме) приведет к существенному завышению выхода продукта.
Известен способ [3 - Патент Китая CN 105646556 "Preparation method and application of porous rare-earth metal organic framework compound". Опубликован 08.06.2016] получения и применения пористого металлоорганического каркасного соединения, содержащего редкоземельные ионы с формулой [Ln3(μ3-ОН)(BDC)3(Н2О)9]⋅3DMF⋅4Н2О, где Ln - ионы редкоземельных металлов Tb, Eu, Dy, Er, Sm, Gd или Yb; BDC - терефталат (бензол-1,4-дикарбоксилат); DMF - диметилформамид, который реализуется следующим образом. В термостойком реакторе гексагидрат нитрата тербия в количестве 18.6 мг и бензол-1,4-дикарбоновая кислоту (терефталевую кислоту) в количестве 9.4 мг растворяют в 2.2 мл диметилформамида, добавляли 0.5 мл воды и 0.3 мл концентрированной азотной кислоты, 30 минут обрабатывают в ультразвуковой ванне, затем закрывают реактор и ставят его в печь на 2-4 дня при температуре 100-110°С. Затем медленно (со скоростью 15-20°С/ч) остужают реактор до комнатной температуры. Образовавшийся продукт промывают диметилформамидом и сушат. При этом выход продукта составил 65%. Вместе с тем рассматриваемый способ не лишен недостатков, а именно большая длительность проведения процесса, жесткое соблюдение регламента процесса из-за необходимости контроля и обеспечения заданного значения кислотности раствора. Так же как и в вышеописанном способе [2 - Патент Китая CN 104672260 "Fluorescent probe material prepared from Ln-MOFs (rare earth metal-organic frameworks) and application of fluorescent probe material". Опубликован 03.06.2015], использование терефталевой кислоты ведет к низкой термической стабильности получаемого металлоорганического каркасного соединения, а оставшийся растворитель в порах продукта в связи с необходимостью вакуумирования при сушке (сушки в вакууме) приведет к существенному завышению выхода продукта.
Известен способ [4 - Патент США US 8617421 В2 "Lanthanide metal-organic frameworks and uses thereof. Опубликован 31.12.2013] получения металлоорганических структур на основе органического лиганда, 2,5-диметокси-1,4-фенилен-ди-2,1-этен-диол-бис-карбоксилата (PVDC), и ионов эрбия и иттербия с формулой Er1-xYbx-PVDC, где х - 0.68, 0.42, 0.30, 0.19. Способ осуществляют следующим образом. В стеклянную виалу помещают раствор 2,5-диметокси-1,4-фенилен-ди-2,1-этендиол-бис-карбоновой кислоты (0.020 ммоль) в диметилформамиде (0.4 мл), к которому приливают раствор пентагидрата нитрата иттербия (0.0025 ммоль) в диметилформамиде (0.050 мл), раствор пентагидрата нитрата эрбия (0.00125 ммоль) в диметилформамиде (0.025 мл) и 1М азотную кислоту (10 мкл). Закрытую виалу помещают в печь при 100°С на 72 часа. После охлаждения полученный продукт промывают в диметилформамиде (3 мл) 4 раза и сушат на воздухе. При этом выход продукта для соединений Er1-xYbx-PVDC с различным содержанием иттербия (х - 0.68, 0.42, 0.30, 0.19) равен 52.8%, 31.4%, 9.9%, 70.7% соответственно. Однако известный способ имеет следующие недостатки: плохая воспроизводимость самоорганизации структуры получаемого соединения из-за использовании органического лиганда большого размера, это же влечет за собой нестабильность выхода продукта для соединений с различным соотношением ионов редкоземельных металлов в структуре и низкую термическую стабильность полученного соединения; большая длительность процесса; жесткие условия проведения процесса из-за необходимости обеспечения определенного значение рН.
Наиболее близким по технической сущности и достигаемому результату к заявляемому изобретению является способ [5 - Патент Японии JP 2014172830 "Method for producing porous metal organic complex". Опубликован 22.09.2014], принятый в качестве прототипа. Известный способ получения пористого металлоорганического каркасного соединения на основе различных карбоновых кислот (бензол-1,4-дикарбоновая кислота, бензол-1,3-дикарбоновая кислота, бифенил-4,4'-дикарбоновая кислота, нафталин-дикарбоновая кислота, бензол-1,3,5-трикарбоновая кислота) и ионов различных металлов, среди которых ионы редкоземельных металлов, а именно или ионы иттрия, или ионы иттербия, или ионы эрбия, состоит в следующем. Для получения пористого металлоорганического каркасного соединения с формулой [Ме(ВТС)H2O], где Me - ион металла, ВТС - бензол-1,3-дикарбоксилат, со структурой MOF-76, приготавливают два раствора: первый раствор состоит из пентагидрата нитрата иттербия Yb(NO3)3⋅5Н2О, муравьиной кислоты для поддержания определенной кислотности раствора (рН), диметилформамида и воды; второй раствор - из бензол-1,3,5-трикарбоновой кислоты, диметилформамида и воды. Оба раствора перемешивают при комнатной температуре в течение 10 минут, затем для получения реакционной смеси первый раствор добавляют ко второму раствору по каплям со скоростью 0.01-5.0 мл/мин и дают конечному раствору постоять не менее 72 часов или после 5 минут стояния помещают эту реакционную смесь в печь при 105°С на не менее чем 24 часа. При этом мольное соотношение соль металла : карбоновая кислота составляет 1:(0.01-1). Далее образовавшийся продукт промывают 3 раза в диметилформамиде и сушат при 300°С в вакууме в течение 1 часа. Получившееся металлоорганическое соединение имеет структуру MOF-76.
Недостатками этого способа являются большая длительность процесса в случае получения продукта как без нагревания, так и с нагреванием; жесткость условий проведения процесса, а именно регламентированный контроль скорости добавления раствора соли металла к раствору карбоновой кислоты, и необходимость обеспечения определенного значение кислотности реакционной смеси.
Техническим результатом изобретения является сокращение длительности проведения процесса, уменьшение трудоемкости проведения процесса благодаря упрощению регламента из-за отсутствия жесткости контроля условий дозированного прикапывания раствора соли к раствору бензол-1,3,5-трикарбоновой кислоты и отсутствия необходимости контроля кислотности реакционной смеси с одновременным уменьшением температуры процесса. Кроме этого, технический результат состоит в повышении выхода продукта, что позволяет масштабировать процесс получения металлоорганического каркасного соединения с люминесцентными свойствами.
Указанный технический результат в заявленном изобретении реализован следующим образом. Способ получения металлоорганической каркасного соединения с люминесцентными свойствами заключается в приготовлении реакционной смеси из двух растворов, предварительно приготовленных путем перемешивания без нагревания. Первый раствор готовят из солей редкоземельных металлов, а именно пентагидрата нитрата иттербия (Yb(NO3)3⋅5Н2О) или пентагидрата нитрата эрбия (Er(NO3)3⋅5Н2О) или одновременно гидратов солей двух этих металлов, и растворителя диметилформамида. В случае когда для получения раствора солей редкоземельных металлов берут соли двух металлов, иттербия и эрбия, мольное соотношение пентагидратов нитратов иттербия и эрбия между собой составляет (Yb(NO3)3⋅5H2O):(Er(NO3)3⋅5H2O)=n:1, где n - мольное содержание пентагидрата нитрата иттербия и должно быть больше 1. Вторым раствором является раствор бензол-1,3,5-трикарбоновой кислоты в растворителе диметилформамиде. Общая концентрация солей редкоземельных металлов в первом растворе не превышает 9 ммоль/л, а общая концентрация бензол-1,3,5-трикарбоновой кислоты во втором растворе составляет не менее 42 ммоль/л. Далее для получения реакционной смеси первый раствор соли редкоземельных металлов прикапывают без контроля скорости при интенсивном перемешивании при комнатной температуре ко второму раствору бензол-1,3,5-трикарбоновой кислоты. Полученную реакционную смесь переливают в тефлоновый сосуд, который плотно закрывают крышкой и помещают в печь, которая нагрета до 85-150°С, и проводят реакцию без перемешивания при указанной температуре в течение 12-16 часов. Далее реакционную смесь охлаждают до комнатной температуры, фильтруют, а образовавшуюся твердую фазу сначала промывают растворителем диметилформамидом, а затем дополнительно промывают в 30 мл этанола не менее трех раз, после чего подвергают ее сушке в течение 30 минут в вакууме, чтобы удалить оставшийся растворитель. Полученное металлоорганическое каркасное соединение демонстрирует высокую термическую стабильность и люминесцентные свойства как при фотовозбуждении светом с длиной волны короче длины волны испускаемого излучения (стоксовая люминесценция), так и при фотовозбуждении светом с длиной волны больше длины волны испускаемого излучения (антистоксовая, или ап-конверсионная, люминесценция).
Предлагаемый способ иллюстрируется Фиг. 1 - Фиг. 9.
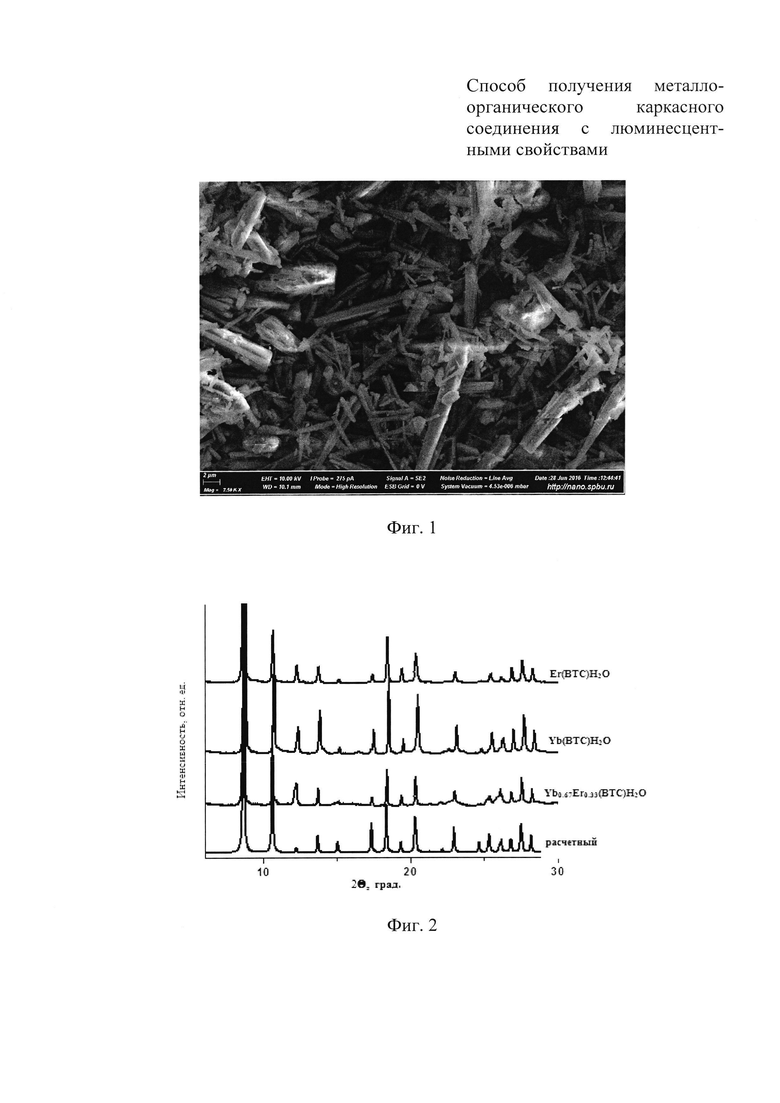
На Фиг. 1 представлена микрофотография микрокристалликов металлоорганического каркасного соединения Yb(BTC)H2O для демонстрации размеров получаемых кристаллитов.
На Фиг. 2 представлена рентгенограмма металлоорганических каркасных соединений Er(ВТС)H2O, Yb(ВТС)Н2О и Yb0.67Er0.33(ВТС)Н2), полученных заявляемым способом, для демонстрации совпадения структуры полученных соединений со структурой металлоорганического каркасного соединения типа MOF-76 по его расчетной рентгенограмме.
На Фиг. 3 представлена структура металлоорганического каркасного соединения типа MOF-76.
На Фиг. 4 представлен инфракрасный колебательный спектр металлоорганического каркасного соединения Yb0.67Er0.33(ВТС)H2O, полученного заявляемым способом, для идентификации состава соединения.
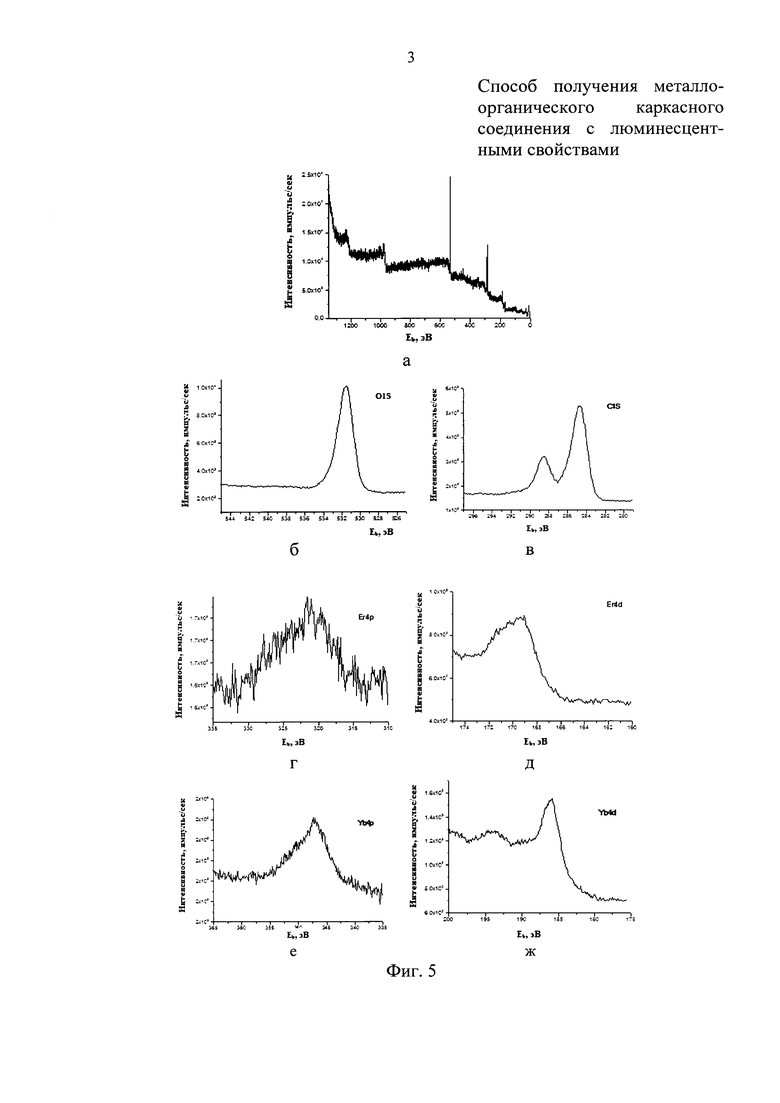
На Фиг. 5 представлены данные рентгеновской фотоэлектронной спектроскопии для металлоорганического каркасного соединения Yb0.67Er0.33(ВТС)Н2), полученного заявляемым способом: обзорный спектр (а) и спектры по элементам - кислород (б), углерод (в), иттербий (г, д) и эрбий (е, ж) для идентификации состава соединения и определения соотношения ионов металлов.
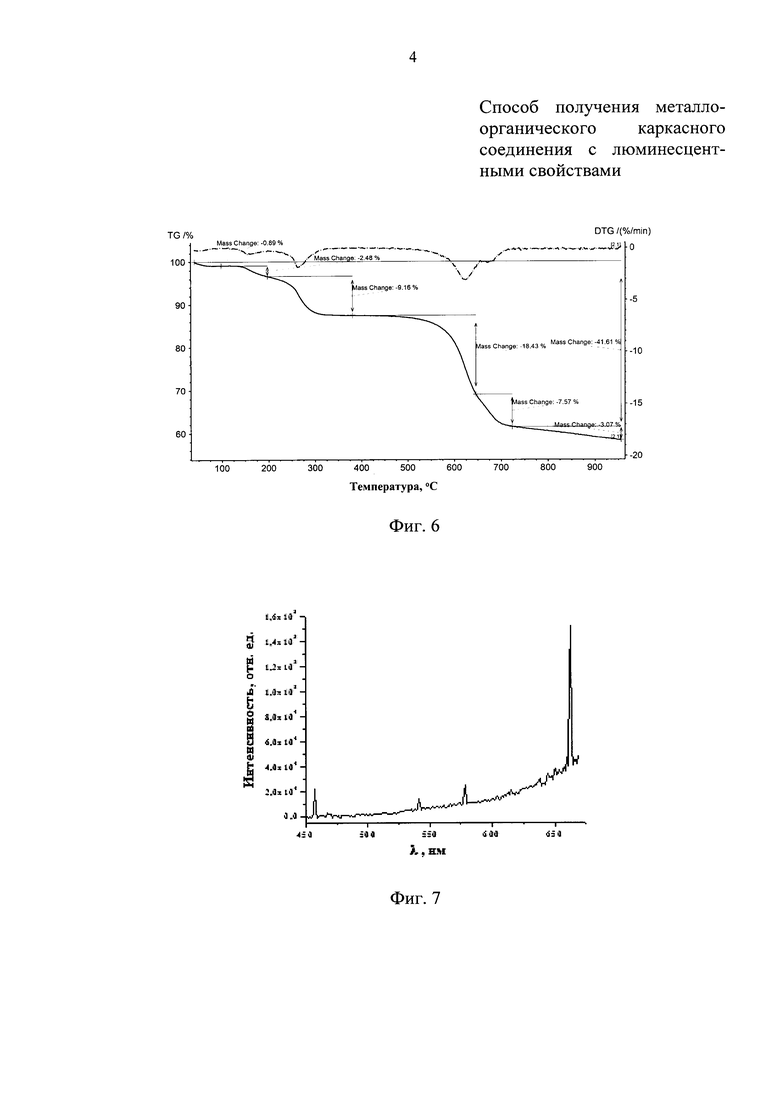
На Фиг. 6 представлена дериватограмма металлоорганического каркасного соединения Yb0.67Er0.33(ВТС)H2O, полученного заявляемым способом, для демонстрации термостабильности продукта.
На Фиг. 7 представлен спектр люминесценции металлоорганического каркасного соединения Er(ВТС)H2O, полученного заявляемым способом, при возбуждении светом с длиной волны 330 нм для демонстрации люминесцентных свойств.
На Фиг. 8 представлены спектры антистоксовой (ап-конверсионной) люминесценции металлоорганических каркасных соединений Yb0.67Er0.33(ВТС)H2O (спектр 1), Yb0.75Er0.25(BTC)H2O (спектр 2) и Er(ВТС)Н2О (спектр 3), полученных заявляемым способом, при возбуждении светом с длиной волны 975 нм при мощности лазера 1 Вт для демонстрации ап-конверсионных люминесцентных свойств полученных продуктов.
На Фиг. 9 представлена зависимость интенсивности линий в спектре ап-конверсионной люминесценции металлоорганического каркасного соединения Yb0.67Er0.33(ВТС)H2O (линии 662 нм (1), 547 нм (2), 526 нм (3), 441 нм (4)) от мощности возбуждающего света с длиной волны 975 нм для описания ап-конверсионных люминесцентных свойств полученного продукта.
Заявленный способ получения металлоорганической каркасного соединения Yb1-xErx(ВТС)H2O с люминесцентными свойствами был апробирован на лабораторной базе в режиме реального времени в Санкт-Петербургском государственном университете.
Результаты испытания подтверждены конкретными условиями реализации способа получения металлоорганической каркасного соединения Yb1-xErx(BTC)H2O, зависимостями выхода продукта от температуры и длительности проведения синтеза металлоорганической каркасного соединения Yb1-xErx(BTC)H2O, результатами сравнения выходов продуктов, полученных заявляемым способом и способом, описанным в прототипе [5 - Патент Японии JP 2014172830 "Method for producing porous metal organic complex". Опубликован 22.09.2014], результатами по определению морфологии частиц, структуры и состава полученного соединения методами электронной микроскопии, рентгеноструктурного анализа, электронной спектроскопии, а также данными по демонстрации высокой термостабильности методом термогравиметрии, спектрами стоксовой и антистоксовой (ап-конверсионной) люминесценции для полученных соединений.
Примеры 1 и 2 демонстрируют конкретные условия апробации заявляемого в изобретении способа получения металлоорганической каркасного соединения Yb(BTC)H2O.
Пример 1.
Пентагидрат нитрата иттербия (Yb(NO3)3⋅5Н2О, 0.225 ммоль) растворяли в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Параллельно с этим растворяют бензол-1,3,5-трикарбоновую кислоту (С6Н3(СООН)3, 1.06 ммоль) в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Далее к раствору карбоновой соли при интенсивном перемешивании прикапывают раствор соли иттербия и помещают полученную реакционную смесь в сосуд, сосуд плотно закрывают крышкой и ставят его в печь при температуре 85°С на 16 часов. Далее сосуд с реакционной смесью охлаждают до комнатной температуры. Образовавшийся продукт отфильтровывают и промывают сначала в 30 мл диметилформамида 3 раза, а затем в 30 мл этанола 3 раза. После этого проводят сушку твердой фазы в вакууме при 300°С в течение 30 минут. При этом выход продукта составил 81.9%.
Пример 2.
Пентагидрат нитрата иттербия (Yb(NO3)3⋅5Н2О, 0.225 ммоль) растворяют в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Параллельно с этим растворяют бензол-1,3,5-трикарбоновую кислоту (С6Н3(СООН)3, 1.06 ммоль) в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Далее к раствору карбоновой соли при интенсивном перемешивании прикапывают раствор соли иттербия и помещают полученную реакционную смесь в сосуд, сосуд плотно закрывают крышкой и ставят в печь при температуре 150°С на 12 часов. Далее реакционную смесь охлаждают до комнатной температуры. Образовавшийся продукт отфильтровывают и промывают сначала в 30 мл диметилформамида 3 раза, а затем в 30 мл этанола 3 раза. После этого проводят сушку твердой фазы в вакууме при 300°С в течение 30 минут. При этом выход продукта составил 96.3%.
Полученные в рамках примеров 1 и 2 металлоорганические каркасные соединения Yb(BTC)H2O имеют кристаллики в виде стержней с размерами от 1 до 20 мкм (Фиг. 1). На Фиг. 2 представлена рентгенограмма металлоорганического каркасного соединения Yb(BTC)H2O, полученного способом, представленным в примере 2. Из Фиг. 2 видно, что соединение имеет структуру металлоорганического каркасного соединения MOF-76, расчетная рентгенограмма которого также представлена на Фиг. 2, а ее строение схематически изображено на Фиг. 3.
Примеры 3 и 4 демонстрируют конкретные условия реализации способа [5 - Патент Японии JP 2014172830 "Method for producing porous metal organic complex". Опубликован 22.09.2014] получения металлоорганической каркасного соединения Yb(BTC)H2O и значения выходов продуктов по известному способу для дальнейшего сравнения их с выходами продуктов, полученных по заявляемому способу.
Пример 3.
Пентагидрат нитрата иттербия (Yb(NO3)3⋅5Н2О, 0.06 ммоль) и муравьиную кислоту (НСООН, 0.1 ммоль) растворяют в 10 мл смеси диметилформамида и воды (1:1 по объему) при комнатной температуре с перемешиванием в течение 10 минут. Кислотность раствора (рН), которая регулируется муравьиной кислотой, должна составлять 3.5, постоянно строго контролируют. Параллельно с этим растворяют бензол-1,3,5-трикарбоновую кислоту (С6Н3(СООН)3, 0.06 ммоль) в 10 мл смеси диметилформамида и воды (1:1 по объему) при комнатной температуре с перемешиванием в течение 10 минут. Далее раствор соли иттербия добавляют по каплям ко второму раствору карбоновой кислоты, строго поддерживая скорость дозированного добавления равной 5.0 мл/мин. Полученную реакционную смесь оставляют при комнатной температуре без перемешивания на 72 часа, затем образовавшийся продукт промывают 3 раза в диметилформамиде и сушат при 300°С в вакууме в течение 1 часа. Полученное металлоорганическое соединение имеет структуру MOF-76. При этом выход продукта составил 46.6%.
Пример 4.
Пентагидрат нитрата иттербия (Yb(NO3)3⋅5Н2О, 0.06 ммоль) и муравьиную кислоту (НСООН, 0.1 ммоль) растворяют в 10 мл смеси диметилформамида и воды (1:1 по объему) при комнатной температуре с перемешиванием в течение 10 минут. Кислотность раствора (рН), которая регулируется муравьиной кислотой, должна составлять 3.5, постоянно строго контролируют. Параллельно с этим растворяют бензол-1,3,5-трикарбоновую кислоту (С6Н3(СООН)3, 0.06 ммоль) в 10 мл смеси диметилформамида и воды (1:1 по объему) при комнатной температуре с перемешиванием в течение 10 минут. Далее раствор соли иттербия добавляют по каплям ко второму раствору карбоновой кислоты, строго поддерживая скорость дозированного добавления равной 5.0 мл/мин. Полученную реакционную смесь оставляют при комнатной температуре без перемешивания на 5 минут, затем помещают в печь при 105°С на 24 часа. После остывания реакционной смеси образовавшийся продукт промывают 3 раза в диметилформамиде и сушат при 300°С в вакууме в течение 1 часа. Полученное металлоорганическое соединение имеет формулу [Yb(BTC)H2O], где ВТС - бензол-1,3-дикарбоксилат, и соответствует структуре металлоорганического соединения MOF-76. При этом выход продукта составил 57.6%.
Для сравнения условия процесса и выходы металлоорганических каркасных соединений YB(ВТС)Н2О, полученных по заявляемому способу и по способу, описанному в прототипе [5 - Патент Японии JP 2014172830 "Method for producing porous metal organic complex". Опубликован 22.09.2014] и реализованные в рамках примеров 1-4, сведены в таблице 1.

Из таблицы 1 видно, что использование предлагаемого способа получения металлоорганической каркасного соединения позволяет получить продукт с более высоким (почти в два раза) выходом при меньших энергетических и временных затратах (температуры и времени проведения процесса), уменьшить трудоемкость и упростить условия процесса, исключив необходимость строгого контроля рН реакционной смеси и контроля за скоростью дозированного прикапывания раствора солей редкоземельных металлов при приготовлении реакционной смеси, также дает возможность масштабирования процесса получения металлоорганической каркасного соединения без потери качества и выхода продукта.
Пример 5.
Пример 5 показывает реальные условия реализации способа получения металлоорганической каркасного соединения Er(ВТС)Н2О.
Пентагидрат нитрата эрбия (Er(NO3)3⋅5Н2О, 0.225 ммоль) растворяют в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Параллельно с этим растворяют бензол-1,3,5-трикарбоновую кислоту (С6Н3(СООН)3, 1.06 ммоль) в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Далее к раствору карбоновой соли при интенсивном перемешивании прикапывают раствор пентагидрата нитрата эрбия и помещают полученную реакционную смесь в сосуд, сосуд плотно закрывают крышкой и ставят в печь при температуре 150°С на 12 часов. Далее реакционную смесь охлаждают до комнатной температуры. Образовавшийся продукт отфильтровывают и промывают сначала в 30 мл диметилформамида 3 раза, а затем в 30 мл этанола 3 раза. После этого проводят сушку в вакууме при 300°С в течение 30 минут. При этом выход продукта составил 96.3%.
На Фиг. 2 представлена рентгенограмма металлоорганического каркасного соединения Er(ВТС)H2O. Из Фиг. 2 видно, что соединение имеет структуру металлоорганического каркасного соединения MOF-76, расчетная рентгенограмма которого также представлена на Фиг. 2, а ее строение схематически изображено на Фиг. 3.
Примеры 6 и 7 показывают реальные условия реализации способа получения металлоорганической каркасного соединения Yb1-xErx(BTC)H2O с различным мольным соотношением пентагидрата нитрата иттербия и пентагидрата нитрата эрбия между собой, а именно Yb(NO3)3⋅5H2O:Er(NO3)3⋅5H2O=2:1 и Yb(NO3)3⋅5H2O:Er(NO3)3⋅5H2O=3:1, при общей концентрации пентагидратов нитратов иттербия и эрбия в растворе соли редкоземельных металлов не более 9 ммоль/л и при концентрации бензол-1,3,5-трикарбоновой кислоты в растворе не менее 42 ммоль/л.
Пример 6.
Способ получения металлоорганической каркасного соединения Yb1-xErx(BTC)H2O с мольным соотношением пентагидрата нитрата иттербия и пентагидрата нитрата эрбия между собой 2:1.
Пентагидрат нитрата иттербия (Yb(NO3)3⋅5H2O, 0.15 ммоль) и пентагидрат нитрата эрбия (Er(NO3)3⋅5Н2О, 0.075 ммоль) растворяют в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Параллельно с этим растворяют бензол-1,3,5-трикарбоновую кислоту (С6Н3(СООН)3, 1.06 ммоль) в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Далее к раствору карбоновой соли при интенсивном перемешивании прикапывают раствор солей редкоземельных металлов и помещают полученную реакционную смесь в сосуд, сосуд плотно закрывают крышкой и ставят в печь при температуре 150°С на 12 часов. Далее реакционную смесь охлаждают до комнатной температуры. Образовавшийся продукт отфильтровывают и промывают сначала в 30 мл диметилформамида 3 раза, а затем в 30 мл этанола 3 раза. После этого проводят сушку в вакууме при 300°С в течение 30 минут. При этом выход продукта составил 95.2%.
На Фиг. 2 представлена рентгенограмма металлоорганического каркасного соединения Yb0,67Er0.33(ВТС)H2O. Из Фиг. 2 видно, что соединение имеет структуру металлоорганического каркасного соединения MOF-76, расчетная рентгенограмма которого также представлена на Фиг. 2, а ее строение схематически изображено на Фиг. 3. Качественный и количественный состав полученного соединения Yb0.67Er0.33(ВТС)H2O подтверждают результаты анализов методами инфракрасной колебательной спектроскопии (Фиг. 4) и рентгеновской электронной спектроскопии (Фиг. 5).
Соотношение ионов иттербия к ионам эрбия в полученном соединении оказалось равным 2:1. Полученное соединение демонстрирует высокую, вплоть до 450°С, термостабильность полученного продукта, что иллюстрирует дериватограмма на Фиг. 6.
Пример 7.
Способ получения металлоорганической каркасного соединения Yb1-xErx(BTC)H2O с мольным соотношением пентагидрата нитрата иттербия и пентагидрата нитрата эрбия между собой 3:1.
Пентагидрат нитрата иттербия (Yb(NO)3)3⋅5Н2О, 0.169 ммоль) и пентагидрат нитрата эрбия (Er(NO)3)3⋅5Н2О, 0.056 ммоль) растворяют в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Параллельно с этим растворяют бензол-1,3,5-трикарбоновую кислоту (С6Н3(СООН)3, 1.06 ммоль) в 25 мл диметилформамида при комнатной температуре с перемешиванием в течение 10 минут. Далее к раствору карбоновой соли при интенсивном перемешивании прикапывают раствор солей редкоземельных металлов и помещают полученную реакционную смесь в сосуд, сосуд плотно закрывают крышкой и ставят в печь при температуре 150°С на 12 часов. Далее реакционную смесь охлаждают до комнатной температуры. Образовавшийся продукт отфильтровывают и промывают сначала в 30 мл диметилформамида 3 раза, а затем в 30 мл этанола 3 раза. После этого проводят сушку в вакууме при 300°С в течение 30 минут. При этом выход продукта составил 93.5%.
Составы металлоорганических каркасных соединений Yb1-xErx(BTC)H2O с мольными соотношениями ионов Yb к ионам Er, равными 2:1 и 3:1, способы реализации которых описаны в примерах 6 и 7, определены по данным, полученным методом электронной спектроскопии для химического анализа, и представлены в таблице 2.


Из таблицы 2 видно, что реализация предлагаемого в изобретении способа получения металлоорганической каркасного соединения Yb1-xErx(BTC)(H2O) с различными мольными соотношениями пентагидратов нитратов иттербия и эрбия в реакционной смеси приводит к получению продуктов с такими же мольными соотношениями ионов иттербия и эрбия с высоким выходом продукта. Примеры 6 и 7 позволяют утверждать, что заявляемый способ легко масштабируется без убыли выхода продукта.
Заявляемое изобретение позволяет получить металлоорганическое каркасное соединение, обладающее ап-конверсионными и люминесцентными свойствами. То, что подобные системы обладают люминесцентными свойствами, уже известно и находит широкое применение в различных областях, например, для определения содержания металлов, органических веществ, для создания сенсоров различных органических соединений. Пример 8 демонстрирует, что предлагаемый новый способ получения металлоорганической каркасного соединения позволяет получать продукты, обладающие люминесцентными свойствами.
Пример 8.
На Фиг. 7 представлен спектр люминесценции металлоорганического каркасного соединения Er(ВТС)Н2О при возбуждении светом с длиной волны 330 нм. Это подтверждает, что металлоорганическое каркасное соединение Er(ВТС)H2O, полученное заявляемым способом при реализации в рамках примера 5, обладает люминесцентными свойствами.
Полученное металлоорганическое каркасное соединение типа Yb1-xErx(BTC)H2O демонстрирует не только люминесцентные свойства при фотовозбуждении светом с длиной волны короче длины волны испускаемого излучения (стоксовая люминесценция), но ап-конверсионные люминесцентные свойства (антистоксовая или ап-конверсионная люминесценция, когда длина возбуждающего света длиннее длины волны излучения). Ап-конверсионная люминесценция не была обнаружена ранее для металлоорганических соединений. В настоящее время системы ап-конверсии, то есть преобразователи инфракрасного излучения в видимый свет, используют как сенсоры и визуализаторы в биомедицине, также для создания коротковолновых (сине-зеленых) лазеров. Одним из потенциальных путей применения таких систем является использование их для увеличения эффективности фотоэлементов. Поэтому поиск и разработка новых фотоактивных материалов, подходящих для создания фотокаталитических и фотоэлектрохимических систем, становится актуальным в связи с развитием такого альтернативного пути развития энергетики, как использование солнечной энергии.
До сих пор среди систем с ап-конверсионными свойствами преобладали неорганические соединения, допированные ионами редкоземельных металлов. Минусом таких систем является хаотичное и неравномерное расположение ионов допанта по объему неорганической матрицы, что приводит к необходимости увеличения концентрации допирования, а это, в свою очередь, затрудняет контроль за распределением интенсивности различных линий люминесценции.
Заявленное изобретение, как показывают многочисленные примеры апробации, позволяет использовать в качестве фотоактивного материала металлоорганические каркасные соединения, а именно, конкретные полученные металлоорганические каркасные соединения типа Yb1-xErx(BTC)H2O. Металлоорганические каркасные соединения, представляющие собой трехмерные гибридные полимерные структуры с развитой сетью пор, к настоящему времени зарекомендовали себя как активные катализаторы для процессов нефтепереработки, как материалы для хранения и транспортировки газов, особенно водорода. В качестве фотокатализаторов металлоорганические каркасные соединения стали использоваться в последние несколько лет. Вместе с тем заявителю и авторам неизвестны случаи использования этих соединений в качестве системы ап-конверсии. Кроме того, их использование для этих целей приводит к ряду преимуществ перед ранее известными неорганическими системами ап-конверсии: 1) упорядоченное расположение ионов редкоземельных металлов по объему материала с легким контролем за концентрацией ионов металлов; 2) развитая структура пор, что является важным условием для проведения фотокаталитических и фотоэлектрохимических процессов.
Пример 9.
Пример 9 демонстрирует ап-конверсионные люминесцентные свойства металлоорганических каркасных соединений Er(ВТС)Н2О и Yb1-xErx(BTC)H2O с различным мольным соотношением ионов иттербия и эрбия в структуре последнего соединения, реализации способа получения которых представлены в рамках примеров 5-7.
Фиг. 8 представляет спектры антистоксовой (ап-конверсионной) люминесценции металлоорганических каркасных соединений Yb0.67Er0.33(ВТС)H2O (спектр 1), Yb0.75Er0.25(BTC)H2O (спектр 2) и Er(ВТС)Н2О (спектр 3), полученных заявляемым способом и реализованных в рамках примеров 5-7, при возбуждении светом с длиной волны 975 нм при мощности лазера 1 Вт, что демонстрирует, что соединения обладают ап-конверсионными люминесцентными свойствами.
Фиг. 9 демонстрирует зависимость интенсивности линии 662 нм (1), линии 547 нм (2), линии 526 нм (3) и линии 441 нм (4) в спектре ап-конверсионной люминесценции металлоорганического каркасного соединения Yb0.67Er0.33(ВТС)H2O, способ получения которого представлен в рамках примера 6, от мощности возбуждающего света с длиной волны 975 нм.
Как показывают примеры 1-9 апробации, заявленный способ получения металлоорганического каркасного соединения с люминесцентными свойствами достигает указанный выше технический результат и подтверждает достоверность сокращения длительности проведения процесса и уменьшения трудоемкости проведения процесса благодаря упрощению регламента из-за отсутствия жесткости контроля условий дозированного прикапывания и кислотности при приготовлении реакционной смеси (примеры 1-7) по сравнению со способом, заявленным в прототипе [5 - Патент Японии JP 2014172830 "Method for producing porous metal organic complex". Опубликован 22.09.2014]. Кроме того, регламент процесса в заявляемом способе позволяет значительно повысить выход продукта и дает возможность масштабировать процесс получения металлоорганического каркасного соединения в требуемых количествах при сохранении высокого выхода продукта. Получаемые металлоорганические каркасные соединения обладают не только люминесцентными, но и ап-конверсионными люминесцентными свойствами (примеры 8, 9), что позволяет использовать их в качестве фотоактивных материалов для преобразования инфракрасного излучения в видимый свет.
Источники информации
1. Патент Китая CN 103965230 "Functional metal-organic framework based on rare earth metal cluster and preparation method thereof. Опубликован 06.08.2014.
2. Патент Китая CN 104672260 "Fluorescent probe material prepared from Ln-MOFs (rare earth metal-organic frameworks) and application of fluorescent probe material". Опубликован 03.06.2015.
3. Патент Китая CN 105646556 "Preparation method and application of porous rare-earth metal organic framework compound". Опубликован 08.06.2016.
4. Патент США US 8617421 B2 "Lanthanide metal-organic frameworks and uses thereof. Опубликован 31.12.2013.
5. Патент Японии JP 2014172830 "Method for producing porous metal organic complex". Опубликован 22.09.2014 (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| Металлорганическая каркасная структура бензолтрикарбоксилата иттрия (III) Y-BTC для аккумулирования водорода и способ её получения | 2022 |
|
RU2796292C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДНЫХ АП-КОНВЕРСИОННЫХ ЛЮМИНОФОРОВ | 2020 |
|
RU2753700C1 |
| СПОСОБ СИНТЕЗА АПКОНВЕРСИОННЫХ ЧАСТИЦ NaYF:Er,Yb | 2019 |
|
RU2725581C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛОИДНЫХ РАСТВОРОВ ЛЮМИНЕСЦЕНТНЫХ НАНОПЛАСТИН ОКСИДОВ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ | 2011 |
|
RU2465299C1 |
| СПОСОБ ПОЛУЧЕНИЯ СТЕКЛОКЕРАМИКИ С НАНОРАЗМЕРНЫМИ КРИСТАЛЛАМИ ТВЕРДЫХ РАСТВОРОВ ТИТАНАТОВ-ЦИРКОНАТОВ ЭРБИЯ И/ИЛИ ИТТЕРБИЯ | 2015 |
|
RU2583470C1 |
| Разнолигандные фторзамещенные ароматические карбоксилаты лантанидов, проявляющие люминесцентные свойства, и органические светодиоды на их основе | 2017 |
|
RU2657496C1 |
| СОЕДИНЕНИЕ ДИ(НИТРАТО)АЦЕТИЛАЦЕТОНАТОБИС (1,10-ФЕНАНТРОЛИН) ЛАНТАНОИД (III), ПРИГОДНОЕ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНОЙ ДОБАВКИ В ЧЕРНИЛА, И ЧЕРНИЛА ДЛЯ СКРЫТОЙ МАРКИРОВКИ ЦЕННЫХ МАТЕРИАЛЬНЫХ ОБЪЕКТОВ | 2007 |
|
RU2373211C2 |
| Сложный силикат редкоземельных элементов | 2024 |
|
RU2832831C1 |
| Способ получения эмиссионного слоя на основе соединений редкоземельных элементов и органический светоизлучающий диод | 2017 |
|
RU2657497C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛАНТАНСОДЕРЖАЩЕГО МЕТАЛЛООРГАНИЧЕСКОГО КАРКАСНОГО СОЕДИНЕНИЯ ТРЁХМЕРНОЙ СТРУКТУРЫ НА ОСНОВЕ ТЕРЕФТАЛЕВОЙ КИСЛОТЫ | 2015 |
|
RU2613976C1 |


Изобретение относится к получению металлоорганического каркасного соединения с люминесцентными свойствами. Способ включает смешение гидрата нитрата иттербия или эрбия или их смеси в диметилформамиде концентрации 9 ммоль/л с раствором бензол-1,3,5,-трикарбоновой кислоты в диметилформамиде концентрации 42 ммоль/л при комнатной температуре. Реакционную смесь далее нагревают в закрытом сосуде 12-16 часов при 85-150°С, охлаждают до комнатной температуры и фильтруют. Полученную твердую фазу промывают диметилформамидом, далее - в 30 мл этанола не менее трех раз и подвергают сушке в вакууме при 300оС в течение 30 минут. Полученные соединения обладают наряду с люминесцентными еще и ап-конверсионными люминесцентными свойствами, что позволяет использовать их в качестве фотоактивных материалов для преобразования инфракрасного излучения в видимый свет. Изобретение обеспечивает получение металлоорганического каркасного соединения структуры MOF-76 с высокой термостабильностью по упрощенной технологии вследствие исключения необходимости жесткого контроля рН смеси и скорости добавления солей металлов, снижения температуры и времени проведения процесса при повышении выхода целевого продукта почти в 2 раза до 96,3%. 3 з.п. ф-лы, 9 ил., 2 табл., 9 пр.
1. Способ получения металлоорганического каркасного соединения с люминесцентными свойствами, заключающийся в получении реакционной смеси путем добавления раствора соли металлов в растворителе диметилформамиде к раствору бензол-1,3,5,-трикарбоновой кислоты в растворителе диметилформамиде с перемешиванием при комнатной температуре, в дальнейшем нагревании реакционной смеси и ее охлаждении до комнатной температуры, после чего реакционную смесь фильтруют, а полученную при этом твердую фазу промывают растворителем диметилформамидом и подвергают сушке в вакууме при 300°С, причем в качестве соли металлов берут гидрат нитрата иттербия или эрбия или их смеси, общая концентрация которого в растворе соли металлов составляет 9 ммоль/л, при этом концентрацию бензол-1,3,5-трикарбоновой кислоты в растворе берут 42 ммоль/л, нагревание реакционной смеси проводят в закрытом сосуде в течение 12-16 часов при температуре 85-150°С, а полученную после этого твердую фазу дополнительно промывают в 30 мл этанола не менее трех раз и затем подвергают ее сушке в течение 30 минут.
2. Способ по п. 1, отличающийся тем, что в качестве гидрата нитрата иттербия берут пентагидрат нитрата иттербия.
3. Способ по п. 1, отличающееся тем, что в качестве гидрата нитрата эрбия берут пентагидрат нитрата эрбия.
4. Способ по п. 1, отличающееся тем, что в качестве смеси гидратов нитратов иттербия и эрбия берут смесь пентагидрата нитрата иттербия и пентагидрата нитрата эрбия, при этом мольное соотношение пентагидрата нитрата иттербия и пентагидрата нитрата эрбия между собой равно 2-3:1 соответственно.
| JP 2014172830 А, 22.09.2014 | |||
| JP 2002128732 А, 09.05.2002 | |||
| WO 2009077671 A2, 25.06.2009 | |||
| RU 2401860 C2, 20.10.2010. |
Авторы
Даты
2018-02-21—Публикация
2016-12-28—Подача