Настоящее изобретение относится к органическим соединениям, полезным для лечения или профилактики у млекопитающих, и в частности, к ингибиторам белков, связывающих жирные кислоты (FABP) 4 и/или 5, более конкретно двойным ингибиторам FABP 4/5 для лечения или профилактики, например, диабета 2 типа, атеросклероза, хронических заболеваний почек, неалкогольного стеатогепатита и рака.
В настоящем изобретении предложены новые соединения формулы (I)
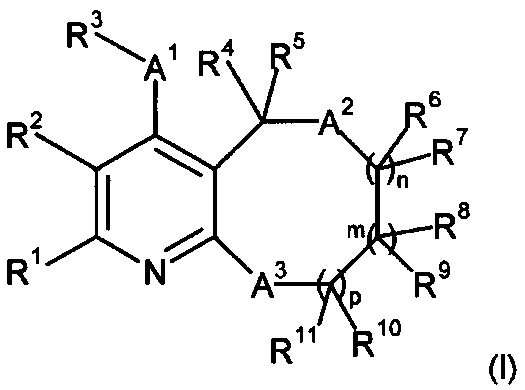
где
R1 представляет собой алкил, галоалкил, циклоалкил, замещенный циклоалкил, алкокси, алкоксиалкил, алкоксиалкокси, алкоксикарбонил, алкоксикарбонилалкил, карбокси, карбоксиалкил, галоалкил, галоалкокси, галоалкоксиалкил, циклоалкокси, замещенный циклоалкокси, циклоалкоксиалкил, замещенный циклоалкоксиалкил, гидроксиалкил, арил, замещенный арил, гетероциклоалкил, замещенный гетероциклоалкил, гетероциклоалкокси, замещенный гетероциклоалкокси, гетероциклоалкилалкокси, замещенный гетероциклоалкилалкокси, гетероарил, замещенный гетероарил, амино, замещенный амино, аминокарбонил или замещенный аминокарбонил, где замещенный циклоалкил, замещенный циклоалкокси, замещенный циклоалкоксиалкил, замещенный арил, замещенный гетероциклоалкил, замещенный гетероциклоалкокси, замещенный гетероциклоалкилалкокси и замещенный гетероарил замещены одним-тремя заместителями, независимо выбранными из гидрокси, оксо, галогена, алкила, циклоалкила, галоалкила, алкилциклоалкила, циклоалкилалкила, алкилциклоалкилалкила, гидроксиалкила, алкилсульфонила, алкилсульфонилалкила, алкоксикарбонила, алкокси и алкоксиалкила и где замещенный амино и замещенный аминокарбонил замещены по атому азота одним-двумя заместителями, независимо выбранными из алкила, циклоалкила, галоалкила, алкилциклоалкила, цикпоалкилалкила, алкилциклоалкилалкила, гидроксиалкила и алкоксиалкила;
R2 представляет собой -СООН, тетразол-5-ил, [1,3,4]оксадиазол-2-он-5-ил, [1,3,4]оксадиазол-2-тион-5-ил, [1,2,4]оксадиазол-5-он-3-ил, [1,2,4]оксадиазол-5-тион-3-ил, [1,2,3,5]оксатиадиазол-2-оксид-4-ил, [1,2,4]тиадиазол-5-он-3-ил, изоксазол-3-ол-5-ил, 5-алкилизоксазол-3-ол-4-ил, 5-циклоалкилизоксазол-3-ол-4-ил, фуразан-3-ол-4-ил, 5-алкилсульфониламино-[1,3,4]оксадиазол-2-ил, 5-циклоалкилсульфониламино-[1,3,4]оксадиазол-2-ил, 5-алкилсульфониламино-[1,2,4]триазол-3-ил, 5-циклоалкилсульфониламино-[1,2,4]триазол-3-ил, 5-алкилизотиазол-3-ол-4-ил, 5-цикпоалкилизотиазол-3-ол-4-ил, [1,2,5]тиадиазол-3-ол-4-ил, 1,4-дигидро-тетразол-5-он-1-ил, тетразол-5-илкарбамоил, тетразол-5-карбонил, [1,2,4]оксадиазолидин-3,5-дион-2-ил, [1,2,4]оксадиазол-5-он-3-ил, 2,4-дигидро-[1,2,4]триазол-3-он-5-сульфанил, [1,2,4]триазол-3-сульфанил, [1,2,4]триазол-3-сульфинил, [1,2,4]триазол-3-сульфонил, 4-алкил-пиразол-1-ол-5-ил, 4-циклоалкил-пиразол-1-ол-5-ил, 4-алкил-[1,2,3]триазол-1-ол-5-ил, 4-циклоалкил-[1,2,3]триазол-1-ол-5-ил, 5-алкил-имидазол-1-ол-2-ил, 5-циклоалкил-имидазол-1-ол-2-ил, 4-алкил-имидазол-1-ол-5-ил, 4-циклоалкил-имидазол-1-ол-5-ил, 4-алкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, 4,4-диалкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, 4-циклоалкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, 4,4-дициклоалкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, тиазолидин-2,4-дион-5-ил, оксазолидин-2,4-дион-5-ил, 3-[1-гидрокси-мет-(Е)-илиден]-пирролидин-2,4-дион-1-ил, 3-[1-гидрокси-мет-(Z)-илиден]-пирролидин-2,4-дион-1-ил, 5-метил-4-гидроксифуран-2-он-3-ил, 5,5-диалкил-4-гидроксифуран-2-он-3-ил, 5-циклоалкил-4-гидроксифуран-2-он-3-ил, 5,5-дициклоалкил-4-гидроксифуран-2-он-3-ил, 3-гидроксициклобут-3-ен-1,2-дион-4-ил или 3-гидроксициклобут-3-ен-1,2-дион-4-амино;
R3 представляет собой фенил, замещенный фенил, замещенный дигидропиридинил, гетероарил или замещенный гетероарил, где замещенный фенил, замещенный дигидропиридинил и замещенный гетероарил замещены одним - тремя заместителями, независимо выбранными из гидрокси, оксо, галогена, алкила, циклоалкила, галоалкила, галоалкокси, алкилциклоалкила, цикпоалкилалкила, алкилциклоалкилалкила, гидроксиалкила, гидроксиалкокси, алкокси, алкоксиалкила, алкилсульфонила, амино и амино, замещенного по атому азота одним - двумя заместителями, независимо выбранными из алкила, циклоалкила, галоалкила, алкилциклоалкила, цикпоалкилалкила, алкилциклоалкилалкила, гидроксиалкила и алкоксиалкила;
А1 представляет собой связь или CR12R13;
А2 представляет собой -CR14R15-, -NR16-, -О-, -S-, -S(O)- или -S(O)2-;
А3 представляет собой -CR17R18-, -C(O)NR19-, -NR19-, -О-, -S-, -S(O)- или -S(O)2-;
R4, R5, R6, R7, R8, R9, R10, R11, R14, R15, R17 и R18 независимо выбраны из H, галогена, алкила, алкокси, циклоалкил, циклоалкилалкокси, галоалкокси и галоалкила.
R12 и R13 независимо выбраны из водорода, алкила, циклоалкила и галоалкила.
R16 и R19 независимо выбраны из водорода, алкила, циклоалкила, галоалкила и алкилкарбонила.
n, m и р независимо выбраны из 0 и 1;
или их фармацевтически приемлемые соли.
FABP4 (аР2) и FABP5 (mal1) являются членами семейства белков, связывающих жирные кислоты. FABP являются белками 14-15 кДа, которые действуют как шапероны для жирных кислот в водной среде в цитозоле и облегчают их перемещение между клеточными компартментами. Пока, по крайней мере девять членов этого семейства были идентифицированы с тканеспецифическими паттернами экспрессии. FABP4 в основном экспрессируется в жировой ткани и в макрофагах, но также и в других типах клеток, тогда как FABP5 экспрессируется в большом диапазоне тканей и органов. FABP ответственны за перемещение жирных кислот в различные клеточные компартменты и, таким образом, участвуют в основных клеточных функциях, таких как хранение липидов в адипоцитах, окисления жирных кислот в митохондриях, ER сигнализация, экспрессии генов, зависимой от жирных кислот, регуляции активности цитозольных ферментов, модуляция воспалительного ответа и синтез лейкотриена. Плазменный FABP4 секретируется жировой тканью у мышей и секреция является разрегулированной при ожирении, и блокировка плазменного FABP4 в естественных условиях антителами повышает чувствительность к инсулину.
Некоторые генетические доказательства у человека подтверждают роль FABP4 и FABP5 в метаболических заболеваниях. Мутация в FABP4 промотере (SNP Т-87С), приводящая к снижению экспрессии генов на 50%, связана с сокращением риска сердечно-сосудистых заболеваний (ССЗ) и сахарного диабета 2 типа (T2D) и к снижению триглицеридов плазмы (TGS). Две мутации в гене FABP5, одна в 5'UTR (rs454550), одна в промоторе (nSNP), связаны, соответственно, с увеличением (коэффициент риска 4,24) и снижением риска (коэффициент риска 0,48) для СД-2. Кроме того, было показано, что уровни белка FABP4 и мРНК в макрофагах атеросклеротических бляшек связаны с нестабильностью бляшек и смертью по причине сердечно-сосудистой патологии. Наконец, большое количество публикаций сообщают о связи между уровнями FABP4 и FABP5 в плазме и тяжестью заболеваний обмена веществ. Повышенные уровни FABP4 в плазме ассоциированы с атерогенной дислипидемией, сниженной эндотелиальной функцией, увеличением толщины интимы-медии (IM), метаболическим синдромом, ожирением и резистентностью к инсулину (ИР). Повышенные уровни FABP5 в плазме ассоциированы с метаболическим синдромом.
Генетические и фармакологические исследования на мышах в основном подтверждают доказательства у человека. Было показано, что с потерей функции в FABP4 и FABP5 улучшается чувствительность к инсулину, снижается глюкоза и присутствует защита от атеросклероза. Мыши с нокаутом FABP4 на диете с высоким содержанием жиров показали улучшение метаболизма, которое регулировалось компенсаторным увеличением FABP5 в жировой ткани. Мыши с делецией гена FABP5 на диете с высоким содержанием жиров (HF) показали снижение веса тела и улучшенную толерантность к глюкозе и инсулину. Мыши с двойным нокаутом FABP4/FABP5 сильно защищены от гипергликемии, резистентности к инсулину и стеатоза печени. Кроме того, на фоне недостаточного АроЕ, удаление FABP4 и FABP5 обладало сильным защитным эффектом против развития атеросклероза и увеличивало продолжительность жизни. Специфичный FABP4 ингибитор (BMS309403), показали в клэмп-тесте на мышах ob/ob уменьшение продукции глюкозы в печени, увеличение поглощения глюкозы в мышцах и жировой ткани и снижение жировой дистрофии печени, но без изменений массы тела и потребления энергии. Кроме того, оно показало снижение формирования атеросклеротических бляшек у мышей АроЕ KO. Двойной ингибитор FABP4/5, соединение 3, описанное в J. Lipid Res. 2011, 52, 646, показало у мышей на диете HF снижение триглицеридов и свободных жирных кислот в плазме, но никаких улучшений в толерантности к инсулину и глюкозе.
Объектами настоящего изобретения являются соединения формулы (I) и их вышеуказанные соли и сложные эфиры, а также их применение в качестве терапевтически активных веществ, способ изготовления указанных соединений, промежуточные соединения, фармацевтические композиции, лекарственные средства, содержащие указанные соединения, их фармацевтически приемлемые соли или сложные эфиры, применение указанных соединений, солей или эфиров для лечения или профилактики заболеваний, особенно для лечения или профилактики диабета 2 типа, метаболического синдрома, атеросклероза, дислипидемии, заболевания печени с участием воспаления, стеатоза и/или фиброза, таких как неалкогольная жировая дистрофия печени, в частности неалкогольный стеатогепатит, ожирения, липодистрофии, такой как наследственная и ятрогенная липодистрофия, рака, глазных заболеваний на фоне эндотелиальной пролиферации и ангиогенеза, таких как макулярная дистрофия и ретинопатия, заболевания легких, такого как астма, бронхолегочная дисплазия и хроническая обструктивная болезнь легких, саркоидоза, хронических заболеваний почек, таких как васкулит, фокальный сегментарный гломерулосклероз, диабетическая нефропатия, волчаночный нефрит, поликистоз почек и лекарственно или токсин-индуцированный хронический тубулоинтерстициальный нефрит, хронических воспалительных и аутоиммунных воспалительных заболеваний, преэклампсии и синдрома поликистозных яичников и применение указанных соединений, солей или эфиров для изготовления лекарственных средств для лечения или профилактики диабета 2 из типа, метаболического синдрома, атеросклероза, дислипидемии, заболевания печени с участием воспаление, стеатоза и/или фиброза, такого как неалкогольная жировая дистрофия печени, в частности неалкогольный стеатогепатит, ожирения, липодистрофии, такой как наследственная и ятрогенная липодистрофия, рака, глазных заболеваний на фоне эндотелиальной пролиферации и ангиогенеза, таких как макулярная дистрофия и ретинопатия, заболевания легких, такого как астма, бронхолегочная дисплазия и хроническая обструктивная болезнь легких, саркоидоза, хронических заболеваний почек, таких как васкулит, фокальный сегментарный гломерулосклероз, диабетическая нефропатия, волчаночный нефрит, поликистоз почек и лекарственно или токсин-индуцированный хронический тубулоинтерстициальный нефрит, хронических воспалительных и аутоиммунных воспалительных заболеваний, преэклампсии и синдрома поликистозных яичников.
Соединения настоящего изобретения являются ингибиторами FABP 4 и/или 5, более конкретно двойными ингибиторами FABP 4 и 5. Некоторые конкретные соединения формулы (I) настоящего изобретения являются также селективными ингибиторами FABP 4 и/или 5 по сравнению с FABP 3 и/или 1.
Термин "алкокси" обозначает группу формулы -O-R', где R' представляет собой алкильную группу. Примеры алкоксигруппы включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси и трет-бутокси. Конкретная алкокси группа включают метокси, этокси и изопропокси. Более конкретно, алкокси группа представляет собой метокси.
Термин "алкоксиалкокси" обозначает алкокси группу, где по меньшей мере один из атомов водорода алкокси группы был заменен другой алкоксигруппой. Пример алкоксиалкокси группы включает метоксиметокси.
Термин "алкоксиалкил" обозначает алкильную группу где по меньшей мере один из атомов водорода алкильной группы заменен на алкоксигруппу. Примеры алкоксиалкил групп включают метоксиметил, этоксиметил, метоксиэтил, метоксидиметилэтил, метоксиметилпентанил, метоксиметилпропанил, этоксиэтил, метоксипропил и этоксипропил. Конкретные алкоксиалкил группы включают метоксиметил и 2-метокси-1,1-диметилэтил.
Термин "алкоксикарбонил" обозначает группу формулы С(O)-R', где R' представляет собой алкоксигруппу. Примеры алкоксикарбонильных групп включают группы формулы С(O)-R', где R' обозначает метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси и трет-бутокси. Конкретная алкоксикарбонильная группа представляет собой группу формулы С(O)-R', где R' представляет собой трет-бутокси.
Термин "алкоксикарбонилалкил" обозначает алкильную группу, где один из атомов водорода алкильной группы заменен на алкоксикарбонильную группу. Конкретные алкоксикарбонилалкил включает 2-трет-бутокси-1,1-диметил-2-оксо-этил.
Термин "алкил" обозначает одновалентную линейную или разветвленную насыщенную углеводородную группу, содержащую от 1 до 12 атомов углерода, в частности от 1 до 7 атомов углерода, более конкретно от 1 до 4 атомов углерода, например метил, этил, пропил, изопропил, н-бутил, изо-бутил, втор-бутил, трет-бутил, этилпропил и диметилпропил. Конкретные алкильные группы включают метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, этилпропил и диметилпропил. Дополнительные конкретные алкильные группы включают метил и этилпропил.
Термин "алкилкарбонил" обозначает группу формулы -C(O)-R', где R' представляет собой алкильную группу. Примеры алкилкарбонильных групп включают группы формулы -C(O)-R', где R' представляет собой метил, этил, пропил, изопропил, н-бутил, изобутил, втор-бутил и трет-бутил. Конкретной алкилкарбонильной группой является группа формулы -C(O)-R', где R' представляет собой метил.
Термин "алкилциклоалкил" обозначает циклоалкильную группу, где по меньшей мере один атом водорода циклоалкильной группы заменен на алкильную группу. Примеры алкилциклоалкила включают метил-циклопропил, диметил-циклопропил, метил-циклобутил, диметил-циклобутил, метил-циклопентил, диметил-циклопентил, метил-циклогексил и диметил-циклогексил. Конкретные алкилциклоалкильные группы включают метил-циклопропил и диметил-циклопропил.
Термин "алкилциклоалкилалкил" обозначает алкильную группу, где по меньшей мере один атом водорода алкильной группы заменен на алкилциклоалкильную группу. Примеры алкилциклоалкилалкила включают метил-циклопропилметил, диметил-циклопропилметил, метил-циклопропилэтил, диметил-циклопропилэтил, метил-циклобутил метил, диметил-циклобутилметил, метил-циклобутилэтил, диметил-циклобутилэтил, метил-циклопентилметил, диметил-циклопентилметил, метил-циклопентилэтил, диметил-циклопентилэтил, метил-циклогексилметил, диметил-циклогексилметил, метил-циклогексилэтил, диметил-циклогексилэтил, метил-циклогептилметил, диметил-циклогептилметил, метил-циклогептилэтил, диметил-циклогептилэтил, метил-циклооктилметил, диметил-циклооктилметил, метил-циклооктилэтил и диметил-циклооктилэтил.
Термин "алкилсульфонил" обозначает группу формулы -S(O)2-R', где R' представляет собой алкильную группу. Примеры алкилсльфонильных групп включают группы формулы -S(O)2-R', где R' представляет собой метил, этил, н-пропил, изопропил, н-бутил, изобутил и трет-бутил. Конкретным примером является группа формулы -S(O)2-R', где R' представляет собой метил.
Термин "алкилсульфонилалкил" обозначает алкильную группу, где один из атомов водорода алкильной группы заменен на алкилсульфонильную группу. Конкретный пример алкилсульфонилалкила представляет собой метилсульфонилметил. Термин "алкилсульфониламино" обозначает группу форммулы -NH-S(O)2-R', где R' представляет собой алкильную группу. Примеры алкилсульфониламино включают метилсульфониламино, этилсульфониламино, пропилсульфониламино, изопропилсульфониламино, н-бутилсульфониламино, изобутилсульфониламино, втор-бутилсульфониламино, и трет-бутилсульфониламино.
Термин "амино" обозначает -NH2 группу.
Термин "аминокарбонил" обозначает группу формулы -C(O)NH2.
Термин "арил" обозначает одновалентную ароматическую карбоциклическую моно- или бициклическую кольцевую систему, содержащую от 6 до 10 кольцевых атомов. Примеры арильной группы включают фенил и нафтил. Конкретной арильной группой является фенил.
Термин "карбонил" обозначает -С(О)- группу.
Термин "циклоалкокси" обозначает группу формулы -O-R', где R' представляет собой циклоалкильную группу. Примеры циклоалкокси группы включают циклопропокси, циклобутокси, циклопентилокси, циклогексилокси, циклогептилокси и циклооктилокси. Конкретной циклоалкокси группой является циклопентилокси.
Термин "циклоалкоксиалкил" обозначает алкильную группу где по меньшей мере один атом водорода алкильной группы заменен на циклоалкокси группу. Примеры циклоалкоксиалкил группы включают циклопропоксиметил, циклопропоксиэтил, циклобутоксиметил, циклобутоксиэтил, циклопентилоксиметил, циклопентилоксиэтил, циклогексилоксиметил, циклогексилоксиэтил, циклогептилоксиметил, циклогептилоксиэтил, циклооктилоксиметил и циклооктилоксиэтил.
Термин "циклоалкил" обозначает моновалентную насыщенную моноциклическую или бициклическую углеводородную группу из 3-10 кольцевых атомов углерода, в частности моновалентную насыщенную моноциклическую углеводородную группу из 3-8 кольцевых атомов углерода. Бициклическая означает состоящая из двух насыщенных карбоциклов, обладающих двумя общими атомами углерода. Конкретными циклоалкильными группами являются циклопропил, циклобутил, циклопентил, циклогексил и циклогептинил. Дополнительными конкретными циклоалкильными группами являются циклобутил, циклопентил и циклогексил.
Термин "циклоалкилалкокси" обозначает алкокси группу где по меньшей мере один атом водорода алкокси группы заменен на циклоалкильную группу. Примеры циклоалкилалкокси включают циклопропилметокси, циклобутилметокси, циклопентилметокси, циклогексилметокси, циклогептилметокси и циклооктилметокси.
Термин "циклоалкилалкил" обозначает алкильную группу где по меньшей мере один атом водорода алкильной группы заменен на циклоалкильную группу. Примеры циклоалкилалкила включают циклопропилметил, циклопропилэтил, циклобутилпропил и циклопентилбутил.
Термин "циклоалкилсульфониламино" обозначает группу формулы -NH-S(O)2-R', где R' представляет собой циклоалкильную группу. Примеры циклоалкилсульфониламино включают циклопропилсульфониламино, циклобутанилсульфониламино, циклопентилсульфониламино или циклогексилсульфониламино.
Термин "галоалкокси" обозначает алкокси группу, где по меньшей мере один атом водорода алкокси группы заменен на одинаковые или разные атомы галогена. Термин "пергалоалкокси" обозначает алкокси группу, где все атомы водорода алкокси группы заменены на одинаковые или различные атомы галогенов. Примеры галоалкокси включают фторметокси, дифторметокси, трифторметокси, трифторэтокси, трифторметилэтокси, трифтордиметилэтокси и пентафторэтокси. Конкретными галоалкокси группами являются трифторметокси, трифторэтокси и трифторметилэтокси.
Термин "галоалкоксиалкил" обозначает алкильную группу, где по меньшей мере один атом водорода алкильной группы заменен на галоалкокси группу. Примеры галоалкоксиалкилов включают фторметоксиметил, дифторметоксиметил, трифторметоксиметил, фторэтоксиметил, дифторэтоксиметил, трифторэтоксиметил, фторметоксиэтил, дифторметоксиэтил, трифторметоксиэтил, фторэтоксиэтил, дифторэтоксиэтил, трифторэтоксиэтил, фторметоксипропил, дифторметоксипропил, трифторметоксипропил, фторэтоксипропил, дифторэтоксипропил и трифторэтоксипропил. Конкретная галоалкоксиалкил группа представляет собой 2,2-дифторэтоксиэтил.
Термин "галоалкил" обозначает алкильную группу, где по меньшей мере один атом водорода алкильной группы заменен на одинаковые или различные атомы галогена. Термин "пергалоалкил" обозначает алкильную группу, где все атомы водорода алкильной группы заменены на одинаковые или различные атомы галогена. Примеры галоалкилов включают фторметил, дифторметил, трифторметил, трифторэтил, трифторметилэтил и пентафторэтил. Конкретной галоалкильной группой является трифторметил и трифторэтил.
Термин "галоген" и "гало" используются здесь взаимозаменяемо и обозначают фтор, хлор, бром или йод. Конкретным галогенами являются хлор и фтор. Более конкретным галогеном является фтор.
Термин "гетероарил" означает одновалентную ароматическую гетероциклическую моно- или бициклическую кольцевую систему из 5-12 кольцевых атомов, содержащую 1, 2, 3 или 4 гетероатома, выбранных из N, О и S, остальные кольцевые атомы являются углеродом. Примеры гетероарильных групп включают пирролил, фуранил, тиенил, имидазолил, оксазолил, тиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридинил, пиразинил, пиразолил, пиридазинил, пиримидинил, триазинил, азепинил, диазепинил, изоксазолил, бензофуранил, изотиазолил, бензотиенил, индолил, изоиндолил, изобензофуранил, бензимидазолил, бензоксазолил, бензизоксазолил, бензотиазолил, бензизотиазолил, бензоксадиазолил, бензотиадиазолил, бензотриазолил, пуринил, хинолинил, изохинолинил, хиназолинил или хиноксалинил. Конкретные гетероарильные группы включают фуранил, тиенил, имидазолил, тиазолил, триазолил, тетразолил, пиридинил, пиразолил, пиридазинил, пиримидинил и изоксазолил.
В случае R1, конкретным гетероарилом является фуранил.
В случае R3, конкретными гетероарилами являются тиенил, имидазолил, тиазолил, триазолил, тетразолил, пиридинил, пиразолил, пиридазинил, пиримидинил и изоксазолил. Также, конкретными гетероарилами являются оксазолил, индолил, пиридинонил и индазолил,
Термин "гетероциклоалкокси" обозначает группу формулы -O-R', где R' представляет собой гетероциклоалкильную группу. Конкретными R' являются тетрагидрофуранил и тетрагидро-2Н-пиранил. Дополнительным конкретным R' является тетрагидрофуранил.
Термин "гетероциклоалкил" означает одновалентную насыщенную или частично ненасыщенную моно- или бициклическую кольцевую систему из 4-9 кольцевых атомов, содержащую 1, 2, или 3 кольцевых гетероатома, выбранных из N, О и S, остальные кольцевые атомы являются углеродами. Бициклический означает состоящий из двух насыщенных циклов с двумя общими кольцевыми атомами, то есть мост, разделяющий два кольца, представляет собой либо простую связь, либо цепь из одного или двух кольцевых атомов. Примерами моноциклических насыщенных гетероциклоалкилов являются 4,5-дигидро-оксазолил, оксетанил, азетидинил, пирролидинил, тетрагидрофуранил, тетрагидро-тиенил, пиразолидинил, имидазолидинил, оксазолидинил, изоксазолидинил, тиазолидинил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиперазинил, морфолинил, тиоморфолинил, 1,1-диоксо-тиоморфолин-4-ил, азепанил, диазепанил, гомопиперазинил или оксазепанил. Примерами бициклических насыщенных гетероциклоалкилов являются 8-аза-бицикло[3.2.1]октил, хинуклидинил, 8-оксо-3-аза-бицикло[3.2.1]октил, 9-аза-бицикло[3.3.1]нонил, 3-окса-9-аза-бицикло[3.3.1]нонил или 3-тиа-9-аза-бицикло[3.3.1]нонил. Примерами частично ненасыщенных гетероциклоалкилов являются дигидрофурил, имидазолинил, дигидро-оксазолил, тетрагидро-пиридинил или дигидропиранил. Частными примерами гетероциклоалкильных групп являются азетидинил, пирролидинил, тетрагидрофуранил, пиперидинил и тетрагидропиранил. Дополнительными частными примерами гетероциклоалкильной группы являются тетрагидрофуранил и пиперидинил.
Термин "гетероциклоалкилалкокси" обозначает алкокси группу где по меньшей мере один из атомов водорода алкокси группы заменен на гетероциклоалкильную группу. Конкретным примером гетероциклоалкилалкокси является тетрагидрофуранилметил.
Термин "гидрокси" обозначает группу -ОН.
Термин "гидроксиалкокси" обозначает алкокси группу где по меньшей мере один из атомов водорода алкокси группы заменен на гидрокси группу. Примеры гидроксиалкокси включают гидроксиэтокси, гидроксипропокси,
гидроксиметилпропокси и дигидроксипропокси. Конкретным примером гидроксиалкокси группы является гидроксиэтокси.
Термин "гидроксиалкил" обозначает алкильную группу, где по меньшей мере один атом водорода алкильной группы заменен на гидрокси группу. Примеры гидроксиалкила включают гидроксиметил, гидроксиэтил, гидроксипропил, гидроксиметилпропил и дигидроксипропил. Конкретными примерами являются гидроксиметил и гидроксиэтил.
Термин "карбокси" обозначает -СООН группу.
Термин "карбоксиалкил" обозначает алкильную группу где один атом водорода алкильной группы заменен на карбокси группу. Конкретная карбоксиалкильная группа представляет собой 1-карбокси-1-метил-этил.
Термин "оксо" обозначает группу =O.
Термин "сульфонил" обозначает группу -S(O)2-.
Термин "фармацевтически приемлемые соли" относится к солям, которые сохраняют биологическую эффективность и свойства свободных оснований или свободных кислот, которые не являются биологически или иным образом нежелательными. Соли образованы с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., предпочтительно, соляная кислота, и органическими кислотами, такими как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота, N-ацетилцистеин и т.п. Кроме того, эти соли могут быть получены путем добавления неорганического основания или органического основания к свободной кислоте. Соли, полученные из неорганических оснований включают, без ограничения, соли натрия, калия, лития, аммония, кальция и магния и т.п. Соли, полученные из органических оснований, включают, без ограничения, соли первичных, вторичных и третичных аминов, замещенных аминов, включая природные замещенные амины, циклические амины и основные ионообменные смолы, такие как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, лизин, аргинин, N-этилпиперидин, пиперидин, полиаминовые смолы и т.п. Конкретными фармацевтически приемлемыми солями соединений формулы (I) являются соли соляной кислоты, соли метансульфоновой кислоты и соли лимонной кислоты. Конкретными фармацевтически приемлемыми солями соединений формулы (I) являются также соли натрия и калия.
"Фармацевтически приемлемые эфиры" означает, что соединения общей формулы (I) могут быть дериватизированы по функциональным группам с получением производных, которые способны превратиться обратно в исходные соединения в условиях in vivo. Примеры таких соединений включают физиологически приемлемые и метаболически лабильные эфирные производные, такие как метоксиметиловые эфиры, метилтиометиловые эфиры и пивалоилоксиметиловые эфиры. Дополнительно, любые физиологически приемлемые эквиваленты соединений общей формулы (I), аналогичные метаболически лабильным эфирам, которые способны превращаться в исходные соединения общей формулы (I) in vivo, включены в объем настоящего изобретения.
Термин "защитная группа" обозначает группу, которая селективно блокирует реакционноспособный участок в многофункциональном соединении таким образом, что химическая реакция может быть проведена селективно в другом незащищенном реакционноспособном участке, в значении обычно связанным с ним в синтетической химии. Защитные группы могут быть удалены на соответствующей стадии. Типичные защитные группы представляют собой амино-защитные группы, карбокси-защитные группы или гидрокси-защитные группы. Конкретные защитные группы представляют собой трет-бутоксикарбонил (ВОС), бензилоксикарбонил (CBZ), флуоренилметилоксикарбонил (Fmoc) и бензил (Bn). Дополнительно конкретными защитными группами являются трет-бутоксикарбонил (ВОС) и флуоренилметилоксикарбонил (Fmoc). Более конкретнымой защитной группой является трет-бутоксикарбонил (ВОС).
Соединение формулы (I) может содержать несколько асимметричных центров и/или стереоосей и может присутствовать в форме оптически чистых энантиомеров, смесей энантиомеров, таких как, например, рацематы, оптически чистых диастереоизомеров, смесей диастереоизомеров, диастереоизомерных рацематов или смесей диастереоизомерных рацематов.
Согласно правилам Кана - Ингольда - Прелога асимметричный атом углерода может быть "R" или "S" конфигурации.
Также воплощением настоящего изобретения являются соединения в соответствии с формулой (I), как здесь описано, и их фармацевтически приемлемые соли или эфиры, в частности, соединения в соответствии с формулой (I), как здесь описано, и их фармацевтически приемлемые соли, более конкретно, соединения в соответствии с формулой (I), как здесь описано.
Воплощением настоящего изобретения являются соединения формулы (I)

где
R1 представляет собой алкил, галоалкил, циклоалкил, замещенный циклоалкил, алкокси, алкоксиалкил, галоалкокси, галоалкоксиалкил, циклоалкокси, замещенный циклоалкокси, циклоалкоксиалкил, замещенный циклоалкоксиалкил, гидроксиалкил, арил, замещенный арил, гетероциклоалкил, замещенный гетероциклоалкил, гетероарил, замещенный гетероарил, амино, замещенный амино, аминокарбонил или замещенный аминокарбонил, где замещенный циклоалкил, замещенный циклоалкокси, замещенный циклоалкоксиалкил, замещенный арил, замещенный гетероциклоалкил и замещенный гетероарил замещены одним - тремя заместителями, независимо выбранными из гидрокси, оксо, галогена, алкила, циклоалкила, галоалкила, алкилциклоалкила, циклоалкилалкила, алкилциклоалкилалкила, гидроксиалкила, алкокси и алкоксиалкила и где замещенный амино и замещенный аминокарбонил замещены по атому азота одним - двумя заместителями, независимо выбранными из алкила, циклоалкила, галоалкила, алкилциклоалкила, циклоалкилалкила, алкилциклоалкилалкила, гидроксиалкила и алкоксиалкила;
R2 представляет собой -СООН, тетразол-5-ил, [1,3,4]оксадиазол-2-он-5-ил, [1,3,4]оксадиазол-2-тион-5-ил, [1,2,4]оксадиазол-5-он-3-ил, [1,2,4]оксадиазол-5-тион-3-ил, [1,2,3,5]оксатиадиазол-2-оксид-4-ил, [1,2,4]тиадиазол-5-он-3-ил, изоксазол-3-ол-5-ил, 5-алкилизоксазол-3-ол-4-ил, 5-циклоалкилизоксазол-3-ол-4-ил, фуразан-3-ол-4-ил, 5-алкилсульфониламино-[1,3,4]оксадиазол-2-ил, 5-циклоалкилсульфониламино-[1,3,4]оксадиазол-2-ил, 5-алкилсульфониламино-[1,2,4]триазол-3-ил, 5-циклоалкилсульфониламино-[1,2,4]триазол-3-ил, 5-алкилизотиазол-3-ол-4-ил, 5-циклоалкилизотиазол-3-ол-4-ил, [1,2,5]тиадиазол-3-ол-4-ил, 1,4-дигидро-тетразол-5-он-1-ил, тетразол-5-илкарбамоил, тетразол-5-карбонил, [1,2,4]оксадиазолидин-3,5-дион-2-ил, [1,2,4]оксадиазол-5-он-3-ил, 2,4-дигидро-[1,2,4]триазол-3-он-5-сульфанил, [1,2,4]триазол-3-сульфанил, [1,2,4]триазол-3-сульфинил, [1,2,4]триазол-3-сульфонил, 4-алкил-пиразол-1-ол-5-ил, 4-циклоалкил-пиразол-1-ол-5-ил, 4-алкил-[1,2,3]триазол-1-ол-5-ил, 4-циклоалкил-[1,2,3]триазол-1-ол-5-ил, 5-алкил-имидазол-1-ол-2-ил, 5-циклоалкил-имидазол-1-ол-2-ил, 4-алкил-имидазол-1-ол-5-ил, 4-циклоалкил-имидазол-1-ол-5-ил, 4-алкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, 4,4-диалкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, 4-циклоалкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, 4,4-дициклоалкил-1,1-диоксо-1λ6-[1,2,5]тиадиазолидин-3-он-5-ил, тиазолидин-2,4-дион-5-ил, оксазолидин-2,4-дион-5-ил, 3-[1-гидрокси-мет-(Е)-илиден]-пирролидин-2,4-дион-1-ил, 3-[1-гидрокси-мет-(Z)-илиден]-пирролидин-2,4-дион-1-ил, 5-метил-4-гидроксифуран-2-он-3-ил, 5,5-диалкил-4-гидроксифуран-2-он-3-ил, 5-циклоалкил-4-гидроксифуран-2-он-3-ил, 5,5-дициклоалкил-4-гидроксифуран-2-он-3-ил, 3-гидроксициклобут-3-ен-1,2-дион-4-ил или 3-гидроксициклобут-3-ен-1,2-дион-4-амино;
R3 представляет собой фенил, замещенный фенил, замещенный дигидропиридинил, гетероарил или замещенный гетероарил, где замещенный фенил, замещенный дигидропиридинил и замещенный гетероарил замещены одним - тремя заместителями, независимо выбранными из гидрокси, оксо, галогена, алкила, циклоалкила, галоалкила, алкилциклоалкила, цикпоалкилалкила, алкилциклоалкилалкила, гидроксиалкила, гидроксиалкокси, алкокси, алкоксиалкила, амино и амино, замещенного по атому азота одним - двумя заместителями, независимо выбранными из алкила, циклоалкила, галоалкила, алкилциклоалкила, цикпоалкилалкила, алкилциклоалкилалкила, гидроксиалкила и алкоксиалкила;
А1 представляет собой связь или CR12R13;
А2 представляет собой -CR14R15-, -NR16-, -О-, -S-, -S(O)- или -S(O)2-;
А3 представляет собой -CR17R18-, -C(O)NR19-, -NR19-, -О-, -S-, -S(O)- или -S(O)2-;
R4, R5, R6, R7, R8, R9, R10, R11, R14, R15, R17 и R18 независимо выбраны из H, галогена, алкила, алкокси, циклоалкила, циклоалкилалкокси, галоалкокси и галоалкила.
R12 и R13 независимо выбраны из водорода, алкила, циклоалкила и галоалкила.
R16 и R19 независимо выбраны из водорода, алкила, циклоалкила, галоалкила и алкилкарбонила.
n, m и р независимо выбраны из 0 и 1;
и их фармацевтически приемлемые соли.
Также, дополнительным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R1 представляет собой алкил, циклоалкил, замещенный циклоалкил, алкокси, алкоксиалкил, алкоксиалкокси, алкоксикарбонилалкил, карбоксиалкил, галоалкил, галоалкокси, замещенный арил, гетероциклоалкил, замещенный гетероциклоалкил, гетероциклоалкокси, замещенный гетероциклоалкилалкокси, гетероарил, замещенный гетероарил, амино или замещенный амино, где замещенный циклоалкил, замещенный арил, замещенный гетероциклоалкил, замещенный гетероциклоалкилалкокси и замещенный гетероарил замещены одним - тремя заместителями, независимо выбранными из галогена, алкила, галоалкила, гидроксиалкила, алкилсульфонилалкила, алкоксикарбонила и алкоксиалкила, и где замещенный амино замещен по атому азота двумя алкилами.
Дополнительным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R1 представляет собой алкил, циклоалкил, замещенный циклоалкил, алкоксиалкил, замещенный арил, гетероциклоалкил, замещенный гетероциклоалкил, гетероарил, амино или замещенный амино, где замещенный циклоалкил, замещенный арил и замещенный гетероциклоалкил замещены одним - тремя заместителями, независимо выбранными из галогена, алкила, галоалкила и алкоксиалкила, и где замещенный амино замещен по атому азота двумя алкилами.
Частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R1 представляет собой циклоалкил, замещенный циклоалкил, гетероциклоалкил, замещенный гетероциклоалкил, гетероциклоалкилалкокси или замещенный амино, где замещенный циклоалкил и замещенный гетероциклоалкил замещены одним алкилом или алкоксиалкилом, и где замещенный амино замещен по атому азота двумя алкилами.
Частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R1 представляет собой циклоалкил, замещенный циклоалкил, гетероциклоалкил или замещенный амино, где замещенный циклоалкил замещен одним алкоксиалкилом, и где замещенный амино замещен по атому азота двумя заместителями, независимо выбранными из алкила.
Дополнительным частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R1 представляет собой циклопентил, замещенный циклопентил, тетрагидрофуранил, замещенный тетрагидрофуранил, тетрагидрофуранилокси, пиперидинил или замещенный амино, где замещенный циклопентил и замещенный тетрагидрофуранил замещены одним алкилом или алкоксиалкилом, и где замещенный амино замещен по атому азота двумя алкилами.
Частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R1 представляет собой циклопентил, замещенный циклопентил, тетрагидрофуранил, пиперидинил или замещенный амино, где замещенный циклопентил замещен одним алкоксиалкилом и где замещенный амино замещен по атому азота двумя заместителями, независимо выбранными из алкила.
Дополнительным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R2 представляет собой -СООН, тетразол-5-ил или [1,3,4]оксадиазол-2-тион-5-ил.
Другим дополнительным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R2 представляет собой тетразол-5-ил.
Другим воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R3 представляет собой фенил, замещенный фенил, замещенный дигидропиридинил, гетероарил или замещенный гетероарил, где замещенный фенил, замещенный дигидропиридинил и замещенный гетероарил замещены одним - тремя заместителями, независимо выбранными из гидрокси, оксо, галогена, алкила, циклоалкила, галоалкила, галоалкокси, гидроксиалкокси, алкокси, алкилсульфонила и амино, замещенного по атому азота одним - двумя заместителями, независимо выбранными из алкила, циклоалкила, галоалкила, алкилциклоалкила, цикпоалкилалкила, алкилциклоалкилалкила, гидроксиалкила и алкоксиалкила.
Другим воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R3 представляет собой фенил, замещенный фенил, замещенный дигидропиридинил, гетероарил или замещенный гетероарил, где замещенный фенил, замещенный дигидропиридинил и замещенный гетероарил замещены одним - тремя заместителями, независимо выбранными из оксо, галогена, алкила, циклоалкила, галоалкила, гидроксиалкокси и алкокси.
Другим частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R3 представляет собой фенил, замещенный фенил или замещенный гетероарил, где замещенный фенил и замещенный гетероарил замещены одним - тремя заместителями, независимо выбранными из галогена и алкила.
Настоящее изобретение также относится к соединениям согласно формуле (I), как здесь описано, где R3 представляет собой фенил, замещенный фенил, замещенный пиразолил или замещенный пиридинил, где замещенный фенил, замещенный пиразолил и замещенный пиридинил замещены одним - тремя заместителями, независимо выбранными из галогена и алкила.
Дополнительным частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R3 представляет собой замещенный пиразолил или замещенный пиридинил, где замещенный пиразолил и замещенный пиридинил замещены одним алкилом.
Частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R3 представляет собой пиридинил замещенный одним алкилом или галогеном.
Более конкретным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R3 представляет собой пиридинил, замещенный одним алкилом.
Также воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где А1 представляет собой связь.
Настоящее изобретение также относится к соединениям согласно формуле (I), как здесь описано, где А2 представляет собой -CR14R15-, -NR16-, -О- или -S-.
Настоящее изобретение также относится к соединениям согласно формуле (I), как здесь описано, где А2 представляет собой -CR14R15-, -NR16- или -О-.
Другим воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где А2 представляет собой -CR14R15.
Дополнительным частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где А3 представляет собой -CR17R18-, -C(O)NR19- или -NR19.
Дополнительным частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где А3 представляет собой -CR17R18- или -NR19.
Частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где А3 представляет собой -CR17R18-.
Также воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где n представляет собой 1.
Дополнительным частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где р представляет собой 0.
Настоящее изобретение также относится к соединениям согласно формуле (I), как здесь описано, где R4, R5, R6, R7, R8, R9, R10 и R11 представляют собой Н.
Другим воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R4 и R5 представляют собой Н.
Настоящее изобретение также относится к соединениям согласно формуле (I), как здесь описано, где R6 и R7 представляют собой Н.
Также воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R8 и R9 представляют собой Н.
Также воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R10 и R11 представляют собой Н.
Другим воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R14 представляет собой Н, галоген, алкил, алкокси или галоалкил.
Частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R15 представляет собой Н, галоген или алкил.
Дополнительным частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R14 и R15 независимо выбраны из Н, галоген и алкил.
Частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R17 и R18 независимо выбраны из Н и алкил.
Более конкретным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R17 и R18 представляют собой Н.
Также частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R16 представляет собой галоалкил или алкилкарбонил.
Также частным воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R19 представляет собой алкил или алкилкарбонил.
Также воплощением настоящего изобретения являются соединения согласно формуле (I), как здесь описано, где R16 и R17 представляют собой галоген.
Конкретные примеры соединений формулы (I), как здесь описано, выбраны из:
2-изопропил-6,8-диметил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
8-ацетил-2-изопропил-6-метил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
8-этил-2-изопропил-6-метил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
4-(3-хлорфенил)-2-циклогексил-8-этил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклогексил-8-этил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклопентил-8-этил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклопентил-8-этил-6-метил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклопентил-6,8-диметил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-изопропил-6-метил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
6-этил-2-изопропил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-изопропил-6,6-диметил-4-фенил-5,6,7,8-тетрагидро-хинолин-3-карбоновая кислота;
2-циклопентил-4-(6-метоксипиридин-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклопентил-4-(6-оксо-1,6-дигидропиридин-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
4-фенил-2-(пиперидин-1-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-(2-метилпирролидин-1-ил)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
6-метил-4-фенил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-(диэтиламино)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
6-метил-2-(2-метилпирролидин-1-ил)-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-(диэтиламино)-6-метил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
4-(3-хлорфенил)-6-метил-2-(пирролидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
4-фенил-2-(пиперидин-1-ил)-6,7-дигидро-5Н-циклопента[b]пиридин-3-карбоновая кислота;
2-(диэтиламино)-4-фенил-6,7-дигидро-5Н-циклопента[b]пиридин-3-карбоновая кислота;
4-(3-хлорфенил)-6-метил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
5-(6-метил-4-фенил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-ил)-1,3,4-оксадиазол-2(3Н)-тион;
6-метил-4-фенил-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
N,N-диэтил-6-метил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин-2-амин;
4-фенил-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
N,N-диэтил-4-фенил-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин-2-амин;
6-метил-4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-фенил-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-фенил-3-(2Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(3-хлорфенил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлорфенил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(4-фторфенил)-6-метил-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(4-фторфенил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-7,8-дигидро-5Н-пирано[4,3-b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилпирролидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(5-хлортиофен-2-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
5-метил-3-(2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)изоксазол;
N,N-диэтил-4-(5-метилизоксазол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилпирролидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(пиперидин-1-ил)-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(5-метилфуран-2-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(5-метилфуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(1,5-диметил-1Н-пиразол-4-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1,5-диметил-1Н-пиразол-4-ил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(5-хлортиофен-2-ил)-2-(3-фторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(3,3-дифторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(4,4-дифторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(4-фторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-3-(1Н-тетразол-5-ил)-2-(4-(трифторметил)пиперидин-1-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(3,3-дифторазетидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(4-метилтиазол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-метил-5-(2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)тиазол;
N,N-диэтил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин-2-амин;
4-(5-хлортиофен-2-ил)-2-(3,3-дифторпирролидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
диэтил-[4-пиримидин-5-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил]-амин;
N,N-диэтил-4-(3-фторпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
N,N-диэтил-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
2-пропил-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пентан-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлорфенил)-2-циклобутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-пиридин-4-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-Н-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-Н-циклогепта[b]пиридин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
5-(2-циклогексил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)пиридин-2(1Н)-он;
5-(2-циклогексил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-1-этилпиридин-2(1Н)-он;
5-(2-циклогексил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-1-метилпиридин-2(1Н)-он;
2-циклогексил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
1-(4-(3-хлорфенил)-2-циклобутил-3-(1Н-тетразол-5-ил)-7,8-дигидро-1,6-нафтиридин-6(5Н)-ил)ethanone;
2-циклопентил-4-(6-метоксипиридин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидро-2Н-пиран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-(3-фторпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(3-фторпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидро-2Н-пиран-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-(2-метилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
5-(2-циклобутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-1-метилпиридин-2(1Н)-он;
2-циклогексил-4-(пиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-метилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиридазин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(6-метилпиридин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиридин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропил-4-(2-изопропилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиримидин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(2-(2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)фенокси)этанол;
2-циклопентил-4-(2-изопропилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропил-4-(2-изопропилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-изопропилпиридин-4-ил)-2-(пентан-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пентан-3-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-6-метил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6,6-дифтор-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-циклогексил-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин-4-ил)-3,5-диметилизоксазол;
4-(2-циклогексил-6-метил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин-4-ил)-3,5-диметилизоксазол;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-фенил-3-(2Н-тетразол-5-ил)-6-(2,2,2-трифторэтил)-5,6,7,8-тетрагидро-1,6-нафтиридин;
2-циклопентил-6,6-диметил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6-метокси-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6-метил-4-(2-метилпиридин-4-ил)-2-трет-пентил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-метокси-2-метилпропан-2-ил)-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6,7-дигидро-5Н-циклопента[b]пиридин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6,7-дигидро-5Н-циклопента[b]пиридин;
2-трет-бутил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(3-фторфенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(4-(трифторметил)фенил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(3-(трифторметил)фенил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3,3-дифторциклобутил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(4-фтор-фенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-трет-бутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)оксазол;
2-трет-бутил-4-(1-метил-1Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(4-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(3-циклопропил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-трет-бутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-2-метилоксазол;
2-трет-бутил-4-(4-хлор-1Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(4-(трифторметил)-1Н-имидазол-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(1Н-1,2,3-триазол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(2-бутил-1Н-имидазол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фуран-2-ил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фтор-бутил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-фторфенил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фтор-бутил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
и их фармацевтически приемлемые соли.
Также, конкретные примеры соединений формулы (I), как здесь описано, выбраны из
4-фенил-2-(R)-тетрагидро-фуран-2-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(S)-тетрагидро-фуран-2-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(R)-4-(2-хлорпиридин-4-ил)-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(2-хлорпиридин-4-ил)-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
(S)-4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
(R)-4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-((S)-2-метил-тетрагидро-фуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-((R)-2-метил-тетрагидро-фуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-метоксифенил)-2-(2-метилтетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-метокси-фенил)-2-((S)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-метокси-фенил)-2-((R)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-метилпиридин-4-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-[(2S)-2-метилоксолан-2-ил]-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-[(2R)-2-метилоксолан-2-ил]-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлорфенил)-2-(2-метилтетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-((S)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-((Р)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метил циклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метилциклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-метоксипиридин-4-ил)-2-(1-метил циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-(1-метилциклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)пиридин-2(1Н)-он;
4-(3-хлор-фенил)-2-(1-метил-циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(1-метил циклогексил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метил циклогексил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксиметил-циклопентил)-4-(2-метил-2Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-фторпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(4-метил-1Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1Н-индол-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этилпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
3-(2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-2-метилфенол;
4-(2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-2-метилоксазол;
4-(1Н-индазол-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-4-(2-(трифторметил)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-4-(2-(2,2,2-трифторэтокси)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этоксипиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(4-фтор-3-метоксифенил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(4-фторфенил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(3-метоксифенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-фтор-5-метоксифенил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5H-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-(1-метоксиметил-циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-(метоксиметил)пентан-3-ил)-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-(метоксиметил)пентан-3-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-этилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-N-метилпиридин-2-амин;
2-циклопентил-3-(1Н-тетразол-5-ил)-4-(2-(трифторметил)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(3-метилпентан-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этилпиридин-4-ил)-2-изопропил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропил-3-(1Н-тетразол-5-ил)-4-(2-(2,2,2-трифторэтокси)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этоксипиридин-4-ил)-2-изопропил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксициклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксициклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-метоксициклопентил)-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-(1-метоксициклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксициклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(1-(4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(1-(4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин-2-ил)циклопентил)метанол;
(1-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(1-(4-(3-хлорфенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(1-(4-(4-фторфенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(S)-трет-бутил 2-(4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пирролидин-1-карбоксилат;
(S)-4-фенил-2-(пирролидин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин 2,2,2-трифторацетат;
2-циклопентил-4-фенил-3-(1Н-тетразол-5-ил)-7,8-дигидро-5Н-пиридо[2,3-с]азепин-9(6Н)-он;
2-(1-метокси-2-метилпропан-2-ил)-6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-2-трет-пентил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-метокси-2-метилпропан-2-ил)-6,6-диметил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-метоксиметил-циклогексил)-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидро-хинолин;
6,6-дифтор-2-(1-(метоксиметил)циклопентил)-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(4-метилтетрагидро-2Н-пиран-4-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(4-метилтетрагидро-2Н-пиран-4-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклопентил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-6,6-дифтор-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-6,6-дифтор-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклогексил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-4-(1-метил-1Н-пиразол-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-6,6-дифтор-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-6,6-дифтор-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-6,6-дифтор-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(1-метил-1Н-пиразол-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3-хлорфенил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-(3-метоксифенил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(4-фтор-3-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метилсульфонилметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-4-(4-фтор-3-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-4-(4-фтор-3-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(3-(метилсульфонил)фенил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(3-метоксифенил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-фтор-5-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-фтор-5-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(этоксиметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(3,3-дифторциклобутил)-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1,5-диметил-1Н-пиразол-4-ил)-4-фенил-3-(2Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3,3-дифторциклобутил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фтор-бутил-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-6,6-дифтор-4-(2-метил-пиридин-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидро-хинолин;
2-трет-бутил-6,6-дифтор-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидро-хинолин;
2-трет-бутил-6,6-дифтор-4-(2-метил-2Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидро-хинолин;
2-трет-бутил-4-фенил-3-(1Н-тетразол-5-ил)-7,8-дигидро-5Н-тиопирано[4,3-b]пиридин;
2-трет-бутил-8,8-диметил-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-трет-бутил-7,7-диметил-4-фенил-3-(1Н-тетразол-5-ил)-6,7-дигидро-5Н-циклопента[b]пиридин;
2-трет-бутил-8,8-диметил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-трет-бутил-8,8-диметил-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклобутил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклобутил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклобутил)-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(перфторэтил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-8,8-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2,4-бис(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропокси-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-метокси-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-этокси-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-фенил-2-(тетрагидрофуран-3-илокси)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил;
(R)-4-фенил-2-(тетрагидрофуран-3-илокси)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил;
2-этокси-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропокси-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-этокси-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(2-метоксиэтокси)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-((тетрагидрофуран-2-ил)метокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-фторпропокси)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(2,2-дифторэтокси)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-фенил-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-метилпиридин-4-ил)-2-(тетрагидро-2Н-пиран-4-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(2-метилпиридин-4-ил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(2-метилпиридин-4-ил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-4-(4-(трифторметил)фенил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-фторфенил)-2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(3-фторфенил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3,5-дифторфенил)-2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(3-фторфенил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(3,5-дифторфенил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-фторфенил)-2-((S)-тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-фторфенил)-2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-4-(тиофен-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-фторпропокси)-3-(1Н-тетразол-5-ил)-4-(тиофен-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-4-(тиофен-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидро-2Н-пиран-4-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метилциклопентил)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
4-(3-хлорфенил)-2-(1-метилциклопентил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
4-(1-метил-1Н-пиразол-5-ил)-2-(1-метилциклогексил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-(1-метилциклогексил)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклогексил-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-(1-метилциклогексил)-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклогексил-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклопентил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-(1-(метоксиметил)циклопентил)-6-пентил-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
трет-бутил 2-метил-2-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пропаноат;
2-метил-2-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пропановая кислота;
и их фармацевтически приемлемые соли.
Дополнительные частные примеры соединений формулы (I), как здесь описано, выбраны из
6-метил-4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3-хлорфенил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-6,6-дифтор-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6,6-диметил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
и их фармацевтически приемлемые соли.
Также дополнительные частные примеры соединений формулы (I), как здесь описано, выбраны из
2-((R)-2-метил-тетрагидро-фуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метил циклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(R)-6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-4-фенил-2-(тетрагидрофуран-3-ил окси)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил;
2-(1-метилциклогексил)-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
и их фармацевтически приемлемые соли.
Способы производства соединений формулы (I), как здесь описано, являются объектом изобретения.
Получение соединений формулы (I) по настоящему изобретению может быть проведено последовательными или конвергентными путями синтеза. Синтезы по изобретению показаны на следующих общих схемах. Навыки, необходимые для проведения реакции и очистки полученных продуктов известны специалистам в данной области техники. В случае, если во время реакции получают смесь энантиомеров или диастереоизомеров, эти энантиомеры или диастереоизомеры могут быть разделены с помощью способов, описанных здесь, или способами, известными специалисту в данной области, такими как, например, хиральная хроматография или кристаллизация.
В случае, если исходное вещество или соединение формулы (I) содержат одну или более функциональных групп, которые нестабильны или являются реакционноспособными в реакционных условиях на одной или более реакционных стадий, могут быть введены подходящие защитные группы перед критической стадией с использованием способов, хорошо известных в уровне техники. Такие защитные группы могут быть удалены на более поздней стадии синтеза с использованием обычных способов, описанных в литературе. Заместители и индексы, используемые в последующем описании способов, обладают данным здесь значением.
Аббревиатуры
Следующие сокращения используются в настоящем изобретении:
д = дни, ДХМ = дихлорметан, ДМА = N,N-диметилацетамид, ДМФ = N,N-диметилформамид, ДМСО = диметилсульфоксид, EtOAc = этилацетат, ESP = электроспрей ионизация, положительные ионы, ESN = электроспрей ионизация, отрицательные ионы, EtOH = этанол, ч = часы, HCl = соляная кислота, МеОН = метанол, мин=минуты, NaOH = гидроксид натрия, Na2SO4 = сульфат натрия, OTf = CF3-SO2-O-, ТГФ = тетрагидрофуран.
Соединения формулы (I), где R2 представляет собой 5-тетразолил могут быть получены, как показано на схеме 1.

Нитрил производные формулы (II) могут быть конвертированы в соединения формулы (I), где R2 представляет собой 5-тетразолил, посредством взаимодействия с азидными реагентами M-N3, где М обозначает натрий, триалкилолово или триалкилсилил, возможно в присутствии вспомогательных веществ, таких как соли цинка или оксид дибутилолова. Обычные условия включают азид натрия в присутствии хлорида цинка в растворителе, таком как ДМФ, при повышенной температуре, азид триметилолова в растворителе, таком как ксилен, при повышенной температуре или триметилсилилазид в присутствии оксида дибутилолова в растворителе, таком как диоксан, при повышенной температуре.
Соединения формулы (I), где R2 представляет собой -СООН, могут быть получены, как показано на схеме 2.
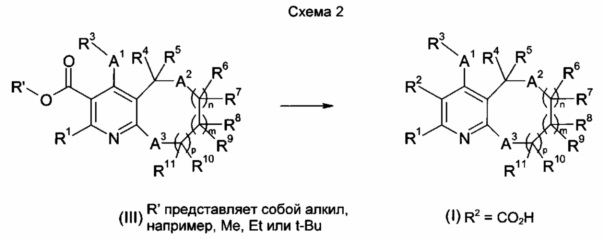
Эфирные производные формулы (III) могут быть конвертированы в соединения формулы (I), где R2 представляет собой -СООН, посредством взаимодействия с гидроксидом металла, таким как лития, натрия или калия гидроксид, в смеси растворителей, содержащей ДМСО-вода, этанол-вода, ТГФ-метанол-вода или метанол-вода, при повышенной температуре. Альтернативно, расщепление эфира может быть выполнено посредством взаимодействия с нуклеофилом, таким как йодид лития в пиридине при повышенных температурах. Эфирные производные формулы (III), где R' представляет собой трет-бутил могут быть конвертированы в соединения формулы (I), где R2 представляет собой -СООН посредством взаимодействия с кислотой, такой как HCl, в растворителе, таком как диоксан или с ТФУ в растворителе, таком как ДХМ. Другие способы расщепления эфиров могут быть найдены в литературе.
Альтернативно, соединения формулы (I), где R2 представляет собой -СООН могут быть получены, как показано на схеме 3.

Нитрил производные формулы (II) могут быть обработаны водным раствором кислоты, такой как HCl, или альтернативно, водным раствором основания, такого как гидроксид калия, при повышенной температуре с получением соединений формулы (I), где R2 представляет собой -СООН. Нитрилы формулы (II) также могут быть конвертированы в соединения формулы (I), где R2 представляет собой -СООН посредством конверсии в соответствующие иминоэфиры с помощью добавления спиртового раствора кислот, таких как HCl, HBr или аналогичных при различных температурах, предпочтительно в диапазоне от 0 до 100°С, с последующим гидролизом иминоэфира до соответствующего эфира и гидролиза эфира, как описано выше.
Нитрил промежуточные соединения формулы (II), где А3 представляет собой -CR17R18-, могут быть получены, как показано на схеме 4.

Четырехкомпонентная реакция подходящих β-кетонитрилов (IV), альдегидов (V), циклических кетонов формулы (VI) и ацетата аммония в инертном растворителе, таком как толуол при повышенной температуре, возможно с удалением воды, дает дигидропиридиновые соединения, которые могут быть окислены до производных формулы (II) с использованием окислительных агентов, таких как аммоний-церий азотнокислый.
Альтернативное получение промежуточных соединений формулы (II), где А3 представляет собой-CR17R18- показано на схеме 5.
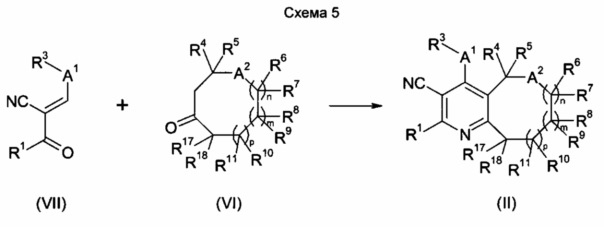
Трехкомпонентная реакция α,β-ненасыщенных кетонитрилов (VII), циклических кетонов формулы (VI) и ацетата аммония при повышенной температуре в воздушной атмосфере дала промежуточные соединения формулы (II). Соединения формулы (VII) могут быть получены посредством конденсации Кневенагеля с использованием подходящих 6-кетонитрилов (IV) и альдегидов (V). Обычные условия для такой трансформации включают взаимодействие соединений формулы (IV) и (V) в спиртовом растворителе, таком как этанол или метанол, возможно в присутствии L-пролина, при комнатной температуре или взаимодействие соединений формулы (IV) и (V) в присутствии амина, такого как пиперидин в толуоле в качестве растворителя при кипении, возможно с удалением воды.
Эфирные производные формулы (III), где А3 представляет собой -CR17R18- и R' представляет собой алкил, такой как метил, этил или трет-бутил, могут быть получены, как показано на схеме 6.

Присоединение Михаэля енолатов, полученных из циклических кетонов формулы (VI) с α,β-ненасыщенными кетоэфирами (VIII) и последующее взаимодействие с ацетатом аммония и окисление дают эфирные промежуточные соединения формулы (III). Образование енолатов из кетонов формулы (VI) может быть выполнено с основанием, таким как LDA, LiHMDS и NaHMDS в инертном растворителе, таком как ТГФ, при низкой температуре. Циклизация получившихся аддуктов реакции Михаэля с ацетатом аммония в присутствии каталитического количества кислоты, такой как п-толуолсульфоновая кислота, в спиртовом растворителе, таком как этанол, при повышенной температуре дает дигидропиридины, которые могут быть окислены до производных формулы (III) с использованием окислительных агентов, таких как DDQ.
Эфирные производные формулы (III), где А3 представляет собой N-R19 и R' представляет собой алкил, такой как метил, этил или трет-бутил, могут быть получены, как показано на схеме 7.

Присоединение Михаэля енолатов, полученных из лактамов формулы (IX) с α,β-ненасыщенными кетоэфирами (VIII) дает соединения формулы (X). Образование енолатов может быть выполнено посредством взаимодействия лактамов формулы (IX) с основанием, таким как LDA, LiHMDS или NaHMDS в растворителе, таком как ТГФ при низкой температуре. Для конверсии соединений формулы (X) в соединения формулы (III), где А3 представляет собой NH необходимо пошаговое взаимодействие с пентахлоридом фосфора, ацетатом аммония и ацетатом меди (I). Производные формулы (III), где А3 представляет собой NH, могут быть присоединены к соединениям формулы (III), где А3 представляет собой N-R19 и R19 представляет собой алкил, циклоалкил и галоалкил, посредством взаимодействия с подходящим реагентом R19-X, где X представляет собой Br или I, в присутствии основания, такого как гидрид натрия. Аналогичным способом, соединения формулы (III), где А3 представляет собой N-R19 и R19 представляет собой алкилкарбонил, могут быть получены с помощью взаимодействия с подходящим ангидридом карбоновой кислоты в присутствии основания, такого как триэтиламин.
Альтернативно, к способам получения, описанным на схемах 4 и 5, нитрил промежуточные соединения формулы (II), где А3 представляет собой -CR17R18- могут быть получены, как показано на схеме 8.

Взаимодействие α,β-ненасыщенных эфиров нитрилов (XI) с кетонами формулы (VI) и ацетата аммония при повышенной температуре в воздушной атмосфере дает соединения формулы (XII). α,β-ненасыщенный эфиры нитрилов (XI) могут быть получены посредством конденсации Кневенагеля с использованием цианоацетатов и альдегидов (V). Обычные условия для такой трансформации включают взаимодействие обоих компонентов в спиртовом растворителе, таком как этанол или метанол при комнатной температуре или взаимодействие обоих компонентов в присутствии амина, такого как пиперидин, в толуоле в качестве растворителя при температуре кипения, возможно с удалением воды. Соединения формулы (XII) могут быть превращены в производные формулы (II) за две стадии. Взаимодействие соединений формулы (XII) с оксихлоридом фосфора дает пиридины формулы (XIII), где X представляет собой CI. Альтернативно, соединения формулы (XII) могут взаимодействовать с N-фенилбис(трифторметансульфонимидом) в присутствии основания, такого как гидрид натрия, с получением производных формулы (XIII), где X представляет собой OTf. Соединения формулы (XIII), где X представляет собой CI или OTf могут взаимодействовать со спиртами в присутствии основания, такого как гидрид натрия, с получением соединений формулы (II), где R1 представляет собой алкокси, галоалкокси, циклоалкокси или галоциклоалкокси. Соединения формулы (XIII), где X представляет собой Cl или OTf также могут взаимодействовать с аминами или амидами, возможно в присутствии основания, такого как триэтиламин, карбонат калия или гидрид натрия с получением соединений формулы (II), где R1 представляет собой гетероциклоалкил, замещенный гетероциклоалкил или замещенный амино.
Альтернативно, к способам получения, описанным на схемах 6 и 7, эфирные производные формулы (III), где А3 представляет собой -CR17R18- и R' представляет собой алкил, такой как метил, этил или трет-бутил, могут быть получены, как показано на схеме 9.

Пиридоновые производные формулы (XV) могут быть получены из α,β-ненасыщенных диэфиров (XIV) и кетонов формулы (VI) за 3 стадии. Аддукты реакции Михаэля, которые получили в результате взаимодействия производных енолатов, полученных из кетонов формулы (VI) и α,β-ненасыщенных диэфиров (XIV), могут быть циклизованы с ацетатом аммония при повышенной температуре. Финальное окисление с использованием окислительного агента, такого как FeCl3 в кипящей пропионовой кислоте дает пиридины формулы (XV). Соединения формулы (XV) могут быть превращены в производные формулы (III) за 2 стадии. Взаимодействие соединений формулы (XV) с оксихлоридом фосфора дает пиридины формулы (XVI), где X представляет собой Cl. Альтернативно, соединения формулы (XV) могут взаимодействовать с N-фенилбис трифторметансульфонимидом) в присутствии основания, такого как гидрид натрия, с получением производных формулы (XVI), где X представляет собой OTf. Соединения формулы (XVI), где X представляет собой Cl или OTf могут взаимодействовать со спиртами в присутствии основания, такого как гидрид натрия, с получением соединений формулы (III), где R1 представляет собой алкокси, галоалкокси, циклоалкокси или галоциклоалкокси. Соединения формулы (XVI), где X представляет собой Cl или OTf также могут взаимодействовать с аминами или амидами, возможно в присутствии основания, такого как триэтиламин, карбонат калия или гидрид натрия, с получением соединений формулы (III), где R1 представляет собой гетероциклоалкил, замещенный гетероциклоалкил или замещенный амино.
Промежуточные соединения нитрила формулы (II), где А3 представляет собой -CR17R18- и R2 представляет собой -NH2, могут быть получены, как показано на схеме 10.

Четырехкомпонентная реакция малононитрила (XVII) с подходящими альдегидами (V), циклическими кетонами формулы (VI) и ацетата аммония в инертном растворителе, таком как бензол, при повышенной температуре дает соединения формулы (II), где R2 представляет собой -NH2.
Альтернативно, к способам получения, описанным на схеме 8, промежуточные соединения формулы (XII), где А3 представляет собой -CR17R18- также могут быть получены, как показано на схеме 11.

α,β-ненасыщенный нитриламиды (XVIII) могут взаимодействовать с кетонами формулы (VI) в присутствии трет-бутоксида калия в полярном апротонном растворителе, таком как ДМСО, при комнатной температуре в воздушной или кислородной атмосфере (R. Jain et. al., Tetrahedron Lett. 1995, 36, 3307) с получением соединений формулы (XII).
Соединения формулы (I), где А3 представляет собой -CR17R18- и R2 представляет собой [1,3,4]-оксадиазол-2-он-ил или [1,3,4]-оксадиазол-2-тион-ил могут быть получены, как описано на схеме 12.

Производные формулы (XV) могут взаимодействовать с гидроксидом лития, натрия или калия в растворителе, таком как метанол или этанол при повышенных температурах с получением карбоновых кислот формулы (XIX). Для превращения соединений формулы (XIX) в производные формулы (XX), где PG представляет собой защитную группу, они могут взаимодействовать сначала с фенилфосфоновым дихлоридом и затем с подходяще защищенным гидразином. Если PG представляет собой 9-фторфенилметоксикарбонильную (Fmoc) группу и в качестве заместителей R1 вводят нециклические или циклические вторичные амины, отщепление защитной группы и нуклеофильное замещение могут быть проведены постадийно через соединения формулы (XXI) или за одну стадию с получением соединений формулы (XXII). Соединения формулы (XXII) могут взаимодействовать с N,N'-карбонилдиимидазолом или 1,1'-тиокарбонилдиимидазолом в присутствии основания, такого как триэтиламин, и в растворителе, таком как ТГФ с получением соединений формулы (I), где R2 представляет собой [1,3,4]-оксадиазол-2-он-ил или [1,3,4]-оксадиазол-2-тион-ил.
Соединения формулы (I), где А3 представляет собой -CR17R18- и R2 представляет собой -СООН также могут быть получены, как показано на схеме 13.

Взаимодействие производных формулы (XIX) с фенилфосфоновых дихлоридом при повышенной температуре дает дихлорпроизводные формулы (XXIII). Производные формулы (XXIV) могут быть получены посредством гидролиза хлорангидридного фрагмента соединения (XXIII) до карбоновой кислоты с помощью воды или ко-растворителя, такого как ТГФ, при комнатной температуре или повышенной температуре. Производные формулы (XXIV) могут взаимодействовать с аминами в присутствии порошка меди, бромида меди (I) и карбоната калия в растворителе, таком как ДМА, при повышенной температуре с получением соединений формулы (I), где R1 представляет собой гетероциклоалкил, замещенный гетероциклоалкил или замещенный амино.
Также воплощением настоящего изобретения является способ получения соединения формулы (I) как определено выше, содержащий взаимодействие соединения формулы (II) в присутствии соединения формулы (XXV), где М представляет собой натрий, триалкилолово, такое как триметилолово, или триалкилсилил, такой как триметилсилил, возможно в присутствии вспомогательных веществ, таких как соли цинка или оксид дибутилолова, в растворителе, таком как ДМФ, ксилен или диоксан, при повышенной температуре.

Также объектом настоящего изобретения является соединение согласно формуле (I), как здесь описано, для применения в качестве терапевтически активного вещества.
Более того, объектом настоящего изобретения является фармацевтическая композиция, содержащая соединение согласно формуле (I), как здесь описано, и терапевтически инертный носитель.
В соответствии с настоящим изобретением, соединения формулы (I) или их фармацевтически приемлемые соли или эфиры могут быть использованы для лечения или профилактики диабета 2 типа, метаболического синдрома, атеросклероза, дислипидемии, заболеваний печени, ожирения, липодистрофии, рака, глазных заболеваний, заболеваний легких, саркоидоза, хронических заболеваний почек, хронических воспалительных и аутоиммунных воспалительных заболеваний и синдрома поликистозных яичников.
Конкретными заболеваниями печения являются заболевания печени с участием воспаления, стеатоз и/или фиброз, такой как, неалкогольная жировая дистрофия печени, более конкретно неалкогольный стеатогепатит.
Конкретной липодистрофией являются наследственная и ятрогенная липодистрофия.
Конкретными заболеваниями глаз являются глазные заболевания на фоне эндотелиальной пролиферации и ангиогенеза, в частности макулярная дистрофия и ретинопатия.
Конкретными заболеваниями легких являются астма, бронхолегочная дисплазия и хроническая обструктивная болезнь легких.
Конкретными хроническими заболеваниями почек являются васкулит, фокальный сегментарный гломерулосклероз, диабетическая нефропатия, волчаночный нефрит, поликистоз почек и лекарственно или токсин-индуцированный хронический тубулоинтерстициальный нефрит.
Настоящее изобретение также относится к применению соединения согласно формулы (I), как здесь описано, для лечения или профилактики диабета 2 типа, метаболического синдрома, атеросклероза, дислипидемии, заболеваний печени, ожирения, липодистрофии, рака, глазных заболеваний, заболеваний легких, саркоидоза, хронических заболеваний почек, хронических воспалительных и аутоиммунных воспалительных заболеваний и синдрома поликистозных яичников.
В частности, настоящее изобретение относится к применению соединения согласно формуле (I), как здесь описано, для лечения или профилактики диабета 2 типа, атеросклероза, рака, хронического заболевания почек и неалкогольного стеатогепатита.
Настоящее изобретение также относится к применению соединения согласно формуле (I), как здесь описано, для лечения или профилактики неалкогольного стеатогепатита.
Частным воплощением настоящего изобретения является соединение согласно формуле (I), как здесь описано, для лечения или профилактики диабета 2 типа, метаболического синдрома, атеросклероза, дислипидемии, заболеваний печени, ожирения, липодистрофии, рака, глазных заболеваний, заболеваний легких, саркоидоза, хронических заболеваний почек, хронических воспалительных и аутоиммунных воспалительных заболеваний и синдрома поликистозных яичников.
Другим частным воплощением настоящего изобретения является соединение согласно формуле (I), как здесь описано, для лечения или профилактики диабета 2 типа, атеросклероза, рака, хронического заболевания почек и неалкогольного стеатогепатита.
Также частным воплощением настоящего изобретения является соединение согласно формуле (I), как здесь описано для лечения или профилактики неалкогольного стеатогепатита.
Настоящее изобретение также относится к применению соединения согласно формуле (I), как здесь описано, для получения лекарственного средства для лечения или профилактики диабета 2 типа, метаболического синдрома, атеросклероза, дислипидемии, заболеваний печени, ожирения, липодистрофии, рака, глазных заболеваний, заболеваний легких, саркоидоза, хронических заболеваний почек, хронических воспалительных и аутоиммунных воспалительных заболеваний и синдрома поликистозных яичников.
Настоящее изобретение, в частности, относится к применению соединения согласно формуле (I), как здесь описано, для получения лекарственного средства для лечения или профилактики диабета 2 типа, атеросклероза, рака, хронического заболевания почек и неалкогольного стеатогепатита.
Также воплощением настоящего изобретения является применение соединения согласно формуле (I), как здесь описано, для получения лекарственного средства для лечения или профилактики неалкогольного стеатогепатита.
Также объектом настоящего изобретения является способ для лечения или профилактики диабета 2 типа, метаболического синдрома, атеросклероза, дислипидемии, заболеваний печени, ожирения, липодистрофии, рака, глазных заболеваний, заболеваний легких, саркоидоза, хронических заболеваний почек, хронических воспалительных и аутоиммунных воспалительных заболеваний и синдрома поликистозных яичников, который включает введение эффективного количества соединения согласно формуле (I), как здесь описано.
Другим объектом настоящего изобретения является способ лечения или профилактики диабета 2 типа, атеросклероза, рака, хронического заболевания почек и неалкогольного стеатогепатита, который включает введение эффективного количества соединения согласно формуле (I), как здесь описано.
Также воплощением настоящего изобретения является способ лечения или профилактики неалкогольного стеатогепатита, который включает введение эффективного количества соединения согласно формуле (I), как здесь описано.
Также воплощением настоящего изобретения является способ лечения или профилактики липодистрофии, который включает введение эффективного количества соединения согласно формуле (I), как здесь описано.
Также частным воплощением настоящего изобретения является соединение согласно формуле (I), как здесь описано, которое получено согласно любому описанному способу.
Способы анализа
Соединения исследовали на активность против FABP4 человека (чFABP4) и/или FABP5 человека (чFABP5) в анализе переноса энергии флуоресценции с разрешением во времени (TR-FRET) с использованием тербия (Tb), контролирующем прямое связывание меченой жирной кислоты Bodipy с мечеными His6 белками FABP (чFABP4 естественно экспрессировался в Е.coli и очищался, чFABP5 покупали в компании Cayman Chemical Co., каталожный №10010364), связанным с меченым тербием антителом против метки His6. Анализ считывает перенос отраженной энергии, после связывания лиганда с белком FABP, из донорной молекулы тербия на акцепторный остаток Bodipy. Конечная концентрация лиганда (125 нМ) аппроксимировала Kd для каждого белка.
Стоковые ДМСО растворы (1.8 мМ) соединений серийно трехкратно разводились для десяти концентраций со 100% ДМСО (50 мкМ до 0.003 мкМ конечных концентраций соединения). 1 мкл этих разведений соединений и 1 мкл меченых жирных кислот Bodipy 4.5 мкМ в 100% ДМСО (Bodipy FL С11, каталожный № D3862, Invitrogen) последовательно разлили в лунки 384-луночных черных полипропиленовых планшетов (Thermo Matrix каталожный №4344). Затем добавили белок FABP4 или FABP5 (28 мкл 64 нМ белка в 25 мМ Tris рН 7.5, 0.4 мг/мл γ-глобулин, 1 мМ DTT, 0.012% NP40, конечная концентрация белка: 50 нМ). Анализ очистил содержащийся лиганд, но не белок. Нейтральный контроль содержал лиганд, но не соединение. После добавления реагента для детекции (Tb антиHis6 антитело, Columbia Biosciences, ТВ-110, 6 мкл 24 нМ раствора антитела в 25 мМ Tris рН 7.5, 0.4 мг/мл γ-глобулин, конечная концентрация Tb антиHis6 антитела: 4 нМ), планшеты центрифугировали одну минуту при 1000 об/мин. В течение инкубирования при комнатной температуре со встряхиванием в течение 30 минут, планшеты считывались с использованием ридера Envision (Perkin Elmer, длина волны экстинции: 340 нм, эмиссии: 490 нм и 520 нм, временная задержка: 100 мкс; временной интервал: 200 мкс, 50 вспышек).
Конечные условия анализа представляли собой: 50 нМ белкаРАВР, 125 нМ меченой жирной кислоты Bodipy, 0.009% (об/об) NP40, 5.5% (об/об) ДМСО в общем конечном анализируемом объеме 36 мкл. Анализ проводился в трех повторах.
Отношение относительных единиц флуоресценции (RFU) (520 нм * 10000/488 нм) использовалось для расчета процента ингибирования: 100 - (RFU отношение соединение - чистая) / нейтральный контроль - чистая) * 100. Эти значения процента ингибирования затем аппроксимировались на кривые доза-ответ с использованием 4-х параметрической логистической модели (сигмоидальная модель Хилла доза-ответ). Значения IC50, отражающие концентрации соединений, связанные с 50% ингибированием активности белка, сравнивались с аналогичными значениями нейтральных контролей.






Соединения формулы (I) и их фармацевтически приемлемые соли или эфиры, как здесь описано, обладают значениями IC50 (ингибирование FABP4) между 0.000001 мкМ и 1000 мкМ, конкретные соединения обладают значениями IC50 между 0.000005 мкМ и 500 мкМ, дополнительные конкретные соединения обладают значениями IC50 между 0.00005 мкМ и 5 мкМ.
Соединения формулы (I) и их фармацевтически приемлемые соли или эфиры, как здесь описано, обладают значениями IC50 (ингибирование FABP5) между 0.000001 мкМ и 1000 мкМ, конкретные соединения обладают значениями IC50 между 0.000005 мкМ и 500 мкМ, дополнительные конкретные соединения обладают значениями IC50 между 0.00005 мкМ и 50 мкМ.
Соединения формулы I, а также их фармацевтически приемлемые соли могут применяться в качестве лекарственных средств (например, в форме фармацевтических препаратов). Фармацевтические препараты могут вводится внутрь, включая перорально (например, в форме таблеток, покрытых оболочкой таблеток, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий), назально (например, в форме назальных аэрозолей) и ректально (например, в форме суппозиториев). Кроме того, введение может осуществляться парентерально, включая внутримышечно и внутривенно (например, в виде растворов для инъекций).
Соединения формулы I и их фармацевтически приемлемые соли могут перерабатываться вместе с фармацевтически инертными, неорганическими или органическими эксципиентами для производства таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. Лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.д. могут применяться в качестве таких эксципиентов, например, для таблеток, драже и твердых желатиновых капсул.
Подходящими адъювантами для мягких желатиновых капсул являются, например, растительные масла, воска, жиры, полутвердые и жидкие полиолы и т.д.
Подходящими адъювантами для изготовления растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.д.
Подходящими адъювантами для инъекционных растворов являются, например, вода, спирты, полиолы, глицерин, растительные масла и т.д.
Подходящими адъювантами для суппозиториев являются, например, природные или гидрогенизированные масла, воска, жиры, полужидкие или жидкие полиолы и т.д.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульгаторы, подсластители, красители, ароматизаторы, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они могут также содержать другие терапевтически ценные вещества.
Дозировка может варьироваться в широких пределах и, конечно, будет подобрана к индивидуальным требованиям в каждом конкретном случае. В общем, в случае перорального введения должна быть подходящей суточная доза от около 0,1 мг до 20 мг на кг массы тела, предпочтительно от около 0,5 мг до 4 мг на кг массы тела (например, приблизительно 300 мг на человека), предпочтительно разделить на 1-3 индивидуальных доз, которые могут состоять, например, из одинакового количества. Однако, будет понятно, что указанный здесь верхний предел может быть превышен когда это необходимо.
В соответствии с настоящим изобретением, соединения формулы (I) или их фармацевтически приемлемые соли или эфиры могут применяться для лечения или профилактики связанных с диабетом 2 типа микрососудистых осложнений (таких как, без ограничения, диабетическая ретинопатия, диабетическая нейропатия и диабетическая нефропатия), ишемической болезни сердца, ожирения и лежащих в основе воспалительных заболеваний, хронических воспалительных и аутоиммунных/воспалительных заболеваний.
Настоящее изобретение далее иллюстрируется Примерами, которые не имеют ограничивающего характера.
В случае, если препаративные примеры получают в виде смеси энантиомеров, чистые энантиомеры могут быть разделены с помощью описанных здесь способов или с помощью способов, известных специалисту в данной области, таких как, например, хиральная хроматография или кристаллизация
Примеры
Все примеры и промежуточные соединения получили в атмосфере аргона если специально не указано иного.
Общий Способ А: Смесь эфира (промежуточное соединение Е) (0.129 ммоль, 1 экв) и йодида лития (10 экв) в пиридине (3 мл) нагревали до 135°С в течение 1-4 дней. Затем пиридин удалили, оставшийся остаток разбавили водой и довели рН до 2-3 посредством добавления 0.1 н HCl. Смесь экстрагировали этилацетатом и объединенные экстракты промыли водой (подкисленной до рН 2-3 с помощью 0.1 н HCl) и солевым раствором, высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии.
Общий Способ В: В раствор эфира (промежуточное соединение Е) (0.1 ммоль, 1 экв) в ДМСО (3 мл) и воде (0.1 мл) добавили NaOH (2 экв) и смесь нагревали до 100°С в закрытой пробирке в течение 1-4 дней. При необходимости, дополнительное количество NaOH (1 экв) и воды (0.15 мл) добавили в течение этого времени. Реакционную смесь затем разбавили водой и рН довели до 2-3 посредством добавления 0.1 н HCl. Смесь экстрагировали этилацетатом и объединенные экстракты промыли водой (подкисленной до рН 2-3 с помощью 0.1 н HCl), высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии.
Общий Способ С: Раствор нитрила (промежуточное соединение N) (0.336 ммоль, 1 экв) и азидотриметилстаннана (3 экв) в ксилене (3.5 мл) нагревали до 120°С в течение 1-7 дней. Преципитат, который образовался, отфильтровали, промыли горячим толуолом и суспендировали в смеси этилацетата и 0.1 н HCl. Суспензию интенсивно перемешали при комнатной температуре до растворения осадков. Слои разделили и водный слой экстрагировали этилацетатом. Объединенные органические слои промыли водой и солевым раствором (оба подкисленные до рН 1 с помощью HCl), высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии.
Если в течение периода нагревания не образовывалось преципитата, реакционную смесь охладили до комнатной температуры и добавили этилацетат и 0.1 н HCl. Смесь перемешивали в течение 1.5 ч, слои разделили и водный слой экстрагировали этилацетатом. Объединенные органические слои промыли водой и солевым раствором (оба подкисленные до рН 1 с помощью HCl), высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии.
Общий Способ D: Смесь нитрила (промежуточное соединение N) (2.5 ммоль, 1 экв), азида натрия (2.2 экв) и хлорида цинка (0.5 экв) в ДМФ (5 мл) кипятили с обратным холодильником в течение 3 дней. После эвапорации растворителя остаток перемешивали с EtOAc/водой. Преципитат отфильтровали, перемешивали с 1 н HCl/водой и отфильтровали. Получившийся осадок тритурировали этанолом и очистили посредством колоночной хроматографии.

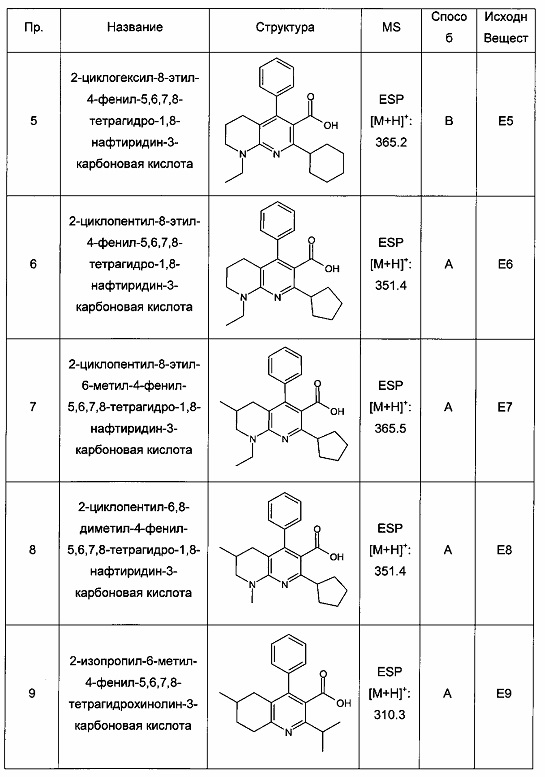

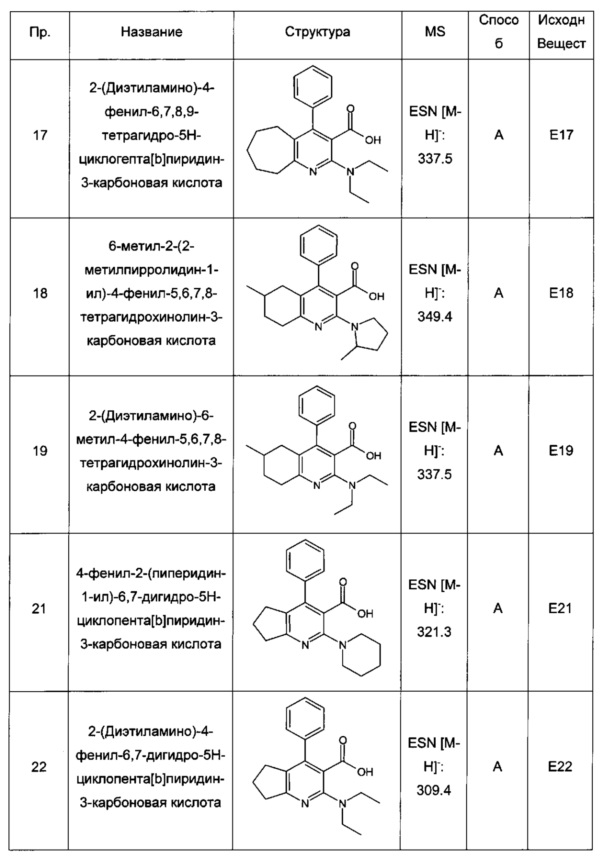
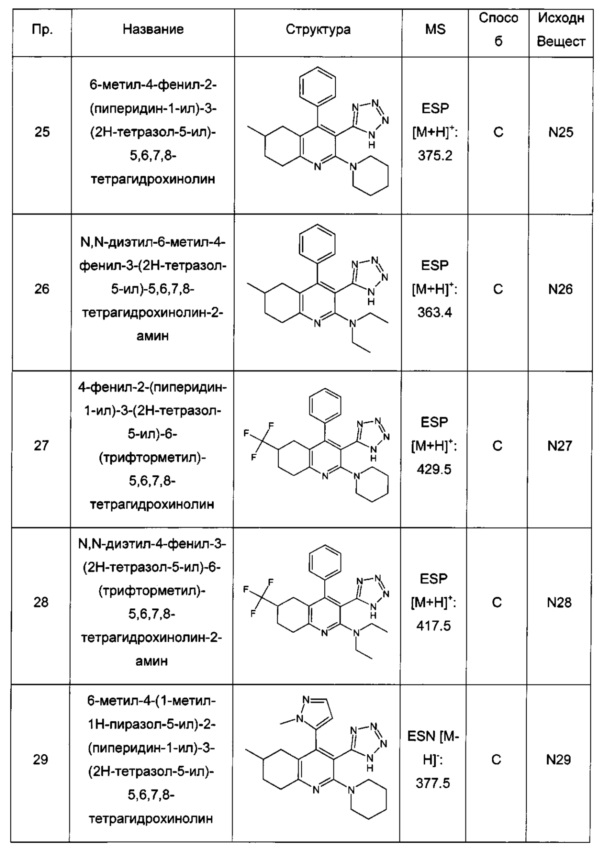






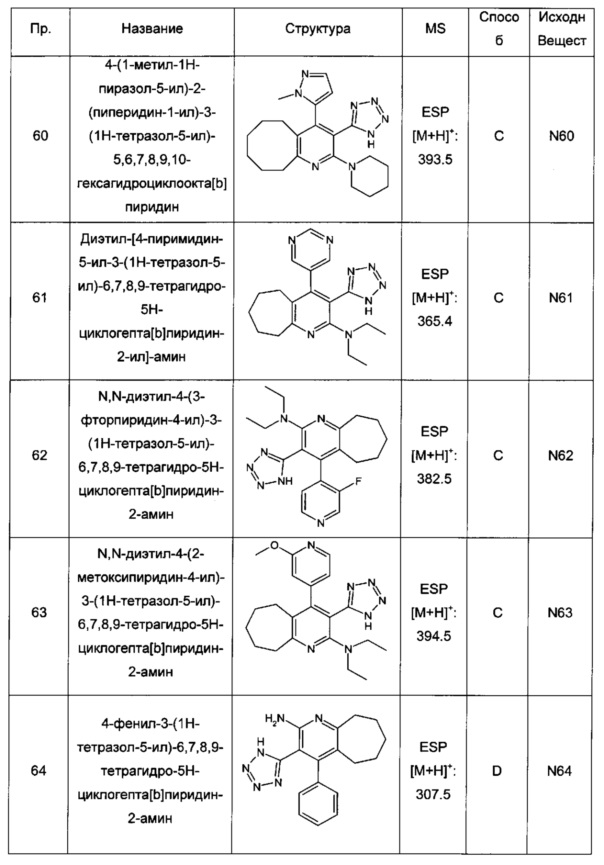

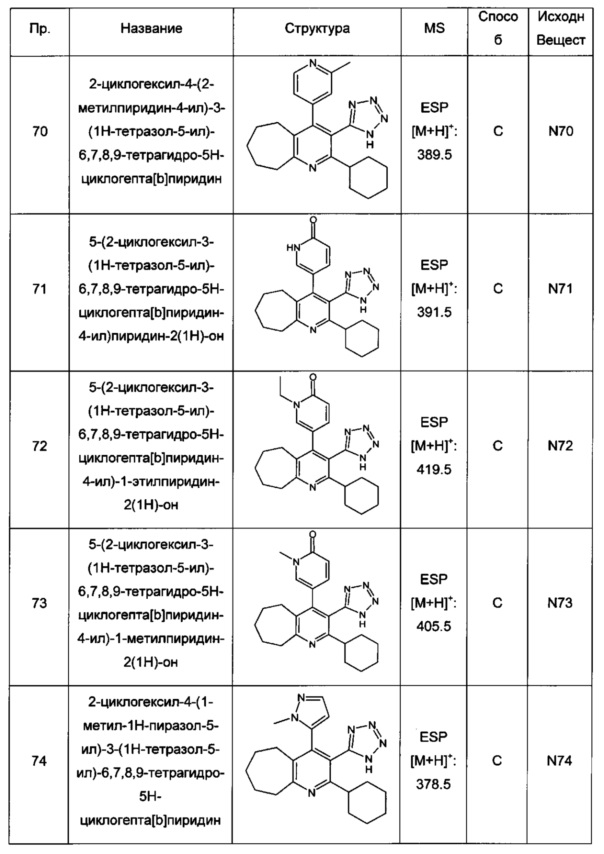
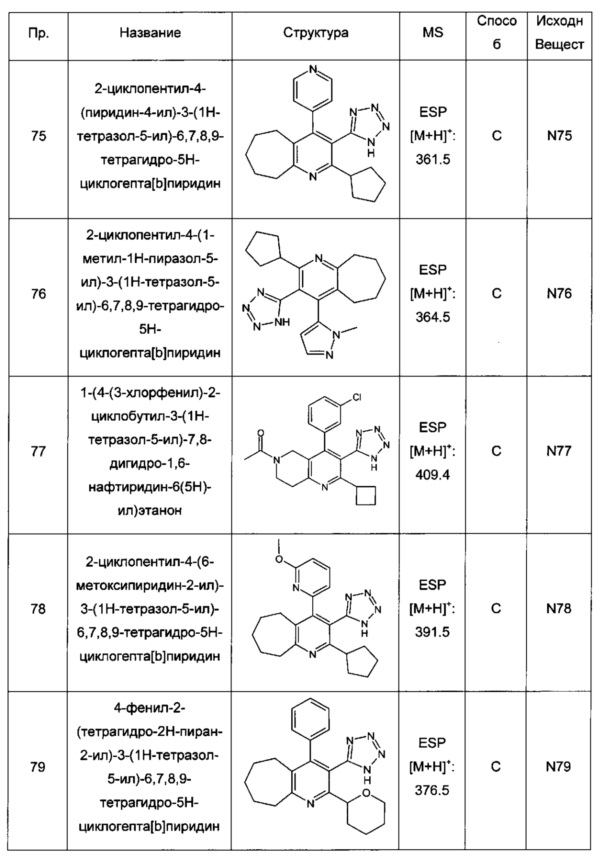










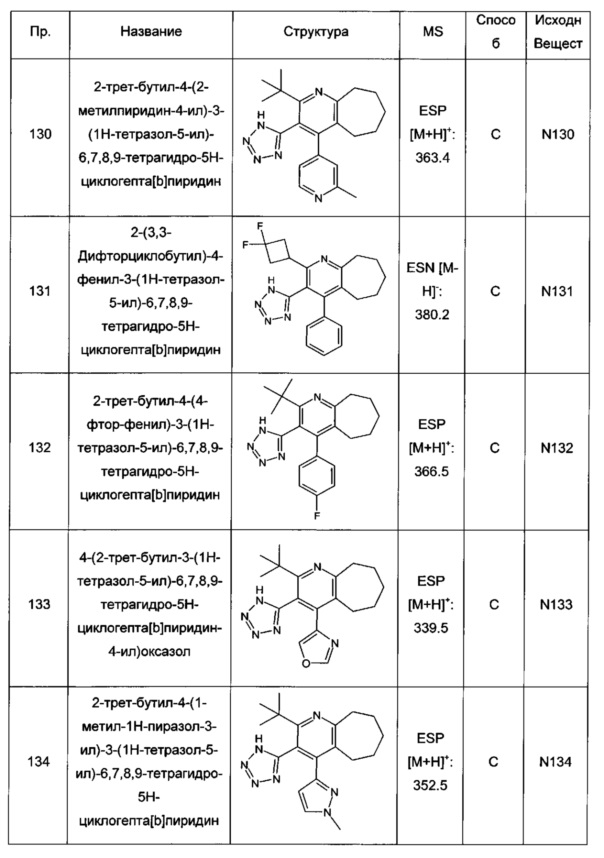

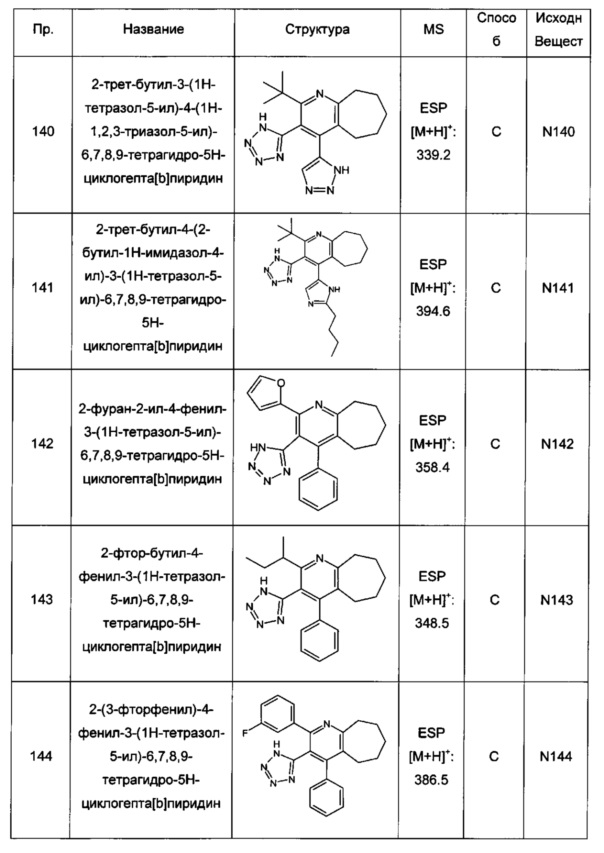
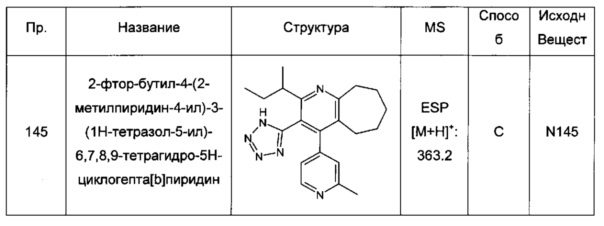
Пример 12
2-циклопентил-4-(6-метоксипиридин-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота

Промежуточное соединение N78 (471 мг) и водную HCl 37% (2.67 г) объединили с диоксаном (20.0 мл) и перемешивали при 100°С в течение 1 ч. После охлаждения до комнатной температуры, смесь разбавили водой и экстрагировали EtOAc. Органические слои высушили над MgSO4 и сконцентрировали под вакуумом. Неочищенное вещество очистили посредством колоночной хроматографии (градиент ДХМ/МеОН 100:0=>80:20) с получением соединения, указанного в заголовке (47 мг), в виде бесцветного аморфного осадка. MS (ESN): m/z=365.4 [М-Н]-.
Пример 13
2-циклопентил-4-(6-оксо-1,6-дигидропиридин-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота
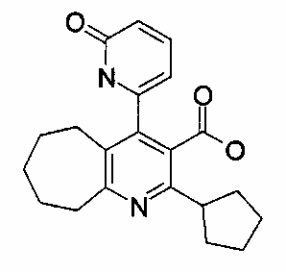
При синтезе примера 12, также получили соединение, указанное в заголовке (114 мг), в виде светло-желтого осадка. MS (ESP): m/z=353.4 [М+Н]+.
Пример 20
4-(3-хлорфенил)-6-метил-2-(пирролидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота

Стадия 1: 4-(3-хлорфенил)-6-метил-2-оксо-1,2,5,6,7,8-гексагидрохинолин-3-карбоновая кислота

Раствор гидроксида лития (104 мг) в воде (4.0 мл) добавили при комнатной температуре в раствор Промежуточного соединения Р20 (500 мг) в EtOH (9.3 мл) и ТГФ (2.7 мл). После добавления, раствор перемешивали при 90°С в течение 4 ч. Органические растворители удалили под вакуумом, остаток разбавили 15 мл водной 1 М NaOH и экстрагировали дихлорметаном. Водный слой подкислили водной 1 М HCl до рН1 и экстрагировали с помощью ДХМ и EtOAc. Объединенные органические слои высушили над MgSO4 и сконцентрировали под вакуумом с получением соединения, указанного в заголовке (452 мг), в виде серо-белого осадка. MS (ESP): m/z=318.1 [М+Н]+.
Стадия 2: 2-хлор-4-(3-хлор-фенил)-6-метил-5,6,7,8-тетрагидро-хинолин-3-карбонил хлорид

Суспензию продукта стадии 1 (440 мг) в фенилфосфоновом дихлориде (863 мг) перемешивали при 135°С в течение 3 ч. После охлаждения до комнатной температуры, смесь разбавили водой (10 мл) и экстрагировали с помощью ДХМ. Органические слои высушили над MgSO4 и сконцентрировали под вакуумом. Неочищенное вещество очистили посредством колоночной хроматографии (градиент ДХМ/МеОН 100:0=>90:10) с получением соединения, указанного в заголовке (271 мг), в виде серо-белого осадка. MS (ESP): m/z=356.0 [М+Н]+.
Стадия 3: 2-хлор-4-(3-хлорфенил)-6-метил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота
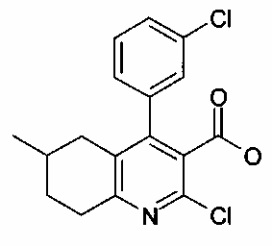
Раствор продукта стадии 2 (138 мг) в ТГФ (1 мл) и воде (1.00 мл) перемешивали в течение 6 дней при комнатной температуре, в течение 5 ч при 50°С и в течение 11 ч при 60°С. Реакционную смесь влили в воду (10 мл)/водную 1 М NaOH (1 мл) и экстрагировали диэтиловым эфиром.
Водный слой подкислили до рН 1 с помощью водной 2 М HCl и снова экстрагировали EtOAc. Органические слои (EtOAc) объединили, высушили над MgSO4 и сконцентрировали под вакуумом с получением соединения, указанного в заголовке (114 мг), в виде серо-белого осадка. MS (ESN): m/z=336.1 [М-Н]-.
Стадия 4: 4-(3-хлорфенил)-6-метил-2-(пирролидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота
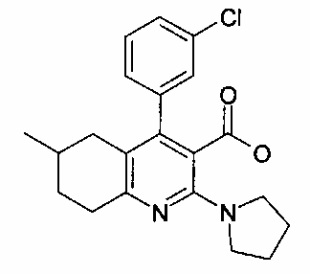
Суспензию продукта стадии 3 (50 мг), карбоната калия (24.7 мг), порошка меди (0.56 мг), бромида меди (I) (1.1 мг) и пирролидина (18.0 мг) в ДМА (0.2 мл) перемешивали при 150°С в течение 4 ч. Реакционной смеси дали остыть до комнатной температуры в течение ночи. Реакционную смесь влили в EtOAc (10 мл) и воду (10 мл) и подкислили до рН 3 с помощью насыщенного водного раствора лимонной кислоты. Смесь экстрагировали EtOAc.Органические слои объединили, высушили над MgSO4 и сконцентрировали под вакуумом. Неочищенное вещество очистили посредством препаративной ТСХ (силикагель, 2.0 мм, ДХМ/МеОН 9:1) с получением соединения, указанного в заголовке (14 мг), в виде серо-белого осадка. MS (ESN): m/z=369.1 [М-Н]-.
Пример 23
4-(3-хлорфенил)-6-метил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота
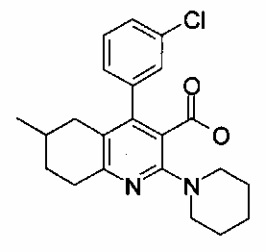
По аналогии с примером 20, Стадия 4, 2-хлор-4-(3-хлорфенил)-6-метил-5,6,7,8-тетрагидрохинолин-3-карбоновую кислоту (Пример 20, стадия 3) конвертировали в соединение, указанное в заголовке посредством взаимодействия с пиперидином в присутствии карбоната калия, порошка меди, бромида меди (I) и ДМА. Серо-белый осадок. MS (ESN): m/z=383.4 [М-Н]-.
Пример 24
5-(6-метил-4-фенил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-ил)-1,3,4-оксадиазол-2(3Н)-тион

Стадия 1: 6-метил-2-оксо-4-фенил-1,2,5,6,7,8-гексагидро-хинолин-3-карбоновая кислота
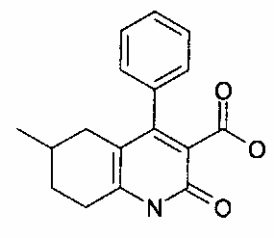
К раствору промежуточного соединения Р16 (660 мг, 2.12 ммоль) в смеси растворителей EtOH (6.6 мл), ТГФ (2.64 мл) и воды (6.6 мл) добавили гидроксид лития (152 мг, 6.36 ммоль) и реакционную смесь нагревали до кипения с обратным холодильником в течение 2 дней. Органические растворители удалили и рН оставшегося водного слоя довели до 14. Водный слой промыли 3 раза диэтиловым эфиром, затем подкислили до рН1 с помощью 1 н HCl и экстрагировали этилацетатом. Объединенные этилацетатные соли промыли водой и солевым раствором, высушили (Na2SO4) и эвапорировали с получением соединения, указанного в заголовке, в виде белого осадка (550 мг). MS (ESP): m/z=284.2 [М+Н]+.
Стадия 2: N'-(2-хлор-6-метил-4-фенил-5,6,7,8-тетрагидро-хинолин-3-карбонил)-гидразинкарбоновой кислоты 9Н-флуорен-9-илметиловый эфир

Смесь 6-метил-2-оксо-4-фенил-1,2,5,6,7,8-гексагидро-хинолин-3-карбоновой кислоты (170 мг, 600 мкмоль) и фенилфосфонового дихлорида (351 мг, 253 мкл, 1.8 ммоль) нагрели до 135°С в атмосфере аргона в течение 6 ч. Реакционную смесь затем сконцентрировали и оставшийся остаток очистили посредством колоночной хроматографии на силикагеле (50 г силикагель, ДХМ). Фракции, содержащие требуемое 2-хлор-6-метил-4-фенил-5,6,7,8-тетрагидро-хинолин-3-карбонил хлоридное промежуточное соединение объединили, эвапорировали и растворили в ДХМ (4 мл). (9Н-Флуорен-9-ил)метил гидразинкарбоксилат (183 мг, 720 мкмоль) добавили и реакционную смесь перемешивали при комнатной температуре в течение 20 ч. Добавили воду и смесь экстрагировали этилацетатом. Объединенные экстракты промыли водой и солевым раствором, высушили (Na2SO4) и эвапорировали с получением соединения, указанного в заголовке (308 мг), в виде белого осадка. MS (ESP): m/z=538.4 [М+Н]+.
Стадия 3: 2-хлор-6-метил-4-фенил-5,6,7,8-тетрагидро-хинолин-3-карбоновой кислоты гидразид

К раствору N'-(2-хлор-6-метил-4-фенил-5,6,7,8-тетрагидро-хинолин-3-карбонил)-гидразинкарбоновой кислоты 9Н-флуорен-9-илметилового эфира (170 мг, 253 мкмоль) в ДМФ (2.25 мл) добавили пиперидин (215 мг, 250 мкл, 2.53 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 ч. Воду добавили и смесь экстрагировали этилацетатом. Объединенные экстракты were промыли водой и солевым раствором, высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии на силикагеле (20 г силикагель, ДХМ/EtOAc 1:1) с получением соединения, указанного в заголовке (71 мг), в виде светло-желтого осадка. MS (ESP): m/z=316.2 [М+Н]+.
Стадия 4: 6-метил-4-фенил-2-пиперидин-1-ил-5,6,7,8-тетрагидро-хинолин-3-карбоновой кислоты гидразид

2-хлор-6-метил-4-фенил-5,6,7,8-тетрагидро-хинолин-3-карбоновой кислоты гидразид (70 мг, 222 мкмоль), пиперидин (189 мг, 219 мкл, 2.22 ммоль) и триэтиламин (67.3 мг, 92.7 мкл, 665 мкмоль) растворили в ДМФ (1 мл) и реакционную смесь нагрели до 120°С в течение 24 ч. Добавили воду и смесь экстрагировали EtOAc. Объединенные экстракты промыли солевым раствором, высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии на силикагеле (10 г силикагель, ДХМ/EtOAc 2:1) с получением соединения, указанного в заголовке (45 мг), в виде белого осадка. MS (ESP): m/z=365.3 [М+Н]+.
Стадия 5: 5-(6-метил-4-фенил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-ил)-1,3,4-оксадиазол-2(3Н)-тион
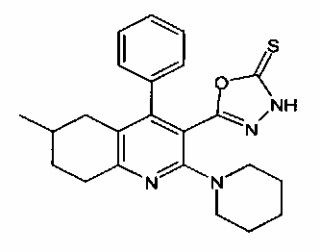
6-метил-4-фенил-2-пиперидин-1-ил-5,6,7,8-тетрагидро-хинолин-3-карбоновой кислоты гидразид (43 мг, 94.4 мкмоль) и 1,1'-тиокарбонилдиимидазол (23.5 мг, 132 мкмоль) растворили в ТГФ (1.1 мл). Затем добавили триэтиламин (15.3 мг, 21.0 мкл, 151 мкмоль) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Воду добавили и смесь экстрагировали этилацетатом. Объединенные экстракты промыли водой и солевым раствором, высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии на силикагеле (5 г силикагель, ДХМ/метанол 95:5). Фракции, содержащие требуемое 6-метил-4-фенил-2-пиперидин-1-ил-5,6,7,8-тетрагидро-хинолин-3-карбоновой кислоты N'-(имидазол-1-карботиоил)-гидразидное промежуточное соединение объединили, эвапорировали и растворили в ТГФ (1.1 мл). Триэтиламин (15.3 мг, 21.0 мкл, 151 мкмоль) добавили и реакционную смесь нагревали в закрытой пробирке до 50°С в течение 4 дней. Воду добавили и смесь экстрагировали этилацетатом. Объединенные экстракты промыли солевым раствором, высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии на силикагеле (5 г силикагель, ДХМ/этилацетат 9:1) с получением соединения, указанного в заголовке (13 мг), в виде белого осадка. MS (ESN): m/z=405.4 [М-Н]-.
Примеры 37 и 43
4-(1-метил-1Н-пиразол-5-ил)-2-(2-метил пиррол идин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин (диастереомерные рацематы)
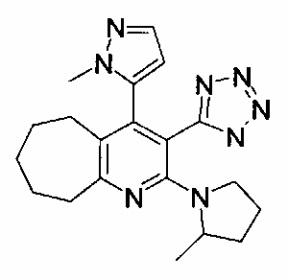
Используя Общий Способ С, Промежуточное соединение N37 конвертировали в тетразол. Два диастереомерных рацемата (в результате атропизомерии) могут быть разделены с помощью препаративной ВЭЖХ (обратно-фазовая хроматография, колонка: Gemini Axia С18 5u 110A 5 микрон 100×30 мм, Растворитель А: вода + 0.01% муравьиная кислота, Растворитель В: ацетонитрил, Способ: градиент 30% - 95% В).
Элюируемый первым изомер (Пример 37): Серо-белый аморфный осадок. MS (ESP): m/z=379.2 [М+Н]+.
Элюируемый вторым изомер (Пример 43): Бесцветный аморфный осадок. MS (ESP): m/z=379.2 [М+Н]+.
Синтез промежуточных соединений
Промежуточное соединение В79
3-оксо-3-(тетрагидро-2Н-пиран-2-ил)пропанонитрил

К суспензии гидрида натрия (55% в минеральном масле, 969 мг) в ТГФ (4.79 мл) добавили при 70°С по каплям раствор метил тетрагидро-2Н-пиран-2-карбоксилата (3 г) и ацетонитрила (994 мг) в ТГФ (1.96 мл). Смесь нагрели до 75°С и перемешивали в течение 2 ч. EtOAc добавили и подкислили с помощью 1 М HCl при перемешивании (экзотермичная). Смесь экстрагировали EtOAc. Органические слои высушили над MgSO4 и сконцентрировали под вакуумом. Неочищенное вещество очистили посредством колоночной хроматографии (градиент н-гептан/EtOAc 1:0=>2:3) с получением соединения, указанного в заголовке (2.42 г), в виде светло-коричневой жидкости. MS (ESP): m/z=152.2 [М+Н]+.
Промежуточное соединение В94
3-(1-(Метоксиметил)циклопентил)-3-оксопропанонитрил

По аналогии с синтезом Промежуточного Соединения В79, метил 1-(метоксиметил)циклопентанкарбоксилат (CAS# 220875-97-8) конвертировали в соединение, указанное в заголовке посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Светло-желтая жидкость. MS (ESN): m/z=180.2 [М-Н]-.
Промежуточные соединения К (посредством конденсации Кневенагеля)
Общий Способ Е: Раствор бета-кетоэфира или бета-кетонитрила или диалкилмалоната (3.5 ммоль, 1 экв), альдегида (1.1 экв), пиперидина (0.15 экв) и уксусной кислоты (0.15 экв) в 2-пропаноле (10 мл) перемешивали при комнатной температуре в течение ночи. Большинство 2-пропанола удалили посредством эвапорации. Смесь разбавили Na2S2O5 (20% г/г раствор) и экстрагировали с помощью ДХМ. Органические слои промыли Na2S2O5 (20% г/г раствор), насыщенным водным раствором NaHCO3 и водой, высушили над Na2SO4 и эвапорировали. Продукты получили в виде цис/транс смесей и использовали на следующей стадии без дополнительной очистки.
Общий Способ F: Раствор альдегида (4.5 ммоль, 1 экв), бета-кетоэфира или бета-кетонитрила или диалкилмалоната или метилцианоацетата (1.1 экв) и пиперидина (0.02 экв) в толуоле (8.4 мл) нагревали до кипения с использованием насадки Дина-Старка в течение 1-2 ч. Реакционную смесь сконцентрировали и продукт можно очистить посредством кристаллизации или хроматографии или он может быть использован на следующей стадии без дополнительной очистки.
Общий Способ G: К суспензии 2-цианоацетамида (1.1 экв) в метаноле (10 мл) и воде (3 мл) добавили альдегид (40 ммоль, 1 экв) и пиперидин (0.2 экв). Смесь перемешивали в течение 1-2 ч. 1М HCl (9 мл) и воду (10 мл) добавили. Преципитат собрали посредством фильтрации, промыли водой и этилацетатом и высушили. Продукт может быть далее очищен посредством кристаллизации или может быть использован на следующей стадии без дополнительной очистки.
Общий Способ Н: Альдегид (7.75 ммоль, 1 экв), метилцианоацетат или бета-кетонитрил (1 экв) и метанол (5.3 мл) объединили и перемешивали в течение 1-4 дней. Если продукт преципитировался, его можно собрать посредством фильтрации. Если продукт не преципитировался, он может быть очищен посредством эвапорации растворителя и кристаллизации или хроматографии или может быть использован на следующей стадии без дополнительной очистки.
Общий Способ I: Альдегид (4.4 ммоль, 1 экв), бета-кетонитрил (1 экв) и L-пролин (0.2 экв) объединили с этанолом или метанолом (6.5 мл) и перемешивали в течение 1-4 дней. Если продукт преципитировался, его можно собрать посредством фильтрации. Если продукт не преципитировался, он может быть очищен посредством эвапорации растворителя и кристаллизации или хроматографии или может быть использован на следующей стадии без дополнительной очистки.

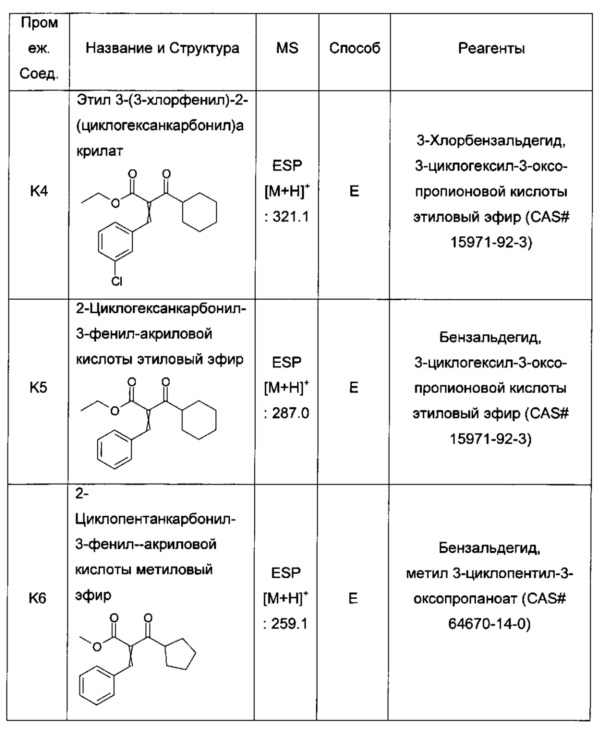












Промежуточное соединение L
5-метил-2-оксо-пиперидин-1-карбоновой кислоты трет-бутиловый эфир
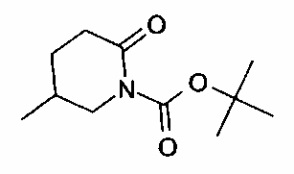
Триэтиламин (447 мг, 616 мкл, 4.42 ммоль), 4-диметиламинопиридин (54.0 мг, 0.442 ммоль) и ди-трет-бутил-дикарбонат (1.45 г, 6.63 ммоль) добавили в раствор 5-метилпиперидин-2-она (CAS# 3298-16-6) (500 мг, 4.42 ммоль) в безводном ДХМ (10 мл) при комнатной температуре и раствор перемешивали в течение 5 ч. Все летучие компоненты удалили и оставшееся масло очистили посредством колоночной хроматографии на силикагеле (50 г силикагель, н-гексан/диэтиловый эфир 1:3) с получением соединения, указанного в заголовке (717 мг), в виде желтого масла. MS (ESP): m/z=214.2 [М+Н]+.
Общий Способ М: Лития бис(триметилсилил)амид (1М раствор в ТГФ, 1.1 экв) добавили к раствору N-защищенного лактама (1 экв) в ТГФ (1 мл/ммоль) при -30°С и смесь перемешивали в течение 25 минут. Смесь затем перенесли в предварительно охлажденный раствор (-20°С) продуктов конденсации Кневенагеля бета-кетоэфиров и альдегидов (1 экв) в безводном ТГФ (1.5 мл/ммоль) и реакционную смесь перемешивали при -20°С в течение 1.5 ч. Затем насыщенный раствор NH4Cl добавили и смесь экстрагировали этилацетатом. Объединенные экстракты высушили (Na2SO4) и эвапорировали. Оставшийся остаток растворили в 1,2-дихлорэтане (4 мл/ммоль), добавили пентахлорид фосфора (1.2 экв) и реакционную смесь нагревали до 65°С в течение 2.5 ч. После охлаждения до 0°С, добавили аммоний в метаноле (2М раствор, 6 экв) и преципитировавшийся осадок отфильтровали. Фильтрат сконцентрировали, добавили метанол (5 мл/ммоль) и ацетат аммония (4 экв) и смесь нагревали до 60°С в течение 4 ч. Затем добавили ацетат меди (I) (1.05 экв) и реакционную смесь нагревали до кипения с обратным холодильником в течение ночи, охладили до комнатной температуры и отфильтровали. Фильтрат сконцентрировали, добавили раствор Na2CO3 (рН 10) и смесь экстрагировали этилацетатом. Объединенные экстракты промыли раствором Na2CO3 (рН 10), высушили (Na2SO4) и эвапорировали и оставшийся остаток очистили посредством колоночной хроматографии.



Общий Способ N: В раствор промежуточного соединения (АР) (1 экв) в безводном ДМФ (7 мл/ммоль) осторожно добавили гидрид натрия (55% в минеральном масле, 1.1 экв) при 0°С и получившуюся смесь перемешивали в течение 45 минут. Затем добавили раствор алкилйодида (1.1 экв) в безводном ДМФ (6 мл/ммоль), смеси дали нагреться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь затем осторожно разбавили водой и довели рН до 10 посредством добавления насыщенного раствора Na2CO3. Смесь экстрагировали этилацетатом и объединенные органические слои промыли раствором Na2CO3 (рН 10), высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии на силикагеле.
Общий Способ О: Смесь промежуточного соединения (АР) (1 экв), триэтиламина (3 экв) и ангидрида карбоновой кислоты (2 экв) в безводном ДХМ (9 мл/ммоль) перемешивали в закрытой пробирке при 50°С в течение 2 дней. Растворитель удалили и оставшийся остаток очистили посредством колоночной хроматографии на силикагеле.
Общий Способ Р: Раствор циклического кетона (0.85 экв) в ТГФ (0.3 мл/ммоль) добавили по каплям в раствор NaHMDS (1М раствор в ТГФ, 1 экв) в ТГФ (0.5 мл/ммоль) при -78°С. Смеси дали нагреться до 0°С и поддерживали при жтой температуре в течение 15 минут перед тем, как ее снова охладили до -78°С. Быстро добавили предварительно охлажденный раствор продуктов конденсации Кневенагеля бета-кетоэфиров и альдегидов (1 экв) в ТГФ (0.5 мл/ммоль) и реакционную смесь перемешивали при -78°С в течение 4 ч. Затем добавили раствор уксусной кислоты (4.3 экв) в ТГФ (0.1 мл/ммоль), смесь нагрели до комнатной температуры, разбавили водой и экстрагировали этилацетатом. Объединенные экстракты промыли водой и солевым раствором, высушили (Na2SO4) и эвапорировали. Оставшийся остаток растворили в этаноле (2.5 мл/ммоль), добавили ацетат аммония (12.5 экв) и моногидрат п-толуолсульфоновой кислоты (0.05 экв) и смесь нагревали до кипения с обратным холодильником в течение 1.5 дней. Реакционную смесь затем сконцентрировали и добавили ДХМ. Белый преципитат отфильтровали и фильтрат эвапорировали. Оставшийся остаток растворили в ДХМ (2.5 мл/ммоль), добавили 2,3-дихлор-5,6-дициано-1,4-бензохинон (0.95 экв) при комнатной температуре и реакционную смесь перемешивали в течение 2-2.5 ч. Затем добавили насыщенный раствор NaHCO3 и смесь экстрагировали с помощью ДХМ. Объединенные органические слои дважды промыли насыщенным раствором NaHCO3, высушили (Na2SO4) и эвапорировали. Оставшийся остаток очистили посредством колоночной хроматографии на силикагеле.






Промежуточные соединения Р
Общий Способ Q:
Стадия 1: Раствор кетона (4.46 ммоль, 0.85 экв) в ТГФ (3 мл) добавили по каплям при -78°С в раствор LiHMDS (1M в ТГФ, 5.24 ммоль, 1 экв) в ТГФ (3 мл). Раствор перемешивали в течение 1 ч при -78°С. Предварительно охлажденный раствор аддукта Кневенагеля (промежуточное соединение K, 5.24 ммоль, 1 экв) в ТГФ (3 мл) добавили быстро через иглу с двойным наконечником при температуре ниже -67°С. Раствор перемешивали при -78°С в течение 5 ч и затем погасили добавлением раствора уксусной кислоты (4.3 экв) в ТГФ (1.5 мл). Смеси дали нагреться до комнатной температуры, разбавили водой и экстрагировали этилацетатом. Органические слои объединили, промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Продукт можно очистить с помощью флеш-хроматографии.
Стадия 2: Продукт со стадии 1 (1.21 ммоль) объединили с ацетатом аммония (10 экв) и нагревали до 120°С в воздушной атмосфере в течение 4-10 ч при перемешивании. После охлаждения до комнатной температуры, смесь экстрагировали этилацетатом. Органические слои объединили, промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом.
Стадия 3: Продукт стадии 2 (1.18 ммоль) объединили с FeCl3 (3 экв) и пропионовой кислотой (5.5 мл) и нагревали до кипения с обратным холодильником в течение 1 ч. Смеси дали охладиться до комнатной температуры, разбавили 1 М HCl и экстрагировали с помощью ДХМ. Органические слои объединили, промыли насыщенным водным раствором NaHCO3 и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Продукт может быть очищен с помощью флеш-хроматографии с получением пиридона (промежуточное соединение Р).
Общий Способ R:
Смесь кетона (1 экв), аддукта Кневенагеля (промежуточное соединение K, 1-2 экв, см. таблицу) и ацетата аммония (10 экв) перемешивали при 170°С в воздушной атмосфере в течение 5-10 ч. После охлаждения до комнатной температуры, смесь разбавили водой и экстрагировали этилацетатом. Органические слои объединили, промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Продукт может быть очищен с помощью флеш-хроматографии или кристаллизации.



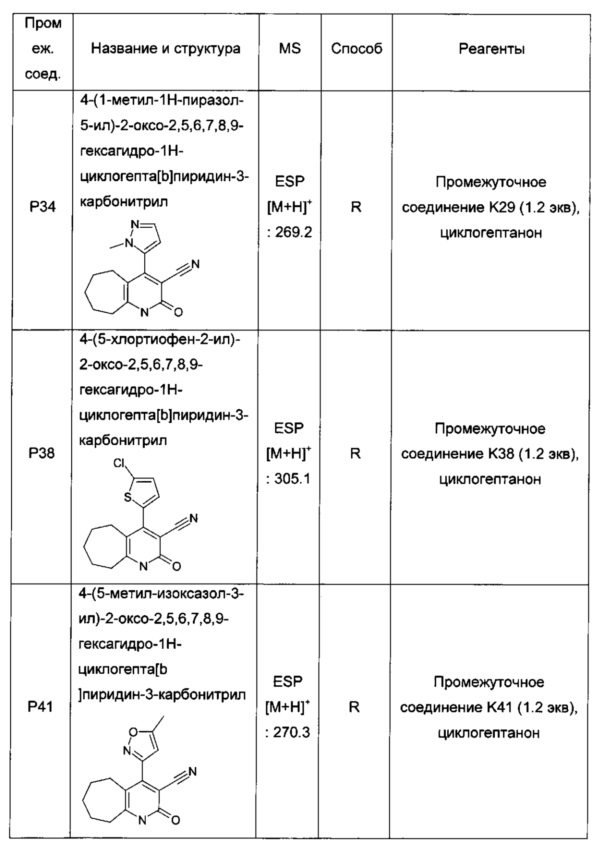

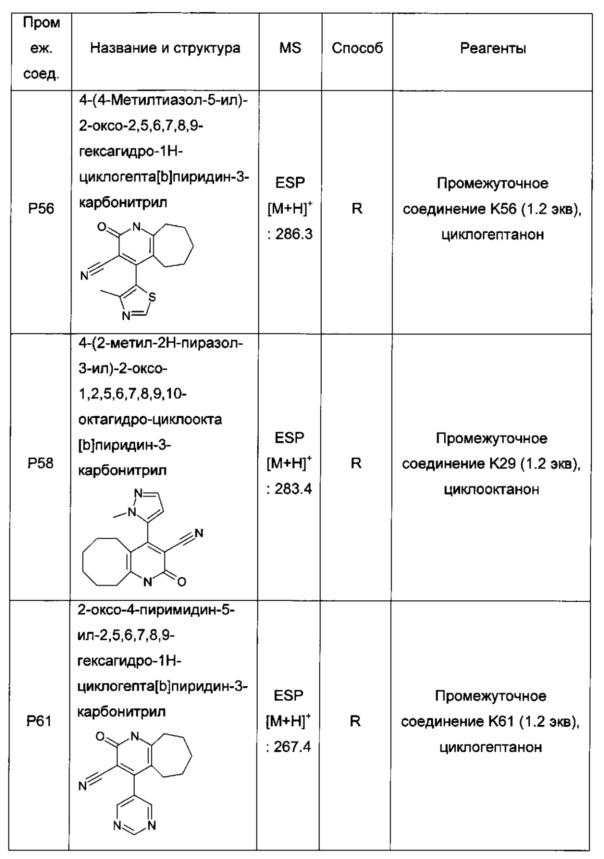

Промежуточное соединение Р35
4-(4-фтор-фенил)-6-метил-2-оксо-1,2,5,6,7,8-гексагидро-хинолин-3-карбонитрил
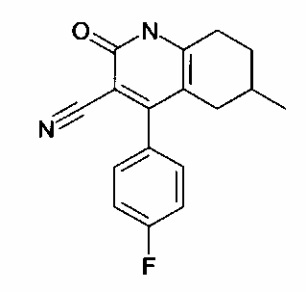
К раствору 2-циано-3-(4-фторфенил)акриламида (промежуточное соединение K35, 2 г) в ДМСО (21.0 мл) добавили 4-метилциклогексанон (1.18 г) и трет-бутоксид калия (1.18 г) при комнатной температуре в воздушной атмосфере с исключением влажности. После перемешивания в течение 30 мин, по данным MS произошло образование аддукта реакции Михаэля. Добавили трет-бутоксид калия (3.54 г) и перемешивание продолжили при комнатной температуре в течение 3 ч. Добавили воду (80 мл) и смесь охладили в ванне со льдом. Смесь медленно подкислили с помощью 25% HCl. Преципитат собрали посредством фильтрации, промыли водой и высушили. Неочищенное вещество очистили с помощью флеш-хроматографии (SiO2, 0%-100% EtOAc в н-гептане) с получением соединения, указанного в заголовке (1.02 г), достаточно чистого для использования на следующей стадии без дополнительной очистки, в виде серо-белого осадка. MS (ESP): m/z=283.3 [М+Н]+.
Промежуточное соединение Р36
4-(4-фтор-Фенил)-2-оксо-1,5,7,8-тетрагидро-2Н-пирано[4,3-b]пиридин-3-карбонитрил

По аналогии с синтезом Промежуточного Соединения Р35, соединение, указанное в заголовке, синтезировали с использованием в качестве исходного вещества 2-циано-3-(4-фторфенил)акриламида (промежуточное соединение K35) и дигидро-2Н-пиран-4(3Н)-она. MS (ESP): m/z=271.0 [М+Н]+.
Промежуточные соединения E/N
Общий Способ S:
Стадия 1: Раствор пиридона (промежуточное соединение Р, 0.51 ммоль, 1 экв) в безводном ДМА (2.73 мл) добавили по каплям к суспензии гидрида натрия (55% в минеральном масле, 1.3 экв) в безводном ДМА (0.91 мл). Смесь перемешивали в течение 45 мин. Раствор N-фенилбис(трифторметансульфонамида) (1.3 экв) в ДМА (2.73 мл) добавили по каплям, затем реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакцию погасили насыщенным водным раствором NH4Cl и экстрагировали этилацетатом. Органические слои объединили, промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Продукт может быть очищен с помощью флеш-хроматографии.
Стадия 2: Суспензию трифлата, полученного на стадии 1 (0.31 ммоль, 1 экв), первичного или вторичного амина (4 экв) и карбоната калия (2 экв) в ТГФ (4.7 мл) нагревали до 70°С в течение 1-10 ч. После охлаждения до комнатной температуры, смесь разбавили водой и экстрагировали этилацетатом. Органические слои объединили, промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Продукт может быть очищен с помощью флеш-хроматографии.
Общий Способ Т:
Стадия 1: Смесь пиридона (промежуточное соединение Р, 3.0 ммоль, 1 экв) и оксихлорида фосфора (30 экв) перемешивали при кипении с обратным холодильником в течение 2-20 ч. После охлаждения до комнатной температуры смесь медленно и осторожно разбавили водой, нейтрализовали 2 М водной NaOH и экстрагировали с помощью ДХМ. Органические слои объединили, промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Продукт может быть очищен с помощью флеш-хроматографии.
Стадия 2: Раствор 2-хлорпиридина, полученного на стадии 1 (0.35 ммоль, 1 экв), первичного или вторичного амина (2 экв) и триэтиламина (3 экв) в ДМФ (1.5 мл) нагревали до 120°С в течение 1-20 ч. Если реакция не проходит полностью, можно добавить дополнительное количество первичного или вторичного амина и триэтиламина. После охлаждения до комнатной температуры, смесь разбавили водой и экстрагировали этилацетатом. Органические слои объединили, промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Продукт может быть очищен с помощью флеш-хроматографии.
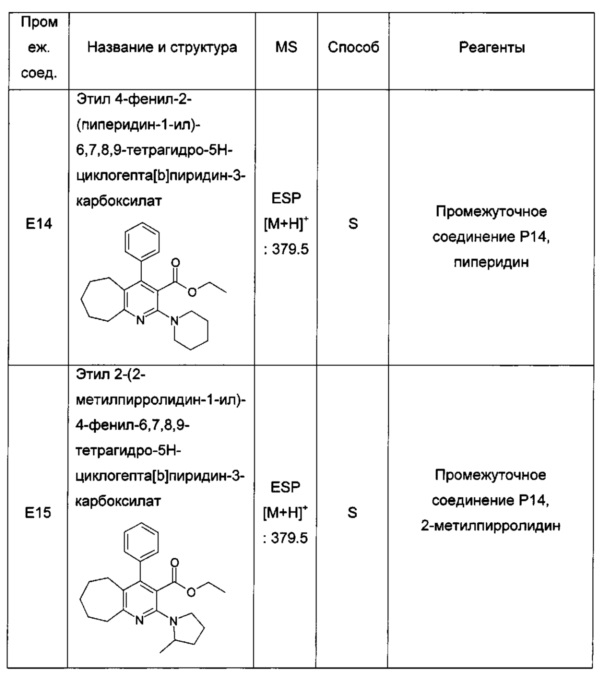
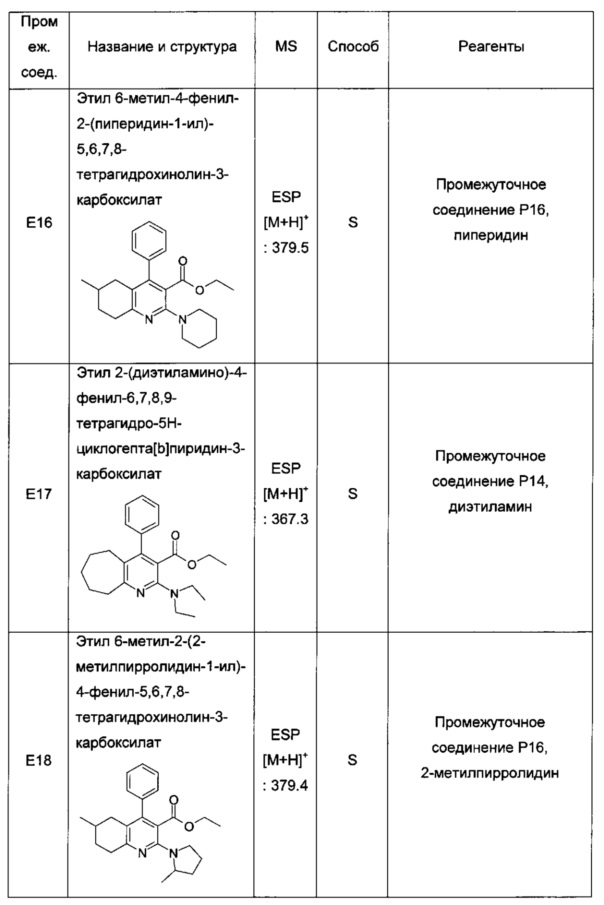

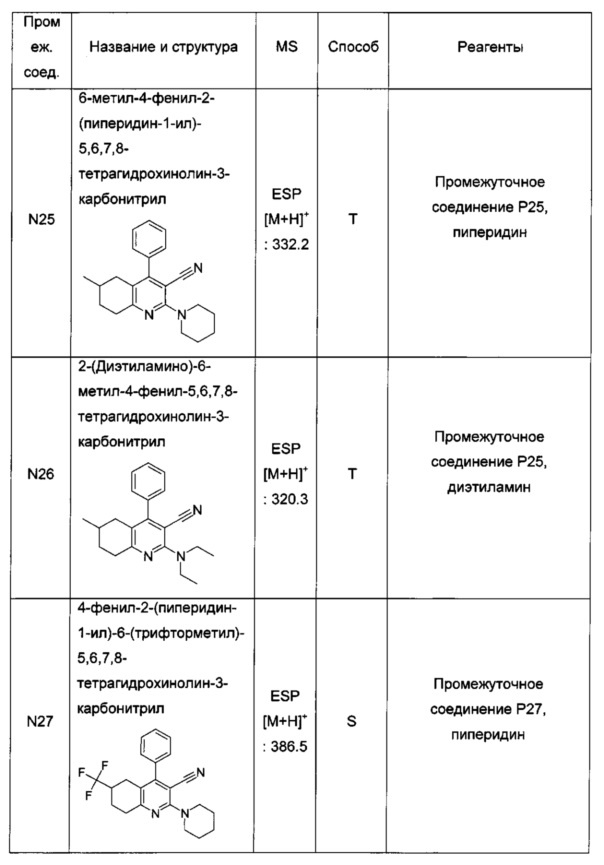

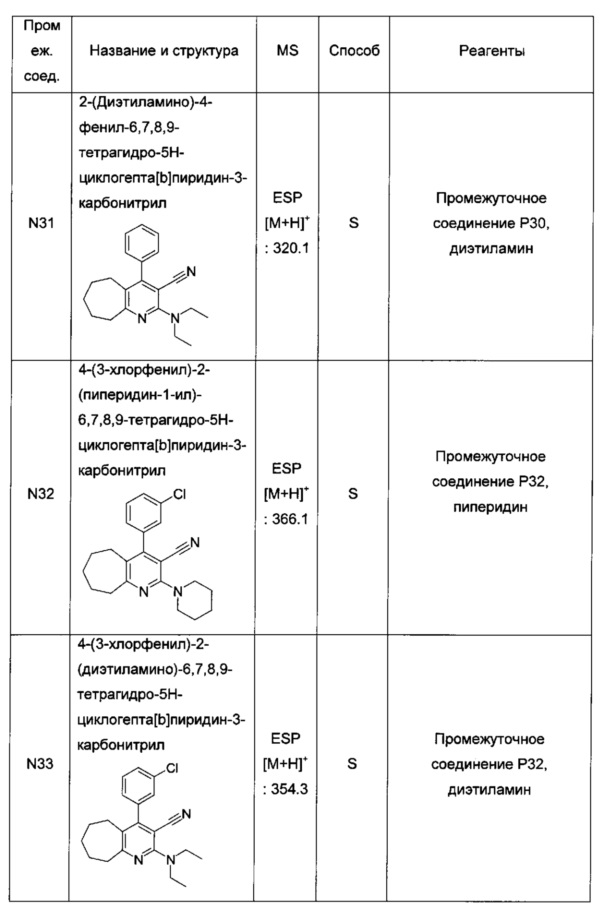



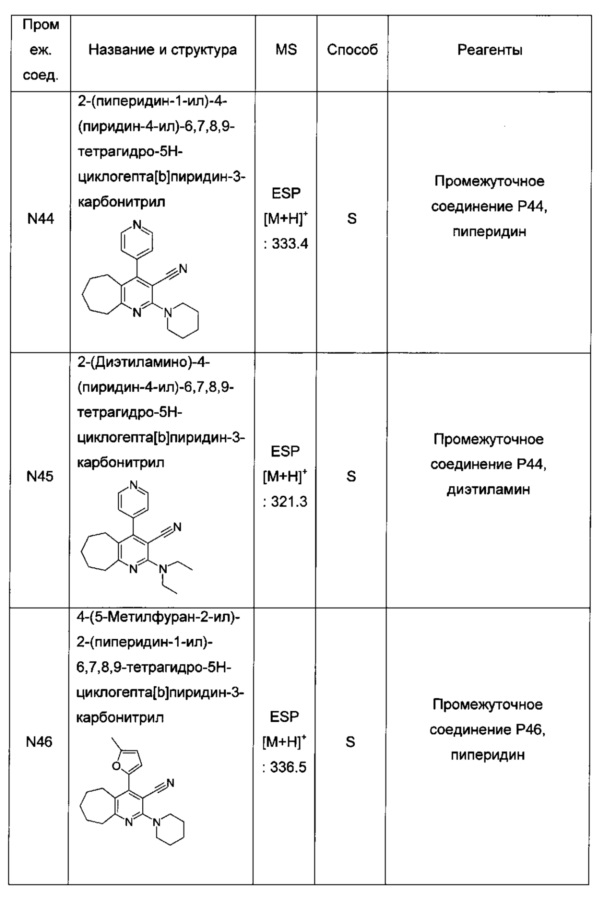




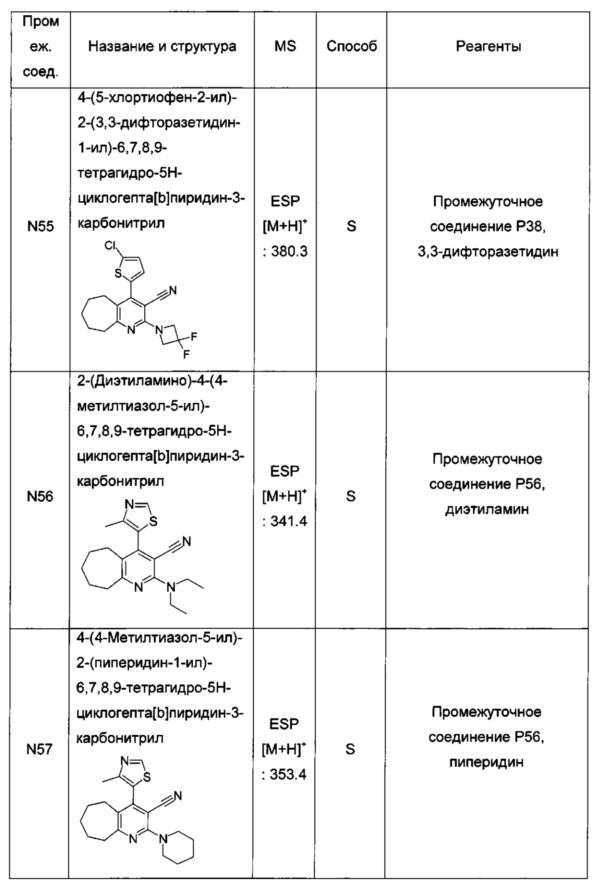
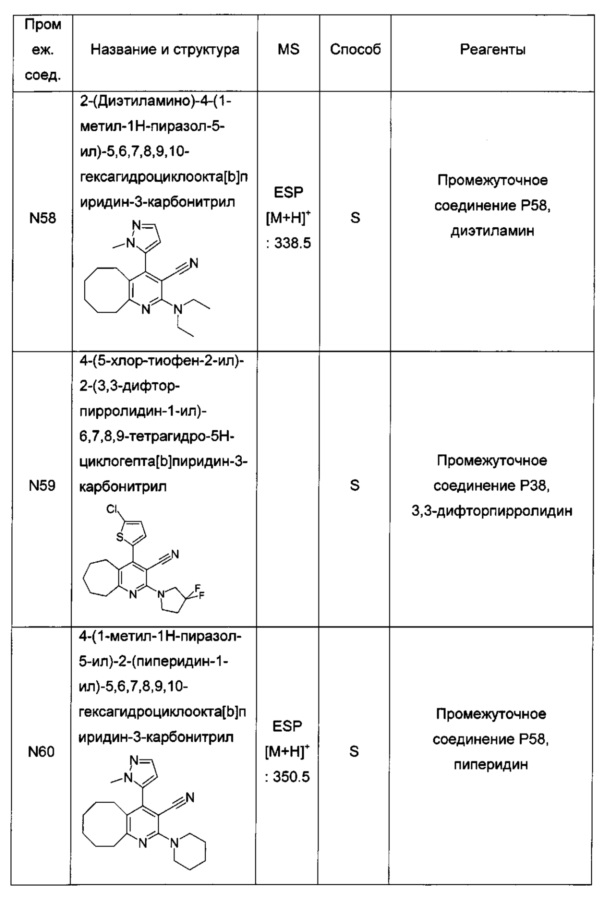

Промежуточное соединение N64
2-амино-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил
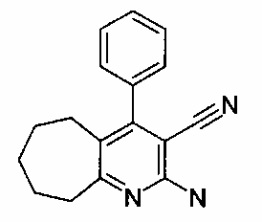
Получили в соответствии с: Kambe, Satoshi; Saito, Koji; Sakurai, Akio; Midorikawa, Hiroshi, Synthesis 1980, 5, 366-8.
Промежуточное соединение N65
2-пропил-4-пиридин-4-ил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил

Промежуточное соединение Р44 конвертировали в 3-циано-4-(пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил трифторметансульфонат с использованием Общего Способа S, стадия 1. 3-циано-4-(пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил трифторметансульфонат (1096 мг), н-пропилбороновую кислоту (727 мг) и трехосновный фосфат калия (1.79 г) объединили с толуолом (34.4 мл), добавили молекулярные сита (4 Å) и смесь перемешивали при комнатной температуре в течение 5 мин. (1,3-Дизопропилимидазол-2-илиден)(3-хлорпиридил)палладий(II) дихлорид (PEPPSI) (150 мг) добавили и реакционную смесь нагревали до 100°С в течение 52 ч. (1,3-Дизопропилимидазол-2-илиден)(3-хлорпиридил)палладий(II) дихлорид (150 мг) добавили и перемешивание при 100°С продолжили в течение 24 ч. Реакционную смесь отфильтровали EtOAc и водой через стекловолокнистую бумагу, затем ее экстрагировали EtOAc, органические фазы промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, 50 г, 5% - 60% EtOAc в н-гептане) с получением соединения, указанного в заголовке (156 мг), в виде серо-белого осадка. MS (ESP): m/z=292.4 [М+Н]+.
Общий Способ U: Продукт конденсации Кневенагеля (промежуточное соединение K, 1.1 ммоль, 1.2 экв), кетон (1 экв) и ацетат аммония (10 экв) объединили и нагревали до 170°С в течение 2.5 ч в открытой колбе. Реакционную смесь охладили до комнатной температуры, разбавили водой и экстрагировали 3 раза EtOAc. Объединенные органические фазы снова экстрагировали водой и солевым раствором и высушили над MgSO4. После эвапорации растворителя проводили или кристаллизацию или очистку хроматографией или использовали соединение как есть на следующей стадии без дополнительной очистки.
Общий Способ V: Суспензию альдегида (2.8 ммоль, 1 экв), кетона (1 экв), кетонитрила (1 экв), ацетата аммония (5 экв) и толуола (9 мл) кипятили с обратным холодильником в течение 50 мин. Реакционную смесь охладили до комнатной температуры, разбавили водой и экстрагировали 3 раза EtOAc. Объединенные органические фазы эвапорировали и дигидропиридиновое промежуточное соединение растворили в ацетоне (14 мл). При комнатной температуре медленно добавили суспензию аммония церия азотнокислого (3.1 г, 2 экв) в воде (2 мл) и желтую реакционную смесь перемешивали в течение 30 мин. После эвапорации растворителей остаток экстрагировали водой/EtOAc (3х). Объединенные органические фазы сконцентрировали и очистили посредством кристаллизации или хроматографии.



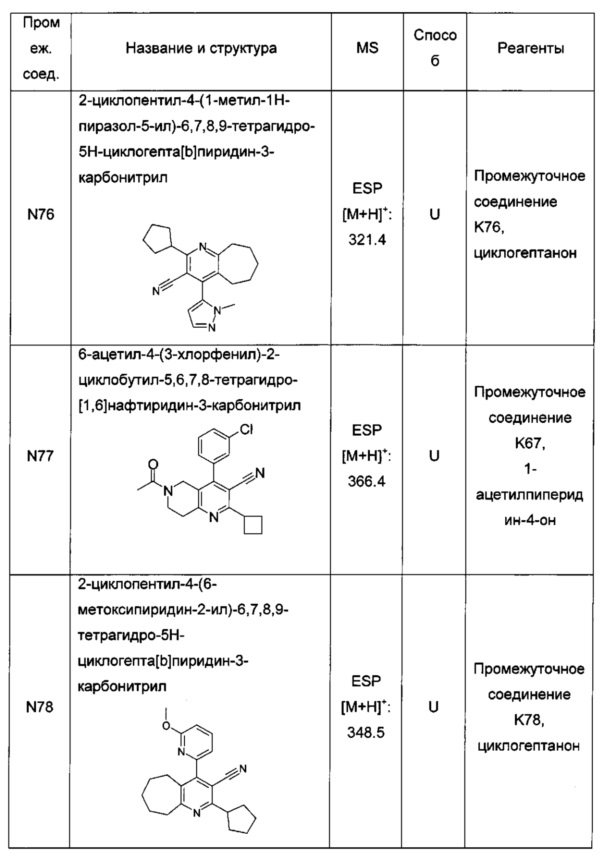




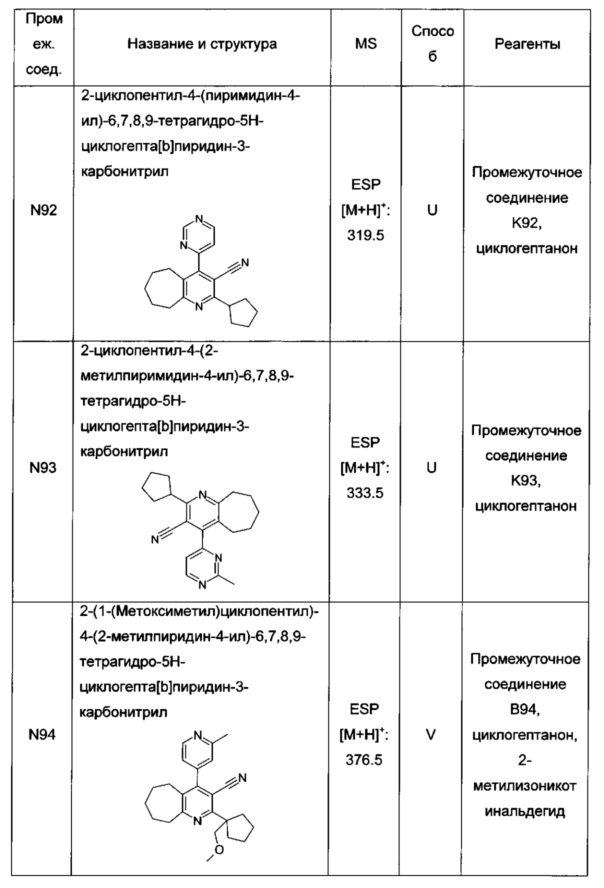







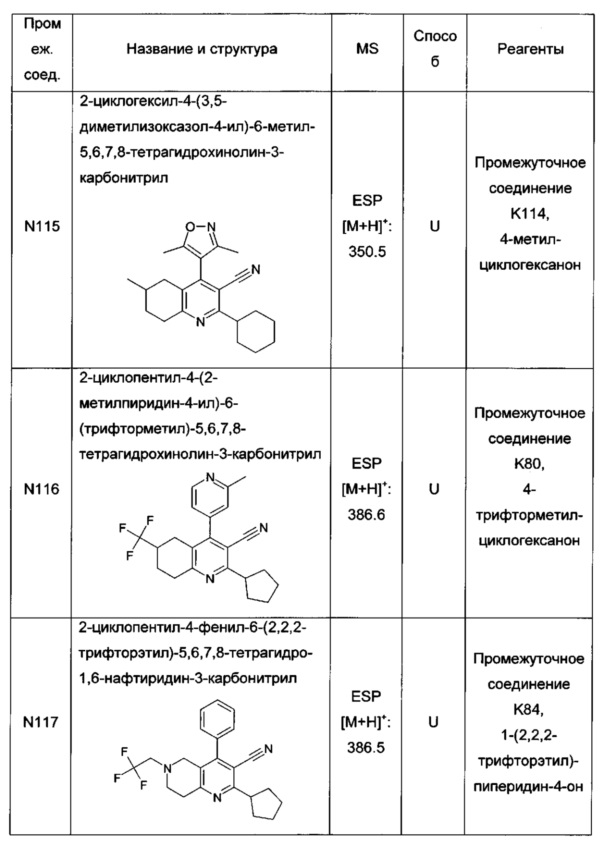


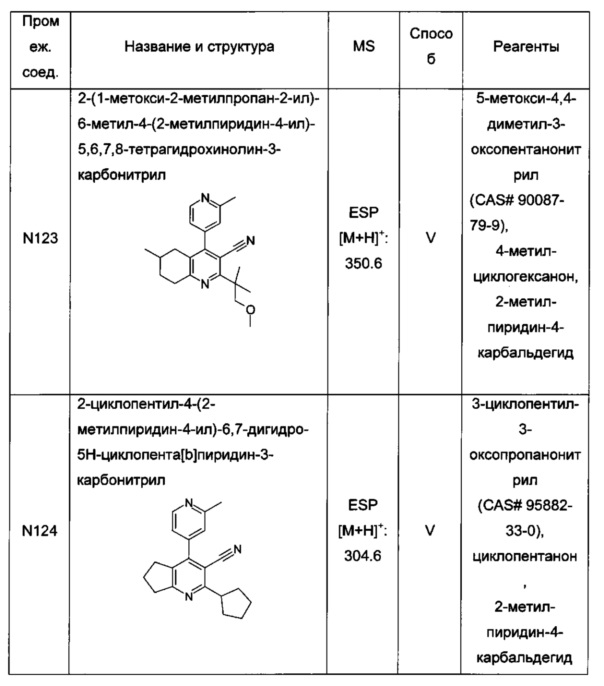


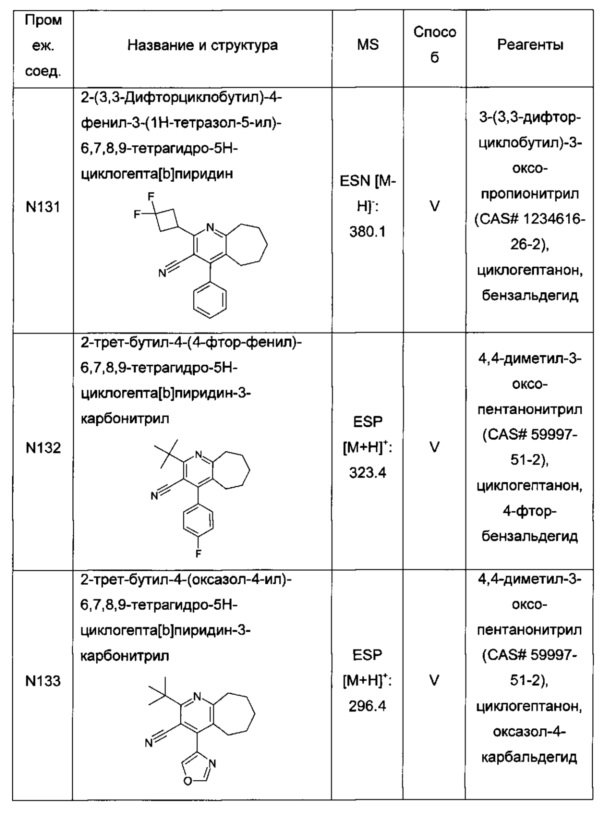

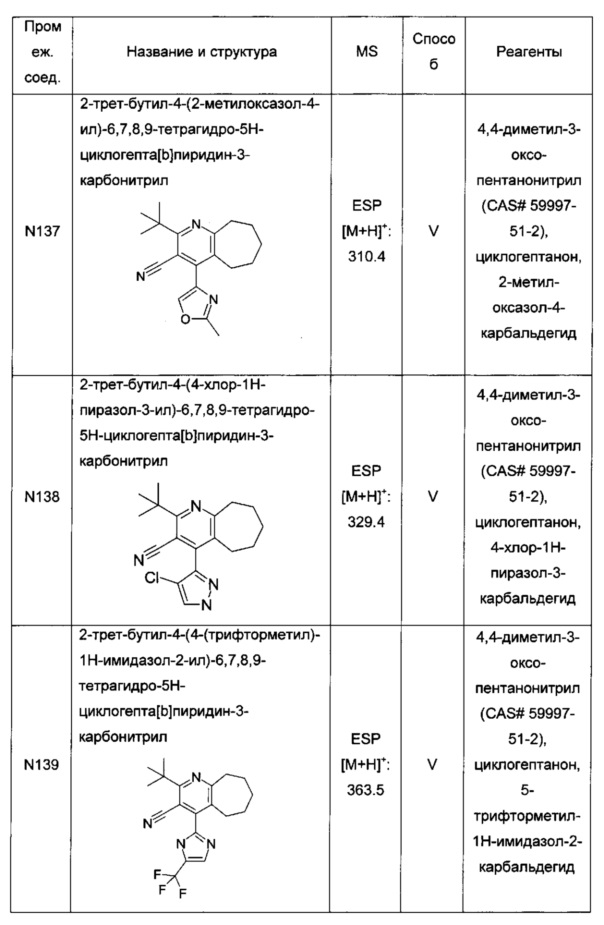

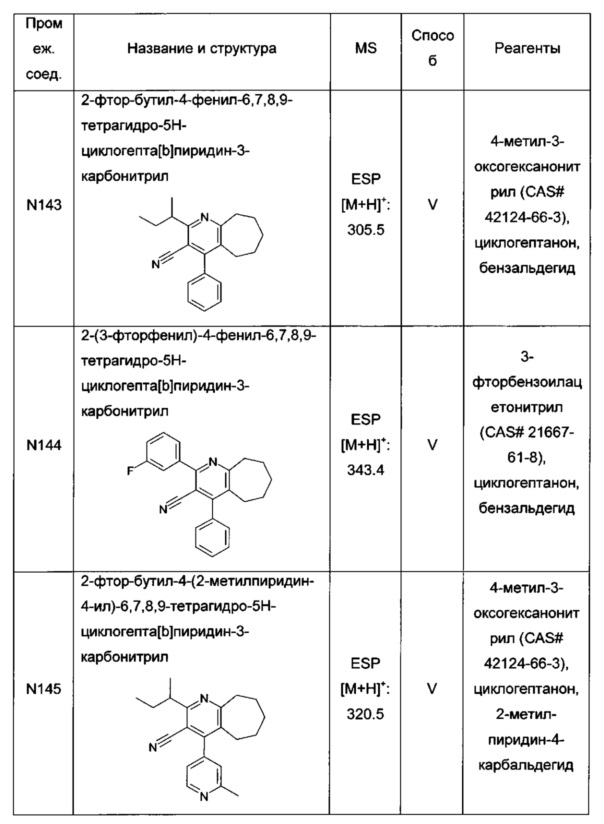
Промежуточное соединение N71
2-циклогексил-4-(6-оксо-1,6-дигидропиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил

Используя Общий Способ R, Промежуточное соединение K71 взаимодействовало с циклогептанон и ацетатом аммония с получением 2-циклогексил-4-(6-метоксипиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрила. 2-циклогексил-4-(6-метоксипиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил (1.162 г) и водную HCl 37% (6.34 г) объединили с диоксаном (47.5 мл) и перемешивали при 100°С в течение 1 ч. После охлаждения до комнатной температуры, смесь разбавили водой и экстрагировали EtOAc. Органические слои сконцентрировали под вакуумом. Неочищенное вещество суспендировали в небольшом количестве EtOAc. Продукт собрали посредством фильтрации, промыли EtOAc и высушили с получением соединения, указанного в заголовке (1.12 г) в виде бесцветного осадка. MS (ESP): m/z=348.5 [М+Н]+.
Промежуточное соединение N72
2-циклогексил-4-(1-этил-6-оксо-1,6-дигидропиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил

Суспензию Промежуточного соединения N71 (250 мг), карбоната калия (109 мг) и этилйодида (118 мг) в ДМА (4.13 мл) перемешивали при комнатной температуре в течение 3 дней. Смесь разбавили водой и экстрагировали EtOAc. Органические слои промыли водой и солевым раствором, высушили над MgSO4 и сконцентрировали под вакуумом. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, 0%-10% МеОН в ДХМ) с получением соединения, указанного в заголовке (184 мг), в виде бесцветной пены. MS (ESP): m/z=376.5 [М+Н]+.
Промежуточное соединение N73
2-циклогексил-4-(1-метил-6-оксо-1,6-дигидропиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил

По аналогии с синтезом Промежуточного Соединения N72, Промежуточное соединение N71 конвертировали в соединение, указанное в заголовке посредством взаимодействия с метилйодидом в присутствии карбоната калия. Бесцветная пена. MS (ESP): m/z=362.5 [М+Н]+.
Промежуточное соединение N90
2-циклобутил-4-(1-метил-6-оксо-1,6-дигидропиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил

Используя Общий Способ R, Промежуточное соединение K90 взаимодействовало с циклогептаноном и ацетатом аммония с получением 2-циклобутил-4-(6-метоксипиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрила. Это соединение конвертировали в 2-циклобутил-4-(6-оксо-1,6-дигидропиридин-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил посредством взаимодействия с HCl в диоксане по аналогии с синтезом Промежуточного Соединения N71. Это соединение конвертировали в соединение, указанное в заголовке посредством взаимодействия с метилйодидом в присутствии карбоната калия по аналогии с синтезом Промежуточного Соединения N72. Серо-белый аморфный осадок. MS (ESP): m/z=334.3 [М+Н]+.
Общий Способ W: Конверсия метоксиметильной группы в гидроксиметильную
Метоксиметильное соединение (1 эквивалент) объединили с 48% водным HBr (29.0 эквивалентов) и перемешивали при 100°С в течение 1-3 ч. После охлаждения до комнатной температуры, продукт собрали посредством фильтрации, промыли водой и высушили. При необходимости, продукт может быть дополнительно очищен хроматографией. Альтернативно, продукт может быть получен экстракцией с использованием, например, EtOAc.
Общий Способ Z: Конверсия нитрила в карбоновую кислоту
Объединили нитрил (1 эквивалент) и серную кислоту (50% в воде, 24 эквивалента). Реакционную смесь нагревали до 145°С (температура нагревательного устройства) и перемешивали в течение 3 ч. После охлаждения до комнатной температуры, смесь поместили в ванну со льдом и охладили до 5-10°С. Медленно добавили раствор нитрита натрия (1.8 эквивалентов) в воде под поверхность реакционной смеси и затем нагрели до 50°С. Реакционную смесь перемешивали в течение ночи при 50°С, и охладили до комнатной температуры. Добавили воду и перемешивали в течение 30 мин. Реакционную смесь влили в 1 М водный NaOH и экстрагировали диэтиловым эфиром. Водный слой подкислили до рН 1 с помощью HCl и экстрагировали EtOAc. Объединенные органические слои высушили над MgSO4, эвапорировали и высушили. Продукт может быть очищен посредством хроматографии.





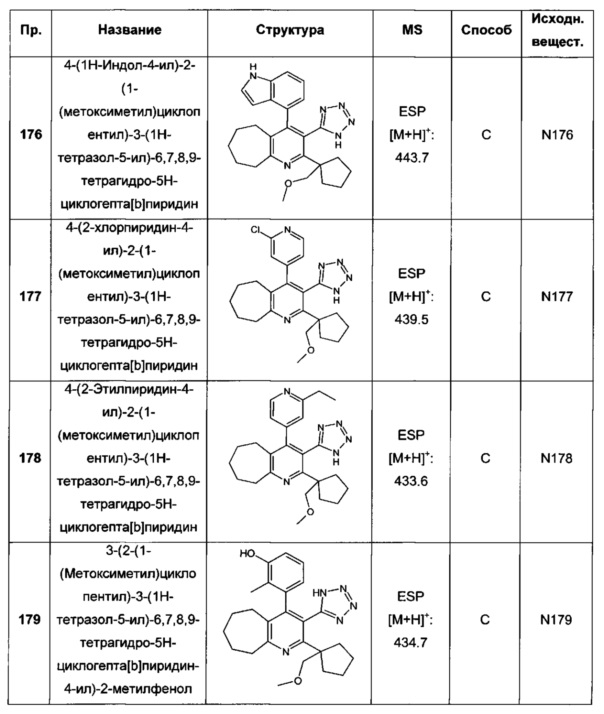

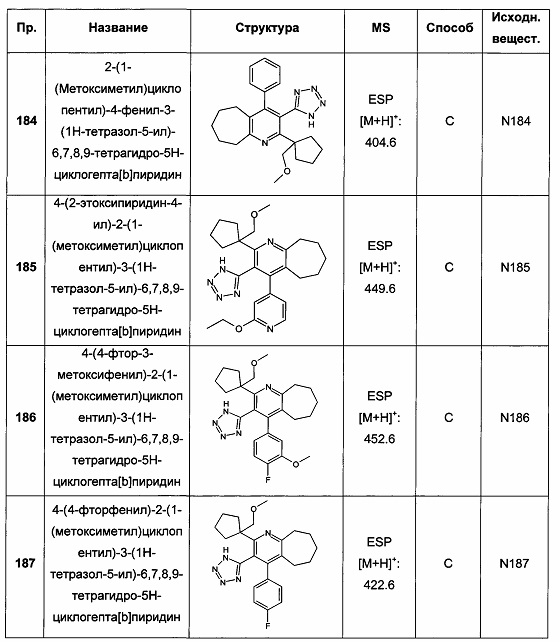
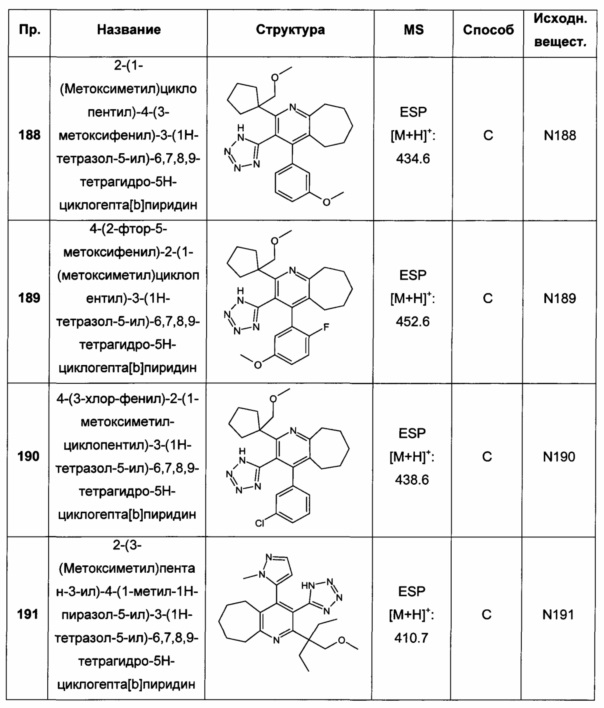


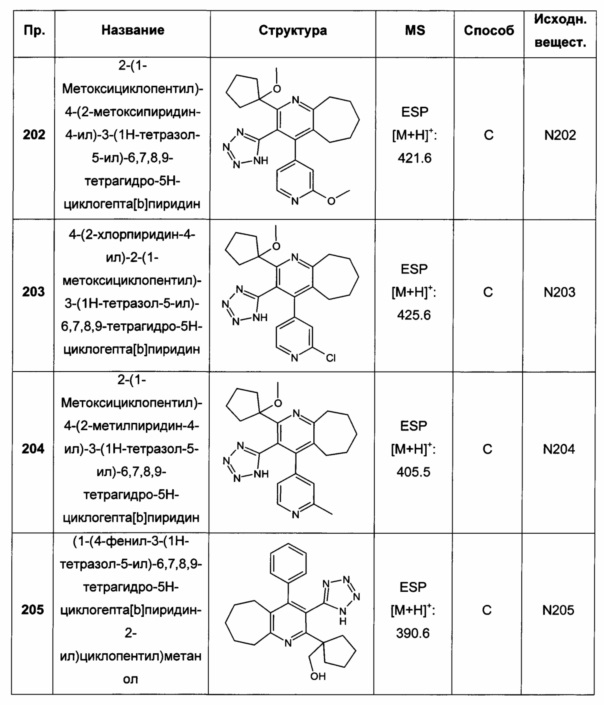


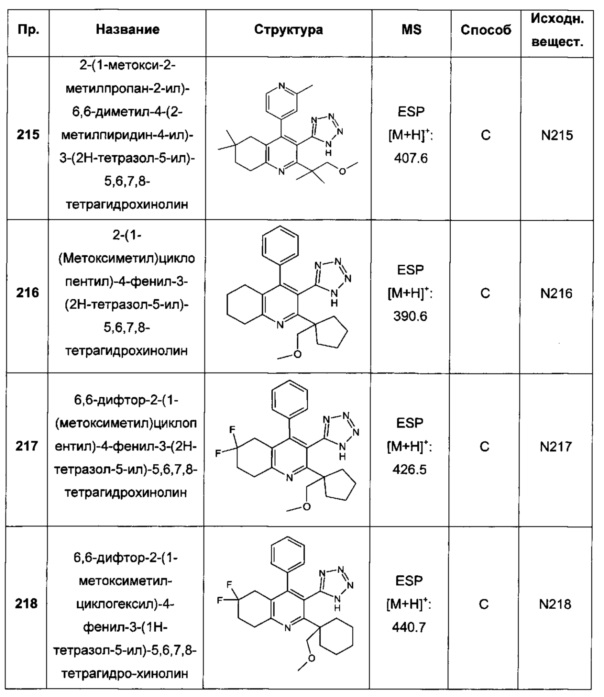







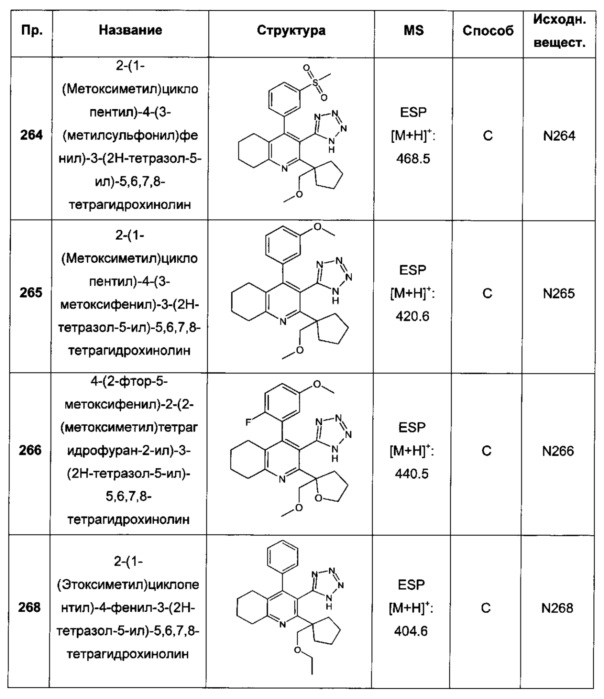



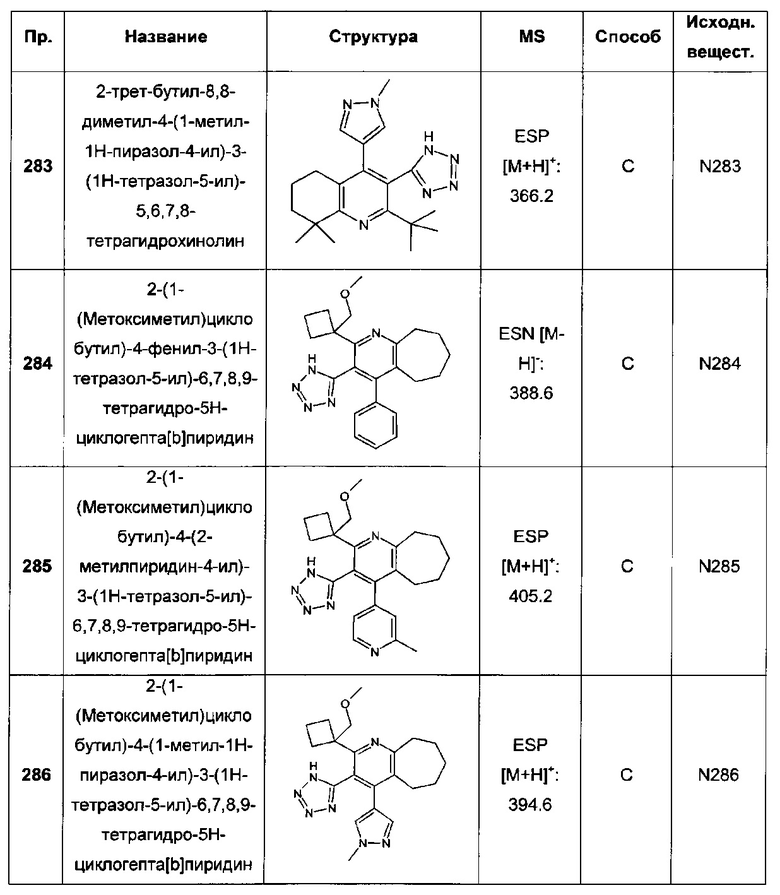

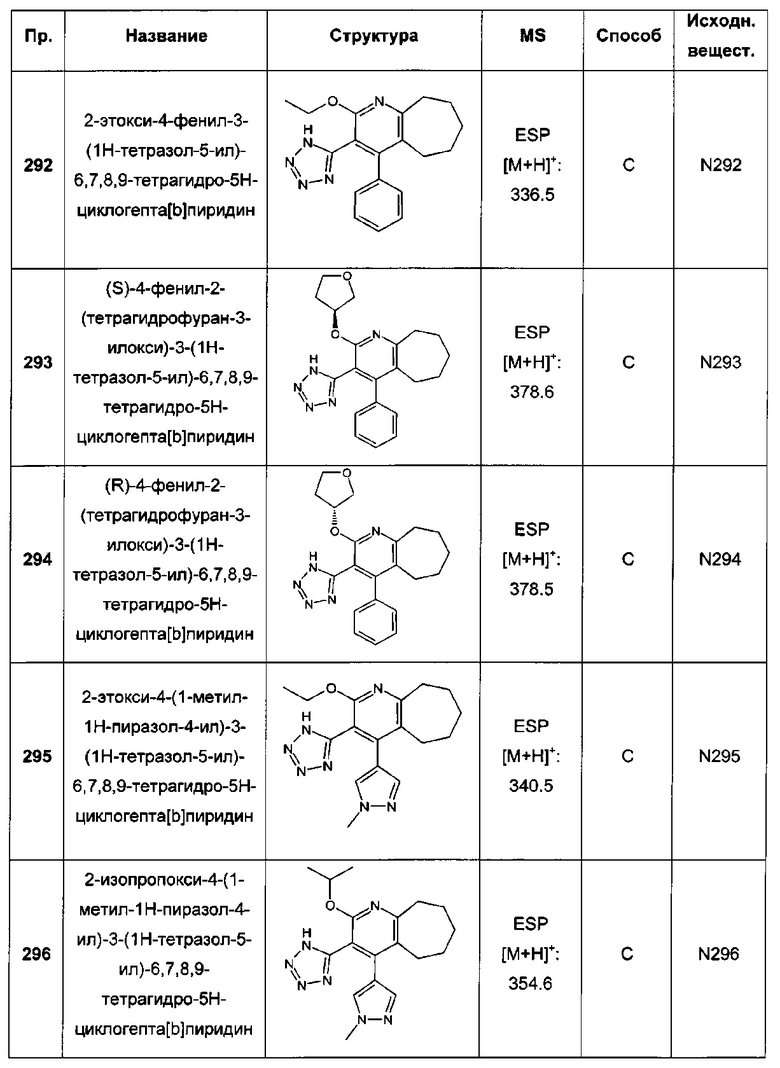






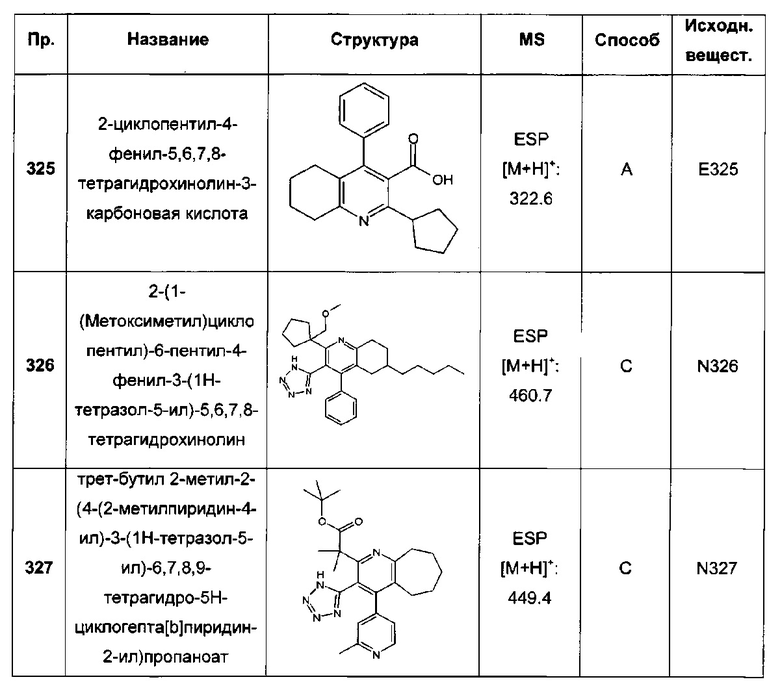
Общий Способ X: Тетразоловые соединения, содержащие стереогенные центры и/или оси могут быть разделены с помощью препаративной ВЭЖХ с использованием следующих условий.
Х1: Reprosil Chiral NR, 15% iPrOH в гептане
Х2: Chiralpak AD-H, 10% EtOH в гептане
Х3: Chiralpak AD, 10% iPrOH в гептане
Х4: Chiralpak AD, 10% EtOH в гептане
Х5: Chiralpak AD, 5% EtOH в гептане
Х6: Chiralpak AD, 15% iPrOH в гептане





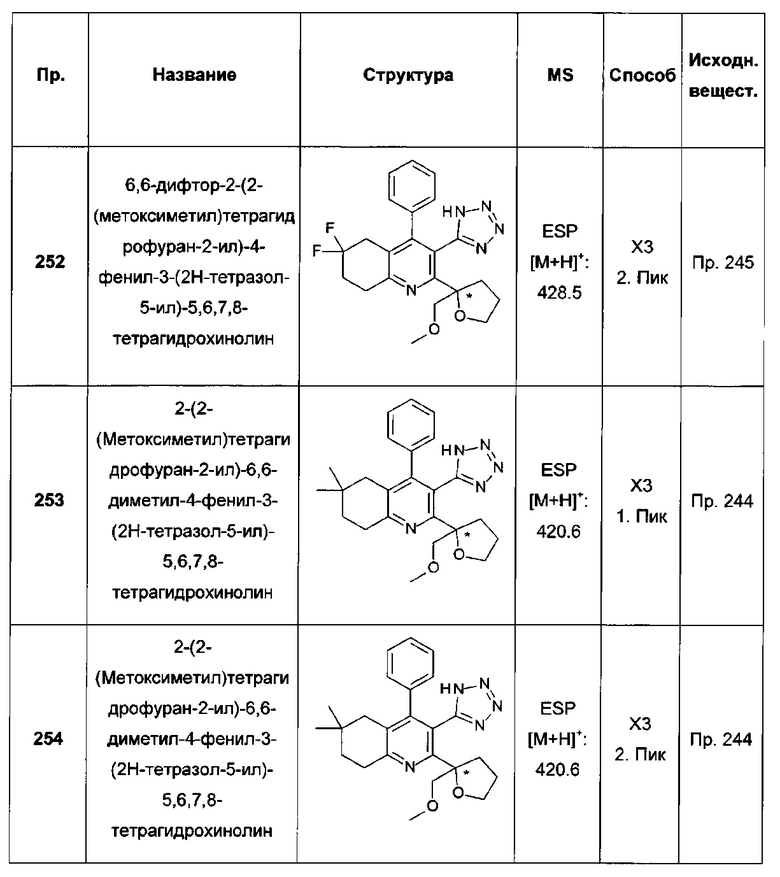
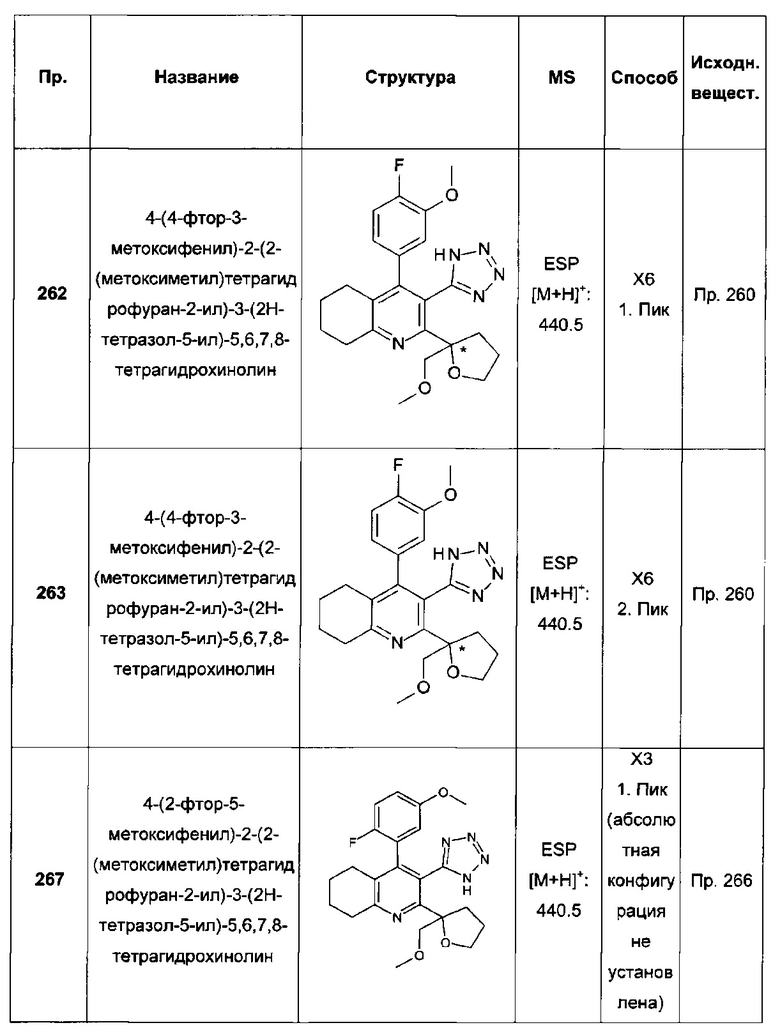
Пример 169
4-(2-(1-Метилциклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)пиридин-2(1Н)-он

4-(2-Метоксипиридин-4-ил)-2-(1-метилциклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин (Пример 168, 68.9 мг) смешали с бромистоводородной кислотой, 33% в уксусной кислоте (1.42 г) и суспензию перемешивали при 70°С в течение 18 ч. Реакционную смесь эвапорировали, дважды эвапорировали водой и очистили с помощью препаративной ВЭЖХ с получением соединения, указанного в заголовке (26 мг), в виде бесцветного осадка. MS (ESP)=391.7 [М+Н]+.
Пример 211
(S)-4-Фенил-2-(пирролидин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин 2,2,2-трифторацетат
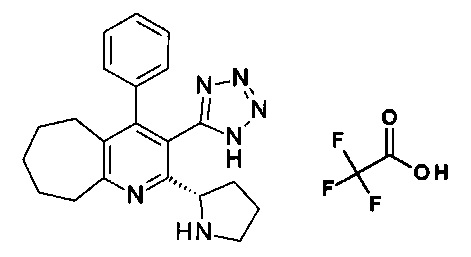
(S)-трет-бутил 2-(4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пирролидин-1-карбоксилат (Пример 210, 140 мг) растворили в ДХМ (2 мл). После добавления ТФУ (1.48 г) реакционную смесь перемешивали в течение 1 ч при КТ. Растворитель эвапорировали и продукт очистили с помощью препаративной ВЭЖХ с получением соединения, указанного в заголовке (55 мг), в виде серо-белого осадка. MS (ESP): m/z=361.6 [М+Н]+.
Пример 328
2-метил-2-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пропановая кислота

Трет-бутил 2-метил-2-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пропаноат (Пример 327, 28 мг) растворили в ДХМ (3 мл). После добавления ТФУ (7.12 мг) реакционную смесь перемешивали в течение 27 ч при КТ. Растворитель эвапорировали и продукт очистили с помощью препаративной ВЭЖХ с получением соединения, указанного в заголовке (8 мг), в виде белого осадка. MS (ESP): m/z=393.5 [М+Н]+.
Промежуточное соединение В154
3-(2-Метилтетрагидрофуран-2-ил)-3-оксо-пропанонитрил
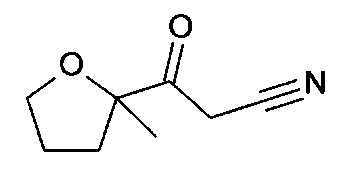
По аналогии с синтезом Промежуточного Соединения В79, метил 2-метилтетрагидрофуран-2-карбоксилат (CAS# 1218915-91-3) конвертировали в соединение, указанное в заголовке посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Бесцветная жидкость. MS (ESP): m/z=154.2 [М+Н]+.
Промежуточное соединение В166
3-(1-Метилциклопентил)-3-оксопропанонитрил

По аналогии с синтезом Промежуточного Соединения В79, метил 1-метилциклопентанкарбоксилат (CAS# 4630-83-5) конвертировали в соединение, указанное в заголовке, посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Желтое масло. MS (ESN): m/z=150.3 [М-Н]-.
Промежуточное соединение В191
4-этил-4-(метоксиметил)-3-оксогексанонитрил
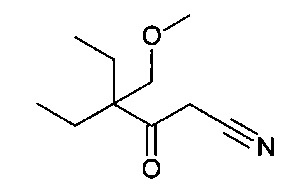
По аналогии с синтезом Промежуточного Соединения В218, этил 2-этилбутаноат (CAS# 2983-38-2) взаимодействовал с диизопропиламидом лития и хлорметилметиловым эфиром с получением этил 2-этил-2-(метоксиметил)бутаноата, который конвертировали в соединение, указанное в заголовке посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Светло-желтая жидкость. MS (ESP): m/z=189.3 [М+Н]+.
Промежуточное соединение В200
3-(1-Метоксициклопентил)-3-оксопропанонитрил
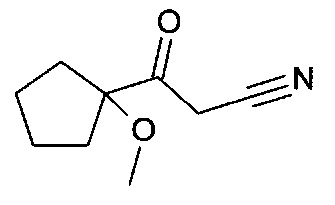
По аналогии с синтезом Промежуточного Соединения В79, метил 1-метоксициклопентанкарбоксилат (CAS# 17860-29-6) конвертировали в соединение, указанное в заголовке, посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Светло-желтая жидкость. MS (ESN): m/z=166.3 [М-Н]-.
Промежуточное соединение В218
3-(1-(Метоксиметил)циклогексил)-3-оксопропанонитрил

К раствору диизопропиламина (3.66 г, 5.15 мл, 36.1 ммоль) в ТГФ (50 мл) в атмосфере аргона медленно добавили н-бутиллитий (1.6 М в н-гексане, 22.5 мл, 36.0 ммоль) при -78°С и смесь перемешивали в течение 30 минут. Затем добавили раствор метилциклогексанкарбоксилата (5 г, 35.2 ммоль) в ТГФ (25 мл) по каплям. Смеси дали нагреться до -40°С и перемешивали в течение 30 минут при этой температуре. Затем раствор хлорметилметилового эфира (2.83 г, 35.2 ммоль) в ТГФ (12.5 мл) добавили по каплям. После завершения добавления, реакционной смеси дали нагреться до КТ. Добавили воду и смесь экстрагировали EtOAc.Объединенные органические экстракты промыли водой и солевым раствором, высушили над Na2SO4 и эвапорировали с получением метил 1-(метоксиметил)циклогексанкарбоксилата в виде светло-желтого масла, которое конвертировали в соединение, указанное в заголовке, по аналогии с синтезом Промежуточного Соединения В79, посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Светло-желтое масло. MS (ESP): m/z=196.5 [М+Н]+.
Промежуточное соединение В242
3-(2-(Метоксиметил)тетрагидрофуран-2-ил)-3-оксопропанонитрил

По аналогии с синтезом Промежуточного Соединения В218, метил тетрагидрофуран-2-карбоксилат (CAS# 37443-42-8) взаимодействовал с диизопропиламидом лития и хлорметилметиловым эфиром с получением метил 2-(метоксиметил)тетрагидрофуран-2-карбоксилата, который конвертировали в соединение, указанное в заголовке, посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Светло-желтое масло. MS (ESN): m/z=182.3 [М-Н]-.
Промежуточное соединение В246
3-(2-Этилтетрагидрофуран-2-ил)-3-оксопропанонитрил
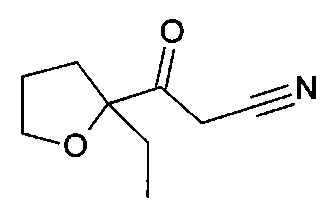
По аналогии с синтезом Промежуточного Соединения В218, метил тетрагидрофуран-2-карбоксилат (CAS# 37443-42-8) взаимодействовал с диизопропиламидом лития и йодометаном с получением метил 2-этилтетрагидрофуран-2-карбоксилата, который конвертировали в соединение, указанное в заголовке, посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Светло-желтое масло. MS (ESN): m/z=166.4 [М-Н]-.
Промежуточное соединение В261
3-(1-(Метилсульфонилметил)циклопентил)-3-оксопропанонитрил
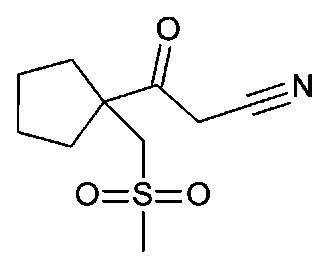
По аналогии с синтезом Промежуточного Соединения В218, метил циклопентанкарбоксилат взаимодействовал с диизопропиламидом лития и (хлорметил)(метил)сульфаном с получением метил 1-(метилтиометил)циклопентанкарбоксилата, который конвертировали в 3-(1-(метилтиометил)циклопентил)-3-оксопропанонитрил посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. 3-(1-(метилтиометил)циклопентил)-3-оксопропанонитрил (210 мг, 1.06 ммоль) затем растворили в дихлорметане (10 мл) и добавили м-хлорпербензойную кислоту (656 мг, 2.66 ммоль) за одну порцию и смесь перемешивали при комнатной температуре в течение ночи. Получившуюся белую суспензию разбавили водой и экстрагировали с помощью ДХМ. Органические экстракты промыли Na2SO3 (15% г/г раствор) и насыщенным водным раствором NaHCO3, высушили над Na2SO4 (содержащем твердый Na2SO3) и эвапорировали с получением соединения, указанного в заголовке, в виде белого осадка. MS (ESN): m/z=228.3 [М-Н]-.
Промежуточное соединение В268
3-[1-(Этоксиметил)циклопентил]-3-оксо-пропанонитрил
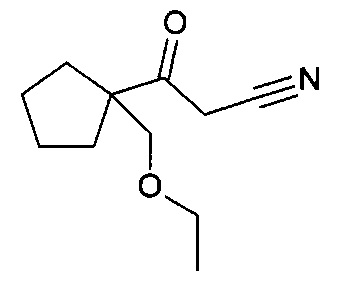
По аналогии с синтезом Промежуточного Соединения В79, метил 1-(этоксиметил)циклопентанкарбоксилат (CAS# 1360569-15-8) конвертировали в соединение, указанное в заголовке, посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Желтая жидкость. MS (ESN): m/z=194.3 [М-Н]-.
Промежуточное соединение В284
3-(1-(Метоксиметил)циклобутил)-3-оксопропанонитрил

По аналогии с синтезом Промежуточного Соединения В218, метил циклобутанкарбоксилат (CAS# 765-85-5) взаимодействовал с диизопропиламидом лития и хлорметилметиловым эфиром с получением метил 1-(метоксиметил)циклобутанкарбоксилата, который конвертировали в соединение, указанное в заголовке посредством взаимодействия с гидридом натрия и ацетонитрилом в ТГФ. Желтая жидкость. MS (ESN): m/z=166.3 [М-Н]-.
Промежуточное соединение В327
трет-бутил 4-циано-2,2-диметил-3-оксобутаноат

Раствор ацетонитрила (0.60 г, 14.6 ммоль) в ТГФ (29 мл) охладили в ванне с сухим льдом. Добавили n-BuLi (9 мл 1.6 М раствора в гексане, 14.4 ммоль) по каплям и перемешивание продолжили в течение 30 мин. Затем медленно добавили раствор 1-трет-бутил 3-метил 2,2-диметилмалоната (CAS# 85293-46-5) (1.5 г, 7.3 ммоль) в ТГФ (7 мл). Смесь перемешивали в течение 2 ч при -78°С. Уксусную кислоту (2.4 мл, избыток) добавили и реакционной смеси дали нагреться до КТ. После экстракции (AcOEt/насыщ. водн. раствор сегнетовой соли) органическую фазу высушили (Na2SO4) и сконцентрировали с получением светло-оранжевой жидкости (1.4 г), которую использовали на следующей стадии без дополнительной очистки.
Дополнительные Промежуточные соединения К (посредством конденсации Кневенагеля)
Общий Способ 72: Продукты реакции Кневенагеля посредством взаимодействия алкилцианоацетата с альдегидом и NH4OAc при КТ
Смесь альдегида (1 экв), алкил 2-цианоацетата (1 экв), ацетата аммония (1.5 экв) и спирта (обычно этанола) перемешивали при КТ в течение 1 ч. После экстракции (AcOEt/H2O) органическую фазу высушили (Na2SO4), отфильтровали и сконцентрировали досуха с получением соединения, указанного в заголовке, в виде осадка, который может быть использован как есть. При необходимости, он может быть дополнительно очищен посредством хроматографии и/или перекристаллизации.

Дополнительные Промежуточные соединения Р (Пиридоны)
Общий Способ Z1: пиридоны из кетонов, аддуктов Кневенагеля, NH4OAc (78°С) с последующим взаимодействием с церий аммоний нитратом
Смесь кетона (1 экв), аддукта Кневенагеля (промежуточное соединение K, 1 экв), ацетата аммония (3 экв) и спирта (обычно этанола) кипятили с обратным холодильником в течение 2-12 ч. Суспензию охладили в ванне со льдом и отфильтровали с получением преципитата 1. Маточную жидкость сконцентрировали, растворили в ацетоне/воде (1/1) и охладили в ванне со льдом. Церий аммоний нитрат (1 экв) добавили и перемешивание продолжили в течение 20 мин -2 ч при КТ. Реакционную смесь отфильтровали с получением преципитата 2. Объединенные осадки высушивают и они могут быть использованы как есть. При необходимости, сырой продукт может быть дополнительно очищен посредством хроматографии и/или кристаллизации с получением чистого образца соединения, указанного в заголовке.
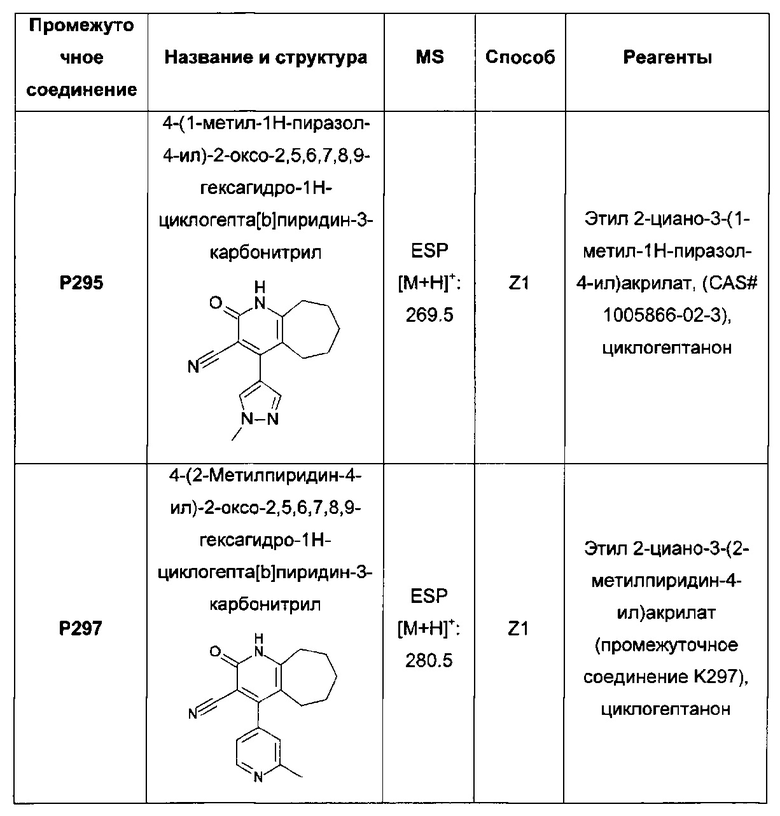



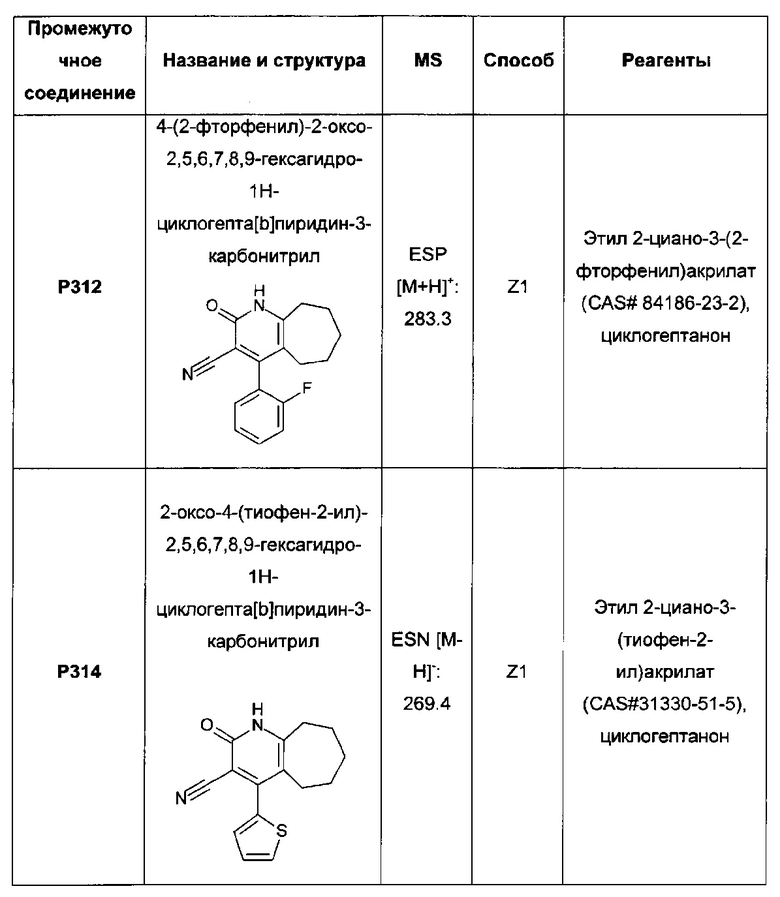

Дополнительные Промежуточные соединения E/N
Общий Способ Y: Конверсия пиридонов в 2-алкоксипиридины через 2-хлорпиридины
Стадия 1: К суспензии пиридона (промежуточное соединение Р, 54.1 ммоль) в оксихлориде фосфора (377 ммоль, 7 экв) медленно добавили ДМФ (23.1 ммоль, 0.43 экв). После того, как экзотермическая реакция закончилась, смесь нагревали до 105°С в течение 4 ч. Все летучие компоненты эвапорировали и маслянистый остаток медленно влили в воду. Суспензию перемешивали в течение 1 ч, отфильтровали, промыли водой и высушили с получением 2-хлорпиридина в виде коричневого осадка. Соединение может быть использовано как есть или дополнительно быть очищено посредством хроматографии.
Стадия 2: Соответствующий спирт (4.2 ммоль, 4 экв) растворили в ТГФ (2 мл). Гидрид натрия (4 экв 55% дисперсия в минеральном масле) добавили. Смесь перемешивали при комнатной температуре в течение 1 ч с последующим добавлением суспензии хлорпиридина, полученного на стадии 1 (1.1 ммоль, 1 экв) в ТГФ (3 мл). Реакционную смесь перемешивали при КТ в течение 3 ч. Экстракция (вода/насыщ. водн раствор бикарбоната натрия) с последующей хроматографией дают целевое соединение.



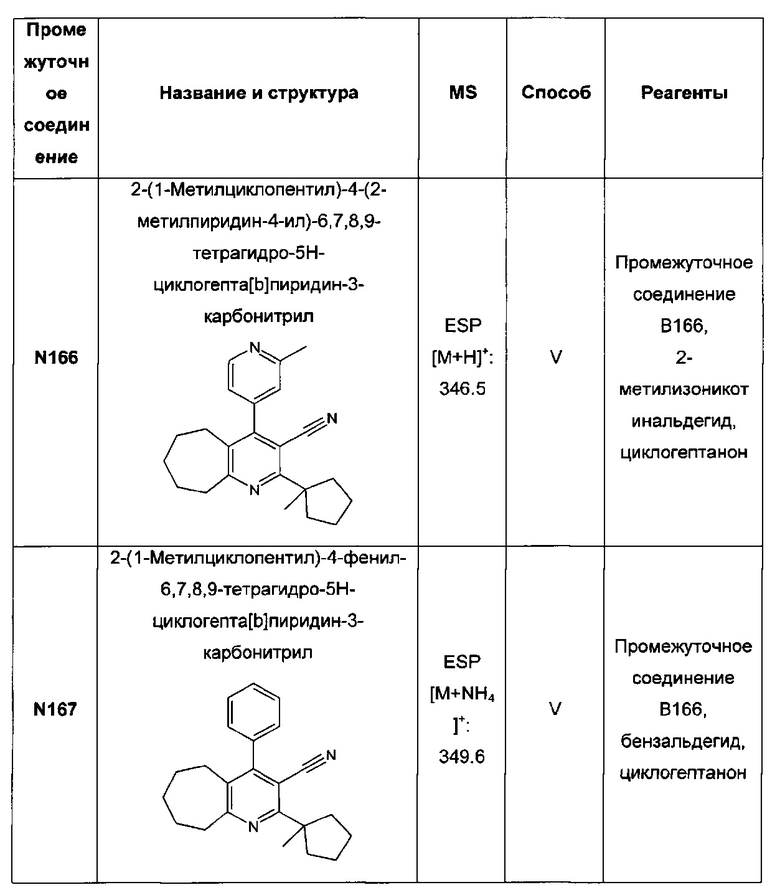





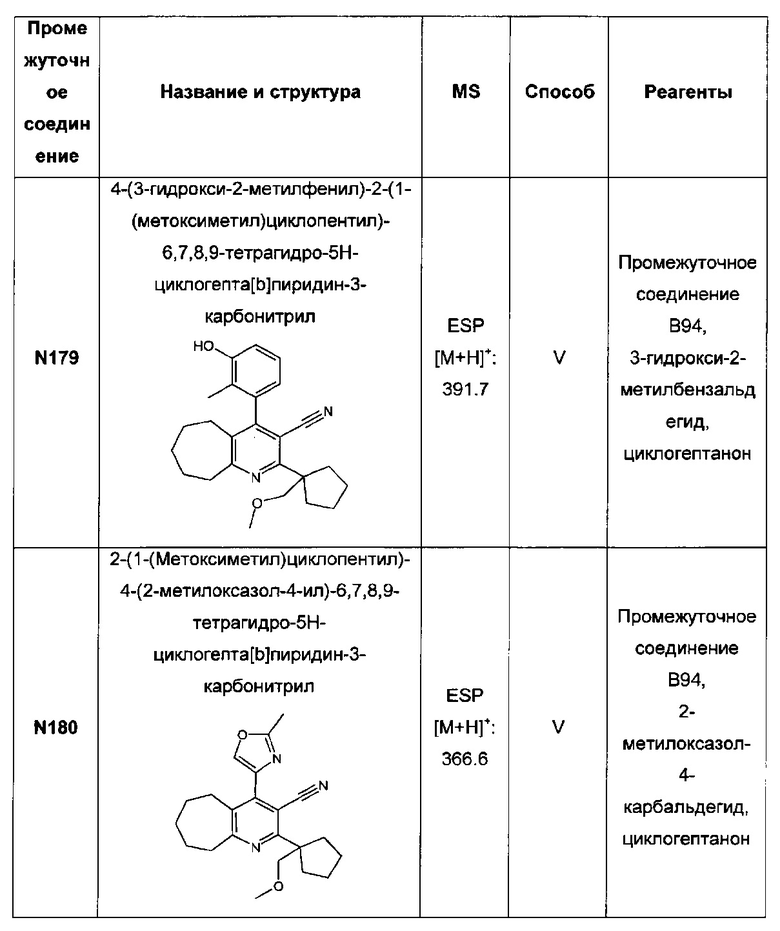

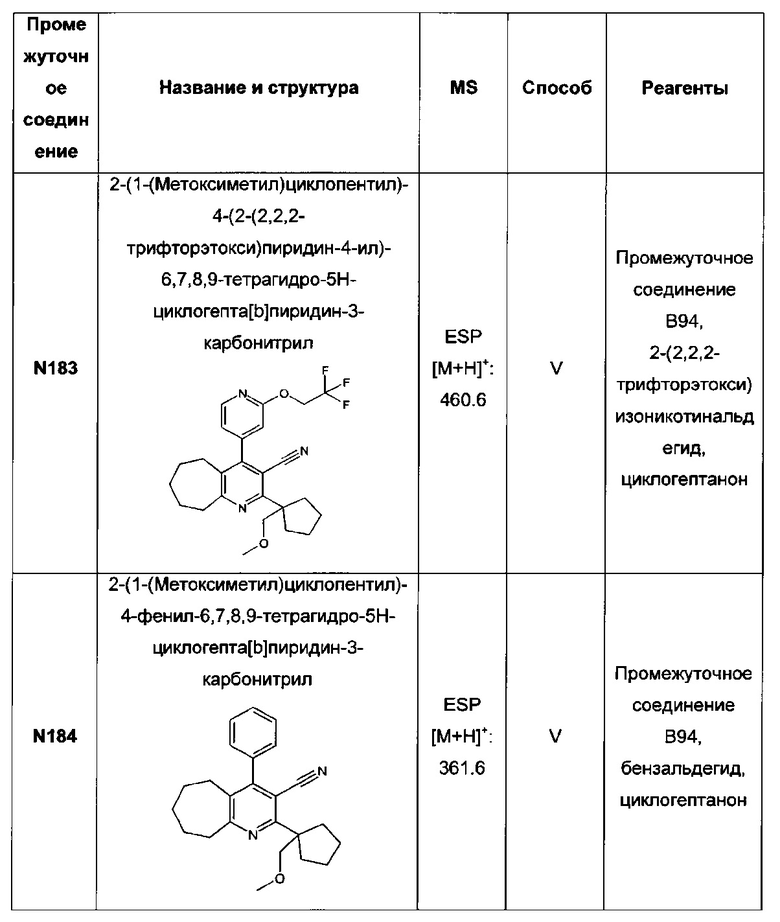


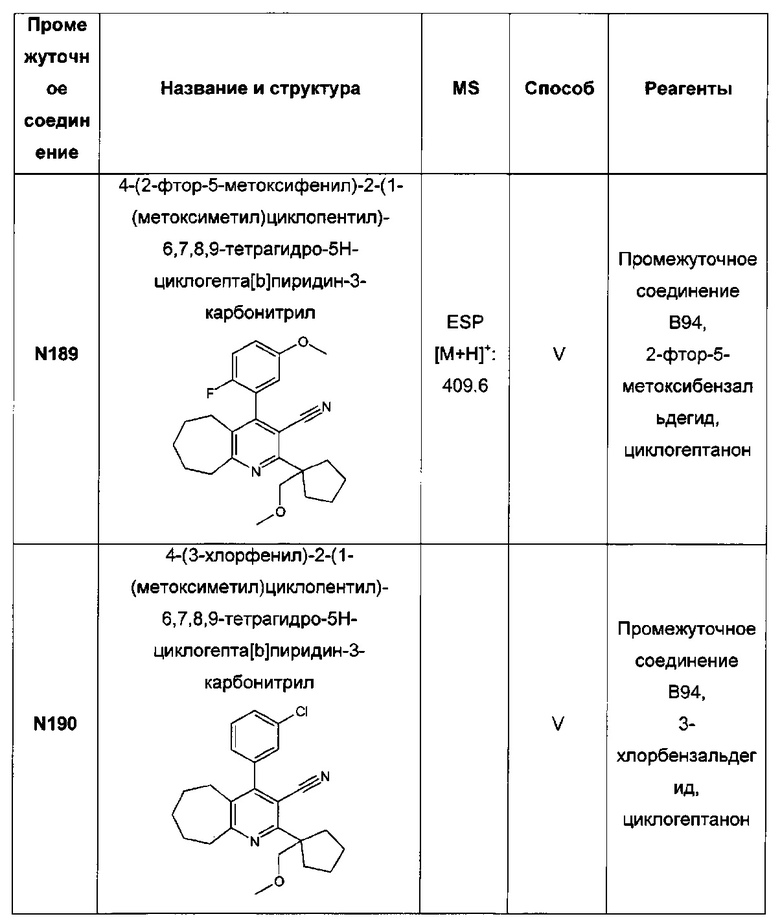







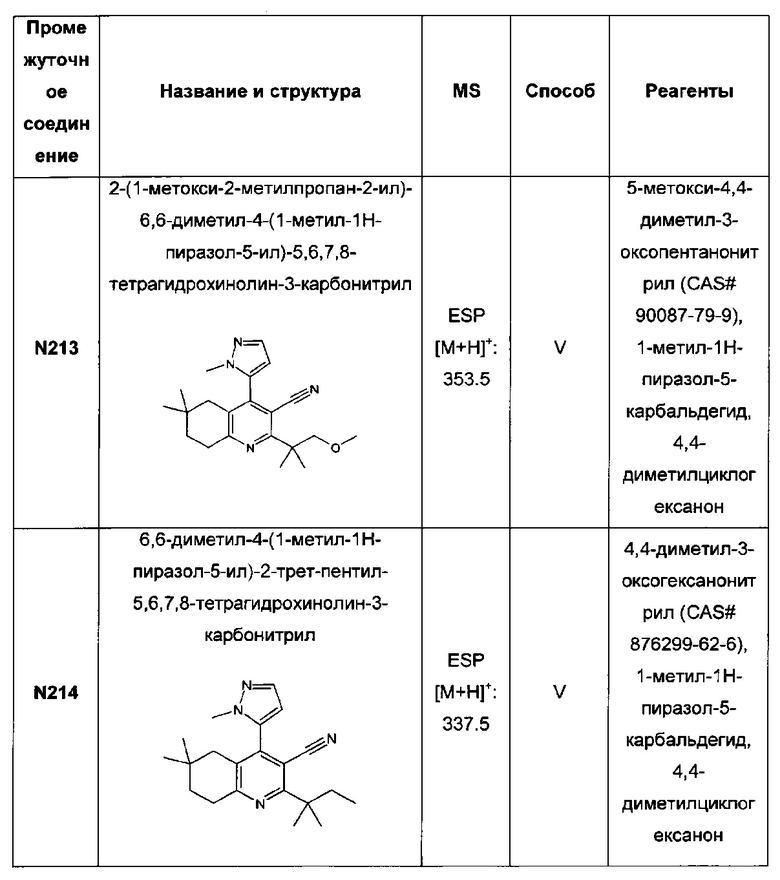
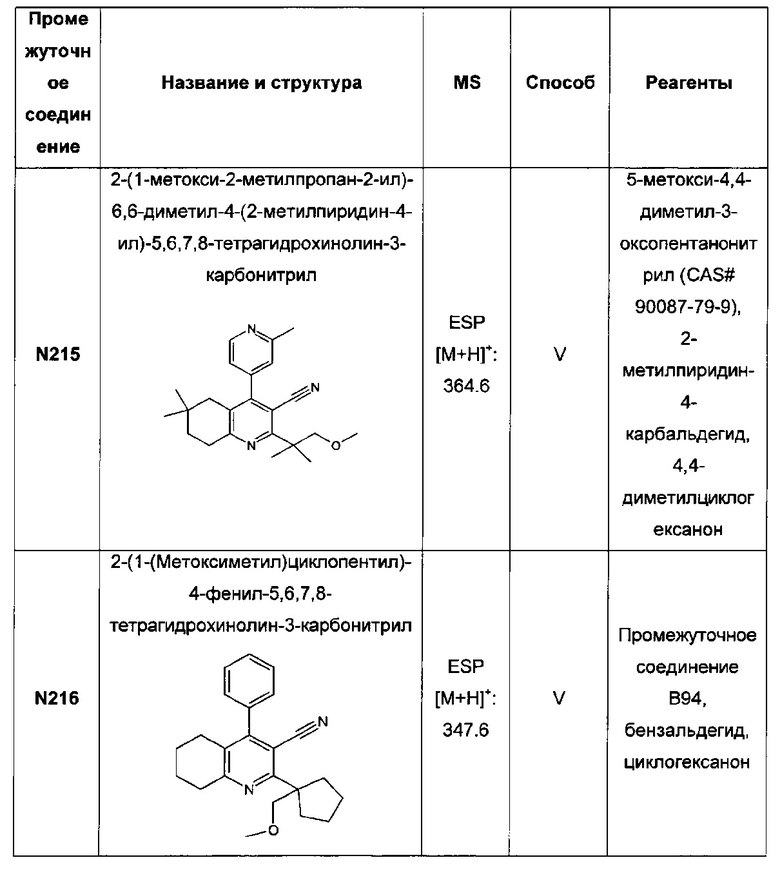



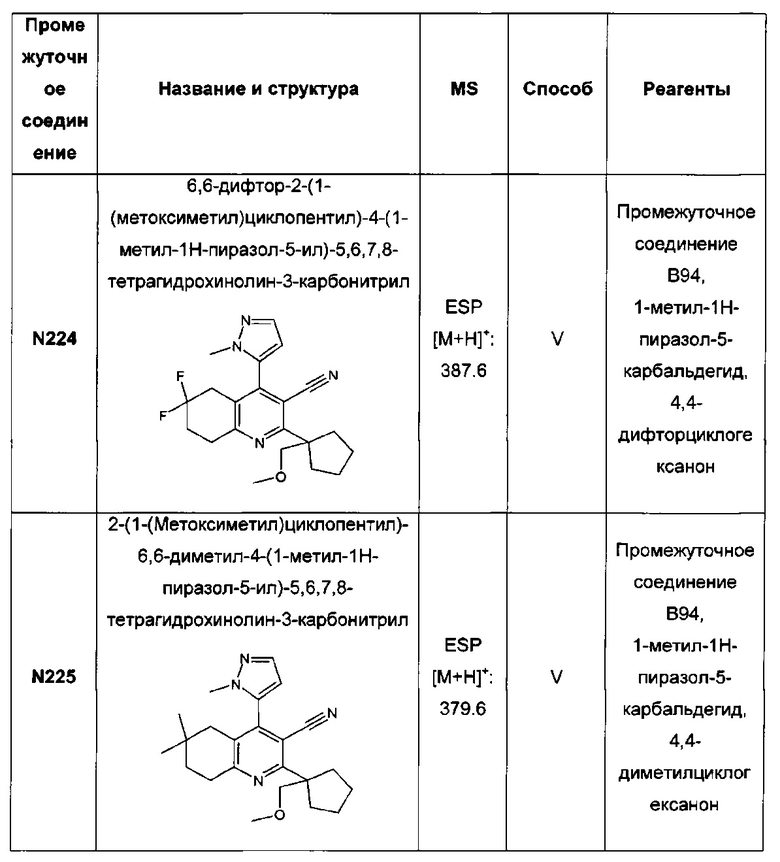

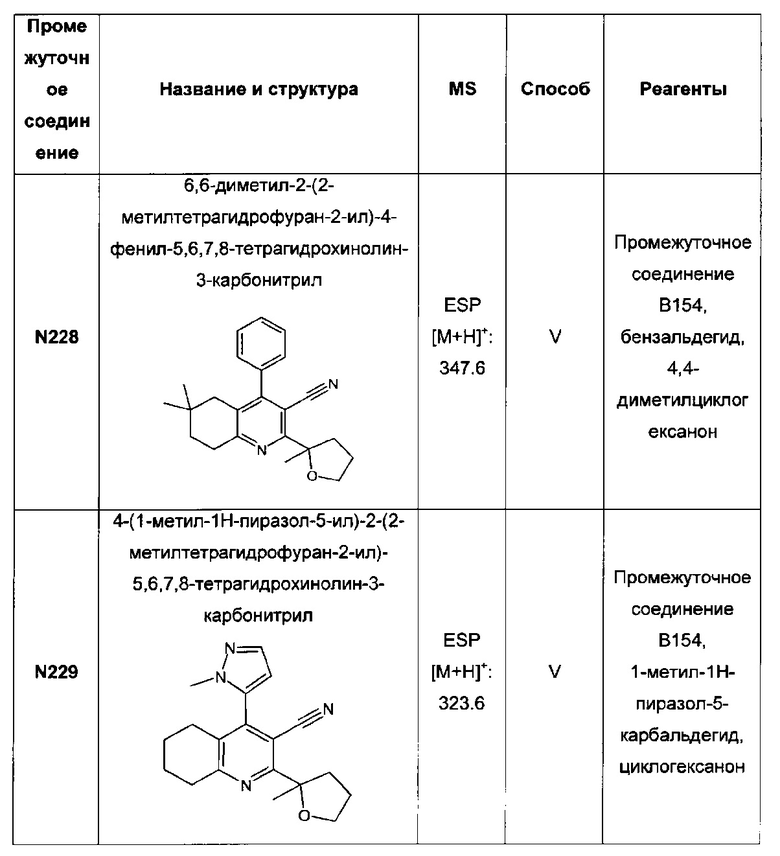







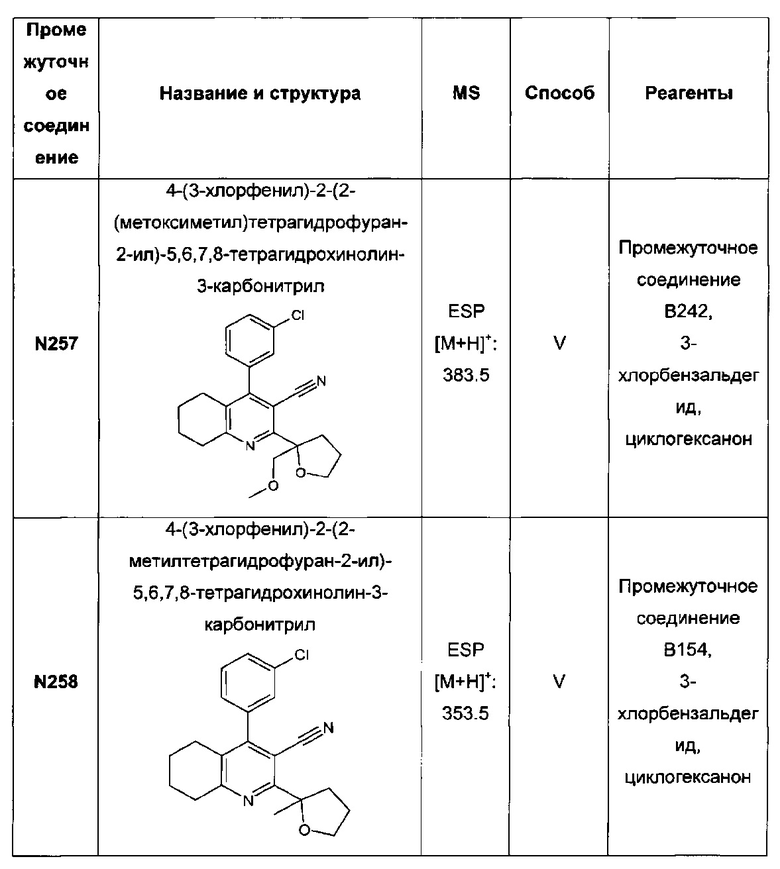

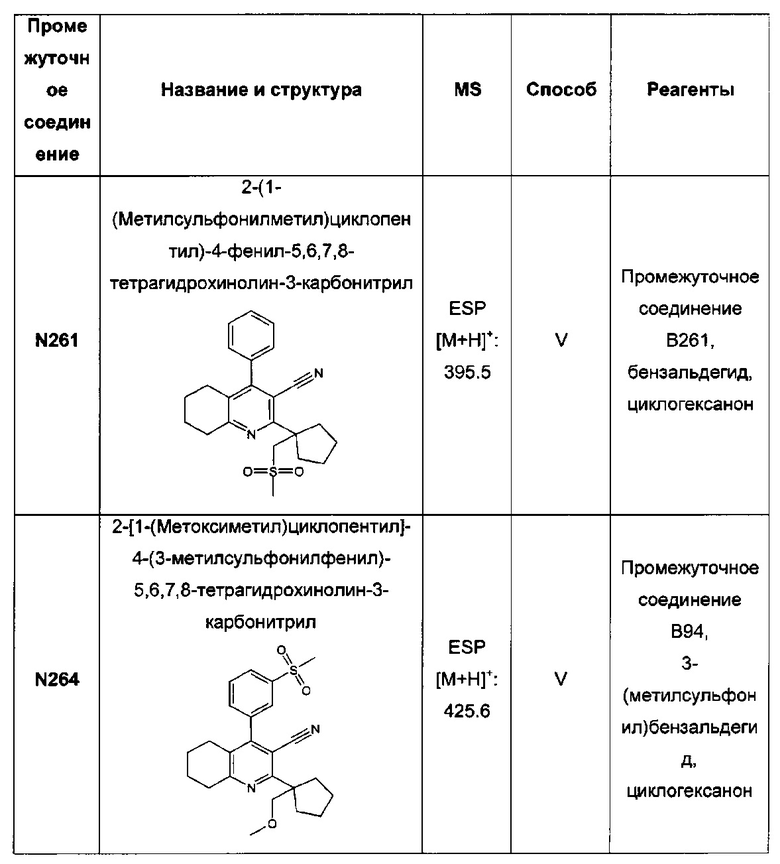

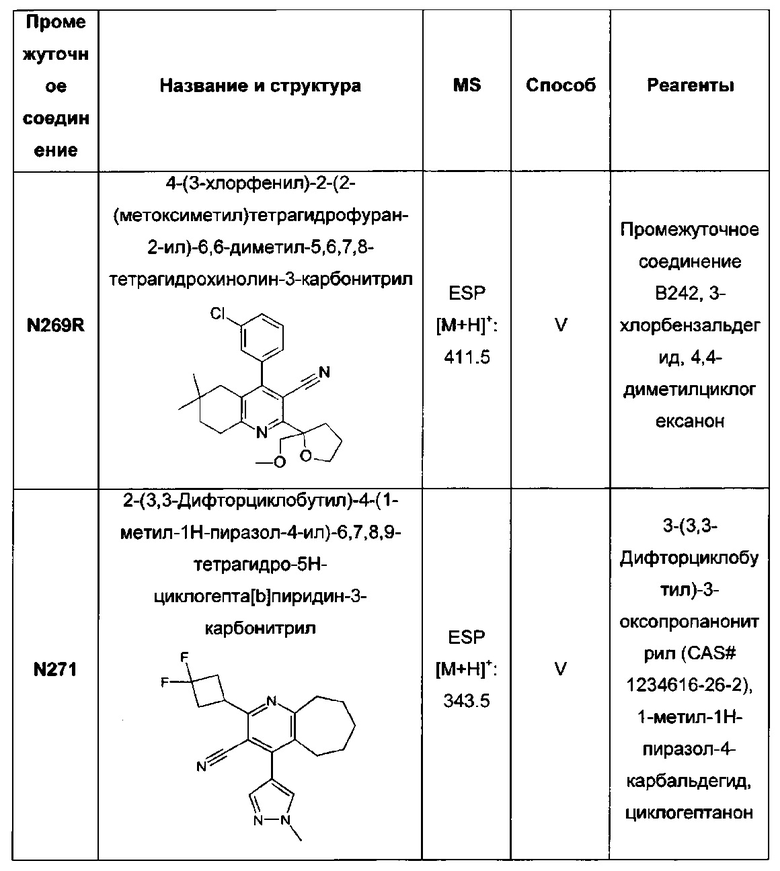






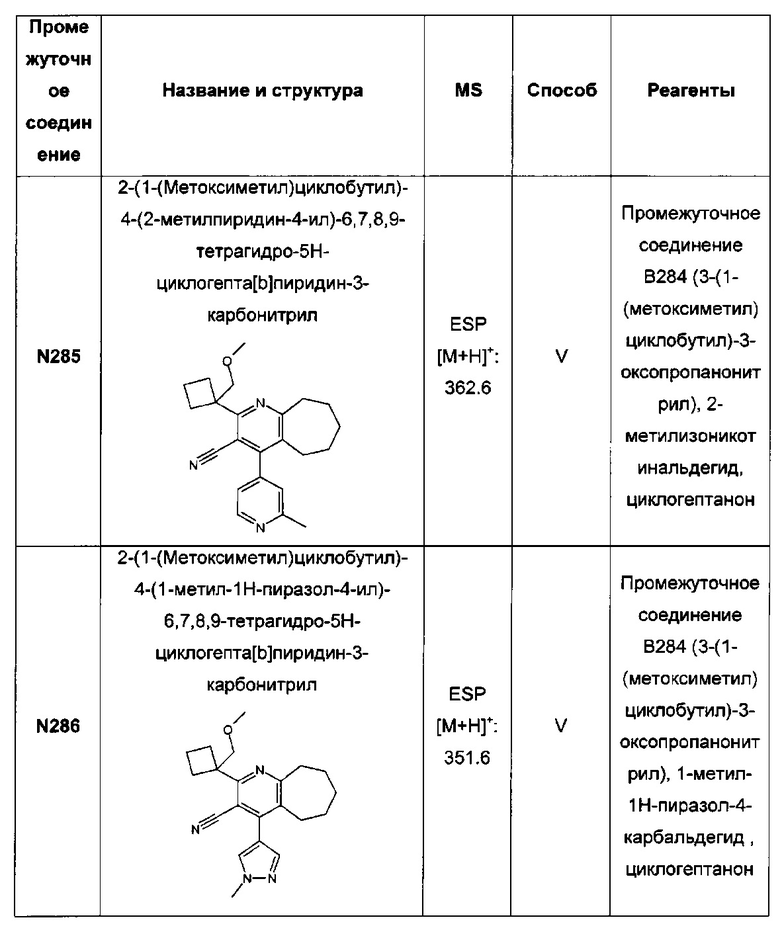






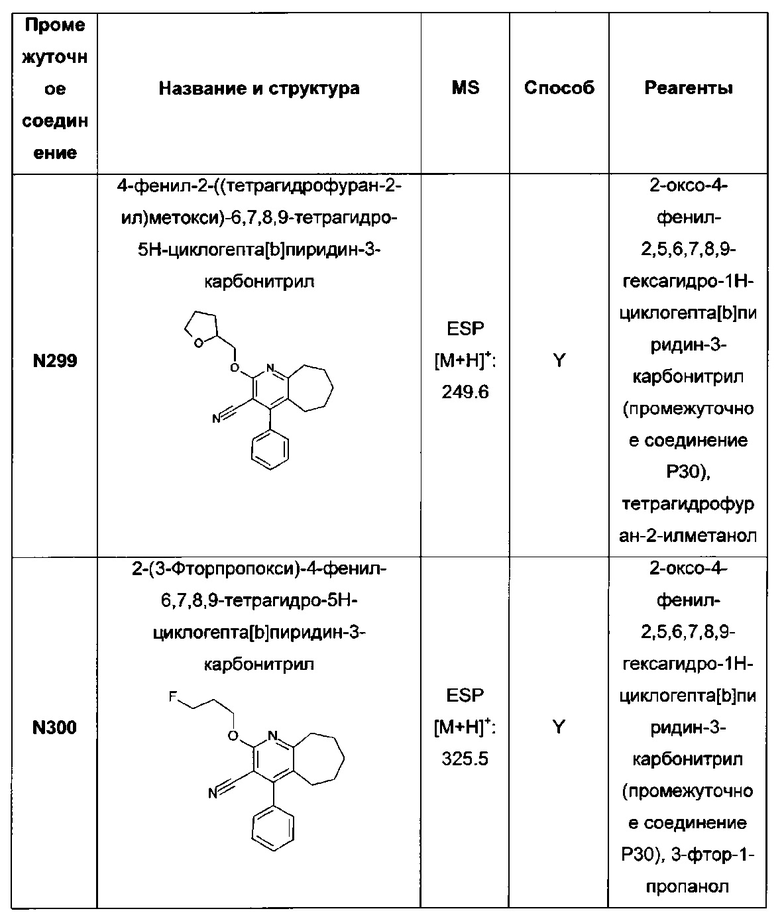

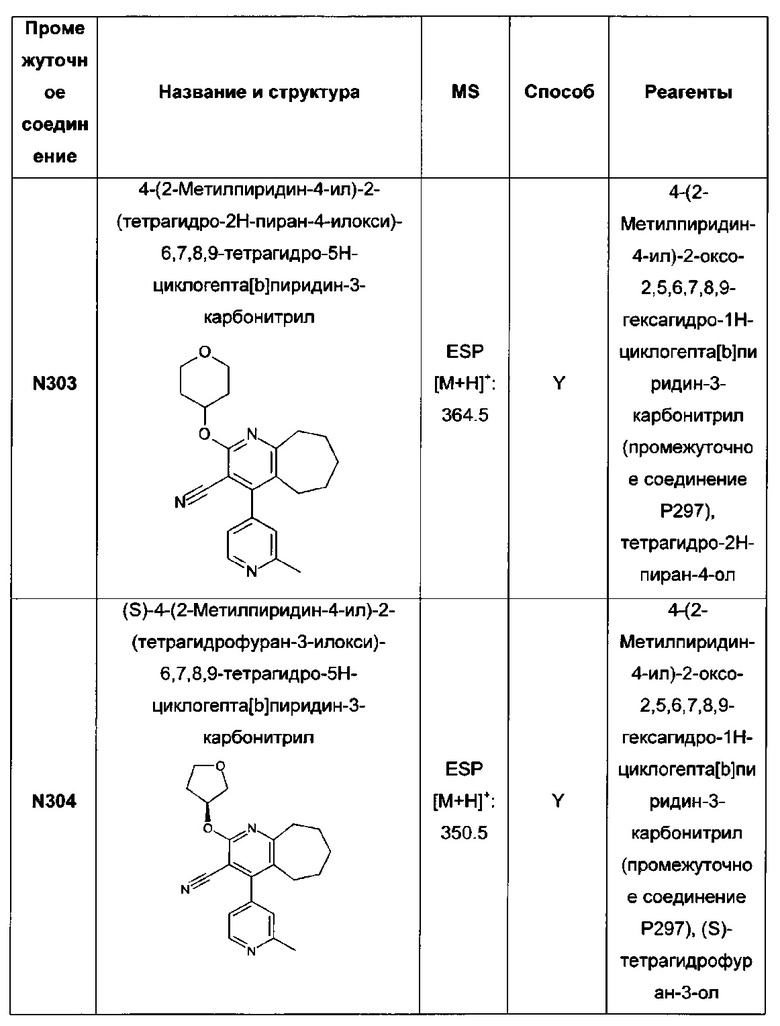
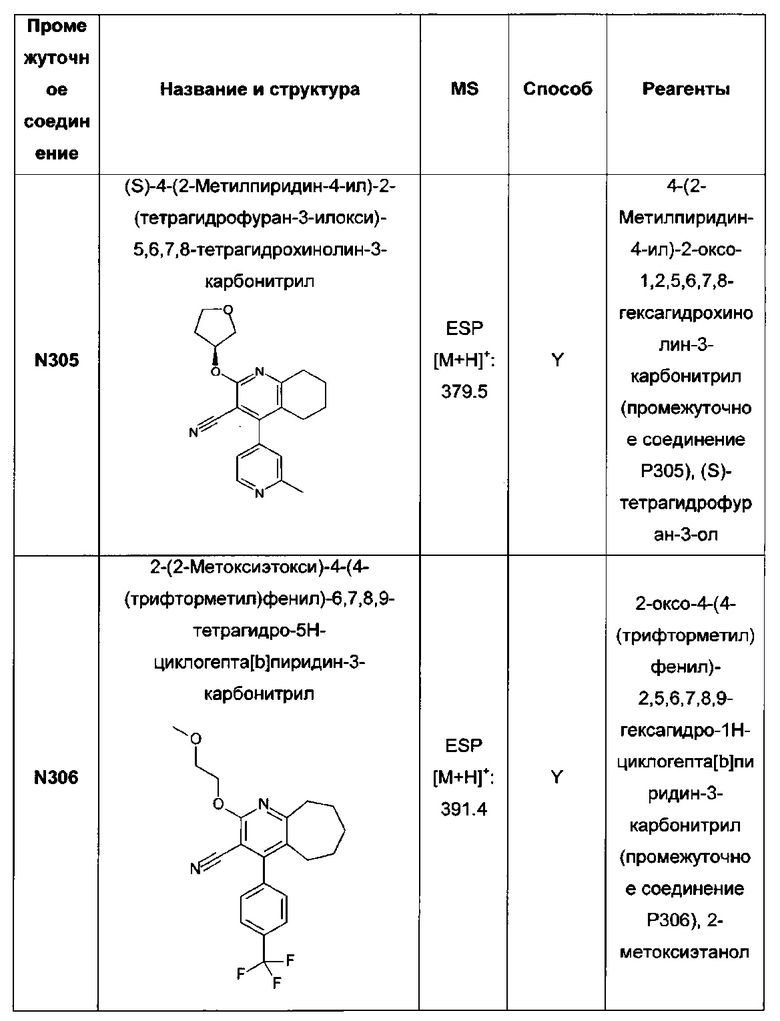


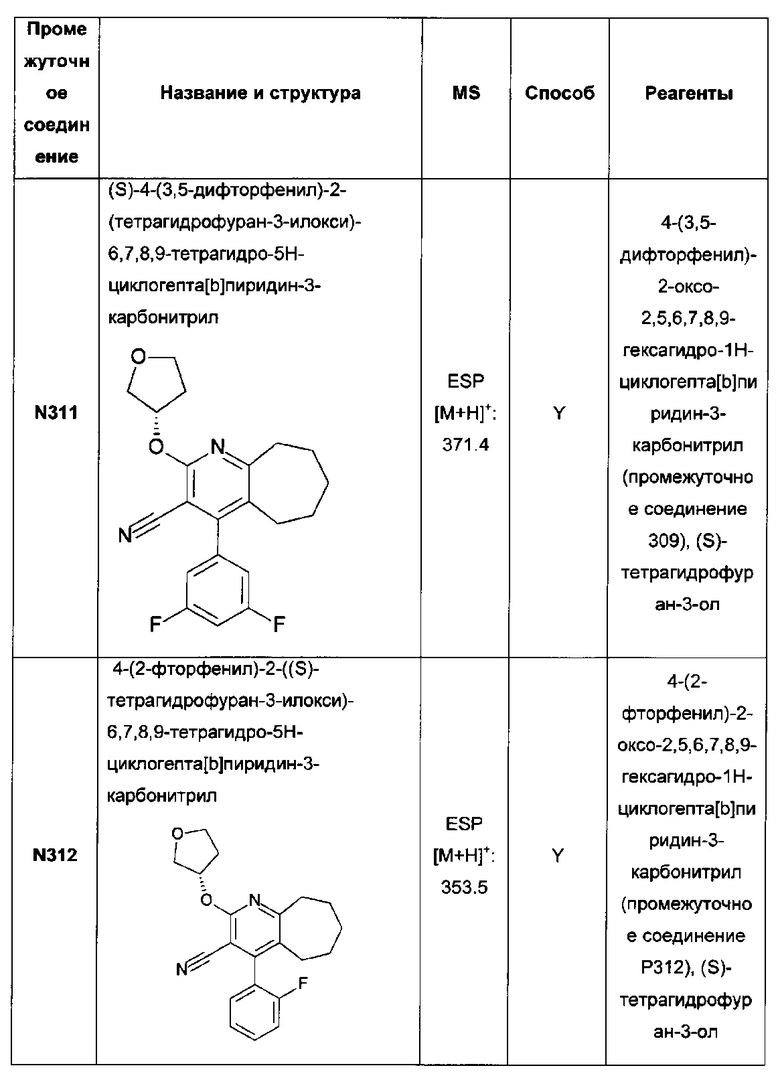





Промежуточные соединения N149 и N150
(R)-4-(2-хлорпиридин-4-ил)-2-(тетрагидрофуран-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил и (S)-4-(2-хлорпиридин-4-ил)-2-(тетрагидрофуран-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил

Промежуточное соединение N149R разделили на энантиомеры с использованием хиральной хроматографии (Chiralpak AD, изопропанол/гептан 1:9) с получением соединений, указанных в заголовках в виде серо-белых осадков. N149 Элюируемый первым энантиомер (+), ESP [М+Н]+: 354.5 N150 Элюируемый вторым энантиомер (-), ESP [М+Н]+: 354.5
Промежуточные соединения N161 и N162
2-[(2S)-2-метилоксолан-2-ил]-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил и 2-[(2R)-2-метилоксолан-2-ил]-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил

Промежуточное соединение N160 разделили на энантиомеры с использованием хиральной хроматографии (Reprosil Chiral NR, 15% EtOH в гептане) с получением соединений, указанных в заголовках в виде светло-желтых осадков. N161 Элюируемый первым энантиомер (-), ESP [М+Н]+: 348.5 N162 Элюируемый вторым энантиомер (+), ESP [М+Н]+: 348.5
Промежуточное соединение N194
2-циклопентил-4-(2-(метиламино)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил
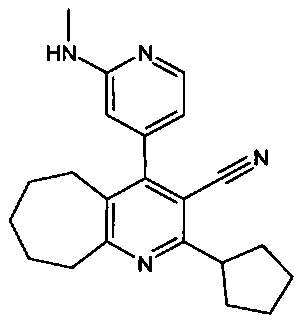
4-(2-хлорпиридин-4-ил)-2-циклопентил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил (промежуточное соединение N103, 209 мг) и метиламин (8М в этаноле, 5 мл) перемешивали 18 ч в автоклаве из нержавеющей стали при 150°С. Реакционную смесь эвапорировали и очистили посредством хроматографии (SiO2, 0-50% EtOAc в гептане) с получением соединения, указанного в заголовке (66 мг), в виде светло-желтого осадка. ESP [М+Н]+: 347.6
Промежуточное соединение N205
2-[1-(гидроксиметил)циклопентил]-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил
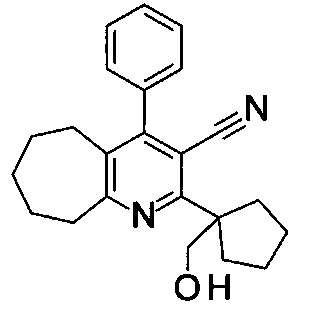
2-(1-(Метоксиметил)циклопентил)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил (промежуточное соединение N184, 200 мг) объединили с ацетонитрилом (2.5 мл) с получением бесцветного раствора. Затем добавили суспензию йодида натрия (166 мг) в ацетонитриле (2.5 мл) и триметилхлорсилан (121 мг) при КТ. После перемешивания при КТ. в течение 1.5 ч, смесь перемешивали в течение 33 ч при 60°С и в течение 17 дней при КТ. За это время дважды добавили дополнительное количество триметилхлорсилана (121 мг) и йодида натрия (166 мг). 5 г силикагеля добавили и реакционную смесь эвапорировали. Неочищенное вещество очистили с помощью флеш-хроматографии (силикагель, 0% - 50% EtOAc в н-гептане) с последующей препаративной ТСХ (силикагель, 2.0 мм, 1:1 н-гептан/AcOEt) с получением соединения, указанного в заголовке (не полностью чистого) в виде светло-коричневой пены (114 мг), которую использовали на следующей стадии без дополнительной очистки. ESP [М+Н]+: 347.6
Промежуточное соединение N212
2-циклопентил-9-оксо-4-фенил-6,7,8,9-тетрагидро-5Н-пиридо[2,3-c]азепин-3-карбонитрил

3-(пиперидин-1-ил)-6,7-дигидро-1Н-азепин-2(5Н)-он (3 г), бензальдегид (1.64 г), 3-циклопентил-3-оксопропанонитрил (2.12 г) и ацетат аммония (5.95 г) смешали с толуоломм (45.0 мл) и кипятили с обратным холодильником в течение 90 мин с удалением воды с использованием насадки Дина-Старка. Реакционную смесь эвапорировали. Оставшийся коричневый полутвердый осадок суспендировали в ацетоне (75.0 мл). После медленного добавления раствора церий аммоний нитрата (16.9 г) в воде (30.0 мл), реакционную смесь перемешивали 30 мин при КТ. Реакционную смесь разбавили водой и этилацетатом и разделили, экстрагировали еще раз этилацетатом. Органические слои промыли один раз водой, высушили над сульфатом натрия и эвапорировали. Оставшуюся красно-коричневую смолу очистили посредством хроматографии (SiO2, 0-100% EtOAc в гептане) с последующим тритурированием с изопропиловым эфиром с получением соединения, указанного в заголовке (1.25 г), в виде серо-белого осадка. ESP [М+Н]+: 332.6
В качестве побочного продукта получили 2-циклопентил-5-оксо-4-фенил-6,7,8,9-тетрагидро-5Н-пиридо[3,2-с]азепин-3-карбонитрил (1.04 г).
Промежуточные соединения N269 и N270
(R)-4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-5,6,7,8-тетрагидрохинолин-3-карбонитрил и (S)-4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-5,6,7,8-тетрагидрохинолин-3-карбонитрил
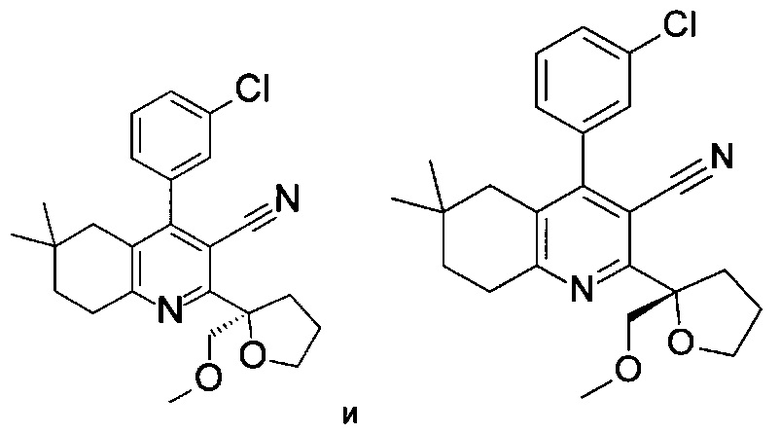
Промежуточное соединение N269R разделили на энантиомеры с использованием хиральной хроматографии (Reprosil Chiral NR, 10% EtOH в гептане) с получением соединений, указанных в заголовках в виде бесцветных осадков. N269 Элюируемый первым энантиомер (-), ESP [М+Н]+: 411.5 N270 Элюируемый вторым энантиомер (+), ESP [М+Н]+: 411.5
Пример А
Соединение формулы (I) может быть использовано самостоятельно в качестве активного ингредиента для производства таблеток следующего состава:


Пример В
Соединение формулы (I) может быть использовано самостоятельно в качестве активного ингредиента для производства капсул следующего состава:

| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРИДАЗИНА | 2006 |
|
RU2401832C2 |
| СЕЛЕКТИВНЫЕ АНТАГОНИСТЫ Н4-ГИСТАМИНОВЫХ РЕЦЕПТОРОВ ДЛЯ ЛЕЧЕНИЯ ВЕСТИБУЛЯРНЫХ НАРУШЕНИЙ | 2009 |
|
RU2589846C2 |
| ИНГИБИТОРЫ Axl ДЛЯ ПРИМЕНЕНИЯ В КОМБИНИРОВАННОЙ ТЕРАПИИ ДЛЯ ПРЕДОТВРАЩЕНИЯ, УСТРАНЕНИЯ ИЛИ ЛЕЧЕНИЯ МЕТАСТAЗИРУЮЩЕГО РАКА | 2010 |
|
RU2555326C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ТИОФЕНИЛАМИДА | 2013 |
|
RU2644565C2 |
| АЦИЛИРОВАННЫЕ ГЕТЕРОАРИЛКОНДЕНСИРОВАННЫЕ ЦИКЛОАЛКЕНИЛАМИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2003 |
|
RU2338743C2 |
| СПОСОБЫ АКТИВАЦИИ КЛЕТОК-ПРЕДШЕСТВЕННИКОВ/СТВОЛОВЫХ КЛЕТОК | 2002 |
|
RU2309741C2 |
| ПРОТИВОВИРУСНЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИЧ-ИНФЕКЦИИ | 2020 |
|
RU2780101C2 |
| ПРОТИВОВИРУСНЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИЧ ИНФЕКЦИИ | 2021 |
|
RU2780103C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ РАЦЕМИЧЕСКОГО АМИНОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОХИНОЛИНА ИЛИ РАЦЕМИЧЕСКОГО АМИНОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОИЗОХИНОЛИНА, СПОСОБЫ ИХ РАЗДЕЛЕНИЯ И РАЦЕМИЗАЦИИ, СПОСОБ ПОЛУЧЕНИЯ КЕТОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОХИНОЛИНА ИЛИ КЕТОЗАМЕЩЕННОГО 5,6,7,8-ТЕТРАГИДРОИЗОХИНОЛИНА, СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРА КОНДЕНСИРОВАННОГО БИЦИКЛИЧЕСКОГО КОЛЬЦА, ЗАМЕЩЕННОГО ПЕРВИЧНЫМ АМИНОМ, ПРОИЗВОДНЫЕ 5,6,7,8-ТЕТРАГИДРОХИНОЛИНА | 2002 |
|
RU2308451C2 |
| НОВОЕ ПРОИЗВОДНОЕ ГЕТЕРОЦИКЛИДЕН АЦЕТАМИДА | 2006 |
|
RU2451014C2 |
Изобретение относится к области органической химии, а именно к гетероциклическому соединению формулы (I) или к его фармацевтически приемлемой соли, где R1 представляет собой С1-6-алкил, С3-6-циклоалкил, замещенный С3-6-циклоалкил, С1-4-алкокси, С1-4-алкокси-С1-6-алкил, С1-4-алкокси-С1-4-алкокси, С1-6-алкоксикарбонил-С1-6-алкил, карбокси-С1-4-алкил, С1-4-галоалкил, С1-4-галоалкокси, замещенный фенил, 5-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, замещенный 4-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, тетрагидрофуран-С1-4-алкокси, тетрагидрофуранилокси, тетрагидропиранилокси, фуран, замещенный 5-6-членный гетероарил, содержащий 1-2 гетероатома, выбранных из N, амино, замещенный амино, где замещенный циклоалкил, замещенный фенил, замещенный гетероциклоалкил и замещенный гетероарил замещены одним-двумя заместителями, независимо выбранными из галогена, С1-6-алкила, С1-4-галоалкила, С1-4-гидроксиалкила, С1-4-алкилсульфонил-С1-4-алкила, С1-4-алкоксикарбонила, С1-4-алкокси и С1-4-алкокси-С1-4-алкила, и где замещенный амино замещен по атому азота одним - двумя заместителями, независимо выбранными из С1-4-алкила; R2 представляет собой -СООН, тетразол-5-ил, [1,3,4]оксадиазол-2-тион-5-ил; R3 представляет собой фенил, замещенный фенил, замещенный дигидропиридинил, 5-9-членный моно или бициклический гетероарил, содержащий 1-3 гетероатома, выбранных из N, S и О, или замещенный 5-6-членный гетероарил, содержащий 1-2 гетероатома, выбранных из N, S и О, где замещенный фенил, замещенный дигидропиридинил и замещенный гетероарил замещены одним-двумя заместителями, независимо выбранными из гидрокси, оксо, галогена, С1-6-алкила, С3-6-циклоалкила, С1-4-галоалкила, С1-4-галоалкокси, гидрокси-С1-4-алкокси, С1-4-алкокси, С1-4-алкилсульфонила, амино, замещенного по атому азота С1-4-алкилом; А1 представляет собой связь; А2 представляет собой -CR14R15-, -NR16-, -О-, -S-; А3 представляет собой -CR17R18-, -C(О)NR19-, -NR19-; R4, R5, R6, R7, R8, R9, R10, R11, R14, R15, R17 и R18 независимо выбраны из H, галогена, С1-6-алкила, С1-4-алкокси и С1-4-галоалкила; R16 и R19 независимо выбраны из водорода, С1-4-алкила, С1-4-галоалкила и С1-4-алкилкарбонила; n, m и р независимо выбраны из 0 и 1. Также изобретение относится к конкретным соединениям, фармацевтической композиции на их основе и их применению. Технический результат: получены новые гетероциклические соединения, полезные для лечения или профилактики заболеваний, при которых полезно ингибирование белков, связывающих жирные кислоты (FABP) 4 и/или 5. 8 н. и 24 з.п. ф-лы, 329 пр.

1. Соединения формулы (I)

где
R1 представляет собой С1-6-алкил, С3-6-циклоалкил, замещенный С3-6-циклоалкил, С1-4-алкокси, С1-4-алкокси-С1-6-алкил, С1-4-алкокси-С1-4-алкокси, С1-6-алкоксикарбонил-С1-6-алкил, карбокси-С1-4-алкил, С1-4-галоалкил, С1-4-галоалкокси, замещенный фенил, 5-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, замещенный 4-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, тетрагидрофуран-С1-4-алкокси, тетрагидрофуранилокси, тетрагидропиранилокси, фуран, замещенный 5-6-членный гетероарил, содержащий 1-2 гетероатома, выбранных из N, амино, замещенный амино, где замещенный циклоалкил, замещенный фенил, замещенный гетероциклоалкил и замещенный гетероарил замещены одним-двумя заместителями, независимо выбранными из галогена, С1-6-алкила, С1-4-галоалкила, С1-4-гидроксиалкила, С1-4-алкилсульфонил-С1-4-алкила, С1-4-алкоксикарбонила, С1-4-алкокси и С1-4-алкокси-С1-4-алкила, и где замещенный амино замещен по атому азота одним-двумя заместителями, независимо выбранными из С1-4-алкила;
R2 представляет собой -СООН, тетразол-5-ил, [1,3,4]оксадиазол-2-тион-5-ил;
R3 представляет собой фенил, замещенный фенил, замещенный дигидропиридинил, 5-9-членный моно или бициклический гетероарил, содержащий 1-3 гетероатома, выбранных из N, S и О, или замещенный 5-6-членный гетероарил, содержащий 1-2 гетероатома, выбранных из N, S и О, где замещенный фенил, замещенный дигидропиридинил и замещенный гетероарил замещены одним-двумя заместителями, независимо выбранными из гидрокси, оксо, галогена, С1-6-алкила, С3-6-циклоалкила, С1-4-галоалкила, С1-4-галоалкокси, гидрокси-С1-4-алкокси, С1-4-алкокси, С1-4-алкилсульфонила, амино, замещенного по атому азота С1-4-алкилом;
А1 представляет собой связь;
А2 представляет собой -CR14R15-, -NR16-, -О-, -S-;
А3 представляет собой -CR17R18-, -C(O)NR19-, -NR19-;
R4, R5, R6, R7, R8, R9, R10, R11, R14, R15, R17 и R18 независимо выбраны из H, галогена, С1-6-алкила, С1-4-алкокси и С1-4-галоалкила;
R16 и R19 независимо выбраны из водорода, С1-4-алкила, С1-4-галоалкила и С1-4-алкилкарбонила;
n, m и р независимо выбраны из 0 и 1;
или их фармацевтически приемлемые соли.
2. Соединение по п.1, где R1 представляет собой С1-6-алкил, С3-6-циклоалкил, замещенный С3-6-циклоалкил, С1-4-алкокси, С1-4-алкокси-С1-6-алкил, С1-4-алкокси-С1-4-алкокси, С1-6-алкоксикарбонил-С1-6-алкил, карбокси-С1-4-алкил, С1-4-галоалкил, С1-4-галоалкокси, замещенный фенил, 5-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, замещенный 4-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, тетрагидрофуран-С1-4-алкокси, тетрагидрофуранилокси, тетрагидропиранилокси, фуран, замещенный 5-6-членный гетероарил, содержащий 1-2 гетероатома, выбранных из N, амино или замещенный амино, где замещенный циклоалкил, замещенный фенил, замещенный гетероциклоалкил и замещенный гетероарил замещены одним-двумя заместителями, независимо выбранными из галогена, С1-6-алкила, С1-4-галоалкила, С1-4-гидроксиалкила, С1-4-алкилсульфонил-С1-4-алкила, С1-4-алкоксикарбонила и С1-4-алкокси-С1-4-алкила, и где замещенный амино замещен по атому азота двумя С1-4-алкилами.
3. Соединение по п.1, где R1 представляет собой С3-6-циклоалкил, замещенный С3-6-циклоалкил, 5-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, замещенный 4-6-членный гетероциклоалкил, содержащий 1 гетероатом, выбранный из N и О, или замещенный амино, где замещенный циклоалкил и замещенный гетероциклоалкил замещены одним С1-6-алкилом или С1-4-алкокси-С1-4-алкилом и где замещенный амино замещен по атому азота двумя С1-4-алкилами.
4. Соединение по п.1, где R1 представляет собой циклопентил, замещенный циклопентил, тетрагидрофуранил, замещенный тетрагидрофуранил, тетрагидрофуранилокси, пиперидинил или замещенный амино, где замещенный циклопентил и замещенный тетрагидрофуранил замещены одним С1-4-алкилом или С1-4-алкокси-С1-4-алкилом и где замещенный амино замещен по атому азота двумя С1-4-алкилами.
5. Соединение по п.1, где R2 представляет собой -СООН.
6. Соединение по п.1, где R2 представляет собой тетразол-5-ил.
7. Соединение по п.1, где R3 представляет собой фенил, замещенный фенил, замещенный дигидропиридинил, 5-9-членный моно или бициклический гетероарил, содержащий 1-3 гетероатома, выбранных из N, S и О, или замещенный 5-6-членный гетероарил, содержащий 1-2 гетероатома, выбранных из N, S и О, где замещенный фенил, замещенный дигидропиридинил и замещенный гетероарил замещены одним-двумя заместителями, независимо выбранными из гидрокси, оксо, галогена, С1-6-алкила, С3-6-циклоалкила, С1-4-галоалкила, С1-4-галоалкокси, гидрокси С1-4-алкокси, С1-4-алкокси, С1-4-алкилсульфонила и амино, замещенного по атому азота С1-4-алкилом.
8. Соединение по п.1, где R3 представляет собой фенил, замещенный фенил или замещенный 5-6-членный гетероарил, содержащий 1-2 гетероатома, выбранных из N, S и О, где замещенный фенил и замещенный гетероарил замещены одним-двумя заместителями, независимо выбранными из галогена и С1-6-алкила.
9. Соединение по п.1, где R3 представляет собой фенил, замещенный фенил, замещенный пиразолил или замещенный пиридинил, где замещенный фенил, замещенный пиразолил и замещенный пиридинил замещены одним-двумя заместителями, независимо выбранными из галогена и С1-6-алкила.
10. Соединение по п.1, где R3 представляет собой замещенный пиразолил или замещенный пиридинил, где замещенный пиразолил и замещенный пиридинил замещены одним С1-6-алкилом.
11. Соединение по п.1, где R3 представляет собой пиридинил, замещенный одним С1-6-алкилом или галогеном.
12. Соединение по п.1, где А1 представляет собой связь.
13. Соединение по п.1, где А2 представляет собой -CR14R15-, -NR16-, -О- и -S-.
14. Соединение по п.1, где А2 представляет собой -CR14R15.
15. Соединение по п.1, где А3 представляет собой -CR17R18-, -C(O)NR19 или -NR19.
16. Соединение по п.1, где А3 представляет собой -CR17R18-.
17. Соединение по п.1, где n представляет собой 1.
18. Соединение по п.1, где р представляет собой 0.
19. Соединение по п.1, где R4, R5, R6, R7, R8, R9, R10 и R11 представляют собой Н.
20. Соединение по п.1, где R14 и R15 независимо выбраны из Н, галогена и С1-6-алкила.
21. Соединение по п.1, где R17 и R18 независимо выбраны из Н и С1-6-алкила.
22. Соединение по п.1, где R16 представляет собой С1-4-галоалкил или С1-4-алкилкарбонил.
23. Соединение по п.1, где R19 представляет собой С1-4-алкил или С1-4-алкилкарбонил.
24. Соединение, выбранное из:
2-изопропил-6,8-диметил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
8-ацетил-2-изопропил-6-метил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
8-этил-2-изопропил-6-метил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
4-(3-хлорфенил)-2-циклогексил-8-этил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклогексил-8-этил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклопентил-8-этил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклопентил-8-этил-6-метил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-циклопентил-6,8-диметил-4-фенил-5,6,7,8-тетрагидро-1,8-нафтиридин-3-карбоновая кислота;
2-изопропил-6-метил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
6-этил-2-изопропил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-изопропил-6,6-диметил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-циклопентил-4-(6-метоксипиридин-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклопентил-4-(6-оксо-1,6-дигидропиридин-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
4-фенил-2-(пиперидин-1-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-(2-метилпирролидин-1-ил)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
6-метил-4-фенил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-(диэтиламино)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
6-метил-2-(2-метилпирролидин-1-ил)-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-(диэтиламино)-6-метил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
4-(3-хлорфенил)-6-метил-2-(пирролидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
4-фенил-2-(пиперидин-1-ил)-6,7-дигидро-5Н-циклопента[b]пиридин-3-карбоновая кислота;
2-(диэтиламино)-4-фенил-6,7-дигидро-5Н-циклопента[b]пиридин-3-карбоновая кислота;
4-(3-хлорфенил)-6-метил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
5-(6-метил-4-фенил-2-(пиперидин-1-ил)-5,6,7,8-тетрагидрохинолин-3-ил)-1,3,4-оксадиазол-2(3Н)-тион;
6-метил-4-фенил-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
N,N-диэтил-6-метил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин-2-амин;
4-фенил-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
N,N-диэтил-4-фенил-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин-2-амин;
6-метил-4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-фенил-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-фенил-3-(2Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(3-хлорфенил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлорфенил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(4-фторфенил)-6-метил-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(4-фторфенил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-7,8-дигидро-5Н-пирано[4,3-b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилпирролидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(5-хлортиофен-2-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
5-метил-3-(2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)изоксазол;
N,N-диэтил-4-(5-метилизоксазол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
2-(пиперидин-1-ил)-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(5-метилфуран-2-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(5-метилфуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(1,5-диметил-1Н-пиразол-4-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1,5-диметил-1Н-пиразол-4-ил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-(5-хлортиофен-2-ил)-2-(3-фторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(3,3-дифторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(4,4-дифторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(4-фторпиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-3-(1Н-тетразол-5-ил)-2-(4-(трифторметил)пиперидин-1-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(5-хлортиофен-2-ил)-2-(3,3-дифторазетидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
N,N-диэтил-4-(4-метилтиазол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-метил-5-(2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)тиазол;
N,N-диэтил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин-2-амин;
4-(5-хлортиофен-2-ил)-2-(3,3-дифторпирролидин-1-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
диэтил-[4-пиримидин-5-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил]-амин;
N,N-диэтил-4-(3-фторпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
N,N-диэтил-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
2-пропил-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пентан-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлорфенил)-2-циклобутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-пиридин-4-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-Н-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-Н-циклогепта[b]пиридин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
5-(2-циклогексил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)пиридин-2(1Н)-он;
5-(2-циклогексил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-1-этилпиридин-2(1Н)-он;
5-(2-циклогексил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-1-метилпиридин-2(1Н)-он;
2-циклогексил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
1-(4-(3-хлорфенил)-2-циклобутил-3-(1Н-тетразол-5-ил)-7,8-дигидро-1,6-нафтиридин-6(5Н)-ил)этанон;
2-циклопентил-4-(6-метоксипиридин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидро-2Н-пиран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-(3-фторпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(3-фторпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидро-2Н-пиран-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклогексил-4-(2-метилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
5-(2-циклобутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-1-метилпиридин-2(1Н)-он;
2-циклогексил-4-(пиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-метилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиридазин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(6-метилпиридин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиридин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропил-4-(2-изопропилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(пиримидин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(2-(2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)фенокси)этанол;
2-циклопентил-4-(2-изопропилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропил-4-(2-изопропилпиримидин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-изопропилпиридин-4-ил)-2-(пентан-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(пентан-3-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-6-метил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6,6-дифтор-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-циклогексил-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин-4-ил)-3,5-диметилизоксазол;
4-(2-циклогексил-6-метил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин-4-ил)-3,5-диметилизоксазол;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6-(трифторметил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-фенил-3-(2Н-тетразол-5-ил)-6-(2,2,2-трифторэтил)-5,6,7,8-тетрагидро-1,6-нафтиридин;
2-циклопентил-6,6-диметил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6-метокси-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6-метил-4-(2-метилпиридин-4-ил)-2-трет-пентил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-метокси-2-метилпропан-2-ил)-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6,7-дигидро-5Н-циклопента[b]пиридин;
2-циклогексил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-6,7-дигидро-5Н-циклопента[b]пиридин;
2-трет-бутил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(3-фторфенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(4-(трифторметил)фенил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(3-(трифторметил)фенил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3,3-дифторциклобутил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(4-фтор-фенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-трет-бутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)оксазол;
2-трет-бутил-4-(1-метил-1Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(4-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(3-циклопропил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-трет-бутил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-2-метилоксазол;
2-трет-бутил-4-(4-хлор-1Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(4-(трифторметил)-1Н-имидазол-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-3-(1Н-тетразол-5-ил)-4-(1Н-1,2,3-триазол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(2-бутил-1Н-имидазол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фуран-2-ил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фтор-бутил-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-фторфенил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фтор-бутил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
и их фармацевтически приемлемые соли.
25. Соединение, выбранное из:
4-фенил-2-(R)-тетрагидро-фуран-2-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(S)-тетрагидро-фуран-2-ил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(R)-4-(2-хлорпиридин-4-ил)-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(2-хлорпиридин-4-ил)-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
(S)-4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
(R)-4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8,9,10-гексагидроциклоокта[b]пиридин;
2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-((S)-2-метил-тетрагидро-фуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-((R)-2-метил-тетрагидро-фуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-метоксифенил)-2-(2-метилтетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-метокси-фенил)-2-((S)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-метокси-фенил)-2-((R)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-метилпиридин-4-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-[(2S)-2-метилоксолан-2-ил]-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-[(2R)-2-метилоксолан-2-ил]-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлорфенил)-2-(2-метилтетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-((S)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-((R)-2-метил-тетрагидро-фуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метилциклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метилциклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-метоксипиридин-4-ил)-2-(1-метилциклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-(1-метилциклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)пиридин-2(1Н)-он;
4-(3-хлор-фенил)-2-(1-метил-циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(1-метилциклогексил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метилциклогексил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксиметил-циклопентил)-4-(2-метил-2Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-фторпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(4-метил-1Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1Н-индол-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этилпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
3-(2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-2-метилфенол;
4-(2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-2-метилоксазол;
4-(1Н-индазол-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-4-(2-(трифторметил)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-4-(2-(2,2,2-трифторэтокси)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этоксипиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(4-фтор-3-метоксифенил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(4-фторфенил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(3-метоксифенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-фтор-5-метоксифенил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-хлор-фенил)-2-(1-метоксиметил-циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-(метоксиметил)пентан-3-ил)-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-(метоксиметил)пентан-3-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-4-(2-этилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-циклопентил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-4-ил)-N-метилпиридин-2-амин;
2-циклопентил-3-(1Н-тетразол-5-ил)-4-(2-(трифторметил)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(1-метил-1Н-пиразол-5-ил)-2-(3-метилпентан-3-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этилпиридин-4-ил)-2-изопропил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропил-3-(1Н-тетразол-5-ил)-4-(2-(2,2,2-трифторэтокси)пиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-этоксипиридин-4-ил)-2-изопропил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксициклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксициклопентил)-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-метоксициклопентил)-4-(2-метоксипиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-(1-метоксициклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метоксициклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(1-(4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(1-(4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин-2-ил)циклопентил)метанол;
(1-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(1-(4-(3-хлорфенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(1-(4-(4-фторфенил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)циклопентил)метанол;
(S)-трет-бутил-2-(4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пирролидин-1-карбоксилат;
(S)-4-фенил-2-(пирролидин-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин 2,2,2-трифторацетат;
2-циклопентил-4-фенил-3-(1Н-тетразол-5-ил)-7,8-дигидро-5Н-пиридо[2,3-с]азепин-9(6Н)-он;
2-(1-метокси-2-метилпропан-2-ил)-6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-2-трет-пентил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-метокси-2-метилпропан-2-ил)-6,6-диметил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклогексил)-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклопентил)-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(4-метилтетрагидро-2Н-пиран-4-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(4-метилтетрагидро-2Н-пиран-4-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклопентил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-6,6-дифтор-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-6,6-дифтор-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-6,6-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(1-(метоксиметил)циклогексил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-4-(1-метил-1Н-пиразол-5-ил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклогексил)-4-(1-метил-1Н-пиразол-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
6,6-дифтор-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-6,6-дифтор-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-6,6-дифтор-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-6,6-дифтор-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-этилтетрагидрофуран-2-ил)-4-(1-метил-1Н-пиразол-5-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(1-метил-1Н-пиразол-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3-хлорфенил)-2-(2-метилтетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-(3-метоксифенил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(4-фтор-3-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метилсульфонилметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-4-(4-фтор-3-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-4-(4-фтор-3-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(3-(метилсульфонил)фенил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклопентил)-4-(3-метоксифенил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-фтор-5-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-фтор-5-метоксифенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(этоксиметил)циклопентил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-4-(3-хлорфенил)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-6,6-диметил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(3,3-дифторциклобутил)-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1,5-диметил-1Н-пиразол-4-ил)-4-фенил-3-(2Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3,3-дифторциклобутил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-фтор-бутил-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-6,6-дифтор-4-(2-метил-пиридин-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-трет-бутил-6,6-дифтор-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-трет-бутил-6,6-дифтор-4-(2-метил-2Н-пиразол-3-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-трет-бутил-4-фенил-3-(1Н-тетразол-5-ил)-7,8-дигидро-5Н-тиопирано[4,3-b]пиридин;
2-трет-бутил-8,8-диметил-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-трет-бутил-7,7-диметил-4-фенил-3-(1Н-тетразол-5-ил)-6,7-дигидро-5Н-циклопента[b]пиридин;
2-трет-бутил-8,8-диметил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-трет-бутил-8,8-диметил-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(1-(метоксиметил)циклобутил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклобутил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклобутил)-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(перфторэтил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-трет-бутил-8,8-диметил-4-(1-метил-1Н-пиразол-5-ил)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2,4-бис(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропокси-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-метокси-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-этокси-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-фенил-2-(тетрагидрофуран-3-илокси)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил;
(R)-4-фенил-2-(тетрагидрофуран-3-илокси)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил;
2-этокси-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-изопропокси-4-(1-метил-1Н-пиразол-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-этокси-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(2-метоксиэтокси)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-((тетрагидрофуран-2-ил)метокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-фторпропокси)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(2,2-дифторэтокси)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-фенил-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(2-метилпиридин-4-ил)-2-(тетрагидро-2Н-пиран-4-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(2-метилпиридин-4-ил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(2-метилпиридин-4-ил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-4-(4-(трифторметил)фенил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(3-фторфенил)-2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(3-фторфенил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3,5-дифторфенил)-2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(3-фторфенил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-4-(3,5-дифторфенил)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-фторфенил)-2-((S)-тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-фторфенил)-2-(2-метоксиэтокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-4-(тиофен-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(3-фторпропокси)-3-(1Н-тетразол-5-ил)-4-(тиофен-2-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(S)-2-(тетрагидрофуран-3-илокси)-3-(1Н-тетразол-5-ил)-4-(тиофен-3-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидро-2Н-пиран-4-илокси)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метилциклопентил)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
4-(3-хлорфенил)-2-(1-метилциклопентил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
4-(1-метил-1Н-пиразол-5-ил)-2-(1-метилциклогексил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-(1-метилциклогексил)-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклогексил-4-фенил-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-(1-метилциклогексил)-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклогексил-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
2-циклопентил-4-фенил-5,6,7,8-тетрагидрохинолин-3-карбоновая кислота;
2-(1-(метоксиметил)циклопентил)-6-пентил-4-фенил-3-(1Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
трет-бутил 2-метил-2-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пропаноат;
2-метил-2-(4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-ил)пропановая кислота;
и их фармацевтически приемлемые соли.
26. Соединение, выбранное из:
6-метил-4-(1-метил-1Н-пиразол-5-ил)-2-(пиперидин-1-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
4-(3-хлорфенил)-N,N-диэтил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-2-амин;
2-циклопентил-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-фенил-2-(тетрагидрофуран-2-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-(метоксиметил)циклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-циклопентил-6,6-дифтор-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6-метил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
2-циклопентил-6,6-диметил-4-(2-метилпиридин-4-ил)-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
и их фармацевтически приемлемые соли.
27. Соединение, выбранное из:
2-((R)-2-метил-тетрагидро-фуран-2-ил)-4-фенил-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
2-(1-метилциклопентил)-4-(2-метилпиридин-4-ил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
4-(2-хлорпиридин-4-ил)-2-(1-(метоксиметил)циклопентил)-3-(1Н-тетразол-5-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин;
(R)-6,6-диметил-2-(2-метилтетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(R)-2-(2-(метоксиметил)тетрагидрофуран-2-ил)-4-фенил-3-(2Н-тетразол-5-ил)-5,6,7,8-тетрагидрохинолин;
(S)-4-фенил-2-(тетрагидрофуран-3-илокси)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбонитрил;
2-(1-метилциклогексил)-4-(2-метилпиридин-4-ил)-6,7,8,9-тетрагидро-5Н-циклогепта[b]пиридин-3-карбоновая кислота;
и их фармацевтически приемлемые соли.
28. Соединение по любому из пп.1-27 для применения в качестве ингибитора белков, связывающих жирные кислоты (FABP) 4 и/или 5.
29. Соединение по любому из пп.1-27 для лечения или профилактики заболеваний, при которых полезно ингибирование белков, связывающих жирные кислоты (FABP) 4 и/или 5.
30. Фармацевтическая композиция, ингибирующая белки, связывающие жирные кислоты (FABP) 4 и/или 5, содержащая соединение по любому из пп.1-27 и терапевтически инертный носитель.
31. Применение соединения по любому из пп.1-27 для лечения или профилактики заболеваний, при которых полезно ингибирование белков, связывающих жирные кислоты (FABP) 4 и/или 5.
32. Применение соединения по любому из пп.1-27 для получения лекарственного средства для лечения или профилактики заболеваний, при которых полезно ингибирование белков, связывающих жирные кислоты (FABP) 4 и/или 5.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Способ приготовления стойких смесей щелочных солей нитрозаминов с азокомпонентамн | 1926 |
|
SU15617A1 |
| Сотенные или десятичные весы | 1925 |
|
SU2607A1 |
Авторы
Даты
2018-03-23—Публикация
2013-08-19—Подача