Область техники
[0001]
Настоящее изобретение относится к слою лекарственного покрытия на основе нерастворимых в воде лекарственных средств и к слою лекарственного покрытия, имеющему конкретную кристаллическую морфологическую форму нерастворимых в воде лекарственных средств.
Уровень техники
[0002]
В последние годы активно проводят разработку баллонов, выделяющих лекарственное средство, (DEB), в которых баллонный катетер покрыт лекарственными средствами, и было сообщено, что они являются эффективными для лечения и предупреждения рестеноза. Баллон покрыт слоем покрытия, включающим лекарственные средства и эксципиенты, и, когда кровеносный сосуд расширяется, баллон сдавливает стенку кровеносного сосуда и доставляет лекарственные средства в ткань-мишень.
[0003]
В последние годы было обнаружено, что морфологическая форма лекарственных средств, нанесенных на поверхность баллона, влияет на свойство высвобождения лекарственных средств и их способность переходить в ткани с поверхности баллона в области очага повреждения, и известно, что является важным контроль кристаллической формы или аморфной формы лекарственных средств.
В PTL 1 и PTL 2 описан способ, в котором с использованием прокаливания с паром растворителя морфологическую форму лекарственных средств, нанесенных на поверхность баллона, изменяют с аморфной на кристаллическую. Кроме того, в PTL 2 описано, что кристаллическая форма паклитаксела, полученная прокаливанием, имеет веерообразную форму и стержневидную форму или иглоподобную форму и что стержневидная кристаллическая форма имеет более высокую способность к переходу лекарственного средства в ткань-мишень по сравнению с веерообразной формой.
Кроме того, в PTL 3 описано, что паклитаксел в кристаллической гидратированной форме является покрытым и кристаллическая гидратированная форма имеет предпочтительное свойство высвобождения лекарственного средства и способность к переходу лекарственного средства в ткани в области очага повреждения по сравнению с негидратированной формой и аморфной формой.
Таким образом, в PTL 3 описано, что баллон, выделяющий лекарственное средство, имеющий паклитаксел в кристаллической форме, проявляет превосходную способность к переходу лекарственных средств в ткани; однако в нем не описана точная морфологическая форма кристалла и эффект ингибирования внутрисосудистого стеноза.
В противоположность этому, существует проблема, состоящая в том, что баллон, выделяющий лекарственное средство, имеющий паклитаксел в кристаллической форме, в некоторых случаях проявляет выраженную токсичность в отношении ткани-мишени. Таким образом, в проведенной недавно разработке баллона, выделяющего лекарственное средство, требовалось, чтобы баллон, выделяющий лекарственное средство, обладал пригодным равновесием между эффективностью и токсичностью, т.е. высоким эффектом (эффект ингибирования внутрисосудистого стеноза) и низкой токсичностью. В PTL 1, PTL 2 и PTL 3 токсичность вообще не описана, и кристаллическая морфологическая форма лекарственного средства, обладающего приемлемым равновесием между эффективностью и токсичностью, не является очевидной.
[0004]
Исходя из описанного выше, поскольку нельзя утверждать, что баллон уровня техники, выделяющий лекарственное средство, имеющий слой покрытия, проявляет достаточно низкую токсичность и высокий эффект на уровень ингибирования стеноза при лечении сегмента стеноза в кровеносном сосуде, является желательным медицинское устройство, имеющее подходящее равновесие между эффективностью и токсичностью.
Список ссылок
Патентная литература
[0005]
PTL 1: Международная публикация PCT № WO2010/124098
PTL 2: JP-T-2012-533338
PTL 3: JP-T-2012-514510
Сущность изобретения
Техническая проблема
[0006]
Настоящее изобретение направлено на предоставление слоя лекарственного покрытия, имеющего морфологическую форму нерастворимых в воде лекарственных средств, у которой эффект ингибирования внутрисосудистого стеноза в области повреждения является высоким при доставке медицинского устройства, покрытого лекарственным средством, в организм, и предоставление медицинского устройства, в котором он используется.
Решение проблемы
[0007]
В результате тщательных исследований для решения описанных выше проблем автор настоящего изобретения обнаружил, что слой лекарственного покрытия, имеющий конкретную кристаллическую морфологическую форму нерастворимого в воде лекарственного средства, обладает высоким эффектом ингибирования внутрисосудистого стеноза в области очага повреждения, и осуществил изобретение.
[0008]
Таким образом, настоящее изобретение относится к следующему.
(1) Слой лекарственного покрытия, который имеет морфологическую форму, включающую множество вытянутых телец с длинной осью, которую каждый кристалл нерастворимого в воде лекарственного средства независимо имеет, на поверхности подложки, причем длинные оси вытянутых частиц имеют практически линейную форму, и длинные оси вытянутых частиц образуют угол в заданном диапазоне, предпочтительно угол в диапазоне от 45° до 135°, относительно плоскости подложки, с которой длинная ось вытянутых телец пересекается.
(2) Слой лекарственного покрытия, описанный в (1), в котором по меньшей мере вблизи дистальной области вытянутое тельце является полым.
(3) Слой лекарственного покрытия, описанный в (1) или (2), в котором форма поперечного сечения поверхности вытянутого тельца, перпендикулярной длинной оси, является многоугольной.
(4) Слой лекарственного покрытия, в котором кристаллы нерастворимого в воде лекарственного средства, имеющие плоскую вытянутую волосообразную форму, бессистемно наслоены на поверхность подложки, и в котором длинные оси кристаллов частично имеют участок, искривленный в форме изгиба, и в той же плоскости кристаллов не примешаны кристаллы, имеющие другие формы.
(5) Слой лекарственного покрытия, описанный в (4), в котором поверхность кристалла нерастворимого в воде лекарственного средства дополнительно покрыта аморфной пленкой.
(6) Слой лекарственного покрытия, включающий кристаллическую морфологическую форму нерастворимого в воде лекарственного средства, в которой частицы кристаллов нерастворимого в воде лекарственного средства расположены регулярно на поверхности подложки и в которой частицы эксципиента, образованные из эксципиента, нерегулярно расположены между частицами кристаллов, где молекулярная масса эксципиента является меньшей, чем молекулярная масса нерастворимого вводе лекарственного средства, доля частиц эксципиента на заданную площадь подложки является меньшей, чем доля частиц кристаллов, и частицы эксципиента не образуют матрикса.
(7) Слой лекарственного покрытия, описанный в любом из (1)-(6), в котором нерастворимое в воде лекарственное средство представляет собой рапамицин, паклитаксел, доцетаксел или эверолимус.
(8) Медицинское устройство, имеющее слой лекарственного покрытия, описанный в любом из (1)-(7), на поверхности медицинского устройства, которое уменьшается в диаметре для доставки, когда его доставляют в организм, и увеличивается в диаметре для высвобождения лекарственного средства из слоя лекарственного покрытия в пораженной области.
(9) Способ доставки лекарственного средства, имеющий стадию доставки медицинского устройства, описанного в (8), в просвет, стадию радиального расширения расширяющейся части, находящейся в медицинском устройстве, и стадию, на которой слой лекарственного покрытия, который имеется в расширяющейся части, прилегает к просвету.
Преимущественные эффекты изобретения
[0009]
Настоящее изобретение может обеспечить слой лекарственного покрытия для медицинского устройства, выделяющего лекарственное средство, у которого эффект ингибирования внутрисосудистого стеноза в области очага повреждения является высоким и/или токсичность является низкой.
Краткое описание чертежей
[0010]
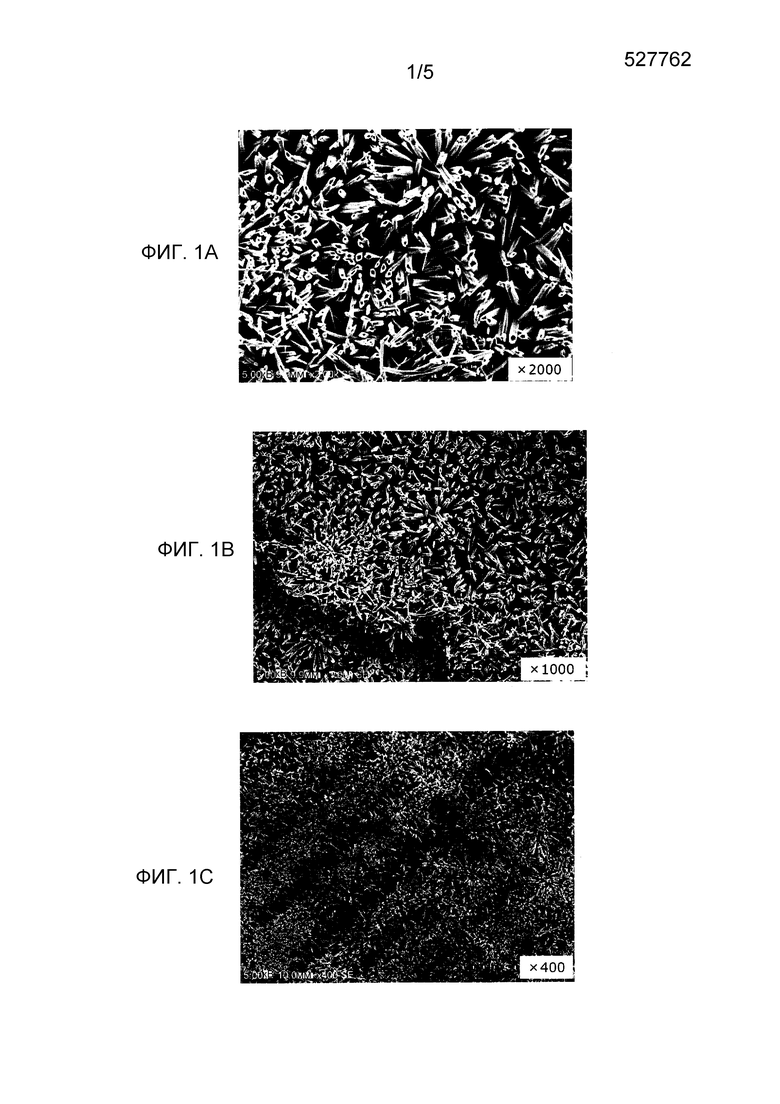
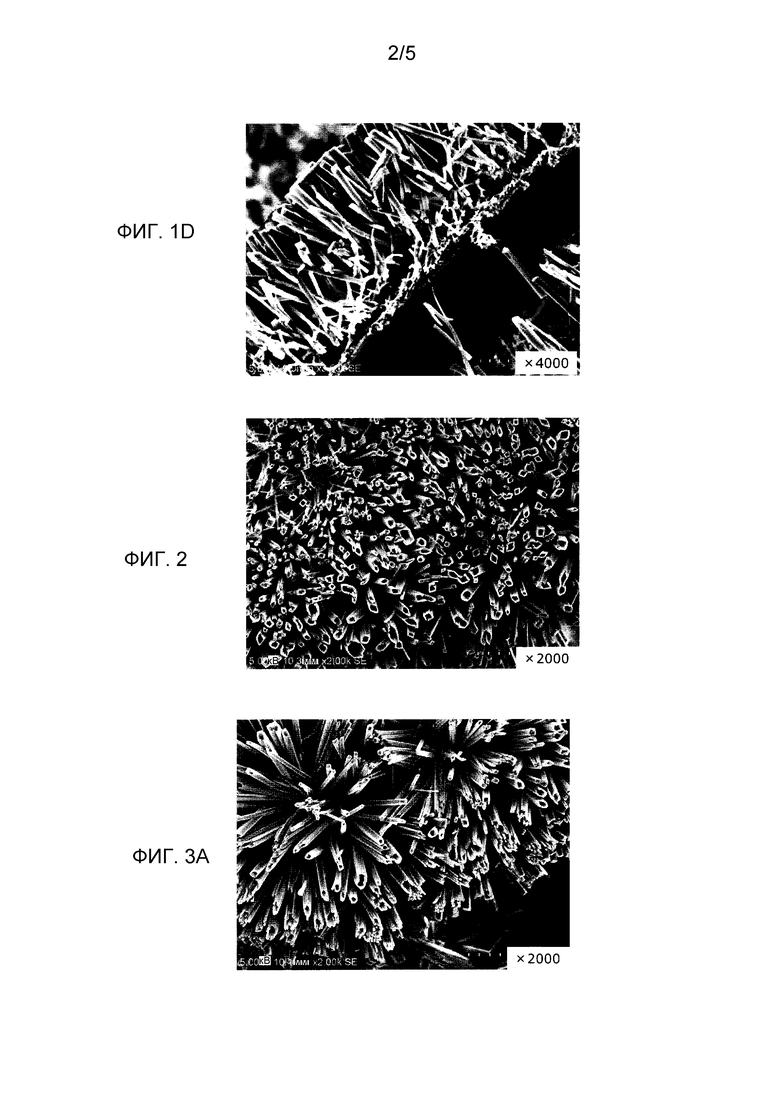
[Фиг.1] На фиг.1 представлена диаграмма, на которой показано изображение, полученное сканирующей электронной микроскопией (далее обозначаемой как SEM), поверхности слоя лекарственного покрытия, полученного согласно примеру 1. На фиг.1A представлено изображение SEM с увеличением в 2000 раз кристаллов, наблюдаемых на поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 1. На фиг.1B представлено изображение SEM с увеличением в 1000 раз кристаллов, наблюдаемых на другой части поверхности подложки, полученной согласно примеру 1. На фиг.1C представлено изображение SEM с увеличением в 400 раз, наблюдаемое на другой части поверхности подложки, полученной согласно примеру 1. На фиг.1D представлено изображение SEM с увеличением в 4000 раз наблюдаемых кристаллов в поперечном сечении, перпендикулярном поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 1.
[Фиг.2] На фиг.2 представлена диаграмма, на которой показано изображение SEM с увеличением в 2000 раз кристаллов, наблюдаемых на поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 2.
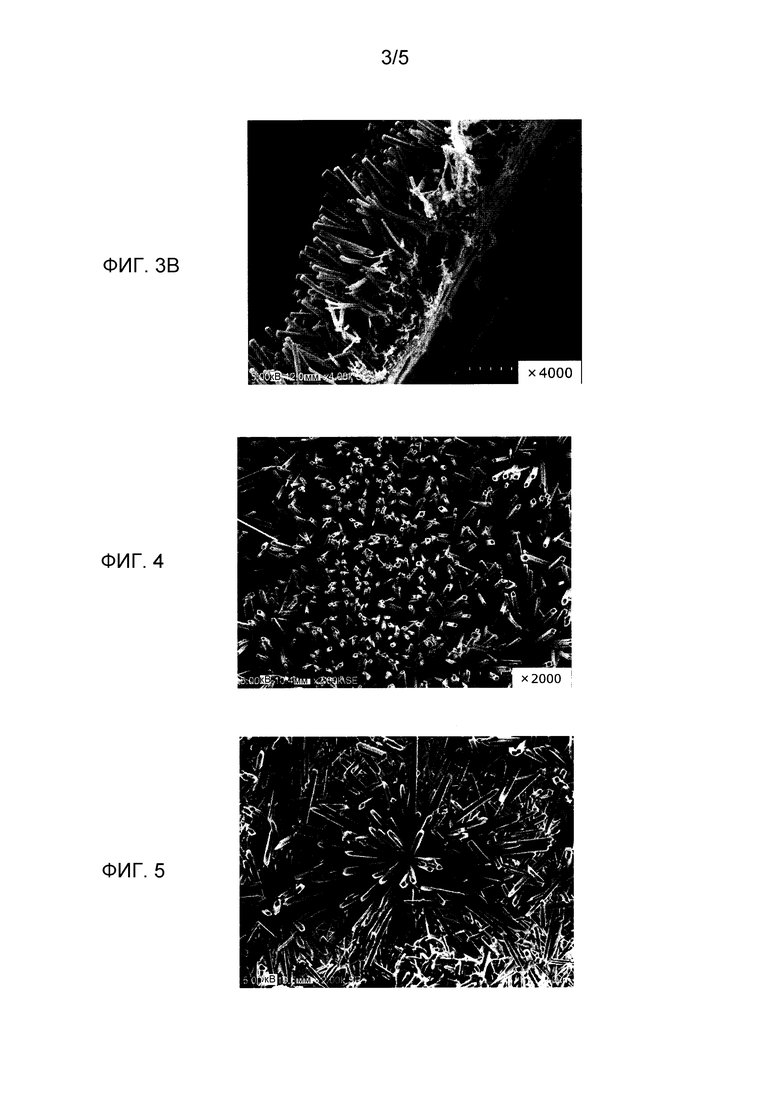
[Фиг.3] На фиг.3A представлена диаграмма, на которой показано изображение SEM с увеличением в 2000 раз кристаллов, наблюдаемых на поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 3. На фиг.3B представлено изображение SEM с увеличением в 4000 раз наблюдаемых кристаллов в поперечном сечении, перпендикулярном поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 3.
[Фиг.4] На фиг.4 представлена диаграмма, на которой показано изображение SEM с увеличением в 2000 раз кристаллов, наблюдаемых на поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 4.
[Фиг.5] На фиг.5 представлена диаграмма, демонстрирующая изображение SEM с увеличением в 2000 раз кристаллов, наблюдаемых на поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 6.
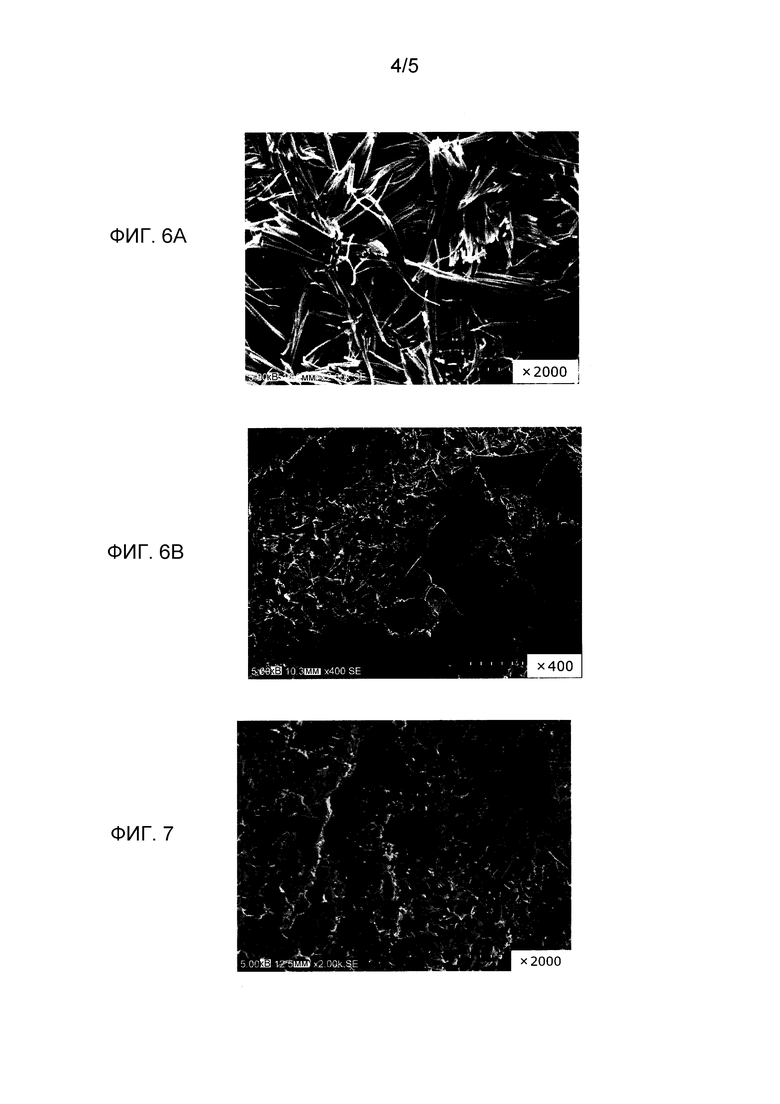
[Фиг.6] На фиг.6A представлена диаграмма, демонстрирующая изображение SEM с увеличением в 2000 раз кристаллов, наблюдаемых на поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 6. На фиг.6B представлена диаграмма, демонстрирующая изображение SEM с увеличением в 400 раз кристаллов, наблюдаемых на другой части поверхности подложки слоя лекарственного покрытия, полученного согласно примеру 6.
[Фиг.7] На фиг.7 представлена диаграмма, демонстрирующая изображение SEM с увеличением в 2000 раз кристаллов, наблюдаемых на поверхности подложки слоя лекарственного покрытия коммерчески доступного баллона, выделяющего лекарственное средство, (IN.PACT), изготовленного INVAtec JAPAN, согласно сравнительному примеру 1.
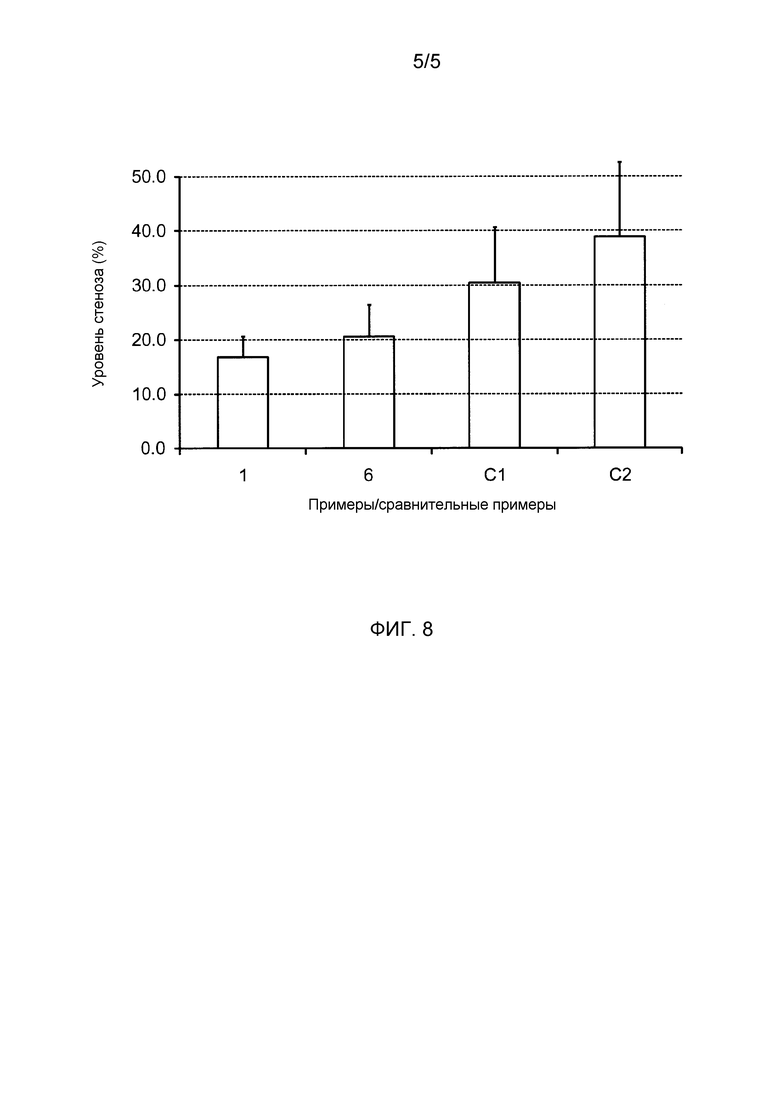
[Фиг.8] На фиг.8 представляет собой график уровня внутрисосудистого стеноза (%), демонстрирующий ингибиторный эффект на внутрисосудистый стеноз в коронарной артерии свиньи.
Описание вариантов осуществления
[0011]
Автор настоящего изобретения обнаружил, что слой лекарственного покрытия, имеющий низкую токсичность в области очага поражения, высокий эффект ингибирования стеноза, имеет конкретную кристаллическую форму нерастворимого в воде лекарственного средства при доставке медицинского устройства, покрытого лекарственным средством, в организм, и осуществил изобретение.
Проиллюстрированы следующие предпочтительные кристаллические формы.
(1) Слой, включающий кристаллическую морфологическую форму длинного полого объекта
Слой, имеющий морфологическую форму, включающую кристаллы длинного полого объекта, представляет собой слой лекарственного покрытия, в котором множество вытянутых телец, имеющих длинные оси, образованных из кристаллов нерастворимого в воде лекарственного средства, присутствует в форме щетки на поверхности подложки. Множество вытянутых телец расположены по окружности в форме щетки на поверхности подложки. Каждое из вытянутых телец присутствует независимо, имеет длину и имеет один конец (проксимальный) вытянутого тельца, фиксированный на поверхности подложки. Вытянутые тельца не образуют составную структуру с соседними вытянутыми тельцами и они не соединены друг с другом. Длинная ось кристалла имеет практически линейную форму. Вытянутое тельце формирует заданный угол относительно плоскости подложки, которую пересекает длинная ось. Заданный угол находится в диапазоне от 45° до 135°. Предпочтительно заданный угол находится в диапазоне от 70° до 110° и более предпочтительно в диапазоне от 80° до 100°. Более предпочтительно, чтобы длинная ось вытянутого тельца образовывала угол около 90° относительно плоскости подложки. По меньшей мере вблизи дистальной области вытянутое тельце является полым. Поперечный срез вытянутого тельца имеет полости на поверхности, перпендикулярной длинной оси вытянутого тельца. Поперечное сечение вытянутого тельца, имеющего полости на поверхности, перпендикулярной длинной оси, является многоугольным. Примеры многоугольника включают четырехугольник, пятиугольник и шестиугольник. Таким образом, вытянутое тельце имеет дистальную область (или дистальную поверхность) и проксимальную область (или проксимальную поверхность), и боковая поверхность между дистальной областью (или дистальной поверхностью) и проксимальной областью (или проксимальной поверхностью) образована в виде длинного многоугольника, который состоит из множества плоскостей. Кристаллическая морфологическая форма составляет всю или по меньшей мере часть плоскости на поверхности подложки. Например, слой, включающий кристаллическую морфологическую форму длинного полого объекта, представляет собой слой, имеющий кристаллическую морфологическую форму, представленную на изображениях SEM на фиг.1-4.
[0012]
Например, характеристики слоя, имеющего морфологическую форму, включающую кристаллы длинного полого объекта, являются следующими.
1) Множество вытянутых телец (стержни) имеют независимые длинные оси, и вытянутое тельце является полым. Вытянутое тельце имеет стержневидную форму.
2) Вытянутые тельца имеют длинные оси и во многих случаях представляют собой многоугольник, в котором поперечное сечение вытянутого тельце на поверхности, перпендикулярной длинной оси, является многоугольным. 50% или более объема кристалла в виде вытянутого тельца представляют собой длинный многоугольник. Боковая поверхность многоугольника в основном представляет собой четырехугольник. В некоторых случаях длинный многоугольник имеет множество поверхностей (бороздок), которые образованы входящим углом, вершина которого вытянута в направлении длинной оси. В настоящем описании входящий угол означает, что по меньшей мере один из внутренних углов многоугольника на поперечном сечении вытянутого тельца в плоскости, перпендикулярной длинной оси, превышает угол 180°.
3) Во многих случаях вытянутое тельце, имеющее длинную ось, представляет собой длинный многоугольник. При рассмотрении в поперечном сечении, перпендикулярном длинной оси, поперечное сечение является многоугольным и выглядит как четырехугольник, пятиугольник или шестиугольник.
4) Множество вытянутых телец, имеющих независимые длинные оси, расположены вертикально в ряд под углом в заданном диапазоне, предпочтительно в диапазоне от 45° до 135° относительно поверхности подложки, т.е. множество вытянутых телец, имеющих независимые длинные оси, практически единообразно располагаются вертикально наподобие леса на поверхности подложки. Область, где вытянутые тельца располагаются вертикально наподобие леса, является практически единообразно сформированной, располагаясь в круговом направлении и осевом направлении на поверхности подложки. Каждый из углов каждого независимого вытянутого тельца относительно поверхности подложки может быть отличающимся или одинаковым, находясь в заданном диапазоне.
[0013]
5) Один конец (проксимальный) каждого вытянутого тельца, имеющий независимую длинную ось, фиксирован на поверхности подложки.
6) В некоторых случаях, в области вблизи поверхности подложки наслоены подобные частицам, подобные коротким стержням или подобные коротким изгибам кристаллы. На поверхности подложки присутствует вытянутое тельце, которое прямо или непрямо имеет длинную ось. Таким образом, существует случай, когда вытянутые тельца, имеющие длинные оси, на слое расположены вертикально наподобие леса.
7) Длина вытянутого тельца, имеющего длинную ось, в осевом направлении, составляет предпочтительно от 5 до 20 мкм, более предпочтительно от 9 до 11 мкм и еще более предпочтительно приблизительно 10 мкм. Диаметр вытянутого тельца, имеющего длинную ось, предпочтительно составляет от 0,01 до 5 мкм, более предпочтительно от 0,05 до 4 мкм и еще более предпочтительно от 0,1 до 3 мкм.
8) Другие морфологические формы (например, пластинчатая морфологическая форма, которая является аморфной) не являются примешанными на поверхности слоя, включающего кристаллическую морфологическую форму длинного полого объекта, и 50% по объему или более и 70% по объему или более кристаллической формы составляют кристаллические морфологические формы 1)-7). Более предпочтительно практически всю форму составляет кристаллическая морфологическая форма 7).
[0014]
9) В кристаллической морфологической форме длинного полого объекта является возможным, чтобы в слое лекарственного покрытия, включающего кристаллы, составляющие нерастворимое в воде лекарственное средство, присутствовали другие соединения. В этом случае, соединения присутствуют в состоянии, распределенном в пространстве между кристаллами (вытянутое тельце) множества нерастворимых в воде лекарственных средств, которые расположены вертикально наподобие леса на поверхности подложки баллона. В этом случае в соотношении материалов, составляющих слой лекарственного покрытия, кристаллы нерастворимых в воде лекарственных средств занимают значительно больший объем, чем другие соединения.
10) В кристаллической морфологической форме длинного полого объекта нерастворимые в воде лекарственные средства, составляющие кристаллы, присутствуют на поверхности подложки баллона. В слое лекарственного покрытия поверхности подложки баллона, имеющей нерастворимые в воде лекарственные средства, составляющие кристаллы, матрикс из эксципиента не образуется. Таким образом, нерастворимые в воде лекарственные средства, составляющие кристаллы, не прикреплены к материалу матрикса. Нерастворимые в воде лекарственные средства, составляющие кристаллы, также не заключены в материал матрикса.
11) В кристаллической морфологической форме длинного полого объекта слой лекарственного покрытия может включать частицы кристаллов нерастворимого в воде лекарственного средства, которые расположены регулярно на поверхности подложки, и частицы эксципиента, образованные из эксципиента, которые нерегулярно расположены между частицами кристаллов. В этом случае молекулярная масса эксципиента является меньшей, чем молекулярная масса нерастворимых в воде лекарственных средств. Таким образом, доля частиц эксципиента на заданную область подложки является меньшей, чем доля частиц кристаллов, и частицы эксципиента не образуют матрикса. В рамках настоящего изобретения частицы кристаллов нерастворимых в воде лекарственных средств могут представлять собой частицы вытянутых телец, и, поскольку частицы эксципиента присутствуют в количестве, значительно меньшем, чем частицы кристаллов нерастворимого в воде лекарственного средства, и распределены среди частиц кристаллов нерастворимого в воде лекарственного средства, существует случай, где частицы эксципиента не наблюдаются на изображении SEM.
[0015]
Кристаллическая морфологическая форма, имеющая форму плоских волосообразных кристаллов, описанная ниже, которая является характеристикой настоящего изобретения, занимает по меньшей мере часть слоя лекарственного покрытия, равную или превышающую 50% по объему, равную или превышающую 80% по объему (равную или превышающую 50% по объему в качестве кристалла и более предпочтительно равную или превышающую 70% по объему) и еще более предпочтительно практически 100% по объему. В случае, когда она занимает практически 100% по объему, она находится в состоянии, когда множество кристаллических морфологических форм не являются смешанными, и присутствует только одна кристаллическая морфологическая форма.
(2) Слой, включающий плоскую волосообразную кристаллическую морфологическую форму
Слой, включающий плоскую волосообразную кристаллическую морфологическую форму, представляет собой слой лекарственного покрытия, в котором кристаллы плоской вытянутой волосообразной формы из нерастворимого в воде лекарственного средства бессистемно наслоены на поверхность подложки и в котором длинные оси кристаллов частично имеют участок, искривленный в форме изгиба, и кристаллы, имеющие другие морфологические формы, не примешаны в той же плоскости кристаллов. В случае, когда присутствует аморфный слой и слой кристаллов, "не в той же плоскости кристаллов" означает, что на слое кристаллов присутствует аморфная пленка. Например, слой, включающий плоскую волосообразную кристаллическую морфологическую форму, представляет собой слой, имеющий кристаллическую форму согласно примеру 6, представленный на фиг.6A.
[0016]
Например, характеристики слоя, включающего кристаллическую плоскую волосообразную морфологическую форму, являются следующими.
1) Кристалл волосообразной формы, имеющий длинную ось, имеет плоскую форму с множеством соединений в ширину, не имеет полости и имеет конусовидную форму.
2) Форма волосообразных кристаллов с соединениями бессистемно наслоена на поверхность подложки. Длинная ось находится в состоянии, наклоненном вдоль поверхности положки.
3) Длинная ось кристаллов частично имеет участок, искривленный в форме изгиба.
4) Длина в направлении длинной оси волосообразного кристалла предпочтительно составляет от 10 до 100 мкм, более предпочтительно приблизительно 20 мкм, и она во многих случаях является большей, чем длина кристаллической морфологической формы длинного полого объекта.
[0017]
(3) Слой, включающий морфологическую форму, в которой аморфная пленка присутствует на поверхности волосообразного кристалла
Слой представляет собой слой лекарственного покрытия, в котором поверхность плоского волосообразного кристалла покрыта аморфной пленкой. Слой, включающий морфологическую форму, в которой аморфная пленка присутствует на поверхности плоского волосообразного кристалла, образован двумя слоями: кристаллическим и аморфным. Например, слой, включающий морфологическую форму, в которой аморфная пленка присутствует на поверхности плоского волосообразного кристалла, представляет собой слой, имеющий кристаллическую форму согласно примеру 6, представленный на фиг.6B.
В частности, на определенной плоскости (плоскость, на которой присутствуют кристаллы/аморфное вещество) определенная кристаллическая форма по меньшей мере частично присутствует или определенная кристаллическая фора присутствует в объеме, равном или превышающем 50%, или в объеме, равном или превышающем 80%, (50% или более по объему в качестве кристалла и более предпочтительно 70% или более по объему), еще более предпочтительно множество кристаллических форм не являются смешанными, и аморфная пленка может присутствовать на внешней стороне определенной плоскости.
[0018]
Кристаллические слои морфологической формы длинного полого объекта, плоской волосообразной морфологической формы и морфологической формы, в которой аморфная пленка присутствует на поверхности плоского волосообразного кристалла, имеют низкую токсичность и высокий эффект ингибирования внутрисосудистого стеноза при доставке медицинского устройства, в котором поверхность подложки покрыта лекарственным средством, в организм в качестве слоя лекарственного покрытия. Автор изобретения считает, что причина этого состоит в том, что растворимость и удерживающая способность в ткани после перехода лекарственного средства, имеющего определенную кристаллическую форму, в ткань изменяются. Например, в случае аморфного вещества, поскольку растворимость является высокой, даже когда лекарственное средство переходит в ткань, оно сразу выходит в кровоток. Таким образом, удерживающая способность в ткани является низкой и, следовательно, превосходный эффект ингибирования стеноза не может быть достигнут. С другой стороны, нерастворимое в воде лекарственное средство, имеющее конкретную кристаллическую форму в соответствии с настоящим изобретением, эффективно действует, ингибируя стеноз, поскольку, когда лекарственное средство переходит в ткань, один единичный кристалл становится небольшим, и, таким образом, его способность проникать в ткань и растворимость являются превосходными. Кроме того, считается, что, поскольку количество лекарственного средства, остающееся в ткани в качестве крупной массы, является небольшим, токсичность является низкой.
В частности, слой, включающий кристаллическую морфологическую форму длинного полого объекта, представляет собой множество практически единообразных вытянутых телец, имеющих длинные оси, и морфологическую форму, которая по существу единообразно расположена вертикально в ряд регулярно на поверхности субстрата. Таким образом, кристаллы, перешедшие в ткань, имеют небольшой размер (длина в направлении длинной оси), составляющий приблизительно 10 мкм. По этой причине лекарственное средство единообразно действует на область очага поражения, и способность перехода в ткань увеличивается. Кроме того, считается, что, поскольку размер переходящих кристаллов является небольшим, избыточное количество лекарственного средства не остается в пораженной области в течение чрезмерного количества времени, и токсичность не появляется, и может проявляться высокий эффект ингибирования стеноза.
[0019]
[Нерастворимое в воде лекарственное средство]
Нерастворимое в воде лекарственное средство означает лекарственное средство, которое является нерастворимым или является малорастворимым в воде, и, в частности, его растворимость в воде составляет менее 5 мг/мл при pH 5-8. Растворимость может составлять менее 1 мг/мл, и, кроме того, она может составлять менее 0,1 мг/мл. Нерастворимое в воде лекарственное средство включает жирорастворимое лекарственное средство.
[0020]
Примеры некоторых предпочтительных нерастворимых в воде лекарственных средств включают иммунодепрессивные лекарственные средства, такие как циклоспорины, включая циклоспорин, иммуноактивные лекарственные средства, такие как рапамицин, лекарственные средства против злокачественной опухоли, такие как паклитаксел, противовирусное лекарственное средство или антибактериальное лекарственное средство, антинеопластическое лекарственное средство, обезболивающее лекарственное средство и противовоспалительное лекарственное средство, лекарственное средство-антибиотик, противоэпилептическое лекарственное средство, анксиолитическое лекарственное средство, лекарственное средство против паралича, антагонист, блокирующее нейроны лекарственное средство, антихолинергическое лекарственное средство и холинэргическое лекарственное средство, антимускариновое лекарственное средство и мускариновое лекарственное средство, антиадренергическое лекарственное средство, антиаритмическое лекарственное средство, антигипертензивное лекарственное средство, гормональное лекарственное средство и пищевую добавку.
Нерастворимое в воде лекарственное средство предпочтительно представляет собой по меньшей мере одно средство, выбранное из группы, состоящей из рапамицина, паклитаксела, доцетаксела и эверолимуса. В настоящем описании рапамицин, паклитаксел, доцетаксел и эверолимус включают их аналоги и/или производные при условии, что они обладают сходной лекарственной эффективностью. Например, паклитаксел является аналогом доцетаксела. Рапамицин является аналогом эверолимуса. Среди них более предпочтительным является паклитаксел.
Нерастворимое в воде лекарственное средство, кроме того, может включать эксципиент. Эксципиент не ограничивается при условии, что он является фармацевтически приемлемым, и его примеры включают растворимые в воде полимеры, сахара, контрастные средства, сложные эфиры лимонной кислоты, сложные эфиры аминокислот, сложные эфиры глицерина и монокарбоновых кислот короткой цепи, фармацевтически приемлемые соли, поверхностно-активные вещества и т.п.
[0021]
[Способ получения кристаллического слоя]
Раствор для покрытия получают путем растворения нерастворимого в воде лекарственного средства в растворителе. Раствор для покрытия наносят на расширенный баллон, так чтобы растворитель раствора для покрытия медленно испарялся. Предпочтительно лекарственное средство высвобождают из дистальной части распределяющей трубки с отверстием, одновременно приводя боковую поверхность дистальной части распределяющей трубки, из которой высвобождают лекарственное средство, в контакт с поверхностью баллонного катетера. Баллонный катетер вращают в противоположном направлении (обратное направление) относительно направления высвобождения лекарственного средства по длинной оси. Затем баллон после нанесения покрытия сушат, тем самым получая слой лекарственного покрытия, включающий кристаллический слой.
(Предпочтительные условия для покрытия баллона раствором для покрытия)
Скорость вращения баллона: от 10 до 200 об/мин
предпочтительно от 30 до 180 об/мин
более предпочтительно от 50 до 150 об/мин
Скорость движения распределителя: от 0,01 до 2 мм/с
предпочтительно от 0,03 до 1,5 мм/с
более предпочтительно от 0,05 до 1,0 мм/с
Диаметр баллона: от 1 до 10 мм
предпочтительно от 2 до 7 мм
Скорость высвобождения лекарственного средства: от 0,01 до 1,5 мкл/с
предпочтительно от 0,01 до 1,0 мкл/c
более предпочтительно от 0,03 до 0,8 мкл/c.
Примером используемого растворителя, который конкретно не ограничен, является тетрагидрофуран, этанол, глицерин (также называемый глицеролом или пропан-1,2,3-триолом), ацетон, метанол, дихлорметан, гексан, этилацетат и вода. Среди них предпочтительным является смешанный растворитель, в котором некоторые из тетрагидрофурана, этанола, ацетона и воды смешаны.
[0022]
<Медицинское устройство>
Медицинское устройство по настоящему изобретению имеет слой лекарственного покрытия прямо или через слой для предварительной обработки, такой как слой затравки на поверхности подложки. Слой лекарственного покрытия содержит лекарственное средство с плотностью от 0,1 до 10 мкг/мм2, предпочтительно с плотностью от 0,5 до 5 мкг/мм2, более предпочтительно с плотностью от 0,5 до 3,5 мкг/мм2, еще более предпочтительно с плотностью от 1,0 до 3,0 мкг/мм2, однако он конкретно не ограничивается ими.
Форма и материалы подложки конкретно не ограничены. В качестве материалов можно использовать металлы и смолы. Материал может представлять собой любой из пленки, пластины, прута и материала неправильной формы, и он может иметь форму частиц.
Используемое медицинское устройство не ограничено. Можно использовать любое медицинское устройство, которое можно трансплантировать или вставлять. Предпочтительным является медицинское устройство, которое является длинным, доставляемым в нерасширенном состоянии с уменьшенным диаметром во внутреннюю полость, такую как кровеносный сосуд, и увеличивается в диаметре в круговом направлении в участке, таком как кровеносный сосуд или ткань, высвобождая лекарственное средство из слоя лекарственного покрытия. Таким образом, медицинское устройство, которое является уменьшенным в диаметре для доставки и увеличивается в диаметре для применения в пораженной области, представляет собой медицинское устройство, имеющее расширяющуюся часть. Слой лекарственного покрытия предоставляется по меньшей мере на части поверхности расширяющейся части. Таким образом, лекарственное средство нанесено по меньшей мере на наружную поверхность расширяющейся части.
[0023]
Материалы расширяющейся части медицинского устройства предпочтительно имеют определенную степень подвижности и определенную степень жесткости, так что лекарственное средство высвобождается из слоя лекарственного покрытия на поверхности при расширении, когда медицинское устройство достигает кровеносного сосуда или ткани. В частности, медицинское устройство содержит металл или смолу, и поверхность расширяющейся части, на которой нанесен слой лекарственного покрытия, предпочтительно состоит из резины. Резина, составляющая поверхность расширяющейся части, конкретно не ограничена, и ее предпочтительные примеры включают полиамиды. Таким образом, по меньшей мере часть поверхности расширяющейся части медицинского устройства, которая покрыта лекарственным средством, состоит из полиамидов. Примеры полиамида, который конкретно не ограничивается при условии, что он представляет собой полимер, имеющий амидную связь, включают гомополимеры, такие как политетраметиленадипамид (нейлон 46), поликапролактам (нейлон 6), полигексаметилен адипамид (нейлон 66), полигексаметилен себакамид (нейлон 610), полигексаметилен додекамид (нейлон 612), полиундеканолактам (нейлон 11), полидодеканолактам (нейлон 12), сополимеры, такие как сополимер капролактам/лауриллактам (нейлон 6/12), сополимер капролактам/аминоундекановая кислота (нейлон 6/11), сополимер капролактам/ω-аминононановая кислота (нейлон 6/9), сополимер капролактам/гексаметилендиаммоний адипат (нейлон 6/66), и ароматические полиамиды, такие как сополимер адипиновой кислоты и м-ксилолдиамина, или сополимер гексаметилендиамина и м,п-фталевой кислоты. Кроме того, полиамидный эластомер, который представляет собой блок-сополимер, в котором нейлон 6, нейлон 66, нейлон 11 или нейлон 12 является жестким сегментом, и полиалкиленгликоль, простой полиэфир или алифатический полиэфир является мягким сегментом, используют в качестве материала подложки для медицинского устройства в соответствии с настоящим изобретением. Можно использовать только полиамиды или можно совместно использовать два или более их типов.
[0024]
В частности, примером медицинского устройства, имеющего расширяющуюся часть, является длинный катетер, имеющий расширяющуюся часть (стент), или расширяющаяся часть (баллон).
В баллоне согласно настоящему изобретению предпочтительно слой лекарственного покрытия по настоящему изобретению формируют на поверхности в момент расширения и баллон заворачивают (складывают), устанавливают в кровеносный сосуд, полость тела или сходные с ними, доставляют в ткань или в пораженную область и увеличивают в диаметре в пораженной в области, после чего высвобождается лекарственное средство.
ПРИМЕРЫ
[0025]
Далее, настоящее изобретение описано с помощью примеров и сравнительных примеров, однако настоящее изобретение не ограничивается примерами.
[0026]
[Изготовление или получение баллона, выделяющего лекарственное средство, или получение не покрытого лекарственным средством баллона]
<Пример 1>
(1) Получение раствора для покрытия 1
Гидрохлорид этилового эфира L-серина (CAS No.26348-61-8) (56 мг) и паклитаксел (CAS No.33069-62-4) (134,4 мг) взвешивали. К ним соответственно добавляли абсолютный этанол (1,2 мл), тетрагидрофуран (1,6 мл) и обработанную с использованием мембраны RO (обратный осмос) воду (далее обозначаемую как RO-вода) (0,4 мл) и растворяли, тем самым получая раствор для покрытия 1.
(2) Нанесение лекарственного средства на баллон
Изготавливали баллонный катетер (изготавливаемый Terumo Corp., материалом баллона (расширяющая часть) является нейлоновый эластомер), имеющий размер: диаметр 3,0 × длина 20 мм (расширяющаяся часть) в расширенном состоянии. Раствор для нанесения покрытия 1 наносили на расширенный баллон так, чтобы растворитель раствора для покрытия медленно испарялся до достижения количества паклитаксела приблизительно 3 мкг/мм2. Предпочтительно лекарственное средство высвобождали из дистальной части распределяющей трубки с отверстием, одновременно приводя боковую поверхность дистальной части распределяющей трубки, из которой высвобождается лекарственное средство, в контакт с поверхностью баллонного катетера. Баллонный катетер вращали в противоположном направлении (обратное направление) относительно направления высвобождения лекарственного средства по длинной оси. Скорость движения баллонного катетера распределяющей трубки по баллонному катетеру и скорость вращения баллона регулировали, и, когда баллон начинал вращаться, лекарственное средство высвобождалось со скоростью 0,053 мкл/с, осуществляя нанесение на баллон. Затем баллон после нанесения покрытия сушили, тем самым получая баллон, выделяющий лекарственное средство.
[0027]
<Пример 2>
(1) Получение раствора для покрытия 2
Гидрохлорид этилового эфира L-серина (70 мг) и паклитаксел (134,4 мг) взвешивали. К ним соответственно добавляли абсолютный этанол (1,5 мл), ацетон (2,0 мл), тетрагидрофуран (0,5 мл) и RO-воду (1 мл) и растворяли, тем самым получая раствор для покрытия 2.
(2) Нанесение лекарственного средства на баллон
Изготавливали баллонный катетер (изготавливаемый Terumo Corp., материалом баллона (расширяющая часть) является нейлоновый эластомер), имеющий размер: диаметр 3,0 × длина 20 мм (расширяющаяся часть) в расширенном состоянии. Раствор для нанесения покрытия 2 наносили на расширенный баллон так, чтобы растворитель раствора для покрытия медленно испарялся до достижения количества паклитаксела приблизительно 3 мкг/мм2. В частности, лекарственное средство наносили на баллон тем же способом, который описан в примере 1, за исключением того, что лекарственное средство высвобождалось со скоростью 0,088 мкл/с. Затем баллон после нанесения покрытия сушили, тем самым получая баллон, выделяющий лекарственное средство.
[0028]
<Пример 3>
(1) Получение раствора для покрытия 3
Гидрохлорид этилового эфира L-серина (70 мг) и паклитаксел (168 мг) взвешивали. К ним соответственно добавляли абсолютный этанол (1,5 мл), тетрагидрофуран (1,5 мл) и RO-воду (1 мл) и растворяли, тем самым получая раствор для покрытия 3.
(2) Нанесение лекарственного средства на баллон
Изготавливали баллонный катетер (изготавливаемый Terumo Corp., материалом баллона (расширяющая часть) является нейлоновый эластомер), имеющий размер: диаметр 3,0 × длина 20 мм (расширяющаяся часть) в расширенном состоянии. Раствор для нанесения покрытия 3 наносили на расширенный баллон так, чтобы растворитель раствора для покрытия медленно испарялся до достижения количества паклитаксела приблизительно 3 мкг/мм2. В частности, лекарственное средство наносили на баллон тем же способом, который описан в примере 1, за исключением того, что лекарственное средство высвобождалось со скоростью 0,101 мкл/с. Затем баллон после нанесения покрытия сушили, тем самым получая баллон, выделяющий лекарственное средство.
[0029]
<Пример 4>
(1) Получение раствора для покрытия 4
Гидрохлорид этилового эфира L-серина (70 мг) и паклитаксел (180 мг) взвешивали. К ним соответственно добавляли абсолютный этанол (1,75 мл), тетрагидрофуран (1,5 мл) и RO-воду (0,75 мл) и растворяли, тем самым получая раствор для покрытия 4.
(2) Нанесение лекарственного средства на баллон
Изготавливали баллонный катетер (изготавливаемый Terumo Corp., материалом баллона (расширяющая часть) является нейлоновый эластомер), имеющий размер: диаметр 3,0 × длина 20 мм (расширяющаяся часть) в расширенном состоянии. Раствор для нанесения покрытия 4 наносили на расширенный баллон так, чтобы растворитель раствора для покрытия медленно испарялся до достижения количества паклитаксела приблизительно 3 мкг/мм2. В частности, лекарственное средство наносили на баллон тем же способом, который описан в примере 1, за исключением того, что лекарственное средство высвобождалось со скоростью 0,092 мкл/с. Затем баллон после нанесения покрытия сушили, тем самым получая баллон, выделяющий лекарственное средство.
[0030]
<Пример 5>
(1) Получение раствора для покрытия 5
Гидрохлорид диметилового эфира L-аспарагиновой кислоты (CAS No.32213-95-9) (37,8 мг) и паклитаксел (81 мг) взвешивали. К ним соответственно добавляли абсолютный этанол (0,75 мл), тетрагидрофуран (0,96 мл) и RO-воду (0,27 мл) и растворяли, тем самым получая раствор для покрытия 5.
(2) Нанесение лекарственного средства на баллон
Изготавливали баллонный катетер (изготавливаемый Terumo Corp., материалом баллона (расширяющая часть) является нейлоновый эластомер), имеющий размер: диаметр 3,0 × длина 20 мм (расширяющаяся часть) в расширенном состоянии. Раствор для нанесения покрытия 5 наносили на расширенный баллон так, чтобы растворитель раствора для покрытия медленно испарялся до достижения количества паклитаксела приблизительно 3 мкг/мм2. В частности, лекарственное средство наносили на баллон тем же способом, который описан в примере 1, за исключением того, что лекарственное средство высвобождалось со скоростью 0,055 мкл/с. Затем баллон после нанесения покрытия сушили, тем самым получая баллон, выделяющий лекарственное средство.
[0031]
<Пример 6>
(1) Получение раствора для покрытия 6
Гидрохлорид этилового эфира L-серина (56 мг) и паклитаксел (134,4 мг) взвешивали. К ним соответственно добавляли абсолютный этанол (0,4 мл), тетрагидрофуран (2,4 мл) и RO-воду (0,4 мл) и растворяли, тем самым получая раствор для покрытия 6.
(2) Нанесение лекарственного средства на баллон
Изготавливали баллонный катетер (изготавливаемый Terumo Corp., материалом баллона (расширяющая часть) является нейлоновый эластомер), имеющий размер: диаметр 3,0 × длина 20 мм (расширяющаяся часть) в расширенном состоянии. Раствор для нанесения покрытия 6 наносили на расширенный баллон так, чтобы растворитель раствора для покрытия медленно испарялся до достижения количества паклитаксела приблизительно 3 мкг/мм2. В частности, лекарственное средство наносили на баллон тем же способом, который описан в примере 1, за исключением того, что лекарственное средство высвобождалось со скоростью 0,053 мкл/с. Затем баллон после нанесения покрытия сушили, тем самым получая баллон, выделяющий лекарственное средство.
[0032]
<Сравнительный пример 1>
Изготавливали IN.PACT (изготавливаемый INVAtec JAPAN), который представляет собой коммерчески доступный баллонный катетер. Баллон согласно сравнительному примеру 1 представляет собой баллон, выделяющий лекарственное средство, поверхность которого покрыта паклитакселом.
[0033]
<Сравнительный пример 2>
Изготавливали баллонный катетер (изготавливаемый Terumo Corp., материалом баллона (расширяющая часть) является нейлоновый эластомер), имеющий размер: диаметр 3,0 × длина 20 мм (расширяющаяся часть) в расширенном состоянии. Баллон согласно сравнительному примеру 2 представляет собой баллон, не покрытый лекарственным средством, поверхность которого не покрыта лекарственным средством.
[0034]
[Измерение количества паклитаксела, нанесенного на баллон]
Для баллона, выделяющего лекарственное средство согласно примерам 1-6, количество паклитаксела, нанесенного на баллон, измеряли по следующей методике.
1. Способ
После того как полученный баллон, выделяющий лекарственное средство, погружали в раствор метанола, его встряхивали с использованием устройства для встряхивания в течение 10 минут, а затем паклитаксел, нанесенный на баллон, экстрагировали. Поглощение при 227 нм раствора в метаноле, которым экстрагировали паклитаксел, измеряли высокоэффективной жидкостной хроматографией с использованием спектрофотометра ультрафиолетовой - видимой области и определяли количество паклитаксела на баллон ([мкг/баллон]). Кроме того, количество паклитаксела на единицу площади баллона ([мкг/мм2]) вычисляли из количества полученного паклитаксела и площади поверхности баллона.
[0035]
2. Результат
В таблице 1 представлены полученные результаты. Кроме того, в таблице 1 "площадь поверхности баллона" соответствует площади поверхности (единицы: мм2), когда баллон является расширенным, "на каждый баллон" в столбце "количество PTX на баллоне" соответствует количеству паклитаксела на один баллон (единицы: мкг/баллон), и "на единицу площади" в столбце "количество PTX на баллоне" обозначает количество паклитаксела на 1 мм2 площади поверхности баллона (единицы: мкг/мм2) соответственно.
Как показано в таблице 1, количество паклитаксела, нанесенного на баллон, во всех примерах 1-6 составляет приблизительно 3 мкг/мм2, и было возможно нанести заданное количество паклитаксела на поверхность баллона.
[0036]
[Таблица 1]
[мкг /баллон]
[0037]
[Наблюдение слоя лекарственного покрытия на баллоне, выделяющем лекарственное средство, с использованием сканирующего электронного микроскопа (SEM)]
1. Способ
Баллоны, выделяющие лекарственное средство, согласно примерам 1-5 (фиг.1-5) и примеру 6 (фиг.6) сушили и после того, как высушенные баллоны, выделяющие лекарственное средство, нарезали на фрагменты соответствующего размера, их помещали на подложку, и на них наносили платину. Кроме того, аналогичным образом, после того, как коммерчески доступный баллон, выделяющий лекарственное средство (IN.PACT), изготавливаемый INVAtec JAPAN, согласно сравнительному примеру 1, также нарезали на фрагменты соответствующего размера, его помещали на подложку, и на него наносили платину. Поверхность и внутреннюю часть слоев лекарственного покрытия этих образцов с нанесенной платиной наблюдали с использованием сканирующего электронного микроскопа (SEM).
2. Результат
В слоях лекарственного покрытия согласно примерам наблюдали кристаллические слои, имеющие морфологическую форму длинного полого объекта, плоскую волосообразную морфологическую форму и морфологическую форму, в которой на поверхности плоских волосообразных кристаллов присутствует аморфная пленка.
Были получены изображения SEM, представленные на фиг.1-5. На фиг.1-4, которые представляют собой изображения SEM согласно примерам 1-4, представлен слой, включающий морфологическую форму длинного полого объекта, и очевидно, что единообразные кристаллы паклитаксела длинных полых объектов, имеющих длину приблизительно 10 мкм, единообразно образовывались на поверхности баллона. Эти кристаллы паклитаксела длинных полых объектов имеют длинные оси, и вытянутые тельца (приблизительно 10 мкм), имеющие длинные оси, образовывались так, что они располагались в направлении, практически перпендикулярном поверхности баллона. Диаметр вытянутого тельца составлял приблизительно 2 мкм. Кроме того, поперечное сечение вытянутого тельца на поверхности, перпендикулярной длинной оси, представляло собой многоугольник. Многоугольник представлял собой, например, четырехугольник. Кроме того, эти практически единообразные длинные полые объекты паклитаксела единообразно и плотно (при той же плотности) образовывались на всей поверхности баллона в одной и той же морфологической форме (структура и форма).
С другой стороны, изображения SEM на фиг.6A и фиг.6B в примере 6 демонстрируют слой, включающий плоскую волосообразную морфологическую форму и морфологическую форму, в которой аморфная пленка присутствует на поверхности кристаллов плоской волосообразной формы, которые представляли собой кристаллы паклитаксела плоской вытянутой волосообразной формы. Многие из этих кристаллов имеют сравнительно большой размер, равный или превышающий 20 мкм, и длинные оси присутствуют в состоянии, наклоненном вдоль поверхности баллона (фиг.6A). Кроме того, как показано на фиг.6B, присутствовала область, в которой верхняя часть слоя, включающая плоскую волосообразную морфологическую форму, покрыта аморфной пленкой. В этой области слой, включающий морфологическую форму, в которой слой аморфной пленки присутствует на плоской кристаллической структуре, образуется два слоя из кристаллов и аморфного вещества, и на поверхности кристаллов плоской волосообразной формы присутствует аморфная пленка.
На фиг.6 согласно сравнительному примеру 1 представлено изображение SEM слоя лекарственного покрытия коммерчески доступного баллона, выделяющего лекарственное средство (IN.PACT), изготавливаемого INVAtec JAPAN. В нем аморфное вещество и кристаллы были смешаны в одной и той же плоскости. Было выявлено, что большинство из них были практически аморфными и подобные иглам кристаллы были частично смешаны в той же плоскости.
[0038]
[Эффект ингибирования внутрисосудистого стеноза в коронарной артерии свиньи и эффект на ремоделирование кровеносных сосудов]
Для примеров 1 и 6, сравнительного примера 1 (C1: коммерчески доступный баллон), и сравнительного примера 2 (C2: не покрытый лекарственным средством баллон), эффект ингибирования внутрисосудистого стеноза в коронарной артерии свиней и эффект на ремоделирование кровеносных сосудов оценивали по следующей методике.
1. Способ
(1) Проводниковый катетер с проволочным проводником помещали в оболочку 8Fr и направляли в открытую часть левой и правой коронарных артерий под контролем рентгеновской флуороскопии.
(2) Проводили ангиографию каждой коронарной артерии (коронарная артерия: левая передняя нисходящая коронарная артерия (LAD), правая коронарная артерия (RCA) и левая огибающая коронарная артерия c (LCX)), и полученный диаметр коронарной артерии измеряли с использованием программного обеспечения QCA.
(3) Выбирали область, в которой диаметр стента в 1,2 раза, а диаметр баллона, выделяющего лекарственное средство, в 1,3 раза превышает диаметр кровеносного сосуда, и проводили исследование после установки стента.
(4) После расширения в течение 30 секунд так, чтобы стент BMS (непокрытый металлический стент) (диаметр стента 3 мм × длина 15 мм) в выбранной коронарной артерии составлял 1,2 раза, баллонный катетер для установки стента удаляли. В области установки стента после того, как баллон, выделяющий лекарственное средство (диаметр баллона 3 мм × длина 20 мм), имеющий слой лекарственного покрытия, полученный согласно примерам 1 и 6 и сравнительным примерам 1 и 2, расширяли в течение 1 минуты так, чтобы он в 1,3 раза превышал диаметр кровеносного сосуда, баллонный катетер удаляли.
(5) После расширения баллона, выделяющего лекарственное средство, направляющий катетер и оболочку удаляли. После лигирования центральной части сонной артерии на щель из расслоившихся мышц разреза цервикальной области накладывали шов, и на кожу накладывали шов с использованием хирургического устройства для наложения скобок.
(6) Через 28 суток после расширения баллона проводили аутопсию.
[0039]
[Способ вычисления уровня внутрисосудистого стеноза]
Уровень внутрисосудистого стеноза вычисляли по следующей методике. Изображения кровеносных сосудов получали с использованием микроскопа Leica и системы визуализации патологии. С использованием этих изображений измеряли внутреннюю площадь внешней эластической пластины, внутреннюю площадь эластической пластины, внутреннюю площадь просвета, внутреннюю площадь стента.
Уровень площади стеноза (%) вычисляли как "уровень площади стеноза = (площадь неоинтимы/ площадь внутренней эластической пластины) × 100".
[0040]
[Способ вычисления содержания фибрина, показатель содержания фибрина]
Оценку содержания фибрина проводили по всему периметру кровеносного сосуда способом Suzuki et al. (NPL 1). NPL 1: Suzuki Y., et. al Stent-based delivery of sirolimus reduces neointimal formation in aprocine coronary model. Circulation 2001; 1188-93.
Показатель содержания фибрина оценивали следующим образом. Показатель 1: наблюдали фибрин, локализованный в кровеносном сосуде, или фибрин умеренно депонировался в области, составляющей менее 25% всего наблюдаемого периметра кровеносного сосуда вблизи ножки стента. Показатель 2: фибрин умеренно депонируется в области, превышающей 25% всего наблюдаемого периметра кровеносного сосуда, или фибрин значительно депонируется в области, составляющей менее 25% всего наблюдаемого периметра кровеносного сосуда между ножками и вблизи ножки. Показатель 3: фибрин значительно депонируется в области, составляющей более 25% от всего наблюдаемого периметра кровеносного сосуда.
Кроме того, все показатели получали путем вычисления средней величины для трех областей, т.е. проксимальной области, средней области и дистальной области участков установки стента для каждого кровеносного сосуда.
[0041]
[Способ вычисления показателя эндотелиализации, показатель эндотелиализации]
Показатель эндотелизации включал следующее. Показатель 1: вплоть до 25% всего наблюдаемого периметра просвета сосуда покрыто эндотелиальными клетками. Показатель 2: от 25% до 75% всего наблюдаемого периметра просвета сосуда покрыто эндотелиальными клетками. Показатель 3: 75% или более всего наблюдаемого периметра просвета сосуда покрыто эндотелиальными клетками.
Кроме того, все показатели вычисляли в качестве средней величины для трех положений, т.е. проксимального, среднего и дистального положения участка установки стента для каждого кровеносного сосуда.
[0042]
2. Результаты для ингибирования внутрисосудистого стеноза в коронарной артерии свиньи
Уровень внутрисосудистого стеноза вычисляли по описанной выше методике. В таблице 2 представлены полученные результаты. В таблице 2, 1 и 6 в колонке примеры/сравнительные примеры представляют собой примеры и C1-C2 представляют собой сравнительные примеры.
Кроме того, на фиг.8 представлен график, на котором показан уровень стеноза кровеносных сосудов в случае примеров 1 и 6, и сравнительных примеров C1-C2 для эффекта ингибирования внутрисосудистого стеноза в коронарных артериях свиней. На фиг.8 горизонтальная ось соответствует примерам или сравнительным примерам, и числа 1 и 6 означают примеры 1 и 6 соответственно, и числа с буквами, т.е. C1 и C2, означают сравнительный пример 1 (C1) и сравнительный пример 2 (C2) соответственно. Кроме того, на вертикальной оси представлен уровень площади стеноза (единицы: %) кровеносного сосуда.
[0043]
В сравнительном примере 2 (C2) уровень площади стеноза кровеносного сосуда, в который вводили не покрытый лекарственным средством баллон в качестве контроля без обработки лекарственным средством, составил 38,9%. Уровень площади стеноза кровеносного сосуда, в который вводили баллон, выделяющий лекарственное средство, согласно примеру 6 составил 20,6% и был подтвержден значительный эффект ингибирования стеноза по сравнению с контролем без обработки лекарственным средством. С другой стороны, уровень площади стеноза кровеносного сосуда, в который вводили коммерчески доступный баллон, выделяющий лекарственное средство, (IN.PACT) согласно сравнительному примеру 1 составил 30,4%, и было обнаружено, что уровень площади стеноза имеет тенденцию к снижению по сравнению с непокрытым лекарственным средством баллоном; однако было оценено, что существует достаточно возможностей для увеличения этого эффекта.
[0044]
В противоположность этому, уровень площади стеноза кровеносного сосуда, в который вводили баллон, выделяющий лекарственное средство, в соответствии с настоящим изобретением согласно примеру 1 составил 16,8%, и наблюдали значительный эффект ингибирования стеноза по сравнению с контролем без обработки лекарственным средством и в IN.PACT сравнительного примера 1 (C1). Кроме того, он продемонстрировал более выраженный эффект, чем пример 6, и был достигнут наилучший эффект ингибирования стеноза.
Исходя из того, что описано выше, стало очевидным, что баллон, выделяющий лекарственное средство, со слоем лекарственного покрытия, имеющим кристаллическую морфологическую форму паклитаксела в соответствии с настоящим изобретением согласно примерам 1 и 6, проявляет значительно более выраженный эффект ингибирования стеноза, чем коммерчески доступный баллон, выделяющий лекарственное средство.
[0045]
[Таблица 2]
[0046]
3. Результаты для ремоделирования кровеносных сосудов после установки стента в коронарную артерию свиньи (токсичность)
В качестве эффекта (токсичность) на ремоделирование кровеносных сосудов после установки стента в коронарную артерию свиньи наблюдали показатель содержания фибрина и показатель эндотелиализации. Результаты представлены в таблице 3. Более того, показатель содержания фибрина отражает, что чем большим является число показателя, тем большим является содержание фибрина, что не является предпочтительным. С другой стороны, показатель эндотелиализации отражает, что чем меньшим является число показателя, тем меньше кровеносного сосуда покрыто эндотелиальным клетками, что не является предпочтительным. В таблице 3, 1 и 6 в столбце примеры/сравнительные примеры представляют собой примеры и C1 и C2 представляют собой сравнительные примеры.
[0047]
Показатель содержания фибрина и показатель эндотелиализации кровеносного сосуда, в который вводили непокрытый лекарственным средством баллон в качестве контроля без обработки лекарственным средством в сравнительном примере 2 (C2), указывает на отсутствие влияния на ремоделирование сосудов, поскольку отсутствует эффект (токсичность) лекарственных средств, и показатели составляли 1,00±0,00 и 3,00±0,00 соответственно.
Показатель содержания фибрина и показатель эндотелиализации для сравнительного примера 1 (C1) составляли 1,27±0,15 и 2,80±0,11 соответственно, и показатели были практически такими же, как и показатели в случае не покрытого лекарственным средством баллона. Было оценено, что эффект (токсичность) на ремоделирование сосудов также является небольшим, поскольку эффект ингибирования стеноза лекарственными средствами является небольшим.
[0048]
С другой стороны, показатель содержания фибрина и показатель эндотелиализации кровеносного сосуда, в который вводили баллон, выделяющий лекарственное средство, в соответствии с настоящим изобретением согласно примеру 6 составляли 2,61±0,16 и 1,78±0,17 соответственно, и было предположено, что эффект на ремоделирование сосудов был более высоким по сравнению со сравнительным примером 1 (C1) и сравнительным примером 2 (C2). Было сделано заключение, что это является следствием того, что эффект ингибирования стеноза является более выраженным, чем в случае сравнительного примера 1 (C1) и сравнительного примера 2 (C2).
В противоположность этому, показатель содержания фибрина и показатель эндотелиализации кровеносного сосуда, в который вводили баллон, выделяющий лекарственное средство, в соответствии с настоящим изобретением согласно примеру 1 составили 1,53±0,17 и 2,87±0,09 соответственно, и очевидно, что эффект (токсичность) на ремоделирование сосудов был таким же, как эффект коммерчески доступного продукта в сравнительном примере 1 (C1), и, несмотря на то, что был достигнут высокий эффект ингибирования стеноза, токсичность была крайне низкой.
На основе того, что описано выше, баллон, выделяющий лекарственное средство из слоя лекарственного покрытия, имеющий кристаллическую морфологическую форму паклитаксела в соответствии с настоящим изобретением согласно примеру 6, имеет значительно более выраженный эффект ингибирования стеноза. Кроме того, стало очевидно, что баллон, выделяющий лекарственное средство из слоя лекарственного покрытия, имеющий кристаллическую морфологическую форму паклитаксела в соответствии с настоящим изобретением согласно примеру 1, имеет значительно более выраженный эффект ингибирования стеноза, практически не проявляет эффекта (токсичность) на ремоделирование сосудов, и, таким образом, он является превосходным баллоном, выделяющим лекарственное средство, с точки зрения эффективности и побочных эффектов (токсичность).
[0049]
[Таблица 3]
Группа изобретений относится к области разработки лекарственных покрытий. Слой лекарственного покрытия имеет морфологическую форму, включающую множество вытянутых телец независимых кристаллов нерастворимого в воде лекарственного средства, имеющих продольные оси на поверхности подложки. При этом продольные оси вытянутых телец имеют линейную форму и образуют угол в диапазоне от 45° до 135° относительно плоскости подложки, с которой длинная ось вытянутых телец пересекается. Также раскрывается медицинское устройство, имеющее слой лекарственного покрытия, и способ доставки лекарственного средства. Группа изобретений обеспечивает повышение эффекта ингибирования внутрисосудистого стеноза в области очага повреждения и понижение токсичности. 3 н. и 4 з.п. ф-лы, 8 ил., 3 табл., 8 пр.
1. Слой лекарственного покрытия, имеющий морфологическую форму, включающую множество вытянутых телец независимых кристаллов нерастворимого в воде лекарственного средства, имеющих продольные оси на поверхности подложки, причем продольные оси вытянутых телец имеют линейную форму, и продольные оси вытянутых частиц образуют угол в диапазоне от 45° до 135° относительно плоскости подложки, с которой длинная ось вытянутых телец пересекается.
2. Слой лекарственного покрытия по п.1, в котором по меньшей мере вблизи дистальной области вытянутое тельце является полым.
3. Слой лекарственного покрытия по п.1 или 2, в котором форма поперечного сечения поверхности вытянутого тельца, перпендикулярной продольной оси, является многоугольной.
4. Слой лекарственного покрытия по п.1, в котором нерастворимое в воде лекарственное средство представляет собой рапамицин, паклитаксел, доцетаксел или эверолимус.
5. Слой лекарственного покрытия по п.1, в котором упомянутая подложка представляет собой непористый баллон.
6. Медицинское устройство, имеющее слой лекарственного покрытия по любому из пп.1-5 на поверхности медицинского устройства, где медицинское устройство уменьшается в диаметре для доставки, когда его доставляют в организм, и увеличивается в диаметре для высвобождения лекарственного средства из слоя лекарственного покрытия в пораженной области.
7. Способ доставки лекарственного средства, включающий доставку медицинского устройства по п.6 в просвет, радиальное расширение расширяющейся части, находящейся в медицинском устройстве, и прикладывание слоя лекарственного покрытия, который имеет расширяющуюся часть, к просвету.
| WO 2010079218 A2, 15.07.2010 | |||
| WO 2011008393 A2, 20.01.2011 | |||
| WO 2011119159 A1, 29.09.2011 | |||
| WO 2009051614 A1, 23.04.2009. |
Авторы
Даты
2018-03-26—Публикация
2014-04-01—Подача