Область техники
Настоящее изобретение относится к комбинированной композиции, содержащей метформин, применяемый для лечения инсулиннезависимого диабета и т.п., и ингибитор HMG-CoA-редуктазы (3-гидрокси-3-метилглутарил-кофермент А редуктаза), применяемый для лечения дислипидемии, а также к способу ее получения.
Предшествующий уровень техники
Диабет представляет собой хроническое заболевание, характеризующееся высокими уровнями глюкозы в крови, и оно может быть подразделено на два типа: диабет 1 типа, который является причиной того, что поджелудочная железа прекращает продуцировать инсулин, и диабет 2 типа, который является причиной повышения инсулинорезистентности и, одновременно с этим, функционального ухудшения бета-клеток поджелудочной железы.
В частности, по причине инсулинорезистентности, а также высоких уровней глюкозы в крови, диабет типа 2 представляет собой опасное заболевание, которое очень тесно связано с сердечно-сосудистыми заболеваниями, отображающими состояние здоровья, такими как состояние ожирения, гипертензии, дислипидемии, чрезмерного свертывания крови и т.п. Таким образом, известно, что для его лечения необходим соответствующий контроль сопутствующего метаболического заболевания наряду с активным контролем уровней глюкозы в крови.
Сердечно-сосудистые заболевания представляют собой очень часто встречающиеся и серьезные заболевания у пациентов с диабетом. Фактически, на макрососудистые осложнения, такие как коронарная недостаточность, цереброваскулярное заболевание и заболевание периферических артерий, приходится примерно 75% причин смерти пациентов с диабетом. Как правило, пациенты с диабетом имеют примерно в 2-4 раза более высокий риск развития сердечно-сосудистого заболевания, чем нормальные люди. Так как сердечнососудистое заболевание проявляется в относительно молодом возрасте и распространяется по всему организму, коэффициент смертности, являющейся следствием заболевания, как известно, является очень высоким. Кроме того, так как в публикации аналитического отчета раскрыто, что пациент с диабетом, имеющий в анамнезе сердечно-сосудистое заболевание, может иметь такую же степень проявления сердечно-сосудистого заболевания или последующей вероятности смерти, как и пациент без диабета, но с сердечнососудистым заболеванием в анамнезе, третья группа экспертов по лечению взрослых (АТР III) Национальной образовательной программы по холестерину США (the National Cholesterol Education Program NCEP) признала диабет эквивалентным по риску сердечно-сосудистому заболеванию (CVD) и рекомендовала, чтобы пациенты с диабетом точно следовали рекомендациям по профилактике в той же степени, что и пациенты с сердечно-сосудистым заболеванием в анамнезе.
Примеры терапевтических способов снижения риска сердечно-сосудистого заболевания у пациентов с диабетом могут включать регулирование кровяного давления, уровней глюкозы и липидов в крови, и среди них наиболее эффективным, как известно, является регулирование уровня липидов. Согласно национальным и зарубежным рекомендациям по лечению, следует активно лечить дислипидемию у пациентов с диабетом и в качестве начального лечения рекомендуется применение ингибитора HMG-СоА-редуктазы, являющегося лекарством на основе статина. Таким образом, применение метформина, то есть инсулиннезависимое лечение диабета за счет эффекта понижения уровней глюкозы в крови, и использование ингибитора HMG-CoA-редуктазы, то есть лечение дислипидемии, описывают как наиболее эффективные способы лечения дислипидемии у пациентов с диабетом. Однако, когда у пациентов с диабетом, которым одновременно вводили ингибитор HMG-CoA-редуктазы и гипогликемический агент путем перорального введения, проверяли соблюдение ими режима приема лекарственного средства в течение двух лет, введение пациентам по меньшей мере 80% этих лекарств показывало соблюдение режима приема лекарства на 52% для ингибитора HMG-CoA-редуктазы и соблюдение режима приема лекарства на 63% для гипогликемического агента при пероральном введении, что, таким образом, подтверждает, что лекарственное средство для лечения дислипидемии демонстрировало относительно низкое соблюдение режима приема лекарства (р<0,001). Следовательно, существует потребность в улучшении соблюдения правильного режима его приема.
В связи с этим в настоящем изобретении предложена комбинированная композиция, содержащая метформин, представляющий собой гипогликемический агент для перорального введения, и ингибитор HMG-CoA-редуктазы в качестве активных ингредиентов, для улучшения соблюдения режима приема лекарственного средства, описанного выше.
Метформин представляет собой эффективный гипогликемический агент для перорального введения, широко используемый для предупреждения и лечения проявления и ухудшения осложнений диабета (например, сердечнососудистого заболевания, и так далее). Однако метформин хорошо растворим в воде, и поэтому важно получать метформин в форме композиции, способной контролировать его эффективное замедленное высвобождение, а это может вызвать проблему в разработке комбинированной композиции, содержащей метформин и другие активные ингредиенты, имеющие разные свойства. А именно, из-за высокой растворимости метформина в воде, когда метформин находится в составе обычной таблетки, он может высвобождаться быстро с вызыванием чрезмерного снижения уровней глюкозы в крови и также может вызывать желудочно-кишечное расстройство. Кроме того, метформин обычно вводят в дозе от 500 мг до 850 мг два или три раза в сутки в виде таблетки с быстрым высвобождением (суточный максимум 2550 мг) и, таким образом, быстрое изменение уровней глюкозы в крови, вследствие его быстрого высвобождения, может спровоцировать неблагоприятные взаимодействия и резистентность к метформину.
Для получения композиций метформина с замедленным высвобождением, в патенте Кореи №10-0774774 раскрыт способ контролирования высвобождения метформина с использованием производного сложного эфира жирной кислоты, являющегося нерастворимым в воде носителем для замедленного высвобождения, и в международной публикации WO 09/117130 раскрыт способ контролирования высвобождения водорастворимых лекарств, содержащих метформин, за счет использования максимум 40% восков. Однако в существующих композициях с замедленным высвобождением хорошо растворимых в воде лекарств, где лекарства внедрены в полимерную матрицу с использованием нерастворимого в воде агента или окружены полимерной мембраной, может иметь место быстрое высвобождение лекарств на начальной стадии из-за медленной скорости гидратации полимера, используемого в них, и последующее быстрое изменение их концентрации в крови может провоцировать вредные взаимодействия и резистентность к метформину из-за быстрого изменения уровней глюкозы в крови. Кроме того, недостаток может заключаться в том, что для создания замедленного высвобождения требуется очень большое количество полимера.
В целях решения этих проблем, в международных публикациях WO 98/055107, WO 99/047125, WO 99/047128, WO 02/036100 и WO 03/028704, а также в патентах Кореи №10-0772980, 10-0791844 и 10-1043816 раскрыты композиции с замедленным высвобождением метформина, в которых используются гидрофильные набухающие полимеры. В этих композициях метформина с замедленным высвобождением, в которых используются гидрофильные набухающие полимеры, стабильный паттерн высвобождения лекарства может быть получен посредством обеспечения немедленной гидратации гидрофильного полимера в водном растворе. Однако такой набухающий полимер, выбранный в качестве носителя для замедленного высвобождения метформина, может создать неизбежную проблему при разработке комбинированных композиций, поскольку такие агенты, имеющие высокую вязкость и высокую молекулярную массу, располагаются на наружной поверхности гранул и задерживают высвобождение лекарств, которые подлежат немедленному высвобождению. Следовательно, существует потребность в разработке технологии для преодоления этой проблемы.
В то же время ингибитор HMG-CoA-редуктазы обладает превосходным эффектом понижения уровня LDL-холестерина, может понижать уровень триглицеридов и повышать уровень HDL-холестерина, в то же время демонстрируя стабильность и резистентность к лекарственному средству с незначительными неблагоприятными эффектами, и, таким образом, широко используется для лечения дислипидемии. Ингибитор HMG-CoA-редуктазы имеет длительный период полувыведения от 20 до 30 часов, но его биодоступность не является высокой. Так как он может абсорбироваться по всему желудочно-кишечному тракту, будет предпочтительно, если активный ингредиент сможет быстро высвобождаться из рассматриваемой композиции.
По имеющимся сообщениям, ингибитор HMG-CoA-редуктазы может быть быстро разложен и/или окислен, когда он подвергается неблагоприятным физическим и/или химическим условиям. Поэтому в течение долгого времени были проведены многочисленные исследования, сфокусированные на улучшении стабильности. Например, в опубликованной заявке на патент Великобритании №2262229 раскрыт фармацевтический препарат натриевой соли 7-замещенной-3,5-дигидрокси-6-гептеновой кислоты, являющейся ингибитором HMG-CoA-редуктазы, и описано, что получение требует щелочной среды (например, карбонат, бикарбонат), способной придавать водному раствору или дисперсии композиции значение рН, равное по меньшей мере 8.
Кроме того, согласно предшествующему сообщению в журнальной статье (Determination of Rosuvastin in the Presence of Its Degradation Products by a Stability-Indicating LC Method (Journal of AOAC International Vol. 88, No. 4, 2005)), кальциевая соль розувастатина может легко разлагаться в кислых условиях при рН, равном 5 или ниже, и в результате окисления, воздействия солнечного света или высокой температуры и, как и в случае композиции, гранулированный продукт с большей поверхностью, подвергающейся воздействию окружающей среды, является менее стабильным, чем непокрытая таблетка, а покрытая пленкой таблетка является более стабильной, чем непокрытая таблетка. Кроме того, в другой журнальной статье (Stability study of cholesterol powering statin drug in aqueous samples using HPLC and LC-MS (Environ Chem Lett (2010) 8; 185)), раскрыты стабильности симвастатина, ловастатина и правастатина в зависимости от рН, солнечного света или растворителя.
В связи с этим, в публикации международной заявки WO 00/35425 раскрыта попытка стабилизировать смесь статина за счет использования буферного агента, способного обеспечивать рН от 7 до 11, и в патенте Кореи №10-0388713 раскрыт трехосновный фосфат, в патенте Кореи №10-0698333 раскрыт способ стабилизации розувастатина за счет использования фармацевтической композиции, в которой противоанион представляет собой неорганическую соль, отличную от фосфата. Кроме того, в патентах США №5686104 и №6126971 раскрыто, что аторвастатин стабилизируют добавлением фармацевтически приемлемого щелочноземельного металла.
В этом аспекте для изготовления комбинированной композиции, содержащей метформин и ингибитор HMG-CoA-редуктазы, необходимо надлежащим образом контролировать высвобождение in vivo каждого активного ингредиента, одновременно с этим обеспечивая, чтобы не могли иметь место неблагоприятные эффекты (например, ухудшение стабильности и т.п.) между двумя ингредиентами вследствие комбинирования двух разных соединений. Конкретно, комбинированную композицию следует компоновать таким образом, чтобы обеспечивать стабильный паттерн замедленного высвобождения активного ингредиента для метформина, обеспечивая при этом стабильность к разложению и окислению для ингибитора HMG-CoA-редуктазы, одновременно при этом делая возможным паттерн немедленного высвобождения указанного активного ингредиента.
Однако, как описано выше, агент замедленного высвобождения для метформина может подавлять немедленное высвобождение ингибитора HMG-CoA-редуктазы, создавая, таким образом, трудность для разработки композиции, которая может одновременно обеспечивать желательные скорости высвобождения для обоих ингредиентов. Стабилизирующий агент для стабилизации ингибитора HMG-CoA-редуктазы может обладать отрицательным воздействием на скорость высвобождения и т.п., метформина. То есть имеет место высокий риск того, что агент замедленного высвобождения или стабилизирующий агент и т.п., которые содержатся в комбинированной композиции, могут оказывать отрицательное воздействие на совместную стабильность лекарств и их скорости высвобождения, и таким образом нелегко разработать комбинированную композицию, способную гарантировать оптимальную стабильность и скорость высвобождения.
С целью контролирования замедленного высвобождения метформина были проведены многочисленные исследования на композициях различных типов, которые могут препятствовать быстрому высвобождению лекарств посредством создания композиции матричного типа, содержащей определенное количество набухающих агентов замедленного высвобождения с высокой молекулярной массой и высокой вязкостью.
Как правило, набухающие агенты для замедленного высвобождения представляют собой гидрофильные полимеры, имеющие трехмерную сетчатую структуру, в которой они плотно связаны физически или химически, и, таким образом, они набухают и образуют гидратированный гель в течение короткого периода времени после приведения в контакт с водным раствором, тем самым препятствуя немедленному высвобождению лекарств. Однако при разработке комбинированной композиции, которая одновременно обеспечивает как замедленное высвобождение типа удерживания в желудке за счет использования набухающих агентов, так и немедленное высвобождение для лекарства, быстро высвобождаемого в начальном высвобождении, имеет место проблема, заключающаяся в том, что высвобождение лекарства, предназначенного для немедленного высвобождения, задерживается из-за высокой вязкости набухающих агентов для замедленного высвобождения.
Для того чтобы решить эти проблемы, в международной заявке РСТ/ЕР2003/004472 раскрыта многослойная таблетка, в которой каждое лекарство содержится в особом слое и между ними предусматривается инертный слой; и в заявке Кореи на патент №10-2012-0120519 также раскрыта многослойная таблетка, в которой каждое лекарство содержится в особом слое и между ними предусмотрен промежуточный слой, который не содержит лекарства.
Технологии, раскрытые выше, предпринимались для минимизации физических и химических взаимодействий между лекарствами с использованием системы на основе многослойной таблетки, тем самым делая возможными улучшенную стабильность и эффективное высвобождение каждого лекарства. Однако многослойная таблетка имеет недостатки, поскольку изготовление многослойных таблеток, состоящих по меньшей мере из трех слоев, вызывает существенную потерю ингредиентов во время обработки, увеличивает продолжительность работы, а также дополнительно увеличивает массу таблетку из-за дополнительного промежуточного слоя, таким образом затрудняя применение такой технологии к композиции с замедленным высвобождением с высокой дозой метформина.
В то же время, в публикации международной заявки WO 03/026637 раскрыта комбинированная композиция, изготовленная посредством нанесения слоя нерастворимого в воде полимера на композицию с контролируемым высвобождением в качестве промежуточного слоя, в то время как в композиции с немедленным высвобождением его наносят на наружный слой, и в патенте Кореи №10-0705210 раскрыт комбинированный препарат, в котором водорастворимый полимер наносят на композицию с замедленным высвобождением в качестве промежуточного слоя, в то время как в композиции с немедленным высвобождением им покрывают наружный слой. Эти технологии описывают нанесение покрытия на промежуточный слой, расположенный между двумя различными лекарствами и таким образом минимизируют физические и химические взаимодействия, улучшают стабильность и снижают массу таблеток.
Однако, поскольку лекарство для немедленного высвобождения следует наносить на наружную часть композиции с замедленным высвобождением, кристаллическая форма активных ингредиентов может быть изменена во время процесса растворения или диспергирования лекарства для немедленного высвобождения, а также существует проблема с коммерческой точки зрения, потому что трудно гарантировать однородность содержимого в течение процесса покрытия в крупномасштабном производстве. Кроме того, может быть желательно применять технологии к тем компонентам, которые, в вышеупомянутых патентах, содержатся в композиции в следовых количествах в качестве активных ингредиентов. Однако существует ограничение для применения этих технологий к лекарствам с относительно высокой дозой и, таким образом, нежелательно применять эти технологии к композиции на основе кальциевой соли аторвастатина, имеющей единичную дозировку от 10 мг до 80 мг.
При таких обстоятельствах авторами настоящего изобретения были приложены интенсивные усилия для разработки композиции, способной гарантировать оптимальную стабильность и скорость высвобождения, и в результате было обнаружено, что, в условиях комбинированной композиции, состоящей из первой композиции с замедленным высвобождением, которая состоит из гранул, содержащих метформин или его фармацевтически приемлемую соль и набухающий полимер, и нерастворимой в воде полимерной пленки, окружающей гранулы, и второй композиции с немедленным высвобождением, содержащей ингибитор HMG-CoA-редуктазы, может быть предложена комбинированная композиция с эффективно улучшенной стабильностью за счет предупреждения физических и химических взаимодействий между активными ингредиентами, которая в то же время обеспечивает стабильное высвобождение каждого активного ингредиента, содержащегося в ней, тем самым завершив настоящее изобретение.
Описание изобретения
Техническая проблема
Целью настоящего изобретения является обеспечение комбинированной композиции с эффективно улучшенной стабильностью за счет предупреждения физических и химических взаимодействий между активными ингредиентами, которая в то же время обеспечивает стабильное высвобождение каждого активного ингредиента, содержащегося в ней, и способ ее получения.
Решение технической проблемы
Цель настоящего изобретения заключается в обеспечении фармацевтической композиции, содержащей метформин, который лечит неинсулинзависимый диабет и т.п., и лекарство на основе статина, которое применяют для лечения дислипидемии и т.п. Более подробно, настоящее изобретение относится к композиции с двухфазной системой, которая способна контролировать начальное «взрывное» высвобождение лекарства для замедленного высвобождения, при этом быстро высвобождая лекарство для немедленного высвобождения на начальной стадии, не подвергаясь воздействию набухающего агента с высокой вязкостью, а также улучшать стабильность лекарства путем изготовления гранул, покрытых нерастворимым в воде полимером, где гранулы содержат метформин или его фармацевтически приемлемую соль и набухающий полимер.
Полезные эффекты изобретения
Система контроля высвобождения лекарственного средства, согласно настоящему изобретению, обеспечивает улучшенные удобство и соблюдение правильного режима введения путем подавления начального «взрывного» высвобождения посредством двойного контроля высвобождения вследствие одновременного использования набухающего полимера и нерастворимого в воде полимера, при этом полимеры используют в небольших количествах. Кроме того, система по настоящему изобретению может контролировать задержку при немедленном высвобождении за счет использования нерастворимой в воде полимерной пленки на гранулах с замедленным высвобождением. Таким образом, система контроля высвобождения лекарственного средства, согласно настоящему изобретению, обеспечивает эффективную двухфазную систему с замедленным высвобождением и с немедленным высвобождением.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
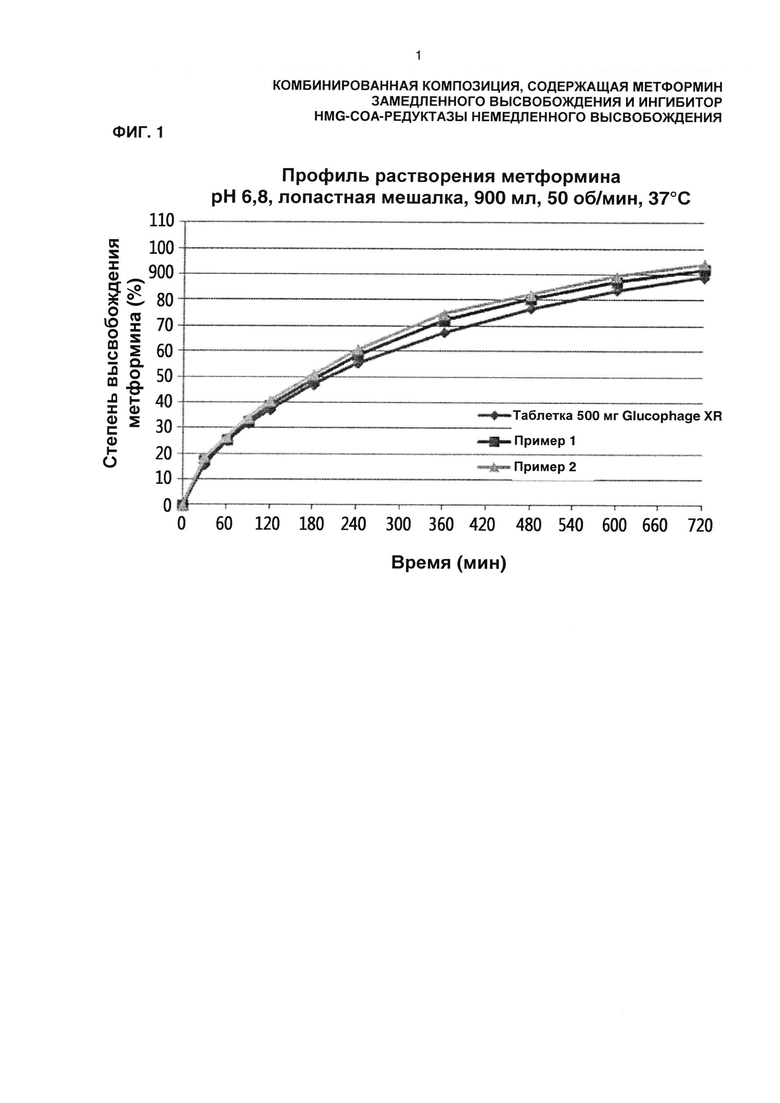
На ФИГ. 1 показаны результаты испытания на высвобождение для комбинированных композиций, полученных в Примерах 1 и 2 настоящего изобретения, и для таблетки Glucophage XR® 500 мг.
На ФИГ. 2 показаны результаты испытания на высвобождение для комбинированных композиций, полученных в Примерах 1 и 2 настоящего изобретения, и для таблетки Lipitor 10 мг.
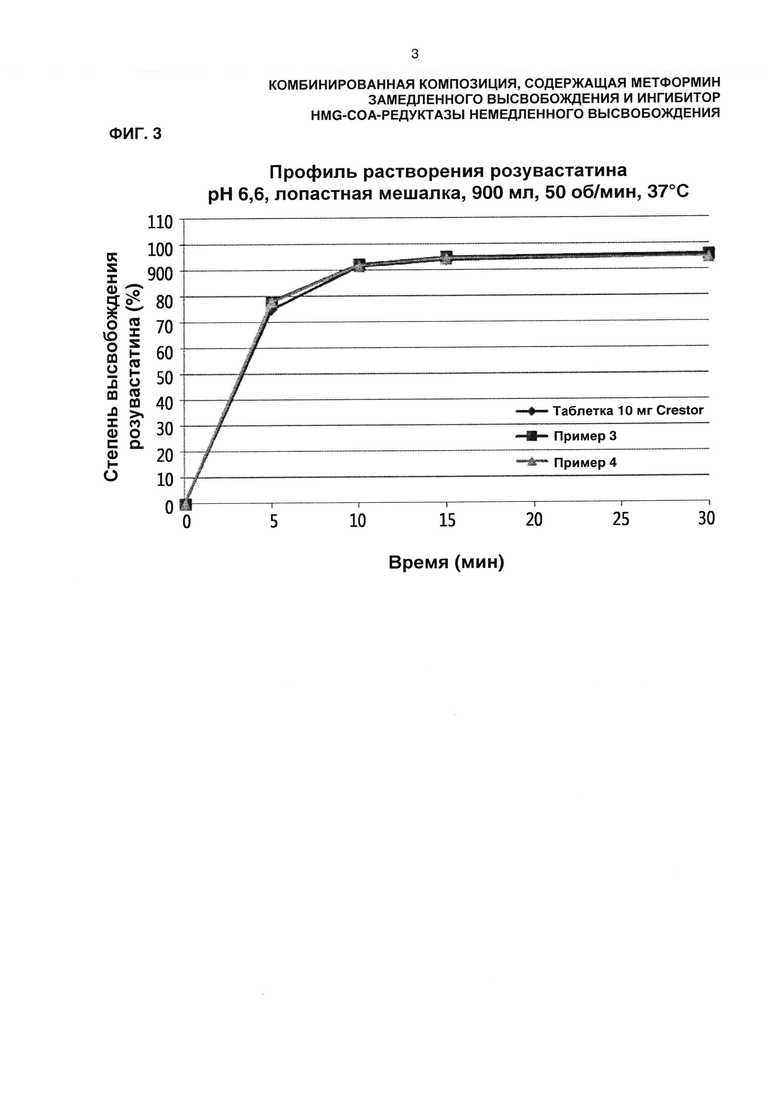
На ФИГ. 3 показаны результаты испытания на высвобождение для комбинированных композиций, полученных в Примерах 3 и 4 настоящего изобретения, и для таблетки Crestor 10 мг.
ЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Предпочтительные воплощения настоящего изобретения более подробно будут описаны ниже со ссылкой на сопутствующего графические материалы. Настоящее изобретение можно, однако, воплощать в разных формах, и оно не должно быть истолковано как ограниченное воплощениями, изложенными в данном описании изобретения. Наоборот, эти воплощения предлагаются для того, чтобы описание настоящего изобретения было всесторонним и полным, а также полностью передавало информацию об объеме настоящего изобретения специалисту в данной области техники.
Для решения вышеупомянутых проблем в настоящем изобретении предложена комбинированная композиция, содержащая первую композицию с замедленным высвобождением, которая включает гранулы, содержащие метформин или его фармацевтически приемлемую соль и набухающий полимер, а также нерастворимую в воде полимерную пленку для покрытия указанных гранул, и вторую композицию с немедленным высвобождением, содержащую ингибитор HMG-CoA-редуктазы.
При использовании в описании настоящего изобретения термин "первая композиция с замедленным высвобождения" относится к композиции, содержащей метформин или его фармацевтически приемлемую соль, способной к длительному высвобождению вышеупомянутых веществ путем предотвращения их быстрого высвобождения. Для замедленного высвобождения метформину или его фармацевтически приемлемой соли вместе с набухающим полимером придают форму гранул и каждую отдельную гранулу покрывают нерастворимой в воде полимерной пленкой.
При использовании в описании настоящего изобретения термин "метформин" относится к соединению с химическим названием N,N-диметилимиддикарбоимид диамид (Формула 1 ниже), который используют в качестве терапевтического агента для предотвращения или лечения неинсулинзависимого диабета.
Формула 1
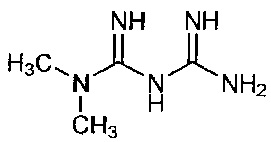 .
.
Метформин можно получать посредством выделения из природных источников, посредством изготовления при помощи химической модификации после его получения из природной источников или, без труда, путем химического синтеза согласно способу, известному специалисту в данной области техники. Альтернативно, для применения можно приобретать имеющийся в продаже метформин.
Предпочтительно, метформин или его фармацевтически приемлемая соль могут содержаться в комбинированной композиции по настоящему изобретению в количестве от 250 мг до 1000 мг.
При использовании в данном описании изобретения термин "набухающий полимер" относится к фармацевтически приемлемому полимеру, который становится набухшим в водном растворе, тем самым позволяя контролировать высвобождение лекарства. В настоящем изобретении набухающий полимер образует гранулы вместе с метформином или его фармацевтически приемлемой солью и обладает свойством замедленного высвобождения вышеупомянутых веществ. Набухающий полимер, который можно использовать в настоящем изобретении, может включать по меньшей мере один, выбранный из группы, состоящей из гидроксипропилметилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилцеллюлозы, полиэтиленоксида, каррагинана, природной камеди, гуаровой камеди, трагаканта, аравийской камеди, камеди бобов рожкового дерева, ксантановой камеди, поливинилового спирта и поливинилпирролидона, и, предпочтительно, гидроксипропилметилцеллюлозу или полиэтиленоксид, но не ограничивающейся ими, а именно он представляет собой фармацевтически приемлемый набухающий полимер, дающий возможность контролируемого высвобождения в соответствии с целями настоящего изобретения. Предпочтительно, набухающий полимер имеет вязкость 100 сП (0,1 Па⋅с) или выше.
Предпочтительно, набухающий полимер может содержаться в комбинированной композиции в количестве от 10% масс. до 40% масс. в расчете на общую массу первой композиции с замедленным высвобождением. Когда набухающий полимер содержится в количестве менее 10% масс., тогда становится трудно выполнять эффективный контроль высвобождения лекарства, тогда как, если набухающий полимер содержится в количестве более 40% масс., то размер таблеток становится слишком большим для введения, и, таким образом, это неуместно.
Гранулы по настоящему изобретению, содержащие метформин или его фармацевтически приемлемую соль и набухающий полимер, формируют посредством покрытия наружной поверхности нерастворимым в воде полимером.
При использовании в данном описании изобретения термин "нерастворимый в воде полимер" относится к фармацевтически приемлемому полимеру, способному к контролируемому высвобождению лекарственного средства, который является нерастворимым в воде или трудно растворимым в воде. Кроме того, цели использования нерастворимого в воде полимера по настоящему изобретению включают не только препятствование высвобождению метформина или его фармацевтически приемлемой соли, но также предотвращение контактирования ингибитора HMG-CoA-редуктазы, содержащегося во второй композиции с немедленным высвобождением, с набухающим полимером. То есть комбинированную композицию согласно настоящему изобретению изготавливают таким образом, чтобы препятствовать физическому контакту и химическому взаимодействию набухающего полимера с ингибитором HMG-CoA-редуктазы за счет покрытия нерастворимой в воде полимерной пленкой.
Настоящее изобретение относится к комбинированной композиции, которая содержит ингибитор HMG-CoA-редуктазы в дополнение к метформину, а набухающий полимер, используемый для замедленного высвобождения метформина или его фармацевтически приемлемой соли, подавляет высвобождение ингибитора HMG-CoA-редуктазы, а также увеличивает количество примесей ингибитора HMG-CoA-редуктазы, тем самым значительно ухудшая стабильность композиции. Таким образом, следует рассматривать тип композиции, которая содержит набухающий полимер для замедленного высвобождения метформина, но не оказывает воздействие на ингибитор HMG-CoA-редуктазы. Для этой цели в настоящем изобретении наружную поверхность гранул, которые содержат метформин или фармацевтически приемлемую соль и набухающий полимер, покрывают нерастворимым в воде полимером, тем самым предотвращая контакт между набухающим полимером и ингибитором HMG-CoA-редуктазы.
В иллюстративном воплощении настоящего изобретения, когда нерастворимый в воде полимер отсутствовал, набухающий полимер имел воздействие на ингибитор HMG-CoA-редуктазы, тем самым снижая скорость высвобождения ингибитора HMG-CoA-редуктазы и увеличивая образование примесей. Напротив, в случае комбинированной композиции по настоящему изобретению с использованием нерастворимой в воде полимерной пленки, первая композиция с замедленным высвобождением и вторая композиция с немедленным высвобождением, соответственно, показывали паттерн высвобождения, аналогичный таковому для одиночной композиции, и отсутствовало увеличение образования примесей. Так как первая композиция с замедленным высвобождением согласно настоящему изобретению не вызывала проблему высокой вязкости в набухающем полимере, при этом эффективно контролируя замедленное высвобождение метформина, эти результаты говорят о том, что агент замедленного высвобождения для метформина не оказывал воздействия на немедленное высвобождение второй композиции с немедленным высвобождением.
Нерастворимый в воде полимер, который можно использовать в настоящем изобретении, может включать по меньшей мере одно вещество, выбранное из группы, состоящей из сополимера метакриловой кислоты, этил целлюлозы, фталата гидроксипропилметилцеллюлозы, гидроксипропилметилцеллюлозы ацетата сукцината, ацетата фталата целлюлозы, жирных кислот, сложных эфиров жирных кислот, спиртов жирных кислот, и восков, и предпочтительно представляет собой сополимер метакриловой кислоты или этилцеллюлозу, однако нерастворимый в воде полимер не ограничивается ими, а именно он представляет собой фармацевтически приемлемый нерастворимый в воде полимер, дающий возможность высвобождения согласно целям настоящего изобретения.
Предпочтительно, нерастворимый в воде полимер согласно настоящему изобретению может содержаться в количестве от 1% масс. до 20% масс. в расчете на общую массу первой композиции с замедленным высвобождением. Когда содержание полимера превышает 20% масс., это будет увеличивать толщину пленки и замедлять гидратацию набухающего полимера, и таким образом не подходит для контролирования начального высвобождения лекарственного средства.
При использовании в описании настоящего изобретения термин "вторая композиция с немедленным высвобождением" относится к композиции, содержащей ингибитор HMG-CoA-редуктазы, которая может полностью распадаться в дистиллированной воде при 37°С в течение 5 минут.
При использовании в данном описании изобретения термин "HMG-CoA," являющийся акронимом для "3-гидрокси-3-метилглутарил-кофермента А", относится к предшественнику для биосинтеза стеринов, включая холестерины. При использовании в описании настоящего изобретения термин "ингибитор HMG-CoA-редуктазы" относится к соединениям, которые обеспечивают эффект понижения уровней общего холестерина и LDL-холестерина in vivo за счет подавления активности HMG-CoA-редуктазы, вовлеченной в ранние стадии превращения HMG-CoA в мевалонат в ходе процесса биосинтеза холестерина. Например, ингибитор HMG-CoA-редуктазы может представлять собой по меньшей мере один, выбранный из розувастатина, аторвастатина, питавастатина, ловастатина, симвастатина, правастатина и флувастатина, или фармацевтически приемлемой соли, но не ограничивается ими. Кроме того, композиции по настоящему изобретению могут дополнительно включать фармацевтически приемлемый подщелачивающий агент. Ингибитор HMG-CoA-редуктазы согласно настоящему изобретению предпочтительно представляет собой аторвастатин или розувастатин. Предпочтительно, ингибитор HMG-CoA-редуктазы может содержаться в комбинированной композиции по настоящему изобретению в количество от 5 мг до 160 мг. Кроме того, в случае розувастатина, он может содержаться в комбинированной композиции по настоящему изобретению в количестве от 5 мг до 40 мг.
Вторая композиция с немедленным высвобождением может дополнительно содержать фармацевтически приемлемый разрыхлитель и/или стимулятор растворения для обеспечения полного распада в дистиллированной воде при 37°С в течение 5 минут. Разрыхлитель и/или стимулятор растворения, которые можно использовать в настоящем изобретении, могут включать по меньшей мере один, выбранный из группы, состоящей из кроскармеллозы натрия, натрия крахмала гликолята, кросповидона, карбоксиметилцеллюлозы натрия, гидроксипропилцеллюлозы с низкой степенью замещения, полисорбата, полоксамера и лаурилсульфата натрия, и предпочтительно, можно использовать кроскармеллозу натрия или кросповидон, но разрыхлитель и/или стимулятор растворения не ограничиваются ими, а именно они представляют собой фармацевтически приемлемые добавки, способные к контролированию распада согласно целям настоящего изобретения.
Комбинированная фармацевтическая композиция согласно настоящему изобретению может сохранять стабильность без каких-либо изменений свойств, даже когда два лекарственные средства метформин или его фармацевтически приемлемая соль и ингибитор HMG-CoA-редуктазы изготовляют и хранят в ходе процесса комбинирования.
При использовании в данном описании изобретения термин "фармацевтически приемлемая соль" относится к такому типу композиции, который не нарушает биологические активности и физические свойства метформина или ингибитора HMG-CoA-редуктазы, подлежащих введению. Фармацевтически приемлемая соль может включать соли присоединения кислоты, которые могут образовывать нетоксичные соли присоединения кислоты, содержащие фармацевтически приемлемые анионы, например, неорганических кислот, таких как соляная кислота, серная кислота, азотная кислота, ортофосфорная кислота, бромистоводородная кислота и иодистоводородная кислота; органических карбоновых кислот, таких как винная кислота, муравьиная кислота, лимонная кислота, уксусная кислота, трихлоруксусная кислота, трифторуксусная кислота, глюконовая кислота, бензойная кислота, молочная кислота, фумаровая кислота, малеиновая кислота и салициловая кислота; сульфоновых кислот, таких как метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота и пара-толуолсульфоновая кислота; и т.п. Например, фармацевтически приемлемая соль может включать соли металлов или соли щелочноземельных металлов, образованные литием, натрием, калием, кальцием, магнием и т.п.; соли аминокислот, таких как лизин, аргинин, гуанидин и т.п.; органические соли, такие как дициклогексиламин, N-метил-D-глюкамин, трис(гидроксиметил)метиламин, диэтаноламин, холин и триэтиламин; и т.п.
Кроме того, комбинированная фармацевтическая композиция по настоящему изобретению может дополнительно включать пленочный слой на наружной поверхности. Пленочный слой может представлять собой, например, защитный пленочный слой, влагонепроницаемый пленочный слой или пленочный слой глюкозы и т.п. Предпочтительно, наружный пленочный слой образован из водорастворимого вещества, которое может включать гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу, ацетат фталат целлюлозы, этилцеллюлозу, метил целлюлозу, полиметакрилат, графт-сополимер поливиниловый спирт-полиэтиленгликоль (Kollicoat®; BASF, Germany), поливиниловый спирт (Opadry®; Colorcon, USA) или их комбинацию, но не ограничивается ими.
Кроме того, комбинированная фармацевтическая композиция по настоящему изобретению может быть изготовлена в виде препарата путем дополнительного применения добавок, обычно используемых в данной области техники, в объеме настоящего изобретения, таких как разбавитель, связывающее вещество, смазывающее вещество, регулятор рН, антивспенивающее вещество, стимулятор растворения, антиоксидант и т.п.
Комбинированная фармацевтическая композиция по настоящему изобретению может быть получена в виде различных типов композиций, например, таблеток, таких как непокрытые таблетки, покрытые пленкой таблетки, однослойные таблетки, двухслойные таблетки, многослойные таблетки, или таблетка с ядром; порошков; гранул; капсул; и т.п. Предпочтительно, комбинированную фармацевтическую композицию по настоящему изобретению получают в форме двухслойной таблетки, состоящей из первой композиции с замедленным высвобождением и второй композиции с немедленным высвобождением.
Полученная таким образом комбинированная фармацевтическая композиция по настоящему изобретению может обеспечивать соответствующие свойства высвобождения, подходящие для каждого из фармацевтически активных ингредиентов за счет длительно высвобождающегося метформина и быстро высвобождающегося ингибитора HMG-CoA-редуктазы во время введения in vivo. Кроме того, удобство введения улучшали за счет снижения содержания агентов замедленного высвобождения, необходимых для замедленного высвобождения метформина, в то время как лекарственное средство для немедленного высвобождения быстро растворяли и стабильность ингибитора HMG-CoA-редуктазы улучшали посредством включения стабилизирующего агента. Таким образом, комбинированную фармацевтическую композицию по настоящему изобретению можно эффективно применять для предупреждения и лечения дислипидемии, дислипидемии, атеросклероза, диабета и осложнений диабета.
В другом типичном воплощении настоящего изобретения предложен способ получения комбинированной композиции, включающий получение первой композиции с замедленным высвобождением путем получения гранул, содержащих метформин или его фармацевтически приемлемую соль и набухающий полимер, с последующим формированием нерастворимой в воде полимерной пленки на гранулах;
получения второй композиции с немедленным высвобождением, содержащей ингибитор HMG-CoA-редуктазы; и
изготовления первой композиции с замедленным высвобождением и второй композиции с немедленным высвобождением в составе единичной композиции.
Кроме того, способ по настоящему изобретению может дополнительно включать формирование пленочного слоя на наружной поверхности комбинированной композиции.
При использовании в данном описании изобретения термины "первая композиция с замедленным высвобождением", "метформин", "набухающий полимер", "нерастворимый в воде полимер", "вторая композиция с немедленным высвобождением", "HMG-CoA", "фармацевтически приемлемая соль" и "пленочный слой" представляют собой такие же, как описано выше.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Ниже настоящее изобретение будет описано более подробно со ссылкой на следующие примеры. Однако эти примеры предназначены только для иллюстративных целей, и не предполагается ограничение изобретения этими примерами.
Пример 1
1) Получение гранул метформина гидрохлорида с замедленным высвобождением
Гранулы метформина гидрохлорида с замедленным высвобождением получали согласно составу и количествам, показанным в таблице 1. Конкретно, метформина гидрохлорид и коллоидный диоксид кремния пропускали через сито 20-меш и смешивали с полиэтиленоксидом (Polyox® WSR301). Затем полученную смесь распыляли с раствором связывающего вещества, в котором смесь растворителей, содержащую изопропиловый спирт, ацетон и очищенную воду, смешанные в соотношении 6:3:1, растворяли в концентрации 10% масс./об. с добавлением сополимера метакриловой кислоты (Eudragit® RS РО), затем сушили в грануляторе с псевдоожиженным слоем, и полученную смесь пропускали через сито 20-меш. Полученный таким образом гранулированный продукт обрабатывали стеаратом магния и перемешивали с получением гранул метформина гидрохлорида с замедленным высвобождением.

2) Получение гранул аторвастатина с немедленным высвобождением
Гранулы аторвастатина с немедленным высвобождением получали согласно составу и количествам, указанным в таблице 2. Конкретно, кальциевую соль аторвастатина, осажденный карбонат кальция, микрокристаллическую целлюлозу, гидрат лактозы и кроскармеллозу натрия смешивали, обрабатывали гидроксипропилцеллюлозой, растворенной в 20% этаноле, с получением гранул, и полученные гранулы сушили в сушилке с псевдоожиженным слоем и затем пропускали через сито 20-меш. Полученный таким образом гранулированный продукт обрабатывали кроскармеллозой натрия и стеаратом магния и перемешивали с получением гранул аторвастатина с немедленным высвобождением.

3) Таблетирование двухслойных таблеток
Гранулы метформина гидрохлорида и аторвастатина, полученные на ввшеуказанных стадиях 1) и 2), таблетировали в двухслойные таблетки в количествах 710 мг и 150 мг, соответственно, посредством этого получая белые таблетки, имеющие стандартную массу 860 мг на таблетку.
4) Получение раствора для нанесения покрытия и нанесение покрытия
Установку для нанесения оболочки на таблетки (Hi-coater, Freund) заполняли таблетками, полученными на вышеуказанной стадии 3), и температуру нагнетаемого воздуха поддерживали примерно от 30°С до 40°С. 10 г покрывающего агента Opadry® 03В64650 (62,5% гидроксипропилметилцеллюлозы 2910, 30,79% оксида титана, 6,25% полиэтиленгликоля 400, 0,27% красителя оксида железа желтого, 0,18% красителя оксида железа красного и 0,01% алюминиевого лака на основе индигокармина) растворяли в 90 г воды для получения раствора для нанесения покрытия, который распыляли на высушенные таблетки, используя распылитель, работающий при атмосферном давлении, и сушили в дополнительно создаваемом потоке приточного воздуха в течение примерно 10 минут, таким образом получая единичные таблетки по настоящему изобретению массой 885 мг, в которых количество покрытия на таблетку составляло 25 мг.
Пример 2
Гранулы метформина гидрохлорида с замедленным высвобождением получали согласно составу и количествам, указанным в таблице 3. Конкретно, метформина гидрохлорид и коллоидный диоксид кремния пропускали через сито 20-меш и смешивали с гипромеллозой (Metolose® 90SH-100,000 cps). Затем полученную смесь распыляли с раствором связывающего вещества, в котором смесь растворителей, содержащая изопропиловый спирт, ацетон и очищенную воду, смешанные в соотношении 6:3:1, растворяли в концентрации 10% масс./об. с добавлением сополимера метакриловой кислоты (Eudragit® RS РО), затем сушили в грануляторе с псевдоожиженным слоем и полученную смесь пропускали через сито 20-меш. Полученный таким образом гранулированный продукт смешивали со стеаратом магния для получения конечных гранул метформина гидрохлорида с замедленным высвобождением. Процессы получения гранул аторвастатина с немедленным высвобождением, таблетирования двухслойных таблеток и нанесения покрытия выполняли таким же образом, как в примере 1.

Пример 3
Гранулы розувастатина с немедленным высвобождением получали согласно составу и количествам, указанным в таблице 4. Конкретно, безводный гидрофосфат кальция использовали в качестве стабилизирующего агента и, конкретно, кальциевую соль розувастатина, микрокристаллическую целлюлозу, гидрат лактозы, кросповидон и стеарат магния смешивали с безводным гидрофосфатом кальция с получением гранул розувастатина с немедленным высвобождением. Процессы получения гранул метформина с замедленным высвобождением, таблетирования двухслойных таблеток и нанесения покрытия выполняли таким же образом, как в примере 1.

Пример 4
Гранулы розувастатина с немедленным высвобождением получали таким же образом, как в примере 3, а процессы получения гранул метформина с замедленным высвобождением, таблетирования двухслойных таблеток и нанесения покрытия выполняли таким же образом, как в примере 2.
Сравнительный пример 1
Гранулы аторвастатина с немедленным высвобождением получали таким же образом, как в примере 1, а затем таблетировали в одиночные таблетки. Количество покрытия на таблетку составляло 5 мг и, поэтому получали стандартные таблетки массой 155 мг.
Сравнительный пример 2
Гранулы розувастатина с немедленным высвобождением получали таким же образом, как в примере 3, а затем таблетировали в одиночные таблетки. Количество покрытия на таблетку составляло 5 мг и, поэтому получали стандартные таблетки массой 155 мг.
Сравнительные примеры 3 и 4
Гранулы метформина гидрохлорида с замедленным высвобождением получали согласно составу и количествам, указанным в таблице 5. Конкретно, метформина гидрохлорид и коллоидный диоксид кремния пропускали через сито 20-меш, смешивали с микрокристаллической целлюлозой и обрабатывали поливинилпирролидоном (K-30), растворенным в дистиллированной воде для гранулирования. Полученную смесь сушили в сушилке с псевдоожиженным слоем и пропускали через сито 20-меш. Полученный таким образом гранулированный продукт смешивали с полиэтиленоксидом (Polyox® WSR301) и стеаратом магния и перемешивали для получения конечных гранул метформина гидрохлорида с замедленным высвобождением.

Процессы получения гранул аторвастатина с немедленным высвобождением, таблетирования двухслойных таблеток и нанесения покрытия выполняли таким же образом, как в примере 1, и масса полученных в итоге таблеток составляла 945 мг (Сравнительный пример 3).
Процессы получения гранул розувастатина с немедленным высвобождением, таблетирования двухслойных таблеток и нанесения покрытия выполняли таким же образом, как в примере 3, и масса полученных в итоге таблеток составляла 945 мг (Сравнительный пример 4).
Сравнительные примеры 5 и 6
Гранулы метформина гидрохлорида с замедленным высвобождением получали согласно составу и количествам, указанным в таблице 6. Конкретно, метформина гидрохлорид и коллоидный диоксид кремния пропускали через сито 20-меш, смешивали с микрокристаллической целлюлозой и обрабатывали поливинилпирролидоном (K-30), растворенным в дистиллированной воде для гранулирования. Полученную смесь сушили в сушилке с псевдоожиженным слоем и пропускали через сито 20-меш. Полученный таким образом гранулированный продукт смешивали с гипромеллозой (Metolose® 90SH-100,000 cps) и стеаратом магния и перемешивали для получения конечных гранул метформина гидрохлорида с замедленным высвобождением.

Процессы получения гранул аторвастатина с немедленным высвобождением, таблетирования двухслойных таблеток и нанесения покрытия выполняли таким же образом, как в примере 1, и масса полученных в итоге таблеток составляла 945 мг (Сравнительный пример 5).
Процессы получения гранул розувастатина с немедленным высвобождением, таблетирования двухслойных таблеток и нанесения покрытия выполняли таким же образом, как в примере 3, и масса полученных в итоге таблеток составляла 945 мг (Сравнительный пример 6).
Примеры 5-8
Гранулы метформина гидрохлорида с замедленным высвобождением получали согласно составу и количествам, указанным в таблице 7. Конкретно, гранулы метформина гидрохлорида с замедленным высвобождением получали таким же образом, как в примере 1, за исключением того что их получали, используя вместо сополимера метакриловой кислоты (Eudragit® RS РО) ингредиенты Eudragit® S100, Ethocel® Std 14, цетиловый спирт и Kollicoat® SR 30D, соответственно (смотри Таблицу 7). Масса каждой таблетки, полученной после таблетирования в двухслойные таблетки и нанесения покрытия, составляла 885 мг.
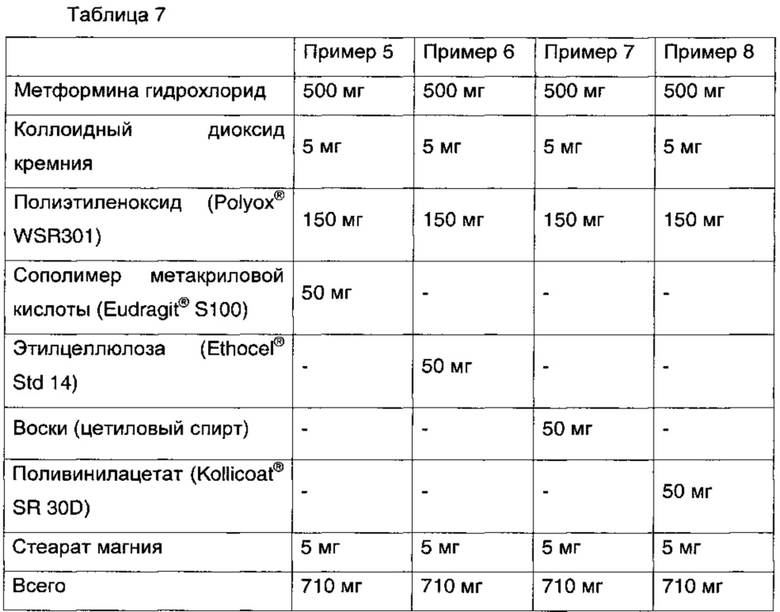
Экспериментальный пример 1: тест на высвобождение метформина
Для того чтобы подтвердить, что комбинированная композиция согласно настоящему изобретению может демонстрировать скорость высвобождения, эквивалентную скорости высвобождения контрольного лекарственного средства, представляющего собой таблетку Glucophage XR® 500 мг, проводили тест для определения высвобождения комбинированных композиций, полученных выше.
Конкретно, композиции с замедленным высвобождением, полученные в примерах 1 и 2 и сравнительных примерах 3 и 5, и имеющуюся в продаже таблетку Glucophage XR® 500 мг, которую использовали в качестве контроля, тестировали при 37°С в 900 мл среды для растворения на основе фосфатного буфера (рН 6,8) при 50 об/мин согласно способу растворения (Способ II), описанному в USP (Фармакопея США). Образцы собирали в заданные моменты времени и анализировали с помощью HPLC (высокоэффективная жидкостная хроматография), вычисляя степень высвобождения. Результаты показаны в таблице 8 и на ФИГ. 1.
Для HPLC использовали следующие условия:
Колонка: Waters XBridge (С18, 150 мм × 4,6 мм, 5 мкм)
Детектор: спектрофотометрический детектор (218 нм)
Подвижная фаза: раствор, полученный растворением 17 г NH4H2PO4 в 1 л воды и регулированием его рН до 3,0 ортофосфорной кислотой
Скорость потока: 1,0 мл/мин
Температура колонки: 40°С
Время анализа: 4 мин
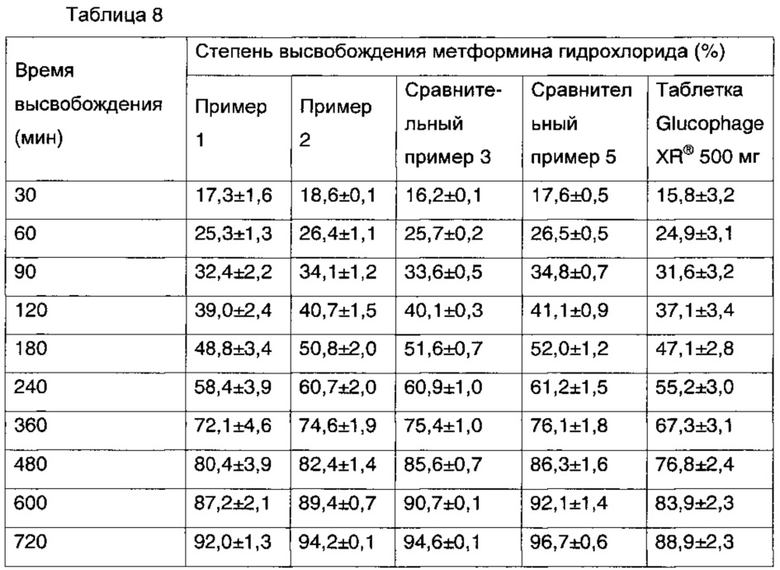
Тесты на высвобождение выполняли для метформина гидрохлорида на комбинированных композициях, полученных в примерах 1 и 2 и сравнительных примерах 3 и 5, и результаты сравнивали с тестами на высвобождение таблетки Glucophage XR® 500 мг, представляющей собой контрольное лекарство. Результаты показывают, что комбинированные композиции демонстрировали скорости высвобождения, аналогичные скоростям высвобождения таблетки Glucophage XR® 500 мг. На основании результатов было подтверждено, что высвобождение лекарства эффективно контролировалось с использованием набухающего полимера и нерастворимого в воде полимера. Контроль высвобождения является весьма значительным, учитывая, что масса таблетки Glucophage XR® 500 мг равняется 1000 мг или выше, в то время как массы таблеток комбинированных композиций согласно настоящему изобретению равняются 900 мг или ниже.
Кроме того, таблетки с замедленным высвобождением, полученные в Примерах 5, 6, 7 и 8, в зависимости от видов нерастворимых в воде полимеров, и коммерческий продукт, таблетку Glucophage XR® 500 мг, которую использовали в качестве контрольного лекарства, анализировали в таких же самых условиях, которые описаны выше, и результаты показаны в таблице 9 ниже. В результате анализа было показано, что таблетки с замедленным высвобождением, полученные в Примерах 5, 6, 7 и 8, имеют паттерн высвобождения, аналогичный паттерну высвобождения таблетки Glucophage XR® 500 мг, представляющего собой контрольное лекарство. На основании этого результата было подтверждено, что высвобождение лекарства эффективно контролируется с использованием набухающего полимера и нерастворимого в воде полимера.
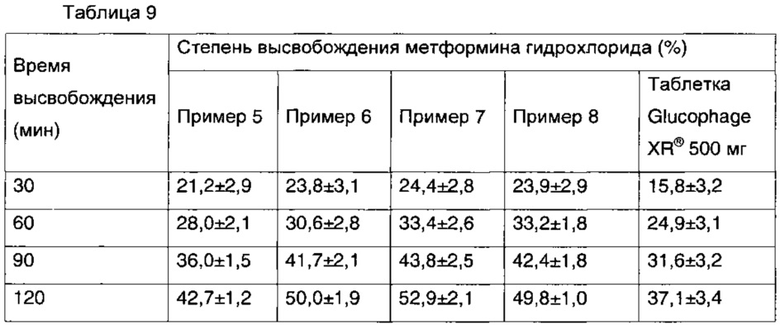

Экспериментальный пример 2: тест на высвобождение аторвастатина
Для того чтобы убедиться в том, что комбинированные композиции согласно настоящему изобретению могут непрерывно поддерживать концентрацию в крови за счет немедленного высвобождения лекарства быстрого действия, таблетку Lipitor® 10 мг, то есть контрольное лекарство на основе кальциевой соли аторвастатина, композиции, полученные в сравнительных примерах 1, 3 и 5 и примерах 1 и 2, тестировали при 37°С в 900 мл среды для растворения на основе дистилированной воды при 50 об/мин согласно способу растворения (Способ II), описанному в USP. Образцы собирали в заданные моменты времени и анализировали с помощью HPLC, вычисляя стерень высвобождения. Результаты показаны в таблице 10 и на ФИГ. 2.
Для HPLC использовали следующие условия:
Колонка: Phenomenex Luna (С18, 250 мм × 4,6 мм, 5 мкм)
Детектор: спектрофотометрический детектор (244 нм)
Подвижная фаза: 0,05 моль/л цитрат аммония (рН 4,0) : ACN (ацетонитрил) : ТНР (тетрагидрофуран) = 2:2:1
Скорость потока: 1,5 мл/мин
Температура колонки: 40°С
Время анализа: 4 мин
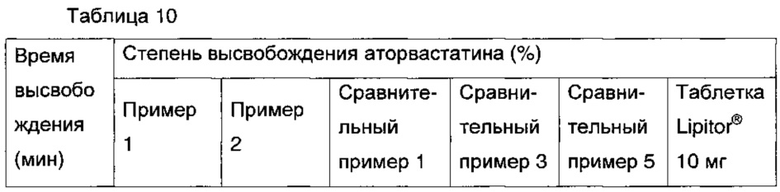

В приведенном выше эксперименте получали композицию сравнительного примера 1 (одиночные таблетки аторвастатина), показывающую скорость высвобождения, аналогичную скорости высвобождения для таблетки Lipitor® 10 мг, представляющего собой контрольное лекарство, и оценивали скорость высвобождения для нее. Когда комбинированные композиции получали с использованием гранул на основе аторвастатина, которые получали таким же образом, как в сравнительном примере 1, согласно способам в сравнительном примере 3 и сравнительном примере 5, имело место задерживание распада слоя гранул аторвастатина с немедленным высвобождением из-за набухающего полимера, за счет чего снижалась скорость высвобождения.
В то же время, в примерах 1 и 2, в которых гранулы метформина с замедленным высвобождением получали путем нанесения покрытия на основе нерастворимого в воде полимера на набухающий полимер и метформина гидрохлорид, время распада аторвастатина обеспечивалось на таком же уровне или на уровне, подобном времени распада одиночных таблеток аторвастатина. То есть, было подтверждено, что путем предотвращения физического контакта между двумя типами гранул согласно настоящему изобретению, гранулы с немедленным высвобождением аторвастатина гидрохлорида распадались и высвобождались таким же образом, что и одиночные таблетки, и это указывает на то, что то же самое может быть эффективно применено к комбинированной композиции, требующей двухфазную систему, состоящую из композиции с замедленным высвобождением и композиции быстрого высвобождения, требующей немедленного высвобождения.
Кроме того, такой же эксперимент выполняли для композиций, полученных в примерах 5-8. Композиции примеров 5-8 получали нанесением покрытия различных нерастворимых в воде полимеров, отличных от сополимера метакриловой кислоты (Eudragit® RS РО), на набухающий полимер и метформина гидрохлорид, в этих композициях гранулы аторвастатина, полученные таким же образом, как в сравнительном примере 1, таблетировали в двухслойные таблетки. Результаты теста на высвобождение показаны в таблице 11 ниже.
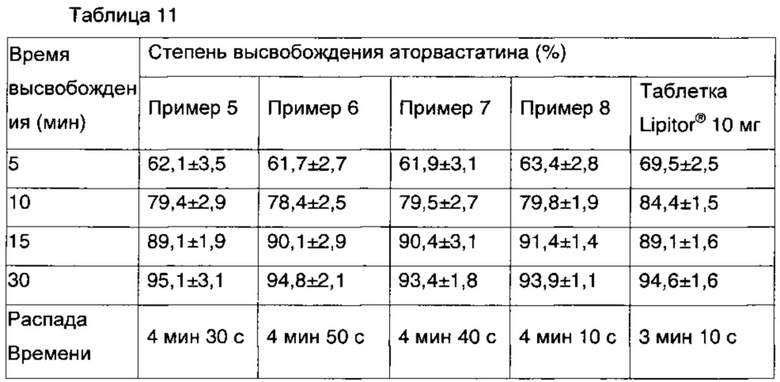
Показано, что скорость высвобождения аторвастатина является аналогичной скорости высвобождения композиции сравнительного примера 1, несмотря на использование набухающего полимера с высокой вязкостью. Кроме того, когда использовали нерастворимый в воде полимер, отличный от сополимера метакриловой кислоты (Eudragit® RS РО), было показано, что эффект предотвращения физического контакта между двумя типами гранул является идентичным.
Экспериментальный пример 3: тест на высвобождение розувастатина
Чтобы установить скорость высвобождения для композиции на основе кальциевой соли розувастатина, таблетку Crestor® 10 мг, то есть контрольное лекарство на основе кальциевой соли розувастатина, и композиции, полученные в сравнительных примерах 2, 4 и 6 и примерах 3 и 4, тестировали при 37°С в 900 мл раствора цитратного буфера (рН 6,6) при 50 об/мин согласно способу растворения (Способ II), описанному в USP. Образцы собирали в заданные моменты времени и анализировали с помощью HPLC, вычисляя степень высвобождения. Результаты показаны в таблице 12 и на ФИГ. 3.
Для HPLC использовали следующие условия:
Колонка: Capcell Рак (С18, 75 мм × 4,6 мм, 3 мкм)
Детектор: спектрофотометрический детектор (242 нм)
Подвижная фаза: очищенная вода : АСN : ортофосфорная кислота = 600:400:1
Скорость потока: 1,0 мл/мин
Температура колонки: комнатная температура
Время анализа: 5 мин
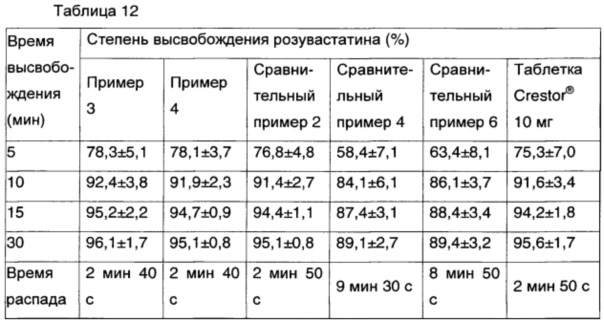
В приведенном выше эксперименте получали композицию сравнительного примера 2 (одиночные таблетки розувастатина), показывающую скорость высвобождения, аналогичную скорости высвобождения для таблетки Crestor® 10 мг, контрольного лекарства, и оценивали для нее скорость высвобождения. В композициях сравнительных примеров 4 и 6, подвергающихся воздействию набухающего полимера, имело место задерживание распада слоя гранул с немедленным высвобождением, за счет чего снижалась скорость высвобождения. Так же, как и в ранее проведенном тесте на высвобождение аторвастатина, было подтверждено, что гранулы быстрого высвобождения высвобождаются немедленно под действием покрытия нерастворимым в воде полимером при получении комбинированных композиций гранул с замедленным высвобождением и гранул с немедленным высвобождением.
Экспериментальный пример 4: тест на стабильность-взаимодействие между кальциевой солью аторвастатина и эксципиентами.
Для того чтобы выбрать наиболее подходящий эксципиент для стабильности кальциевых солей аторвастатина, проводили тест на химическую стабильность между кальциевыми солями аторвастатина и эксципиентами. Конкретно, 1 г кальциевой соли аторвастатина и 5 г каждого из эксципиентов, соответственно, смешивали при комнатной температуре и упаковывали во флаконы в порошкообразном состоянии. Флаконы хранили в течение 4 недель в стрессовых условиях (60°С, относительная влажность 80%), содержание примесей (%) изучали с помощью HPLC, а результаты показаны в таблице 13 ниже.
Для HPLC использовали следующие условия:
Колонка: Gemini (С18, 250 мм × 4,6 мм, 5 мкм)
Детектор: спектрофотометрический детектор (244 нм)
Подвижная фаза: 0,05 М цитрат аммония (рН 4,0) : ACN : THF = 53:27:20
Скорость потока: 1,5 мл/мин
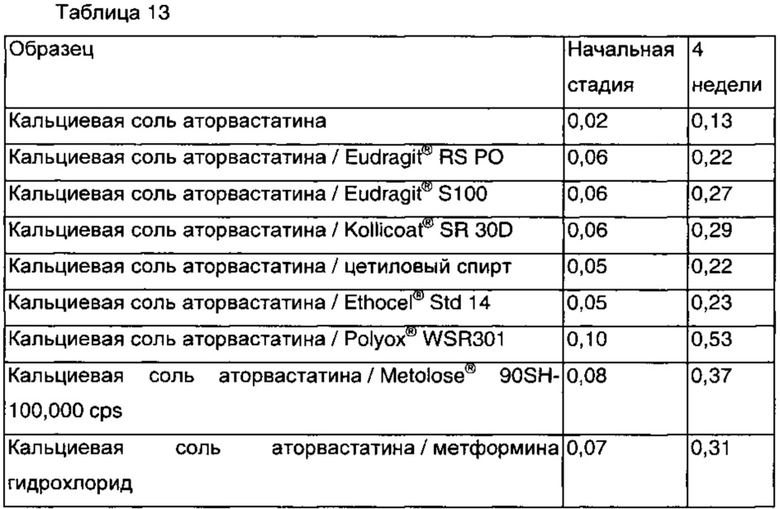
Как можно увидеть в таблице 13, кальциевые соли аторвастатина показывали разные значения общего содержания примесей, в зависимости от эксципиентов, смешанных с ними. Значений общего содержания примесей при использовании других составляющих комбинированную композицию компонентов, таких как метформина гидрохлорид, и набухающих полимеров, таких как полиэтиленоксид (Polyox® WSR301) и гипромеллоза (Metolose® 90SH-100,000 cps), показывали относительно высокие значения общих примесей по сравнению с таковыми для нерастворимых в воде полимеров. Таким образом, было подтверждено, что когда эти составляющие компоненты непосредственно приводят в контакт с кальциевой солью аторвастатина, это значительно снижает стабильность комбинированных композиций, содержащих вышеупомянутые компоненты.
Показано, что среди нерастворимых в воде полимеров увеличение количества примесей в случае использования сополимера метакриловой кислоты (Eudragit® RS РО), восков (цетиловый спирт) и этилцеллюлозы (Ethocel® Std 14) является более низким, чем количества примесей, когда при получении комбинированных композиций применяют другие нерастворимые в воде полимеры вместе с набухающим полимером и метформина гидрохлоридом, таким образом делая возможным обеспечение более выгодных с точки зрения стабильности композиций, чем при получении композиций с помощью существующих способов получения типов композиций метформина с замедленным высвобождением, известных в данной области техники.
Специалисту в данной области техники из вышеизложенного будет понятно, что настоящее изобретение может быть воплощено в других конкретных формах без отклонения от его сущности или основных характеристик. Описанные воплощения должны рассматриваться во всех отношениях только в качестве иллюстративных и неограничивающих. Объем настоящего изобретения, следовательно, обозначен прилагаемой формулой изобретения, а не вышеизложенным описанием. Все изменения, которые входят в содержание и диапазон эквивалентности формулы изобретения, подлежат включению в объем настоящего изобретения.

Изобретение относится медицине, в частности к стабильной фармацевтической комбинированной композиции, содержащей метформин, используемый для лечения неинсулинзависимого диабета, и ингибитор HMG-CoA-редуктазы, используемый для лечения дислипидемии, а также к способу получения устойчивой комбинированной композиции. Осуществление изобретения позволяет получить композицию с эффективно улучшенной стабильностью за счет обеспечения стабильного высвобождения соответствующих активных ингредиентов и блокирования физических и химических взаимодействий между активными ингредиентами. 2 н. и 14 з.п. ф-лы, 3 ил, 13 табл., 14 пр.
1 Стабильная фармацевтическая комбинированная композиция, содержащая:
первую композицию с замедленным высвобождением, которая содержит гранулы, содержащие метформин или его фармацевтически приемлемую соль и набухающий полимер, покрытые нерастворимой в воде полимерной пленкой; и
вторую композицию с немедленным высвобождением, содержащую ингибитор HMG-CoA (3-гидрокси-3-метилглютарил-кофермент А)-редуктазы.
2. Стабильная фармацевтическая комбинированная композиция по п. 1, где набухающий полимер представляет собой по меньшей мере один, выбранный из группы, состоящей из гидроксипропилметилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилцеллюлозы, полиэтиленоксида, каррагинана, природной камеди, гуаровой камеди, трагаканта, аравийской камеди, камеди бобов рожкового дерева, ксантановой камеди, поливинилового спирта и поливинилпирролидона.
3. Стабильная фармацевтическая комбинированная композиция по п. 1, где набухающий полимер имеет вязкость 100 сП (0,1 Па⋅с) или выше.
4. Стабильная фармацевтическая комбинированная композиция по п. 1, где нерастворимый в воде полимер представляет собой по меньшей мере один, выбранный из группы, состоящей из сополимера метакриловой кислоты, этилцеллюлозы, целлюлозы ацетата сукцината, целлюлозы ацетата фталата, жирных кислот, сложных эфиров жирных кислот, спиртов жирных кислот и восков.
5. Стабильная фармацевтическая комбинированная композиция по п. 4, где жирная кислота и сложный эфир жирной кислоты представляют собой по меньшей мере один, выбранный из группы, состоящей из глицерилпальмитостеарата, глицерилстеарата, глицерилбегената, цетилпальмитата, глицерилмоноолеата, стеариновой кислоты и их смеси;
спирт жирной кислоты представляет собой по меньшей мере один, выбранный из группы, состоящей из цетостеарилового спирта, цетилового спирта, стеарилового спирта и их смеси;
и воск представляет собой по меньшей мере один, выбранный из группы, состоящей из карнаубского воска, пчелиного воска, микрокристаллического воска и их смеси.
6. Стабильная фармацевтическая комбинированная композиция по п. 1, где метформин или его фармацевтически приемлемая соль содержится в количестве от 250 мг до 1000 мг.
7. Стабильная фармацевтическая комбинированная композиция по п. 1, где нерастворимый в воде полимер содержится в количестве от 1% мас. до 20% мас. в расчете на общую массу первой композиции с замедленным высвобождением.
8. Стабильная фармацевтическая комбинированная композиция по п. 1, где набухающий полимер содержится в количестве от 1% мас. до 40% мас. в расчете на общую массу первой композиции с замедленным высвобождением.
9. Стабильная фармацевтическая комбинированная композиция по п. 1, где ингибитор HMG-CoA-редуктазы представляет собой по меньшей мере один, выбранный из группы, состоящей из розувастатина, аторвастатина, питавастатина, ловастатина, симвастатина, правастатина и флувастатина.
10. Стабильная фармацевтическая комбинированная композиция по п. 1, где ингибитор HMG-CoA-редуктазы содержится в количестве от 5 мг до 160 мг.
11. Стабильная фармацевтическая комбинированная композиция по п. 1, где вторая композиция с немедленным высвобождением полностью распадается в дистиллированной воде при 37°C в течение 5 мин.
12. Стабильная фармацевтическая комбинированная композиция по п. 1, которая изготовлена таким образом, что физическому контакту или химическому взаимодействию между указанным набухающим полимером в первой композиции с замедленным высвобождением и указанным ингибитором HMG-CoA-редуктазы препятствует нерастворимая в воде полимерная пленка.
13. Стабильная фармацевтическая комбинированная композиция по п. 1, которая представляет собой непокрытую таблетку, покрытую пленкой таблетку, двухслойную таблетку, многослойную таблетку или таблетку с ядром.
14. Стабильная фармацевтическая комбинированная композиция по п. 1, где первая композиция с замедленным высвобождением и вторая композиция с немедленным высвобождением находятся в форме двухслойной таблетки.
15. Способ получения комбинированной композиции по п. 1, включающий:
получение первой композиции с замедленным высвобождением путем получения гранул, содержащих метформин или его фармацевтически приемлемую соль и набухающий полимер, с последующим формированием нерастворимой в воде полимерной пленки на указанных гранулах;
получение второй композиции с немедленным высвобождением, содержащей ингибитор HMG-CoA-редуктазы; и
изготовление первой композиции с замедленным высвобождением и второй композиции с немедленным высвобождением в составе единичной композиции.
16. Способ по п. 15, дополнительно включающий формирование пленочного слоя на наружной поверхности комбинированной композиции.
| WO 2011081493 A2, 07.07.2011 | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| СРЕДСТВО "АБИСИЛ-1", ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ, АНТИБАКТЕРИАЛЬНОЙ И РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ | 1995 |
|
RU2054945C1 |
Авторы
Даты
2018-04-19—Публикация
2014-07-25—Подача