Область техники
Изобретение относится к фармацевтическому комбинированному препарату, содержащему ингибитор HMG-CoA редуктазы и ингибитор абсорбции холестерина.
Предшествующий уровень техники
Жиры, абсорбируемые в кровь, а именно нейтральный жир, холестерин, фосфолипид, свободная жирная кислота и так далее, объединяются с белками с образованием водорастворимого липопротеина, называемого липидом сыворотки крови. Состояние, когда уровень такого липида в сыворотке крови является аномально высоким, называют дислипидемией. Для циркуляции в системе кровообращения липид, такой как холестерин, который нерастворим в воде, окружен белком, диффундированным в кровь и циркулирующим в крови в виде комплексов липида и белка, называемых липопротеинами. Липопротеины для связывания и транспортирования холестерина классифицированы на липопротеины высокой плотности (HDL) и липопротеины низкой плотности (LDL). HDL удаляет холестерин из ткани и в результате уменьшает риск атеросклероза. Наоборот, LDL способствует накоплению холестерина на стенке кровеносного сосуда, тем самым увеличивая риск артериосклероза.
Основная причина атеросклероза представляет собой непрерывное нарастание не являющихся необходимыми веществ, таких как холестерин, на стенке кровеносного сосуда. Среди причин, если уровень основного причинного фактора, LDL, увеличивается, тогда холестерин откладывается на кровеносном сосуде, затем отложенный холестерин не только сужает кровеносный сосуд, тем самым мешая потоку крови, но также способствует фиброзу, который вызывает повреждение и затвердевание клеточной стенки. Соответственно кровеносный сосуд теряет свою эластичность, способствуя артериосклерозу, который в конечном итоге приводит к сердечно-сосудистым заболеваниям.
Применяются различные способы лечения дислипидемии, среди которых ингибиторы синтеза холестерина, а именно ингибиторы 3-гидрокси-3-метилглутарил-коэнзим A (HMG-CoA) редуктазы, известны как наиболее эффективный класс лекарственных средств для лечения дислипидемии. Ингибиторы HMG-CoA редуктазы, которые представляют собой препараты первой линии для лечения дислипидемии, могут повышать риск побочных действий в зависимости от дозы. Таким образом, когда монотерапия ингибиторами HMG-CoA редуктазы не позволяет достичь достаточного терапевтического действия, тогда дополнительное введение любого другого лекарственного средства с другим механизмом действия является более предпочтительным, чем лечение высокой дозой ингибиторов НМС-СоА редуктазы. Кроме того, дислипидемия может быть вызвана сочетанием нескольких факторов, таких как увеличение в крови общего уровня холестерина, LDL-холестерина (холестерина липопротеинов низкой плотности), нейтрального жира, увеличения уровней HDL-холестерина (холестерина липопротеинов высокой плотности) и так далее. Таким образом, когда имеется сочетание двух или более факторов, может быть предусмотрена комбинированная терапия несколькими лекарственными средствами.
В частности, когда пациенту требуется значительно большее снижение уровня LDL-холестерина, чем при монотерапии ингибиторами HMG-CoA редуктазы, тогда комбинированная терапия эзетимибом является эффективной. Эзетимиб представляет собой новый терапевтический агент для лечения дислипидемии, который избирательно ингибирует абсорбцию холестерина в тонком кишечнике. Поскольку эзетимиб отличается от статинов по механизму действия, можно ожидать дополнительного эффекта при его назначении вместе со статинами.
Розувастатин или его фармацевтически приемлемая соль представляет собой [(Е)-7-[4-(4-фторфенил)-6-изопропил-2-[метил(метилсульфонил)амино]-пиримидин-5-ил]-(3R,5S)-3,5-дигидроксигепт-6-еновую кислоту] (розувастатин) и ее натриевую или кальциевую соль. В частности, они используются для лечения гиперхолестеринемии и смешанной дислипидемии, а розувастатин кальция имеется в продаже под товарным знаком CRESTOR™. Розувастатин кальция представляет собой аморфный белый или бледно-желтый порошок, который растворим в N,N-диметилформамиде, ацетоне или ацетонитриле, но умеренно растворим в воде.
Эзетимиб представляет собой [1-(4-фторфенил)-(3R)-[3-(4-фторфенил)-(3S)-гидроксипропил]-(4S)-(4-гидроксифенил)-2-азетидинон)]. Он блокирует С1-подобный белок 1 Ниманна-Пика (Niemanpick С1-like 1 protein), который, как известно, вовлечен в транспорт холестерина из внутренних органов. Известно, что уровень холестерина липопротеина низкой плотности (LDL-C) снижается при введении эзетимиба, и также известно, что такой эффект может значительно усиливаться при его введении в комбинации со статинами. Эзетимиб имеется в продаже под товарным знаком EZETROL™ на местном рынке и ZETIA™ в США. Эзетимиб представляет собой белый порошок, который является легкорастворимым или очень легкорастворимым в этаноле, метаноле или ацетоне, но практически нерастворимым в воде. Точка плавления эзетимиба составляет приблизительно 163°С, и сообщается о том, что он стабилен при комнатной температуре.
Кроме того, когда монотерапия с использованием статинов менее эффективна для контроля LDL-C, тогда комбинированная терапия с использованием эзетимиба, который ингибирует абсорбцию холестерина в тонком кишечнике, рекомендуется как эффективная. В качестве примера комбинированной терапии разработан и имеется в продаже VYTORIN™ (симвастатин/эзетимиб) (международная заявка на патент № PCT/US 2003/022889), а также Liptruzet™ (аторвастатин/эзетимиб), недавно одобренный FDA (Управление по контролю за продуктами питания и лекарственными средствами США).
В целом, может быть приготовлен комбинированный препарат, содержащий два или более чем два активных ингредиента, путем использования различных способов, таких как разработка композиции, которая может минимизировать разложение каждого активного ингредиента, с использованием ингредиентов, комбинированных для минимизации нежелательных побочных продуктов разложения и для достижения желаемого срока годности, или добавления стабилизатора, который может улучшить стабильность активных ингредиентов.
В частности, комбинированный препарат может содержать селективный эксципиент, который может обеспечивать такое же растворение и такой же фармакокинетический (РK) профиль, как и контрольный препарат с единственным ингредиентом.
Описание изобретения
Техническая задача
Таким образом, авторы изобретения провели обширное исследование для того, чтобы предложить комбинированный препарат, который содержит оба активных ингредиента ингибитор HMG-CoA редуктазы и ингибитор абсорбции холестерина, в частности розувастатин и эзетимиб, который проявляет такие же растворение и РK (фармакокинетический) профиль, как и контрольный препарат, и в то же время является стабильным. В результате, авторы изобретения обнаружили, что может быть приготовлен такой комбинированный препарат, который физико-химически стабилен и проявляет такие же растворение и РK профиль, как и контрольный препарат, тем самым создав изобретение.
Техническое решение
Изобретение заключается в том, чтобы предложить комбинированный препарат, содержащий одновременно два активных ингредиента (ингибитор HMG-CoA редуктазы и ингибитор абсорбции холестерина), где картина растворения каждого активного ингредиента в комбинированном препарате является такой же, как картина для каждого активного ингредиента в препаратах с единственным ингредиентом.
Полезные эффекты
Фармацевтический комбинированный препарат в соответствии с изобретением одновременно содержит два активных ингредиента (ингибитор HMG-CoA редуктазы и ингибитор абсорбции холестерина) и отличается тем, что картина растворения каждого активного ингредиента в комбинированном препарате является такой же, как картина для каждого активного ингредиента в препаратах с единственным ингредиентом, тем самым значительно улучшая удобство для пациента и соблюдение пациентом схемы лечения.
Описание графических материалов
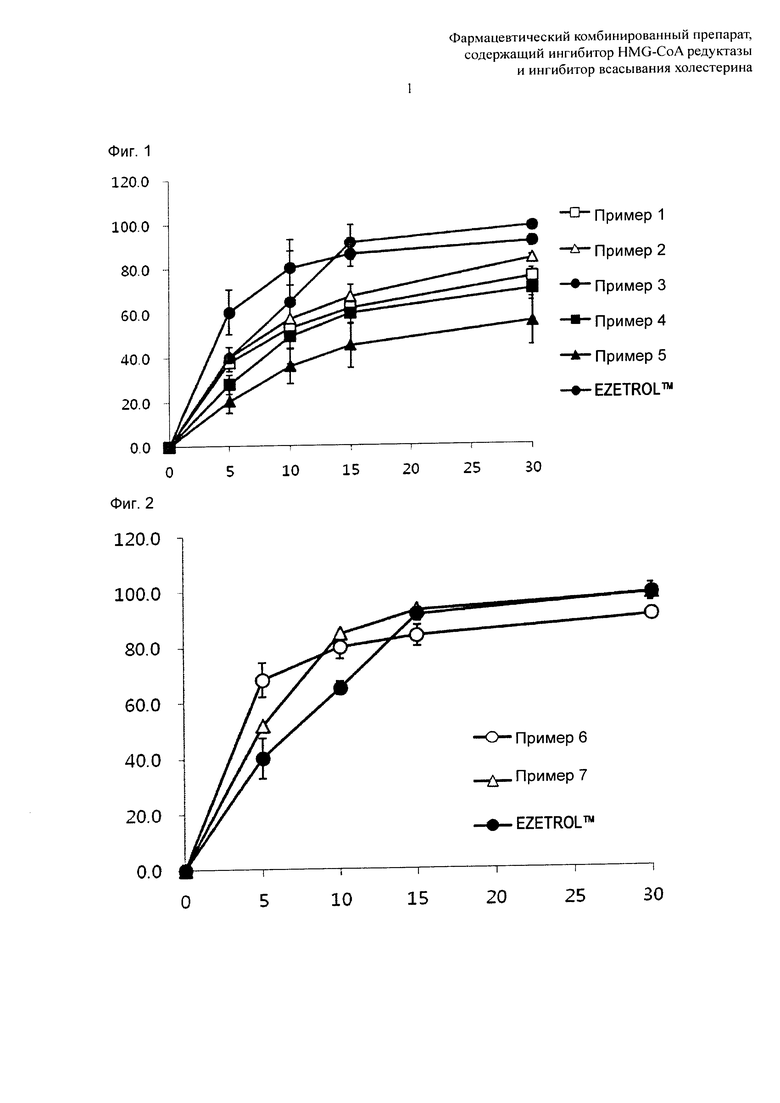
Фиг. 1 представляет собой график, демонстрирующий картины растворения эзетимиба в препаратах в соответствии с примерами.
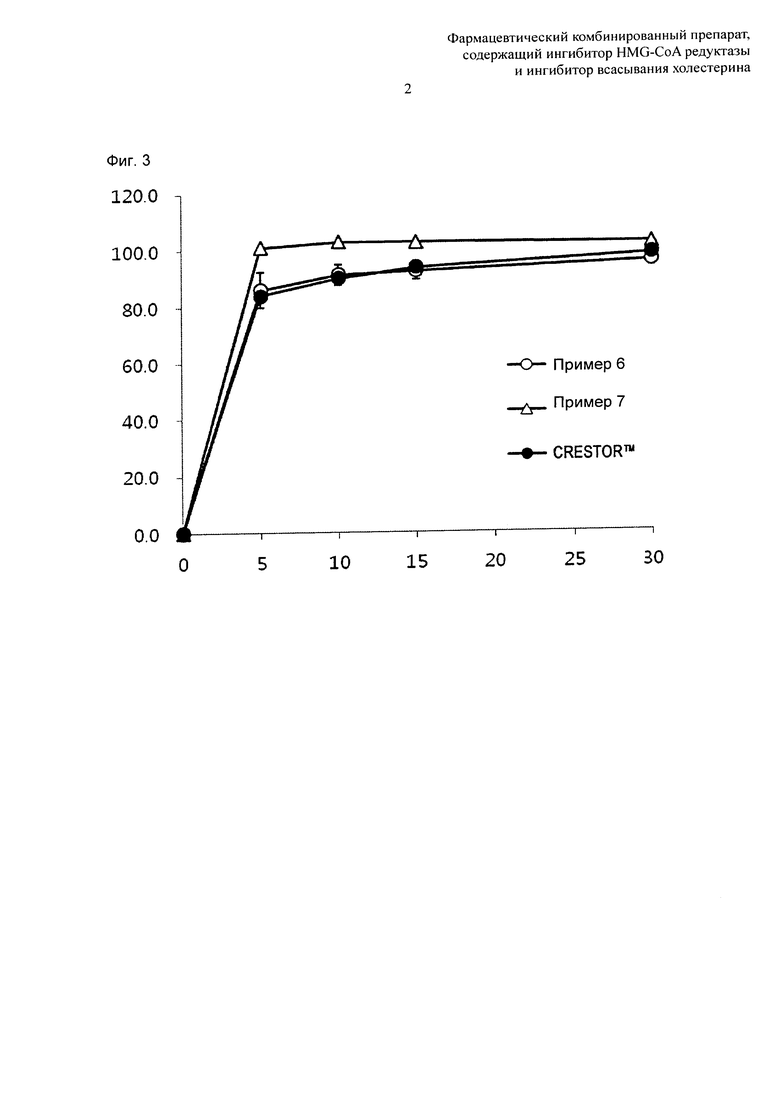
Фиг. 2 представляет собой график, демонстрирующий картины растворения эзетимиба в комбинированных препаратах в соответствии с примерами.
Фиг. 3 представляет собой график, демонстрирующий картины растворения розувастатина в комбинированных препаратах в соответствии с примерами.
Лучший вариант
В изобретении предложен фармацевтический комбинированный препарат, содержащий от 5 до 15 массовых долей ингибитора HMG-CoA редуктазы; от 5 до 15 массовых долей ингибитора абсорбции холестерина; от 4,5 до 12 массовых долей крахмалгликолята натрия; и от 25 до 35 массовых долей гидроксипропилцеллюлозы с низкой степенью замещения.
Используемый здесь термин "ингибитор HMG-CoA редуктазы" означает лекарственное средство, ингибирующее HMG-CoA редуктазу (3-гидрокси-3-метилглутарил-коэнзим А редуктазу), которая представляет собой фермент, действующий на стадии превращения HMG-CoA в мевалоновую кислоту, представляющую собой стадию, определяющую скорость синтеза холестерина. Указанный ингибитор HMG-CoA редуктазы обладает превосходными эффектами снижения уровня LDL-холестерина и нейтрального жира при увеличении уровня HDL-холестерина и является безопасным и хорошо переносимым с относительно низкой частотой неблагоприятных побочных эффектов. Таким образом, в настоящее время он наиболее широко используется в лечении дислипидемии. Ингибитор HMG-CoA редуктазы может представлять собой, например, любой из симвастатина, ровастатина, аторвастатина, флувастатина, правастатина, церивастатина, питавастатина, розувастатина и их фармацевтически приемлемых солей.
В соответствии с изобретением указанный ингибитор HMG-CoA редуктазы содержится в количестве от 5 до 15 массовых долей, предпочтительно от 9 до 11 массовых долей, в фармацевтическом комбинированном препарате.
Предпочтительно указанный ингибитор HMG-CoA редуктазы представляет собой розувастатин или его фармацевтически приемлемую соль, который может содержаться в количестве от 5 мг до 50 мг в фармацевтический комбинированном препарате.
Используемый здесь термин "ингибитор абсорбции холестерина" обозначает лекарственное средство, ингибирующее абсорбцию холестерина из тонкой кишки в систему кровообращения. Указанные ингибиторы абсорбции холестерина могут включать, например, эзетимиб или его фармацевтически приемлемые соли. Они могут содержаться в количестве от 5 мг до 50 мг в фармацевтическом комбинированном препарате.
В соответствии с изобретением указанный ингибитор абсорбции холестерина содержится в фармацевтическом комбинированном препарате в количестве от 5 до 15 массовых долей, предпочтительно от 9 до 11 массовых долей.
Фармацевтический комбинированный препарат по изобретению одновременно содержит оба указанных активных ингредиента (ингибитор HMG-CoA редуктазы и ингибитор абсорбции холестерина) и отличается тем, что картина растворения каждого активного ингредиента в комбинированном препарате является такой же, как для каждого активного ингредиента в препаратах с единственным ингредиентом. Соответственно комбинированный препарат по изобретению может значительно улучшать удобство для пациента и соблюдение пациентом схемы лечения. Предпочтительно фармацевтический комбинированный препарат по изобретению одновременно содержит розувастатин и эзетимиб.
Важно подходящим образом выбрать тип и количество эксципиентов для того, чтобы картина растворения каждого активного ингредиента в комбинированном препарате, содержащем оба активных ингредиента (ингибитор HMG-CoA редуктазы и ингибитор абсорбции холестерина), могла быть такой же, как для каждого активного ингредиента в препаратах с единственным ингредиентом.
В изобретении, во-первых, тип и количество эксципиентов выбраны и скорректированы в расчете на эзетимиб. В частности, крахмалгликолят натрия выбран в качестве подходящего эксципиента в примерах 1-5. В соответствии с примерами 1-5 кроскармеллоза натрия, крахмалгликолят натрия или прежелатинизированный крахмал использовали в качестве эксципиента для эзетимиба, но использование крахмалгликолята натрия (пример 3) приводило в результате к наилучшему растворению, аналогичному картине растворения EZETROL™, который представляет собой препарат с единственным ингредиентом эзетимибом.
В соответствии с изобретением указанный крахмалгликолят натрия содержится в фармацевтическом комбинированном препарате в количестве от 4,5 до 12 массовых долей, предпочтительно от 11 до 12 массовых долей.
При приготовлении комбинированного препарата путем добавления розувастатина к указанному эксципиенту, выбранному исходя из указанного эзетимиба, скорость растворения эзетимиба может уменьшаться. В частности, в примере 6 продемонстрировано, что скорость растворения эзетимиба была несколько ниже. Не желая быть связанными какой-либо теорией, на скорость растворения, по-видимому, влияет какое-либо взаимодействие между эзетимибом и розувастатином.
Таким образом, в изобретении тип и количество эксципиентов выбраны для увеличения скорости растворения эзетимиба и, в то же время, для контролирования скорости растворения розувастатина, аналогичной скорости растворения препарата с единственным ингредиентом.
В частности, в примере 7 продемонстрировано, что добавление гидроксипропилцеллюлозы с низкой степенью замещения обеспечивает наиболее превосходное растворение, аналогично картине растворения препарата с единственным ингредиентом эзетимибом EZETROL™. Кроме того, картина растворения розувастатина была аналогична таковой для препарата с единственным ингредиентом розувастатином CRESTOR™.
Используемый здесь термин "гидроксипропилцеллюлоза с низкой степенью замещения" означает гидроксипропилцеллюлозу, где гидроксильные группы частично замещены группами гидроксипропокси в доле от 5% до 16%. В фармацевтическом комбинированном препарате по изобретению указанная гидроксипропилцеллюлоза с низкой степенью замещения содержится в количестве от 30 до 35 массовых долей.
В дополнение к вышеприведенным ингредиентам, фармацевтический комбинированный препарат в соответствии с изобретением может дополнительно содержать гидрофосфат кальция для увеличения стабильности указанного ингибитора HMG-CoA редуктазы. Указанный гидрофосфат кальция предпочтительно содержится в количестве от 10 до 15 массовых долей. Помимо вышеприведенного, фармацевтический комбинированный препарат в соответствии с изобретением может дополнительно содержать любые добавки, используемые при приготовлении обычных композиций, а также добавки, не изменяющие эффективность фармацевтического комбинированного препарата. Например, можно упомянуть микрокристаллическую целлюлозу, стеарат магния и так далее.
Фармацевтический комбинированный препарат в соответствии с изобретением отличается тем, что ингибитор HMG-CoA редуктазы обладает скоростью растворения 85% или более, предпочтительно 90% или более, более предпочтительно 95% или более, в течение 30 мин при измерении в условиях растворения в буферном растворе при рН 6,6 (900 мл) при 37±0,5°С и при скорости перемешивания 50 об/мин в соответствии со способом 2 в тесте растворения по Корейской фармакопее (способ с лопатками).
Кроме того, фармацевтический комбинированный препарат в соответствии с изобретением отличается тем, что ингибитор абсорбции холестерина обладает скоростью растворения 80% или более, предпочтительно 85% или более, более предпочтительно 90% или более, в течение 15 мин при измерении в условиях растворения в буферном растворе при рН 7,0 (900 мл; SDS (додецилсульфат натрия) 0,5%) при 37±0,5°С и при скорости перемешивания 50 об/мин в соответствии со способом 2 в тесте растворения по Корейской фармакопее (способ с лопатками).
Фармацевтический комбинированный препарат в соответствии с изобретением может быть приготовлен из одного экструдата, содержащего два активных ингредиента (ингибитор HMG-CoA редуктазы и ингибитор абсорбции холестерина); или двух отдельных экструдатов, каждый из которых содержит один активный ингредиент; или одного экструдата, который содержит один или более чем один активный ингредиент, и затем обработан одним или более чем одним активным ингредиентом, который не представлен в виде экструдата. Каждый из указанных экструдатов может также содержать добавки в соответствии с изобретением.
Фармацевтический комбинированный препарат в соответствии с изобретением находится в состоянии, в котором ингредиенты однородно смешаны друг с другом, и может быть приготовлен способами, известными в данной области техники, такими как прямое прессование, влажное гранулирование, гранулирование в псевдоожиженном слое, экструзия, выпаривание растворителя и так далее.
Хотя общая масса фармацевтического комбинированного препарата в соответствии с изобретением может отличаться в зависимости от назначения, она предпочтительно находится в диапазоне от 160 мг до 1000 мг.
Кроме того, для фармацевтического комбинированного препарата в соответствии с изобретением предложен способ лечения различных расстройств, возникающих вследствие повышенного уровня холестерина, таких как дислипидемия, гиперлипидемия, гиперхолестеринемия, атеросклероз, артериосклероз, сердечно-сосудистое заболевание, заболевание сердечной артерии, ишемическая болезнь сердца, расстройство сердечно-сосудистой системы и связанные с ними расстройства, путем введения его терапевтически эффективного количества млекопитающим, нуждающимся в этом, в соответствии с подходящими схемами введения лекарственного средства.
Вариант осуществления изобретения
Ниже приведены предпочтительные примеры, служащие для лучшего понимания изобретения. Тем не менее, следующие примеры приведены исключительно для более легкого понимания изобретения, но не предназначены ограничивать объем изобретения.
Примеры 1-5. Приготовление гранул эзетимиба
Для рекомендованного приготовления умеренно растворимого эзетимиба готовили гранулы эзетимиба без розувастатина в соответствии с примерами 1-5.
1) Пример 1
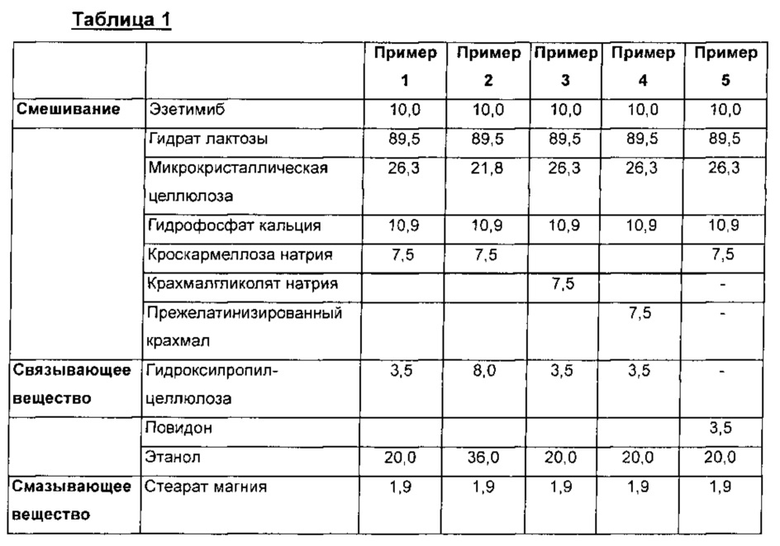
Сначала готовили раствор путем растворения 3,5 мг гидроксипропилцеллюлозы в 20,0 мг этанола. Смешивали вместе 10,0 мг эзетимиба, 89,5 мг гидрата лактозы, 26,3 мг микрокристаллической целлюлозы, 10,9 мг гидрофосфата кальция и 7,5 мг кроскармеллозы натрия, после чего смесь объединяли с вышеприведенным раствором с получением влажной смеси. Эту влажную смесь пропускали через сито от #12 до #25 меш и сушили в печи. Высушенную гранулу пропускали через сито от #16 до #30 меш с получением смеси гранул. К полученной смеси гранул добавляли 1,9 мг стеарата магния, после чего ее непрерывно перемешивали в течение от 1 до 3 мин. Состав представлен в таблице 1.
2) Пример 2
Осуществляли ту же самую процедуру, как в примере 1, за исключением того, что использовали 8,0 мг гидроксипропилцеллюлозы. Состав представлен в таблице 1.
3) Пример 3
Осуществляли ту же самую процедуру, как в примере 1, за исключением того, что использовали 7,5 мг крахмалгликолята натрия. Состав представлен в таблице 1.
4) Пример 4
Осуществляли ту же самую процедуру, как в примере 1, за исключением того, что использовали 7,5 мг прежелатинизированного крахмала. Состав представлен в таблице 1.
5) Пример 5
Осуществляли ту же самую процедуру, как в примере 1, за исключением того, что использовали 3,5 мг повидона. Состав представлен в таблице 1.

6) Тест растворения эзетимиба
Осуществляли тест растворения с использованием препаратов примеров 1-5 в условиях, изложенных ниже. EZETROL™, который представляет собой препарат с единственным ингредиентом эзетимибом, использовали в качестве контроля.
<Условие тестирования>
Образец: Примеры 1-5 и EZETROL™
Среды для теста растворения: рН 7,0 + SDS 0,5%, 900 мл, 37±0,5°С
Способ растворения: Способ 2 в соответствии с тестом растворения по Корейской фармакопее (способ с лопатками), 50 об/мин.
Результаты вышеприведенного теста растворения эзетимиба представлены в таблице 2 и на фиг. 1.
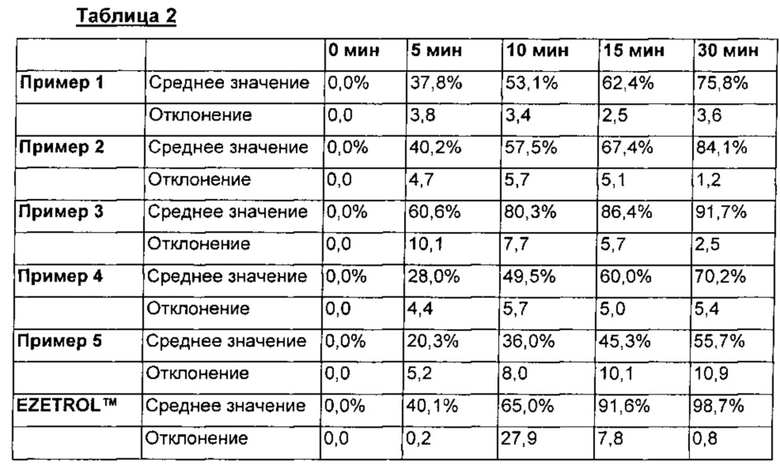
Как показано в таблице 2 и на фиг. 1, в контрольной группе EZETROL™ растворение происходило полностью через приблизительно 30 мин, и препарат примера, демонстрирующий наиболее близкую к этой картине растворения, представлял собой препарат примера 3. Соответственно фармацевтический комбинированный препарат в соответствии с изобретением готовили на основе примера 3.
Примеры 6-9. Комбинированный препарат эзетимиба и розувастатина
Основываясь на примере 3, готовили комбинированные препараты, дополнительно содержащие розувастатин, как показано в примерах 6 и 7.
1) Пример 6
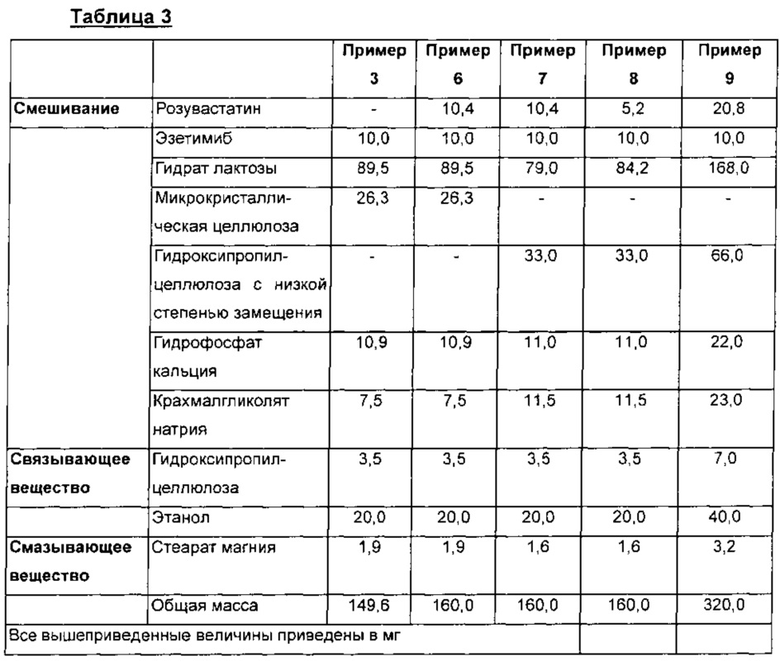
Сначала готовили раствор путем растворения 3,5 мг гидроксипропилцеллюлозы в 20,0 мг этанола. Смешивали вместе 10,4 мг розувастатина, 10,0 мг эзетимиба, 89,5 мг гидрата лактозы, 26,3 мг микрокристаллической целлюлозы, 10,9 мг гидрофосфата кальция и 7,5 мг крахмалгликолята натрия, после чего смесь объединяли с вышеприведенным раствором с получением влажной смеси. Эту влажную смесь пропускали через сито от #12 до #25 меш и сушили в печи. Высушенную гранулу пропускали через сито от #16 до #30 меш с получением смеси гранул. К полученной смеси гранул добавляли 1,9 мг стеарата магния, после чего ее непрерывно перемешивали в течение от 1 до 3 мин. Состав представлен в таблице 3. Для приготовления таблетки с оболочкой использовали 4,8 мг покрывающего агента Opadry на таблетку.
2) Пример 7
Сначала готовили раствор путем растворения 3,5 мг гидроксипропилцеллюлозы в 20,0 мг этанола. Смешивали вместе 10,4 мг розувастатина, 10,0 мг эзетимиба, 79,0 мг гидрата лактозы, 33,0 мг гидроксипропилцеллюлозы с низкой степенью замещения, 11,0 мг гидрофосфата кальция и 11,5 мг крахмалгликолята натрия, после чего смесь объединяли с вышеприведенным раствором с получением влажной смеси. Эту влажную смесь пропускали через сито от #12 до #25 меш и сушили в печи. Высушенную гранулу пропускали через сито от #16 до #30 меш с получением смеси гранул. К полученной смеси гранул добавляли 1,6 мг стеарата магния, после чего ее непрерывно перемешивали в течение от 1 до 3 мин. Состав представлен в таблице 3. Для приготовления таблетки с оболочкой использовали 4,8 мг покрывающего агента Opadry на таблетку.
3) Примеры 8 и 9
Осуществляли такую же методику, как в примере 7, за исключением того, что ингредиенты добавляли в количествах, представленных в таблице 3.
Составы композиций примеров 6-9 представлены в таблице 3. Для сравнения, также здесь показан пример 3.
Экспериментальный пример 1: Тесты растворения
1) Тест растворения эзетимиба
Осуществляли тест растворения с использованием препаратов примеров 6 и 7 в условиях, изложенных ниже. EZETROL™, который представляет собой препарат с единственным ингредиентом эзетимибом, использовали в качестве контроля.
<Условия тестирования>
Образец: Примеры 6 и 7 и EZETROL™
Среды для теста растворения: рН 7,0 + SDS 0,5%, 900 мл, 37±0,5°С
Способ растворения: Способ 2 в соответствии с тестом растворения по Корейской фармакопее (способ с лопатками), 50 об/мин.
Результаты вышеприведенного теста растворения эзетимиба представлены в таблице 4 и на фиг. 2.
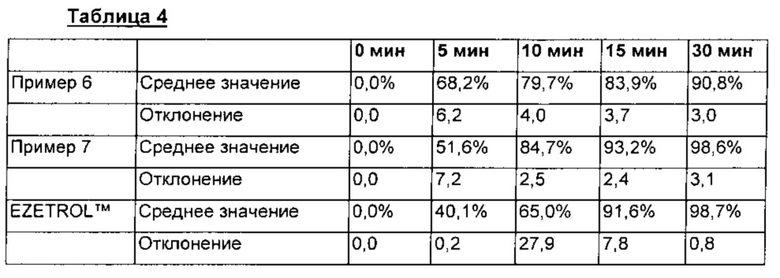
Как показано в таблице 4 и на фиг. 2, комбинированный препарат в соответствии с примером 6, где розувастатин просто добавлен к примеру 3, демонстрирует, что скорость растворения эзетимиба была несколько ниже (15 мин и 30 мин). Напротив, комбинированный препарат в соответствии с примером 7, где дополнительно добавлена гидроксипропилцеллюлоза с низкой степенью замещения, демонстрирует, что скорость растворения эзетимиба приблизительно совпадала со скоростью растворения EZETROL™, и его картина растворения была почти такой же.
2) Тест растворения розувастатина
Тест растворения осуществляли с использованием препаратов примеров 6 и 7 в условиях, изложенных ниже. CRESTOR™, который представляет собой препарат с единственным ингредиентом розувастатином, использовали в качестве контроля.
<Условия тестирования>
Образец: Примеры 6 и 7 и CRESTOR™
Среды для теста растворения: рН 6,6, 900 мл, 37±0,5°С
Способ растворения: Способ 2 в соответствии с тестом растворения по Корейской фармакопее (способ с лопатками), 50 об/мин.
Результаты вышеприведенного теста растворения розувастатина представлены в таблице 5 и на фиг. 3.
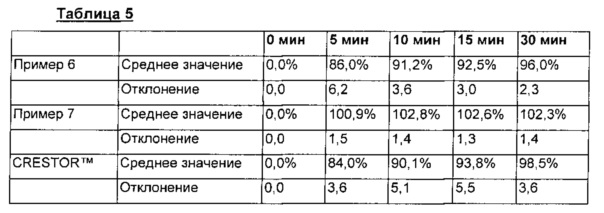
Как показано в таблице 5 и на фиг. 3, оба препарата примеров 6 и 7 демонстрируют картину растворения, аналогичную картине растворения CRESTOR™, но препарат примера 7 демонстрирует лучшее растворение.
Экспериментальный пример 2: фармакокинетические тесты in vivo
Для сравнения фармакокинетики in vivo комбинированного препарата в соответствии с примером 7, таблетки розувастатина кальция, имеющегося в продаже как CRESTOR™ (таблетка, содержащая 10 мг розувастатина), и таблетки эзетимиба, имеющегося в продаже в виде таблетки 10 мг EZETROL™, их вводили в одних и тех же условиях восемнадцати собакам породы бигль (три группы, шесть собак на группу). Результаты представлены в таблицах 6 и 7.
<Условия тестирования>
Образец: Комбинированный препарат в соответствии с примером 7, таблетка 10 мг CRESTOR™, таблетка 10 мг EZETROL™
Количество индивидуумов в группе: шесть собак в группе, три группы, всего 18 собак.
Введение: Однократное введение комбинированного препарата в соответствии с примером 7 давали группе 1, таблетку 10 мг CRESTOR™ группе 2 и таблетку 10 мг EZETROL™ группе 3 соответственно. Собак породы бигль случайным образом распределяли в каждую из групп.


Результаты фармакокинетического теста для комбинированного препарата в соответствии с примером 7, CRESTOR™ и EZETROL™ представлены в таблицах 6 и 7 выше. Отсутствовало статистически значимое различие в максимальной концентрации в плазме крови (Смакс) между CRESTOR™ и препаратом примера 7 и между EZETROL™ и препаратом примера 7. Кроме того, отсутствовало статистически значимое различие в площади пика под кривой (AUC). Таким образом, препарат примера 7 демонстрирует фармакокинетический профиль в организме, эквивалентный каждому из контролей.
Изобретение относится к химико-фармацевтической промышленности и представляет собой фармацевтический комбинированный препарат для лечения расстройств, возникающих вследствие повышенного уровня холестерина, содержащий от 5 до 15 массовых долей розувастатина или его фармацевтически приемлемых солей; от 5 до 15 массовых долей эзетимиба или его фармацевтически приемлемой соли; от 4,5 до 12 массовых долей крахмалгликолята натрия; и от 20 до 35 массовых долей гидроксипропилцеллюлозы с низкой степенью замещения по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата. Изобретение позволяет значительно улучшить удобство введения лекарственного средства для пациента, поскольку два типа лекарственных средств содержатся в одном препарате и картина растворения этих двух типов лекарственных средств при растворении комбинированного препарата является такой же, как картина растворения каждого лекарственного средства в препарате с единственным ингредиентом. 9 з.п. ф-лы, 3 ил., 7 табл., 2 пр.
1. Фармацевтический комбинированный препарат для лечения расстройств, возникающих вследствие повышенного уровня холестерина, содержащий
от 5 до 15 массовых долей розувастатина или его фармацевтически приемлемых солей;
от 5 до 15 массовых долей эзетимиба или его фармацевтически приемлемой соли;
от 4,5 до 12 массовых долей крахмалгликолята натрия; и
от 20 до 35 массовых долей гидроксипропилцеллюлозы с низкой степенью замещения по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата.
2. Фармацевтический комбинированный препарат по п. 1, где указанный розувастатин или его фармацевтически приемлемые соли содержатся в количестве от 9 до 11 массовых долей по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата.
3. Фармацевтический комбинированный препарат по п. 1, где указанный эзетимиб или его фармацевтически приемлемая соль содержится в количестве от 9 до 11 массовых долей по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата.
4. Фармацевтический комбинированный препарат по п. 1, где указанный крахмалгликолят натрия содержится в количестве от 11 до 12 массовых долей по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата.
5. Фармацевтический комбинированный препарат по п. 1, где указанная гидроксипропилцеллюлоза с низкой степенью замещения содержится в количестве от 30 до 35 массовых долей по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата.
6. Фармацевтический комбинированный препарат по п. 1, дополнительно содержащий гидрофосфат кальция по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата.
7. Фармацевтический комбинированный препарат по п. 6, где указанный гидрофосфат кальция содержится в количестве от 10 до 15 массовых долей по отношению к 100 массовым долям общей массы фармацевтического комбинированного препарата.
8. Фармацевтический комбинированный препарат по любому из пп. 1-7, где указанный розувастатин или его фармацевтически приемлемые соли имеет скорость растворения 85% или более в течение 30 мин при измерении в условиях растворения в буферном растворе при рН 6,6 при 37±0,5°С и при скорости перемешивания 50 об/мин в соответствии со способом 2 в тесте растворения по Корейской фармакопее.
9. Фармацевтический комбинированный препарат по любому из пп. 1-7, отличающийся тем, что указанный эзетимиб или его фармацевтически приемлемая соль имеет скорость растворения 80% или более в течение 15 мин при измерении в условиях растворения в буферном растворе при рН 7,0 при 37±0,5°С и при скорости перемешивания 50 об/мин в соответствии со способом 2 в тесте растворения по Корейской фармакопее.
10. Фармацевтический комбинированный препарат по любому из пп. 1-7, где общая масса указанного фармацевтического комбинированного препарата находится в диапазоне от 160 мг до 1000 мг.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| WO2006134604 A1, 21.12.2006 | |||
| Raymond C Rowe, Paul J Sheskey, Marian E Quinn, Handbook of Pharmaceutical Excipients, No 6, 2009, p | |||
| Уровень для полета по прямой траектории | 1923 |
|
SU917A1 |
| WO 2008101723 A2, 28.08.2008 | |||
| RU 2011121388 A, 10.12.2012 | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| М.И | |||
| Лутай | |||
| Новые возможности комбинированной липидоснижающей терапии: опыт клинического применения фиксированной комбинации аторвастатина и эзетимиба // Украинский кардиологический журнал | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| - С | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
Авторы
Даты
2018-04-04—Публикация
2014-12-18—Подача