По настоящей заявке испрашивается приоритет в соответствии с предварительной заявкой на патент США №61/857044, поданной 22 июля 2013 г., которая полностью включена в настоящий документ посредством ссылки.
Область техники
Предусмотрены способы и среды для снижения содержания селена в биомассе, полученной после ферментации содержащих СО газообразных субстратов. Более конкретно, предусмотрены способы и среды, которые эффективны для снижения содержания селена в биомассе после ферментации при сохранении высокого уровня производительности по этанолу.
Уровень техники
Процессы ферментации происходят в определенных жидких средах. Эти среды будут, как правило, содержать различные макро- и микроисточники питательных веществ, которые важны для улучшения продуктивности ферментации. Среды, используемые в связи с менее распространенными субстратами, такими как газообразные субстраты, требуют четко определенных сред для оптимизации производительности. Анаэробные процессы ферментации также требуют хорошо определенных сред.
Анаэробные микроорганизмы могут производить этанол из монооксида углерода (СО) путем ферментации газообразных субстратов. Ферментации с использованием анаэробных микроорганизмов из рода Clostridium производят этанол и другие полезные продукты. Например, в патенте США №5173429 описан Clostridium ljungdahlii АТСС №49587, анаэробный микроорганизм, который производит этанол и ацетат из газа для химического синтеза. В патенте США №5807722 описан способ и устройство для преобразования газообразных отходов в органические кислоты и спирты с использованием Clostridium ljungdahlii АТСС №55380. В патенте США №6136577 описан способ и устройство для преобразования газообразных отходов в этанол с использованием Clostridium ljungdahlii АТСС №55988 и 55989.
В патенте США №7285402 описаны среды, известные для использования в анаэробной ферментации газообразных субстратов для получения этанола. Различные компоненты и концентрации компонентов в среде эффективны для обеспечения высокого уровня производительности по этанолу. Устранение некоторых компонентов и уменьшение требуемых концентрационных уровней других компонентов при сохранении производительности по этанолу может обеспечить значительную экономию средств, особенно в промышленном масштабе ферментации.
Путь Вуда-Люнгдала хорошо известен в настоящей области техники и включает в себя реакции, которые могут быть разделены на две части: (1) метиловая часть и (2) карбонильная часть. Метиловая часть преобразует синтез-газ в метилтетрагидрофолат (метил-ТГФ), тогда как карбонильная часть преобразует метил-ТГФ в ацетил-КоА. Ацетил-КоА может затем быть преобразован в этанол. Ферменты катализируют реакции в пути Вуда-Люнгдала и эти ферменты требуют различных элементов для оптимальной функциональности. Например, формиатдегидрогеназа, важный фермент в пути Вуда-Люнгдала, требует наличия селена для оптимальной активности.
Сущность изобретения
Способ ферментации синтез-газа и среда ферментации обеспечивает высокую производительность по этанолу при удалении компонентов среды, которые ранее считались необходимыми. Удаление некоторых компонентов среды и снижение концентраций других компонентов среды обеспечивает значительную экономию эксплуатационных затрат в коммерческом масштабе.
Способ снижения содержания селена в клеточной биомассе после ферментации содержащего СО газообразного субстрата включает ферментацию содержащего СО газообразного субстрата в ферментационной среде. Способ эффективно обеспечивает специфическую объемную производительность, составляющую по меньшей мере приблизительно 1 г этанола/(л ⋅ день ⋅ грамм клеток), и содержание селена в клеточной биомассе, выходящей после ферментации, составляющее приблизительно 1 ppm или менее.
Способ ферментации содержащего СО газообразного субстрата включает ферментацию содержащего СО газообразного субстрата в ферментационной среде, содержащей менее чем приблизительно 1 ppm селена. Способ эффективно обеспечивает специфическую объемную производительность, составляющую по меньшей мере приблизительно 1 г этанола/(л ⋅ день ⋅ грамм клеток).
Ферментационная среда содержит по меньшей мере приблизительно 112 мг азота на грамм клеток, по меньшей мере приблизительно 10,5 мг фосфора на грамм клеток или по меньшей мере приблизительно 26 мг калия на грамм клеток. Ферментационная среда содержит менее чем приблизительно 1,04 ppm бора, менее чем приблизительно 0,16 ppm марганца, менее чем приблизительно 0,26 ppm молибдена, менее чем приблизительно 1 ppm селена или менее чем приблизительно 0,16 ppm меди.
Краткое описание чертежей
Вышеуказанные и другие аспекты, особенности и другие преимущества нескольких аспектов способа будут более очевидны из следующих чертежей.
На фиг. 1 показаны конверсии газов и плотность клеток после внесения Clostridium ljungdahlii С-01 в среду, не содержащую селен.
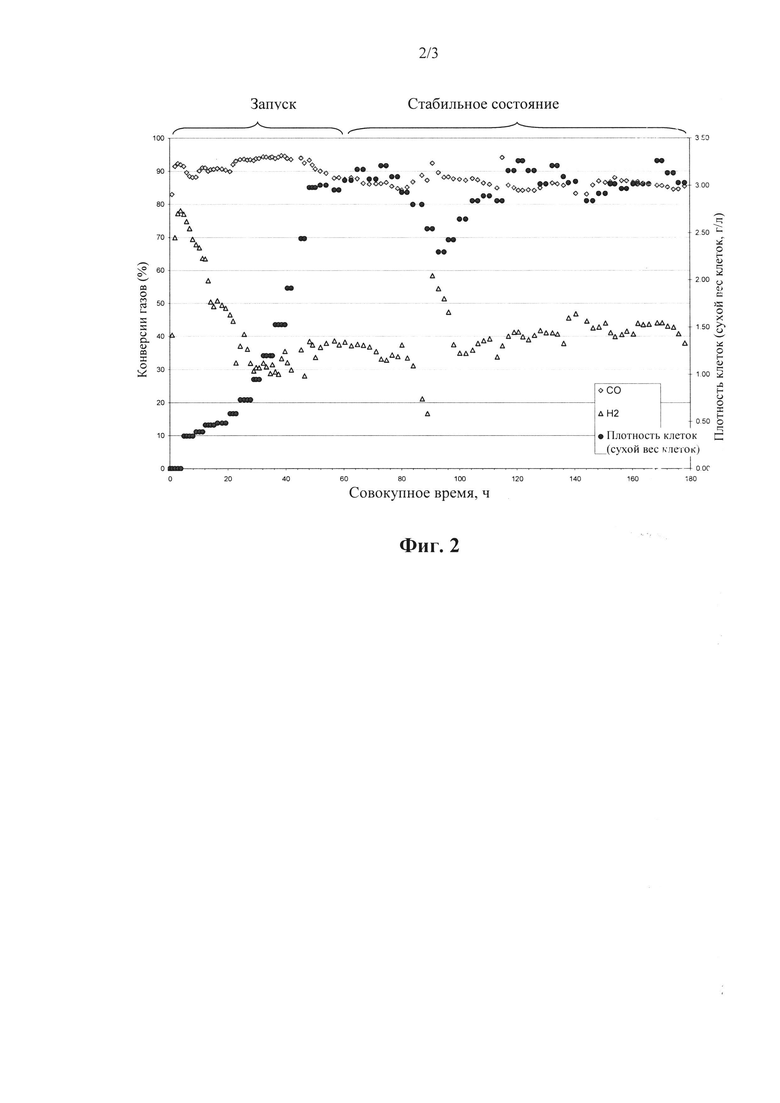
На фиг. 2 показаны конверсии газов и плотность клеток после внесения Clostridium ljungdahlii С-01 в среду, содержащую селен.
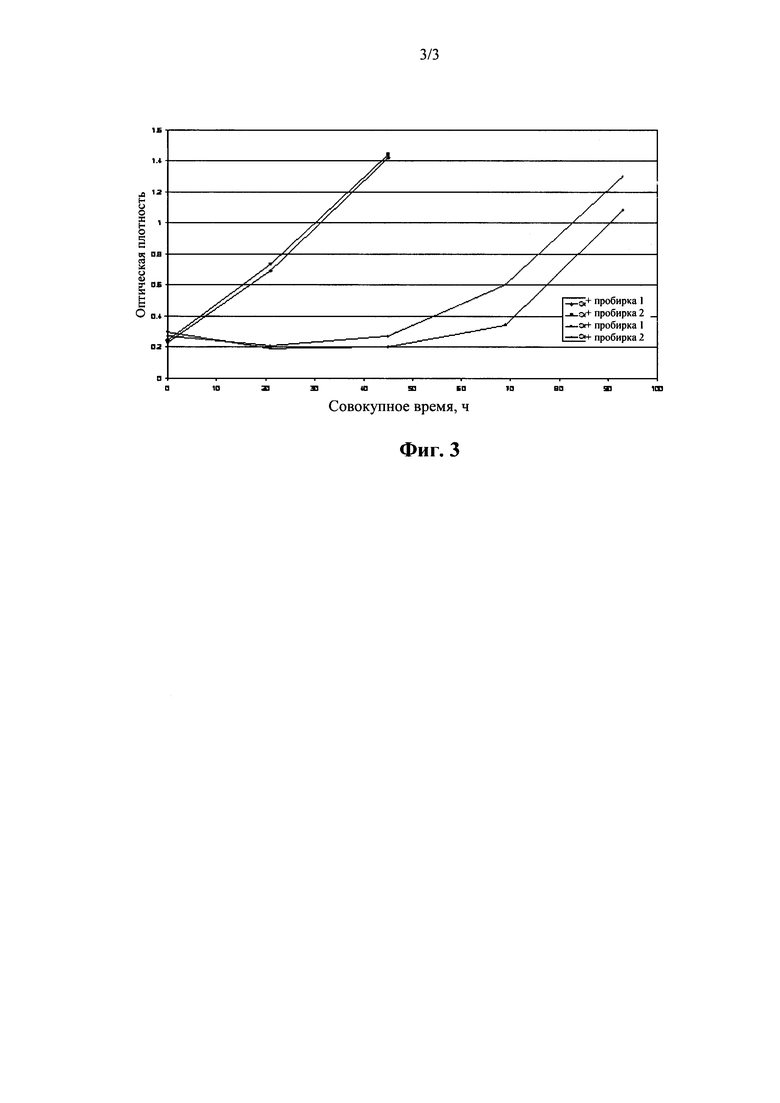
На фиг. 3 показано сравнение между кривыми роста культур С.autoethanogenum, выращенных в культуральных пробирках со средой, содержащей и не содержащей селен.
Подробное описание изобретения
Последующее описание не следует рассматривать в ограничительном смысле, оно приводится только с целью характеристики общих принципов иллюстративных аспектов. Объем настоящего изобретения определяется на основании формулы настоящего изобретения.
Предусмотрены способ и состав среды, которые удивительно и неожиданно обеспечивают высокий уровень производительности по этанолу даже после удаления или уменьшения концентрации селена, который раньше считался необходимым или требуемым в определенных концентрациях.
Ферментацию синтез-газа проводили в биореакторах с описанными в настоящем документе средой и ацетогенными бактериями, которые эффективно обеспечивают конверсию СО в синтез-газе в спирты и другие продукты. Согласно этому аспекту производительность может быть выражена как STY (объемная производительность, выраженная как г общего спирта/(л ⋅ день). Согласно этому аспекту способ эффективно обеспечивает STY (объемную производительность), составляющую по меньшей мере приблизительно 10 г или более общего спирта/(л ⋅ день). Возможные значения STY включают в себя от приблизительно 10 г общего спирта/(л ⋅ день) до приблизительно 200 г общего спирта/(л ⋅ день), согласно другому аспекту от приблизительно 10 г общего спирта/(L ⋅ день) до приблизительно 160 г общего спирта/(л ⋅ день), согласно другому аспекту от приблизительно 10 г общего спирта/(л ⋅ день) до приблизительно 120 г общего спирта/(л ⋅ день), согласно другому аспекту от приблизительно 10 г общего спирта/(л ⋅ день) до приблизительно 80 г общего спирта/(л ⋅ день), согласно другому аспекту от приблизительно 20 г общего спирта/(л ⋅ день) до приблизительно 140 г общего спирта/(л ⋅ день), согласно другому аспекту от приблизительно 20 г общего спирт/(л ⋅ день) до приблизительно 100 г общего спирта/(л ⋅ день), согласно другому аспекту от приблизительно 40 г общего спирта/(л ⋅ день) до приблизительно 140 г общего спирта/(л ⋅ день) и согласно другому аспекту от приблизительно 40 г общего спирта/(л ⋅ день) до приблизительно 100 г общего спирта/(л ⋅ день).
Определения
Если не указано иное, следующие термины, используемые в настоящем описании для настоящего изобретения, определяются следующим образом и могут включать формы либо единственного, либо множественного числа определенных ниже определений.
Термин "приблизительно", модифицирующий любое количество, относится к изменению в количестве, встречающемуся в реальных условиях, например, в лаборатории, на опытном заводе или производственном объекте. Например, количество ингредиента или измерение, используемое в смеси, или количество при модификации с помощью "приблизительно", включает изменение и степень, обычно используемую в измерении в экспериментальных условиях в производственной установке или лаборатории. Например, количество компонента продукта при модификации с помощью "приблизительно" включает изменение между партиями в нескольких экспериментах на заводе или в лаборатории и вариацию, присущую аналитическому способу. При наличии модификации или без нее с помощью "приблизительно" количества включают эквиваленты этих сумм. Любая величина, указанная в настоящем документе и модифицированная с помощью "приблизительно", может быть также использована в настоящем изобретении, так как количество не модифицировано с помощью "приблизительно".
Термин "газообразный субстрат" используется в неограничивающем смысле, чтобы включить в себя субстраты, содержащие или полученные из одного или нескольких газов.
Термин "синтез-газ" или "синтетический газ" означает газ для химического синтеза, который представляет собой название, данное газовой смеси, содержащей различные количества монооксида углерода и водорода. Примеры способов производства включают паровой риформинг природного газа или углеводородов для получения водорода, газификацию угля, а в некоторых видах установки газификации отходов в энергию. Название происходит от их использования в качестве промежуточных соединений в создании синтетического природного газа (SNG) и для получения аммиака или метанола. Синтез-газ представляет собой горючий и часто используется в качестве источника топлива или в качестве промежуточного продукта для производства других химических веществ.
Термин "ферментер" включает устройство ферментации, состоящее из одного или нескольких расположенных определенным образом сосудов и/или башен или трубопроводов, которые включают в себя непрерывный реактор с мешалкой (CSTR), иммобилизованный клеточный реактор (ICR), реактор с орошаемым слоем (TBR), биопленочный реактор с плавающей загрузкой (MBBR), барботажную колонку, газлифтный ферментер, мембранный реактор, такой как биореактор с системой полых волокон (HFMBR), статический смеситель или другой сосуд или другое устройство, подходящее для контакта газ-жидкость.
Термины "ферментация", "способ ферментации" или "реакция ферментации" и т.п. предназначены для охвата, как фазы роста, так и фазы биосинтеза продукта способа. Согласно одному аспекту ферментация относится к конверсии СО в спирт.
Термин "плотность клеток" означает массу клеток микроорганизмов на единицу объема ферментационного бульона, например, г/л.
Термин "повышение эффективности", "повышенная эффективность" и т.п. при использовании в отношении способа ферментации включает увеличение одного или нескольких из следующего: скорость роста микроорганизмов при ферментации, объем или масса требуемого продукта (такого как спирты), полученного на потребленную единицу объема или массу субстрата (такого как окись углерода), скорость производства или уровень производства требуемого продукта и относительная доля полученного желательного продукта по сравнению с другими побочными продуктами ферментации.
Используемый в настоящем документе термин "общий спирт" включает этанол, бутанол, пропанол и метанол. Согласно одному аспекту общий спирт может содержать по меньшей мере приблизительно 75 массовых процентов или более этанола, согласно другому аспекту приблизительно 80 массовых процентов или более этанола, согласно другому аспекту приблизительно 85 массовых процентов или более этанола, согласно другому аспекту приблизительно 90 массовых процентов или более этанола и согласно другому аспекту приблизительно 95 массовых процентов или более этанола. Согласно другому аспекту общий спирт может включать в себя приблизительно 25 массовых процентов или менее бутанола.
Термин "специфическое поглощение СО" означает количество СО в ммоль, потребляемых единицей массы клеток микроорганизмов (г) за единицу времени в минуты, т.е. ммоль/г/мин.
Содержащий СО субстрат
Содержащий СО субстрат может содержать любой газ, который содержит СО. Согласно этому аспекту содержащий СО газ может включать синтез-газы, промышленные газы и их смеси.
Синтез-газ может быть получен из любого известного источника. Согласно одному аспекту синтез-газ может быть получен путем газификации углеродсодержащих материалов. Газификация включает частичное сжигание биомассы в ограниченном доступе кислорода. Полученный газ в основном содержит СО и Н2. Согласно этому аспекту синтез-газ будет содержать по меньшей мере приблизительно 10 мольных % СО, согласно одному аспекту по меньшей мере приблизительно 20 мольных %, согласно одному аспекту приблизительно от 10 до 100 мольных %, согласно другому аспекту приблизительно от 20 до 100 мольных % СО, согласно другому аспекту от приблизительно 30 до приблизительно 90 мольных % СО, согласно другому аспекту от приблизительно 40 до приблизительно 80 мольных % СО и согласно другому аспекту приблизительно от 50 до 70 мольных % СО. Некоторые примеры подходящих способов и устройство газификации предусмотрены в патентах США с серийными номерами 61/516667, 61/516704 и 61/516646, каждый из которых был подан 6 апреля 2011 г., и в патентах США с серийными номерами 13/427144, 13/427193 и 13/427247, каждый из которых был подан 22 марта 2012 г., и каждый из которых включен в настоящий документ посредством ссылки.
Согласно другому аспекту способ характеризуется применением для поддержания производства спирта из газообразных субстратов, таких как большие объемы содержащих СО промышленных дымовых газов. Согласно некоторым аспектам газ, который содержит СО, получают из углеродсодержащих отходов, например, промышленных отходов газов или газификацией других отходов. Таким образом, процессы представляют собой эффективные процессы для захвата углерода, которые иначе должны были быть выделены в окружающую среду. Примеры промышленных дымовых газов включают в себя газы, произведенные в ходе производства продуктов из черных металлов, производства продуктов из цветных металлов, процессов переработки нефти, газификации угля, газификации биомассы, производства электроэнергии, производства сажи, производства аммиака, метанола и производства производственного кокса.
В зависимости от состава содержащего СО субстрата содержащий СО субстрат может быть предусмотрен непосредственно в способе ферментации или может быть дополнительно модифицирован, чтобы включать соответствующее молярное отношение Н2 к СО. Согласно одному аспекту содержащий СО субстрат, помещенный в ферментер, характеризуется молярным отношением Н2 к СО, составляющим приблизительно 0,2 или более, согласно другому аспекту 0,25 или более и согласно другому аспекту приблизительно 0,5 или более. Согласно другому аспекту содержащий СО субстрат, помещенный в ферментер, может содержать приблизительно 40 мольных процентов или более СО плюс Н2 и приблизительно 30 мольных процентов или менее СО, согласно другому аспекту приблизительно 50 мольных процентов или более СО плюс Н2 и приблизительно 35 мольных процентов или менее СО, и согласно другому аспекту приблизительно 80 мольных процентов или более СО плюс Н2 и приблизительно 20 мольных процентов или менее СО.
Согласно одному аспекту содержащий СО субстрат содержит в основном СО и Н2. Согласно этому аспекту содержащий СО субстрат содержит по меньшей мере приблизительно 10 мольных % СО, согласно одному аспекту по меньшей мере приблизительно 20 мольных %, согласно одному аспекту приблизительно от 10 до 100 мольных %, согласно другому аспекту от приблизительно 20 до приблизительно 100 мольных % СО, согласно другому аспекту от приблизительно 30 до приблизительно 90 мольных % СО, согласно другому аспекту от приблизительно 40 до приблизительно 80 мольных % СО и согласно другому аспекту приблизительно от 50 до 70 мольных % СО. Содержащий СО субстрат будет характеризоваться соотношением СО/СО2, составляющим по меньшей мере приблизительно 0,75, согласно другому аспекту по меньшей мере приблизительно 1,0 и согласно другому аспекту по меньшей мере приблизительно 1,5.
Согласно одному аспекту газовый сепаратор выполняют с возможностью по существу отделять по меньшей мере одну часть газового потока, причем часть содержит один или несколько компонентов. Например, газовый сепаратор может отделять СО2 из газового потока, содержащего следующие компоненты: СО, СО2, Н2, причем СО2 может быть передан в устройство для удаления СО2, а остальная часть газового потока (содержащего СО и Н2) может быть передана в биореактор. Может быть использован любой газовый сепаратор, известный в настоящей области техники. Согласно этому аспекту, помещенный в ферментер синтез-газ будет характеризоваться содержанием СО2, составляющим приблизительно 10 мольных % или менее, согласно другому аспекту приблизительно 1 мольный % или менее СО2 и согласно другому аспекту приблизительно 0,1 мольного % или менее СО2.
Некоторые газовые потоки могут содержать высокую концентрацию СО и низкие концентрации Н2. Согласно одному аспекту может быть желательно оптимизировать состав потока субстрата с целью достижения более высокой эффективности производства спирта и/или общего улавливания углерода. Например, концентрация Н2 в потоке субстрата может быть увеличена перед тем, как поток пропускают в биореактор.
В соответствии с конкретными аспектами настоящего изобретения потоки из двух или более источников могут быть объединены и/или смешаны с получением желаемого и/или оптимизированного потока субстрата. Например, поток, содержащий высокую концентрацию СО, такой как выхлопной поток на преобразователе сталелитейного завода, может быть объединен с потоком, содержащим высокие концентрации Н2, таким как отходящий газ из металлургическом коксовой печи.
В зависимости от состава газового содержащего СО субстрата, также может быть желательно обработать его, чтобы удалить ненужные примеси, такие как частицы пыли, перед введением в ферментацию. Например, газообразный субстрат может быть отфильтрован или очищен с использованием известных способов.
Разработка и эксплуатация биореактора
Описания разработок ферментеров охарактеризованы в патентах США с серийными номерами 13/471827 и 13/471858, оба поданные 15 мая 2012 г., и в патенте США с серийным номером 13/473167, поданном 16 мая 2012 г., каждый из которых включен в настоящий документ посредством ссылки.
В соответствии с одним аспектом способ ферментации начинается с добавления среды в реакционный сосуд. Некоторые примеры состава среды описаны в патентах США с серийными номерами 61/650098 и 61/650093, поданных 22 мая 2012 г., и в патенте США №7285402, поданном 23 июля 2001 г., каждый из которых включен в настоящий документ посредством ссылки. Среда может быть стерилизована для удаления нежелательных микроорганизмов, и в реактор вносят желаемые микроорганизмы. Стерилизация не всегда требуется.
Согласно одному аспекту используемые микроорганизмы включают в себя ацетогенные бактерии. Примеры полезных ацетогенных бактерий включают в себя бактерии из рода Clostridium, такие как штаммы Clostridium ljungdahlii, включающие в себя те, которые описаны в публикации международной заявки 2000/68407, Европейском патенте 117309, патентах США №5173429, 5593886 и 6368819, публикации международной заявки 1998/00558 и публикации международной заявки 2002/08438, штаммы Clostridium autoethanogenum (DSM 10061 и DSM 19630 в DSMZ, Германия), включая в себя те, которые описаны в публикации международной заявки 2007/117157 и публикации международной заявки 2009/151342, и Clostridium ragsdalei (P11, АТСС ВАА-622) и Alkalibaculum bacchi (СР11, АТСС ВАА-1772), включая в себя те, которые описаны, соответственно, в патенте США №7704723 и "Biofuels and Bioproducts from Biomass-Generated Synthesis Gas", Hasan Atiyeh, представленном на ежегодной государственной конференции EPSCoR в Оклахоме 29 апреля 2010 г., и Clostridium carboxidivorans (АТСС РТА-7827), описанные в заявке на патент США №2007/0276447. Другие подходящие микроорганизмы включают в себя микроорганизмы из рода Moorella, включающие в себя Moorella sp. HUC22-1 и из рода Carboxydothermus. Каждая из этих ссылок включена в настоящий документ посредством ссылки. Могут быть использованы смешанные культуры двух или более микроорганизмов.
Некоторые примеры полезных бактерий включают в себя Acetogenium kivui, Acetoanaerobium noterae, Acetobacterium woodii, Alkalibaculum bacchi CP11 (ATCC BAA-1772), Blautia producta, Butyribacterium methylotrophicum, Caldanaerobacter subterraneous, Caldanaerobacter subterraneous pacificus, Carboxydothermus hydrogenoformans, Clostridium aceticum, Clostridium acetobutylicum, Clostridium acetobutylicum P262 (DSM 19630 из DSMZ, Германия), Clostridium autoethanogenum (DSM 19630 из DSMZ, Германия), Clostridium autoethanogenum (DSM 10061 из DSMZ, Германия), Clostridium autoethanogenum (DSM 23693 из DSMZ, Германия), Clostridium autoethanogenum (DSM 24138 из DSMZ, Германия), Clostridium carboxidivorans P7 (АТСС PTA-7827), Clostridium coskatii (АТСС РТА-10522), Clostridium drakei, Clostridium ljungdahlii PETC (ATCC 49587), Clostridium ljungdahlii ERI2 (ATCC 55380), Clostridium ljungdahlii C-01 (ATCC 55988), Clostridium ljungdahlii O-52 (ATCC 55889), Clostridium magnum, Clostridium pasteurianum (DSM 525 of DSMZ Germany), Clostridium ragsdali P11 (ATCC BAA-622), Clostridium scatologenes, Clostridium thermoaceticum, Clostridium ultunense, Desulfotomaculum kuznetsovii, Eubacterium limosum, Geobacter sulfurreducens, Methanosarcina acetivorans, Methanosarcina barkeri, Morrella thermoacetica, Morrella thermoautotrophica, Oxobacter pfennigii, Peptostreptococcus productus, Ruminococcus productus, Thermoanaerobacter kivui и их смеси.
Все штаммы этой группы характеризуются размером генома, составляющим приблизительно 4,2 Мбит (Kорkе et al., 2010), и составом GC, равным приблизительно 32% моль (Abrini et al., 1994; Kорkе et al., 2010; Tanner et al., 1993) (публикация международной заявки 2008/028055; патент США №2011/0229947), и законсервированными основными ключевыми генными оперонами, кодирующими ферменты пути Вуда-Люнгдала (дегидрогеназу монооксида углерода, формилтетрагидрофолатсинтетазу, метилентетрагидрофолатдегидрогеназу, формилтетрагидрофолатциклогидролазу, метилентетрагидрофолатредуктазу и дегидрогеназу монооксида углерода/ацетил-КоА-синтазу) гидрогеназу, формиатдегидрогеназу, Rnf комплекс (rnfCDGEAB), пируват : ферредоксин оксидоредуктазу, альдегид : ферредоксин оксидоредуктазу (Kорkе et al., 2010, 2011). Было обнаружено, что организация и количество генов пути Вуда-Люнгдала, ответственных за поглощение газа, одинаково у всех видов, несмотря на различия в последовательности нуклеиновых кислот и аминокислот (Kорkе et al., 2011).
Все штаммы характеризуются аналогичной морфологией и размером (логарифмические растущие клетки составляют от 0,5 до 0,7×3-5 мкм), представляют собой мезофильные (оптимальная температура роста от 30 до 37°С) и строго анаэробные (Abrini et al., 1994; Tanner et al., 1993) (публикация международной заявки 2008/028055). Кроме того, все они разделяют одни и те же основные филогенетические черты, такие как одинаковый диапазон рН (рН 4-7,5, с оптимальным начальным рН 5,5-6), сильный автотрофный рост на содержащих СО газах с аналогичными темпами роста и метаболический профиль с этанолом и уксусной кислотой в качестве основного конечного продукта ферментации, с небольшими количествами 2,3-бутандиола и молочной кислоты, образованными при определенных условиях (Abrini et al., 1994; Kорkе et al., 2011; Tanner et al., 1993) (публикация международной заявки 2008/028055). Продукция индола наблюдалась у всех видов. Тем не менее, виды различаются в утилизации субстрата в виде различных сахаров (например, рамнозы, арабинозы), кислот (например, глюконат, цитрат), аминокислот (например, аргинин, гистидин) или других субстратов (например, бетаин, бутанол). Некоторые из видов оказались ауксотрофами к некоторым витаминам (например, тиамину, биотину), а другие нет.
Описанные черты, поэтому, не относятся к одному организму, подобному С. autoethanogenum или С. ljungdahlii, но представляют собой общие черты для карбоксидотрофных, синтезирующих этанол Clostridia. Таким образом, можно ожидать, что настоящее изобретение будет работать с помощью этих штаммов, хотя могут быть различия в производительности.
Способ ферментации желательно проводить в соответствующих условиях для получения желаемой ферментации (например, СО до этанола). Условия реакции, которые следует учитывать, включают в себя давление, температуру, расход газа, скорость потока жидкости, рН сред, окислительно-восстановительный потенциал сред, скорость перемешивания (если происходит с использованием реактора с механическим перемешиванием), содержание высеваемого материала, максимальные концентрации газового субстрата, чтобы обеспечить то, что СО в жидкой фазе не станет ограничивающим, и максимальные концентрации продукта, чтобы избежать ингибирования продукции.
Способы согласно настоящему изобретению могут быть использованы для поддержания жизнеспособности микробной культуры, причем микробная культура ограничена в СО, так что скорость передачи СО в раствор меньше, чем скорость поглощения культурой. Такие ситуации могут возникнуть, когда субстрат, содержащий СО, обеспечивается не непрерывно для микробной культуры; скорость переноса массы низкая или недостаточно СО в потоке субстрата для поддержания жизнеспособности культуры при оптимальной температуре. Согласно таким вариантам осуществления микробная культура будет быстро истощать СО, растворенный в жидкой питательной среде, и становиться ограниченной в субстрате, поскольку дополнительный субстрат не может быть обеспечен достаточно быстро.
Запуск: После внесения начальная скорость подачи исходного газа устанавливается эффективной для поддержания исходной популяции микроорганизмов. Выходящий газ анализируют для определения содержания выходящего газа. Результаты анализа газа используются для управления скоростью подаваемого газа. Согласно этому аспекту способ включает расчетное соотношение концентрации СО к исходной плотности клеток, составляющее от приблизительно 0,5 до приблизительно 0,9, согласно другому аспекту от приблизительно 0,6 до приблизительно 0,8, согласно другому аспекту от приблизительно 0,5 до 0,7 и согласно другому аспекту от приблизительно 0,5 до приблизительно 0,6.
Согласно другому аспекту способ ферментации включает предоставление синтез-газа в ферментационную среду в таком количестве, которое эффективно обеспечивает начальную расчетную концентрацию СО в ферментационной среде, составляющую от приблизительно 0,15 мМ до приблизительно 0,70 мМ, согласно другому аспекту от приблизительно 0,15 мМ до приблизительно 0,50 мМ, согласно другому аспекту от приблизительно 0,15 мМ до приблизительно 0,35 мМ, согласно другому аспекту от приблизительно 0,20 мМ до приблизительно 0,30 мМ и согласно другому аспекту от приблизительно 0,23 мМ до приблизительно 0,27 мМ. Способ представляет собой эффективный для повышения плотности клеток, по сравнению с начальной плотностью клеток.
После запуска: При достижении желаемого содержания, жидкую фазу и клеточный материал извлекают из реактора и пополняют средой. Способ эффективно повышает плотность клеток до приблизительно 2,0 г/л или более, согласно другому аспекту от приблизительно 2 до приблизительно 30 г/л, согласно другому аспекту от приблизительно 2 до приблизительно 25 г/л, согласно другому аспекту от приблизительно 2 до приблизительно 20 г/л, согласно другому аспекту от приблизительно 2 до приблизительно 10 г/л, согласно другому аспекту от приблизительно 2 до приблизительно 8 г/л, согласно другому аспекту от приблизительно 3 до приблизительно 30 г/л, согласно другому аспекту от приблизительно 3 до приблизительно 6 г/л и согласно другому аспекту от приблизительно 4 до приблизительно 5 г/л.
Состав среды
Согласно одному аспекту среда содержит по меньшей мере один или несколько источников азота, по меньшей мере один или несколько источника фосфора и по меньшей мере один или несколько источников калия. Среда может содержать любой из трех, любую комбинацию из трех и согласно одному важному аспекту содержит все три. Источник азота может включать источник азота, выбранный из группы, состоящей из хлорида аммония, гидроксида аммония, фосфата аммония, сульфата аммония, нитрата аммония и их смесей. Источник фосфора может включать источник фосфора, выбранный из группы, состоящей из фосфорной кислоты, фосфата аммония, фосфата калия и их смесей. Источник калия может включать источник калия, выбранный из группы, состоящей из хлорида калия, фосфата калия, нитрата калия, сульфата калия и их смесей.
Согласно одному аспекту среда содержит одно или несколько из следующего: железо, вольфрам, никель, кобальт, магний, сера и тиамин. Среда может содержать любой из этих компонентов, любую их комбинацию и согласно одному важному аспекту содержит все эти компоненты. Железо может включать источник железа, выбранный из группы, состоящей из хлористого железа, сульфата железа и их смесей. Источник вольфрама может включать источник вольфрама, выбранный из группы, состоящей из вольфрамата натрия, вольфрамата кальция, вольфрамата калия и их смесей. Источник никеля может включать источник никеля, выбранный из группы, состоящей из хлорида никеля, сульфата никеля, нитрата никеля и их смесей. Источник кобальта может включать источник кобальта, выбранный из группы, состоящей из хлорида кобальта, фторида кобальта, бромида кобальта, иодида кобальта и их смесей. Источник магния может включать источник магния, выбранный из группы, состоящей из хлорида магния, сульфата магния, фосфата магния и их смесей. Источник серы может включать в себя цистеин, сульфид натрия и их смеси.
Концентрации различных компонентов таковы:


Процесс работы поддерживает рН в диапазоне от приблизительно 4,2 до приблизительно 4,8. Среда содержит менее чем приблизительно 0,01 г/л дрожжевого экстракта и менее чем приблизительно 0,01 г/л углеводов.
Согласно этому аспекту среда может характеризоваться сниженными концентрациями одного или нескольких питательных веществ, которые включают в себя B, Mn, Mo и Cu. Концентрации питательных веществ в среде могут быть следующими:
В: менее чем приблизительно 1,04 ppm В, согласно другому аспекту менее, чем приблизительно 1,0 ppm В, согласно другому аспекту менее чем приблизительно 0,75 ppm В, согласно другому аспекту менее чем приблизительно 0,5 ppm В и согласно другому аспекту менее чем приблизительно 0,025 ppm В;
Mn: менее чем приблизительно 0,16 ppm Mn, согласно другому аспекту менее чем приблизительно 0,15 ppm Mn, согласно другому аспекту менее чем приблизительно 0,10 ppm Mn, согласно другому аспекту менее чем приблизительно 0,05 ppm Mn и согласно другому аспекту менее чем приблизительно 0,0025 м.д. Mn;
Mo: менее чем приблизительно 0,26 ppm Mo, согласно другому аспекту менее чем приблизительно 0,25 ppm Mo, согласно другому аспекту менее чем приблизительно 0,20 ppm Mo, согласно другому аспекту менее чем приблизительно 0,10 ppm Mo и согласно другому аспекту менее чем приблизительно 0,001 ppm Mo или
Cu: менее чем приблизительно 0,16 ppm Cu, согласно другому аспекту менее чем приблизительно 0,15 ppm Cu, согласно другому аспекту менее чем приблизительно 0,10 ppm Cu, согласно другому аспекту менее чем приблизительно 0,05 ppm Cu и согласно другому аспекту менее чем приблизительно 0,01 ppm Cu.
Согласно другому аспекту массовые соотношения могут быть следующими:
NH4+ к В: приблизительно 625:1 или более, согласно другому аспекту приблизительно 650:1 или более, согласно другому аспекту приблизительно 675:1 или более, согласно другому аспекту приблизительно 700:1 или более, согласно другому аспекту приблизительно 750:1 или более и согласно другому аспекту приблизительно 800:1 или более или
NH4+ к Mn: приблизительно 4050:1 или более, согласно другому аспекту приблизительно 4100:1 или более, согласно другому аспекту приблизительно 4200:1 или более, согласно другому аспекту приблизительно 4300:1 или более, согласно другому аспекту приблизительно 4400:1 или более и согласно другому аспекту приблизительно 4500:1 или более; или
NH4+ к Mo: приблизительно 2500:1 или более, согласно другому аспекту приблизительно 2600:1 или более, согласно другому аспекту приблизительно 2700:1 или более, согласно другому аспекту приблизительно 2800:1 или более, согласно другому аспекту приблизительно 2900:1 или более и согласно другому аспекту приблизительно 3000:1 или более; или
NH4+ к Cu: приблизительно 4050:1 или более, согласно другому аспекту приблизительно 4100:1 или более, согласно другому аспекту приблизительно 4200:1 или более, согласно другому аспекту приблизительно 4300:1 или более, согласно другому аспекту приблизительно 4400:1 или более и согласно другому аспекту приблизительно 4500:1 или более; или
Р к B: приблизительно 30:1 или более, согласно другому аспекту приблизительно 35:1 или более, согласно другому аспекту приблизительно 40:1 или более, согласно другому аспекту приблизительно 45:1 или более, согласно другому аспекту приблизительно 50:1 или более и согласно другому аспекту приблизительно 100:1 или более; или
Р к Mn: приблизительно 190:1 или более, согласно другому аспекту приблизительно 200:1 или более, согласно другому аспекту приблизительно 225:1 или более, согласно другому аспекту приблизительно 250:1 или более, согласно другому аспекту приблизительно 275:1 или более и согласно другому аспекту приблизительно 300:1 или более; или
Р к Мо: приблизительно 120:1 или более, согласно другому аспекту приблизительно 130:1 или более, согласно другому аспекту приблизительно 140:1 или более, согласно другому аспекту 150:1 или более, согласно другому аспекту приблизительно 175:1 или более и согласно другому аспекту приблизительно 200:1 или более; или
Р к Cu: приблизительно 190:1 или более; согласно другому аспекту приблизительно 200:1 или более, согласно другому аспекту приблизительно 225:1 или более, согласно другому аспекту приблизительно 250:1 или более, согласно другому аспекту приблизительно 275:1 или более и согласно другому аспекту приблизительно 300:1 или более; или
К к B: приблизительно 35:1 или более, согласно другому аспекту приблизительно 40:1 или более, согласно другому аспекту приблизительно 45:1 или более, согласно другому аспекту приблизительно 50:1 или более, согласно другому аспекту приблизительно 75:1 или более и согласно другому аспекту приблизительно 100:1 или более; или
К к Mn: приблизительно 245:1 или более, согласно другому аспекту приблизительно 250:1 или более, согласно другому аспекту приблизительно 260:1 или более, согласно другому аспекту приблизительно 270:1 или более, согласно другому аспекту приблизительно 280:1 или более и согласно другому аспекту приблизительно 300:1 или более; или
К к Mo: приблизительно 150:1 или более, согласно другому аспекту приблизительно 250:1 или более, согласно другому аспекту приблизительно 260:1 или более, согласно другому аспекту приблизительно 270:1 или более, согласно другому аспекту приблизительно 280:1 или более и согласно другому аспекту приблизительно 300:1 или более; или
К к Cu: приблизительно 245:1 или более, согласно другому аспекту приблизительно 250:1 или более, согласно другому аспекту приблизительно 260:1 или более, согласно другому аспекту приблизительно 270:1 или более, согласно другому аспекту приблизительно 280:1 или более и согласно другому аспекту приблизительно 300:1 или более.
Согласно другому аспекту способ и среды эффективно обеспечивают конверсию по меньшей мере от приблизительно 5% до приблизительно 99% СО, согласно другому аспекту от приблизительно 10% до приблизительно 90%, согласно другому аспекту от приблизительно 20% до приблизительно 80%, согласно другому аспекту от приблизительно 30% до приблизительно 70% и согласно другому аспекту от приблизительно 40% до приблизительно 90%.
Согласно другому аспекту способ и среда эффективно обеспечивают содержание селена в биомассе, выходящей из ферментации, составляющее приблизительно 1 ppm или менее. Согласно другому аспекту приблизительно 0,75 ppm или менее и согласно другому аспекту приблизительно 0,5 ppm или менее, все на основе сухой массы. Согласно другому аспекту содержание селена в биомассе после выхода из ферментации может составлять приблизительно от 0,01 до приблизительно 1 ppm, согласно другому аспекту от приблизительно 0,01 до приблизительно 0,9 ppm, согласно другому аспекту от приблизительно 0,01 до приблизительно 0,75 ppm, согласно другому аспекту от приблизительно 0,01 до приблизительно 0,5 ppm, согласно другому аспекту от приблизительно 0,01 до приблизительно 0,25 ppm, согласно другому аспекту от приблизительно 0,025 до приблизительно 1 ppm, согласно другому аспекту от приблизительно 0,025 до приблизительно 0,9 ppm, согласно другому аспекту от приблизительно 0,025 до приблизительно 0,75 ppm, согласно другому аспекту от приблизительно 0,025 до приблизительно 0,5 ppm, согласно другому аспекту от приблизительно 0,5 до 1 ppm, согласно другому аспекту от приблизительно 0,5 до приблизительно 0,9 ppm и согласно другому аспекту от приблизительно 0,5 до 0,75 ppm. Согласно одному аспекту Se может включать другие формы селена, включающие в себя состояния окисления -2, +2, +4 и +6, и может включать, например, Селенит и селенат. Указанные диапазоны относятся к эквивалентам Se.
ПРИМЕРЫ
Пример 1: Оценка роста культуры в среде с селенитом натрия
Получение среды: Среду получали следующим образом:
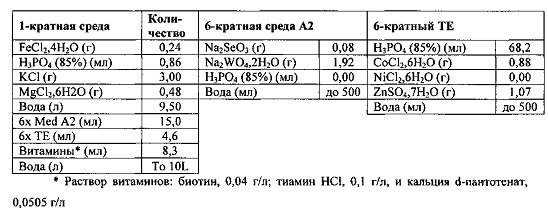
Засевание и поддерживание реактора: реактор серии BioFlo 310 (Нью-Брансуик) настраивали для анаэробной ферментации, чтобы включить проведение газа, как внутрь, так и наружу, продувку культуры, проведение питания и систему рециркуляции клеток, включающую в себя вытяжку фильтрата. Перед посевом реактор заполняли средой в объеме 2 л и продували синтез-газом в течение по меньшей мере 2 часов, температуру повышали до 38°С и рН доводили до и поддерживали между 4,4 и 4,7 с использованием 0,5 М NH4OH. Гидросульфид натрия (0,2% об./об.) смешивали с реакторной средой до конечной концентрации 9×10-4% об./об. На протяжении эксперимента перемешивание поддерживали при 800 оборотах в минуту.
В реактор вносили экспоненциально растущие клетки из исходного реактора для достижения начальной концентрации клеток 0,3 г/л (сухая масса клеток). Начиная со скорости потока газа 15 мл/мин синтез-газа (30% СО, 15% Н2, 10% СО2), 10% увеличение скорости потока газа выполняли на почасовой основе для поддержания роста клеток и поддерживали конверсию Н2 и СО >25% и >80%, соответственно, что определено способом газовой хроматографии (ГХ, SRI 8610С). На протяжении эксперимента скорость потока газа поддерживали между 250-300 мл/мин. Средний поток доводили до достижения 18-24 ч времени удерживания жидкости и плотность клеток контролировали с использование клеточной регенерационной системы на основе полого волокна. Гидросульфид натрия (0,2% об./об.) непрерывно смешивали непосредственно с реакторной средой с постоянной скоростью 0,2 мл/мин. После того как культура достигала плотности клеток от 2,5 до 3 г/л сухой массы клеток (определяемая OD580), систему рециркуляции клеток отключали и реактор работал как прямоточная система. Для анализа образования продукта жидкие образцы отбирали каждые 4 часа и анализировали с помощью жидкой ГХ, Shimadzu GC-2014. Реакторы поддерживали в устойчивом состоянии на протяжении по меньшей мере 5 дней.
В следующей таблице приведены характеристики стационарного состояния ферментации в среде, содержащей селен (Se(+)), и на фиг. 1 показан рост клеток и конверсии газа с течением времени.
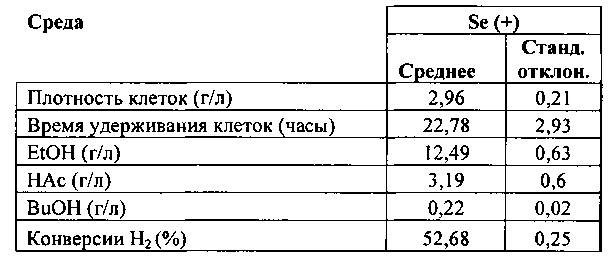

Пример 2. Оценка роста культуры в среде без селенита натрия
Получение среды: Среду без селена (-) готовили, как в примере 1, за исключением того, что селенит натрия был опущен из рецепта.
Засевание и поддерживание реактора: Использовали установку, которая описана в примере 1.
В следующей таблице приведено выполнение ферментации в среде без селена (Se (-)) и на фиг. 2 показан рост клеток и конверсии газов с течением времени.
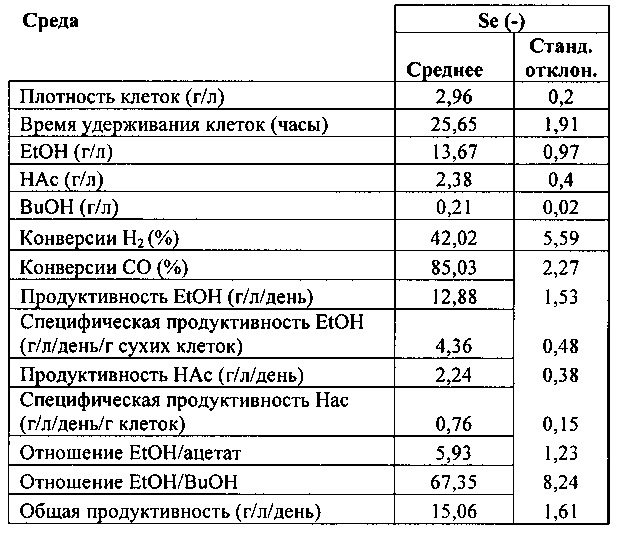
Пример 3: Количественное определение Se в клеточной массе.
Во время остановки реактора, 200 мл культуры удаляли и центрифугировали при 4000 оборотов в минуту в течение 5 мин при 4°С в центрифуге Allegra 25R (Beckman Coulter). Затем осадок промывали и ресуспендировали в охлажденном льдом 0,8% растворе хлорида натрия объемом 50 мл и снова центрифугировали. Полученный осадок хранили при -80°С до обработки. Параллельно образцы среды анализировали на наличие Se с использованием стандартного способа анализа индуктивно-связанной плазмы (ICP), как описано в "Standard Methods for the Examination of Water and Wastewater" 19th edition, A.D. Eaton, L.S. Clesceri и A.E. Greenberg, 1995, pp 3-34 Chapter 3120 B.
Клеточный анализ: Содержание селена клеток определяли с использованием анализа индуктивно-связанной плазмы (ICP). Образцы первоначально расщепляли с азотной кислотой (5% об./об.) и Н2О2 (10% об./об.) при 120°С в течение 2 часов, чтобы растворить клетки ('Standard Methods for the Examination of Water and Wastewater" 19th edition, A.D. Eaton, L.S. Clesceri and A.E. Greenberg, 1995, pp 3-5,Chapter 3030 E) и полученный продукт расщепления подвергали ICP.
Результаты: Оценка содержания селена в средах. В таблице ниже приведено содержание металла в среде с селеном Se (+) и без Se, используемой в эксперименте. Обратите внимание, что содержание селена в среде без Se находится на пределе обнаружения, используя стандартный анализ ICP и представляет собой 0,03 ppm (*)
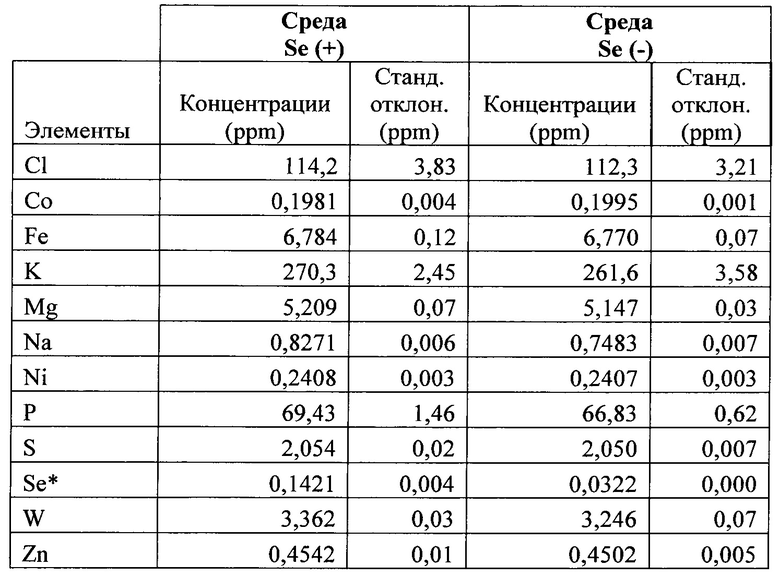
Результаты: Оценка содержания селена в клетках. Анализ Se в клетках показывает, что клетки, выращенные в отсутствие селенита натрия, характеризуются содержанием Se, составляющим 484 частицы на миллиард (~ 0,5 частиц на миллион) по сравнению с 34 частицами на миллион в клетках, выращенных в присутствии соли селена. Это представляет собой снижение на 98,5% содержания Se клеток.
Пример 4: Оценка скорости клеточного роста С. autoethanogenum в свободной от Se среде с использованием культуральных пробирок.
Следующую среду (1% MES) использовали для роста в пробирках с культурой.
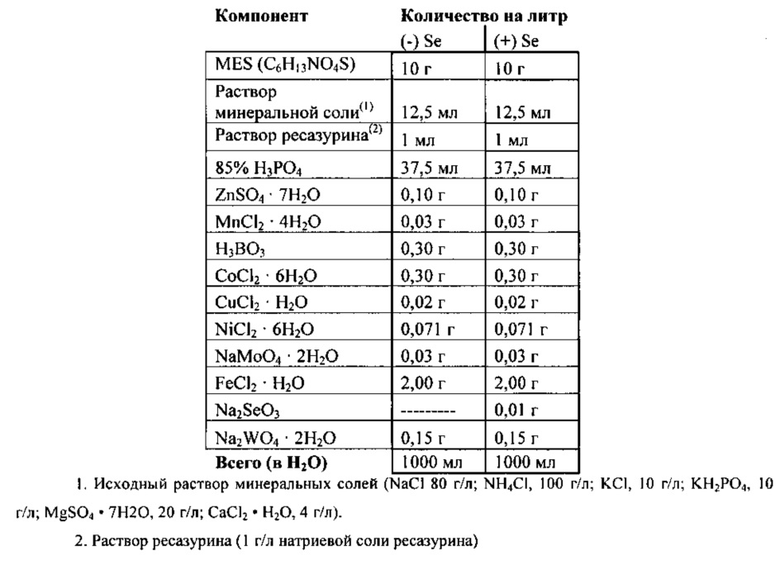
В культуральные пробирки, наполненные 4 мл соответствующей среды, вносили замороженный запас С. autoethanogenum (DSM #10061) и создавали повышенное давление синтез-газом до 4 атм. Для подготовки посевных культур в пробирки подавали синтез-газ ежедневно до тех пор, пока культура не достигала OD580 1,2. Четыре мл 1% MES +Se и/или 1% MES -Se засевали живыми клетками и создавали давление синтез-газа. Посевной материал первый раз центрифугировали при 3000 оборотах в минуту для осаждения клеток в анаэробных условиях. Осадок затем ресуспендировали в свежей среде Se(+) или Se(-) и использовали для засеянных новых культуральных пробирок при необходимой OD580 = 0,3. Затем культуры оставляли расти при 37°С в инкубаторе при встряхивании, составляющем 70 оборотов в минуту. Культуральные пробирки с засеянными С. autoethanogenum при начальной OD580 = 0,3 в среде 1% MES Se(+) или Se(-) наблюдали в течение долгого времени. Оптическую плотность каждой пробирки измеряли непосредственно после засевания и один раз в день после этого. Как видно на фиг. 3, клетки в обеих средах выросли до OD580 >1. Во время экспоненциальной фазы обе среды поддерживали ту же скорость роста.
Пример 5: Оценка функционирования и продуктивности ферментации С.autoethanogenum со средой без Se в биореакторе.
Культуру С. autoethanogenum использовали для внесения в посевной реактор, содержащий лабораторную среду (реактор объемом 1 л, биореактор с мешалкой SR0700ODLS, DASGIP). Внесение и поддерживание реактора осуществлялось по существу, как описано в примере 1. После того, как эта культура достигала стационарного состояния, ее использовали для засевания второго реактора, содержащего лабораторную среду без селена. Дочерней культуре позволяли достичь устойчивого состояния и в течение не менее 72 часов выдерживали в этом состоянии. Исходный реактор так же контролировали в это время в качестве сравнения.
В следующей таблице приведен состав среды для экспериментов с С. autoethanogenum.

Примечание: Отдельный MPFN готовили без Na2SeO3 для части эксперимента, в котором культуру выращивали в среде, не содержащей селен.
В таблице ниже представлены данные о функциональности ферментации С. autoethanogenum в стационарном состоянии в средах Se(+) и Se(-). Параметры в обоих случаях упали в пределах ожидаемого диапазона функциональности и не показали существенных различий между ними.

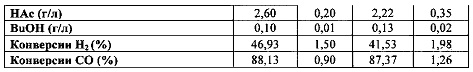
Аналогичные тенденции можно наблюдать в производительности каждой культуры, как показано ниже.
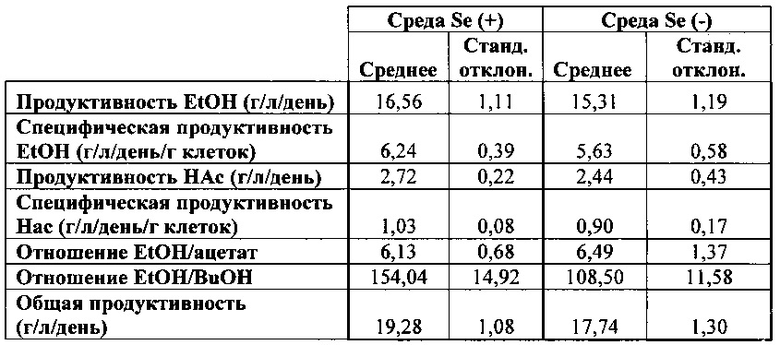
Хотя раскрытое в настоящем документе настоящее изобретение было описано с помощью конкретных аспектов, примеров и приложений, специалистами в настоящей области техники могут быть сделаны многочисленные модификации и вариации, не выходя за пределы объема настоящего изобретения, изложенного в формуле настоящего изобретения.

Изобретение относится к биотехнологии. Предложен способ снижения содержания селена в биомассе после ферментации содержащего СО газообразного субстрата. Способ включает ферментацию СО содержащего газообразного субстрата ацетогенными бактериями, причем ферментационная среда содержит менее 1 ppm селена, от 112 до 125 мг азота на грамм клеток, от 10,5 до 15 мг фосфора на грамм клеток, от 26 до 36 мг калия на грамм клеток. Способ обеспечивает объемную производительность по этанолу и снижение содержания селена в клеточной биомассе после ферментации. 5 з.п. ф-лы, 3 ил., 9 табл., 5 пр.
1. Способ снижения содержания селена в клеточной биомассе после ферментации содержащего СО газообразного субстрата, включающий:
ферментацию содержащего СО газообразного субстрата в ферментационной среде с ацетогенными бактериями;
причем ферментационная среда содержит менее чем 1 ppm селена и ферментационная среда содержит:
от 112 до 125 мг азота на грамм клеток,
от 10,5 до 15 мг фосфора на грамм клеток или
от 26 до 36 мг калия на грамм клеток;
причем способ обеспечивает специфическую STY, составляющую по меньшей мере 1 г этанола/(л ⋅ день ⋅ грамм клеток), и
причем способ обеспечивает содержание селена в биомассе клеток, выходящей из ферментации, равное 1 ppm или менее.
2. Способ по п. 1, при котором рН ферментационной среды поддерживают в интервале от 4,2 до 4,8.
3. Способ по п. 1, при котором синтез-газ характеризуется соотношением СО/СО2, составляющим по меньшей мере 0,75.
4. Способ по п. 1, при котором селен находится в виде селенита.
5. Способ по п. 1, при котором селен находится в виде селената.
6. Способ по п. 1, при котором ацетогенные бактерии выбирают из группы, состоящей из Acetogenium kivui, Acetoanaerobium noterae, Acetobacterium woodii, Alkalibaculum bacchi CP11 (ATCC BAA-1772), Blautia producta, Butyribacterium methylotrophicum, Caldanaerobacter subterraneous, Caldanaerobacter subterraneous pacificus, Carboxydothermus hydrogenoformans, Clostridium aceticum, Clostridium acetobutylicum, Clostridium acetobutylicum P262 (DSM 19630 из DSMZ, Германия), Clostridium autoethanogenum (DSM 19630 из DSMZ, Германия), Clostridium autoethanogenum (DSM 10061 из DSMZ, Германия), Clostridium autoethanogenum (DSM 23693 из DSMZ, Германия), Clostridium autoethanogenum (DSM 24138 из DSMZ, Германия), Clostridium carboxidivorans P7 (ATCC PTA-7827), Clostridium coskatii (АТСС РТА-10522), Clostridium drakei, Clostridium ljungdahlii PETC (ATCC 49587), Clostridium ljungdahlii ERI2 (ATCC 55380), Clostridium ljungdahlii C-01 (ATCC 55988), Clostridium ljungdahlii O-52 (ATCC 55889), Clostridium magnum, Clostridium pasteurianum (DSM 525 из DSMZ, Германия), Clostridium ragsdali P11 (ATCC BAA-622), Clostridium scatologenes, Clostridium thermoaceticum, Clostridium ultunense, Desulfotomaculum kuznetsovii, Eubacterium limosum, Geobacter sulfurreducens, Methanosarcina acetivorans, Methanosarcina barkeri, Morrella thermoacetica, Morrella thermoautotrophica, Oxobacter pfennigii, Peptostreptococcus productus, Ruminococcus productus, Thermoanaerobacter kivui и их смесей.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| EP 200300158 А, 28.08.2003 | |||
| SAXENA J., TANNER R.S | |||
| "Effect of trace metals on ethanol production from synthesis gas by the ethanologenic acetogen, Clostridium ragsdalei".// Journal of Industrial Microbiology and Biotechnology, 2011, vol.38, p.513-521 | |||
| YING GUO ET AL, "Medium optimization for ethanol production with Cloctridium autoethanogenum with carbon monoxide as sole carbon source".// Bioresource Technology, 2010, vol.101, p.8784-8789. | |||
Авторы
Даты
2018-05-21—Публикация
2014-07-18—Подача