Приоритет настоящей заявки испрашивается на основании предварительных заявок на патент США 61/650098 и 61/650093, поданных 22 мая 2012 г., и предварительной патентной заявки США 61/726225, поданной 14 ноября 2012 г., которые во всей полноте в виде ссылки включены в настоящую заявку.
Область техники
В изобретении предложен способ ферментации синтез-газа, позволяющий снижать проводимость и обеспечивать STY спирта около 10 г этанола/(л⋅сутки) или более. Более точно, способ включает обеспечение скорости подачи азота в реакционный сосуд в количестве около 100 мг или более азота на грамм синтезируемых клеток.
Уровень техники
Анаэробные микроорганизмы способны синтезировать этанол из СО путем ферментации газообразных носителей. В результате ферментации с участием анаэробных микроорганизмов рода Clostridium образуется этанол и другие полезные продукты. Например, в патенте US 5173429 описан анаэробный микроорганизм Clostridium ljungdahlii (ATCC №49587), который синтезирует этанол и ацетат из синтез-газа. В патенте US 5807722 описаны способ и устройство для конверсии отходящих газов в органические кислоты и спирты с использованием Clostridium ljungdahlii (ATCC №55380). В патенте US 6136577 описаны способ и устройство для конверсии отходящих газов в этанол с использованием Clostridium ljungdahlii (ATCC №55988 и 55989).
Для стабильной продуктивности и производительности по этанолу ацетогенным бактериям требуется постоянный источник азота в форме аммиака. Чаще всего источником аммиака является хлорид аммония, представляющий собой поток среды с низким рН. Гидроокись аммония является предпочтительной за счет своей стоимости и доступности. Тем не менее, поскольку гидроокись аммония является основанием, ее требуется добавлять в виде отдельного потока среды. Этот добавляемый поток с высоким рН может затруднять ферментацию. Кроме того, при более высокой производительности (>50 STY) с использованием более концентрированной среды ионная сила ферментационной среды повышается до уровня, отрицательно воздействующего на ее продуктивность.
Сущность изобретения
Предложен способ ферментации синтез-газа, снижающий проводимость и повышающий STY спирта. Способ включает подачу в реакционный сосуд синтез-газа и обеспечение скорости подачи в реакционный сосуд азота в количестве около 100 мг или более азота на грамм синтезируемых клеток. Путем ферментации синтез-газа обеспечивается ферментационная среда со средней проводимостью около 16 мСм/см или менее и STY 10 г этанола/(л⋅сутки) или более. Согласно этой особенности азот поступает из источника, который включает безводный аммиак, водный аммиак, гидроокись аммония, ацетат аммония, органические или неорганические нитраты и нитрилы, амины, имины, амиды, аминокислоты, аминоспирты и их смеси. Согласно одной из особенностей источником азота является гидроокись аммония. Способ включает подачу синтез-газа с соотношением СО/СО2 около 0,75 или более и ферментацию синтез-газа ацетогенными бактериями одного или нескольких видов. Путем ферментации обеспечивается плотность клеток около 1,0 г/л или более и конверсия от около 5 до около 99% СО. Согласно одной из особенностей ферментационная среда содержит около 0,01 г/л или менее дрожжевого экстракта и около 0,01 г/л или менее углеводов.
Согласно одной из особенностей предложен способ снижения проводимости при ферментации, включающий подачу синтез-газа в реакционный сосуд с ферментационной средой. Способ включает подачу в реакционный сосуд азота в количестве около 100 мг или более азота на грамм синтезируемых клеток, при этом хлорид аммония в подаваемом азоте замещен гидроокисью аммония. За счет подачи обеспечивается проводимость около 16 мСм/см или менее и рН от около 4,2 до около 4,8.
Согласно другой особенности способ снижения проводимости ферментационной среды включает подачу в реакционный сосуд синтез-газа и подачу в реакционный сосуд азота в количестве около 100 мг или более азота на грамм синтезируемых клеток. Согласно этой особенности хлорид аммония в подаваемом азоте замещен гидроокисью аммония. Способ обеспечивает снижение проводимости по меньшей мере примерно на 20% по сравнению с ферментацией, когда подаваемым азотом является хлорид аммония. Согласно одной из особенностей ферментационная среда содержит от около 100 до около 340 мг азота на грамм синтезируемых клеток, от около 10,5 до около 15 мг фосфора на грамм синтезируемых клеток или от около 26 до около 36 мг калия на грамм синтезируемых клеток. Согласно этой особенности источником азота является гидроокись аммония.
Подробное описание изобретения
Следующее далее описание не следует считать ограничивающим, и оно имеет целью лишь изложение общих принципов примеров осуществления. Объем изобретения следует определять на основании формулы изобретения.
Описанная в изобретении ферментация синтез-газа в биореакторах со средой и ацетогенными бактериями обеспечивает конверсию содержащейся в синтез-газе СО в спирты и другие продукты. За счет использования гидроокиси аммония в качестве источника азота и снижения проводимости обеспечиваются высокие уровни производительности. Согласно этой особенности производительность по спирту может выражаться как STY (выход продукта за один проход в единицу в граммах этанола/(л⋅сутки). Согласно этой особенности способ обеспечивает STY по меньшей мере около 10 г этанола/(л⋅сутки). Возможные величины STY включают от около 10 г этанола/(л⋅сутки) до около 200 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки) до около 160 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки) до около 120 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки) до около 80 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки) до около 15 г этанола/(л⋅сутки), согласно другой особенности от около 15 г этанола/(л⋅сутки) до около 20 г этанола/(л⋅сутки), согласно другой особенности от около 20 г этанола/(л⋅сутки) до около 140 г этанола/(л⋅сутки), согласно другой особенности от около 20 г этанола/(л⋅сутки) до около 100 г этанола/(л⋅сутки), согласно другой особенности от около 40 г этанола/(л⋅сутки) до около 140 г этанола/(л⋅сутки), согласно другой особенности от около 40 г этанола/(л⋅сутки) до около 100 г этанола/(л⋅сутки), согласно другой особенности от около 10 г этанола/(л⋅сутки), согласно другой особенности от около 15 г этанола/(л⋅сутки) и согласно другой особенности около 16 г этанола/ (л⋅сутки).
Определения
Если не указано иное, следующие термины, используемые в описании настоящего изобретения, имеют следующее значение согласно приведенным далее определениям в единственном или множественном числе.
Термины "проводимость" и "средняя проводимость" означают способность проводить электричество. Вода проводит электричество, поскольку в ней растворены твердые частицы, являющиеся носителями электрических зарядов. Например, хлорид, нитрат и сульфат являются носителями отрицательных зарядов, а натрий, магний и кальций являются носителями положительных зарядов. Эти растворенные твердые частицы влияют на способность воды проводить электричество. Проводимость измеряют зондом, который прилагает напряжение между двумя электродами. Перепад напряжения используется для измерения сопротивления воды, которое затем преобразуют в проводимость. Средняя проводимость может измеряться известными методами и способами. Некоторые примеры измерения средней проводимости приведены в стандарте ASTM D1125 под названием "Standard Test Methods for Electrical Conductivity and Resistivity of Water" и в стандарте Американской ассоциации работников здравоохранения, Американской ассоциации водоподготовки и Федерации защиты водной окружающей среды под названием "Standard Methods for the Examination of Water and Wastewater", 1999 г., оба из которых в порядке ссылки включены в настоящую заявку.
Термин "около", предшествующий любому численному значению, означает отклонение от указанного значения в реальных условиях, например, в лаборатории, на экспериментальной установке или эксплуатационном объекте. Например, численное значение с предшествующим ему термином "около" применительно к ингредиенту смеси или измерению количества, включает отклонение и степень точности, обычно применяемую при измерениях в экспериментальных условиях на промышленной установке или в лаборатории. Например, численное значение с предшествующим ему термином "около" применительно к компоненту продукта включает отклонение в зависимости от партий во множестве экспериментов на установке или в лаборатории и отклонение, присущее методу анализа. Независимо от использования термина "около" численные значения включают эквиваленты этих значений. Любое приведенное в описании численное значение с предшествующим ему термином "около" также может применяться в настоящем изобретении без термина "около".
Термином "синтез-газа" или "синтетический газ" называют газовую смесь, содержащую варьирующие количества окиси углерода и водорода. Примеры получения синтез-газа включают паровой реформинг природного газа или углеводородов с целью получения водорода, газификацию каменного угля и получение энергии путем газификации отходов на установках некоторых типов. Происхождение термина объясняется тем, что синтез-газ используется в качестве промежуточного продукта при получении заменителя природного газа (SNG) и производстве аммиака или метанола. Синтез-газа является горючим и часто используется в качестве источника топлива или промежуточного продукта при производстве других химикатов.
Термины "ферментация", "процесс ферментации" или "реакция ферментации" и т.п. относятся как к фазе роста, так и фазе биосинтеза продуктов. Согласно одной из особенностей ферментация означает конверсию СО в спирт.
Термин "плотность клеток" означает массу клеток микроорганизмов на единицу объема ферментационной среды, например, грамм/литр. Согласно этой особенности способ и среды обеспечивают плотность клеток по меньшей мере примерно на 1,0 г/л. Плотность клеток может составлять от около 1 до около 25 г/л, согласно другой особенности от около 1 до около 20 г/л, согласно другой особенности от около 1 до около 10 г/л, согласно другой особенности от около 10 до около 20 г/л, согласно другой особенности от около 12 до около 18 г/л, согласно другой особенности от около 14 до около 16 г/л, согласно другой особенности от около 2 до около 8 г/л, согласно другой особенности от около 3 до около 6 г/л и согласно другой особенности от около 4 до около 5 г/л. Термин "рециркуляция клеток" означает отделение клеток микроорганизмов от ферментационной среды и возврат всех или части этих отделенных клеток микроорганизмов в ферментер. Обычно для отделения и используется фильтрационное устройство.
Термин "ферментер", "реакционный сосуд" или "биореактор" означает ферментационное устройство из одного или нескольких сосудов и/или башен или трубопроводных обвязок, включая реактор с непрерывным перемешиванием (CSTR), реактор с иммобилизованными клетками (ICR), реактор с капельным слоем (TBR), реактор с подвижным биопленочным слоем (MBBR), барботажную колонну, газлифтный ферментер, мембранный реактор, такой как мембранный биореактор с системой полых волокон (HFMBR), статический смеситель или другой сосуд или устройство, применимое для введения в контакт газа и жидкости.
Содержащий СО газообразный носитель
Согласно одной из особенностей способ применим для обеспечения производства спирта из газообразных носителей, таких как большие объемы содержащих СО промышленных дымовых газов. Согласно некоторым особенностям газ, содержащий СО, получают из углеродсодержащих отходов, например, промышленных отходящих газов или продуктов газификации других отходов. По существу, способ позволяет эффективно использовать углерод, который в противном случае выпускался бы в окружающую среду. Примеры промышленных дымовых газов включают газы, образующиеся при производстве изделий из черных металлов, цветных металлов, при переработке нефти, газификации угля, биомассы, при производстве электроэнергии, сажи, метанола и кокса.
Согласно другой особенности содержащим СО газообразным носителем может являться синтез-газ. Может использоваться синтез-газа из любого известного источника. Согласно одной из особенностей источником синтез-газа может являться газификация углеродистых материалов. Газификация предусматривает частичное сжигание биомассы в условиях ограниченной подачи кислорода. Образующийся газ по большей части содержит СО и H2. Согласно этой особенности синтез-газа содержит по меньшей мере около 10 мол. % СО, согласно одной из особенностей по меньшей мере около 20 мол. %, согласно одной из особенностей от около 10 до около 100 мол. %, согласно другой особенности от около 20 до около 100 мол. % СО, согласно другой особенности от около 30 до около 90 мол. % СО, согласно другой особенности от около 40 до около 80 мол. % СО и согласно другой особенности от около 50 до около 70 мол. % СО. Синтез-газа имеет молярное соотношение СО/СО2 по меньшей мере около 0,75, согласно другой особенности по меньшей мере около 1,0, согласно другой особенности по меньшей мере около 1,5, согласно другой особенности по меньшей мере около 2,0, согласно другой особенности по меньшей мере около 2,5, согласно другой особенности по меньшей мере около 3,0 и согласно другой особенности по меньшей мере около 3,5. Некоторые примеры применимых способов и устройств для газификации описаны в заявках US 13/427144, 13/427193 и 13/427247, поданных 22 марта 2012 г. и в порядке ссылки включенных в настоящую заявку.
Согласно другой особенности синтез-газом, используемым для распространения ацетогенных бактерий, может являться преимущественно СО. Используемый оборот "преимущественно СО" означает, что газ содержит по меньшей мере около 50 мол. % СО, согласно другой особенности по меньшей мере около 60 мол. % СО, согласно другой особенности по меньшей мере около 70 мол. % СО, согласно другой особенности по меньшей мере около 80 мол. % СО и согласно другой особенности по меньшей мере около 90 мол. % СО.
В зависимости от состава содержащего СО газообразного носителя также может быть желательным очищать его с целью удаления любых нежелательных примесей, таких как частицы пыли, до подачи его в ферментер. Например, газообразный носитель может подвергаться фильтрации или очистке в скруббере известными способами.
Среда
Согласно одной из особенностей ферментация начинается с добавления применимой среды в реакционный сосуд. Жидкость в реакционном сосуде может содержать применимую питательную или ферментационную среду любого типа. Питательная среда содержит витамины и минералы, обеспечивающие рост используемых микроорганизмов. Известны анаэробные среды, применимые для ферментации этанола с использованием СО в качестве источника углерода. Один из примеров применимой ферментационной среды описан в патенте US 7285402, который в порядке ссылки включен в настоящую заявку. Другие примеры применимой среды описаны в заявках US 61/650098 и 61/650093, поданных 22 мая 2012 и в порядке ссылки включенных в настоящую заявку. Согласно одной из особенностей используемая среда, содержит менее около 0,01 г/л дрожжевого экстракта и менее около 0,01 г/л углеводов. Согласно одной из особенностей способ включает подачу в реакционный сосуд азота в количестве около 100 мг или более азота на грамм синтезируемых клеток. Согласно другой особенности подают азот в количестве от около 100 до около 340 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 160 до около 340 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 160 до около 200 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 160 до около 180 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 160 до около 170 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 170 до около 190 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 170 до около 180 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 200 до около 330 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 170 до около 175 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 175 до около 190 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 175 до около 185 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 175 до около 180 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 180 до около 200 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 180 до около 190 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 180 до около 185 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 185 до около 210 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 185 до около 200 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 185 до около 190 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 190 до около 210 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 190 до около 200 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 190 до около 195 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 210 до около 320 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 220 до около 310 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 230 до около 300 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 240 до около 290 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 250 до около 280 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 260 до около 270 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 195 до около 300 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 195 до около 275 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 195 до около 250 мг азота на грамм синтезируемых клеток, согласно другой особенности от около 195 до около 225 мг азота на грамм синтезируемых клеток и согласно другой особенности от около 195 до около 200 мг азота на грамм синтезируемых клеток. Согласно этой особенности азот поступает из источника, который включает безводный аммиак, водный аммиак, гидроокись аммония, ацетат аммония, органические или неорганические нитраты и нитрилы, амины, имины, амиды, аминокислоты, аминоспирты и их смеси. Согласно одной из особенностей источником азота является гидроокись аммония.
Согласно другой особенности способ обеспечивает среднюю проводимость около 16 мСм/см или менее, согласно другой особенности около 12 мСм/см или менее, согласно другой особенности около 8 мСм/см или менее, согласно другой особенности около 6,5 мСм/см или менее, согласно другой особенности около 6,0 мСм/см или менее, согласно другой особенности около 5,5 мСм/см или менее, согласно другой особенности около 5,0 мСм/см или менее, согласно другой особенности около 4,7 мСм/см или менее, согласно другой особенности около 4,5 мСм/см или менее, согласно другой особенности от около 4,0 мСм/см до около 6,5 мСм/см, согласно другой особенности от около 5,0 мСм/см до около 6,0 мСм/см и согласно другой особенности от около 4,0 мСм/см до около 5,0 мСм/см.
Согласно одной из особенностей способ включает регулирование проводимости с поддержанием STY на желаемых уровнях. Замещение или замена хлорида аммония гидроокисью аммония в среде позволяет снижать проводимость и поддерживать STY на желаемых уровнях. Согласно этой особенности добавляют гидроокись аммония в качестве компонента среды и/или используют с целью регулирования рН среды. Согласно этой особенности замещение хлорида аммония гидроокисью аммония позволяет снижать проводимость среды примерно на 20% или более, согласно другой особенности примерно на 25% или более, согласно другой особенности на от около 20 до около 30% и согласно другой особенности на от около 25 до около 30%. Согласно другой особенности подача азота в любом количестве от около 100 до около 340 мг азота на грамм синтезируемых клеток обеспечивает среднюю проводимость около 16 мСм/см или менее и поддержание STY на уровне от около 10 г этанола/(л⋅сутки) до около 200 г этанола/(л⋅сутки). Согласно одной из более конкретных особенностей подача азота в количестве от около 190 до около 210 мг азота на грамм синтезируемых клеток обеспечивает среднюю проводимость около 4 до около 6,5 мСм/см, согласно другой особенности от около 5 до около 6 мСм/см и согласно другой особенности от около 4 до около 5 мСм/см. Согласно другой более конкретной особенности подача азота в количестве от около 190 до около 200 мг азота на грамм синтезируемых клеток обеспечивает среднюю проводимость около 4 до около 6,5 мСм/см, согласно другой особенности от около 5 до около 6 мСм/см и согласно другой особенности от около 4 до около 5 мСм/см. Согласно другой более конкретной особенности подача азота в количестве от около 190 до около 195 мг азота на грамм синтезируемых клеток обеспечивает среднюю проводимость около 4 до около 6.5 мСм/см, согласно другой особенности от около 5 до около 6 мСм/см и согласно другой особенности от около 4 до около 5 мСм/см. Согласно другой более конкретной особенности подача азота в количестве от около 195 до около 200 мг азота на грамм синтезируемых клеток обеспечивает среднюю проводимость около 4 до около 6,5 мСм/см, согласно другой особенности от около 5 до около 6 мСм/см и согласно другой особенности от около 4 до около 5 мСм/см.
Согласно одной из особенностей среда содержит по меньшей мере один или несколько источников азота, по меньшей мере один или несколько источников фосфора и по меньшей мере один или несколько источников калия. Среда может содержать любой из трех компонентов, любое их сочетание и согласно одной из важных особенностей содержит все три компонента. Источник фосфора может включать источник фосфора, выбранный из группы, включающей фосфорную кислоту, фосфат аммония, фосфат калия и их смеси. Источник калия может включать источник калия, выбранный из группы, включающей хлорид калия, фосфат калия, нитрат калия, сульфат калия и их смеси.
Согласно одной из особенностей среда содержит одно или несколько из следующего: железо, вольфрам, никель, кобальт, магний, серу и тиамин. Среда может содержать любой один из этих компонентов, любое их сочетание и согласно одной из важных особенностей содержит все эти компоненты. Источник железа может включать источник железа, выбранный из группы, включающей хлорид железа, сульфат железа и их смеси. Источник вольфрама может включать источник вольфрама, выбранный из группы, включающей вольфрамат натрия, вольфрамат кальция, вольфрамат калия и их смеси. Источник никеля может включать источник никеля, выбранный из группы, включающей хлорид никеля, сульфат никеля, нитрат никеля и их смеси. Источник кобальта может включать источник кобальта, выбранный из группы, включающей хлорид кобальта, фторид кобальта, бромид кобальта, йодид кобальта и их смеси. Источник магния может включать источник магния, выбранный из группы, включающей хлорид магния, сульфат магния, фосфат магния и их смеси. Источник серы может включать цистеин, сульфид натрия и их смеси. Далее приведены концентрации различных компонентов.
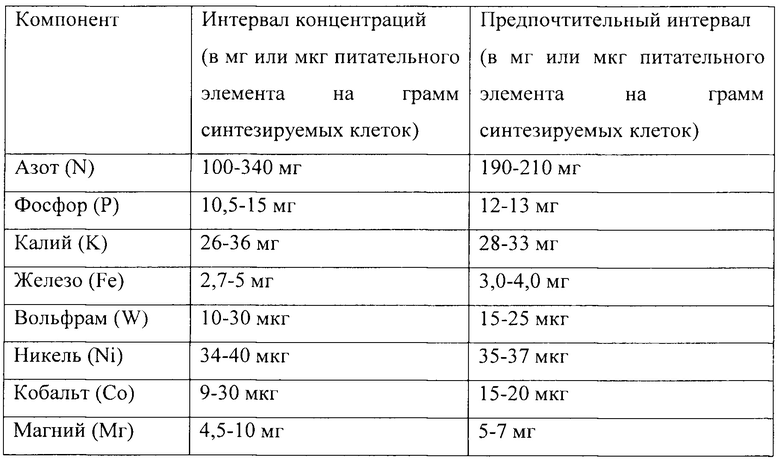

При осуществлении способа поддерживается рН на уровне от около 4,2 до около 4,8. Среда содержит менее около 0,01 г/л дрожжевого экстракта и менее около 0,01 г/л углеводов.
Биореактор
Согласно одной из особенностей ферментация начинается с добавления среды в реакционный сосуд. Стерилизуют среду, чтобы удалить нежелательные микроорганизмы, и засевают реактор желаемыми микроорганизмами. Согласно одной из особенностей используемые микроорганизмы включают ацетогенные бактерии. Примеры применимых ацетогенных бактерий включают бактерии рода Clostridium, такие как штаммы Clostridium ljungdahlii, включая штаммы, описанные в WO 2000/68407, ЕР 117309, патентах US 5173429, 5593886 и 6368819, WO 1998/00558 и WO 2002/08438, штаммы Clostridium autoethanogenum (DSM 10061 и DSM 19630, депонированные в DSMZ, Германия), включая штаммы, описанные в WO 2007/117157 и WO 2009/151342, Clostridium ragsdalei (P11, ATCC BAA-622) и Alkalibaculum bacchi (CP11, ATCC BAA-1772), включая штаммы, описанные, соответственно, в патенте US 7704723 и докладе "Biofuels and Bioproducts from Biomass-Generated Synthesis Gas", Hasan Atiyeh от 29 апреля 2010 г.на Ежегодной Конференции по экспериментальной программе содействия исследовательским проектам в штате Оклахома (Oklahoma EPSCoR Annual State Conference) и Clostridium carboxidivorans (ATCC PTA-7827), описанные в патентной заявке US 2007/0276447. Другие применимые микроорганизмы включают микроорганизмы рода Moorella, в том числе Moorella sp.HUC22-1, и микроорганизмы рода Carboxydothermus. Каждый из указанных документов в порядке ссылки включен в настоящую заявку. Могут использоваться смешанные культуры из двух или более микроорганизмов.
Некоторые примеры применимых бактерий включают Acetogenium kivui, Acetoanaerobium noterae, Acetobacterium woodii, Alkalibaculum bacchi CP11 (ATCC BAA-1772), Blautia producta, Butyribacterium methylotrophicum, Caldanaerobacter subterraneous, Caldanaerobacter subterraneous pacificus, Carboxydothermus hydrogenoformans, Clostridium aceticum, Clostridium acetobutylicum, Clostridium acetobutylicum P262 (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 10061, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 23693, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 24138, депонирована в DSMZ, Германия), Clostridium carboxidivorans P7 (ATCC PTA-7827), Clostridium coskatii (ATCC РТА-10522), Clostridium drakei, Clostridium ljungdahlii PETC (ATCC 49587), Clostridium ljungdahlii ERI2 (ATCC 55380), Clostridium ljungdahlii C-01 (ATCC 55988), Clostridium ljungdahlii O-52 (ATCC 55889), Clostridium magnum, Clostridium pasteurianum (DSM 525, депонирована в DSMZ, Германия), Clostridium ragsdali P11 (ATCC BAA-622), Clostridium scatologenes, Clostridium thermoaceticum, Clostridium ultunense, Desulfotomaculum kuznetsovii, Eubacterium limosum, Geobacter sulfurreducens, Methanosarcina acetivorans, Methanosarcina barkeri, Morrella thermoacetica, Morrella thermoautotrophica, Oxobacter pfennigii, Peptostreptococcus productus, Ruminococcus productus, Thermoanaerobacter kivui и их смеси.
После инокуляции устанавливают начальный расход подаваемого газа для обеспечения начальной популяции микроорганизмов. Анализируют выходящий газ с целью определения его содержания. Используют результаты анализа для регулирования расхода подаваемого газа. После достижения желаемых уровней удаляют из реактора жидкую фазу и клеточный материал и пополняют среду. Согласно этой особенности поддерживают в биореакторе плотность клеток по меньшей мере около 2 грамм/литр и согласно другой особенности от около 2 до около 50 грамм/литр, согласно различным другим особенностям от около 5 до около 40 грамм/литр, от около 5 до около 30 грамм/литр, от около 5 до около 20 грамм/литр, от около 5 до около 15 грамм/литр, от около 10 до около 40 грамм/литр, от около 10 до около 30 грамм/литр, от около 10 до около 20 грамм/литр, от около 15 до около 20 и от около 10 до около 15 грамм/литр. Плотность клеток может регулироваться посредством фильтра рециркуляции. Некоторые примеры биореакторов описаны в заявках US 61/571654 и 61/571565, поданных 30 июня 2011 г., заявке US 61/573845, поданной 13 сентября 2011 г., заявках US 13/471827 и 13/471858, поданных 15 мая 2012 г., и заявке US 13/473167, поданной 16 мая 2012 г., все из которых в порядке ссылки включены в настоящую заявку. Согласно одной из особенностей способ обеспечивает конверсию от около 5 до около 99% СО, согласно другой особенности конверсию от около 10 до около 90% СО, согласно другой особенности от около 20 до около 80%, согласно другой особенности от около 30 до около 70%, согласно другой особенности от около 40 до около 60%, согласно другой особенности от около 50 до около 95%, согласно другой особенности от около 60 до около 95%, согласно другой особенности от около 70 до около 95%, согласно другой особенности от около 80 до около 95% и согласно другой особенности от около 80 до около 90%.
Примеры
Пример 1
Использование NH4OH в качестве источника азота
Были проведены эксперименты в биореакторе (New Brunswick BioFlo I или IIc), который использовался как прямоточный CSTR без контура рециркуляции.
Использовали следующие условия эксплуатации биореактора:
тип культуры: Clostridium ljungdahlii С01,
поддерживаемая температура культуры: около 38°С,
скорость перемешивания: около 800 об/мин на цифровом индикаторе,
объем культуры: около 2450-2500 мл.
Установили значение рН культуры около 4,5-4,6. Использовали 5% раствор NaHCO3 Для регулирования рН.
В качестве газа использовали синтезированную смесь 15% Н2, 45% N2, 30% СО и 10% СО2, которую подавали в культуру со скоростью около 411 мл/мин.
Скорость подачи среды в реактор составляла около 1,3 мл/мин или около 1870 мл/сутки.
Время удержания жидкости и клеток составляло приблизительно 29-31 час. Довели культуры микроорганизмов до стабильного состояния в биореакторе. Исходным источником аммония являлся NH4Cl. После достижения стабильного состояния заменили источник аммония на NH4OH путем удаления хлорида аммония из исходной среды. Далее приведены компоненты среды и их концентрации.

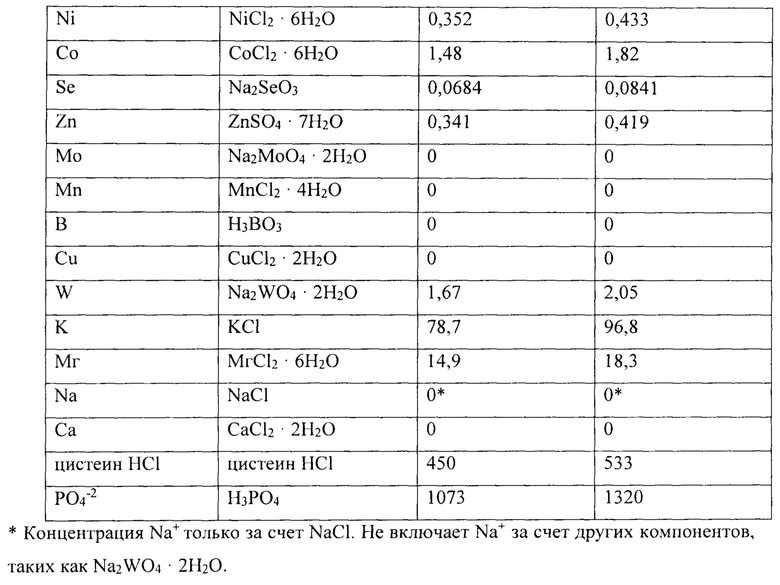
При замене источника аммония были выполнены следующие операции.
Снизили скорость подачи исходной среды с целью компенсации скорости подачи
среды с NH4OH и поддержания такого же потока жидкости, поступающего в систему.
Повысили процентные концентрации компонентов в исходной среде пропорционально снижению скорости подачи среды с целью поддержания такой же общей скорости подачи компонентов, несмотря на снижение концентрации в исходной среде.
Контролировали следующие параметры:
конверсию и потребление газа,
концентрацию продуктов,
плотность клеток,
рН культуры,
базовый уровень в резервуаре,
XRT/LRT.
Замена источника аммония на гидроокись аммония дала следующие результаты:
снижение средней проводимости примерно на 20%,
повышение концентрации этанола примерно на 18%,
повышение выхода этанола на 13% с 16,2 до 18,3 г/л⋅сутки,
повышение измеренной рН культуры до около 4,6%,
снижение усредненной скорости добавления основания примерно на 86%.
Сначала произошло повышение концентрации уксусной кислоты, после чего концентрация стабильно снижалась.
Замена источника аммония не привела к значительному заметному изменению потребления газа, конверсии газа, плотности клеток или концентрации бутанола. Были получены следующие результаты:

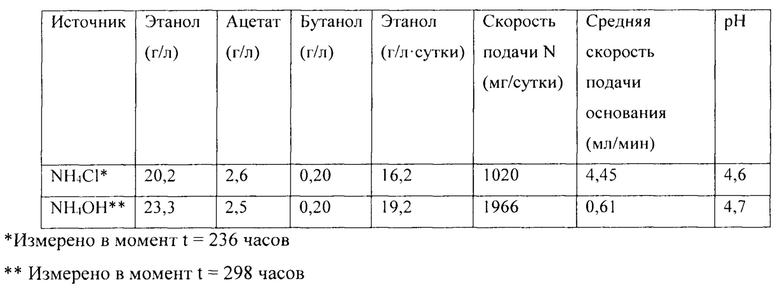
Хотя рассмотренное изобретение описано со ссылкой на конкретные варианты его осуществления, примеры и применения, специалисты в данной области техники могут внести в него множество модификаций и изменений, не выходящих за пределы его изобретения согласно формуле изобретения.
Группа изобретений относится к ферментации синтез-газа. Способ ферментации синтез-газа включает подачу синтез-газа, содержащего по меньшей мере 10 мол.% СО, в реакционный сосуд с ферментационной средой, обеспечение скорости подачи в реакционный сосуд азота в количестве около 100 мг или более азота на грамм ацетогенных клеток, содержащихся в ферментационной среде, и ферментацию синтез-газа. При этом азот обеспечивается гидроокисью аммония. Способ обеспечивает среднюю проводимость около 16 мСм/см или менее и выход продукта за один проход в единицу (STY) 10 г этанола/(л·сутки) или более. Предложен также вариант способа ферментации синтез-газа, включающий подачу синтез-газа, содержащего по меньшей мере 10 мол.% СО, в реакционный сосуд с ферментационной средой, введение синтез-газа в контакт с ацетогенными бактериями обеспечение скорости подачи в реакционный сосуд азота в количестве около 100 мг или более азота на грамм клеток, содержащихся в ферментационной среде, и ферментацию синтез-газа. При этом в качестве источника азота используют гидроокись аммония. Группа изобретений обеспечивает снижение проводимости среды примерно на 20% по сравнению со средой, где азот обеспечивается хлоридом аммония. 2 н. и 15 з.п. ф-лы, 3 табл., 1 пр.
1. Способ ферментации синтез-газа, включающий:
подачу синтез-газа в реакционный сосуд с ферментационной средой, где синтез-газ содержит по меньшей мере 10 мол.% СО,
обеспечение скорости подачи в реакционный сосуд азота в количестве около 100 мг или более азота на грамм клеток, содержащихся в ферментационной среде, где указанные клетки представляют собой ацетогенные бактерии, и где азот обеспечивается гидроокисью аммония; и
ферментацию синтез-газа,
при этом способ обеспечивает среднюю проводимость около 16 мСм/см или менее и выход продукта за один проход в единицу (STY) 10 г этанола/(л·сут) или более,
где способ обеспечивает снижение проводимости среды примерно на 20% по сравнению со средой, где азот обеспечивается хлоридом аммония.
2. Способ ферментации по п.1, в котором синтез-газ имеет соотношение СО/СО2 около 0,75 или более.
3. Способ ферментации по п.1, в котором ферментация включает введение синтез-газа в контакт с ацетогенными бактериями одного или нескольких видов.
4. Способ ферментации по п.3, в котором ацетогенные бактерии выбраны из группы, включающей Acetogenium kivui, Acetoanaerobium noterae, Acetobacterium woodii, Alkalibaculum bacchi CP11 (ATCC BAA-1772), Blautia producta, Butyribacterium methylotrophicum, Caldanaerobacter subterraneous, Caldanaerobacter subterraneous pacificus, Carboxydothermus hydrogenoformans, Clostridium aceticum, Clostridium acetobutylicum, Clostridium acetobutylicum P262 (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 10061, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 23693, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 24138, депонирована в DSMZ, Германия), Clostridium carboxidivorans P7 (ATCC PTA-7827), Clostridium coskatii (ATCC РТА-10522), Clostridium drakei, Clostridium ljungdahlii PETC (ATCC 49587), Clostridium ljungdahlii ERI2 (ATCC 55380), Clostridium ljungdahlii C-01 (ATCC 55988), Clostridium ljungdahlii O-52 (ATCC 55889), Clostridium magnum, Clostridium pasteurianum (DSM 525, депонирована в DSMZ, Германия), Clostridium ragsdali P11 (ATCC BAA-622), Clostridium scatologenes, Clostridium thermoaceticum, Clostridium ultunense, Desulfotomaculum kuznetsovii, Eubacterium limosum, Geobacter sulfurreducens, Methanosarcina acetivorans, Methanosarcina barkeri, Morrella thermoacetica, Morrella thermoautotrophica, Oxobacter pfennigii, Peptostreptococcus productus, Ruminococcus productus, Thermoanaerobacter kivui и их смеси.
5. Способ ферментации по п.1, обеспечивающий плотность клеток около 1,0 г/л или более.
6. Способ ферментации по п.1, обеспечивающий конверсию от около 5 до около 99% СО.
7. Способ ферментации по п.1, в котором ферментационная среда содержит около 0,01 г/л или менее дрожжевого экстракта.
8. Способ ферментации по п.1, в котором ферментационная среда содержит около 0,01 г/л или менее углеводов.
9. Способ ферментации синтез-газа, включающий:
подачу синтез-газа в реакционный сосуд с ферментационной средой, где синтез-газ содержит по меньшей мере 10 мол.% СО,
введение синтез-газа в контакт с ацетогенными бактериями,
обеспечение скорости подачи в реакционный сосуд азота в количестве около 100 мг или более азота на грамм клеток, содержащихся в ферментационной среде, где указанные клетки представляют собой ацетогенные бактерии и где азот обеспечивается гидроокисью аммония; и
ферментацию синтез-газа,
где способ обеспечивает снижение проводимости среды примерно на 20% по сравнению со средой, где азот обеспечивается хлоридом аммония.
10. Способ по п.9, обеспечивающий среднюю проводимость около 16 мСм/см или менее.
11. Способ по п.10, обеспечивающий STY около 10 г этанола/(л·сут) или более.
12. Способ ферментации по п.9, в котором синтез-газ имеет соотношение СО/СО2 около 0,75 или более.
13. Способ ферментации по п.9, в котором ацетогенные бактерии выбраны из группы, включающей Acetogenium kivui, Acetoanaerobium noterae, Acetobacterium woodii, Alkalibaculum bacchi CP11 (ATCC BAA-1772), Blautia producta, Butyribacterium methylotrophicum, Caldanaerobacter subterraneous, Caldanaerobacter subterraneous pacificus, Carboxydothermus hydrogenoformans, Clostridium aceticum, Clostridium acetobutylicum, Clostridium acetobutylicum P262 (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 19630, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 10061, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 23693, депонирована в DSMZ, Германия), Clostridium autoethanogenum (DSM 24138, депонирована в DSMZ, Германия), Clostridium carboxidivorans P7 (ATCC PTA-7827), Clostridium coskatii (ATCC РТА-10522), Clostridium drakei, Clostridium ljungdahlii PETC (ATCC 49587), Clostridium ljungdahlii ERI2 (ATCC 55380), Clostridium ljungdahlii C-01 (ATCC 55988), Clostridium ljungdahlii O-52 (ATCC 55889), Clostridium magnum, Clostridium pasteurianum (DSM 525, депонирована в DSMZ, Германия), Clostridium ragsdali P11 (ATCC BAA-622), Clostridium scatologenes, Clostridium thermoaceticum, Clostridium ultunense, Desulfotomaculum kuznetsovii, Eubacterium limosum, Geobacter sulfurreducens, Methanosarcina acetivorans, Methanosarcina barkeri, Morrella thermoacetica, Morrella thermoautotrophica, Oxobacter pfennigii, Peptostreptococcus productus, Ruminococcus productus, Thermoanaerobacter kivui и их смеси.
14. Способ ферментации по п.9, обеспечивающий плотность клеток около 1,0 г/л или более.
15. Способ ферментации по п.9, обеспечивающий конверсию от около 5 до около 99% СО.
16. Способ ферментации по п.9, в котором ферментационная среда содержит около 0,01 г/л или менее дрожжевого экстракта.
17. Способ ферментации по п.9, в котором ферментационная среда содержит около 0,01 г/л или менее углеводов.
| WO 2002008438 A2, 31.01.2002 | |||
| WO 2007117157 A1, 18.10.2007 | |||
| СПОСОБ ПРЕОБРАЗОВАНИЯ ГАЗООБРАЗНОГО УГЛЕВОДОРОДНОГО СЫРЬЯ В ЖИДКОЕ ТОПЛИВО | 2009 |
|
RU2418070C2 |
| YOUNESI H | |||
| ET AL | |||
| Ethanol and acetate production from synthesis gas via fermentation processes using anaerobic bacterium, Clostridium ljungdahlii // Biochemical Engineering Journal, 2005, 27, pp | |||
| Прибор, автоматически записывающий пройденный путь | 1920 |
|
SU110A1 |
Авторы
Даты
2017-06-22—Публикация
2013-05-15—Подача