Настоящее изобретение относится к способу получения раствора человеческого альбумина, в частности, изобретение относится к способу, включающему стадию снижения уровня растворенного кислорода в указанном растворе альбумина до концентрации, равной или меньшей чем 0,5 м.д. С помощью способа в соответствии с настоящим изобретением можно получить раствор человеческого альбумина с состоянием окисления/восстановления, близким состоянию окисления/восстановления альбумина, присутствующего в плазме крови человека.
Человеческий альбумин является негликозилированным белком с молекулярной массой 66 кДа. Количественно он представляет собой наиболее значимый белок плазмы, и его концентрация в нормальной плазме находится между 35 и 50 г/л, что составляет до 60% от общего белка плазмы (Peters Т.J.: All About Albumin; Biochemistry, Genetics and Medical Applications. Academic Press, San Diego, 1996).
Структура человеческого альбумина состоит из полипептида, имеющего 585 аминокислот, при этом приблизительно 67% молекул находятся в форме альфа-спиралей, в то время как бета-листы отсутствуют (Otagiri M., Chuang V.T.: Pharmaceutically important pre - and posttranslational modifications on human serum albumin. Biol Pharm Bull 2009; 32:527-534). Человеческий альбумин содержит 6 остатков метионина и 35 остатков цистеина, участвующих в образовании 17 дисульфидных связей. Cys-34 является единственным свободным остатком цистеина во всей молекуле. Человеческий альбумин обладает специфическими антиоксидантными функциями в силу способности связываться с множественными лигандами и свойством захватывать радикалы, причем оба свойства тесно связаны с его структурой.
Хотя существует много возможностей окисления альбумина, Cys-34 является областью, особенно чувствительной к окислению/восстановлению. Следовательно, в общем случае вполне закономерно говорить о состоянии окисления/восстановления альбумина с точки зрения Cys-34. При хроматографическом разделении альбумина образуются три фракции, согласно состоянию окисления/восстановления Cys-34 (Peters, 1996, op. cit.):
(i) восстановленная форма, в которой цистеин находится в виде свободной тиоловой группы, называемая человеческим меркаптальбумином (НМА);
(ii) окисленная форма, в которой цистеин образует дисульфидную связь с небольшим тиоловым соединением, главным образом цистеином или цистеинилглицином, хотя также и с гомоцистеином и глутатионом, называемая человеческим безмеркаптальбумином-1(HNA1); и
(iii) наиболее окисленная форма, в которой цистеин находится в форме сульфиновой или сульфоновой кислоты, называемая человеческим безмеркаптальбумином-2 (HNA2).
У здорового человека приблизительно 50-69% общего альбумина находится в форме НМА, 27-42% находится в форме HNA1 и 3-5% находится в форме HNA2 (Oettl K., et al. Oxidative damage of albumin in advanced liver disease. Biochim. Biophys. Acta 2008; 1782: 469-473; Oettl K. and Marsche G. Redox State of human serum albumin in terms of cysteine-34 in health and disease. Methods Enzymol. 2010; 474:181-95; and Oettl K. et al. Oxidative albumin damage in chronic liver failure: Relation to albumin binding capacity; liver dysfunction and survival. J Hepatol, 2013, 59:978-983). В целом считается, что окисление НМА до HNA1 является обратимым, тогда как окисление до HNA2 представляет собой необратимый процесс.
Альбумин может подвергаться различным структурным модификациям как in vivo, так и в ходе применения способов, задействованных в производстве терапевтического альбумина, что приводит к изменению его конформации и, как следствие, его связывающих свойств, а также состояния окисления/восстановления (Oettl, K. et al, 2010, op. cit.).
Широко используемым способом фракционирования плазмы человека для получения очищенных белков, среди которых находится и альбумин, является способ Кона (Cohn E.J. et al. 'Preparation and properties of serum plasma proteins, IV. A system for the separation into fractions of the protein and lipoprotein components of biological tissues and fluids. J. Am. Chem. Soc. (1946) 68, 459-475) или его незначительные модификации.
При способе Кона плазму человека сначала подвергают последовательным стадиям осаждения и разделения. На каждой стадии получают осадок, обогащенный одним из белков плазмы, и декантированный супернатант. Для достижения осаждения последовательных фракций по Кону (фракция I, фракции II+III, фракция IV и фракция V) необходимо изменить параметры раствора, например, в числе прочего, рН, диэлектрическую постоянную, температуру, концентрацию белка и ионную силу, с целью изменения растворимости различных белков. Дополнительно следует отметить, что указанные фракции по Кону содержат возрастающие концентрации этанола. Как следствие, альбумин, содержащийся в супернатанте фракции IV, осаждается примерно 40% (объем/объем) этанолом и продолжает образовывать часть осадка фракции V.
После получения фракции V ее ресуспендируют в растворе и подвергают различным стадиям до получения конечного продукта. Обычно эти стадии включают: диафильтрацию, термообработку, стерилизацию, разлив во флаконы и окончательную пастеризацию в указанных флаконах, а затем передачу указанных флаконов на карантин, обычно составляющий не менее чем 14 дней при 30-32°С, с целью обеспечения стерильности конечного продукта.
Авторы настоящего изобретения обнаружили, что в процессе получения раствора альбумина из плазмы человека происходят изменения состояния окисления/восстановления Cys-34 альбумина. Эти модификации происходят в основном при хранении в присутствии кислорода, в силу чего они обнаруживаются главным образом после стадии карантина. На примере нескольких производственных партий (n=7) было установлено, что уровни HMA, HNA1 и HNA2 составляют 40-53%, 39-44% и 7-16% (масса/объем), соответственно, и, как следствие, преимущественно уровни HMA и HNA2 отличаются от уровней, описанных у здоровых людей (Oettl K. 2008, 2010 and 2013, ops. cit.). Это может быть очень важным, например, в случае HNA2, в силу того, что окисление до HNA2 представляет собой необратимый процесс, как указано выше.
Неожиданно авторы изобретения обнаружили, что посредством добавления в процесс производства раствора человеческого альбумина стадии, включающей снижение уровня растворенного кислорода в растворе до концентрации равной или меньшей чем 0,5 м.д., достигалось снижение окисления Cys-34, и полученное состояние окисления/восстановления альбумина очень сходно с состоянием окисления/восстановления альбумина, присутствующего в плазме крови. Это приводит к тому, что полученный альбумин обладает свойствами, например, антиоксидантными свойствами, более сходными со свойствами альбумина в крови, что может способствовать улучшению его терапевтической эффективности во многих вариантах применения.
Соответственно, в настоящем изобретении выявлен способ получения раствора человеческого альбумина, отличающийся тем, что он включает стадию снижения уровня растворенного кислорода в указанном растворе альбумина, причем уровень кислорода снижается до концентрации, равной или меньшей чем 0,5 м.д. Предпочтительно, после стадии снижения уровня растворенного кислорода в растворе альбумина, указанный раствор альбумина выдерживают в атмосфере инертного газа.
Указанную стадию снижения уровня растворенного кислорода в растворе альбумина можно осуществить различными способами, известными в данной области техники. Предпочтительно можно осуществлять обработку поверхности раствора альбумина инертным газом или ь пропускать пузырьки инертного газа через слой указанного раствора альбумина. Указанный инертный газ, используемый в способе согласно настоящему изобретению, может быть азотом, гелием или аналогичным газом.
Способ согласно настоящему изобретению можно применить для получения растворов альбумина с концентрацией альбумина между приблизительно 4 и 25% (масса/объем). Предпочтительно полученный альбумин представляет собой терапевтический альбумин.
Кроме того, альбумин согласно настоящему изобретению может представлять собой альбумин, полученный в рекомбинантной или трансгенной форме. Молекула рекомбинантного или трансгенного альбумина идентична человеческому альбумину с точки зрения аминокислотной последовательности, она не подвергается гликозилированию и, при необходимости сохранения функциональности, она должна находиться в такой же конформации, как и альбумин, имеющий человеческое плазматическое происхождение. В случае если это не так, он не может быть введен человеку из-за риска иммуногенности, помимо других возможных неблагоприятных последствий, вызванных указанными различиями.
Стадию снижения уровня растворенного кислорода в растворе альбумина, согласно настоящему изобретению, можно осуществлять до или после стадии пастеризации указанного раствора альбумина, или, более того, ее можно осуществлять без осуществления стадии пастеризации указанного раствора альбумина, независимо от способа получения исходного раствора альбумина.
Для получения лучших результатов с точки зрения состояния окисления/восстановления Cys-34 в растворе альбумина, полученного посредством способа согласно настоящему изобретению, предпочтительно, после стадии снижения уровня растворенного кислорода в растворе альбумина, указанный раствор альбумина выдерживают в атмосфере инертного газа. Указанная атмосфера инертного газа может представлять собой азот, гелий или аналогичные газы.
Хотя можно применять любую емкость, в которую упакован и/или в которой хранят альбумин, полученный посредством способа согласно настоящему изобретению, в предпочтительном случае указанная емкость должна быть изготовлена из материала, непроницаемого для кислорода, более предпочтительно из стекла.
Еще одна цель настоящего изобретения заключается в выявлении композиции, содержащей человеческий альбумин, полученный посредством способа согласно настоящему изобретению, и в ее применении в качестве медикамента.
Наконец, в настоящем изобретении показано применение композиции, содержащей альбумин, полученный в соответствии с вышеописанным способом, для получения медикамента.
Настоящее изобретение подробно описано ниже в отношении примеров и сравнительных примеров, не содержащих ограничений изобретения. Кроме того, даны ссылки на фигуры, где:
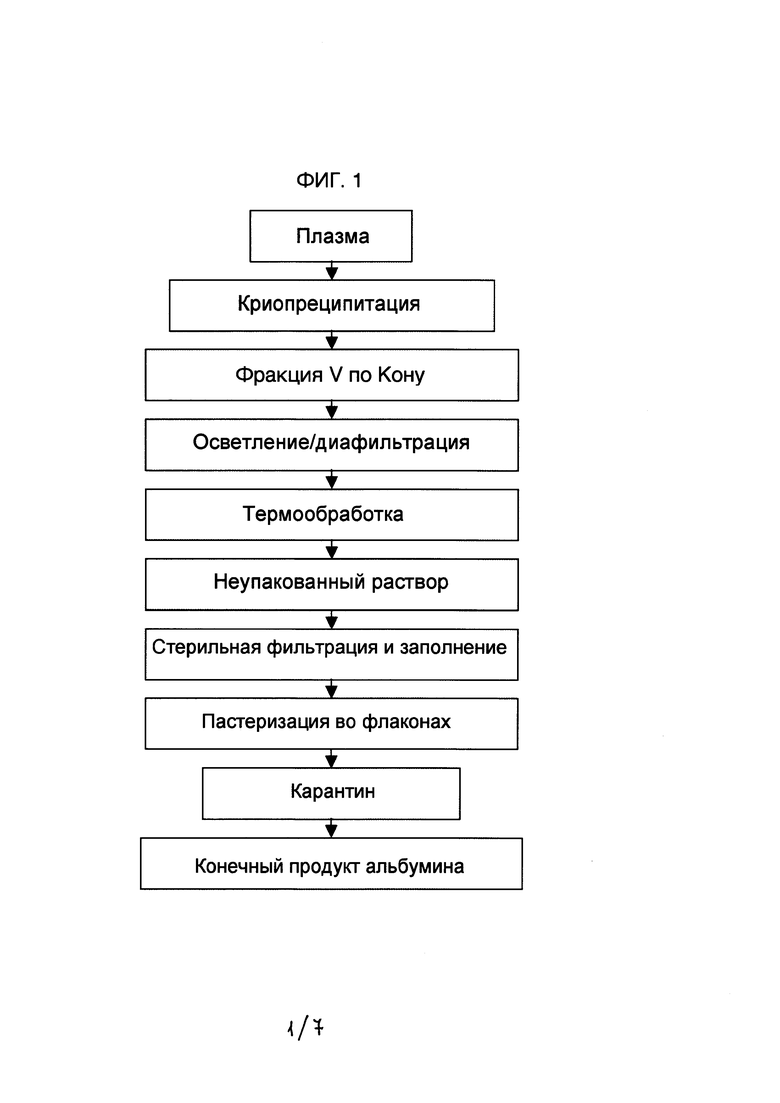
- На Фигуре 1 показана схема способа получения терапевтического человеческого альбумина из плазмы, использовавшегося в предшествующем уровне техники.
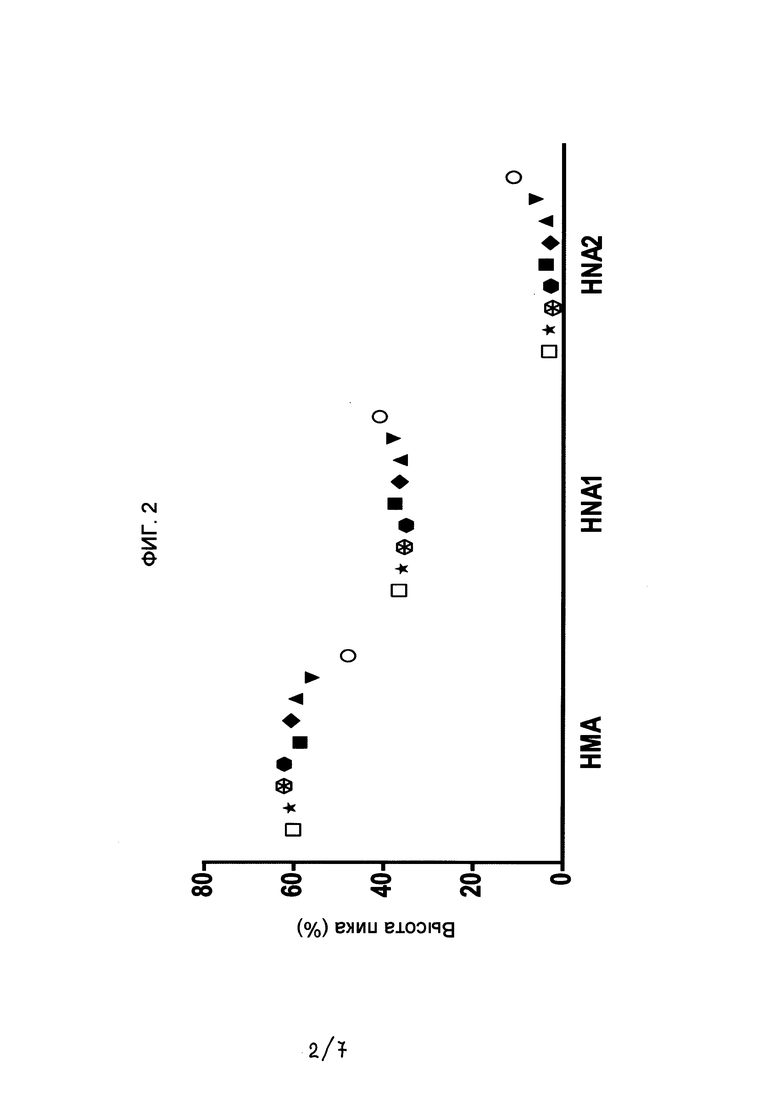
- На Фигуре 2 показан график концентрации форм Cys-34 альбумина НМА, HNA1 и HNA2, выраженных в виде высоты пиков, полученных с помощью хроматографии на различных стадиях способа, использовавшегося в предшествующем уровне техники до настоящего изобретения:  плазма здоровых доноров (n=59);
плазма здоровых доноров (n=59);  супернатант после криопреципитации (n=3);
супернатант после криопреципитации (n=3);  раствор альбумина до добавления стабилизаторов и до термообработки (n=3);
раствор альбумина до добавления стабилизаторов и до термообработки (n=3);  раствор альбумина со стабилизаторами до термообработки (n=1);
раствор альбумина со стабилизаторами до термообработки (n=1);  раствор альбумина со стабилизаторами после термообработки (n=1);
раствор альбумина со стабилизаторами после термообработки (n=1);  20% раствор альбумина перед стерильной фильтрацией (n=3);
20% раствор альбумина перед стерильной фильтрацией (n=3);  стерильный 20% раствор альбумина в конечной емкости (n=4);
стерильный 20% раствор альбумина в конечной емкости (n=4);  пастеризованный 20% раствор альбумина в конечной емкости до карантина (n=4); и
пастеризованный 20% раствор альбумина в конечной емкости до карантина (n=4); и  конечный продукт 20% альбумина (n=7); где n представляет собой количество проанализированных партий.
конечный продукт 20% альбумина (n=7); где n представляет собой количество проанализированных партий.
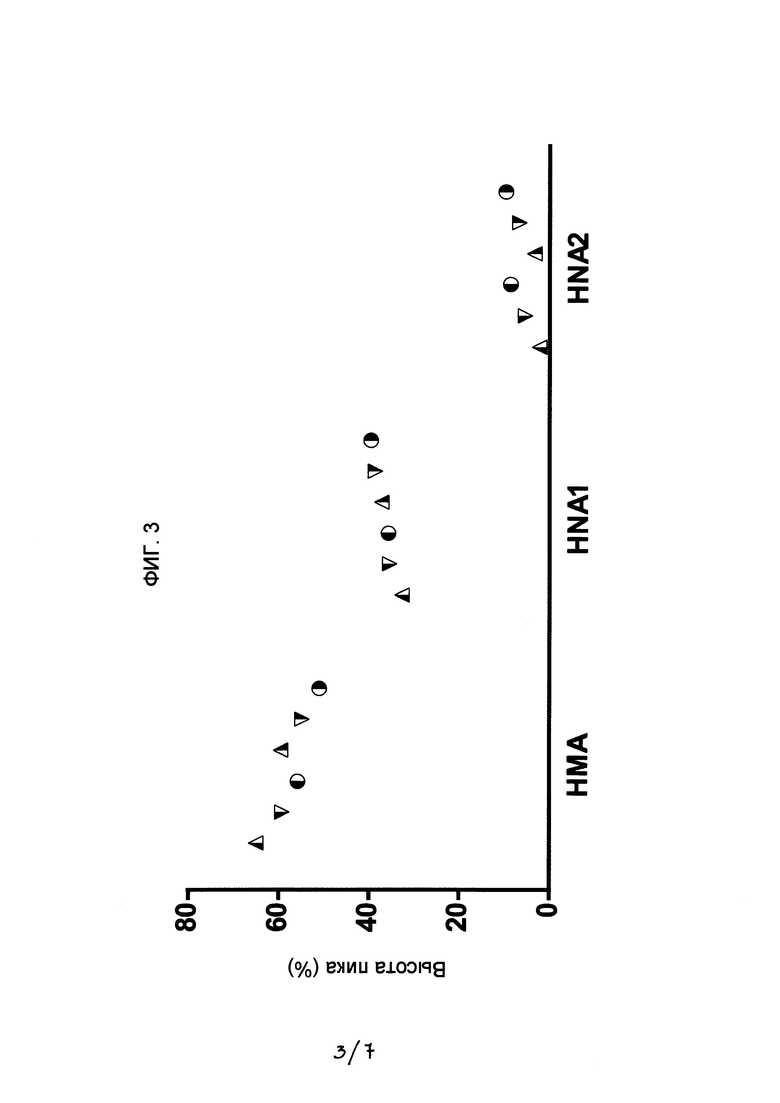
- На Фигуре 3 показан график концентрации форм Cys-34 альбумина (НМА, HNA1 и HNA2), выраженных в виде высоты пиков, полученных с помощью хроматографии на различных стадиях способа, использовавшегося в предшествующем уровне техники до настоящего изобретения:  стерильный 25% раствор альбумина в конечной емкости (n=1);
стерильный 25% раствор альбумина в конечной емкости (n=1);  пастеризованный 25% раствор альбумина до карантина (n=1); и
пастеризованный 25% раствор альбумина до карантина (n=1); и  конечный продукт 25% альбумина (n=1);
конечный продукт 25% альбумина (n=1);  стерильный 5% раствор альбумина в конечной емкости (n=1);
стерильный 5% раствор альбумина в конечной емкости (n=1);  пастеризованный 5% раствор альбумина в конечной емкости до карантина (n=1); и
пастеризованный 5% раствор альбумина в конечной емкости до карантина (n=1); и  конечный продукт 5% альбумина (n=1); где n представляет собой количество проанализированных партий.
конечный продукт 5% альбумина (n=1); где n представляет собой количество проанализированных партий.
- На Фигуре 4 показан график концентрации форм Cys-34 альбумина (НМА, HNA1 и HNA2), выраженных в виде высоты пиков, полученных с помощью хроматографии на различных стадиях с применением способа согласно настоящему изобретению, где применяли стадию обработки поверхности раствора газообразным азотом до пастеризации:  стерильный 20% раствор альбумина в конечной емкости (n=3);
стерильный 20% раствор альбумина в конечной емкости (n=3);  пастеризованный 20% раствор альбумина в конечной емкости до карантина (n=3); и
пастеризованный 20% раствор альбумина в конечной емкости до карантина (n=3); и  конечный продукт 20% альбумина (n=3); где n представляет собой количество проанализированных партий.
конечный продукт 20% альбумина (n=3); где n представляет собой количество проанализированных партий.
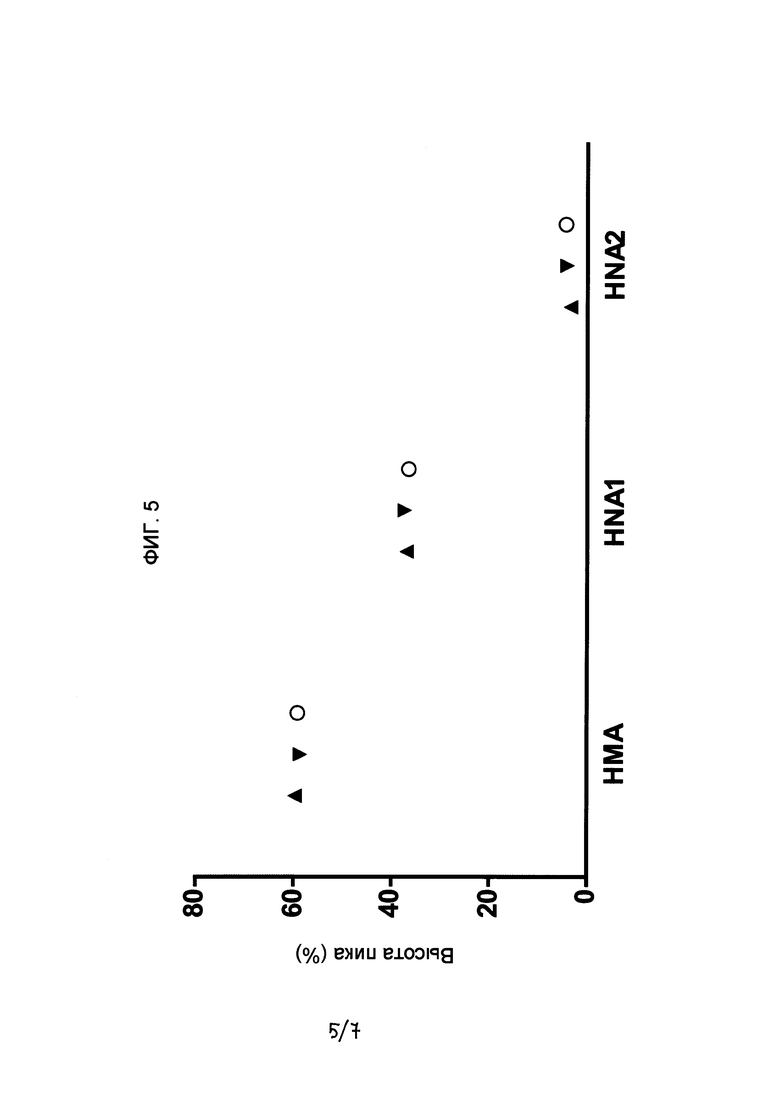
- На Фигуре 5 показан график концентрации форм Cys-34 альбумина (НМА, HNA1 и HNA2), выраженных в виде высоты пиков, полученных с помощью хроматографии на различных стадиях с применением способа согласно настоящему изобретению, где применяли стадию обработки путем пропускания пузырьков газообразного азота через раствор альбумина до пастеризации:  стерильный 20% раствор альбумина в конечной емкости (n=3);
стерильный 20% раствор альбумина в конечной емкости (n=3);  пастеризованный 20% раствор альбумина в конечной емкости до карантина (n=3); и
пастеризованный 20% раствор альбумина в конечной емкости до карантина (n=3); и  конечный продукт 20% альбумина (n=3); где n представляет собой количество проанализированных партий.
конечный продукт 20% альбумина (n=3); где n представляет собой количество проанализированных партий.
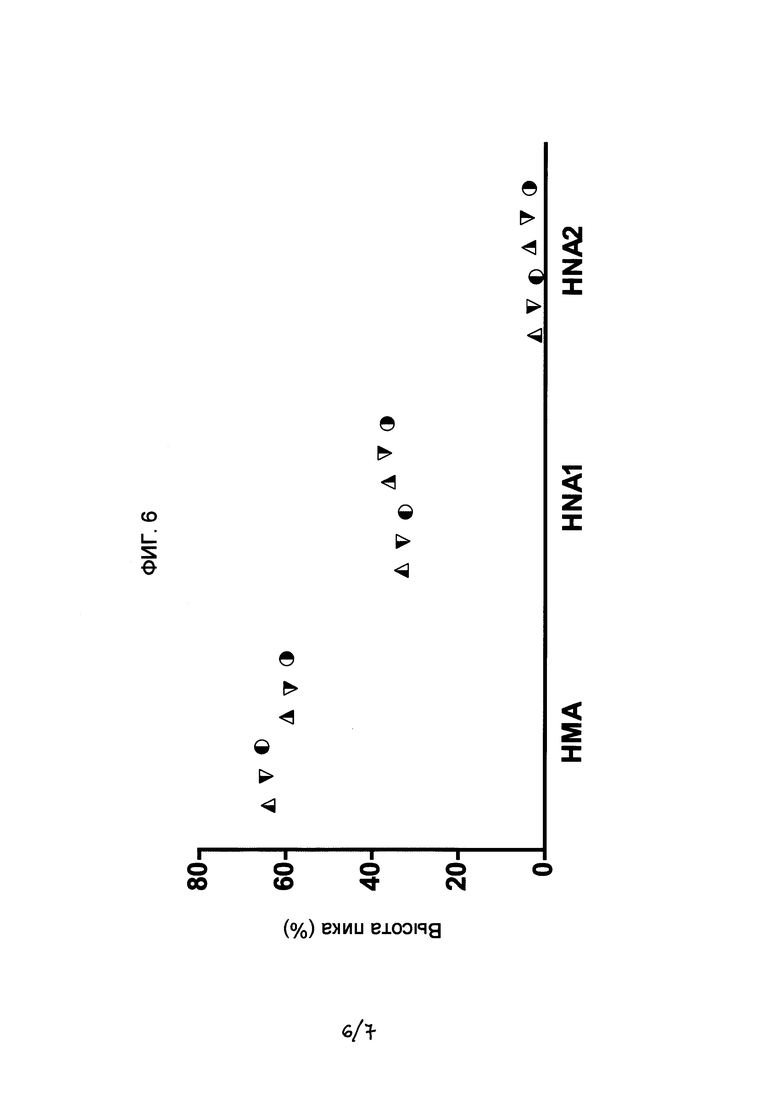
- На Фигуре 6 показан график концентрации форм Cys-34 альбумина (НМА, HNA1 и HNA2), выраженных в виде высоты пиков, полученных с помощью хроматографии на различных стадиях с применением способа согласно настоящему изобретению, где применяли стадию обработки поверхности раствора газообразным азотом до пастеризации:  стерильный неупакованный 25% раствор альбумина (n=1);
стерильный неупакованный 25% раствор альбумина (n=1);  пастеризованный 25% раствор альбумина до карантина (n=1); и
пастеризованный 25% раствор альбумина до карантина (n=1); и  конечный продукт 25% альбумина (n=1);
конечный продукт 25% альбумина (n=1);  стерильный 5% раствор альбумина в конечной емкости (n=1);
стерильный 5% раствор альбумина в конечной емкости (n=1);  пастеризованный 5% раствор альбумина в конечной емкости до карантина (n=1); и
пастеризованный 5% раствор альбумина в конечной емкости до карантина (n=1); и  конечный продукт 5% альбумина (n=1); где n представляет собой количество проанализированных партий.
конечный продукт 5% альбумина (n=1); где n представляет собой количество проанализированных партий.
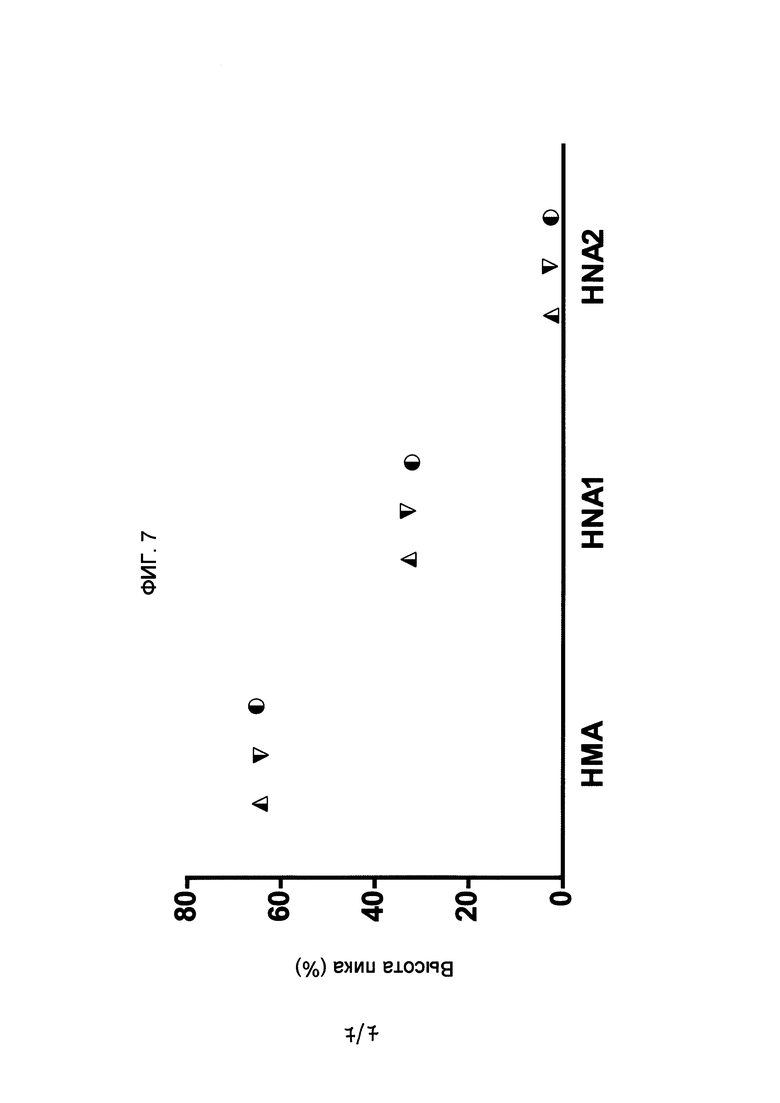
- На Фигуре 7 показан график концентрации форм Cys-34 альбумина (НМА, HNA1 и HNA2), выраженных в виде высоты пиков, полученных с помощью хроматографии на различных стадиях с применением способа согласно настоящему изобретению, где применяли стадию обработки поверхности раствора альбумина газообразным гелием до пастеризации:  стерильный 25% раствор альбумина в конечной емкости (n=1);
стерильный 25% раствор альбумина в конечной емкости (n=1);  пастеризованный 25% раствор альбумина в конечной емкости до карантина (n=1); и
пастеризованный 25% раствор альбумина в конечной емкости до карантина (n=1); и  конечный продукт 25% альбумина; где n представляет собой количество проанализированных партий.
конечный продукт 25% альбумина; где n представляет собой количество проанализированных партий.
ПРИМЕРЫ
Пример 1: Способ получения альбумина, ранее использовавшийся в данной области техники
Плазму человека, полученную от здоровых доноров, подвергали последовательным стадиям осаждения и разделения в соответствии со способом Кона (Cohn E.J. et al, 1946, op. cit.), начиная со стадии получения супернатанта после начальной криопреципитации и до получения осадка фракции V (см. фигуру 1). Фракцию V по Кону суспендировали в холодной воде для инъекций (WFI), доводили рН до 7,0 и осветляли с помощью погружаемых фильтров. Осветленный раствор подвергали диафильтрации при постоянном объеме, применяя диализный раствор, образованный солями одновалентных ионов (хлоридом натрия) и поддерживая температуру при 5°С (фигура 1, стадия осветления/диафильтрации). К раствору, полученному в результате диафильтрации, добавляли каприлат натрия и N-ацетилтриптофан в качестве стабилизаторов. Указанный раствор подвергали термообработке при 60°С (фигура 1, стадия термообработки). Затем раствор после термообработки разбавляли WFI или концентрировали в зависимости от желательной конечной концентрации белка (например, 5%, 20% или 25% (масса/объем)) (фигура 1, неупакованный раствор). Затем конечный раствор фильтровали в стерильных условиях (0,22 мкм-фильтры) и проводили заполнение конечных стерильных емкостей в асептической зоне (фигура 1, стадия стерильной фильтрации и заполнения). Раствор в конечной емкости нагревали при 60°С в течение не меньше чем 10 ч (фигура 1, стадия пастеризации во флаконах). Наконец, флаконы инкубировали при 30-32°С в течение не меньше чем 14 дней (фигура 1, стадия карантина). После указанного периода флаконы визуально осматривали, отсеивая любые признаки микробного заражения (фигура 1, конечный продукт альбумина).
Окислительное состояние образцов альбумина на различных стадиях процесса получения альбумина (фигура 2) анализировали с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) на основе способа, описанного Oettl K., 2010, op. cit., как подробно описано ниже.
Исследуемые образцы альбумина разбавляли 0,3 M буфером, хлоридом натрия, 0,1 M фосфатом натрия, рН 6,87, до концентрации 6,5 мг/мл, и 5 мкл вводили в анионообменную колонку Shodex Asahipak ES-502N с ДЭАЭ (7,5×100 мм, Shodex, Япония) при скорости потока 1,0 мл/мин. Разделение образцов альбумина на три фракции (НМА, HNA1 и HNA2), согласно окислительному состоянию, достигалось после проведения их элюирования градиентом 50 мМ ацетата натрия и 400 мМ сульфата натрия при рН 4,85 вплоть до достижения 6% концентрации этанола при постоянной скорости потока 1,0 мл/мин при температуре 35°С.
Первые 5 минут элюирования проводили в отсутствие этанола. Затем концентрацию этанола линейно увеличивали до 6% с 5 до 35 минуты, а затем поддерживали ее на постоянном уровне в течение следующих 5 минут. Наконец, с 40 до 45 минуты концентрацию этанола снова снижали до 0%. После еще 5-и минут элюирования без этанола можно было анализировать следующий образец.
Обнаружение трех фракций альбумина, в зависимости от их окислительного состояния, проводили с помощью флюоресценции, используя длину волны возбуждения и излучения 280 и 340 - нм, соответственно. Количественное определение концентрации НМА-, HNA1- и HNA2-форм Cys-34 альбумина осуществляли с учетом высоты каждого из исследуемых пиков, полученных на соответствующей хроматограмме.
На фигуре 2 показано изменение окислительного состояния образцов сывороточного человеческого альбумина на разных стадиях процесса получения альбумина, ранее применявшегося в данной области техники. Данные демонстрируют рост уровня HNA1- и HNA2-форм за счет снижения уровня НМА-формы, особенно после стадии пастеризации с последующим карантином (конечный продукт 20% альбумина). Поведение окислительного состояния альбумина после стадий пастеризации и карантина очищенных препаратов с 5% и 25% концентрацией альбумина, полученного из плазмы человека посредством способа, ранее применявшегося в данной области техники (фигура 3), эквивалентно поведению, наблюдаемому для конечных продуктов 20% альбумина после применения аналогичной методики (фигура 2). Полученные данные на обеих фигурах демонстрируют рост уровня HNA1- и HNA2-форм за счет снижения уровня НМА-формы, особенно после стадии пастеризации с последующим карантином.
Пример 2: Способ получения альбумина согласно настоящему изобретению с применением стадии обработки поверхности азотом до пастеризации
Способ получения альбумина согласно настоящему изобретению соответствует способу, описанному в примере 1, но дополнительно включает стадию снижения уровня растворенного кислорода в растворе альбумина, как описано ниже.
После получения стерильного раствора в конечной емкости (фигура 1, стадии стерильной фильтрации и заполнения) с целью вытеснения кислорода, присутствующего в содержимом емкости, осуществляли обработку поверхности азотом, вставляя в хлорбутиловую пробку флакона две иглы для подкожных инъекций (серийного типа Braun Sterican 21G×1½'', 0,80×40 мм, Германия, или аналогичные), подключенные к двум 0,22-мкм ПВДФ-фильтрам (серийного типа Millex GV Millipore, 0,22 мкм, ПВДФ, 13-мм фильтр, США, или аналогичным), избегая контакта игл с раствором альбумина. Одна из игл была предназначена для впуска газообразного азота, а другая для его выпуска с целью предотвращения избыточного давления в емкости. Обработку поверхности азотом осуществляли при комнатной температуре в течение двух часов, поддерживая постоянную скорость потока азота с целью наблюдения движения жидкости в емкости без ее разбрызгивания.
После завершения обработки поверхности азотом продолжали осуществлять способ получения альбумина из плазмы человека, как описано в примере 1 (фигура 1, стадия пастеризации во флаконах), до получения конечного продукта альбумина. Как и в примере 1, окислительное состояние образцов с концентрацией 20%, полученных посредством методики согласно настоящему изобретению, анализировали с помощью анионообменной хроматографии. В частности, анализировали образцы альбумина, подвергавшиеся стадии обработки поверхности азотом до пастеризации, образцы альбумина после пастеризации и до карантина и образцы альбумина после периода карантина. На фигуре 4 показаны полученные результаты, на которых наблюдалось отсутствие снижения уровня НМА-формы и отсутствие увеличения уровня HNA1- и HNA2-форм, наблюдавшихся на фигурах 2 и 3 при использовании применявшегося в предшествующем уровне техники способа получения альбумина.
Помимо анализа окислительного состояния выполняли измерение растворенного кислорода, присутствующего в образцах после обработки поверхности азотом; в результате во всех случаях концентрация растворенного кислорода была равной или меньше чем 0,5 м.д.
Определение проводили при комнатной температуре с использованием датчика измерения растворенного кислорода (многопараметрический измерительный прибор серийного типа HI 9828 Multiparameter Meter, Hanna Instruments, США). В частности, емкость с раствором альбумина, ранее подвергавшегося поверхностной обработке азотом, открывали в кабине с атмосферой азота и немедленно погружали в раствор датчик измерения кислорода в образце. Применяемый датчик, функционирование которого было основано на принципе гальванического элемента, включал серебряный (Ag) анод с оплеткой из платиновой (Pt) проволоки, действующей в качестве катода. Вышеописанный агрегат вставляли в защитный кожух, заполненный электролитическим раствором хлорида калия и закрытый на конце мембраной из Teflon®, газопроницаемого материала, обеспечивающего проникновение кислорода, присутствующего в растворе, но не самого раствора. При подаче потенциала 790 мВ кислород, присутствующий в ячейке, восстанавливался до гидроксид-ионов (ОН-) на катоде, а хлорид серебра осаждался на аноде. Указанная реакция приводила к возникновению тока с силой, пропорциональной количеству кислорода, присутствующего в образце. Затем измерительный прибор преобразовывал измеряемый ток в соответствующую концентрацию растворенного кислорода.
Пример 3: Способ получения альбумина согласно настоящему изобретению с применением стадии пропускания пузырьков азота через раствор до пастеризации
Способ получения альбумина согласно настоящему изобретению соответствует способу, описанному в примере 1, но включает стадию, описанную ниже. После получения стерильного раствора в конечной емкости (фигура 1, стадии стерильной фильтрации и заполнения) с целью вытеснения кислорода, присутствующего в содержимом емкости, осуществляли обработку путем пропускания пузырьков азота, вставляя в хлорбутиловую пробку флакона две иглы для подкожных инъекций (серийного типа Braun Sterican 21G×1½'', 0,80×40 мм, Германия, или аналогичные), подключенные к двум 0,22-мкм ПВДФ-фильтрам (серийного типа Millex GV Millipore, 0,22 мкм, ПВДФ, 13-мм фильтр, США, или аналогичным). Иглу, предназначенную для впуска газообразного азота (иглу для спинальной инъекции серийного типа Terumo Spinal Needle, 18G×3½'', 1,20×90 мм, Япония, или аналогичную), погружали в раствор альбумина, а игла для подкожной инъекции (серийного типа Braun Sterican 21G×1½'', 0,80×40 мм, Германия, или аналогичная), размещенная так, чтобы не контактировать с жидкостью, была предназначена для выхода газа с целью предотвращения избыточного давления в емкости. Обработку путем пропускания пузырьков азота осуществляли при комнатной температуре в течение двух часов, поддерживая постоянную скорость потока азота с целью возможности наблюдения небольших пузырьков в жидкости.
После завершения обработки путем пропускания пузырьков азота продолжали осуществлять способ получения альбумина из плазмы человека, как описано в примере 1 (фигура 1, стадия пастеризации во флаконах), до получения конечного продукта альбумина.
Как и в примерах 1 и 2, окислительное состояние образцов с 20% концентрацией альбумина, полученных посредством методики согласно настоящему изобретению, анализировали с помощью анионообменной хроматографии. В частности, анализировали образцы альбумина, подвергавшиеся стадии пропускания пузырьков азота до стадии пастеризации, образцы альбумина после пастеризации и до карантина и образцы альбумина после периода карантина. На фигуре 5 показаны полученные результаты, аналогичные результатам, отображенным на фигуре 4 и полученным при применении стадии поверхностной обработки азотом до пастеризации. Наблюдалось отсутствие снижения уровня НМА-формы и отсутствие увеличения уровня HNA1- и HNA2-форм, наблюдавшихся на фигурах 2 и 3 при применении способа получения альбумина, применявшегося в предшествующем уровне техники.
В этом случае измерение растворенного кислорода, присутствующего в образцах после пропускания пузырьков азота, также проводили аналогично описанию в примере 2; в результате во всех случаях концентрация растворенного кислорода была равной или меньшей чем 0,5 м.д.
Пример 4: Способ получения альбумина согласно настоящему изобретению с применением стадии обработки поверхности азотом до пастеризации при других конечных концентрациях альбумина
Способ получения альбумина согласно настоящему изобретению соответствует способу, описанному в примере 2, но применяется к другим концентрациям альбумина, например, 5 и 25%. Как и в примере 2, окислительное состояние образцов с 5 и 25% концентрацией альбумина, полученных с помощью методики согласно настоящему изобретению, анализировали посредством анионообменной хроматографии. В частности, анализировали образцы 5 и 25% альбумина, подвергавшиеся стадии обработки поверхности азотом до пастеризации, образцы 5 и 25% альбумина после пастеризации и до карантина и образцы 5 и 25% альбумина после периода карантина. На фигуре 6 показаны полученные результаты, аналогичные результатам, представленным на фигуре 4 для альбумина в 20% концентрации. Наблюдалось отсутствие снижения уровня НМА-формы и отсутствие увеличения уровня HNA1- и HNA2-форм, наблюдавшихся на фигурах 2 и 3 при применении способа получения альбумина, ранее применявшегося в данной области техники.
Помимо анализа окислительного состояния выполняли измерение растворенного кислорода, присутствующего в образцах после обработки поверхности азотом; в результате во всех случаях концентрация растворенного кислорода была равна или меньше чем 0,5 м.д.
Пример 5: Способ получения альбумина согласно настоящему изобретению с применением стадии обработки поверхности гелием до пастеризации
Способ получения альбумина согласно настоящему изобретению соответствует способу, описанному в примере 1, но включает стадию, описанную ниже. После получения стерильного раствора в конечной емкости (фигура 1, стадии стерильной фильтрации и заполнения) с целью вытеснения кислорода, присутствующего в воздушной камере, остающейся во флаконе, осуществляли обработку поверхности гелием, вставляя в хлорбутиловую пробку флакона две иглы для подкожных инъекций (серийного типа Braun Sterican 21G×1½'', 0,80×40 мм, Германия, или аналогичные), подключенные к двум 0,22-мкм ПВДФ-фильтрам (серийного типа Millex GV Millipore, 0,22 мкм, ПВДФ, 13-мм фильтр, США, или аналогичным), избегая контакта игл с раствором альбумина. Одна из игл была предназначена для впуска газообразного гелия, а другая предназначена для его выпуска с целью предотвращения избыточного давления в емкости. Обработку поверхности гелием осуществляли при комнатной температуре в течение двух часов, поддерживая постоянную скорость потока гелия с целью наблюдения движения жидкости в емкости без ее разбрызгивания.
После завершения обработки поверхности гелием продолжали осуществлять способ получения альбумина из плазмы человека, как описано в примере 1 (фигура 1, стадия пастеризации во флаконах), до получения конечного продукта альбумина.
Как и в примерах 1-4, окислительное состояние образцов альбумина, полученных посредством методики согласно настоящему изобретению, анализировали с помощью анионообменной хроматографии. В частности, анализировали образцы альбумина, подвергавшиеся стадии обработки поверхности гелием до пастеризации, образцы альбумина после пастеризации и до карантина и образцы альбумина после периода карантина. На фигуре 7 показаны полученные результаты, аналогичные результатам, представленным на фигурах 4 и 6 и полученным с применением стадии обработки поверхности азотом до пастеризации, а также результатам, представленным на фигуре 5 и полученным с применением стадии пропускания пузырьков азота через раствор до пастеризации. Наблюдалось отсутствие снижения уровня НМА-формы и отсутствие увеличения уровня HNA1- и HNA2-форм, наблюдавшихся на фигурах 2 и 3 при применении способа получения альбумина, ранее применявшегося в данной области техники.
В этом случае измерение растворенного кислорода, присутствующего в образцах после пропускания пузырьков гелия, также проводили аналогично описанию в примере 2; в результате во всех случаях концентрация растворенного кислорода была равна или меньше чем 0,5 м.д.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностирования in vitro болезни Альцгеймера на основании редокс-статуса альбумина в спинномозговой жидкости | 2017 |
|
RU2696485C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЭФФЕКТИВНОГО ЧЕЛОВЕЧЕСКОГО АЛЬБУМИНА ДЛЯ ПРИМЕНЕНИЯ В ДЕТОКСИКАЦИОННОЙ ТЕРАПИИ | 2008 |
|
RU2424822C2 |
| СПОСОБ ОЧИСТКИ ГЕМОГЛОБИНА В КОММЕРЧЕСКОМ МАСШТАБЕ | 1994 |
|
RU2145873C1 |
| ИНАКТИВАЦИЯ ВИРУСОВ С ПРИМЕНЕНИЕМ КАПРИЛАТА | 2013 |
|
RU2633059C2 |
| ОБЕДНЕННАЯ ПРЕКАЛЛИКРЕИНОМ АЛЬБУМИНОВАЯ ФРАКЦИЯ ПЛАЗМЫ КРОВИ | 2003 |
|
RU2321421C2 |
| ВИНО, УПАКОВАННОЕ В АЛЮМИНИЕВЫЕ ЕМКОСТИ | 2017 |
|
RU2693945C2 |
| КОМПОЗИЦИИ ТЕТРАГИДРОБИОПТЕРИНА И СПОСОБЫ ЕГО КОЛИЧЕСТВЕННОЙ ОЦЕНКИ | 2008 |
|
RU2486899C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭЛЕМЕН, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ЕЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2838027C1 |
| СЕЛЕКТИВНОЕ ВОССТАНОВЛЕНИЕ ЦИСТЕИНОВЫХ ОСТАТКОВ В АНТИТЕЛАХ ПРОТИВ IL-17 | 2015 |
|
RU2719563C2 |
| СПОСОБ КОНЕЧНОЙ ИНАКТИВАЦИИ ПАТОГЕННЫХ МИКРООРГАНИЗМОВ | 2013 |
|
RU2629866C1 |

Группа изобретений относится к медицине и касается способа получения раствора человеческого альбумина, включающего стадию снижения уровня растворенного кислорода в указанном растворе альбумина, причем уровень кислорода снижается до концентрации равной или меньшей чем 0,5 м.д. Группа изобретений также касается композиции человеческого альбумина, где альбумин получен указанным способом. Группа изобретений обеспечивает получение раствора человеческого альбумина с состоянием окисления/восстановления, аналогичным состоянию окисления/восстановления альбумина, присутствующего в плазме крови человека. 2 н. и 11 з.п. ф-лы, 5 пр., 7 ил.
1. Способ получения раствора человеческого альбумина, отличающийся тем, что он включает стадию снижения уровня растворенного кислорода в указанном растворе альбумина, причем уровень кислорода снижается до концентрации равной или меньшей чем 0,5 м.д.
2. Способ по п. 1, отличающийся тем, что стадию снижения уровня растворенного кислорода в растворе альбумина осуществляют посредством обработки поверхности раствора альбумина инертным газом.
3. Способ по п. 1, отличающийся тем, что стадию снижения уровня растворенного кислорода в растворе осуществляют посредством пропускания пузырьков инертного газа через слой указанного раствора альбумина.
4. Способ по любому из пп. 1-3, отличающийся тем, что альбумин имеет плазматическое, рекомбинантное или трансгенное происхождение.
5. Способ по любому из пп. 1-3, отличающийся тем, что концентрация альбумина в растворе альбумина составляет от примерно 4 до 25% (масса/объем).
6. Способ по п. 2 или 3, отличающийся тем, что используемый инертный газ представляет собой азот или гелий.
7. Способ по любому из пп. 1-3, отличающийся тем, что стадию снижения уровня растворенного кислорода в растворе альбумина осуществляют до стадии пастеризации указанного раствора альбумина.
8. Способ по любому из пп. 1-3, отличающийся тем, что стадию снижения уровня растворенного кислорода в растворе альбумина осуществляют после стадии пастеризации указанного раствора альбумина.
9. Способ по любому из пп. 1-3, отличающийся тем, что после стадии снижения уровня растворенного кислорода в растворе альбумина указанный раствор альбумина выдерживают в атмосфере инертного газа.
10. Способ по п. 9, отличающийся тем, что атмосфера инертного газа состоит из газообразного азота или гелия.
11. Способ по любому из пп. 1-3 и 10, отличающийся тем, что раствор альбумина упаковывают и/или хранят в емкости, изготовленной из материала, непроницаемого для кислорода.
12. Способ по п. 11, отличающийся тем, что материал, непроницаемый для кислорода, представляет собой стекло.
13. Композиция человеческого альбумина, где альбумин получен способом по любому из пп. 1-12, отличающаяся тем, что концентрация растворенного кислорода в ней равна или меньше чем 0,5 м.д.
| CN 102816230 B, 12.02.2014 | |||
| ВОДНЫЙ РАСТВОР ФАКТОРА VIII СО СНИЖЕННОЙ КОНЦЕНТРАЦИЕЙ КИСЛОРОДА | 1994 |
|
RU2142290C1 |
| US 5691451 A, 25.11.1997 | |||
| MEDIC P | |||
| et al | |||
| [Preparation of human albumin preparations] | |||
| [Article in Croatian] Bilt Hematol Transfuz | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
Авторы
Даты
2018-06-14—Публикация
2015-05-18—Подача