Описание изобретения
Настоящее изобретение относится к способу получения человеческого альбумина с высокой способностью к транспортировке молекул для применения, среди прочего, например, в детоксикационной терапии или для клеточных культур. Изобретение основано на экспериментах, проведенных по очистке человеческого альбумина с высокой связывающей способностью для транспортировки молекул и за счет этого по повышению эффективности детоксикационной терапии посредством выведения токсинов из крови предпочтительно способами инфузии альбумина, плазмофереза и замещения альбумина экстракорпоральной системой. Этот способ согласно изобретению включает способ получения раствора альбумина с инактивированными вирусами для терапевтического применения, характеризующегося высокой связывающей способностью, без стабилизирующих агентов или со специфичными стабилизирующими агентами, позволяющими поддерживать высокую связывающую способность.
Сущность изобретения определена в п.1 формулы изобретения.
Зависимые пункты 2-22 определяют другие предпочтительные аспекты изобретения.
Предшествующий уровень техники
В количественном отношении альбумин является наиболее важным белком в плазме человека и играет фундаментальную роль в поддержании коллоидно-осмотического давления крови. Альбумин обладает также и другими свойствами, такими как его антиоксидантная активность и активность против свободных радикалов, а также, среди других лигандов, его сродство к связыванию различных эндогенных и экзогенных веществ, таких как липиды, жирные кислоты, соли желчных кислот, лекарства и токсичные вещества.
Терапевтическое применение альбумина указано согласно нескольким авторам как заместительная терапия у пациентов с тяжелым дефицитом альбумина, гиповолемическим синдромом или шоком (тяжелые ожоги, травмы или кровотечения), гипопротеинемией вследствие хронических заболеваний почек и цирроза печени, а также в случаях экстракорпорального кровообращения, острого респираторного дистресс-синдрома, гемодиализа и гипербилирубинемии. Альбумин также применяют при лечении асцита, острых нефрозов, панкреатита, внутрибрюшных инфекций и острой печеночной недостаточности.
Как основная транспортная молекула в крови сывороточный альбумин имеет специфичные сайты связывания для липофильных веществ, таких как жирные кислоты, билирубин и т.д. Большинство лигандов альбумина связываются с одним из двух сайтов связывания I или II. Свободные жирные кислоты, ионы металлов, таких как медь, и билирубин селективно связываются со специфичными связывающими доменами.
Обычно эти вещества транспортируются альбумином в печень, где они расщепляются. В случаях печеночной недостаточности эти токсичные вещества остаются связанными с альбумином, насыщая его связывающую способность, что приводит к повышению уровня в крови токсинов, которые накапливаются в тканях и вызывают общую мультиорганную недостаточность, которая может привести к смерти пациента. В таких случаях лечение можно осуществлять с помощью экстракорпоральных систем поддержания печени, для которых полезна связывающая способность имеющегося в продаже терапевтического альбумина. Наличие альбумина с более высокой связывающей способностью могло бы быть более эффективно при данном типе лечения.
Способность альбумина захватывать и транспортировать большое количество разнообразных веществ, таких как метаболиты, металлы, токсины, жирные кислоты, гормоны и т.д., делают этот белок крайне важным.
Процессы получения альбумина из человеческой плазмы обычно начинают с Фракции V (FrV) спиртового фракционирования плазмы согласно способу Коэна (Cohn et al., J Am Chem Soc, 1946, 68, 459-475). Хотя и реже, можно использовать другие исходные вещества, такие как надосадочные (S/N) жидкости этого фракционирования по Коэну, например, S/N Фракции IV или S/N Фракции II+III, включая дополнительную стадию очистки, такую как ионообменная хроматография.
Способы очистки, при которых в качестве исходных веществ используют эти промежуточные соединения фракционирования по Коэну, при уровне чистоты альбумина >90-95%, как правило, основаны на отделении полимеров, агрегатов и других соединений, таких как липопротеины, не растворившихся в результате действия этанола, присутствующего в растворе. Для оптимального отделения этих соединений целесообразно добавлять к суспензии альбумина вспомогательные добавки для фильтрации (кизельгур) и/или нерастворимые неорганические силикаты (бентониты) либо коллоидный диоксид кремния. Возможно в соответствии с типом белковых примесей исходного материала может быть целесообразно добавлять ионообменники для поддержания условий, препятствующих адсорбции альбумина.
Далее, удаления этанола из раствора достигают путем диафильтрации в оборудовании для ультрафильтрации, что также дает возможность элиминировать ионы металлов и анионы органических карбоновых кислот, такие как цитрат (Испанский патент Р 2.107.390). Такая ультрафильтрация также позволяет достичь требуемой концентрации раствора альбумина.
Кроме того, также возможно проводить термическую обработку раствора (предпочтительно тепловой шок при температуре от 56°С до 63°С) в целях денатурации и снижения растворимости каких-либо термолабильных соединений, остающихся в растворе альбумина, которые могут дестабилизировать конечный продукт. Такая тепловая обработка также полезна при уменьшении активности активатора прекалликреина (РКА), являющегося одной из наиболее распространенных примесей альбумина.
Описаны различные способы очистки альбумина, представляющие собой вариации приведенных выше, с точки зрения последовательности стадий или добавления дополнительных стадий очистки.
Другие способы включают очистку альбумина путем ионообменной хроматографию начиная с фракции V или надосадочной жидкости FrlV, как описано в патенте США 5346992 или ЕР 0367220. В патенте США 4288154 предложен способ начиная с надосадочной жидкости Fr II+III, а также ионообменная хроматография с предшествующей стадией гель-фильтрации.
Растворы человеческого альбумина для терапевтического применения, полученные из плазмы известными на современном уровне техники способами, в форме концентрированного раствора, как правило, с концентрацией от 15% до 25% общего белка, являются гиперосмотическими и вызывают движение жидкостей из экстраваскулярного в интраваскулярный компартмент либо в форме изотонического раствора с концентрацией от 3,5% до 5% общего белка, являющегося изотоническим с плазмой. Препараты этих растворов содержат альбумин, имеющий уровень чистоты выше 95% общего белка, и стабилизаторы.
При получении растворов альбумина из пулов плазмы крови человека, как и в случае других биологических продуктов, нельзя исключить риск передачи инфекции вирусами или другими патогенными возбудителями. Несмотря на это, современный терапевтический альбумин считают безопасным продуктом крови перед лицом этого риска. Это, в основном, является следствием того факта, что растворы альбумина пастеризуют (проводят термическую обработку по меньшей мере в течение 10 часов при 60-63°С, как правило, в готовом флаконе).
Начиная с 1941 года, когда впервые был приготовлен раствор альбумина в результате фракционирования плазмы крови человека (Cohn et al. Chem. Rev., 1941, 28, 395), были начаты исследования по стабилизации растворов альбумина, и в 1945 году была достигнута стабилизация раствора альбумина N-ацетилтриптофаном, каприлатом натрия или смесью этих двух веществ (Scatchard G, et al., J. Chem. Invest. 24:671-676, 1945). Стабилизация растворов альбумина продолжает быть предметом исследований (Finlayson J.S. et al., Vox Sang. 47:7-18, 1984); (Finlayson J.S. et al., Vox Sang. 47:28-40, 1984), однако до сих пор не было предложено существенных изменений, и такая форма стабилизации принята нормативно-правовыми органами разных стран (например: Европейская фармакопея, Human Albumin Solution monograph 0255). Следовательно, в настоящее время имеющиеся в продаже препараты альбумина, в основном, содержат в качестве стабилизаторов каприлат и/или N-ацетилтриптофан, чтобы избежать полимеризации в процессе пастеризации и гарантировать стабильность при хранении продукта в течение его срока годности.
В случаях, когда терапевтический эффект альбумина осуществляется по механизму захвата токсичных соединений до их выведения, например при лечении гипербилирубинемии, эффективность лечения зависит от наличия свободных сайтов связывания альбумина.
В исследованиях на моделях гипербилирубинемии у новорожденных Ebbesen F. (Acta Pediatr. Scand 71:85-90, 1982) было установлено, что N-ацетилтриптофан активно замещает билирубин, таким образом, снижая эффективность альбумина, стабилизированного N-ацетилтриптофаном и каприлатом по сравнению с альбумином, стабилизированным только каприлатом. Несмотря на то что любой из этих двух препаратов является эффективным при защите от энцефалопатии, вызванной билирубином, эти данные, по-видимому, показывают, что стабилизация N-ацетилтриптофаном не должна быть пригодной для лечения гипербилирубинемии, и демонстрируют преимущество стабилизации альбумина каприлатом.
В других исследованиях предметом которых также является сродство и способность альбумина к связыванию различных веществ, включая триптофан и каприлат, установлено, что существует конкуренция между различными соединениями за сайты связывания альбумина (Kragh-Hansen U. Biochem. J. (1991) 273, 641-644), и признано, что, в то время как триптофан связывается с молекулой альбумина в специфичном сайте, каприлат (октаноат) связывается с молекулой альбумина в различных сайтах, вызывая снижение способности альбумина к связыванию с другими соединениями.
В настоящее время не существует сомнений, что эти стабилизаторы связываются по меньшей мере с сайтом связывания II альбумина и, таким образом, препятствуют транспортной функции пастеризованного альбумина, а также могут ингибировать, по меньшей мере частично, связывание эндогенных лигандов (токсинов и т.д.) после внутривенной инфузии этого альбумина.
Были сделаны попытки в направлении разработки способов получения альбумина, которые бы позволили избежать использования N-ацетилтриптофана и/или каприлата натрия как в процессе очистки, так и в конечной композиции.
Патент WO 2004071524 относится к способу получения альбумина, который позволяет избежать включения стабилизаторов из групп N-ацетилтриптофана и каприлата. Для стадии инактивации вируса вместо пастеризации авторы изобретения выбрали обработку растворителем-детергентом (РД). Обработка РД показала высокую эффективность при инактивации вируса с липидной оболочкой, однако она не обладает значительным эффектом при уничтожении вирусов без оболочки. Другим недостатком данного способа является необходимость в удалении реагентов для инактивации РД, требующая включения стадий экстракции, которые являются сложными, длительными и делают этот способ более дорогостоящим. Наконец, как наблюдали авторы изобретения, присутствие РКА в растворах альбумина частично снижается в результате нагревания. Поскольку данный патент не включает термическую обработку, он должен также включать специальную стадию для удаления РКА, что еще более усложняет способ.
Патент США 5919907 также касается попыток получить альбумин с более высокой связывающей способностью путем разработки способа, который позволяет избежать пастеризации и, следовательно, добавления стабилизаторов групп N-ацетилтриптофана и каприлата. В данном способе используют преимущество бактерицидных свойств соединений йода. Благодаря сродству молекул альбумина к йоду и, следовательно, способности альбумина нейтрализовать его бактерицидный эффект, данный способ требует в соответствии с указанным патентом добавления соединения йода в количестве, достаточном для насыщения связывающей способности альбумина, а также дает возможность достаточному количеству свободного йода оставаться в растворе с бактерицидным эффектом. В связи с этим воспроизводимость данного способа не кажется легко достижимой, причем данный аспект является фундаментальным для стадии элиминации патогенов. Кроме того, данный способ требует удаления реагента для инактивации, что также требует включения стадий экстракции, которые являются сложными, длительными и делают этот способ более дорогостоящим. Другим аспектом, заслуживающим внимания и не упомянутым в указанном патенте, является присутствие РКА в растворе альбумина. Как и в предыдущем случае, если термическую обработку не проводят, должна быть включена специальная стадия удаления РКА, что усложняет процесс.
Краткое описание графических материалов
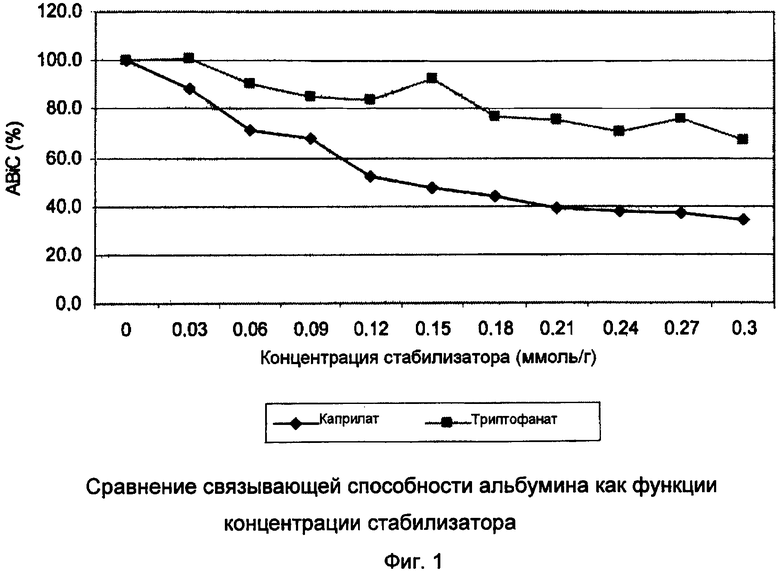
На Фиг.1 представлено сравнение связывающей способности альбумина как функции концентрации стабилизатора.
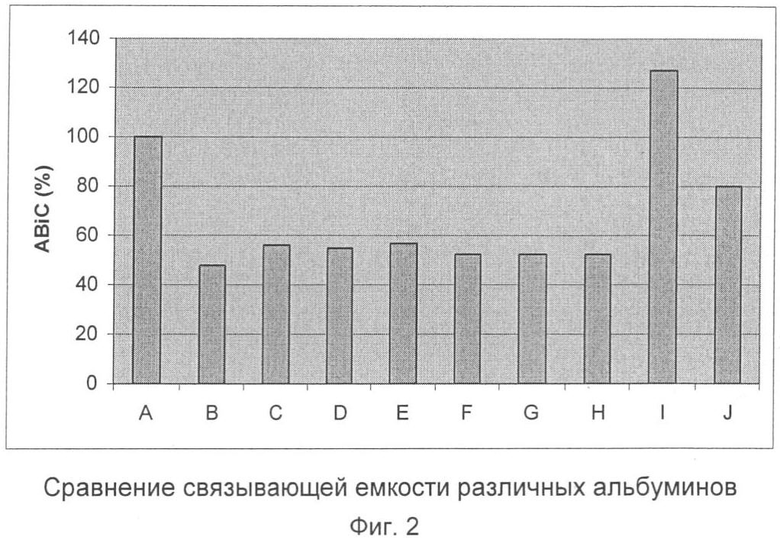
На Фиг.2 представлено сравнение связывающей емкости различных альбуминов.
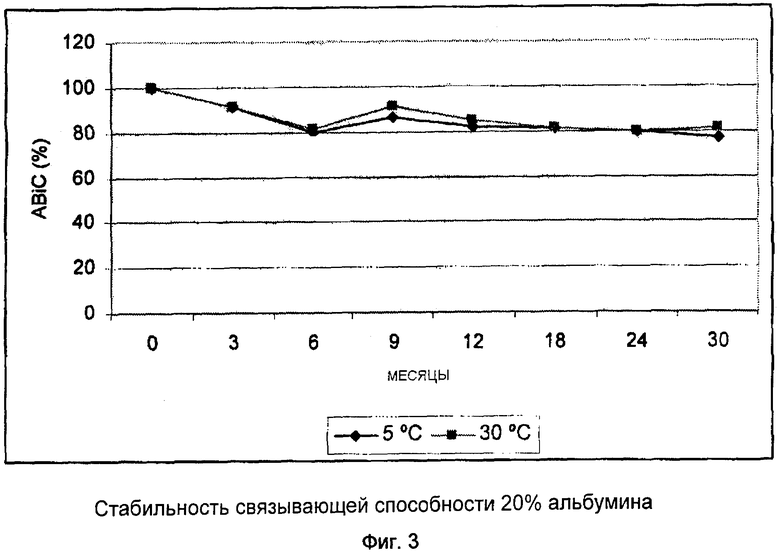
На Фиг.3 продемонстрирована стабильность связывающей способности 20% альбумина.
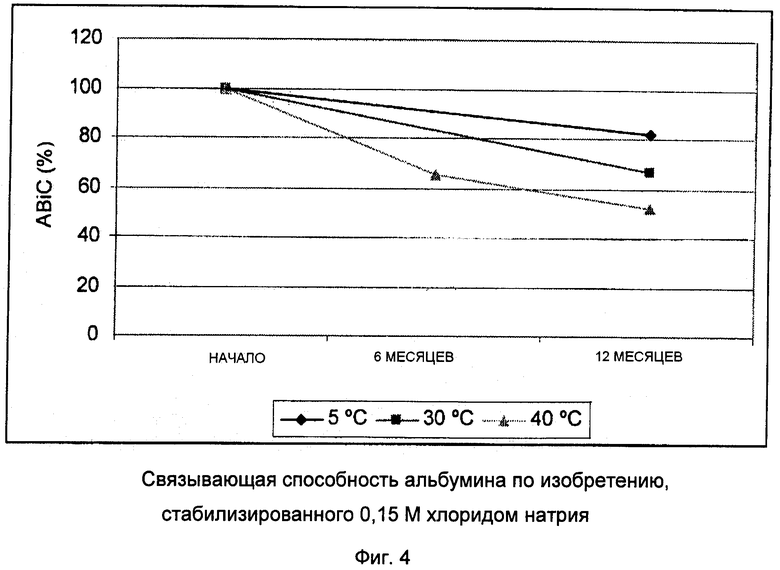
На Фиг.4 продемонстрирована связывающая способность альбумина по изобретению, стабилизированного 0,15 М хлоридом натрия.
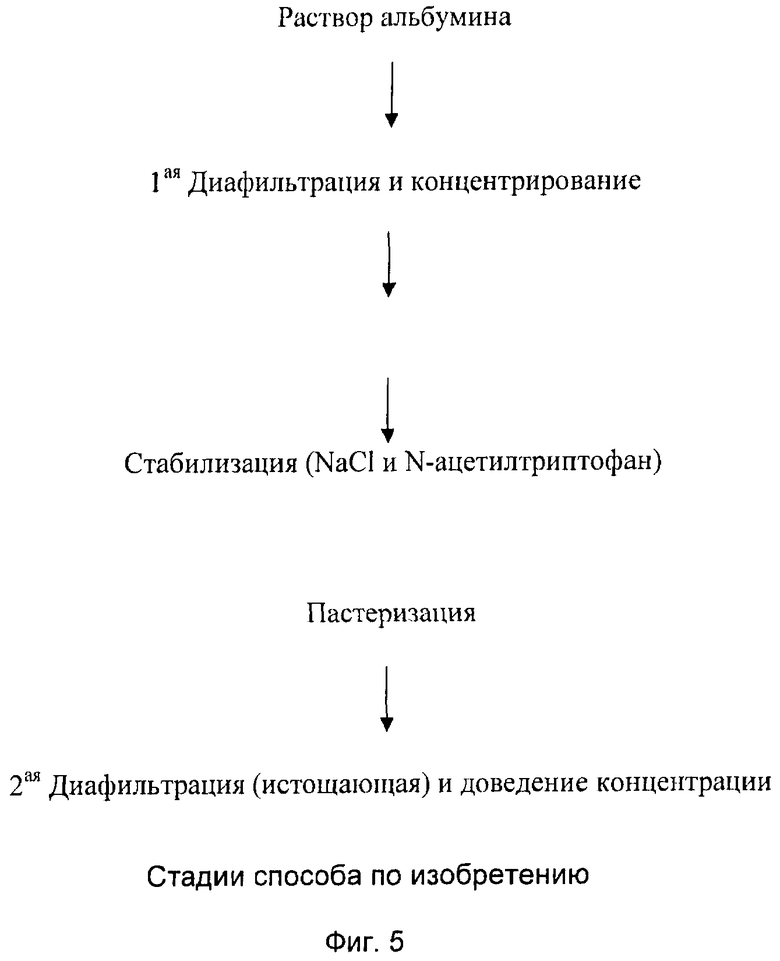
На Фиг.5 представлена диаграмма, иллюстрирующая способ по изобретению.
Описание изобретения
Путем проведенных исследований авторами изобретения установлено, что связывание между каприлатом натрия и молекулами альбумина является трудно обратимым, что приводит в результате к меньшей способности альбумина, стабилизированного каприлатом, к связыванию токсинов. Кроме того, авторы изобретения установили, что связывание между N-ацетилтриптофаном и альбумином (для терапевтического применения, полученного методом Коэна и его модификациями) является более легко обратимым. Возможность стабилизации N-ацетилтриптофаном и без каприлата позволяет получать альбумин способом, включающим стадию инактивации вирусов путем пастеризации, так что альбумин стабилизируют в присутствии по меньшей мере одной аминокислоты и хлорида натрия, но без добавления жирных кислот. Неожиданно способ очистки этого пастеризованного альбумина, включающий процесс истощающего диализа (диафильтрации), приводит в результате к большей связывающей способности пастеризованного альбумина.
Согласно способу, описанному в данном изобретении, возможно проводить стадию инактивации вируса путем пастеризации в качестве промежуточной фазы процесса. Таким образом, можно поддерживать отличный уровень безопасности, проявляемый терапевтическими альбуминами, известный к настоящему времени в отношении возможного риска передачи патогенов, и добиться снижения содержания РКА.
Способом, разработанным в настоящем изобретении, также возможно получать альбумин с превосходной связывающей способностью, включая связывающую способность нормального альбумина, присутствующего в плазме, поскольку разработанный способ дает возможность снизить содержание соединений (особенно липидов и жирных кислот), тесно связанных с альбумином в его природном состоянии и вызывающих снижение его связывающей способности, и в результате этого к меньшей эффективности в качестве улавливателя и переносчика веществ, например, в клеточных культурах и при детоксикационной терапии. Этот способ также позволяет снизить количество стабилизаторов, добавляемых при проведении пастеризации в промежуточной фазе процесса. Альбумин, полученный таким способом, обладает очень высокой способностью к связыванию и переносу молекул и ассоциированных соединений.
Для получения такого альбумина с высокой связывающей способностью можно использовать в качестве исходного вещества частично очищенный концентрат альбумина, например в виде пасты (в виде осадка). Исходным материалом для такого альбумина может служить Фракция V или Фракция VR (переосажденная), полученная спиртовым фракционированием методом Коэна (или одной из модификаций) либо другими способами фракционирования, позволяющими получить альбумин эквивалентной чистоты, как правило, ≥95% альбумина.
Другими источниками альбумина могут служить спиртовые надосадочные жидкости (S/N) данного фракционирования по Коэну, например, S/N фракции IV или S/N Фракции IV (1)+IV (4), либо Фракции IV (4), либо других надосадочных жидкостей (S/N Фракции IV (1) или S/N Фракции II+III), которые следует подвергнуть дополнительной стадии очистки, например хроматографии, в целях достижения требуемой степени чистоты (≥95% альбумина).
Альбумин, полученный таким образом, растворяют в водной среде до получения концентрации более 1%, как правило, 8±2% (на белок), итоговое значение рН, как правило, составляет 4,7±0,5, что является близким к собственной изоэлектрической точке альбумина.
Если альбумин получен из Фракции V или надосадочной жидкости фракционирования по Коэну, содержание остаточного этанола, как правило, составляет ≥6%. В другом случае этанол добавляют до указанной минимальной концентрации 6%. Во время добавления этанола или во время растворения исходного материала суспензию охлаждают до температуры от -3°С до 10°С и поддерживают температуру в данном интервале для предотвращения денатурализующего воздействия водно-спиртовой среды.
В этих условиях не растворившиеся соединения остаются в осадке, тогда как к суспензии альбумина добавляют добавки для облегчения фильтрации (кизельгур) и/или нерастворимые неорганические силикаты (бентониты), либо коллоидный диоксид кремния. Возможно, в зависимости от типа нежелательных белковых примесей в исходном материале рекомендуют добавлять неорганические ионообменники типа перлита или даже синтетические вещества с амино/аммонийными функциональными группами (DEAE, QAE), например DEAE-Sephadex, причем рН остается на уровне 4,2-5,2 для предотвращения адсорбции альбумина. В отсутствие ионообменников рН суспензии можно довести до значения от 4,2 до 7,5 и предпочтительно довести до рН 6,8-7,2.
Ниже описано суспендирование путем ультрафильтрации с использованием фильтров с таким размером пор, который обеспечивает удерживание частиц размером ≥0,2 мкм. Фильтрат представляет собой раствор альбумина, по существу свободный от нерастворимых остатков денатурализованного белка и других соединений (в основном, липопротеинов), не растворимых в этаноле.
Полученный продукт подвергают диафильтрации через мембраны из полиэфирсульфона или его эквивалентов, номинально пропускающих молекулы размером от 1 до 50 кДа, предпочтительно от 10 до 30 кДа. Диафильтрация с водой для инъекций или предпочтительно с физиологическим раствором с концентрацией NaCl≥0,15 М может быть достигнута в тех же условиях рН от 4,2 до 7,5, которые находятся в фильтрате, полученном на предыдущей стадии, но предпочтительно, в зависимости от присутствия липидов, следует делать выбор в пользу доведения рН до 4,2-5,2. Кроме того, концентрация физиологического раствора также способствует диссоциации ионов металлов, таких как алюминий или железо, и анионов более сильно диссоциирующих органических карбоновых кислот, таких как цитрат.
В соответствии с общепринятой методикой ультрафильтрации авторы изобретения выполнили первую стадию концентрирования, достигая примерно между 8 и 15% белка, а затем провели диафильтрацию путем добавления растворителя при постоянном объеме. Количество раствора для диафильтрации не должно составлять менее 3 объемов, предпочтительно более 7 объемов.
Раствор альбумина, доведенный до значения рН, близкого к нейтральному, можно стабилизировать добавлением NaCl до концентрации ≥0,15 М и по меньшей мере одной аминокислоты, предпочтительно используя N-ацетилтриптофан в количестве ≥0,096 ммоль/г альбумина. Этот стабилизированный раствор можно стерилизовать полной фильтрацией через фильтры с размером пор 0,2 мкм, собирая в общей массе в качестве промежуточного материала для его дальнейшей пастеризации в этой фазе.
Инактивация вирусов пастеризацией имеет то преимущество, что эффективность данного способа не зависит от наличия или отсутствия липидной оболочки у вируса, и это является очевидным преимуществом перед химической обработкой, например с использованием РД.
Далее основной объем промежуточного, термически обработанного раствора очищают фильтрацией и подвергают истощающей диафильтрации для уменьшения количества стабилизаторов, добавленных в течение предыдущей стадии.
Вторую стадию диафильтрации выполняют при таких же условиях нанесения, как и в начальной стадии перед термической обработкой, позволяя конечному раствору альбумина достичь изотонии (примерно, 0,15 М NaCl), и концентрацию белка доводят до желаемой величины, примерно между 3,5% и 25%.
Учитывая, что N-ацетилтриптофан, используемый в качестве стабилизатора, интенсивно удаляется в форме, указанной диафильтрацией, число нанесенных объемов раствора для диафильтрации устанавливают в зависимости от количества остающегося стабилизатора.
Возможно также включение в способ стадии элиминации вирусов посредством нанофильтрации. Эффективность удаления вирусов нанофильтрацией, так же как в случае пастеризации, также эффективно независимо от наличия у вируса оболочки. Эффективность нанофильтрации является функцией размера пор используемого нанофильтра в зависимости от фильтруемого раствора. В случае растворов альбумина нанофильтрация возможна при размерах пор 15 нм, при которых можно гарантировать существенное снижение содержания вирусов, считающихся наименьшими. Включение стадии нанофильтрации с использованием пор очень маленького размера в качестве дополнения к пастеризации не требует наличия стабилизаторов, таким образом, связывающая емкость полученного альбумина остается неизменной. Кроме того, сочетание пастеризации и нанофильтрации повышает уровень безопасности продукта, если достижение более высокого уровня безопасности целесообразно.
Для того чтобы достичь нанофильтрации альбумина, которая является действительно эффективной в отношении некоторых вирусов, передаваемых через кровь, включая самые мелкие, необходимо, чтобы содержание соединений с высокой молекулярной массой или агрегатов, присутствующих в продукте, было крайне дискретным, следовательно, целесообразно выполнять эту стадию до термической обработки.
К настоящему времени описано использование имеющихся в продаже нанофильтров с различным размером пор фильтрации, эффективность удерживания которых по отношению к вирусам варьирует в зависимости от выбранного размера пор. Для применения в случае альбумина можно использовать фильтры с размером пор 50 нм, 35 нм, 20 нм и 15 нм, которые также можно объединять в серии по два фильтра или более с образованием градиента уменьшения размера пор. Также возможно достижение двойной нанофильтрации, используя фильтры с одинаковым размером пор, что повышает возможность удерживания возможных патогенов.
Условия для концентрирования белка варьируют в зависимости от размера пор нанофильтра. Поэтому для размеров менее чем 15 и 20 нм рекомендуют тщательно разбавлять альбумин до концентрации менее 5%, предпочтительно между 0,5 и 2%. Однако когда размеры пор составляют между 35 и 50 нм или более, возможна непосредственная нанофильтрация при концентрациях альбумина ≥5%. Условия температуры окружающей среды (18-25°С) и примерно нейтрального уровня рН наиболее пригодны для облегчения фильтрации.
В любом случае концентрирование путем ультрафильтрации после нанофильтрации может быть необходимо для доведения конечного состава препарата.
Приемлемой формой консервирования высокоэффективного альбумина по изобретению является лиофилизация, которая не требует использования стабилизаторов.
Для концентрирования альбумина в растворе может быть необходима его стабилизация, и ее можно осуществить с помощью раствора хлорида натрия ≥0,15 М. Альбумин, стабилизированный в такой форме, обладает соответствующим уровнем стабильности при хранении в холоде (между 2°С и 8°С).
Другую форму стабилизации можно осуществить с хлоридом натрия ≥0,15 М и N-ацетилтриптофаном при концентрации ≥0,096 ммоль/грамм альбумина, предпочтительно 0,16 ммоль/грамм альбумина. Раствор, стабилизированный таким составом, обладает соответствующим уровнем стабильности при хранении в течение 30 месяцев в жидком состоянии при температуре ниже или вплоть до 30°С или в течение более короткого периода времени, но при более высокой температуре. В любом случае необходимо избегать включения жирных кислот.
Для определения связывающей способности альбумина (ABiC) используют способ, основанный на изменении флуоресценции при связывании специфичного флуоресцентного маркера, такого как дансилсаркозин, с сайтом связывания альбумина II. После разбавления различных образцов альбумина до одинаковой концентрации и инкубации их с маркером несвязанные молекулы маркера отделяют фильтрованием, и количество свободного дансилсаркозина оценивают с помощью флуориметрического обнаружения (λ возбуждения=355 нм и λ излучения=460 нм). Связывающую способность рассчитывают следующим образом:

(RFU: относительная единица флуоресценции)
Определив связывающую способность таким способом, используя в качестве эталона связывающую способность альбумина натуральной плазмы крови человека (100%), авторы изобретения рассчитали, что высокая связывающая способность составляет не менее 80% связывающей способности альбумина натуральной плазмы крови человека.
В целях настоящего изобретения высокую степень связывающей способности альбумина определяли как величину ABiC в %, большую по сравнению с таковой для имеющихся в продаже альбуминов, стабилизированных каприлатом натрия или смесью каприлата натрия и N-ацетилтриптофана.
Конкретно настоящее изобретение заключается в способе получения пастеризованного раствора альбумина с высокой способностью к связыванию молекул, включающем следующие стадии:
а) первичный диализ (диафильтрация)
б) стабилизация раствора NaCl и по меньшей мере одной аминокислотой
в) нагревание раствора
г) второй диализ (диафильтрация)
Данный способ применим для любого раствора альбумина независимо от его происхождения как имеющего происхождение из плазмы крови человека, так и полученного рекомбинантными или трансгенными способами.
Способ получения раствора альбумина с высокой способностью к связыванию молекул включает нагревание раствора альбумина (пастеризацию) с целью инактивации вирусов и снижения содержания РКА. Нагревание выполняют при температуре 61±2°С в течение 10,5±0,5 часов.
Для того чтобы раствор альбумина можно было нагреть, его стабилизируют хлорид натрия (NaCl) при концентрации 0,15 М или выше и добавлением по меньшей мере одной аминокислоты. Аминокислота предпочтительно представляет собой N-ацетилтриптофан в количестве более 0,096 ммоль N-ацетилтриптофана/г альбумина.
Особенным отличием способа является отсутствие стадии добавления жирных кислот к раствору альбумина.
Способ, описанный для получения раствора альбумина с высокой связывающей способностью по отношению к молекулам, включает удаление путем диафильтрации связанных с альбумином веществ, которые снижают его связывающую способность. Такие вещества, связанные с альбумином, могут представлять собой природные лиганды, всегда связанные с альбумином до его очистки, или вещества (стабилизаторы), добавленные во время очистки.
Удаление с помощью диафильтрации веществ, связанных с альбумином, выполняется в две стадии. Первая стадия диафильтрации выполняется перед стабилизацией, для того чтобы нагреть раствор. Во второй стадии диафильтрации удаляют аминокислоту, добавленную в качестве стабилизатора.
В способе, описанном для получения раствора альбумина с высокой связывающей емкостью по отношению к молекулам, стадии диафильтрации выполняют, используя не менее 3 объемов раствора NaCl, предпочтительно 7 объемов. После диафильтрации раствора NaCl проводится диафильтрация в воде для того, чтобы установить концентрацию солей в растворе до требуемого значения.
Настоящее изобретение далее описано более подробно в примерах, которые, однако, не ограничивают объем изобретения.
Пример 1.
Сравнение влияния на связывающую способность альбумина (ABiC) стабилизаторов N-ацетилтриптофана и каприлата натрия
Для того чтобы получить альбумин с высокой связывающей способностью, было принято решение оценить, какое количество стабилизаторов каприлата натрия и N-ацетилтриптофана, обычно используемых для стабилизации имеющихся в продаже препаратов, влияет на связывающую способность альбумина без стабилизации.
Для этого установленным способом определяли ABiC, но в качестве эталона использовали альбумин без стабилизаторов. Приготовили отдельные растворы каждого наполнителя (N-ацетилтриптофан и каприлат) с увеличивающимися концентрациями. 1 мл каждого раствора инкубировали с 1 мл альбумина без стабилизаторов (конечная концентрация альбумина 1%). Далее к каждой смеси добавляли 1 мл дансилсаркозина, далее следовал обычный процесс с использованием способа количественного определения связывающей способности альбумина.
Полученные результаты (Фиг.1) показывают, что при одной и той же концентрации наполнителя связывающая способность альбумина ниже в случае добавления каприлата по сравнению со случаем добавления N-ацетилтриптофана.
Пример 2
Сравнение связывающей способности альбумина плазмы (AbiC) с различными имеющимися в продаже концентратами альбумина и с альбумином, полученным способом, описанным в настоящем изобретении, без использования стабилизаторов и стабилизированных N-ацетилтриптофаном в количестве 0,16 ммоль/г.
Принимая в качестве эталона (100%) связывающую способность альбумина натуральной плазмы (колонка А, Фиг.2), авторы изобретения обнаружили, что в случае различных имеющихся в продаже альбуминов с добавлением стабилизаторов N-ацетилтриптофана и каприлата натрия в концентрациях от 0,064 до 0,096 ммоль/г альбумина наблюдается падение связывающей способности альбумина в том же порядке для всех образцов (от 48% до 57%) (колонки В-G) и в таком же порядке падает связывающая способность имеющегося в продаже альбумина, стабилизированного только каприлатом натрия (0,099 ммоль/г) (52%) (колонка Н). Эти значения меньше значения связывающей способности альбумина плазмы.
Самая высокая связывающая способность альбумина была обнаружена в случае альбумина по настоящему изобретению без стабилизаторов (127%) (колонка I), также самое высокое значение получено для стабилизированного N-ацетилтриптофаном в количестве 0,16 ммоль/г (80%) (колонка J) по сравнению с имеющимися в продаже концентратами альбумина.
Данные результаты показывают, с одной стороны, преимущество способа очистки, описанного для альбумина с высшей связывающей способностью, и, с другой стороны, существенное влияние на связывающую способность альбумина проанализированных стабилизаторов, каприлата натрия и N-ацетилтриптофана.
Пример 3
Стабильность раствора альбумина
Раствор альбумина концентрации 20%, полученный способом, описанным в настоящем изобретении, стабилизировали 0,15 М раствором хлорида натрия и N-ацетилтриптофаном в количестве 0,16 ммоль/г альбумина, далее изучали стабильность в соответствии с существующими инструкциями по изучению стабильности, согласованными на международном уровне, Q5C «Испытание стабильности биотехнологических/биологических продуктов» и Q1A (R2) «Испытание стабильности новых лекарств, веществ и продуктов».
Данные стабильности в режиме реального времени для 3 партий показывают, что продукт остается стабильным. В частности, не наблюдается существенного изменения связывающей способности по сравнению с началом исследования, по меньшей мере, в течение 30 месяцев при хранении при температуре 5°С±3°С и при 30°С±2°С (Фиг.3). Фактически со временем наблюдались параллельные колебания связывающей способности при 5°С и при 30°С, поэтому они могут быть в большей степени приписаны фактической нестабильности теста, выполняемого в разные дни, истинной нестабильности связывающей способности.
Пример 4
Стабильность раствора альбумина, полученного способом по настоящему изобретению и стабилизированного 0,15 М хлоридом натрия
Данные исследования стабильности при температурах хранения 5°С, 30°С и 40°С в режиме реального времени показывают, что продукт остается стабильным при температуре 5°С. При этой температуре не отмечено существенных изменений связывающей способности (Фиг.4) по сравнению с началом исследования, также по сравнению с альбумином, стабилизированным N-ацетилтриптофаном. Молекулярное распределение и данные мутности также подтверждают стабильность данного раствора альбумина.
Стабильность альбумина по изобретению, стабилизированного 0,15 М хлоридом натрия.
Как можно увидеть из вышеприведенных материалов, авторы изобретения продемонстрировали существенное преимущество применения человеческого альбумина с высокой связывающей способностью для детоксикационной терапии путем исследований в отношении изучения стабилизации альбумина и устранения стабилизаторов, связанных с альбумином, и их влияния на связывающую способность альбумина.
Человеческий альбумин, применяемый для детоксикационной терапии, отличается тем, что в его конечном препарате полностью отсутствуют стабилизаторы или содержатся стабилизирующие агенты, приводящие к повышению связывающей способности.
Детоксикационную терапию можно проводить путем инфузии альбумина пациенту, плазмафереза и замены альбумина у пациента либо используя экстракорпоральные системы.
Хотя настоящее изобретение было объяснено в приведенном выше описании в соответствии с приведенными примерами, не ограничивающими объем настоящего изобретения, следует считать, что все варианты, включающие приведенную ниже формулу изобретения, находятся в пределах объема настоящего изобретения.
Группа изобретений относится к способу получения человеческого альбумина с высокой связывающей способностью для применения, в частности, в детоксикационной терапии. Способ получения раствора человеческого альбумина из плазмы крови человека включает: а) получение фильтрата из плазмы крови, представляющего собой раствор альбумина, по существу свободный от нерастворимых остатков денатурированного белка и других соединений, не растворимых в этаноле; b) первую стадию диафильтрации; с) стабилизацию продукта, полученного на стадии (b), раствором NaCl и N-ацетилтриптофаном без добавления жирных кислот; d) пастеризацию продукта, полученного на стадии (с); е) вторую стадию диафильтрации до полного удаления N-ацетилтриптофа с получением раствора человеческого альбумина. Предложенный способ обеспечивает получение раствора человеческого альбумина с инактивированными вирусами, обладающего высокой способностью к связыванию и переносу молекул и ассоциированных соединений, который может быть использован для применения в детоксикационной терапии посредством выведения токсинов из крови предпочтительно способами инфузии альбумина, плазмофереза и замены альбумина или с помощью экстракорпоральной системы. 2 н. и 12 з.п. ф-лы, 1 табл., 5 ил.
1. Способ получения раствора человеческого альбумина из плазмы крови человека, включающий:
a) получение фильтрата из плазмы крови, представляющего собой раствор альбумина, по существу, свободный от нерастворимых остатков денатурированного белка и других соединений, не растворимых в этаноле;
b) первую стадию диафильтрации;
c) стабилизацию продукта, полученного на стадии (b), раствором NaCl и N-ацетилтриптофаном без добавления жирных кислот;
d) пастеризацию продукта, полученного на стадии (с);
e) вторую стадию диафильтрации до полного удаления N-ацетилтриптофа с получением раствора человеческого альбумина.
2. Способ по п.1, где пастеризацию выполняют при температуре 61±2°С.
3. Способ по п.2, где пастеризацию выполняют в течение 10,5±0,5 ч.
4. Способ по п.1, где стабилизацию выполняют раствором NaCl в концентрации ≥0,15М и раствором N-ацетилтриптофана в количестве ≥0,096 ммоль N-ацетилтриптофана/г альбумина.
5. Способ по п.1 первую стадию диализа выполняют до стабилизации, выполняемой для обеспечения пастеризации.
6. Способ по п.1, где вторую стадию диализа выполняют после пастеризации.
7. Способ по п.6, где удаление аминокислоты, добавленной в качестве стабилизатора, проводят на второй стадии диализа.
8. Способ по п.1, где диализ проводят в растворе NaCl.
9. Способ по п.8, где диализ проводят не менее чем 3 объемами раствора NaCl, предпочтительно 7 объемами.
10. Способ по п.8, где после диализа в растворе NaCl выполняют диализ в воде для доведения концентрации солей в растворе до желаемой величины.
11. Применение раствора, полученного способом по пп.1-10, для изготовления лекарственного средства для применения в детоксикационной терапии путем инфузии альбумина, плазмофереза и замены альбумина или с помощью экстракорпоральной системы.
12. Применение по п.11, при котором введение осуществляют путем инфузии альбумина.
13. Применение по п.11, при котором введение осуществляют путем плазмофереза и замены альбумина.
14. Применение по п.11, при котором детоксикационную терапию проводят с помощью экстракорпоральной системы.
| WO 2006120226 A1, 16.11.2006 | |||
| Устройство для охлаждения свежесформованных химических нитей | 1978 |
|
SU787498A1 |
| WO 2006066595 A2, 29.06.2006 | |||
| US 4043997 A, 23.08.1977 | |||
| РАСТВОР АЛЬБУМИНА И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2004 |
|
RU2305556C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬБУМИНА | 1998 |
|
RU2140287C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ АЛЬБУМИНА | 0 |
|
SU301158A1 |
| ВЫДВИЖНОЙ ПОДПОЧВЕННЫЙ ГИДРАНТ | 0 |
|
SU367220A1 |
| US 5919907 A, 06.07.1999 | |||
| SHRAKE A et al | |||
| Thermal stability of human albumin measured by differential scanning calorimetry | |||
| I | |||
| Effect of caprylate and N-acetyltryptophanate | |||
| Vox Sang, 1984; 47(1):7-18. | |||
Авторы
Даты
2011-07-27—Публикация
2008-11-11—Подача