Изобретение относится к области медицины, а именно к кардиологии.
Современная демографическая ситуация отражает процесс неуклонно продолжающегося постарения населения, происходящий практически во всех экономически развитых и развивающихся странах мира, в том числе и в России. При этом, основной проблемой для здоровья пожилых людей являются неинфекционные, в частности сердечно-сосудистые заболевания. Как известно, заболеваемость ишемической болезнью сердца (ИБС) с наиболее частым и грозным ее осложнением, нередко приводящим к летальному исходу, острым инфарктом миокарда (ИМ), увеличивается с возрастом, достигая своего пика у лиц 60 лет и старше [1]. Удельный вес пациентов данной возрастной группы в структуре больных острым ИМ составляет более 60% [2]. При этом, как известно, с увеличением возраста происходит накопление факторов риска и коморбидной патологии, и лица старших возрастных групп оказываются наиболее уязвимыми в отношении развития атипичных форм острого ИМ и его осложненного течения, что в свою очередь повышает риск летального исхода как в ближайшем, так и в отдаленном периоде [3]. Согласно данным европейских исследователей, от 5 до 15% пациентов умирает в течение 1 года после перенесенного ИМ, последующая ежегодная летальность составляет 2-5% [4]. Наряду с этим, по данным Кужелевой Е.А., полученным в ходе проспективного популяционного исследования, летальность в группе пациентов 20 лет и старше в г. Томске составила 35% в течение пяти лет наблюдения [5]. Однако у пациентов старших возрастных групп в силу сочетания факторов риска и сопутствующих патологий можно ожидать более высоких уровней летальности.
Известные способы оценки риска летального исхода (GRACE, РЕКОРД) призваны стратифицировать риск в течение периода пребывания больного в стационаре и в течение полугода после свершившегося коронарного события. В настоящее время идет активное изучение отдаленных исходов острого ИМ и поиск прогностических показателей, наиболее полно и точно отражающих влияние на исходы заболевания. Разработаны способы прогнозирования развития летальных исходов в отдаленном постинфарктном периоде [6, 7]. Однако в данных способах не учитываются в достаточной степени особенности анамнеза и клинического течения заболевания, присущие пациентам пожилого и старческого возраста, которые несомненно вносят значительный вклад в прогноз заболевания. Данные способы не могут обеспечить персонифицированного подхода в оказании медицинской помощи данной категории пациентов.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не обнаружено.
Задача изобретения - разработать способ прогнозирования летального исхода у пациентов пожилого и старческого возраста в течение пяти лет после перенесенного ИМ.
Поставленная задача решается путем формирования когорты больных 60 лет и старше из числа постоянных жителей г. Томска, перенесших ИМ в 2008-2009 гг. (410 человек), в отношении которых удалось получить достаточный для статистической обработки объем информации. Отбор пациентов осуществляют с использованием информационно-аналитической базы данных «Регистр острого инфаркта миокарда» (РОИМ). За период 5-летнего наблюдения погибли 42,4% пациентов. Таким образом, группу исследования составили пациенты, выжившие в процессе 5-летнего проспективного наблюдения (236 человек) и умершие в течение пяти лет постинфарктного периода от сердечно-сосудистых и прочих причин (174 человека).
Для выявления прогностических факторов летального исхода в течение пяти лет после перенесенного ИМ у пациентов пожилого и старческого возраста в анализ были включены следующие признаки, которые теоретически могли оказать влияние на исходы заболевания:
1. Демографические показатели:
• Пол (мужской, женский);
• Возраст пациентов:
- возраст на момент индексного ИМ (годы);
- возраст на момент индексного ИМ (1 - менее 75 лет, 2-75 лет и более);
2. Анамнестические данные:
• Гипертоническая болезнь в анамнезе (да/нет);
• Стенокардия напряжения в анамнезе (да/нет);
• Перенесенный в прошлом ИМ (да/нет);
• Наличие хронической сердечной недостаточности (ХСН) на момент индексного ИМ (да/нет);
• Острое нарушение мозгового кровообращения (ОНМК) в анамнезе (да/нет);
• Наличие патологии углеводного обмена (да/нет);
• Наличие сахарного диабета 2 типа (да/нет);
• Курение (да/нет);
3. Клинические, лабораторные, инструментальные данные в остром периоде ИМ:
• Наличие дислипидемии (да/нет);
• Избыточная масса тела (да/нет);
• Ожирение (да/нет), степени ожирения (1-I, 2-II, 3-III);
• Величина индекса массы тела (кг/м2);
• Уровень систолического и диастолического артериального давления (АД) (мм рт. Ст.);
• Величина скорости клубочковой фильтрации (СКФ), рассчитанная по формуле CKD-EPI (мл/мин/1,73 м2);
• Снижение СКФ менее 90 мл/мин/1,73 м2 (да/нет);
• Снижение СКФ менее 60 мл/мин/1,73 м2 (да/нет);
• Нарушение систолической функции левого желудочка: фракция выброса менее 50% (да/нет);
• Выраженное нарушение систолической функции левого желудочка: фракция выброса менее 40% (да/нет);
• Гипертрофия левого желудочка (да/нет);
• Атипичная клиническая картина ИМ (да/нет);
• Глубина поражения миокарда (крупноочаговый, мелкоочаговый);
• Многососудистое поражение по данным коронароангиографии (КАГ) (да/нет);
• Стенозирующий атеросклероз ствола левой коронарной артерии (да/нет);
• Наличие осложнений острого периода (да/нет);
• Характер осложнений острого периода:
- острая левожелудочковая недостаточность (ОЛЖН) (отек легких и кардиогенный шок) (да/нет),
- аневризматическая деформация левого желудочка (ЛЖ) (да/нет),
- рецидивирующее течение ИМ (да/нет),
- нарушения ритма и проводимости сердца (да/нет);
4. Госпитализация в профильный стационар (да/нет);
5. Особенности течения 1 года после перенесенного ИМ:
• Повторный ИМ в течение 1 года после коронарной катастрофы (да/нет);
• Нарушения ритма сердца, выявленные в первый год наблюдения (да/нет);
6. Стратегия восстановления коронарного кровотока:
• Проведение медикаментозного тромболизиса в остром периоде ИМ (да/нет);
• Интервенционное и/или хирургическое восстановление коронарного кровотока в остром периоде и в течение года после индексного ИМ (да/нет);
• Фармакоинвазивная стратегия реперфузии (да/нет);
• Первичное чрескожное коронарное вмешательство (ЧKB) (да/нет);
• Восстановление коронарного кровотока любым из способов в остром периоде и в течение года после индексного ИМ (да/нет);
7. Особенности медикаментозной терапии:
• Соответствие медикаментозной терапии существующим рекомендациям (назначение четырех основных групп препаратов - антиагрегантов, бета-адреноблокаторов, ингибиторов ангиотензинпревращающего фермента (иАПФ), статинов (ABCD-терапия)) (да/нет);
• Количество назначенных при выписке жизненно необходимых препаратов (ABCD) (0, 1, 2, 3, 4);
• Назначение препаратов группы бета-адреноблокаторов в остром периоде и при выписке из стационара (да/нет);
• Назначение статинов в остром периоде и при выписке из стационара (да/нет);
• Назначение иАПФ в остром периоде и при выписке из стационара (да/нет);
• Назначение антиагрегантной терапии в остром периоде и при выписке из стационара (да/нет);
• Назначение двойной антиагрегантной терапии в остром периоде и при выписке из стационара (да/нет).
Для выявления факторов, оказывающих наиболее значимое влияние в дифференциацию групп с летальным исходом и благоприятным исходом, а также для оценки степени их воздействия был использован метод обратной пошаговой регрессии (последовательное исключения переменных, не оказывающих значимого влияния на качество математической модели). Статистическая значимость оценивалась с использованием критерия хи-квадрат. Был проведен ROC - анализ с определением площади под кривой (AUC) равной 0,774 (95% ДИ 0,728-0,820; р<0,001), найден оптимальный порог отсечения (0,4), при котором достигаются достаточно высокие цифры как чувствительности, так и специфичности метода.
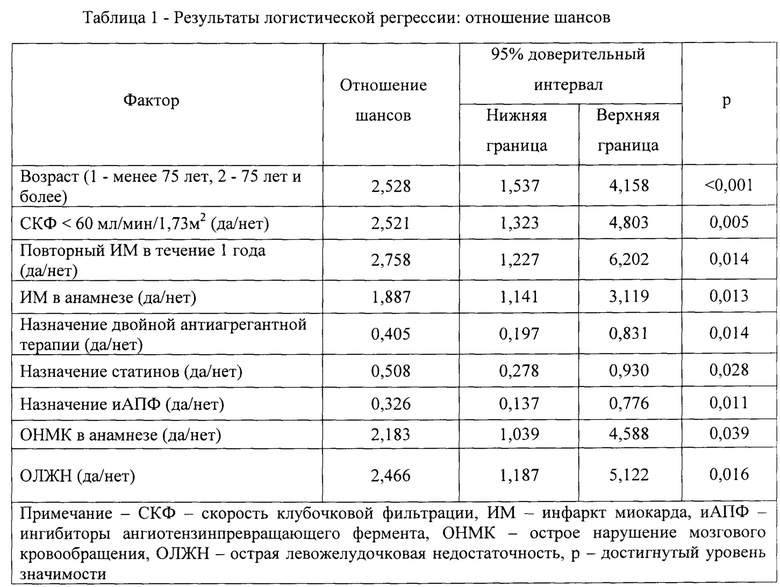
В результате пошаговой процедуры исключения факторов были определены следующие факторы, вошедшие в формулу (таблица 1):
1. Возраст на момент индексного ИМ (1 - менее 75 лет, 2-75 лет и более) (р<0,001) (да/нет);
2. Снижение СКФ менее 60 мл/мин/1,73 м2 (р=0,005) (да/нет);
3. Повторный ИМ в течение 1 года после коронарной катастрофы (р=0,014) (да/нет);
4. Перенесенный в прошлом ИМ (р=0,013) (да/нет);
5. Назначение двойной антиагрегантной терапии в остром периоде и при выписке из стационара (р=0,014) (да/нет);
6. Назначение статинов в остром периоде и при выписке из стационара (р=0,028) (да/нет);
7. Назначение иАПФ в остром периоде и при выписке из стационара (р=0,011) (да/нет);
8. ОНМК в анамнезе (р=0,039) (да/нет);
9. ОЛЖН (отек легких и кардиогенный шок) как осложнение острого периода ИМ (р=0,016) (да/нет).
Таким образом, при опросе пациента и анализе медицинской документации выясняют возраст пациента (старше 75 лет (да/нет), наличие снижения СКФ<60 мл/мин/1,73 м2, развитие повторного ИМ в течение 1 года наблюдения, наличие в анамнезе перенесенного ИМ, назначение в остром периоде и при выписке из стационара двойной антиагрегантной терапии, статинов, иАПФ, наличие в анамнезе перенесенного ОНМК, развитие в остром периоде ОЛЖН.
Вероятность летального исхода у пациентов пожилого и старческого возраста в течение пяти лет после перенесенного инфаркта миокарда рассчитывают по следующей формуле:
p=1/1+exp(-z),
где р - вероятность летального исхода;
z - значение дискриминантной функции,
а значение дискриминантной функции определяют по формуле:
Z=a+bx1+cx2+dx3+ex4+fx5+gx6+hx7+ix8+jx9,
где а - константа,
x1-x9 - значения переменных, соответствующих рассматриваемым показателям, коэффициенты b, c, d, e, f, g, h, i, j - весовые коэффициенты соответствующих показателей:
а=-0,630,
x1 - возраст пациента,
x1=l - менее 75 лет,
x1=2-75 лет и более,
b=0,927,
x2 - наличие снижения скорости клубочковой фильтрации менее 60 мл/мин/1,73 м2,
x2=1 - при снижении скорости клубочковой фильтрации менее 60 мл/мин/ 1,73 м2,
x2=0 - при скорости клубочковой фильтрации более 60 мл/мин/1,73 м2,
с=0,925,
х3 - повторный инфаркт миокарда в течение 1 года после перенесенного инфаркта миокарда,
х3=1 - при развитии повторного инфаркта миокарда в течение 1 года после перенесенного инфаркта миокарда,
х3=0 - при отсутствии повторного инфаркта миокарда в течение 1 года после перенесенного инфаркта миокарда,
d=1,015,
x4 - инфаркт миокарда в анамнезе,
x4=l - при наличии в анамнезе инфаркта миокарда,
x4=0 - при отсутствии в анамнезе инфаркта миокарда,
е=0,635,
x5 - назначение двойной антиагрегантной терапии в остром периоде инфаркта миокарда и при выписке из стационара,
х5=1 - при назначении двойной антиагрегантной терапии в остром периоде инфаркта миокарда и при выписке из стационара,
x5=0 - при отсутствии назначения двойной антиагрегантной терапии в остром периоде инфаркта миокарда и при выписке из стационара,
f=-0,905,
x6 - назначение статинов в остром периоде инфаркта миокарда и при выписке из стационара,
x6=1 - при назначении статинов в остром периоде инфаркта миокарда и при выписке из стационара,
x6=0 - при отсутствии назначения статинов в остром периоде инфаркта миокарда и при выписке из стационара,
g=-0,677,
x7 - назначение ингибиторов ангиотензинпревращающего фермента в остром периоде инфаркта миокарда и при выписке из стационара,
x7=1 - при назначении ингибиторов ангиотензинпревращающего фермента в остром периоде инфаркта миокарда и при выписке из стационара,
x7=0 - при отсутствии назначения ингибиторов ангиотензинпревращающего фермента в остром периоде инфаркта миокарда и при выписке из стационара,
h=-1,122,
x8 - острое нарушение мозгового кровообращения в анамнезе,
x8=1 - при наличии острого нарушения мозгового кровообращения в анамнезе,
x8=0 - при отсутствии острого нарушения мозгового кровообращения в анамнезе,
i=0,781,
x9 - развитие острой левожелудочковой недостаточности в остром периоде инфаркта миокарда,
x9=1 - при развитии острой левожелудочковой недостаточности в остром периоде инфаркта миокарда,
x9=0 - при отсутствии острой левожелудочковой недостаточности в остром периоде инфаркта миокарда,
j=0,902.
Полученное значение варьирует в пределах от 0 до 1. Условная граница, разделяющая больных на 2 группы (с благоприятным и неблагоприятным летальным исходом), определенная при ROC-анализе равна 0,4. Таким образом, если вероятность развития летального исхода в течение 5 лет после перенесенного ИМ менее 0,4 - предсказывается исход 0 (благоприятный), в случае если полученное значение равно или больше 0,4 - предсказывается исход 1 (неблагоприятный).
Общий процент правильно классифицированных исходов (коэффициент конкордации) - 71,5. Чувствительность модели - 64,4%, специфичность - 76,7%. Ложноположительных результатов - 23,3%, ложноотрицательных - 35,6%.
Статистическая значимость полученной модели составила: хи-квадрат=102,406, р<0,001. Качество подгонки модели хорошее (критерий Хосмер-Лемешева: хи-квадрат=1,248 р=0,990). Доля совокупной дисперсии, описываемая построенной моделью, недостаточная - R2 Найджелкерка = 0,316.
Новым в предлагаемом изобретении является выявление основных факторов, оказывающих значимое влияние на развитие летального исхода в течение пяти лет после перенесенного ИМ у пациентов пожилого и старческого возраста, формула для определения вероятности развития летального исхода в течение пяти лет после перенесенного ИМ у данной категории пациентов, конкретное значение р≥0,4, позволяющее прогнозировать летальный исход.
Полученный способ определяет совокупность факторов, оказывающих значимое влияние на исход заболевания. Благоприятно влияет на отдаленный прогноз заболевания назначение статинов, иАПФ и двойной антиагрегантной терапии во время госпитализации и при выписке из стационара. Негативное действие на исход заболевания оказывает возраст пациента старше 75 лет, снижение СКФ<60 мл/мин/1,73 м2, перенесенный в прошлом ИМ и ОНМК, повторный ИМ в течение 1 года, ОЛЖН в остром периоде ИМ (отек легких, кардиогенный шок).
Клинический пример №1
Пациентка Ю., 80 лет. Выявлены следующие факторы риска ИБС: гипертоническая болезнь, дислипидемия. В анамнезе у пациентки перенесенный ИМ. В мае 2009 г. женщина вызвала скорую медицинскую помощь в связи с затяжным ангинозным приступом, на электрокардиограмме зарегистрирован зубец Q, подъем сегмента ST, был выставлен диагноз ИМ, и больная была направлена на госпитализацию в НИИ кардиологии. Заболевание осложнилось развитием ОЛЖН. Во время госпитализации выявлено снижение СКФ до уровня 47 мл/мин/1,73 м2. Пациентке была выполнена КАГ, на которой выявлено многососудистое поражение коронарного русла, однако реваскуляризирующие процедуры не выполнялись. После выписки из стационара больная принимала кардиомагнил 75 мг/сутки, бисопролол 5 мг/сутки, фелодипин 5 мг/сутки, лизиноприл 10 мг/сутки, варфарин 2,5 мг/сутки (по поводу постоянной формы фибрилляции предсердий), аторвастатин 10 мг/сутки. Через 1 год (в мае 2010 года) пациентка перенесла повторный ИМ. При оценке риска развития летального исхода был использован разработанный способ:
z=-0,630+0,927*2+0,925*1+1,015*1+0,635*1-0,905*0-0,677*1-1,122*1-0,781*0+0,902*1, р=0,94
Поскольку полученное значение р>0,4, прогнозируется летальный исход в течение пяти лет после перенесенного ИМ. Действительно, в 2011 году пациентка скончалась от повторного ИМ.
Клинический пример №2
Пациент Б., 72 лет. Выявлены следующие факторы риска ИБС: гипертоническая болезнь, дислипидемия, курение. В марте 2008 г. мужчина вызвал скорую медицинскую помощь в связи с затяжным ангинозным приступом, на электрокардиограмме зарегистрирован зубец QS, подъем сегмента ST, отрицательный зубец Т. Больной с диагнозом острый ИМ был госпитализирован в НИИ кардиологии. Заболевание осложнилось развитием острой аневризмы левого желудочка. Во время госпитализации выявлено незначительное снижение СКФ до уровня 87 мл/мин/1,73 м2, что считается вариантом физиологической нормы у пациентов старше 60 лет. Пациенту не проводилось процедур восстановления коронарного кровотока. Лечение было консервативным, так как пациент отказался от проведения КАГ. После выписки из стационара больной принимал кардиомагнил 75 мг/сутки, клопридогрел 75 мг/сутки, бисопролол 5 мг/сутки, периндоприл 4 мг/сутки, аторвастатин 10 мл/сутки. При оценке риска развития летального исхода был использован предлагаемый в качестве изобретения способ:
z=-0,630+0,927*1+0,925*0+1,015*0+0,635*0-0,905*1-0,677*1-1,122*1-0,781*0+0,902*0, р=0,08
Таким образом, поскольку полученное значение р<0,4, прогноз заболевания на ближайшие пять лет после ИМ - благоприятный. Действительно, пациент преодолел рубеж 5-летнего наблюдения, посетив кардиолога в апреле 2013 г.
Предлагаемый в качестве изобретения способ апробирован на 410 пациентах и позволяет с высокой точностью определить вероятность летального исхода.
Список литературы
1. World Population Ageing 2013 [Electronic resource]. - Available at: ST/ESA/SER.A/348. http://www.un.org/en/development/desa/population/publications/ageing/WorldPopulationAgeing2013.shtml.
2. Гарганеева A.A., Округин С.А., Борель K.H. и соавт. Инфаркт миокарда на рубеже двух столетий: демографические и социальные тенденции // Клиническая медицина 2016; 94 (6):463-466.
3. Арьева Г.Т., Советкина Н.В., Овсянникова Н.А. и соавт. Коморбидные и мультиморбидные состояния в гериатрии (обзор) // Успехи геронтологии 2011; 24 (4): 612-619.
4. Antman, Е.М. АСС/АНА Guidelines for the Management of Patients with ST-Elevation Myocardial Infarction / Antman E.M., Anbe D.T., Armstrong P.W. et al. // Circulation 2004; 110:282-92.
5. Кужелева E.A. «Фармакоэпидемиология инфаркта миокарда и влияние приверженности лечению на течение постинфарктного периода у больных ишемической болезнью сердца» - автореферат диссертации на соискание ученой степени канд. мед. наук по специальности 14.01.05 - кардиология, Томск - 2015.
6. Борель К.Н. «Прогнозирование сердечно-сосудистых событий у пациентов трудоспособного возраста, перенесших инфаркт миокарда (по данным проспективного 5-летнего клинико-эпидемиологического исследования), автореферат диссертации на соискание ученой степени канд. мед. наук по специальности 14.01.05 - кардиология, Томск - 2015.
7. Пат. 2502464 Российская Федерация, МПК: А61В 5/02, А61В 10/00, G01N 33/48. Способ определения риска смерти в отдаленном периоде после перенесенного инфаркта миокарда / Марцевич С.Ю., Кутишенко Н.П., Гинзбург М.Л. и соавт.; заявитель и патентообладатель Государственный научно-исследовательский центр профилактической медицины, Москва - №2012135837/14; заявл. 24.08.2012; опубл. 27.12.2013, Бюл. №36.
Изобретение относится к медицине, а именно к кардиологии. Определяют возраст пациента, скорость клубочковой фильтрации, развитие повторного инфаркта миокарда в течение 1 года наблюдения. Выявляют наличие в анамнезе перенесенного инфаркта миокарда, назначение в остром периоде и при выписке из стационара двойной антиагрегантной терапии, статинов, ингибиторов ангиотензинпревращающего фермента. Выявляют наличие в анамнезе перенесенного острого нарушения мозгового кровообращения, развитие в остром периоде острой левожелудочковой недостаточности. Вероятность летального исхода (р) определяют по заявленной формуле. При значении р больше или равно 0,4 прогнозируют летальный исход в течение пяти лет постинфарктного периода. Способ позволяет с высокой точностью прогнозировать летальный исход у пациентов пожилого и старческого возраста в течение пяти лет после перенесенного инфаркта миокарда за счет оценки комплекса наиболее значимых показателей. 1 табл., 2 пр.
Способ прогнозирования летального исхода у пациентов пожилого и старческого возраста в течение пяти лет после перенесенного инфаркта миокарда характеризуется тем, что определяют факторы: возраст пациента 75 лет и старше, наличие снижения скорости клубочковой фильтрации менее 60 мл/мин/1,73 м2, развитие повторного инфаркта миокарда в течение 1 года наблюдения, наличие в анамнезе перенесенного инфаркта миокарда, назначение в остром периоде и при выписке из стационара двойной антиагрегантной терапии, статинов, ингибиторов ангиотензинпревращающего фермента, наличие в анамнезе перенесенного острого нарушения мозгового кровообращения, развитие в остром периоде острой левожелудочковой недостаточности и вероятность летального исхода определяют по формуле:
p=1/1+exp(-z),
где р - вероятность летального исхода;
z - значение дискриминантной функции,
а значение дискриминантной функции определяют по формуле:
z=a+bx1+cx2+dx3+ex4+fx5+gx6+hx7+ix8+jx9,
где а - константа,
x1-x9 - значения переменных, соответствующих рассматриваемым показателям,
коэффициенты b, c, d, e, f, g, h, i, j - весовые коэффициенты соответствующих показателей:
а=-0,630,
x1 - возраст пациента,
x1=1 - менее 75 лет,
x1=2 - 75 лет и более,
b=0,927,
x2 - наличие снижения скорости клубочковой фильтрации менее 60 мл/мин/1,73 м2,
x2=1 - при снижении скорости клубочковой фильтрации менее 60 мл/мин/1,73 м2,
x2=0 - при скорости клубочковой фильтрации более 60 мл/мин/1,73 м2,
с=0,925,
x3 - повторный инфаркт миокарда в течение 1 года после перенесенного инфаркта миокарда,
x3=1 - при развитии повторного инфаркта миокарда в течение 1 года после перенесенного инфаркта миокарда,
х3=0 - при отсутствии повторного инфаркта миокарда в течение 1 года после перенесенного инфаркта миокарда,
d=1,015,
x4 - инфаркт миокарда в анамнезе,
x4=1 - при наличии в анамнезе инфаркта миокарда,
x4=0 - при отсутствии в анамнезе инфаркта миокарда,
е=0,635,
x5 - назначение двойной антиагрегантной терапии в остром периоде инфаркта миокарда и при выписке из стационара,
x5=1 - при назначении двойной антиагрегантной терапии в остром периоде инфаркта миокарда и при выписке из стационара,
x5=0 - при отсутствии назначения двойной антиагрегантной терапии в остром периоде инфаркта миокарда и при выписке из стационара,
f=-0,905,
x6 - назначение статинов в остром периоде инфаркта миокарда и при выписке из стационара,
x6=1 - при назначении статинов в остром периоде инфаркта миокарда и при выписке из стационара,
x6=0 - при отсутствии назначения статинов в остром периоде инфаркта миокарда и при выписке из стационара,
g=-0,677,
x7 - назначение ингибиторов ангиотензинпревращающего фермента в остром периоде инфаркта миокарда и при выписке из стационара,
x7=1 - при назначении ингибиторов ангиотензинпревращающего фермента в остром периоде инфаркта миокарда и при выписке из стационара,
x7=0 - при отсутствии назначения ингибиторов ангиотензинпревращающего фермента в остром периоде инфаркта миокарда и при выписке из стационара,
h=-1,122,
x8 - острое нарушение мозгового кровообращения в анамнезе,
x8=1 - при наличии острого нарушения мозгового кровообращения в анамнезе,
х8=0 - при отсутствии острого нарушения мозгового кровообращения в анамнезе,
i=0,781,
x9 - развитие острой левожелудочковой недостаточности в остром периоде инфаркта миокарда,
x9=1 - при развитии острой левожелудочковой недостаточности в остром периоде инфаркта миокарда,
x9=0 - при отсутствии острой левожелудочковой недостаточности в остром периоде инфаркта миокарда,
j=0,902,
и при значении р более или равно 0,4 прогнозируют летальный исход в течение пяти лет постинфарктного периода.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЛЕТАЛЬНОГО ИСХОДА В ТЕЧЕНИЕ ПЯТИ ЛЕТ ПОСЛЕ ПЕРЕНЕСЕННОГО ИНФАРКТА МИОКАРДА | 2015 |
|
RU2590869C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА ЗАБОЛЕВАНИЯ У БОЛЬНЫХ ПОЖИЛОГО И СТАРЧЕСКОГО ВОЗРАСТА С СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2007 |
|
RU2353933C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА ЛЕТАЛЬНОГО ИСХОДА ИНФАРКТА МИОКАРДА | 2008 |
|
RU2406091C2 |
| УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОЙ ОСТАНОВКИ ГИЛЬЗОВОЙ МАШИНЫ | 1950 |
|
SU92081A1 |
| БОРЕЛЬ К.Н | |||
| Прогнозирование сердечно-сосудистых событий у пациентов трудоспособного возраста, перенесших инфаркт миокарда (по данным проспективного 5-летнего клинико-эпидемиологического исследования) | |||
| Дисс | |||
| на соиск | |||
| уч | |||
| ст | |||
| к.м.н | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| AENGUS MURPHY C | |||
| Declining renal function after myocardial infarction predicts poorer long-term outcome | |||
| Eur J Cardiovasc Prev Rehabil | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
Авторы
Даты
2018-06-28—Публикация
2017-06-26—Подача