Изобретение относится к области медицины, а именно к кардиологии, терапии, и может быть использовано для прогнозирования острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST левого желудочка на стационарном этапе лечения.
По данным клинических исследований пациенты с инфарктом миокарда с подъемом сегмента ST (ИМпST) имеют худший краткосрочный прогноз по сравнению с инфарктом миокарда без подъема сегмента ST (ИМбпST) (Park Н. W., Yoon С.Н., Kang S. Н., et al. Early- and late-term clinical outcome and their predictors in patients with ST-segment elevation myocardial infarction and non-ST-segment elevation myocardial infarction. International Journal of Cardiology. 2013;169(4):254-261. doi: 10.1016/j.ijcard.2013.08.132.).
Одной из основных причин осложнений инфаркта миокарда (ИМ) в динамике госпитального лечения является острая сердечная недостаточность (ОСИ). Актуальным является изучение острой сердечной недостаточности при остром инфаркте миокарда (ОИМ): частота развития, клиническая и гемодинамическая характеристики, факторы, влияющие на течение и прогноз, современные подходы к лечению (Хирманов В.Н., Павлыш Е.Ф. Острая сердечная недостаточность: определение понятия, стратификация риска, классификация, формулировка диагноза // Клиническая фармакология и терапия. - 2020. - №29 (2). - С. 5-11).
Пациенты с ОСН нуждаются в срочном обследовании с последующим началом или усилением лечения, в т.ч. внутривенной терапии или процедур. Диагностическое обследование ОСН начинается с момента осмотра пациента на догоспитальном этапе врачом поликлиники или скорой медицинской помощи и продолжается в стационаре с целью выявления клинических проявлений, а также диагностики и лечения. Острая левожелудочковая недостаточность включает отек легких и кардиогенный шок, что соответствует классификации ОСН Killip III и IV классов соответственно (2021 Рекомендации ESC по диагностике и лечению острой и хронической сердечной недостаточности. Российский кардиологический журнал. 2023;28(1):5168. doi:10.15 829/1560-4071-2023-5168).
Благодаря тому, что способы диагностики и лечения в терапии и кардиологии постоянно совершенствуются, становится возможным прогнозирование риска развития острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST левого желудочка на стационарном этапе лечения.
В настоящее время изучена госпитальная летальность пациентов с ИМпST и ИМбпST с учетом клинической характеристики. Общая госпитальная летальность пациентов ОИМ составила 6,4%, при этом для ИМпST была выше 4,2%, чем при ИМбпST 2,2%. Пациенты с ИМпST чаще имели хроническую болезнь почек, хроническую сердечную недостаточность, кардиогенный шок, частые осложнения, низкую фракцию выброса (ФВ) левого желудочка (ЛЖ) по эхокардиографии (ЭХОКГ), чем в группе ИМбпST. Согласно полученным результатам, среди молодых и пациентов среднего возраста часто встречался ИМпST - 35,5%, тогда как ИМбпST встречался у пожилых и пациентов старческого возраста. Таким образом, авторы отмечают высокую летальность пациентов ИМпST в стационаре, клинические особенности, осложнения связаны с развитием кардиогенного шока и критериями низкой ФВ по данным ЭХОКГ (Кедельбаева К.М., Дуйсенова Ж.Б., Самитова С.Б. и соавт. Особенности клинической характеристики острого инфаркта миокарда в условиях профильного стационара г Алматы: ретроспективное исследование // Клиническая медицина и фармакология. Февраль, №1 (246), С 75-82. 2023) анализировалась.
Однако авторы исследования не предлагают методы ранней диагностики или прогнозирования осложнений у пациентов ИМпST в условиях стационара.
Изучено прогнозирование развития сердечно-сосудистых осложнений у пациентов с ОИМ на основании шкалы GRACE 2.0. Выявлено, что с развитие осложнений в течение года после ОИМ связаны с возрастом, развитием ОСН III и IV классов классификации Killip при поступлении, консервативной тактикой лечения, наличием в брахиоцефальных артериях нестабильных атеросклеротических бляшек или стеноза от 50% и более по данным ультразвукового исследования, повышением концентраций сосудистого эндотелиального фактора роста и стимулирующего фактора роста. Включение данных показателей в прогностическую модель увеличивает диагностическую ценность шкалы GRACE 2.0 при определении годичного прогноза (Салатова Л.Н. Прогнозирование развития сердечно-сосудистых осложнений у пациентов с инфарктом миокарда (клинико-морфологическое исследование). // Автореферат диссертации на соискание ученой степени кандидата медицинских наук. - Самара, 2017. - 23 с).
Общими недостатками этих способов прогнозирования сердечно-сосудистых осложнений у пациентов в остром периоде ИМ являются:
- сложность технического исполнения;
- большое количество биохимических исследований;
- необходимость использования дорогостоящих реактивов;
- неоднозначность полученных результатов.
Известен способ, прогностической значимости уровня фракталкин (ФКН) у пациентов с ОИМ после проведенного чрескожного коронарного вмешательства (ЧКВ). Согласно данному аналогу установлено, что у пациентов с ОИМ после ЧКВ высокий уровень ФКН является достоверным прогностическим маркером неблагоприятных сердечно-сосудистых событий (Хи В., Qian Y., Zhao Y., Fang Z., Tang K., Zhou N., Li D., Wang J. Prognostic value of fractalkine/CX3CL1 concentration in patients with acute myocardial infarction treated with primary percutaneous coronary intervention // Cytokine. - 2019. - 113. - P. 365-370.).
Недостатками указанного аналога являются то, что он не может быть использован для прогнозирования риска развития острой левожелудочковой недостаточности у пациентов в ОИМ вследствие:
- изучения уровня ФКН у пациентов с ОИМ только после ЧКВ;
- отсутствия алгоритма прогнозирования риска развития острой левожелудочковой недостаточности;
- сложности технического исполнения.
Известен способ прогнозирования риска отдаленных фатальных сердечных и цереброваскулярных событий путем определения таких исходных перед ЧКВ клинических характеристик пациента: исходный уровень глюкозы в крови натощак, функциональный класс недостаточности кровообращения по NYHA перед ЧКВ, наличие или отсутствие исходно сопутствующей фибрилляции предсердий, а также двух показателей, которые должны быть оценены через 1 год после вмешательства: уровень креатинина в крови и скорость клубочковой фильтрации (СКФ), рассчитанная по формуле CKD-EPI, и вероятность развития отдаленных фатальных сердечно-сосудистых событий после ЧКВ определяют по формуле: P=eF/(1+eF),
где Р - вероятность развития фатальных сердечно-сосудистых событий в течение 6 лет после ЧКВ;
е - основание натурального логарифма (е=2,7183);
F - расчетное значение функции, равное
F(x)=b0+b1⋅х1+b2⋅х2+b3⋅х3+b4⋅х4+b5⋅х5, где
x1 - уровень сывороточного креатинина через 1 год после ЧКВ, мкмоль/л;
x2 - исходный уровень глюкозы в крови натощак, ммоль/л;
x3 - СКФ через 1 год после ЧКВ, рассчитанная по формуле CKD-EPI, мл/мин/1,73 м2;
x4 - функциональный класс недостаточности кровообращения по классификации NYHA перед ЧКВ;
x5 - исходное наличие у пациента фибрилляции предсердий: 2 - нет; 1 - да;
b0 - свободный член уравнения, константа (b0=-18,534);
b1, b2, b3, b4, b5 представляют собой коэффициенты и имеют следующие значения: b1=0,132; b2=-2,621; b3=0,339; b4=-2,887; b5=3,763,
и при значении Р<0,71 прогнозируют высокий риск развития фатальных сердечно-сосудистых и цереброваскулярных событий в течение 6 лет после плановых чрескожных коронарных вмешательств, а при значении Р>0,71 течение заболевания после эндоваскулярного вмешательства на коронарных артериях благоприятное (патент РФ №2 683 691, Опубликовано: 01.04.2019).
Недостатки данного способа в том, что прогноз осуществляется только для пациентов после ЧКВ, не определяется прогноз развития осложнений на стационарном этапе лечения, не используются параметры сократительной функции миокарда по данным ЭХОКГ.
Известен способ прогнозирования ургентных сердечно-сосудистых осложнений при остром коронарном синдроме (ОКС) у больных с онкологическим заболеванием в анамнезе, включающий подсчет баллов по шкале GRACE при поступлении, определение содержания NT-proBNP (пг/мл) в крови в 1-е сутки госпитализации, отличающийся тем, что у больных острым коронарным синдромом с онкологическим заболеванием в анамнезе определяют суммарный показатель «ОЗ.GRACE - NT-proBNP» путем подставления полученных числовых значений в уравнение логистической регрессии ОЗ. GRACE - NT-proBNP=-8,87992+(0,048438 × баллы по шкале GRACE)+(0,0031794 × величина NT-proBNP (пг/мл)), и при величине показателя «ОЗ.GRACE - NT-proBNP» более -0,1667 прогнозируют возможное развитие ургентных сердечно-сосудистых осложнений в госпитальном периоде при ОКС у больных с онкологическим заболеванием в анамнезе (патент РФ№2 741 195, Опубликовано: 22.01.2021).
Недостатки данного способа в том, что определяется прогноз только у онкологических больных, авторы не разделяют пациентов на группы ОКС с подъемом сегмента ST и ОКС без подъема сегмента ST.
Наиболее близким к заявленному техническому решению является способ прогнозирования риска развития острой левожелудочковой недостаточности в виде кардиогенного шока или отека легких у пациентов с острым коронарным синдромом в сочетании с синдромом недифференцированной дисплазии соединительной ткани (СНДСТ) на основе определения в сыворотке крови лабораторных показателей, отличающийся тем, что для прогнозирования кардиогенного шока или отека легких у пациентов с острым коронарным синдромом в сочетании с синдромом недифференцированной дисплазии соединительной ткани определяют уровень гомоцистеина и магния методом иммуноферментного анализа и рассчитывают вероятность развития кардиогенного шока или отека легких в течение последующих 7 дней по формуле:
Р=1/(1+e-z), где:
Р - вероятность развития предполагаемого исхода развития острой левожелудочковой недостаточности в виде кардиогенного шока или отека легких у пациентов с ОКС в сочетании с СНДСТ;
е - число Эйлера (константа), равное 2,71828;
z=26,588-0,121×ГЦ-45,165×МГ, где:
-0,121 - коэффициент первой переменной,
ГЦ - уровень гомоцистеина, мкмоль/л,
-45,165 - коэффициент второй переменной,
МГ - уровень магния, ммоль/л,
26,588 - константа;
и при р<0,5 прогнозируют низкий риск развития кардиогенного шока или отека легких, а при р≥0,5 прогнозируют высокий риск развития кардиогенного шока или отека легких (патент РФ№2782490, опубл. 28.10.2022).
Недостатками данного технического решения является, то, что он используется только для пациентов с синдромом недифференцированной дисплазии соединительной ткани, не учитываются возрастной критерий и параметры ЭХОКГ, позволяющие определить нарушения систолической функции миокарда ЛЖ в прогнозе кардиогенного шока или отека легких.
Учитывая все вышеизложенное необходимы дальнейшие разработки предикторов прогрессирования острой левожелудочковой недостаточности у пациентов ИМпST, которые позволили бы использовать не инвазивные и рациональные методы прогнозирования риска кардиогенного шока и отека легких. Создание способа, предназначенного для прогнозирования острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка на стационарном этапе лечения, является важной научно-медицинской задачей.
Задача изобретения - разработать достоверный способ прогнозирования острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка на стационарном этапе лечения.
Поставленная задача решается тем, что способ прогнозирования острой левожелудочковой недостаточности у пациентов с острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка включает на стационарном этапе исследование в сыворотке крови уровня стимулирующего фактора роста экспрессируемый геном 2, определяют размер левого предсердия, фракции выброса по данным эхокардиографии, количество баллов по шкале GRACE, скорость клубочной фильтрации, возраст пациента и рассчитывают вероятность развития острой левожелудочковой недостаточности по формуле:
Р=1/(1+e-z)×100%, где
Р - вероятность развития острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка;
е - число Эйлера (константа) равное 2,71828,
z=-40,529+0,001X1+0,403Х2-0,050Х3+0,204Х4+0,017Х5-0,223Х6, где
X1 - уровень стимулирующего фактора роста, экспрессируемый геном 2 в крови при госпитализации в первые сутки ИМпST в нг/мл;
Х2 - размер левого предсердия по данным эхокардиографии, мм;
Х3 - фракция выброса левого желудочка по данным эхокардиографии, %;
Х4 - количество баллов по шкале госпитальной летальности GRACE, в баллах;
Х5 - показатель скорости клубочной фильтрации CKD-EPI, мл/мин/ 1,73 м2;
Х6 - возраст пациента, лет,
и при Р≥0,469 прогнозируют высокий риск развития острой левожелудочковой недостаточности, а при Р<0,469 прогнозируют низкий риск развития острой левожелудочковой недостаточности.
Заявляемый способ прогнозирования острой левожелудочковой недостаточности у пациентов с острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка обладает высокой точностью и достоверностью. Его использование в клинике поможет обоснованно подобрать объем профилактических и лечебных мероприятий у пациентов с ИМпST передней стенки левого желудочка, снизить риск развития острой левожелудочковой недостаточности.
Новым в предлагаемом изобретении является выявление прогностических факторов, оказывающих значимое влияние развитие острой левожелудочковой недостаточности у пациентов ИМпST с помощью, разработанной нами формулы для определения вероятности развития осложнения в течение стационарного этапа лечения у данной категории пациентов.
Для улучшения прогноза пациентов с ИМпST необходимо изучение дополнительных маркеров, в том числе и лабораторных биомаркеров, с наибольшей прогностической значимостью.
Заявляемый способ определяет совокупность факторов, оказывающих значимое влияние развитие острой левожелудочковой недостаточности у пациентов ИМпST на стационарном этапе лечения. Весомое негативное действие на острую левожелудочковую недостаточность у больных ИМпST оказывают увеличение размеров левого предсердия (мм) по данным эхокардиографии, увеличение количества баллов по шкале GRACE (баллы) и возраст пациентов (лет).
Предпосылками для выбора и использования параметров, оказывающих влияние на вероятность развития острой левожелудочковой недостаточности, послужили наши многочисленные исследования, в ходе которых удалось выделить статистически значимые факторы.
ST2 (Growth STimulation expressed gene 2, СТимулирующий фактор роста, экспрессируемый геном 2, так же известный как IL1RL1) - член семейства рецепторов интерлейкина-1 (IL-1). Это новейший маркер, использующийся для прогнозирования и стратификации риска развития сердечной недостаточности (СН), прогнозирования неблагоприятных исходов и смерти пациентов с подтвержденным диагнозом СН, развития сердечно-сосудистых заболеваний (ССЗ) в будущем в популяции в целом, а также для мониторинга и подбора наиболее эффективной терапии больных СН. ST2 экспрессируется в сердце в ответ на патологические изменения, вызванные хроническими заболеваниями и/или острыми повреждениями. Он отражает ремоделирование желудочков и фиброз сердца.
Установлено, что ST2 является предиктором сердечной недостаточности и смерти у пациентов с HMnST, надежным биомаркером риск-стратификации пациентов с СН (Yu J, Oh PC, Kim M, et al. Improved early risk stratification of patients with ST-segment elevation myocardial infarction undergoing primary percutaneous coronary intervention using a combination of serum soluble ST2 and NT-proBNP. PLoS One 2017; 12 (8):e0182829; DOI: 10.1371/journal.pone.0182829.)
Осложнения госпитального периода ИМ ассоциируются с более высоким содержанием ST2. Повышенное содержание ST2 в сыворотке крови сопровождается развитием дезадаптивного варианта ремоделирования сердца (Дылева Ю.А., Учасова Е.Г., Груздева О.В., Федорова Н.В., Кашталап В.В. Клинико-диагностическое значение стимулирующего фактора проста для оценки ранних осложнений инфаркт миокарда. Сибирский медицинский журнал, 2016, Том 31, №1, 27-31).
По данным Хоролец Е.В., Хаишева Л.А., Шлык СВ. (2017) у пациентов ИМпST уровень стимулирующего фактора роста, экспрессируемый геном 2 (ST2) является прогностическим маркером прогрессирования ОСН. Больные с уровнем ST2≥35 нг/мл имеют наиболее неблагоприятный прогноз развития сердечной недостаточности (Хоролец Е.В., Хаишева Л.А., Шлык С.В. Показатели NT-prpBNP и ST2 у пациентов с острым инфарктом миокарда с подъемом сегмента ST. Атеросклероз 2017. Т. 13. №7.18-24).
У пациентов ОИМ метод ЭХОКГ входит в стандарт оказания медицинской помощи (Стандарт оказания медицинской помощи взрослым при остром инфаркте миокарда с подъемом сегмента ST электрокардиограммы (диагностика, лечение и диспансерное наблюдение. Приказ МЗ РФ №612n от 10.06.2021.)).http://rkdb.ru/wp-content/uploads/2021/07/LAW390019_0_20210614_131306_57070.pdf).
Рекомендуется выполнение ЭХОКГ у пациентов ИМпST для подтверждения диагноза, оценки тяжести и определения прогноза в первые сутки заболевания. Необходимо определение фракции выброса ЛЖ (ФВ ЛЖ), патологии колебания стенок, функции правого желудочка, наличии клапанных пороков сердца и нагрузки объемом. Связанные с ОИМ проявления СН, острой тяжелой митральной регургитации, механические осложнения являются основными провоцирующими причинами развития кардиогенного шока (Клинические рекомендации ИМпST электрокардиограммы. 2020). Изменения размеров камер сердца, расчетных показателей систолической функции при ИМпST выявляются в первые сутки заболевания с дальнейшим ремоделированием миокарда.
По ЭХОКГ в первый день ОИМ имеет значимость ФВ ЛЖ для оценки прогноза заболевания (Moller J.E., Hillis G.S., Oh J.K., et al., 2006) и является предиктором общей смертности в течение девятнадцати месяцев наблюдения пациентов.
Снижение сократительной функции миокарда за счет повреждения миокарда, дилатации ЛЖ приводит к формированию низкой ФВ ЛЖ. Большая зона ОИМ, рубцовые изменения миокарда является следствием увеличением размеров ЛЖ. В прогнозе пациентов ОИМ доказана значимость других параметров ЭХОКГ. Авторы White H.D., et al. (1987) утверждают, что конечно-систолический (КСО) и конечно-диастолический объемы (КДО) ЛЖ являются предикторами прогноза, а не ФВ ЛЖ.
В кардиологической практике широко используются шкалы прогноза пациентов в течение госпитального этапа лечения и зависят от ряда параметров.
Среди известных шкал прогноза пациентов ОИМ, шкала риска GRACE (Global Registryof Acute Coronary Events, https://cardiograf.com/kalkulyator/grace.html), предлагает наилучшие дискриминативные характеристики.
Шкала GRACE 2,0 является общепринятой с возможностью оценки прогноза госпитальной летальности по критериям используемых в реальной клинической практике. В качестве факторов риска шкала GRACE 2.0 учитывает возраст, класс Killip, показатели гемодинамики, уровень креатинина, наличие нарушения проводимости, повышения уровня кардиоспецифических ферментов и элевацию сегмента ST на электрокардиограмме при поступлении пациента в клинику.
Это наиболее информативная модель, позволяющая оценить риск смерти и повторного ИМ как в период госпитализации, так и на протяжении ближайших 6 месяцев и в более отдаленные периоды.
GRACE 2.0 применима для всех больных вне зависимости от метода реперфузии миокарда и рекомендуется к использованию в клинических рекомендациях по ведению больных с ИМ. Она позволяет оценить риск летальности на госпитальном этапе и в течение последующих шести месяцев, 1 и 3 лет и определить оптимальный способ лечения пациента. https://www.outcomes-umassmed.org/grace/acs_risk2/index.html
Нарушение функции почек является распространенной проблемой среди пациентов, перенесших ОИМ, что ухудшает госпитальный и отдаленный прогнозы. Средние показатели скорости клубочковой фильтрации (СКФ) у больных с ИМ ниже, чем у больных с нестабильной стенокардией, что говорит о снижении функции почек. (Балашкевич Н.А., Дюсенова Л.Б., Жетписбаев Б.А., Казымов М.С., Избасарова И.А., Боровикова О.А.3, Шалгумбаева Г.М. Сравнительная оценка функционального состояния почек у лиц, перенесших острый коронарный синдром Российский кардиологический журнал. 2019;24(3):48-53 http://dx.doi.org/10.15829/1560-4071-2019-3-48-53).
Методом расчета СКФ была рекомендованная в настоящее время для пациентов формула CKD-EPI которая имеет минимальные отличия от измеренной «золотым методом» СКФ (Chronic Kidney Desease Epidemiology Collaboration) - новая формула для оценки СКФ (Andrew S. Levey, Lesley A. Stevens, Christopher H. Schmid et al, «A New Equation to Estimate Glomerular Filtration Rate», Ann Intern Med. 2009 May 5; 150 (9):604-12).
Для расчета СКФ по формуле CKD-EPI можно воспользоваться калькуляторами, представленными в интернете (http://www.kidney.org/professionals/kdoqi/gfr_calculator.cfm http://nkdep.nih.gov/professionals/gfr_calculators/index.htm), специальными приложениями для мобильных устройств (QxMDCalculator).
Тяжелая почечная дисфункция является независимым фактором риска развития сердечно-сосудистых осложнений и ассоциируется с неблагоприятным прогнозом (Liu Y., Gao L., Xue Q., et al. Impact of renal dysfunction on long-term outcomes of elderly patients with acute coronary syndrome: a longitudinal, prospective observational study. BMC Nephrology. 2014; 15:78. http:www.biomedcentral.com/1471-2369/15/78).
Возраст вносит свой вклад в прогноз пациентов ОИМ, контроль ряда факторов в остром периоде ИМ отражают влияние на течение заболевания. Установлено, что ишемическая болезнь сердца (ИБС) и ОИМ в частности являются доминирующими причинами смерти и инвалидности для пожилых людей. Удельный вес пациентов старших возрастных групп в структуре больных ОИМ составляет более 60% (Гарганеева А.А., Округин С.А., Борель К.Н. и соавт. Инфаркт миокарда на рубеже двух столетий: демографические и социальные тенденции // Клиническая медицина 2016; 94 (6):463-466).
Разработаны программы прогнозирования неблагоприятных сердечно-сосудистых событий у пациентов пожилого и старческого возраста в течение пяти лет после перенесенного ИМ характеризующиеся тем, что определяют основные факторы: наличие снижения СКФ<60 мл/мин/1,73 м2, определяемое во время госпитализации по поводу ИМ, наличие хронической сердечной недостаточности в анамнезе II А стадии и выше, наличие осложнений острого периода ИМ, регулярность амбулаторного наблюдения после перенесенного ИМ, и вероятность развития неблагоприятных сердечно-сосудистых событий (Свидетельство о государственной регистрации программы для ЭВМ 2691617, 28.03.2018). Таким образом, возраст является одним из не корригируемым фактором риска сердечно-сосудистых заболеваний и определяет прогноз пациентов как на госпитальном, так и на амбулаторном этапах наблюдения пациентов после ИМпST.
Подробное описание способа и примеры его клинического выполнения
У пациентов, госпитализированных с ОИМ в кардиологическое отделение в первые сутки заболевания, постановка диагноза и лечение ОИМ осуществлялось согласно клиническим рекомендациям «4-е Универсальное определение инфаркта миокарда, 2019 г».
Для определения уровня исследуемых для прогнозирования острой левожелудочковой недостаточности маркеров у пациента утром натощак производили забор крови из вены 10,0 мл. Плазму выделяли путем центрифугирования и помещали в силиконовые пробирки. Образцы замораживали и доставляли в специальном холодильнике, где хранили при t=-70°C до проведения анализа. Уровень стимулирующего фактора роста, экспрессирующийся геном 2 (ST2) определяли в плазме крови иммуноферментным методом (с помощью тест-систем фирмы Presage ST2 Assay Critical Diagnostics, UC).
Вносили показатель X1.
На ультразвуковом аппарате Samsung Medison Ugeo Н60 выполняли ЭХОКГ исследования пациентам. Исследование проводилось в положении пациента на левом боку с незначительно приподнятой верхней половиной туловища. Определяли в В-режиме значения: размер левого предсердия (ЛП) (мм); конечный диастолический объем левого желудочка (КДО ЛЖ), конечный систолический объем левого желудочка (КСО ЛЖ). Фракция выброса левого желудочка (ФВ ЛЖ) (%) по Симпсону является расчетным показателем: ФВ ЛЖ = (КДО ЛЖ - КСО ЛЖ)/КДО ЛЖ, где КДО ЛЖ - конечный диастолический объем левого желудочка, КСО ЛЖ - конечный систолический объем левого желудочка.
Вносили показатели Х2 и Х3 соответственно.
Расчет баллов по шкале по шкале госпитальной летальности GRACE проводили данным таблиц в формате онлайн калькулятора https://www.outcomes-umassmed.org/grace/acs_risk2/index.html.
Вносили показатель Х4.
Показатель скорости клубочной фильтрации (СКФ) определяли онлайн калькулятором https://www.cardioneurology.ru/skf/.
СКФ рассчитывали по формуле CKD-EPI (мл/мин/ 1,73 м2) (Chronic Kidney Disease Epidemiology Collaboration с учетом пола, возраста, расы, уровня креатинина крови. Формула CKD-EPI:
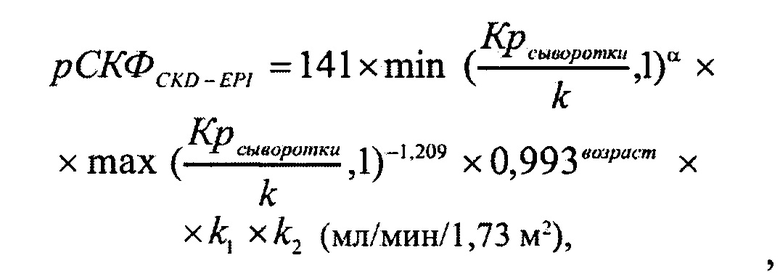
где 141 - коэффициент, учитывающий среднюю площадь поверхности тела (ППТ) и корректировку по референсному IDMS-методу; k - пороговое значение креатинина сыворотки, математически разделяющее здоровых индивидов и пациентов с хронической болезнью почек: 0,7, если женщина; 0,9, если мужчина (мг/дл); min - оставляется данное отношение, если значение креатинина в сыворотке пациента меньше порогового значения k; либо 1, если значение креатинина в сыворотке пациента больше порогового значения k; max - оставляется данное отношение, если значение креатинина в сыворотке пациента больше порогового значения k; либо 1, если значение креатинина в сыворотке пациента меньше порогового значения k; α - степень: - 0,329, если женщина; - 0,411, если мужчина; возраст - возраст (годы); k1 - поправка на пол пациента: 1,018, если женщина; 1, если мужчина; k2 - поправка на расу пациента: 1,159, если афроамериканцы; 1, если не афроамериканцы; Крсыворотки - концентрация креатинина в сыворотке (мг/дл); (возможно перевести значения концентрации креатинина из мкмоль/л в мг/дл, полученный результат в мкмоль/л необходимо разделить на 88,4).
Определение креатинина крови - это лабораторный метод исследования, который применяют для оценки функции почек. Проводили забор венозной 6,0 мл крови. Значения креатина в крови определяли кинетическим методом (метод Яффе) (мкмоль/л). Затем использовали уровень креатинина в формуле CKD-EPI для оценки СКФ. Предложенное уравнение CKD-EPI позволяет получить адекватные расчетные значения СКФ у здоровых людей, в также улучшить оценку риска развития ССЗ при хронической болезни почек.
Вносили показатель Х5.
Вносили показатель Х6 - возраст пациента в полных годах на момент развития ИМпST.
Указанные показатели в абсолютных величинах подставляют в формулу расчета z. После этого рассчитывали вероятность развития острой левожелудочковой недостаточности по формуле:
Р=1/(1+e-z)×100%, где
Р - вероятность развития острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка;
е - число Эйлера (константа), равное 2,71828;
z=-40,529+0,001X1+0,403Х2-0,050Х3+0,204Х4+0,017Х5-0,223Х6, где
X1 - уровень стимулирующего фактора роста, экспрессируемый геном 2 в крови при госпитализации в первые сутки ИМпST в нг/мл;
Х2 - размер левого предсердия по данным эхокардиографии, мм;
Х3 - фракция выброса левого желудочка по данным эхокардиографии, %;
Х4 - количество баллов по шкале госпитальной летальности GRACE, в баллах;
Х5 - показатель скорости клубочной фильтрации CKD-EPI, мл/мин/ 1,73 м2;
Х6 - возраст пациента, лет,
и при Р≥0,469 прогнозируют высокий риск развития острой левожелудочковой недостаточности, а при Р<0,469 прогнозируют низкий риск развития острой левожелудочковой недостаточности.
Работоспособность заявляемого способа подтверждается следующими клиническими примерами:
Пример 1.
Пациент А-ев, 73 лет, госпитализирован в кардиологическое отделение с диагнозом: ИБС. Инфаркт миокарда с подъемом сегмента передней стенки ЛЖ. ОСН Killip I. Артериальная гипертензия III ст. 2 степени, риск 4. При поступлении пациент предъявлял жалобы на боль за грудиной давящего характера длительностью более 40 минут, общая слабость, потливость.
Объективные данные: состояние тяжелое. Сознание ясное. Положение активное. Телосложение: нормостеническое. Кожные покровы умеренно бледной окраски, нормальной влажности. Лимфатические узлы не увеличены. Опорно-двигательный аппарат не изменен, тонус и сила мышц не нарушены. Периферических отеков нет. При перкуссии легочный звук над всей поверхностью легких. В легких дыхание везикулярное, хрипов нет, частота дыхательных движений (ЧДД) 18 в мин. Границы относительной сердечной тупости расширены влево до левой срединно-ключичной линии. Тоны сердца приглушены, ритмичные, частота сердечных сокращений (ЧСС) 50 в мин., артериальное давление (АД) 120/70 мм рт. ст. Живот мягкий, при пальпации безболезненный, печень не увеличена. Мочеиспускание без особенностей. Симптом поколачивания отрицательный.
Лабораторные исследования. Общий анализ крови: эритроциты 3,91×1012/л, гемоглобин 114 г/л, лейкоциты (л) 4,44×109/л, тромбоциты - 152×109/л, скорость оседания эритроцитов (СОЭ) 11 мм/ час. Биохимический анализ крови: глюкоза 4,4 ммоль/л, общий холестерин (ХС) 8,0 ммоль/л, ХС липопротеины низкой плотности (ЛПНП) 4,0 ммоль/л, ХС липопротеины высокой плотности (ЛПВП) 1,5 ммоль/л, триглицериды 3,24 ммоль/л.
Электрокардиография. Ритм синусовый, правильный. ЧСС=60 ударов в минуту. Инфаркт миокарда с подъемом сегмента ST передней стенки ЛЖ, острая стадия. Рентгенография органов грудной клетки (в прямой проекции): в легких - без видимых очаговых и инфильтративных теней. Легочный рисунок склеротически изменен. Корни структурны, уплотнены. Синусы свободны, диафрагма ровная. Сердце умеренно расширено в поперечнике, за счет ЛЖ, аорта уплотнена.
Для прогнозирования развития острой левожелудочковой недостаточности у пациента в первые сутки инфаркта миокарда определяли: уровень X1 - уровень стимулирующего фактора роста ST2=123,9 нг/мл; Х2 - размер левого предсердия по данным ЭХОКГ=50 мм, по данным ЭХОКГ; Х3 - фракция выброса левого желудочка по данным ЭХОКГ=43%, по шкале GRACE рассчитывали Х4 - количество баллов - 200; Х5 - показатель скорости клубочной фильтрации CKD-EPI=48 мл/мин/1,73 м2; Х6 - возраст пациента - 73 лет.
Подставили полученные данные в формулу и вычислили вероятность развития острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка:
Р=1/(1+e-z)×100%
z=-40,529+0,001*123,9(X1)+0,403*50(Х2)-0,050*43(Х3)+0,204*200(Х4)+0,017*48(Х5)-0,223*73(Х6)=2,9319
Р=0,949
Полученный результат Р=0,949 (94,9%), что согласно разработанной нами методике больше критического значения 46,9%, а значит, у пациента вероятность развития острой левожелудочковой недостаточности высокая - 94,9%. Высокий риск развития острой левожелудочковой недостаточности, на вторые сутки нахождения в стационаре у пациента развилась острая левожелудочковая недостаточность, которая была успешно купирована.
Пример 2.
Пациент В-ин, 83 год, поступил в кардиологическое отделение с диагнозом: ИБС. Инфаркт миокарда с подъемом сегмента передней стенки ЛЖ. ОСН Killip II. Нарушение ритма по типу желудочковой экстрасистолией. Артериальная гипертензия III ст. 2 степени, риск 4. Жалобы при поступлении: боль за грудиной и в левой половине грудной клетки пекущего характера длительностью более 30 минут, общая слабость, головная боль.
Объективные данные: состояние тяжелое. Сознание ясное. Положение активное. Кожные покровы бледной окраски, нормальной влажности. Лимфатические узлы не увеличены. Опорно-двигательный система без особенностей, тонус и сила мышц не нарушены. Периферических отеков нет. При перкуссии легочный звук над всей поверхностью легких. Аускультативно в легких дыхание везикулярное, единичные влажные хрипы в базальных отделах легких, ЧДД 17 в мин. Относительная граница сердечной тупости расширена влево до левой срединно-ключичной линии. Сердечная деятельность ритмичная, нарушена экстрасистолами, тоны приглушены, ЧСС 70 ударов в мин., АД 140/80 мм рт. ст. Язык чистый, влажный. Живот мягкий, при пальпации безболезненный, печень не увеличена. Мочеиспускание без особенностей. Симптом поколачивания отрицательный.
Лабораторные исследования. Общий анализ крови: эритроциты 4,18×1012/л, гемоглобин 110 г/л, лейкоциты (л) 11,9×109/л, тромбоциты - 183×109/л, СОЭ 10 мм/ час. Биохимический анализ крови: глюкоза 4,1 ммоль/л, ХС 6,84 ммоль/л, ХС ЛПНП 3,5 ммоль/л, ХС ЛПВП 1,6 ммоль/л, триглицериды 0,72 ммоль/л.
Электрокардиография. Ритм синусовый, нарушен единичной желудочковой экстрасистолией. ЧСС=70 ударов в минуту. Инфаркт миокарда с подъемом сегмента ST передне-перегородночной стенки ЛЖ, острая стадия. Рентгенография органов грудной клетки. В легких - без видимых очаговых и инфильтративных теней. Корни структурны, уплотнены. Синусы свободны, диафрагма ровная. Сердце умеренно расширено в поперечнике, за счет ЛЖ.
Для прогнозирования развития острой левожелудочковой недостаточности у пациента в первые сутки инфаркта миокарда определяли: X1 - уровень стимулирующего фактора роста ST2=76,2 нг/мл; Х2 - размер левого предсердия по данным ЭХОКГ=40 мм, по данным ЭХОКГ; Х3 - фракция выброса левого желудочка по данным ЭХОКГ=30%, по шкале GRACE рассчитывали Х4 - количество баллов - 212; Х5 - показатель скорости клубочной фильтрации CKD-EPI=57 мл/мин/1,73 м2; Х6 - возраст пациента - 83 лет.
Подставили полученные данные в формулу и вычислили вероятность развития острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка:
Р=1/(1+e-z)×100%
z=-40,529+0,001*76,2(X1)+0,403*40(Х2)-0,050*30(Х3)+0,204*212(Х4)+0,017*57(Х5)-0,223*83(Х6)=-0,1248
Р=0,469
Полученный результат Р=0,469 (46,9%), что равно критическому значению 46,9%, а значит, согласно разработанной нами методике, у данного пациента имеется вероятность развития острой левожелудочковой недостаточности 46,9%. На третьи сутки нахождения в стационаре у пациента развилась острая левожелудочковая недостаточность, которая была успешно купирована.
Пример 3.
Пациент В-ев, 64 год, доставлен скорой медицинской помощью и госпитализирован в кардиологическое отделение с диагнозом: ИБС. Инфаркт миокарда с подъемом сегмента передней стенки ЛЖ. ОСН Killip II. Артериальная гипертензия III ст. 2 степени, риск 4. Жалобы на момент поступления: боль пекущего характера за грудиной и в области левой лопатки длительностью до одного часа, общая слабость, потливость, страх.
Объективные данные: состояние тяжелое. Сознание ясное, эмоционально лабилен. Кожные покровы бледной окраски, нормальной влажности. Лимфатические узлы не увеличены. Опорно-двигательный система без патологии, тонус и сила мышц не нарушены. Периферических отеков нет. При перкуссии легочный звук над всей поверхностью легких. При аускультации легких дыхание везикулярное, единичные влажные хрипы в базальных отделах легких, ЧДД 18 в мин. Относительная граница сердечной тупости расширена влево до левой срединно-ключичной линии. Сердечная деятельность ритмичная, тоны приглушены, ЧСС=78 ударов в мин., АД 110/70 мм рт. ст. Язык чистый, сухой. Живот мягкий, при пальпации безболезненный, печень не увеличена. Мочеиспускание без особенностей. Симптом поколачивания отрицательный.
Лабораторные исследования. Общий анализ крови: эритроциты 4,95×1012/л, гемоглобин 141 г/л, лейкоциты (л) 9,8×109/л, тромбоциты - 115×109/л, СОЭ 7 мм/ час. Биохимический анализ крови: глюкоза 5,1 ммоль/л, ХС 6,75 ммоль/л, ХС ЛПНП 3,3 ммоль/л, ХС ЛПВП 1,36 ммоль/л, триглицериды 1,6 ммоль/л.
Электрокардиография. Ритм синусовый, нарушен единичной предсердной экстрасистолой. ЧСС=78 ударов в минуту. Инфаркт миокарда с подъемом сегмента ST передне-перегородночной стенки ЛЖ, острая стадия. Рентгенография органов грудной клетки. В легких - без видимых очаговых и инфильтративных теней. Корни структурны, уплотнены. Синусы свободны, диафрагма ровная. Сердце без особенностей.
Для прогнозирования развития острой левожелудочковой недостаточности у пациента в первые сутки инфаркта миокарда определяли: X1 - уровень стимулирующего фактора роста ST2=42,151 нг/мл; Х2 - размер левого предсердия по данным ЭХОКГ=38 мм; Х3 - фракция выброса левого желудочка по данным ЭХОКГ=38%, по шкале GRACE рассчитывали Х4 - количество баллов - 194; Х5 - показатель скорости клубочной фильтрации CDK-EPI=94 мл/мин/1,73 м2; Х6 - возраст пациента - 64 лет.
Подставили полученные данные в формулу и вычислили вероятность развития острой левожелудочковой недостаточности у пациентов острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка:
Р=1/(1+e-z)×100%
z=-40,529+0,001*42,151(X1)+0,403*38(Х2)-0,050*38(Х3)+0,204*194(Х4)+0,017*94(Х5)-0,223*64(Х6)=-0,17085
Р=0,457.
Полученный результат Р=0,457 (45,7%), что меньше критического значения 46,9%, а значит, согласно разработанной нами методике, у данного пациента отсутствует вероятность развития острой левожелудочковой недостаточности 46,9%. В течение стационарного лечения пациент с ИМпST был стабильным, выписан из кардиологического отделения в удовлетворительном состоянии без осложнений.
В ходе наших исследований, была сформирована когорта больных ИМпST госпитализированных в кардиологическое отделение в первые сутки заболевания. В исследуемой группе пациентов (n=152) удалось получить достаточный для статистической обработки объем информации. Оценивали факторы, влияющих на развития острой левожелудочковой недостаточности пациентов ИМпST на стационарном этапе лечения в первые сутки заболевания. Под острой левожелудочковой недостаточностью подразумевали развитие отека легких и/или кардиогенного шока у больных ИМпST.
С помощью пошаговой бинарной логистической регрессии нами был произведен отбор факторов-предикторов для создания прогностического алгоритма с наибольшей точностью предсказания. Полученная регрессионная модель является статистически значимой (р<0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 79% наблюдаемой дисперсии показателя «острая левожелудочковая недостаточность».
С целью выявления прогностических предикторов развития острой левожелудочковой недостаточности в течение стационарного лечения пациентов ИМпST в анализ были включены факторы, теоретически способные оказать влияние на исходы заболевания, такие как пол, возраст на момент развития индексного ИМпST, значения гемодинамики, показатели ЭХОКГ, оценка СКФ рассчитанная по формуле CKD-EPI, подсчет баллов по шкале GRACE при госпитализации пациентов, лабораторные данные включая уровень стимулирующего фактора роста (ST2).
Для выявления факторов, оказывающих наибольшее влияние на развитие острой левожелудочковой недостаточности у пациентов ИМпST:
• лабораторный показатель: уровень ST2 (нг/мл) при госпитализации пациентов ИМпST в первые сутки заболевания;
• данные ЭХОКГ: размер левого предсердия (ЛП) (мм), фракция выброса левого желудочка (ФВ ЛЖ) (%);
• величина СКФ, рассчитанная по формуле CKD-EPI (Chronic Kidney Desease Epidemiology Collaboration) мл/мин/ 1,73 м2);
• возраст пациента на момент ИМпST (годы).
Для выявления факторов, имеющих значимое влияние на развитие острой левожелудочковой недостаточности у пациентов ИМпST на стационарном этапе лечения, был использован критерий U-Манна-Уитни для независимых выборок. Была разработана прогностическая модель для определения вероятности показателя «острой левожелудочковой недостаточности у пациентов ИМпST» в зависимости от показателя «стимулирующего фактора роста 2 (ST2) (нг/мл) на этапе госпитализации в стационар», показателя «размера левого предсердия по данным эхокардиографии» (ЛП ЭХОКГ), показателя «фракции выброса левого желудочка по данным эхокардиографии» (ФВ ЭХОКГ), показателя «риска госпитальной летальности по шкале GRACE (баллы)», показателя «скорость клубочной фильтрации CKD-EPI (мл/мин/1,73 м2), «возраста (лет)» методом бинарной логистической регрессии с пошаговым (принудительном включением).
Условная граница, разделяющая пациентов на 2 группы (с благоприятным и осложненным острой левожелудочковой недостаточностью течением острого инфаркта миокарда), определенная при ROC-анализе. Проведен ROC - анализ с определением площади под кривой (AUC) равной 0,958±0,027 с 95% ДИ: 0,904 - 1,000. Полученная модель была статистически значимой (р<0,001). Полученное значение варьирует от 0 до 1. Условная граница, разделяющая пациентов на 2 группы (с благоприятным и осложненным острой левожелудочковой недостаточностью течением острого инфаркта миокарда), определенная при ROC-анализе. Пороговое значение логистической функции Р в точке cut-off, которому соответствовало наивысшее значение индекса Юдена, составило 0,469 (46,9%). Острая левожелудочковая недостаточность прогнозировалось при значении логистической функции Р выше данной величины или равном ей. Чувствительность и специфичность модели составили 88,9% и 97,6%, соответственно.
Заявляемый способ прогнозирования острой левожелудочковой недостаточности у пациентов с острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка обладает высокой точностью и достоверностью. Его использование в клинике поможет обоснованно подобрать объем профилактических и лечебных мероприятий у пациентов с ОИМ с подъемом сегмента ST передней стенки левого желудочка, снизить риск развития острой левожелудочковой недостаточности. Заявляемый способ апробирован на большом клиническом материале и может быть рекомендован к использованию в кардиологии.
Изобретение относится к медицине, а именно к кардиологии и терапии, и может быть использовано для прогнозирования острой левожелудочковой недостаточности у пациентов с острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка (ИМпST). Определяют уровень стимулирующего фактора роста, экспрессируемый геном 2 в крови при госпитализации в первые сутки ИМпST (X1), размер левого предсердия по данным эхокардиографии (X2), фракцию выброса левого желудочка по данным эхокардиографии (X3), количество баллов по шкале GRACE (Х4), показатель скорости клубочной фильтрации CKD-EPI (Х5) и возраст пациента (X6). Рассчитывают вероятность развития острой левожелудочковой недостаточности по формуле Р=1/(1+e-z)×100%, где z=-40,529+0,001X1+0,403Х2-0,050Х3+0,204X4+0,017Х5-0,223Х6. При Р≥0,469 прогнозируют высокий риск развития острой левожелудочковой недостаточности. При Р<0,469 прогнозируют низкий риск. Способ обеспечивает достоверное прогнозирование острой левожелудочковой недостаточности у пациентов с острым ИМпST на стационарном этапе лечения за счет использования прогностического алгоритма на основе предикторов развития острой левожелудочковой недостаточности. 3 пр.
Способ прогнозирования острой левожелудочковой недостаточности у пациентов с острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка, включающий на стационарном этапе исследование сыворотки крови, отличающийся тем, что определяют уровень стимулирующего фактора роста, экспрессируемый геном 2 в крови при госпитализации в первые сутки ИМпST; размер левого предсердия по данным эхокардиографии, фракцию выброса левого желудочка по данным эхокардиографии, количество баллов по шкале GRACE, показатель скорости клубочной фильтрации CKD-EPI, возраст пациента и рассчитывают вероятность развития острой левожелудочковой недостаточности по формуле:
Р=1/(1+e-z)×100%, где
Р - вероятность развития острой левожелудочковой недостаточности у пациентов с острым инфарктом миокарда с подъемом сегмента ST передней стенки левого желудочка;
е - число Эйлера (константа), равное 2,71828;
z=-40,529+0,001X1+0,403Х2-0,050Х3+0,204X4+0,017Х5-0,223Х6,
где
X1 - уровень стимулирующего фактора роста, экспрессируемый геном 2 в крови при госпитализации в первые сутки ИМпST в нг/мл;
X2 - размер левого предсердия по данным эхокардиографии, мм;
X3 - фракция выброса левого желудочка по данным эхокардиографии, %;
Х4 - количество баллов по шкале госпитальной летальности GRACE, в баллах;
Х5 - показатель скорости клубочной фильтрации CKD-EPI, мл/мин/1,73 м2;
X6 - возраст пациента, лет,
и при Р≥0,469 прогнозируют высокий риск развития острой левожелудочковой недостаточности, а при Р<0,469 прогнозируют низкий риск развития острой левожелудочковой недостаточности.
Авторы
Даты
2023-07-21—Публикация
2023-04-25—Подача