Изобретение относится к фармацевтической промышленности и касается способа получения лекарственного препарата в форме таблеток на основе биологически активных соединений (БАС) жидкой фазы послеспиртовой зерновой барды, предназначенного для использования в гастроэнтерологии в качестве противоязвенного препарата, стимулятора желудочной секреции и моторики желудочно-кишечного тракта.
Описан способ получения лекарственного средства (ЛС) «Био-бардин» в форме порошка из зерновой (пшеничной, кукурузной, ячменной, просяной) послеспиртовой барды (Кайшева Н.Ш., Кайшев А.Ш. Антиоксидантное лекарственное средство на основе зерновой послеспиртовой барды. Пат. РФ 2404766, МПК A61K 31/375, опубл. 10.09.10, 9с.). Способ заключается в предварительном фракционировании барды на жидкую и твердую фазы. Далее жидкую фазу концентрируют до плотности 1,480 г/мл, обрабатывают спиртом этиловым 95 об. % (по объему 1:3); полученный высушенный осадок представляет собой густую, вязкую массу желто-коричневого цвета с запахом барды, легко растворимую в воде с образованием большого объема пены. Твердую фазу барды экстрагируют водой (70°С, масса/объем 1:10) вихревой экстракцией (8000 обор./мин, 8 мин) с последующим выделением продукта аналогично выделению из жидкой фазы; полученный высушенный осадок представляет собой легкий, сыпучий порошок светло-бежевого цвета, без запаха, легко растворимый в воде с образованием пены. Оба осадка смешивают, высушивают (60°С) до получения порошка. Целевой продукт (технологический выход 2,9 мас. % к барде) содержит (мас. %): 22,7 олигогалактуронидов, 4,5 биогенных элементов (Р, Mn, Mg, Zn, Fe, Cu, Со, Mo, Cr, V, Ni), витаминов E (0,00342), A (0,00115), С (0,00055), 1,61 олеиновой и линолевой кислот, 0,32 флавоноидов. Данный способ получения ЛС из послеспиртовой зерновой барды наиболее близок к предлагаемому способу.
К недостаткам описанного способа получения ЛС относятся:
- отсутствие испытаний фармакологической активности по отдельности каждой субстанции, выделенной из жидкой и твердой фаз барды, учитывая их различный состав БАС (мас. %): из жидкой фазы - 3,45 биогенных элементов (Р, Mn, Mg, Zn, Fe, Cu, Со, Mo, Cr, V, Ni), 54,0 белков и аминокислот (в т.ч. 10,7 незаменимых аминокислот: треонин, валин, метионин, изолейцин, лейцин, фенилаланин, гистидин лизин, аргинин), 8,8 восстанавливающих сахаров в пересчете на глюкозу, 0,46 флавоноидов в пересчете на рутин, 0,00055 витамина С; из твердой фазы - 0,93 биогенных элементов (Р, Mn, Mg, Zn, Fe, Cu, Со, Mo, Cr, V, Ni), 16,0 белков и аминокислот, 22,7 олигогалактуронидов, 1,61 ненасыщенных жирных кислот (олеиновой, линолевой), 0,00342 витамина Е, 0,00115 витамина A, 0,32 флавоноидов;
- отсутствие испытаний гастропротекторного действия, потенциально обусловливаемого выше приведенным составом БАС;
- подверженность лекарственной формы (порошка) к неблагоприятным воздействиям света, влаги и кислорода воздуха в процессе хранения, что способствует деструкции, окислению, а, значит, и снижению фармакологического эффекта ЛС;
- отсутствие точности дозирования порошка при его употреблении в качестве ЛС;
- неэффективность технологических свойств порошка: отсыревание из-за высокой гигроскопичности, снижение сыпучести вследствие слеживаемости порошка, расслоение из-за различных размеров частиц;
- небольшой срок хранения (1 месяц);
- некомфортность употребления порошка для больного, вызванная неприятными органолептическими свойствами (кислый вкус и специфический дрожжевой запах) и необходимостью предварительного растворения порошка.
Помимо порошка другой формой выпуска БАС барды являются гранулы. Известен способ получения белковой кормовой смеси в виде гранул «Биобардин-Г» (Опытно-промышленный технологический регламент по производству белковой кормовой смеси «Биобардин» ОПТР 10-032-00334586-2006, М.: ГНУ ВНИИПБТ, 2006, 64 с; Технические условия ТУ 9296-042-00334586-06: Смесь белковая кормовая «Биобардин», М.: ГНУ ВНИИПБТ, 2006, 14с.). Способ заключается в приготовлении культуры консорциума молочнокислых и пропионово-кислых бактерий, ферментации барды этим консорциумом (30-37°С, 24 час, рН 5,5-6,5) в присутствии щелочного реагента (натрия гидроксида, калия гидроксида, мела или кальция гидроксида), кобальта хлорида или сульфата (0,1 мг % к питательной среде) и аммония гидрофосфата (0,1-0,2% к питательной среде), центрифугировании барды, концентрировании жидкой фазы, смешивании ее с твердой фазой, высушивании (80-90°С) и сухом гранулировании порошка с применением в качестве склеивающего вещества микрокристаллической целлюлозы. Гранулы «Биобардина-Г» представляют собой крупинки (зернышки) круглой и цилиндрической формы размером 1,2-1,5 мм желто-коричневого цвета, кислого вкуса, с запахом, свойственным барде, со сроком хранения 2 года. Гранулы являются кормовым продуктом, содержащим белки, аминокислоты, витамины, микроэлементы, штаммы микроорганизмов и обладающим антиоксидантным, пробиотическим и биопротекторным действием. Указанные факторы: состав БАС, твердая форма выпуска с продолжительным сроком хранения, пригодность для внутреннего применения и биологическая активность - обусловили выбор заявляемого способа в качестве прототипа. Недостатками выбранного за прототип способа являются:
- несоответствие физико-химических характеристик гранул по: диаметру частиц (1,2-1,5 мм), частичной распадаемости в воде при температуре 37°С (30 мин, присутствие твердой фазы барды), растворению в воде при температуре 37°С в течение 45 мин (38%), потере в массе при истирании (±7,2%) требованиям Государственной фармакопеи Российской Федерации (ГФ РФ, М: Научный центр экспертизы средств медицинского применения, XIII изд., 2015), предъявляемым к гранулам для фармацевтического использования (должно быть соответственно: 0,2-0,3 мм; не более 15 мин; не менее 75%; не более ±3%);
- низкая биодоступность гранул, как следствие их малой растворимости в воде из-за наличия нерастворимой твердой фазы барды;
- невозможность точного дозирования ЛС в гранулах, что осуществляется чайными или столовыми ложками (Гроссман В.А. Фармацевтическая технология, М.: ГЭОТАР-Медиа, 2014, 320с.);
- отсутствие испытаний токсичности и гастроэнтерологического влияния продукта для оценки фармацевтического использования;
- неприятные органолептические свойства гранул (запах барды (ТУ 9296-042-00334586-06) и кислый вкус), ограничивающие их пригодность в медицинской практике, особенно педиатрии;
- относительно небольшая продолжительность хранения (2 года) (ОПТР 10-032-00334586-2006; ТУ 9296-042-00334586-06);
- необходимость предварительного растворения гранул перед их употреблением (Гроссман В.А., 2014).
Цель изобретения - разработка состава и технологии таблеток на основе БАС жидкой фазы барды, пригодных для гастроэнтерологии, обладающих оптимальными для фармацевтического использования показателями: органолептическими, физическими (прочностью на истирание, прочностью на раздавливание, однородностью массы дозированной лекарственной формы), физико-химическими (распадаемостью, растворением), химическими (количественным содержанием БАС), продолжительным сроком хранения.
Поставленная цель достигается тем, что сначала из жидкой фазы зерновой послеспиртовой барды известным способом (Пат. РФ 2404766) получают ЛС (фармацевтическую субстанцию) «Биобардин» в виде густой, вязкой массы желто-коричневого цвета. Далее в гранулят, приготовленный смешиванием в равном массовом соотношении лактозы (наполнителя) и полипласдона «Polyplasdone XL-10» (связывающего вещества) в течение 5 мин до образования однородной смеси светло-коричневого цвета, вводят концентрированный (50 мас. %) водный раствор субстанции, растирают смесь в ступке до образования однородной массы, подсушивают в псевдоожиженном слое при температуре 40°С в течение 30 мин (до остаточной влажности гранулята 3,3%), сухой гранулят пропускают через сито с диаметром отверстий 1,5 мм (сито №15), «опудривают» кальция стеаратом (смазывающее вещество) и прессованием получают плоскоцилиндрические таблетки «Биобардин». Состав одной таблетки «Биобардин» диаметром 13 мм, высотой 6 мм, массой 0,85 г: субстанции «Биобардин» 0,25 г, лактозы 0,30 г, полипласдона «Polyplasdone XL-10» 0,30 г, кальция стеарата 0,001 г.
Заявляемый способ, в отличие от прототипа, предусматривает изготовление таблеток, как лекарственной формы БАС. Это связано с тем, что апробированной в фармацевтической практике лекарственной формой ЛС, подобных компонентам «Биобардина», являются таблетки (Машковский М.Д. Лекарственные средства: в 2 т., М.: Новая волна, 2012, 14-е изд.):
- ЛС на основе аминокислот (по 0,2-0,5 г в одной таблетке): Кислота глутаминовая, Метионин, Декамевит, Панангин, Аспаркам и др.,
- ЛС на основе минеральных элементов (по 0,05-0,5 г фосфора, 0,04-0,18 г калия, 0,01-0,5 г магния, 0,02-0,25 г железа, 0,005 г меди, 0,00009 г кобальта в одной таблетке) в сочетании с аминокислотами: Кальция глицерофосфат, Фитин, Гефефитин, Церебролецитин, Панангин, Аспаркам, Магния окись, Магния карбонат основной, Железо восстановленное, Гемостимулин, Фитоферролактол, Бло, Ферамид, Ферковен и др.,
- ЛС на основе аскорбиновой кислоты в сочетании с флавоноидами, глюкозой (по 0,05-0,5 г аскорбиновой кислоты, 0,02-0,05 г рутина, 0,02-0,1 г кверцетина, 0,2 г глюкозы в одной таблетке): Кислота аскорбиновая, Аснитин, Гептавит, Декамевит, Аскорутин, Галаскорбин, Аэровит, Тетравит, Рутозид, Кверцетин и др.
Целевой продукт, полученный из жидкой фазы послеспиртовой барды известным способом (Пат. РФ 2404766), представляет собой густую, вязкую массу желто-коричневого цвета с запахом барды, легко растворимую в воде с образованием большого объема пены. Целевой продукт, полученный по способу - прототипу (ОПТР, 2006; ТУ, 2006), является смесью концентрата жидкой фазы с твердой фазой; в этом случае достижение оптимальных технологических свойств (однородности, сыпучести и др.) при изготовлении гранул, даже при использовании микрокристаллической целлюлозы, невозможно сухой грануляцией. В заявляемом способе при получении таблеток оптимальные физико-химические и технологические свойства гранулируемой массы достигнуты применением влажного гранулирования.
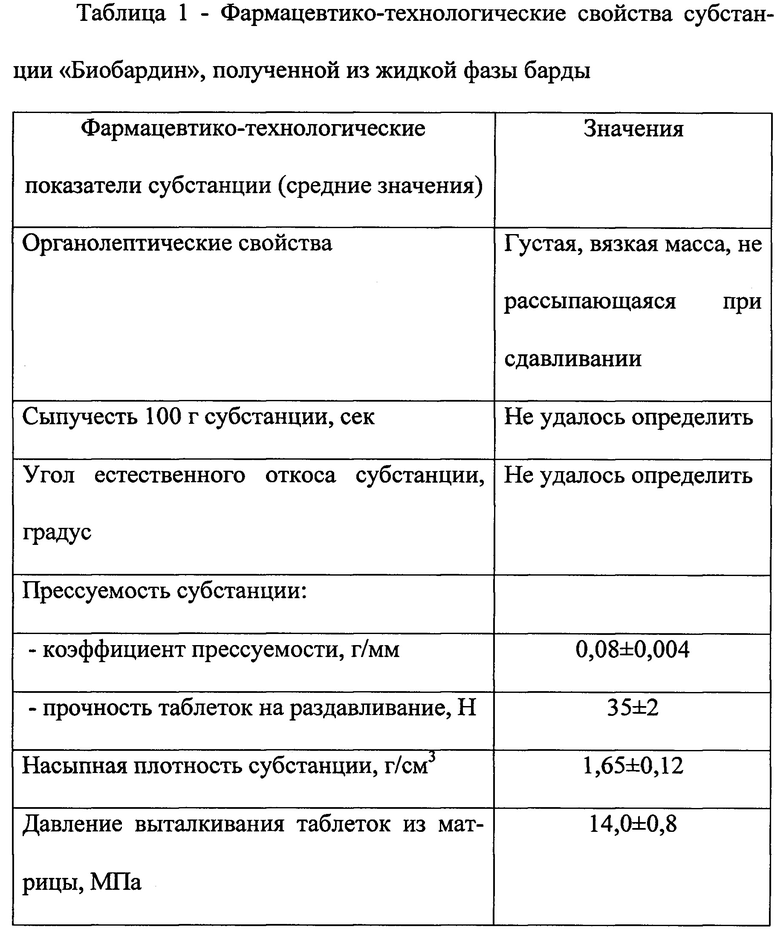
Оценка фармацевтико-технологических свойств субстанции «Биобардин», полученной известным способом (Пат. РФ 2404766), для определения возможности получения из нее таблеток проведена по следующим показателям и методикам (ГФ РФ, XIII, 2015; Промышленная технология лекарств, под ред. В.И. Чуешова, Харьков: НФАУ, 2002, т. 2, 716 с.):
- органолептические свойства,
- сыпучесть порошка (способность высыпаться под силой собственной тяжести и равномерно заполнять матричный канал таблеточной машины) - время (сек) прохождения 100 г порошка через выходное отверстие диаметром 15 мм вибрационного устройства «ВП-12А» (среднее значение из 3 определений);
- угол естественного откоса порошка (в угловых градусах) -трехмерный угол относительно горизонтальной поверхности, сформированный конусообразной пирамидкой сыпучего материала, оценивался на вибрационном устройстве «ВП-12А» при помощи угломера (среднее значение из 3 определений);
- прессуемость порошка - способность частиц к когезии под давлением, определена путем оценки 10 таблеток, полученных на ротационной таблеточной машине «РТМ-12» в матрице с диаметром пуансонов 13 мм при давлении 120 МПа, по среднему коэффициенту прессуемости (отношению массы таблетки к ее высоте, г/мм) и средней прочности таблеток на раздавливание (ньютоны) в приборе «Эрвека»;
- насыпная (объемная) плотность (г/см3) - масса единицы объема порошка, определена на приборе «545Р-АК-3» (среднее значение из 3 определений);
- давление (сила) выталкивания (МПа) получаемых таблеток из матрицы определена по показаниям манометра пресса на ротационной таблеточной машине «РТМ-12» в матрице с диаметром пуансонов 13 мм при давлении 120 МПа (среднее значение из 3 определений).
Полученные средние результаты (таблица 1) свидетельствуют о неудовлетворительных фармацевтико-технологических показателях субстанции, для которой, в силу ее органолептических свойств, даже не представилась возможной оценка показателей сыпучести и угла естественного откоса. Эти неудовлетворительные характеристики дополняются тяжестью субстанции, малой прочностью таблеток на раздавливание и высоким давлением выталкивания изготовленных таблеток. Представленные данные обусловили необходимость подбора вспомогательных веществ, способных оптимизировать фармацевтико-технологические показатели субстанции «Биобардин».
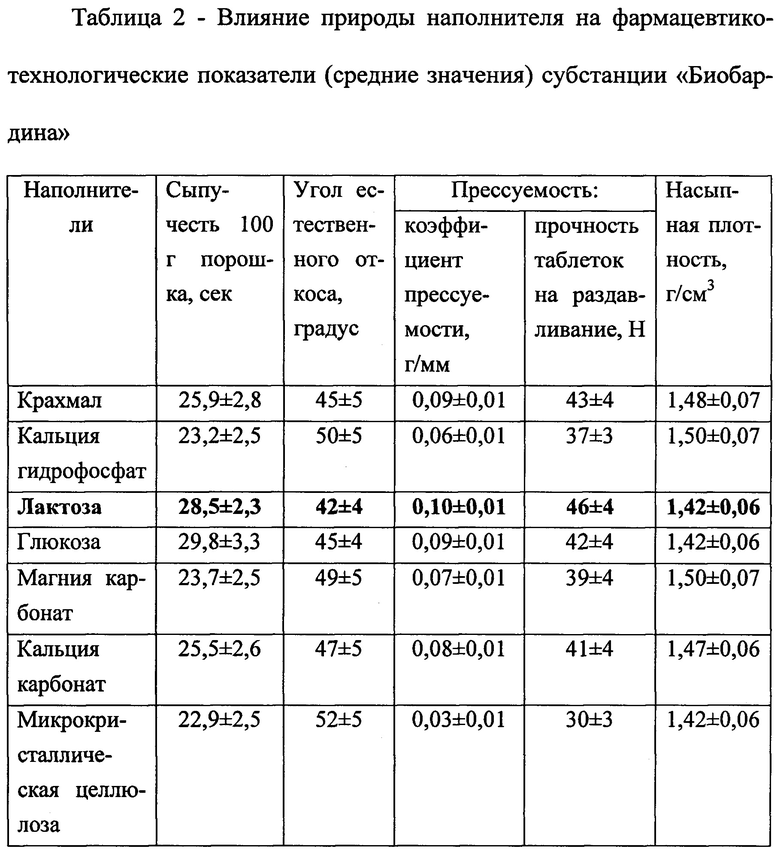
С целью коррекции технологических показателей субстанции «Биобардин» для таблетирования осуществлен подбор наполнителей среди разрешенных к фармацевтическому использованию (ГФ РФ, XIII, 2015): крахмал, кальция гидрофосфат, лактоза, глюкоза, кальция карбонат, магния карбонат, микрокристаллическая целлюлоза. Практический опыт производства таблеток (Промышленная технология лекарств, 2002) показывает, что оптимальной продолжительностью смешивания 2-4-компонентных прописей является 5 мин; именно в течение такого периода смешивалась субстанция «Биобардина» с наполнителями. Критериями подбора наполнителей служили: сыпучесть, угол естественного откоса, прессуемость и насыпная плотность порошка (таблица 2). Результаты испытания свидетельствуют о том, что по сыпучести не менее 25 сек (ГФ РФ XIII, 2015) удовлетворительными оказались 4 наполнителя: крахмал, лактоза, глюкоза и кальция карбонат, однако, отклонения от среднего результата в пределах 10% (ГФ РФ XIII, 2015) удалось достичь только при использовании лактозы (±8,0%). По значению угла естественного откоса лактоза, глюкоза, крахмал обусловили удовлетворительную степень сыпучести: в пределах 45 град., другие наполнители - неудовлетворительную (ГФ РФ XIII, 2015). По прессуемости порошка наилучший результат достигнут при применении лактозы в качестве наполнителя, хотя, согласно ГФ РФ XIII, для таблеток диаметром 13 мм рекомендована минимально допустимая прочность 50 Н. По насыпной плотности все наполнители, кроме лактозы, глюкозы и микрокристаллической целлюлозы, способствуют сильному уплотнению порошка. Таким образом, в качестве оптимального наполнителя для таблеток «Биобардин» выбрана лактоза (молочный сахар).
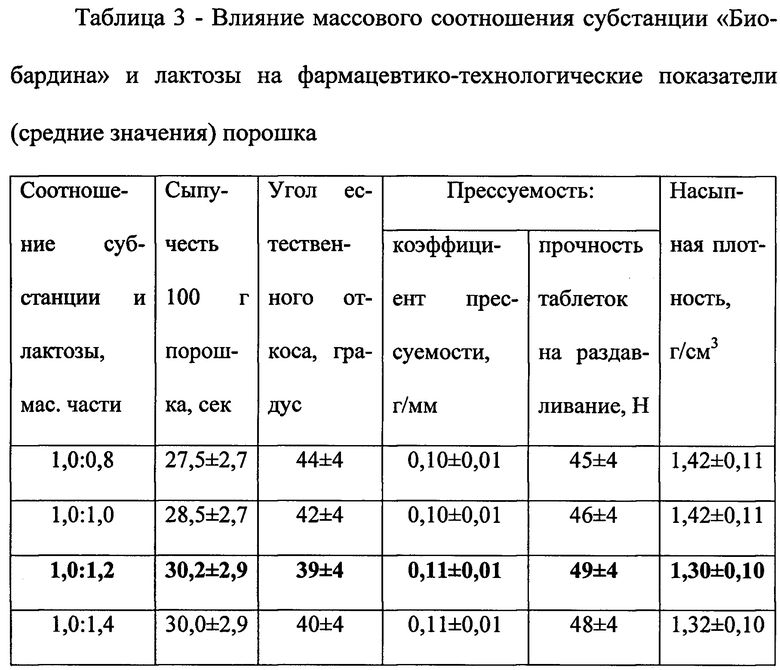
Далее осуществлен подбор оптимального соотношения субстанции и лактозы по указанным выше технологическим показателям (таблица 3). Полученные данные свидетельствуют о том, что добавка к субстанции «Биобардин» лактозы в массовом соотношении 1,0:1,2 обеспечивает наиболее оптимальную сыпучесть, удовлетворительный угол естественного откоса, улучшенные показатели прессуемости и насыпной плотности порошка.
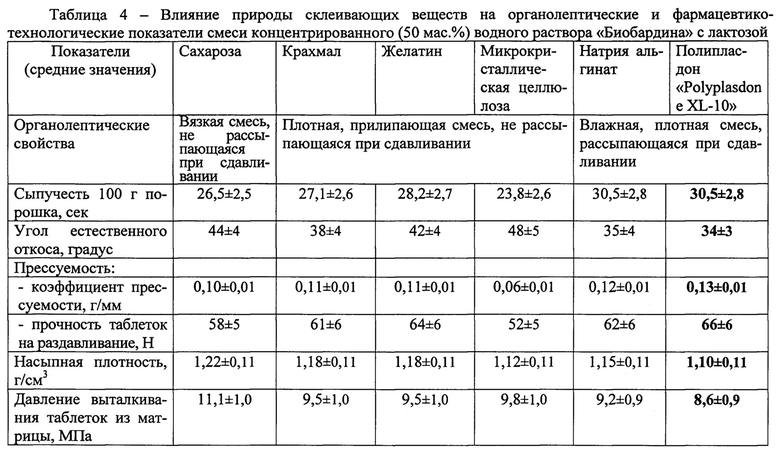
Для достижения необходимой силы сцепления между частицами порошка и сравнительно небольшого давления при таблетировании порошка требуются склеивающие (связывающие) вещества, увеличивающие контактную поверхность и когезионную способность (Промышленная технология лекарств, 2002). Результаты подбора склеивающих (связывающих) веществ, добавляемых к смеси концентрированного (50 мас. %) водного раствора «Биобардина» с лактозой для получения гранулята, с учетом рекомендаций ГФ РФ XIII, приведены в таблице 4. Полученные данные свидетельствуют об обеспечении наиболее оптимальных органолептических свойств и фармацевтико-технологических показателей, особенно сыпучести и прессуемости, смеси раствора «Биобардина» с лактозой при использовании в качестве связывающего вещества полипласдона «Polyplasdone XL-10». Следует отметить, что указанное склеивающее вещество благоприятствует сжатию порошка «Биобардина» под давлением. Неудовлетворительные результаты получены при применении других связывающих веществ, способствующих образованию оплывающей, плохо гранулируемой массы.
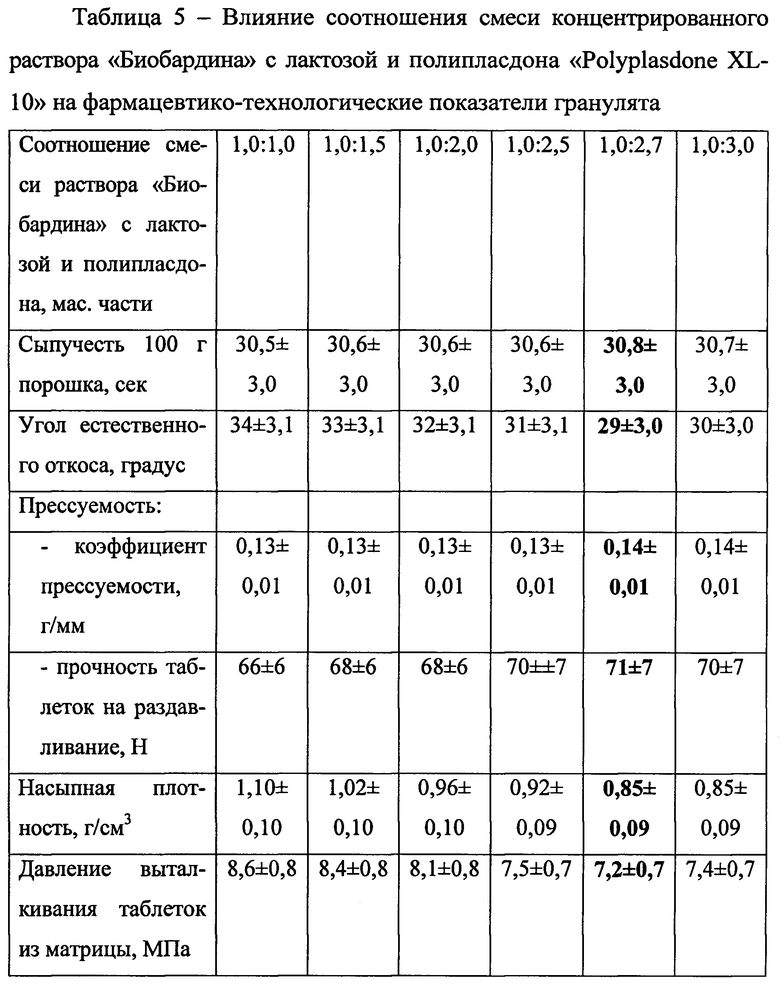
Далее авторами изучено влияние массового соотношения смеси концентрированного раствора «Биобардина» с лактозой и полипласдона «Polyplasdone XL-10» на фармацевтико-технологические показатели гранулята (таблица 5). Полученные данные свидетельствуют о том, что наиболее благоприятные технологические параметры гранулят приобретает при массовом соотношении смеси концентрированного раствора «Биобардина» с лактозой и полипласдона «Polyplasdone XL-10» -1,0:2,7. Таким образом, в приготовленном грануляте массовые части лактозы и полипласдона «Polyplasdone XL-10» равны и они составляют по 1,2 массовой части к 1 массовой части субстанции.
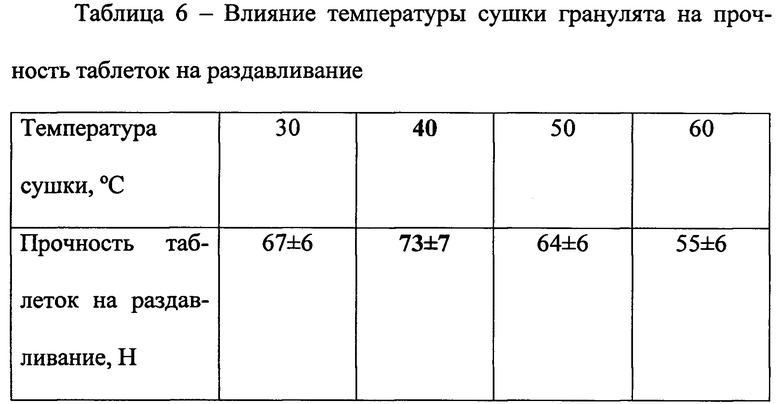
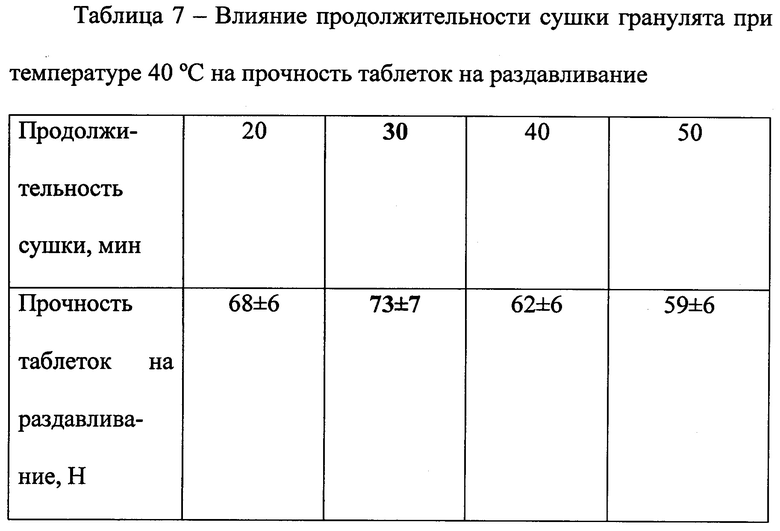
Получаемые гранулы должны быть подсушены до некоторой остаточной влажности, благоприятной для процесса прессования. В заявляемом способе подсушивание гранулята предусматривается в псевдоожиженном слое в сушилке модели «СП-30», обеспечивающем низкую продолжительность сушки материала (Промышленная технология лекарств, 2002). Критерием подбора температуры и продолжительности сушки гранул служила прочность получаемых таблеток на раздавливание (таблицы 6, 7). Полученные данные свидетельствуют о том, что наибольшая прочность таблеток «Биобардина» (73 Н) достигается при температуре сушки гранулята 40°С и продолжительности сушки в течение 30 мин; при этих условиях остаточная влажность гранулята составляет 3,3%. При меньших значениях температуры и продолжительности сушки образуется недосушенный гранулят с остаточной влажностью 3,5-4,5%, прилипающий к пуансонам и неравномерно заполняющий матрицу таблеточной машины; кроме того, образующиеся таблетки характеризуются меньшей прочностью на раздавливание. Повышение температурных параметров способствует снижению остаточной влажности гранулята (менее 3,0%) и, как следствие, затруднению процесса прессования и деформации краев таблеток.
Для обеспечения равномерного фракционного состава подсушенных гранул, а, значит, и постоянной массы таблеток гранулы протирают через сито с диаметром отверстий 1,5 мм (сито №15) (Промышленная технология лекарств, 2002).
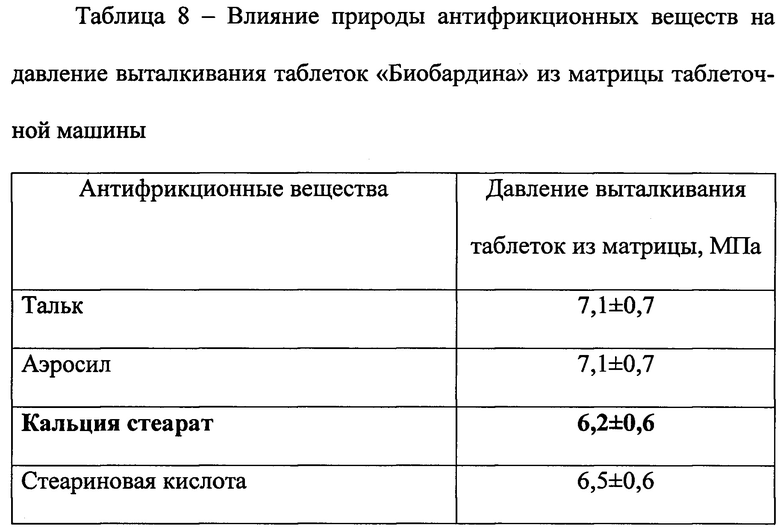
Выбор вспомогательных веществ, необходимых для «опудривания» гранул «Биобардина», осуществлен из антифрикционных веществ, разрешенных для фармацевтического производства таблеток (ГФ РФ, XIII, 2015): тальк, аэросил (скользящие вещества), стеариновая кислота, кальция стеарат (смазывающие вещества). Критерием выбора антифрикционных веществ служило давление выталкивания таблеток из матрицы таблеточной машины (таблица 8). Из полученных данных следует, что наилучшим антифрикционным веществом, обусловливающим наименьшее давление выталкивания таблеток из матрицы, является смазывающее вещество кальция стеарат.
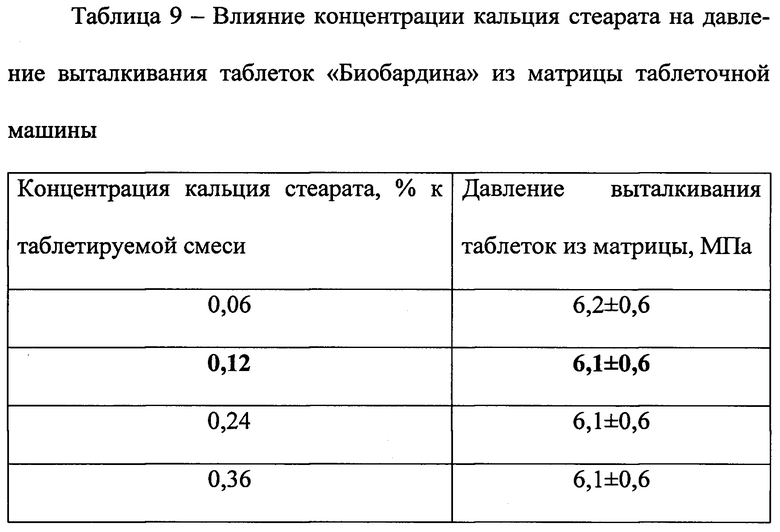
Результаты изучения влияния концентрации кальция стеарата на давление выталкивания таблеток «Биобардина» из матрицы таблеточной машины (таблица 9) свидетельствуют о концентрации кальция стеарата 0,12% к таблетируемой смеси, как к оптимальной концентрации. Подобранная концентрация кальция стеарата согласуется с нормами, рекомендуемыми ГФ РФ (XIII, 2015) для данного вспомогательного вещества: не более 1,0% от общей массы.
Контроль качества растертого порошка заявляемых таблеток «Биобардина» без оболочки диаметром 13 мм, высотой 6 мм, средней массой одной таблетки 0,85 г проведен по показателям:
- описание (ГФ РФ XIII, 2015),
- подлинность (белки и аминокислоты, восстанавливающие сахара, флавоноиды, витамин С) (ГФ РФ XIII, 2015; Кайшева Н.Ш., Кайшев А.Ш., Орловская Т.В. Способ количественного определения восстанавливающих сахаров. Пат. РФ 2403566, МПК G01N 33/15. Опубл. 10.11.10.),
- однородность массы дозированных лекарственных форм (ГФ РФ XIII, 2015),
- прочность таблеток на истирание (ГФ РФ XIII, 2015),
- распадаемость таблеток в воде при температуре 37±2°С (ГФ РФ XIII, 2015),
- растворение таблетки (ГФ РФ XIII, 2015),
- вспомогательные вещества (кальция стеарат) (ГФ РФ XIII, 2015),
- количественное определение (минеральный состав, белки и аминокислоты, в т.ч. незаменимые аминокислоты, восстанавливающие сахара, флавоноиды, витамин С (ГФ РФ XIII, 2015 Пат. РФ 2403566).
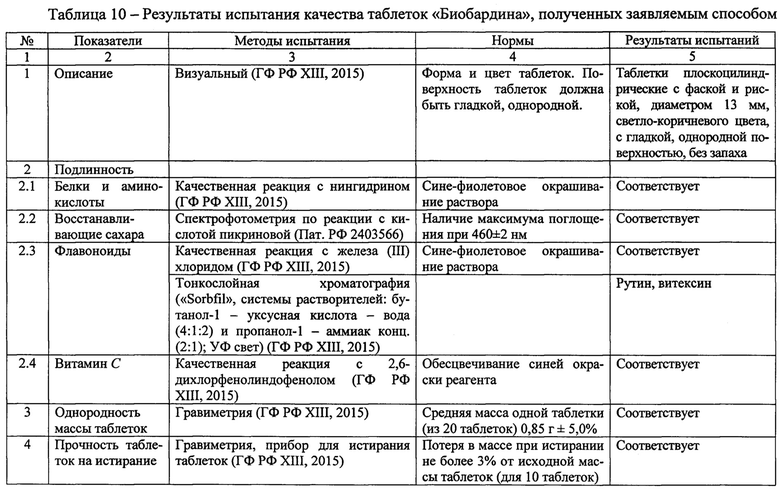
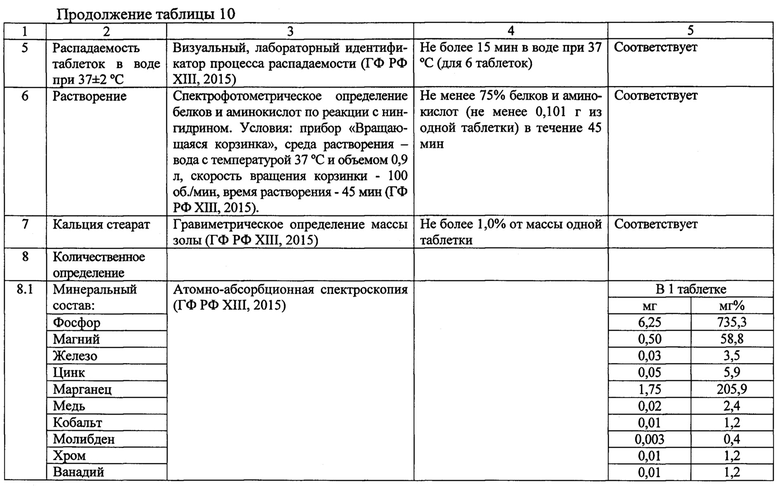
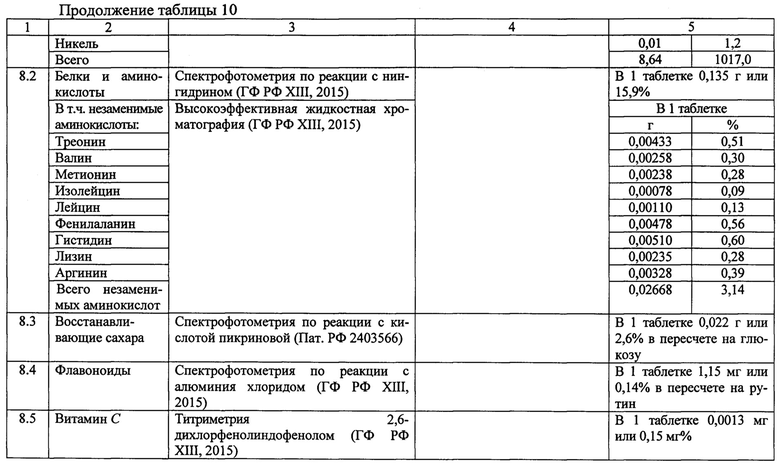
Результаты испытания качества заявляемым таблеток «Биобардина» в сравнении с нормами (ГФ РФ XIII, 2015; Пат. РФ 2403566), приведены в таблице 10. В отличие от известных лекарственных препаратов, содержащих 1-2 группы активных веществ, заявляемые таблетки являются комбинированным препаратом (5 групп соединений).
Стабильность таблеток «Биобардина» в процессе хранения изучена с помощью метода ускоренного хранения (ускоренного старения) (Беликов В.Г. Фармацевтическая химия. В 2 ч. Пятигорск, 2003, с. 142-146.). Для этого 3 серии таблеток (по 6 штук) хранили в термостатах при температурах 40, 50 и 60°С соответственно в течение 114, 57 и 29 суток. Показатели качества таблеток, приведенные в таблице 10, контролировали через 11 (при 40°С), 6 (при 50°С) и 2,9 (при 60°С) суток. В течение экспериментальных сроков хранения ни одна серия таблеток не отклонилась от показателей, приведенных в таблице 10. На основании экспериментальных сроков хранения, используя математическое выражение правила Вант-Гоффа, рассчитан срок годности таблеток «Биобардина» при температуре 20°С, составивший 5 лет.
Способ получения заявляемых таблеток «Биобардин», изготовленных на основе жидкой фазы послеспиртовой зерновой барды и пригодных для использования в гастроэнтерологии, поясняется следующим конкретным примером.
Пример 1.
1. Вначале из жидкой фазы послеспиртовой барды, произведенной из любого вида зерна (пшеницы, кукурузы, ячменя или проса), получают субстанцию «Биобардин» по известному способу (Кайшева Н.Ш., Кайшев А.Ш. Пат. РФ 2404766, МПК A61K 31/375). Для этого барду (100 мл) разделяют на жидкую и твердую фазы путем декантации и процеживания через мешковину. Жидкую фазу барды фильтруют через бумажный фильтр с зеленой полосой (средний объем 72,5 мл и плотность 1,005 г/мл), упаривают на кипящей водяной бане до получения концентрата плотностью 1,480 г/мл, обрабатывают этиловым спиртом 95% в объемном соотношении концентрат: спирт 1:3. Выпавший осадок фильтруют через бумажный фильтр с зеленой полосой, высушивают при температуре 60±5°С. Средний выход осадка составляет 2,3925 г или 3,3% к жидкой фракции барды. Осадок - фармацевтическая субстанция «Биобардин» - представляет собой густую, вязкую массу желто-коричневого цвета, кислого вкуса, со специфическим дрожжевым запахом. Субстанция содержит БАС: 3,45% биогенных элементов (Р, Mn, Mg, Zn, Fe, Cu, Со, Mo, Cr, V, Ni), 54,0% белков и аминокислот (в т.ч. 10,7% незаменимых аминокислот: треонин, валин, метионин, изолейцин, лейцин, фенилаланин, гистидин лизин, аргинин), 8,8% восстанавливающих сахаров в пересчете на глюкозу, 0,46% флавоноидов в пересчете на рутин, 0,00055% витамина С.
2. Далее из субстанции «Биобардин» получают таблетки (в примере все числовые данные приведены в расчете на 1 таблетку). Для этого готовят гранулят, смешивая в ступке 0,30 г лактозы (наполнитель) и 0,30 г полипласдона «Polyplasdone XL-10» (связывающее вещество) в течение 5 мин до образования однородной смеси светло-коричневого цвета. В приготовленный гранулят добавляют 0,5 мл 50 мас. % водного раствора субстанции «Биобардин», растирают смесь в ступке до образования однородной массы (примерно 5 мин). Полученную влажную массу подсушивают в псевдоожиженном слое в сушилке модели «СП-30» при температуре 40°С в течение 30 мин до остаточной влажности гранулята 3,3% (влажность определяют методом высушивания в сушильном шкафу при температуре 100±5°С; ГФ РФ XIII, 2015). Полученный сухой гранулят протирают через сито №15 (диаметр отверстий 1,5 мм). Далее гранулы «опудривают» кальция стеаратом (смазывающее вещество) массой 0,001 г, прессуют на ротационной таблеточной машине «РТМ-12» в матрице с диаметром пуансонов 13 мм при давлении 120 МПа. Целевой продукт - плоскоцилиндрические таблетки «Биобардин» с фаской и риской, диаметром 13 мм, высотой 6 мм, с гладкой и однородной поверхностью, светло-коричневого цвета, без запаха. Состав одной таблетки «Биобардин» со средней массой 0,85 г: субстанции «Биобардин» 0,25 г, лактозы 0,30 г, полипласдона «Polyplasdone XL-10» 0,30 г, кальция стеарата 0,001 г.
3. Фармацевтико-технологические характеристики таблеток «Биобардина»
Показатели гранулята: сыпучесть 100 г порошка 30,8 сек, угол естественного откоса 29°, насыпная плотность 0,85 г/см3. Показатели таблеток: коэффициент прессуемости 0,14 г/мм, прочность таблеток на раздавливание 73 Н, давление выталкивания таблеток из матрицы 6,1 МПа.
Средняя масса одной таблетки из 20 испытанных таблеток находилась в пределах 0,808 г-0,893 г; отклонение массы каждой из 20 таблеток от средней массы одной таблетки не превысило ±1,5%. Потеря в массе 10 таблеток при истирании составила 0,7% от исходной массы таблеток. В течение 15 мин в воде при температуре 37°С все 6 испытуемых таблеток распадались. При испытании одной таблетки «Биобардин» по тесту «растворение» в приборе «Вращающаяся корзинка» со скоростью вращения корзинки 100 об./мин в воде с температурой 37°С и объемом 0,9 л в течение 45 мин обнаружено 0,132 г (97,8%) белков и аминокислот. Среднее содержание вспомогательного вещества кальция стеарата в одной таблетке составило 0,12%.
По химическому составу в одной таблетке «Биобардина» содержится: 8,64 мг биогенных элементов, 0,1350 г белков и аминокислот, в т.ч. 0,0267 г незаменимых аминокислот, 0,0220 г восстанавливающих сахаров в пересчете на глюкозу, 1,15 мг флавоноидов в пересчете на рутин, 0,0013 мг витамина С.
Срок годности таблеток «Биобардина», оцененных с помощью метода ускоренного хранения (ускоренного старения) по показателям таблицы 10, при температуре 20°С составил 5 лет.
Биологические испытания таблеток «Биобардина» проведены по тестам: острая токсичность, гастропротекторное действие и влияние на моторно-эвакуаторную функцию кишечника в опытах на животных, каждая группа которых включала 6 особей. Результаты испытаний обработаны методом множественной статистики (ГФ РФ XIII, 2015) с использованием параметрического критерия Стьюдента, определением средней арифметической величины и отклонения от нее, вероятности различий результатов сравниваемых групп животных.
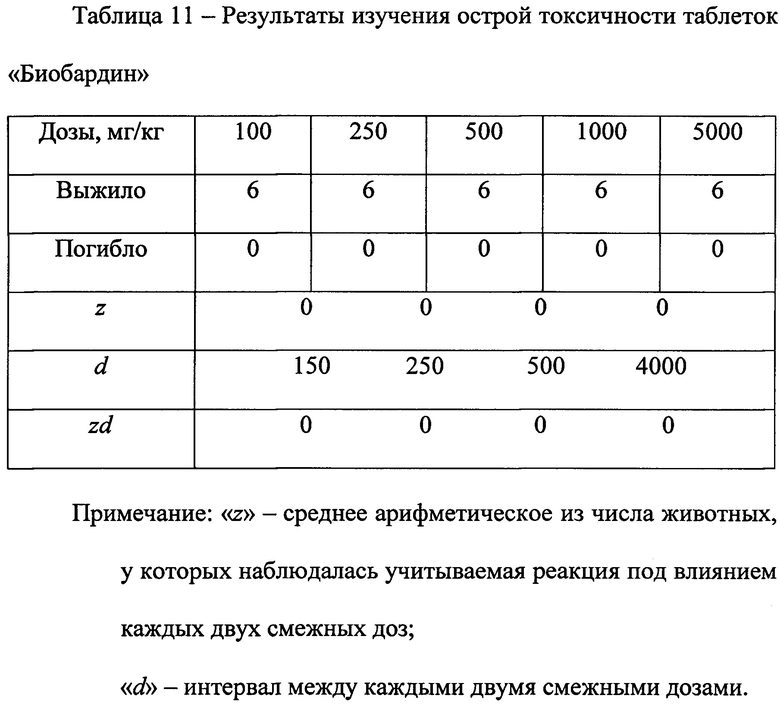
Острая токсичность заявляемых таблеток «Биобардин» определена методом Кербера (Сидоров К.К. Методы определения острой токсичности и опасности химических веществ (токсикометрия). М.: Медицина, 1970, 117 с.) путем перорального однократного введения мышам массой 20 г таблеток в дозах (мг субстанции / кг веса мыши): 100, 250, 500, 1000, 5000 в 5 мл раствора. За время наблюдения за состоянием животных (14 дней) их гибели не отмечено. При вскрытии животных, через 14 дней после введения таблеток, изменений со стороны печени, почек, селезенки не обнаружено. Результаты изучения острой токсичности таблеток «Биобардин» (таблица 11) свидетельствуют о том, что даже максимально введенная доза (5000 мг/кг) не вызывала токсичности, поэтому рассчитать LD50 не представилось возможным, очевидно, LD50>5000 мг/кг. В этой связи, согласно классификации токсических веществ (Сидоров К.К., 1970), заявляемые таблетки «Биобардин» отнесены к группе практически нетоксичных веществ.
Гастропротекторное действие заявляемых таблеток «Биобардин» оценивали по их влиянию на развитие экспериментальных язв желудка у крыс линии Вистар массой 180-220 г: состоянию слизистой оболочки, а также секреторной и протеолитической функций желудка. Модель «острой язвы желудка» создавали однократным пероральным введением крысам преднизолона в дозе 20 мг/кг (в виде 80% спиртового раствора) (Василенко Ю.К. и др. Исследование противоязвенной активности полисахаридов семян льна. Фармация, 1997, №5, с. 35-37) за 3 час перед последним ежедневным однократным введением таблеток «Биобардин» в дозе 500 мг субстанции/кг в день в течение 5 дней.
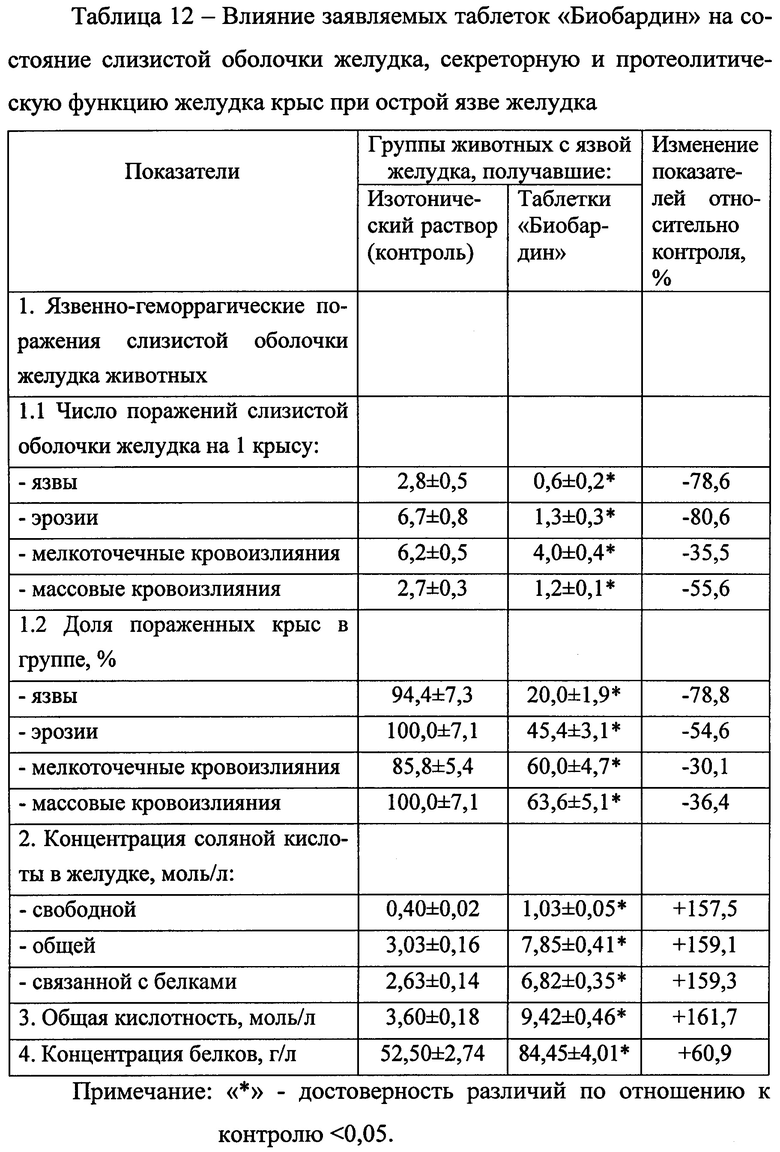
Через сутки после окончания эксперимента животных умерщвляли, извлекали желудок, вскрывали его по малой кривизне, отбирали содержимое желудка. После промывания водой, желудок исследовали под лупой (×10), подсчитывая количество язв, эрозий, геморрагий. Для изучения секреторной функции содержимое желудка анализировали по концентрации соляной кислоты (свободной, общей, связанной с белками) и общей кислотности методом алкалиметрии (Строев Е.А., Макарова В.Г. Практикум по биологической химии. М.: ВШ, 1986, 231 с.). Оценку протеолитической функции желудка по содержанию белков проводили методом фотометрии по реакции с биуретовым реактивом (Строев Е.А., 1986). Контролем служила группа крыс с экспериментальной язвой желудка, получавших изотонический раствор натрия хлорида вместо исследуемых таблеток. Результаты изучения влияния таблеток «Биобардин» на состояние слизистой оболочки желудка, секреторную и протеолитическую функцию желудка крыс с экспериментальной язвой приведены в таблице 12. Согласно полученным данным, заявляемые таблетки «Биобардин» проявляют достоверно выраженное противоязвенное действие: на фоне контроля они наиболее эффективно снижают количество эрозий (в 5,2 раз) и язв (в 4,7 раз), в относительно меньшей степени - число массовых (в 2,25 раз) и мелкоточечных (в 1,55 раз) кровоизлияний в желудке. Под влиянием таблеток «Биобардин» доля пораженных животных в группе, особенно с язвами и эрозиями желудка, снижается в 1,4-4,7 раз. Наряду с этим, таблетки «Биобардин» положительно влияют на секреторную функцию желудка крыс, на фоне контроля достоверно повышая в 2,6 раз содержание свободной и связанной с белками соляной кислоты и общей кислотности желудочного содержимого, стимулируют протеолитическую функцию желудка, достоверно увеличивая в 1,6 раз концентрацию белков в желудочном содержимом. Таким образом, заявляемые таблетки «Биобардин» обладают выраженным гастропротекторным действием: стимулируют заживление язвенных дефектов слизистой оболочки желудка, секреторную и протеолитическую функции желудка животных на фоне острой язвы.
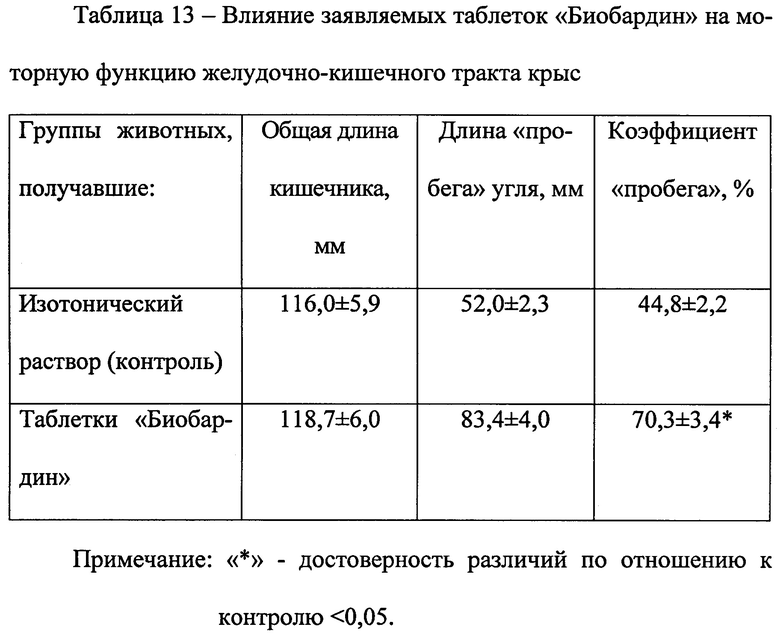
Влияние таблеток «Биобардин» на моторную функцию желудочно-кишечного тракта крыс изучали по величине пассажа с использованием метки - 0,5 мл 10% взвеси активированного угля, приготовленной на 2% крахмальной слизи, перорально вводимой животным через 1 час после последнего ежедневного однократного введения испытуемых таблеток в дозе 500 мг субстанции/кг в течение 5 дней. Через 10 мин после введения угля животных умерщвляли, извлекали кишечник, измеряли его общую длину и длину «пробега» угля, определяли степень продвижения угля по кишечнику (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М.: Медицина, 2000, 523с.). Полученные результаты свидетельствуют о достоверном повышении на 25,5% моторики желудочно-кишечного тракта крыс под влиянием заявляемых таблеток «Биобардин» по сравнению с контролем. По-видимому, этот эффект связан с богатым минеральным составом препарата. Таким образом, исследуемый препарат перспективен для коррекции функциональных расстройств толстой кишки.
Таким образом, по результатам проведенных биологических испытаний заявляемые таблетки «Биобардин» относятся к группе практически нетоксичных веществ, обладают гастропротекторным действием (противоязвенным, стимулирующим секреторную и протеолитическую функции желудка) и способностью стимулировать моторику желудочно-кишечного тракта.
Таким образом, предлагаемый способ получения гастроэнтерологических таблеток «Биобардин» на основе жидкой фазы послеспиртовой зерновой барды обеспечивает следующий положительный эффект:
1. Возможность фармацевтического использования целевого продукта (таблетки «Биобардин»), в отличие от способа-прототипа (гранулы «Биобардин-Г»). Это подтверждается соответствием физико-химических характеристик, а, следовательно, и биологической доступности заявляемого продукта требованиям, предъявляемым ГФ РФ XIII, в отличие от гранул, полученных по способу-прототипу. Различия заявляемого и известного целевых продуктов выражаются в показателях:
- распадаемость твердой лекарственной формы в воде при температуре 37°С (по ГФ РФ XIII - не более 15 мин): в течение 15 мин (заявляемый способ), частичная распадаемость в течение 30 мин и наличие твердой фазы (низкая биодоступность) (прототип);
- растворение в воде при температуре 37°С в течение 45 мин (по ГФ РФ XIII - не менее 75% действующих веществ): 97,8% белков и аминокислот (заявляемый способ), 38% (прототип);
- размер твердой лекарственной формы (по ГФ РФ XIII - диаметр таблеток 4-13 мм, размер гранул - 0,2-0,3 мм): 13 мм (заявляемый способ), 1,2-1,5 мм (прототип);
- прочность на истирание твердой лекарственной формы (по ГФ РФ XIII - потеря в массе при истирании не более 3% от исходной массы): 0,7% (заявляемый способ), 7,2% (прототип).
2. Упрощенность состава заявляемых таблеток «Биобардин», содержащих только три вспомогательных вещества: лактозу (наполнитель), полипласдон «Polyplasdone XL-10» (связывающее вещество), кальция стеарат (смазывающее вещество). Эти вспомогательные вещества разрешены для фармацевтического использования; концентрация кальция стеарата в 1 таблетке (0,12%) не превышает норму (по ГФ РФ XIII - не более 1,0%). Отсутствие в составе гранул «Биобардин-Г» (прототип) связывающих и смазывающих веществ, по-видимому, обусловливает неудовлетворительные фармацевтико-технологические показатели продукта.
3. Оптимизация в заявляемом способе в соответствии с ГФ РФ XIII фармацевтико-технологических показателей, как гранулята (сыпучесть 30,8 сек, угол естественного откоса 29°, насыпная плотность 0,85 г/см3), так и таблеток (коэффициент прессуемости 0,14 г/мм, прочность таблеток на раздавливание 73 Н, давление выталкивания таблеток из матрицы 6,1 МПа) путем подбора оптимального состава вспомогательных веществ.
4. Использование в заявляемом способе современных и доступных для любого фармацевтического производства вспомогательных веществ.
5. Равномерность смешивания субстанции «Биобардин» и вспомогательных веществ без разделения частиц и расслоения массы, улучшение пластичности, сыпучести и уплотнение гранулята, достигнутое путем влажного гранулирования смеси в заявляемом способе и не достигнутое путем сухого гранулирования в способе-прототипе. Это особенно актуально, если учесть, что сам «Биобардин-Г» является неоднородной смесью концентрата жидкой фазы с твердой фазой барды.
6. «Щадящий» технологический режим подсушивания гранул в заявляемом способе: в псевдоожиженном слое при температуре 40°С в течение 30 мин, в отличие от высокой температуры (80-90°С) по способу-прототипу, способствует сохранению термолабильных компонентов заявляемого «Биобардина» (белков и аминокислот, флавоноидов, витамина С, сахаров), а значит, проявлению ими выраженного фармакологического эффекта.
7. Таблетки относятся к лекарственным формам со строго определенной средней массой одной таблетки и дозой лекарственных веществ в ней, в то время как применение гранул осуществляется чайными или столовыми ложками. В этой связи, назначение таблеток со средней массой одной таблетки 0,85 г ±5,0% предполагает точную дозу БАС в каждой таблетке «Биобардина»: 8,64 мг биогенных элементов, 0,1350 г белков и аминокислот, в т.ч. 0,0267 г незаменимых аминокислот, 0,0220 г восстанавливающих сахаров, 1,15 мг флавоноидов, 0,0013 мг витамина С (заявляемый способ). Дозирование гранул «Биобардина-Г» чайными (5 г ±12%) или столовыми (10 г ±15%) ложками (прототип) обусловливает значительные колебания концентраций потребляемых действующих веществ, что относится и к порошку «Биобардина» (Пат. РФ 2404766).
8. Фармакологическими испытаниями заявляемых таблеток «Биобардин» доказана их практическая нетоксичность, стимуляция заживления язвенных дефектов слизистой оболочки желудка (снижение числа язв, эрозий и кровоизлияний в 1,6-5,2 раза), стимуляция секреторной (в 2,6 раз) и протеолитической (в 1,6 раз) функции желудка на фоне острой язвы, стимуляция моторики желудочно-кишечного тракта (в 1,6 раз). Эти данные создают перспективу применения заявляемых таблеток в фармацевтической практике.
9. Стабильность заявляемых таблеток «Биобардин», выражающаяся продолжительным сроком годности (5 лет), в отличие от гранул «Биобардин-Г» (2 года) и субстанции «Биобардин» (1 месяц). Длительная устойчивость компонентов заявляемого целевого продукта, в отличие от прототипа, очевидно, связана с угнетением развития штаммов микроорганизмов, происходящим при обработке жидкой фазы барды этиловым спиртом 95%. Продолжительная стабильность таблеток, в сравнении с субстанцией, обеспечивается лекарственной формой, предотвращающей неблагоприятное воздействие света, влаги и кислорода воздуха.
10. Оптимальные потребительские свойства заявляемых таблеток: отсутствие запаха, кислого вкуса и готовность к употреблению. Потребительские свойства продукта, полученного по способу-прототипу, (дрожжевой запах, кислый вкус), а также необходимость предварительного растворения перед употреблением, ограничивают его пригодность в медицинской практике, особенно педиатрии. Последнее относится и к субстанции «Биобардин», получаемой по пат. РФ 2404766.
11. Использование в заявляемом способе доступного для любого фармацевтического производства технологического оборудования (сушилок модели «СП-30», ротационной таблеточной машины «РТМ-12» и др.).
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ ТАБЛЕТКИ "БИОБАРДИНА" АНТИОКСИДАНТНОГО ДЕЙСТВИЯ, ПОЛУЧЕННЫЕ НА ОСНОВЕ ПОСЛЕСПИРТОВОЙ ЗЕРНОВОЙ БАРДЫ | 2016 |
|
RU2630466C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ - АЗОТСОДЕРЖАЩИХ БЕТАИНОВ ГИДРОХЛОРИДОВ - НА ОСНОВЕ ПОСЛЕСПИРТОВОЙ КУКУРУЗНОЙ БАРДЫ | 2019 |
|
RU2736186C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТИИШЕМИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2545833C1 |
| ЭКСТРАКТ Cetraria islandica (L.) Ach. СУХОЙ, ТАБЛЕТИРОВАННАЯ ФОРМА | 2006 |
|
RU2321419C1 |
| ТВЕРДАЯ ЛЕКАРСТВЕННАЯ ФОРМА ТЕРБИНАФИНА ГИДРОХЛОРИДА | 2001 |
|
RU2200003C1 |
| Лекарственная форма азатиоприна | 2020 |
|
RU2748339C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОЯЗВЕННОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2019 |
|
RU2736184C1 |
| Фармацевтическая композиция с противогрибковой активностью и способ ее получения | 2016 |
|
RU2624857C1 |
| АНТАЦИДНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2013 |
|
RU2567800C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ ДЛЯ ЛЕЧЕНИЯ ЦЕРЕБРОВАСКУЛЯРНЫХ РАССТРОЙСТВ | 2014 |
|
RU2611339C2 |
Группа изобретений относится к фармацевтической промышленности и касается способа получения лекарственного препарата в форме таблеток на основе биологически активных соединений жидкой фазы послеспиртовой зерновой барды, предназначенного для использования в гастроэнтерологии в качестве противоязвенного препарата, стимулятора желудочной секреции и моторики желудочно-кишечного тракта. Твердая форма в виде таблеток для перорального применения в качестве противоязвенного препарата, стимулятора желудочной секреции и моторики желудочно-кишечного тракта содержит 0,30 г лактозы, 0,30 г полипласдона «Polyplasdone XL-10», 0,001 г кальция стеарата, 0,25 г биологически активных соединений жидкой фазы зерновой послеспиртовой барды, включающих 54,0 мас.% белков и аминокислот, в тот числе 10,7 мас.% незаменимых аминокислот: треонин, валин, метионин, изолейцин, лейцин, фенилаланин, гистидин лизин, аргинин; 8,8 мас.% восстанавливающих сахаров; 3,45 мас.% биогенных элементов: P, Mn, Mg, Zn, Fe, Cu, Со, Mo, Cr, V, Ni; 0,46 мас.% флавоноидов, 0,00055 мас.% витамина С. Также предлагается способ получения твердой формы. Группа изобретений обеспечивает получение таблеток, обладающих оптимальной прочностью, однородностью массы, растворимостью, продолжительным сроком хранения. 2 н.п. ф-лы, 13 табл., 1 пр.
1. Твердая форма в виде таблеток для перорального применения для фармацевтического использования в качестве противоязвенного препарата, стимулятора желудочной секреции и моторики желудочно-кишечного тракта, содержащая 0,30 г лактозы, 0,30 г полипласдона «Polyplasdone XL-10», 0,001 г кальция стеарата и 0,25 г биологически активных соединений (БАС) жидкой фазы зерновой послеспиртовой барды, включающих 54,0 мас.% белков и аминокислот, в том числе 10,7 мас.% незаменимых аминокислот: треонин, валин, метионин, изолейцин, лейцин, фенилаланин, гистидин лизин, аргинин; 8,8 мас.% восстанавливающих сахаров; 3,45 мас.% биогенных элементов: P, Mn, Mg, Zn, Fe, Cu, Со, Mo, Cr, V, Ni; 0,46 мас.% флавоноидов, 0,00055 мас.% витамина С.
2. Способ получения твердой формы по п.1, включающий получение осадка БАС из жидкой фазы зерновой послеспиртовой барды, который растворяют в воде для получения 50 мас.% раствора, 0,5 мл которого вводят в гранулят, приготовленный смешиванием в течение 5 мин 0,30 г наполнителя лактозы и 0,30 г связывающего вещества полипласдона «Polyplasdone XL-10»; смесь растирают до образования однородной массы, подсушивают в псевдоожиженном слое при температуре 40°C в течение 30 мин до остаточной влажности гранулята 3,3 мас.%, протирают через сито №15 с диаметром отверстий 1,5 мм, «опудривают» 0,001 г смазывающего вещества кальция стеарата; полученный гранулят с сыпучестью 30,8 сек, углом естественного откоса 29°, насыпной плотностью 0,85 г/см3 прессуют для получения таблеток.
| АНТИОКСИДАНТНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ЗЕРНОВОЙ ПОСЛЕСПИРТОВОЙ БАРДЫ | 2009 |
|
RU2404766C1 |
| КАЙШЕВ А.Ш | |||
| и др | |||
| Биологически активные вещества отходов спиртового производства // Фармация и фармакология, N4 (5), 2014, стр.3-22 | |||
| КАЙШЕВ А.Ш | |||
| и др | |||
| Разработка биокомпозиций антиоксидантного и гастропротекторного действия на основе спиртовых отходов // Известия ВУЗов | |||
| Пищевая технология, N5-6, 2012, стр.52-55. | |||
Авторы
Даты
2018-07-23—Публикация
2016-11-23—Подача