Изобретение относится к области биомедицины и направлено на создание «ростовой добавки», пригодной для 2D и 3D культивирования клеток и микроорганных культур, в том числе на этапах получения клеточных продуктов, предназначенных для введения в организм человека, тканеинженерных конструкций и 3D биопечати, также для создания мягких лекарственных и косметических форм.
Культивирование и наращивание клеток человека in vitro является начальным, промежуточным этапом или самостоятельной процедурой во многих сферах и, в частности, включает:
- культивирование и наращивание разных типов клеток для экспериментальных разработок;
- культивирование и наращивание клеток гибридом с целью получения моноклональных антител;
- культивирование и наращивание клеток разных типов (дифференцированных, прогениторных, стволовых) в целях клеточной терапии;
- культивирование и наращивание клеток как этап создания тканеинженерных конструкций для регенеративной медицины;
- культивирование и наращивание клеток для биотехнологических целей (включая генетическую инженерию);
- культивирование герминогенных клеток в рамках репродуктивных технологий;
- формирование, культивирование и 3D биопечать клеток, клеточных сфероидов и микроорганных культур;
- 3D культивирование клеток, микроорганов и клеточных сфероидов из нормальных и патологически измененных, в том числе, опухолевых клеток в целях тестирования новых лекарственных средств.
Культивирование клеток человека in vitro осуществляют в коммерческих питательных средах разных типов, которые обогащают добавками (supplements). Добавки делятся на два основных типа:
- традиционно используемые как источники факторов роста (далее - ФР), гормонов, витаминов - сыворотки крови крупного рогатого скота, в т.ч. эмбриональная телячья сыворотка (далее - ЭТС);
- специальные добавки для решения конкретных задач.
Одной из актуальных проблем регенеративной медицины является безопасность биомедицинских клеточных продуктов и тканеинженерных конструкций, использование которых способствовало бы восстановлению структуры и функции утраченных органов и тканей у пациентов без угрозы возникновения у них различных осложнений, в том числе, иммунологических.
Для стандартизации и валидации процесса получения безопасных биомедицинских клеточных продуктов (включая тканеинженерные конструкции и 3D биопечать) требуется разработка регламента их получения. К этому разделу относится и разработка безопасных технологий культивирования клеток, в частности, с использованием подходящих культуральных сред и добавок.
Для надежного скрининга новых лекарственных средств in vitro более адекватным на сегодняшний день считается не традиционно используемое 2D, а 3D культивирование клеток, их ассоциатов (в частности, клеточных сфероидов) и микрорганных культур. В 3D культурах клетки находятся в более физиологичных и приближенных к реальному организму условиях, в сравнении с таковыми в 2D культурах, и, как показано, отличаются от последних по своей морфологии, активности сигнальных путей, организации межклеточного матрикса и дифференцировочной активности (Astashkina, А. & Grainger, D. W., 2014. Critical analysis of 3-D organoid in vitro cell culture models forhigh-throughput drug candidate toxicity assessments. Advanced Drug Delivery Reviews, Volume 69-70, pp. 1-18; Akkerman, N. & Defize, L.H., 2017. Dawn of the organoid era. BioEssays, 39(4), pp. 1600244 (1-10).
3D культивирование также требует нексеногенных биологически активных матриксов для культивирования. Одной из моделей 3D культур является культивирование клеток в геле, в частности, в биосовместимых гидрогелях (Kuo, Y.-C. & Wang, С.-С., 2010. Effect of bovine pituitary extract on the formation of neocartilage in chitosan/gelatin scaffolds. Journal of the Taiwan Institute of Chemical Engineers., Том 40, pp. 150-156; Napolitano, А. и др., 2007. Scaffold-free three-dimensional cell culture utilizing micromolded nonadhesive hydrogels. Biotechniques, 43(494), pp. 496-500). К таковым относятся, в частности, фибриновые гели Hakkinen, К., Harunaga, J., Doyle, А. & Yamada, K., 2011. Direct comparisons of the morphology, migration, cell adhesions, and actin cytoskeleton of fibroblasts in four different three-dimensional extracellular matrices. Tissue Eng A, Volume 17, pp. 713-724.
Традиционно в качестве ростовой добавки для культивирования клеток используют ЭТС, которая является комплексной смесью высоко- и низкомолекулярных биомолекул с физиологическим балансом стимулирующих и блокирующих ФР, а также с низким содержанием антител- γ-глобулинов - ингибиторов роста и пролиферации клеток (Bieback, K., 2013. Platelet Lysate as Replacement for Fetal Bovine Serum in Mesenchymal Stromal Cell Cultures. Transfus Med Hemother, 40(5), p. 326-335; Mojica-Henshaw, M. et al., 2013. Serum-converted platelet lysate can substitute for fetal bovine serum in human mesenchymal stromal cell cultures. Cytotherapy, 15(12), pp. 1458-68).
Однако использование ЭТС, представляющей собой источник ксеногенных протеинов, при культивировании клеток на этапах приготовления клеточных препаратов и тканеинженерных конструкций, предназначенных для введения человеку, в настоящее время не рекомендуется вследствие возможности аллергических реакций, а также переноса в организм человека вирусов, прионов и возбудителей зоонозных инфекций (Azouna, N. et al., 2012. Phenotypical and functional characteristics of mesenchymal stem cells from bone marrow: comparison of culture using different media supplemented with human platelet lysate or fetal bovine serum. Stem Cell Res Then, 3(1), p. 6; Warnke, P., Humpe, A., Strunk, D. & et al., 2013. A clinically-feasible protocol for using human platelet lysate and mesenchymal stem cells in regenerative therapies. J Craniomaxillofac Surg., Volume 41, pp. 153-161). В частности, показано, что при введении человеку мультипотентных мезенхимальных стромальных клеток (ММСК), культивированных с ЭТС, могут вырабатываться антитела, опосредующие развитие реакции Артюса (Selvaggi, Т., Walker, R. & Fleisher, Т., 1997. Development of antibodies to fetal calf serum with arthus-like reactions in human immunodeficiency virus-infected patients given syngeneic lymphocyte infusions. Blood, 89(3), pp. 776-779). Возможная экспрессия главного комплекса гистосовместимости II типа (МНС II) в ММСК в присутствии ЭТС, по мнению ряда авторов, также ограничивает использование ЭТС в технологиях регенеративной медицины (Griffiths, S. и др., 2013. Human platelet lysate stimulates high-passage and senescent human multipotent mesenchymal stromal cell growth and rejuvenation in vitro. Cytotherapy, 15(12), p. 1469). He исключено, что генетическая нестабильность ММСК ряда доноров in vitro также может быть индуцирована компонентами ЭТС (Crespo-Diaz, R. et al. Platelet lysate consisting of a natural repair proteome supports human mesenchymal stem cell proliferation and chromosomal stability. Cell Transplant., 20(6), pp. 797-811).
Кроме того, известно, что состав ЭТС значительно варьирует по содержанию активных компонентов от лота к лоту, что не дает возможности стандартизовать ее по наиболее значимым компонентам (Naaijkens, В. и др., 2012. Human platelet lysate as a fetal bovine serum substitute improves human adipose-derived stromal cell culture for future cardiac repair applications. Cell Tissue Res., 348(1), pp. 119-130). Это часто создает технические, экономические и научные трудности при подборе ЭТС для определенных клеточных линий, а в ряде случаев - при сопоставлении результатов, полученных при использовании разных лотов ЭТС даже в одной лаборатории, а также сходных результатов, полученных в разных лабораториях. При этом подбор ЭТС для конкретной культуры является время- и трудозатратным процессом. Кроме того, ограниченность каждой партии ЭТС определяет необходимость проведения повторных тестирований в полном объеме.
Основными недостатками ЭТС, как ростовой добавки для культивирования клеток, предназначенных для введения человеку являются:
- ЭТС - ксеногенный (в отношении человека) материал;
- возможность переноса с ЭТС инфекционных агентов, включая микоплазму, зоонозы, прионы и вирусы (в т.ч. вирус бычьей диареи, парвовирусы, вызывающие бычью энцефалопатию, а также неидентифицированные вирусы);
- возможность переноса с ЭТС свободной ксеногенной ДНК;
- возможность переноса с ЭТС нежелательных метаболитов;
- возможность иммунологического ответа на ЭТС, в т.ч. аллергических реакций на ксеногенные компоненты;
- изменение экспрессии ряда маркеров в клетках человека, культивируемых в присутствии ЭТС;
- нестандартизованность ЭТС по функциональной активности.
В странах западной Европы запрет на использование ЭТС при производстве клеточных продуктов регламентируется «Guidance of Minimizing the Risk of Transmitting Animal Spongiform Encephalopathy Agents via Human and Veterinary Medical Products (EMA/410/01), в России - ФЗ №180 от 23.06.2016 г. «О биомедицинских клеточных продуктах».
На этапах разработки гуманизированных ростовых добавок к культуральным средам были апробированы экстракты различных тканей, биологические жидкости и бессывороточные среды с рекомбинантными ФР, однако удовлетворительные результаты получены не были (Kuo, Y.-C. & Wang, С.-С., 2010. Effect of bovine pituitary extract on the formation of neocartilage in chitosan/gelatin scaffolds. Journal of the Taiwan Institute of Chemical Engineers., Том 40, pp. 150-156). Аллогенные сыворотки в качестве замены ЭТС вызывали задержку пролиферации и гибель ММСК (Shahdadfar, A. F. K., Haug, Т., Reinholt, F. & Brinchmann, J., 2005. In vitro expansion of human mesenchymal stem cells: choice of serum is a determinant of cell proliferation, differentiation, gene expression, and transcriptome stability. Stem Cells, 23(9), pp. 1357-66). В аутологичных сыворотках ММСК пролиферировали адекватно, но делать ее дорого и непрактично. Несмотря на существующую возможность использования аутологичной сыворотки, получение ее в объемах, необходимых для наращивания терапевтически значимого количества клеток крайне затруднено, особенно в случаях забора крови от пациентов, ослабленных возрастными изменениями или сопутствующими патологическими процессами (Kobayashi, Т. и др., 2005. Motility and growth of human bone-marrow mesenchymal stem cells during ex vivo expansion in autologous serum. J Bone Joint Surg Br., 87(10), pp. 1426-33).
В последние годы внимание исследователей обращено к тромбоцитам - естественным источникам многих ФР (PDGF, изоформы АА, АВ, ВВ; TGFα1, -β; HGF; IGF-1; VEGF; EGF; FGFb), в частности, к лизату тромбоцитов (ЛТ) человека для замены ЭТС (Azouna, N. et al., 2012. Phenotypical and functional characteristics of mesenchymal stem cells from bone marrow: comparison of culture using different media supplemented with human platelet lysate or fetal bovine serum. Stem Cell Res Then, 3(1), p.6; Ruggiu, A. et al., 2013. The effect of Platelet Lysate on osteoblast proliferation associated with a transient increase of the inflammatory response in bone regeneration. Biomaterials, 34(37), pp. 9318-30). В ряде работ показаны также регенеративные свойства препаратов на основе тромбоцитов; накоплен определенный положительный клинический опыт по использованию богатой тромбоцитами плазмы при длительно незаживающих ранах, таких как трофические язвы, травматические повреждения кожного покрова, заболевания языка и некоторые другие патологии покровных и мягких тканей (Chandra, R. K. et al., 2007. Histologic effects of autologous platelet gel in skin flap healing. Arch Facial Plast Surg., 9(4), pp. 260-263;  , J. P., Martineau, I. & Gagnon, G., 2005. Platelet-rich plasmas: growth factor content and roles in wound healing. J Dent Res, 84(5), pp. 434-439). Вместе с тем, JIT представляет собой водную смесь биологически активных веществ с относительно невысокой стабильностью, и в силу своей гидрофильности ограниченно проникающих через кожные покровы. Решением данной проблемы является создание лекарственных форм ЛТ, содержащих необходимые вспомогательные веществ, обеспечивающие стабильность ЛТ и его доставку в пораженные участки кожи.
, J. P., Martineau, I. & Gagnon, G., 2005. Platelet-rich plasmas: growth factor content and roles in wound healing. J Dent Res, 84(5), pp. 434-439). Вместе с тем, JIT представляет собой водную смесь биологически активных веществ с относительно невысокой стабильностью, и в силу своей гидрофильности ограниченно проникающих через кожные покровы. Решением данной проблемы является создание лекарственных форм ЛТ, содержащих необходимые вспомогательные веществ, обеспечивающие стабильность ЛТ и его доставку в пораженные участки кожи.
Известен способ получения ЛТ из тромбомассы человека (Сергеева, Н. и др., 2016. Способ получения ростовой добавки на основе лизата тромбоцитов из тромбоцитарной массы доноров к среде для наращивания клеточной массы стволовых, прогениторных, дифференцированных и опухолевых клеток. Россия, Патент №Заявка №2016115622), в котором использована технологическая схема, подобная, но не идентичная указанной в заявляемом способе.
Отличия заявляемого нами изобретения:
- полученный ЛТ в заявляемом способе лиофилизируют.
- лиофилизированный ЛТ далее подвергают описанным в формуле изобретения технологическим процедурам для получения следующих видов продукта: ЛТ, богатый фибриногеном, который можно использовать в качестве ростовой добавки; ЛТ, обедненный фибриногеном, который можно использовать в качестве ростовой добавки и в качестве активного компонента при приготовлении мягких лекарственных и косметологических форм; ЛТ, обедненный фибриногеном в среде для культивирования, который можно использовать для культивирования клеток; гель на основе ЛТ, который можно использовать для 2D и 3D культивирования клеток, сфероидов, микроорганов и 3D биопечати.
Известен способ получения ЛТ из богатой тромбоцитами плазмы крови взрослых животных (Persson, A. et al., 2006. Blood Platelet Lysate and Method of Producing The Same. Sweden, Patent No. WO 2006137778) в котором лизис тромбоцитов осуществляют добавлением к тромбоцитам в плазме растворимых солей кальция либо деионизированной воды. Далее смесь центрифугируют и фильтруют.
Однако полученный по данному способу ЛТ обогащен солями кальция и может быть токсичным для ряда клеточных культур. Высокие концентрации кальция в среде культивирования могут изменять функционирование клеток, так как Са2+ - один из ключевых ионов-регуляторов жизнедеятельности.
Отличительными признаками предложенного нами способа являются:
- использование тромбоцитарной массы (ТМ) человека;
- способ дегрануляции тромбоцитов (для выхода ФР в плазму) - замораживание/оттаивание ТМ.
Известен способ приготовления ЛТ и культуральной среды с ЛТ (Holmovist, О. & Westermark, В., 1994. Blood Platelet Lysate, Method Of Its Preparation And A Cell Culture Medium Containing Said Blood Platelet Lysate. Sweden, Patent No. WO 89/10398) из цельной крови животных для выращивания гибридом с целью получения антител.
Отличия от нашего изобретения:
- использование периферической крови взрослых животных с бойни;
- получаемый в результате ЛТ - ксеногенный продукт, при этом внутрисердечная пункция эмбриона коровы исключена;
- способ разрушения и дегрануляции тромбоцитов - добавление Ca2+.
Как и в предыдущем известном способе, полученный ЛТ оказывается обогащенным солями кальция, что связано с повышенным риском токсичности в отношении клеточных культур человека и животных.
Известен способ получения ростовой добавки из обогащенной тромбоцитами плазмы крови животных (Holmovist, О. & Westermark, В., 1993. Preparation of a blood platelet lysate for use in a cell culture medium for hybridoma cells. USA, Patent No. US 5198357) для культивирования гибридомных клеток. ЛТ получают из цельной крови животных с раствором цитрата натрия для предотвращения коагуляции крови. Способ лизиса - добавление солей кальция, что одновременно приводит к коагуляции фибриногена. Сепарацию производят путем центрифугирования, стерилизацию - путем последующей фильтрации. Используют как более дешевую альтернативу ЭТС.
Известен способ получения ростовой добавки из обогащенной тромбоцитами плазмы крови (Strunk, D., Schallmoser, K. & Rohde, Е., 2012. Plasma-free platelet lysate for use as a supplement in cell cultures and for the preparation of cell therapeutics. Austria, Patent No. US 20120276632), включающий температурный лизис тромбоцитов (замораживание/оттаивание).
В отличие от предлагаемого нами метода, непосредственно перед лизисом тромбоцитов авторы освобождают ТМ от плазмы крови посредством центрифугирования и разводят тромбоциты в среде, содержащей альбумин человеческой сыворотки, декстран и гидроксиэтилкрахмал для восстановления осмолярности.
Известен способ изготовления и применения ЛТ (Shuming, Z., Shichun, W., Yahan, F. & Chunmeng, S., 2015. Method for preparing platelet lysate and application of platelet lysate. China, Patent No. CN 104673747) из тромбомассы, полученной с помощью афереза. Лизис осуществляют путем однократного замораживания (-80°C) - оттаивания (+37°C) тромбомассы с последующей обработкой ультразвуком (100-400 вт, 3-6 секунд), повторяя последнюю процедуру от 5 до 15 раз. Далее ЛТ центрифугируют для осаждения дебриса, очищают от фибрина рекальцинацией (глюконатом кальция или хлоридом кальция) и используют ЛТ как ростовую добавку для культивирования ММСК. В полученном ЛТ определяют содержание VEGF, PDGF, заявляя их как наиболее важные компоненты ЛТ, обеспечивающие для его функциональную активность.
Известен способ приготовления композиции, содержащий лизат тромбоцитов (Dietz, А. В., Gustafson, М. Р. & Butler, G. W., 2010. Compositions Containing Platelet Contents. USA, Patent No. WO 2010033605). Приготовление ЛТ включает в себя не менее 2-х циклов замораживания (-80°C) - оттаивания (+37°C) и последующее центрифугирование (2000-4000g, оптимально - 3000g) в течение 30 минут. Для стерилизации ЛТ осуществляют ультрафильтрацию (размер пор - 0,45 мкм и 0,2 мкм). Полученный ЛТ в концентрации 5-10% от объема культуральной среды используют в качестве ростовой добавки для культивирования ММСК из жировой ткани (ЖТ), фибробластов человека (ФЧ) или культур опухолевых клеток (глиомы), что обеспечивает длительную (более 30 дней) пролиферацию этих культур in vitro с динамикой нарастания клеточной популяции, сходной с таковой при использовании 5-10% ЭТС. В предложенном способе оценку качества приготовленного ЛТ проводят по содержанию фактора роста эндотелия сосудов VEGF - не менее 200 пг/мл.
В заявляемом нами способе стандартизацию проводят по функциональным свойствам. Полученный ЛТ в заявляемом способе лиофилизируют и далее используют для приготовления богатой фибриногеном или лишенной фибриногена ростовой добавки или гидрогеля для 3D культивирования клеток, а также активного композита для создания мягких лекарственных и косметологических средств.
Известны способы приготовления композита на основе ЛТ (Copland, I. В. & Galipeau, J., 2014. Compositions, uses, and preparation of platelet lysates. s.l. Patent No. US 20140127314 A1; Woods, E. J. & Taylor, C. G., 2015. Bioactive Compositions Derivable from Platelet Concentrates, and Methods for Preparing and Using Same. USA, Patent No. WO 2015031465) для использования в качестве компонента среды культивирования клеток, включающие лизис тромбоцитов, освобождение путем центрифугирования от клеточного дебриса, очищение от фибриногена путем добавления солей металлов, в частности, хлорида кальция.
Известен способ приготовления ЛТ путем отделения плазмы крови от тромбоцитов, отмывания тромбоцитов от плазмы, их лизиса, отмывания от дебриса и фильтрацию, и далее разведение ЛТ в отделенной ранее плазме крови для усиления свойства ЛТ как ростовой добавки in vitro или активного компонента средств для ухода за кожей, предотвращающих появление морщин, и для заживления кожных ран в целях профилактики рубцевания (Barlow, J., Davey, W. & Tressler, R., 2017. Compositions and Methods for Cell Culture. USA, Patent No. US 20170175080). В заявляемом нами способе не производится отмывка тромбоцитов от плазмы, а осуществляется разведение/концентрация, в зависимости от истинного содержания тромбоцитов в исходной ТМ.
Известен способ получения ЛТ из периферической крови доноров, включающий выделение обогащенной тромбоцитами плазмы крови с ее лизисом и последующей лиофилизацией. Полученный ЛТ соединяли в различных соотношениях с выделенной параллельно обедненной тромбоцитами лиофилизированной фракцией плазмы и применяли для культивирования стволовых и прогениторных клеток (Muraglia, A. et al., 2015. Combined platelet and plasma derivatives enhance proliferation of stem/progenitor cells maintaining their differentiation potential. Cytotherapy, 17(12), pp. 1793-806.),
Известна композиция для заживления язв кожи, включающая лизат мезенхимальных стволовых клеток пуповины, нативный и лифилизированный в виде пудры и богатую тромбоцитами плазму крови (Chen, В. и др., 2012. The effects of human platelet lysate on dental pulp stem cells derived from impacted human third molars. Biomaterials, 33(20), pp. 5023-35).
Известна композиция для заживления диабетических язв, включающая ЛТ, коммерческий гидрогель и водорастворимый полимер Pluronic F-127 (Cerecedo, М. D. A. et al., 2013. Pharmaceutical Composition of a Platelet Lysate with Wound Healing Activity. Argentina, Patent No. MX2013011483).
Известен способ получения лиофилизированного ЛТ (Patel А., 2012. Lyophilized platelet lysates. USA, Patent No. US 9682104 B2) из периферической крови индивидуальных доноров путем лизиса концентрата тромбоцитов и последующим 3-6-кратным замораживанием при -80-190°C в течение 24 часов/оттаиванием при +37°C. Полученный ЛТ лиофилизируют и хранят при -80°C до использования. Полученный продукт используют в качестве ростовой добавки для культивирования ММСК из жировой ткани и костного мозга человека. Также полученные продукты используют для лечения ран (в виде порошка, в том числе под окклюзионной повязкой, или раствора для орошения, в концентрациях 5-50% об.), для ингаляций (при растворении порошковой формы). Лиофилизированные продукты могут быть использованы совместно с другими терапевтическими средствами (антибактериальными, противогрибковыми, противовирусными, содержащими ФР), в зависимости от назначения.
В заявляемом нами способе источником тромбоцитов является не цельная кровь, а тромбоцитарная масса в цитратной плазме крови. Кроме того, ЛТ получают из крови индивидуального донора, в то время как в заявляемом способе осуществляют стандартизацию путем объединения как минимум 12 индивидуальных образцов ЛТ. Получение композиций в указанном источнике не предусматривает их очистку от фибриногена, негативно влияющего на состояние клеток в культуре, в случае соответствующего использования (в заявляемом способе возможно получение продукта как содержащего фибриноген, так и очищенного от него).
Наиболее близким прототипом является заявка на патент на способ получения ростовой добавки на основе ЛТ (RU 2016115622 А). Исходным продуктом для получения ЛТ является ТМ, нормированная по содержанию тромбоцитов путем центрифугирования ТМ при 3130g в течение 40 минут при 20°C и ресуспендирования осадка в супернатанте заданного объема до концентрации тромбоцитов 1,75×109 клеток/мл. ТМ подвергают 3-кратному температурному лизису путем замораживания на сутки до -80°C и размораживания при +37°C. Клеточный дебрис осаждают путем центрифугирования при 3130g в течение 40 минут при 20°C. ЛТ в супернатанте подвергают микроскопическому контролю (×200) на наличие в поле зрения не более 3-х фрагментов тромбоцитов и далее стандартизируют его путем пулирования равных по объему образцов, полученных из ТМ не менее 12 доноров обеих тендерных групп. Пулированный ЛТ центрифугируют при 3130g в течение 40 минут при 20°C и дважды фильтруют (0,45 мкм и 0,22 мкм) с последующим разливанием по аликвотам требуемого объема.
Анализ выявил следующие отличия прототипа от нашего изобретения:
- Полученный ЛТ хранят в замороженном состоянии и ex tempore размораживают и используют в жидком виде (в заявляемом способе - ЛТ после фильтрации лиофилизируют, что позволяет исключить этап размораживания перед получением ростовой среды)
- ЛТ используется только как ростовая добавка для культивирования клеток, в то время как в заявляемом способе предполагается также использование лиофилизата ЛТ для получения для получения полной ростовой среды (как содержащей фибриноген, так и очищенной от нее), отдельно для создания гидрогеля для 3D культивирования, и отдельно для введения ЛТ в состав лекарственных средств для дермального применения.
- Получаемый ЛТ не подвергается очистке от фибриногена, негативно влияющего на состояние некоторых клеточных линий in vitro (в заявляемом способе, в зависимости от цели использования, возможно применение ЛТ как содержащего фибриноген, так и очищенного от него).
Технический результат направлен на разработку технологии получения спектра медицинских продуктов на основе ЛТ, пригодных для культивирования клеток разных типов, клеточных сфероидов, микроорганных культур, а также получения мягких лекарственных форм и косметических средств для наружного применения.
Особенность заявляемого способа заключается в том, что полученный пулированный ЛТ лиофилизируют. Далее, в зависимости от конкретных задач, подвергают дополнительным стадиям технологической обработки. Для получения среды с ростовой добавкой, содержащей фибриноген, лиофилизированный ЛТ доводят стерильной водой для инъекций до исходного (до лиофилизации) объема и при дальнейшей работе in vitro добавляют к среде для культивирования с гепарином (1-2 ЕД/мл среды) в количестве 5-10% от ее общего объема. Для получения среды с ростовой добавкой, очищенной от фибриногена, добавляют лиофилизированный ЛТ к среде культивирования, содержащей ионы Са2+, без гепарина в количестве 5-10% от ее объема, помещают в термостат (при 37°C в течение 4 часов), сформированный фибриновый сгусток стабилизируют в холодильнике (при 4°C в течение 16 часов), затем отделяют сгусток от стенок пробирки и центрифугируют (280g в течение 10 минут при комнатной температуре), супернатант фильтруют через сито с диаметром отверстий 40 мкм и фильтрат используют для культивирования клеток. Для получения ЛТ, очищенного от фибриногена, к разведенному (до исходного объема) в воде для инъекций лиофилизированному ЛТ добавляют CaCl2 до конечной концентрации 16-20 ммоль/л для формирования сгустка, далее помещают в термостат (при 37°C на 4 часа), сформированный в ЛТ фибриновый сгусток стабилизируют в холодильнике (при 4°C в течение 16 ч), далее сгусток отделяют от плазмы и центрифугируют (280 g, 10 минут при комнатной температуре) и полученный супернатант, свободный от фибриногена, используют в качестве ростовой добавки к средам для культивирования клеток и для получения мягких лекарственных форм накожного применения в целях регенеративной медицины и для создания косметических средств. Для получения гидрогеля в целях использования при 3D культивировании лиофилизированный ЛТ разводят в воде для инъекции до исходного объема, добавляют в количестве 10-15% в ростовую среду, содержащую Са2+ в концентрации 10-30 ммоль/л и сформированный гидрогель используют для культивирования клеток, клеточных ассоциатов, микроорганов, а также в качестве «чернил» для 3D биопечати.
Таким образом, описанными способами, получают четыре продукта:
1. Лиофилизированный ЛТ на основе плазмы крови, богатого фибриногеном.
2. ЛТ на основе плазмы крови, свободного от фибриногена, полученного растворением лиофилизата ЛТ в стерильной воде для инъекций, в составе ростовой среды.
3. ЛТ на основе плазмы крови, свободного от фибриногена, полученного растворением лиофилизата ЛТ в стерильной воде для инъекций, содержащего CaCl2.
4. Гидрогеля на основе 10-15% лиофилизированного ЛТ, растворенного в воде для инъекций, в ростовой среде, содержащей Ca2+.
Изобретение поясняется подробным описанием, клиническими примерами, таблицами и иллюстрациями, на которых изображено:
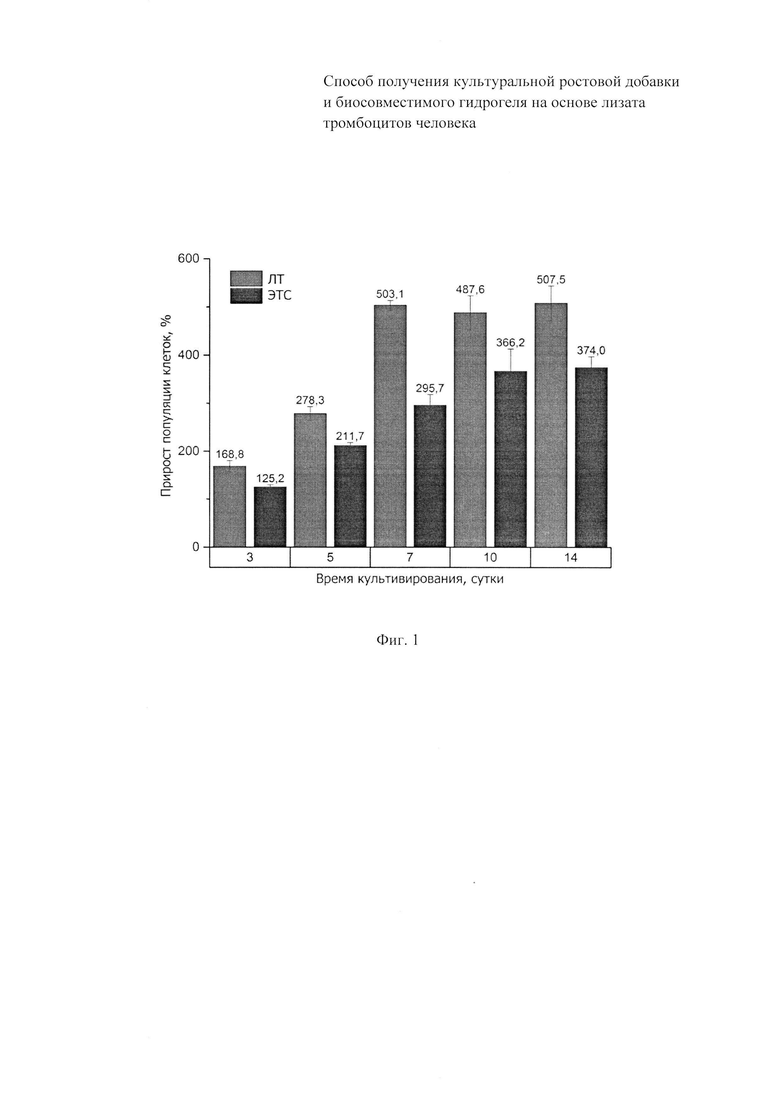
Фиг. 1 - Прирост популяции ММСК в присутствии 10% ЛТ и ЭТС (относительно 1-х суток, принятых за 100%).
Фиг. 2 - Морфология НЕр-2 in vitro в присутствии ЛТ и ЭТС в различные сроки наблюдения (фазово-контрастная микроскопия): А-Д) - ЛТ 10%; Д-З) - ЭТС 10%; А,Д) - 0 ч; Б,Е) - 1 сутки; В,Ж) - 3 сут; Г,З) - 7 суток.
Фиг. 3 - Морфология MCF-7 in vitro в присутствии ЛТ и ЭТС в различные сроки наблюдения (фазово-контрастная микроскопия): А-Д) - ЛТ 10%; Е-К) - ЭТС 10%; А,Е) - 0 ч; Б,Ж) - 1 сутки; В,З) - 2 суток; Г,И) - 3 суток; Д,К) - 7 суток.
Фиг. 4 - Формирование фолликулов щитовидной железы через 2,5 месяца культивирования фрагментов ткани в трансвелле на границе раздела двух сред - жидкой/воздушной в геле на основе ЛТ в ПРС.
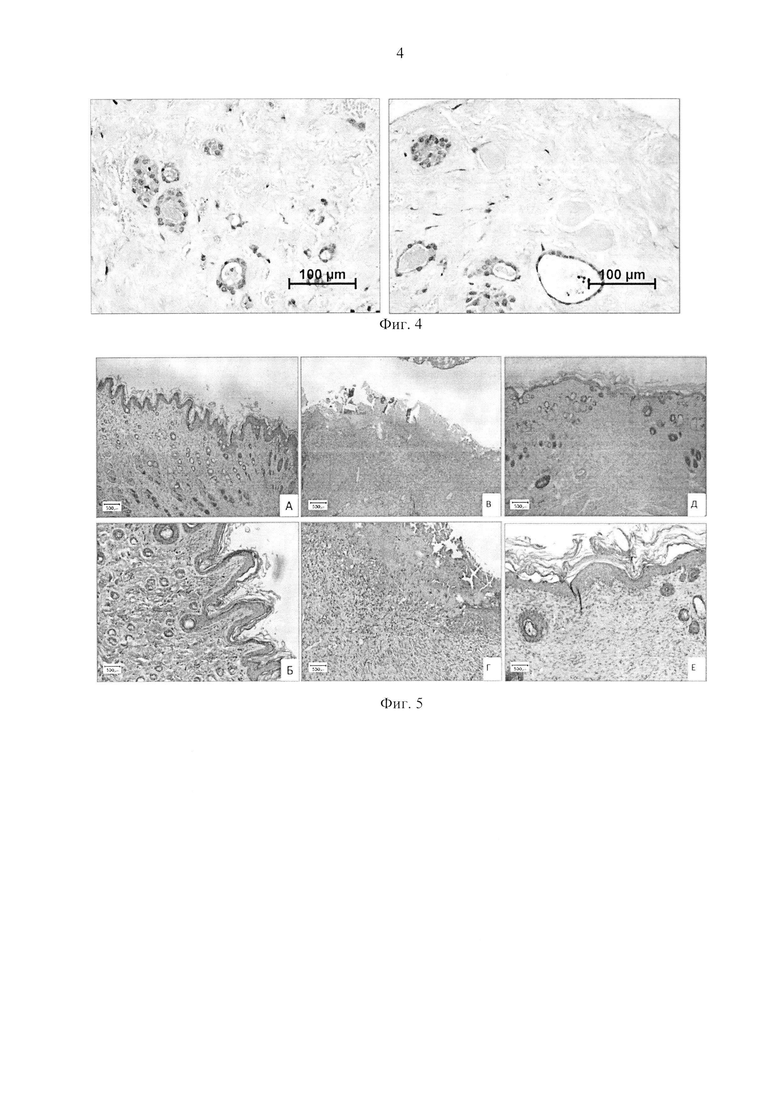
Фиг. 5 - Динамика формирования кожного регенерата в контрольной группе животных. Окраска - гематоксилин-эозин; А, Б - до операции; В, Г, - 7 сутки, Д, Е-13 сутки.
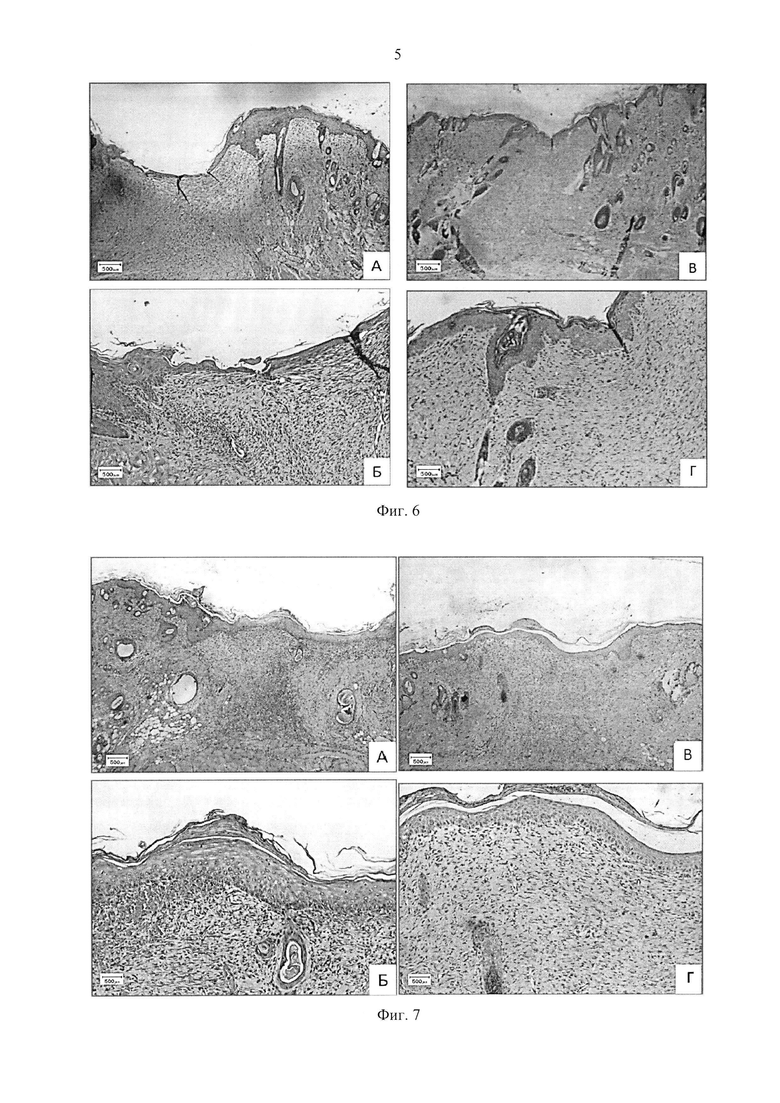
Фиг. 6 - Формирование кожного регенерата на 7-13 сутки после операции при обработке раневой поверхности 20% ЛТ. Окраска: гематоксилин-эозин; А, Б - 7 сутки; В, Г - 13 сутки.
Фиг. 7 - Формирование кожного регенерата на 7-13 сутки после операции при обработке раневой поверхности 100% ЛТ. Окраска: гематоксилин-эозин; А, Б - 7 сутки; В,Г - 13 сутки.
Способы получения указанных продуктов, согласно заявляемому изобретению, осуществляют следующим образом.
1. Получение лиофилизированного ЛТ.
Материал для получения лиофилизированного ЛТ - образцы ТМ доноров, полученные путем тромбоцитафереза (например, на аппаратном комплексе Amicus (Швейцария)). Процедура заготовки ТМ валидирована и предполагает контаминацию лейкоцитами в количестве не более 1×106 на дозу (объем 230-300 мл) (~2×1011 тромбоцитов), что контролируется техническим регламентом «О требованиях безопасности крови, ее продуктов, кровезамещающих растворов и технических средств, используемых в трансфузионно-инфузионной терапии» (постановление №29 ПРФ от 26 января 2010 г.), а также Стандартом №9 «Донорская кровь и ее компоненты: характеристики и контроль качества. IX. Тромбоциты, полученные методом афереза» (Общероссийская общественная организация «Российская ассоциация трансфузиологов»)» от 1.04.2005 г.
Полученный образец ТМ доноров (объемом около 300 мл) в пластиковом контейнере в стерильных условиях тщательно перемешивают и отбирают точечные пробы объемом 0,5 мл для определения концентрации тромбоцитов с помощью автоматического гематологического анализатора (например, Sysmex KX20, Япония). ТМ переносят в пластиковые пробирки объемом 50 мл (например, Corning, США). Перед измерением пробу разводят в 10 раз цитратным буфером ACD-A.
Образец ТМ нормируют по концентрации тромбоцитов. Для этого ТМ центрифугируют в указанных пробирках при 3000g в течение 40 мин при 20°C (например, центрифуга Eppendorf 5810R, Германия). Осадок тромбоцитов ресуспендируют в супернатанте рассчитанного объема, обеспечивающего требуемую концентрацию тромбоцитов (1,75×109 тромбоцитов/мл).
Для получения ЛТ пробирки с образцом ТМ, нормированным по концентрации тромбоцитов, подвергают процедуре температурного лизиса: быстро замораживают до -80°C (низкотемпературный холодильник, например, Sanyo MDF-U500VX) и через 18-24 ч размораживают при +37°C в течение 40-60 мин (термостат, например ТС-80М-2, или водяная баня, например, Biosan WB-4MS) до достижения указанной температуры. Процедуру повторяют трехкратно.
Для осаждения фрагментов разрушенных тромбоцитов (клеточного дебриса) пробирки с ЛТ центрифугируют при 3000g в течение 40 мин при 20°C с минимальной скоростью торможения (например, центрифуга Eppendorf 5810R, Германия). После завершения этапа центрифугирования супернатант, представляющий собой ЛТ, собирают в стерильные пластиковые пробирки объемом 50 мл (например, Corning, США).
Пробу образца ЛТ оценивают на наличие/отсутствие видимых целых тромбоцитов и/или их фрагментов под световым микроскопом (например, Leica LEITZ DM IL, Германия) при увеличении ×200. Очистку считают адекватной при наличии в поле зрения не более 3 фрагментов тромбоцитов.
В основу принципа пулирования положены функциональные свойства ЛТ как ростовой добавки - его способность обеспечивать пролиферацию иммортализованных фибробластов кожи человека (например, ФЧ, штамм 1608h TERT, ФГБУН «Институт молекулярной биологии им. В.А. Энгельгардта» РАН), с тем условием, что по этому признаку пулы ЛТ не должны отличаться более чем на 10% (Сергеева, и др., 2016. Способ получения ростовой добавки на основе лизата тромбоцитов из тромбоцитарной массы доноров к среде для наращивания клеточной массы стволовых, прогениторных, дифференцированных и опухолевых клеток. Россия, Патент №Заявка №2016115622). Для получения стандартизованного по функциональным характеристикам ЛТ объединяют (пулируют) равные объемы ЛТ, полученные из ТМ 12 доноров.
ЛТ фильтруют через фильтр (диаметр отверстий 0,45 мкм и 0,22 мкм, например, Millipore, США) и аликвоты по 10 мл разливают в стерильные стеклянные флаконы объемом 20 мл, после чего маркируют с указанием номера, даты изготовления и объема образца ЛТ.
Аликвотированный ЛТ подвергают лиофилизации с использованием аппаратной лиофильной сушки (например, PowerDry PL3000 Freeze Dryer 3kg/24hrs, Thermofisher, США) в соответствии с рекомендованным производителем режимом, который определяется объемом образцов.
Лиофилизированный ЛТ растворяют в стерильной воде для инъекций (ФС 2.2.0019.15), доводя объем ЛТ до такового перед лиофилизацией и далее в количестве 5-10% (по объему) вводят в состав среды для культивирования клеток, содержащей гепарин (1-2 ЕД/мл) в целях предотвращения выпадения осадка фибрина (например, в среду для культивирования ММСК, состав которой указан далее в табл. 1 настоящей заявки или в другую среду для культивирования клеток).
2. Получение ЛТ, содержащего фибриноген в составе ростовой среды.
Лиофилизированный стандартизованный по функциональной активности ЛТ получают в соответствии со Способом 1.
Лиофилизированный ЛТ растворяют в стерильной воде для инъекций (ФС 2.2.0019.15), доводя его объем до исходного объема ЛТ до лиофилизации.
Растворенный ЛТ в количестве 5-10% (по объему) вводят в состав ростовой среды, содержащей гепарин 1-2 ЕД/мл (например, DMEM, ПанЭко, Россия, табл. 1), в стерильном стеклянном или пластиковом флаконе. Далее флакон со средой выдерживают при 37°C (термостат, например ТС-80М-2, или водяная баня, например, Biosan WB-4MS) в течение 4 часов для перевода фибриногена в среде в нерастворимый фибрин, а затем в холодильник (например, Liebherr LKUv 1610, Германия) на 16-18 часов при 4°C для стабилизации образовавшегося фибринового сгустка.
Сгусток отделяют от стенок пробирки и центрифугируют (например, центрифуга Eppendorf 5810R, Германия) при 280g в течение 10 минут при комнатной температуре с последующим декантированием очищенного от фибриногена супернатанта в стеклянный или пластиковый флакон.
Супернатант фильтруют через сито 40 мкм (например, производства компании BD, США) в стеклянный или пластиковый флакон и фильтрат далее используют как полную ростовую среду для культивирования клеток. Оценка функциональной активности образца пулированного лиофилизированного ЛТ в составе ростовой среды (табл. 1) осуществляется в тестах in vitro, например, на модели ММСК человека.

3. Получение ЛТ, очищенного от фибриногена, в составе ростовой среды.
Лиофилизированный стандартизованный по функциональной активности ЛТ получают в соответствии со Способом 1.
Лиофилизированный ЛТ растворяют в стерильной воде для инъекций (ФС 2.2.0019.15), доводя объем до исходного до лиофилизации ЛТ.
Разведенный ЛТ добавляют к ростовой среде, содержащей кальций (например, DMEM/F-12), перемешивают путем пипетирования и выдерживают при 37°C (термостат, например ТС-80М-2, или водяная баня, например, Biosan WB-4MS) в течение 4 часов для перевода фибриногена в нерастворимый фибрин, а затем в холодильник (например, Liebherr LKUv 1610, Германия) на 16-18 часов при 4°C для стабилизации образовавшегося фибринового сгустка.
Сгусток отделяют от ЛТ и центрифугируют (например, центрифуга Eppendorf 5810R, Германия) при 280g в течение 10 минут при комнатной температуре с последующим декантированием очищенного от фибриногена супернатанта в стеклянный или пластиковый флакон.
Супернатант пропускают через сито с диаметром отверстий 40 мкм (например, BD, США) и фильтрат далее используют для культивирования клеток. Оценка функциональной активности образца пулированного лиофилизированного ЛТ в составе ростовой среды (табл. 1) осуществляется в тестах in vitro, например, на модели перевивной клеточной линии остеосаркомы человека (MG-63) или иммортализованных фибробластов кожи человека (ФЧ).

4. Получение ростовой добавки на основе ЛТ, очищенной от фибриногена.
Лиофилизированный стандартизованный по функциональной активности ЛТ получают в соответствии со Способом 1.
Лиофилизированный ЛТ растворяют в стерильной воде для инъекций (ФС 2.2.0019.15), доводя объем до исходного до лиофилизации ЛТ.
К разведенному ЛТ добавляют раствор кальция хлорида 10% до конечной концентрации 16-22 ммоль/л для формирования фибринового сгустка. Перемешивают путем пипетирования и выдерживают при 37°C (термостат, например ТС-80М-2, или водяная баня, например, Biosan WB-4MS) в течение 4 часов для перевода фибриногена в нерастворимый фибрин, а затем в холодильник (например, Liebherr LKUv 1610, Германия) на 16-18 часов при 4°C для стабилизации образовавшегося фибринового сгустка.
Сгусток отделяют от ЛТ и центрифугируют (например, центрифуга Eppendorf 5810R, Германия) при 280g в течение 10 минут при комнатной температуре с последующим декантированием очищенного от фибриногена супернатанта в стеклянный или пластиковый флакон.
Супернатант пропускают через сито с диаметром отверстий 40 мкм (например, BD, США) и фильтрат далее используют в качестве ростовой добавки для культивирования клеток.
5. Получение ЛТ, очищенного от фибриногена, в целях регенеративной медицины.
ЛТ, очищенный от фибриногена, получают из лиофилизированного стандартизированного по функциональной активности ЛТ в соответствии со Способом 4.
Оценку регенеративной активности полученного ЛТ при накожном применении оценивают in vivo на модели искусственного дефекта кожных покровов (например, раневой дефект кожных покровов у мелких лабораторных животных - крыс, мышей, морских свинок).
6. Получение гидрогеля на основе ЛТ.
Фибриновый гидрогель получают из лиофилизированного ЛТ в соответствии со Способом 3. К ростовой среде добавляют 10-15% растворенного ЛТ (полная ростовая среда, ПРС) и используют сразу после приготовления.
Для образования гидрогеля полученную ПРС сразу после приготовления в асептических условиях помещают в камеру Бойдена с полупроницаемыми мембранами (например, Corning, Transwell, 0.4 um, США), заселяют монослойными клеточными культурами (стволовыми/прогениторными/дифференцированными/опухолевыми клетками), клеточными ассоциатами (сфероидами) или микроорганами и помещают в CO2-инкубатор (например, Sanyo MCO-20AIC, Япония) на 4 часа при 37°C для формирования гидрогеля, после чего культивируют в соответствии с дизайном экспериментов. При длительном культивировании при необходимости производят добавление свежих порций ПРС, содержащих ЛТ, в культуральную систему.
Все процедуры в Способах 1-6 осуществляют в стерильных условиях.
Пример конкретного исполнения №1.
1. Заготовка образцов тромбоцитарной массы доноров.
В стерильных условиях методом тромбоцитафереза (аппаратный комплекс Amicus, Швейцария) получено 12 индивидуальных образцов ТМ (6 мужчин, 6 женщин). Перед процедурой заготовки ТМ доноры проходили обследование на наличие ВИЧ I и II типа, HBs-антигена, вируса HCV, возбудителя сифилиса. Также был осуществлен клинический анализ крови.
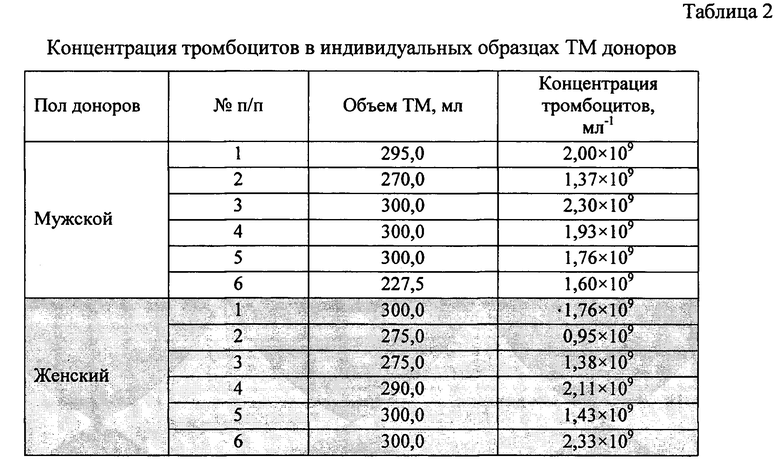
Через 24 часа после процедуры тромбоцитафереза образцы ТМ доноров объемом 200-400 мл в специальных пластиковых мешках помещали в транспортировочный контейнер и переносили в лабораторию с прилагаемой сопроводительной информацией (ФИО донора, пол, возраст, дата заготовки ТМ, результаты лабораторных исследований), где в асептических условиях (ламинарный бокс 2-класса защиты) тщательно перемешивали, отбирали 3 точечных пробы по 0,5 мл для определения концентрации тромбоцитов и затем и переносили в пластиковые пробирки (Corning, США), по 40-50 мл. Объем полученной ТМ доноров варьировал от 228 до 330 мл (Табл. 2).
2. Определение концентрации тромбоцитов в образцах ТМ.
Производили определение концентрации тромбоцитов в образце ТМ каждого донора. Для этого отобранные точечные пробы ТМ объединяли, ресуспендировали путем тщательного перемешивания с использованием механической пипетки на 1,0 мл Eppendorf или Biohit. Далее отбирали пробу объемом 50,0 мкл для определения в ней концентрации тромбоцитов и переносили в пластиковую пробирку (Eppendorf, Германия) объемом 0,5 или 1,0 мл. В пробирку с пробой добавляли 450,0 мкл цитратного буфера ACD-A для получения рабочего разведения пробы 1:10. Разведенную пробу вносили в лабораторный анализатор Sysmex KX21 (Япония) и измеряли концентрацию тромбоцитов (табл. 2).
3. Нормирование образцов ТМ по количеству тромбоцитов.
Образцы ТМ в указанных закрытых пробирках помещали в лабораторную центрифугу (Eppendorf 5810R, Германия) и центрифугировали при 3130g в течение 40 мин при 20°C для осаждения тромбоцитов.
Нормирование тромбоцитов производили в расчете на стандартную концентрацию: рассчитывали объем супернатанта для разведения в нем осадка тромбоцитов, необходимый для достижения концентрации 1,75×109 тромбоцитов/мл. При концентрации тромбоцитов меньше заданной (образцы ТМ от доноров - мужчин №№2, 6 и №№2, 3 и 5 доноров - женщин), удаляли избыточный объем супернатанта и ресуспендировали осадок тромбоцитов в нужном для достижения указанной концентрации объеме. При концентрации тромбоцитов больше заданной (образцы №1, 3, 4, 5 от доноров - мужчин и №№1, 4, 6 от доноров - женщин) ТМ разводили плазмой, аналогичной по составу бесклеточной фракции ТМ.
4. Температурный лизис образцов ТМ.
Образцы ТМ доноров, нормированные по концентрации тромбоцитов, в указанных закрытых пробирках переносили в низкотемпературный холодильник (Sanyo MDF-U500VX, Япония) и выдерживали при температуре -80°C в течение 1 суток. По истечении указанного времени содержимое пробирок размораживали при +37°C (термостат ТС-80М-2 или водяная баня Biosan WB-4MS) в течение 40-60 мин. Циклы замораживания / оттаивания повторяли 3 раза.
5. Центрифугирование образцов ЛТ.
Для освобождения образцов лизированной тромбомассы от фрагментов тромбоцитов производили их центрифугирование. Пробирки с образцами ЛТ переносили в лабораторную центрифугу (Eppendorf 5810R, Германия) и центрифугировали при 3130g в течение 40 мин при комнатной температуре для осаждения фрагментов тромбоцитов. Супернатант переносили в новые стерильные пластиковые пробирки (50 мл, Corning, США).
6. Микроскопический контроль образцов ЛТ доноров.
Осуществляли с помощью светового микроскопа (Leica LEITZ DM IL, Германия) при увеличении ×200, оценивая наличие/отсутствие видимых нелизированных тромбоцитов и/или их фрагментов. Содержание частиц клеточного дебриса и цельных тромбоцитов в пробах ЛТ от каждого из 12 доноров в каждом поле зрения не превосходило 2.
7. Пулирование, фильтрация и аликвотирование образцов ЛТ доноров.
На заключительном этапе производили пулирование образцов ЛТ доноров. Для этого равные объемы 12 образцов ЛТ в стерильных условиях объединяли путем переноса в пластиковые флаконы для центрифугирования объемом 250 мл (Corning, США).
Флаконы с пулированным ЛТ помещали в лабораторную центрифугу (Eppendorf 5810R, Германия) и центрифугировали при 3130g в течение 15 мин при комнатной температуре для дополнительного осаждения остаточного дебриса. Пробирки извлекали из центрифуги и в стерильных условиях осуществляли фильтрацию супернатанта, последовательно через фильтры 0,45 мкм и 0,2 мкм (Millipore, США) в пробирки аналогичного типа. Далее пулированный ЛТ разливали в стеклянные флаконы на 20,0 мл по аликвотам (по 10,0 мл) и маркировали.
8. Лиофильная сушка ЛТ.
Аликвотированные образцы ЛТ объемом 10,0 мл подвергали лиофильной сушке с использованием аппарата Heto PowerDry PL3000 (Thermofisher, США) при остаточном давлении в камере 5-10 Па и температуре -35°C в течение 24 часов с последующим досушиванием при остаточном давлении 1-2 Па и температуре +20°C в течение 12 часов.
Пример конкретного исполнения №2.
1. Получение лиофилизированного ЛТ.
Для культивирования ММСК, выделенных из жировой ткани (ЖТ) человека (пассаж 4), использовали образец лиофилизированного пулированного ЛТ, полученного из ТМ 12 доноров по методике, описанной в «Примере конкретного исполнения №1».
2. Приготовление рабочего раствора ЛТ.
Лиофилизированный ЛТ растворяли в стерильной воде для инъекций (ФС 2.2.0019.15), доводя объем до исходного объема образца до лиофилизации (10,0 мл).
3. Приготовление ростовой среды с ЛТ.
Растворенный ЛТ в объеме 10,0 мл вводили во флакон с 90,0 мл ростовой среды на основе DMEM/F-12, содержащей гепарин (2 ЕД/мл, «ПанЭко», Россия) (табл. 3).

Супернатант после центрифугирования пропускали через сито 40 мкм (BD, США) и далее использовали как полную ростовую среду для культивирования клеток.
4. Оценка функциональной активности полной ростовой среды с ЛТ.
ММСК культивировали в ПРС, представляющей собой фильтрат из п. 5.
На сроках культивирования 1, 3, 6 суток определяли жизнеспособность клеток с помощью МТТ-теста (МТТ, Sigma, США). Сравнительные эксперименты in vitro по оценке динамики роста культур ММСК с использованием пулированного образца ЛТ доноров и образца ЭТС (РАА, Австрия, лот № А10106-0671) в качестве ростовых добавок к среде культивирования из п. 5 осуществляли в 96-луночных планшетах (Corning, США) с плотностью посева 1,5×104 кл./см2 и со сменой среды дважды в неделю. На сроках культивирования 1, 3, 6 суток определяли пул жизнеспособных клеток с помощью МТТ-теста (МТТ, Sigma, США). Для проведения МТТ-теста по окончании срока культивирования из каждой лунки отбирали по 100 мкл среды и вносили по 25 мкл раствора МТТ в концентрации 5 мг/мл. Через 3 ч инкубации в термостате (Sanyo МСО-20AIC, Япония) при 5% СО2, 37°C из каждой лунки полностью удаляли среду и производили растворение образовавшегося формазана с помощью изопропилового спирта (200 мкл/лунку). От осадка, образующегося в результате преципитации белков в изопропиловом спирте, освобождались центрифугированием планшета в течение 10 мин при 3000 об/мин (Jouan, Франция). Далее из каждой лунки переносили по 100 мкл супернатанта в 96-луночный планшет для спектрофотометрии (Costar, США) и оценивали оптическую плотность (OD) раствора формазана на спектрофотометре FC (Thermoscientific, США) при длине волны 540 нм.
Полученные данные (Фиг. 1) свидетельствовали о том, что уже на 3-й сутки культивирования ММСК величина прироста (относительно 1-х суток) клеточной популяции в присутствии ЛТ была достоверно выше, чем в присутствии ЭТС. На 7-е сутки культивирования (vs 1 сутки) в присутствии ЛТ величина прироста ММСК составила 503,1%, после чего произошел переход культуры в стационарную фазу. В присутствии ЭТС прирост культуры ММСК происходил медленнее. Переход ММСК в стационарную фазу отмечен лишь на 10-е сутки культивирования; прирост клеточной популяции к этому сроку составил 374,0%.
Таким образом, среда для культивирования ММСК, содержащая в качестве ростовой добавки ЛТ, полученный растворением лиофилизата ЛТ, и не содержащая фибриноген и гепарин, поддерживали пролиферацию ММСК in vitro активнее, чем ЭТС.
Пример конкретного исполнения №3.
1. Получение лиофилизированного ЛТ.
Для культивирования ФЧ (штамм hTERT 1018) и MG-63, выделенных из жировой ткани (ЖТ) человека (пассаж 4), использовали образец лиофилизированного пулированного ЛТ, полученного из ТМ 12 доноров по методике, описанной в «Примере конкретного исполнения №1».
2. Приготовление рабочего раствора ЛТ.
Лиофилизированный ЛТ растворяли в стерильной воде для инъекций (ФС 2.2.0019.15), доводя объем до исходного объема образца до лиофилизации (10,0 мл).
3. Формирование фибринового сгустка.
Растворенный ЛТ в объеме 10,0 мл вводили во флакон с 90,0 мл ростовой среды на основе DMEM/F-12, содержащей ионы Са2+(DMEM/F-12, «ПанЭко», Россия) и помещали в термостат (ТС-80М-2, Россия) на 4 часа при 37°C для перевода фибриногена в нерастворимый фибрин, а затем в холодильник (Liebherr LKUv 1610, Германия) на 16-18 часов при 4°C для стабилизации образовавшегося фибринового сгустка. Состав ростовой среды представлен в табл. 3.


4. Удаление фибринового сгустка из ростовой среды с ЛТ.
Фибриновый сгусток отделяли от стенок флакона и центрифугировали (Eppendorf 581 OR, Германия) при 280g в течение 10 минут при комнатной температуре с последующим декантированием супернатанта в стеклянный или пластиковый флакон.
5. Фильтрация ростовой среды с ЛТ без фибрина.
Супернатант после центрифугирования пропускали через сито 40 мкм (BD, США) и далее использовали как полную ростовую среду для культивирования клеток.
6. Проверка функциональной активности образца пулированного лиофилизированного ЛТ в составе ростовой среды, содержащей гепарин, на модели культивирования перевивной клеточной линии остеосаркомы человека (MG-63) и иммортализованных фибробластов кожи человека (ФЧ).
Сравнительные эксперименты in vitro по оценке динамики роста культур MG-63 и ФЧ (штамм 1608h TERT) с использованием пулированного образца ЛТ доноров и образца ЭТС (РАА, Австрия, лот № А10106-0671) в качестве ростовых добавок к среде культивирования из п. 5 осуществляли в 96-луночных планшетах (Corning, США) с плотностью посева 1,5×104 кл./см2 и со сменой среды дважды в неделю. На сроках культивирования 1, 3, 6 суток определяли пул жизнеспособных клеток с помощью МТТ-теста (МТТ, Sigma, США). Для проведения МТТ-теста по окончании срока культивирования из каждой лунки отбирали по 100 мкл среды и вносили по 25 мкл раствора МТТ в концентрации 5 мг/мл. Через 3 ч инкубации в термостате (Sanyo МСО-20AIC, Япония) при 5% СО2, 37°C из каждой лунки полностью удаляли среду и производили растворение образовавшегося формазана с помощью изопропилового спирта (200 мкл/лунку). От осадка, образующегося в результате преципитации белков в изопропиловом спирте, освобождались центрифугированием планшета в течение 10 мин при 3000 об/мин (Jouan, Франция). Далее из каждой лунки переносили по 100 мкл супернатанта в 96-луночный планшет для спектрофотометрии (Costar, США) и оценивали оптическую плотность (OD) раствора формазана на спектрофотометре FC (Thermoscientific, США) при длине волны 540 нм.
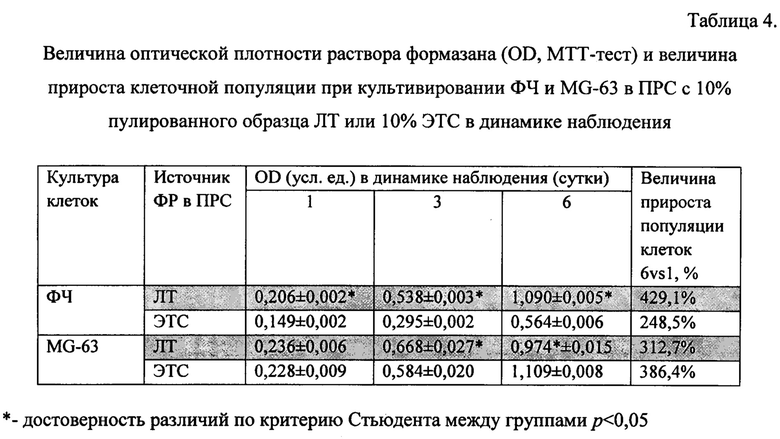
На основании результатов МТТ-теста рассчитывали величину прироста популяции клеток Д (в процентах) в конкретный срок наблюдения по формуле:
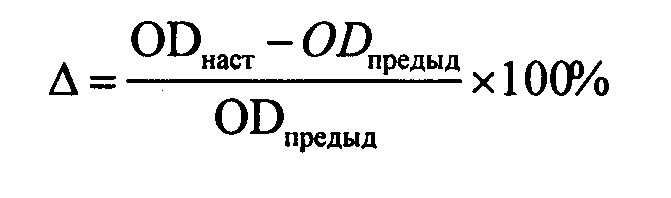
где ODнаст. - оптическая плотность раствора формазана в условных единицах в конкретный срок эксперимента, ODпред. - оптическая плотность раствора формазана в предыдущий срок эксперимента. Результаты оценки функциональной активности клеток при культивировании приведены в Таблице 4.
Показано, что при данном способе пулирования образцов ЛТ, популяция ФЧ при культивировании в ПРС, обогащенной 10% ЛТ, эффективно нарастает и, начиная с 3-х суток наблюдения, статистически достоверно превышает популяцию ФЧ в ПРС с 10% ЭТС. Так, показатель OD раствора формазана на 6-е сутки культивирования ФЧ в ПРС с 10% ЛТ составил 1,090 vs 0,564 при культивировании клеток в ПРС с 10% ЭТС, а величина прироста популяции ФЧ - 429% vs 248%, соответственно (табл. 4).
Скорость пролиферации клеток линии остеосаркомы человека MG-63 при условии ее культивирования в ПРС с 10% пулированного ЛТ доноров или в ПРС с 10% ЭТС при плотности посева 5 тыс. кл. на лунку практически не отличалась: величина OD раствора формазана составляла на 5 сутки 0,974 vs 1,109 для ПРС с 10% пула ЛТ и ПРС с 10% ЭТС, соответственно, а величина прироста - 313% и 386%, соответственно (табл. 4).
Пример конкретного исполнения №4.
1. Получение лиофилизированного ЛТ
Для приготовления ЛТ, очищенного от фибриногена, использовали лиофилизированный ЛТ, полученный по методике, описанной в «Примере конкретного исполнения №1»(п.п. 1-8).
2. Приготовление рабочего раствора ЛТ
Лиофилизированный ЛТ растворяли в стерильной воде для инъекций (ФС 2.2.0019.15), доводя до исходного объема образца до лиофилизации (10 мл).
3. Формирование фибринового сгустка
К растворенному ЛТ объемом 10 мл добавляли 0,02 мл 10% раствора CaCl2 («ПанЭко», Россия). Флакон с ЛТ в асептических условиях помещали в термостат (ТС-80М-2, Россия) или на водяную баню (Biosan WB-4MS) на 4 часа при 37°C для перевода фибриногена в нерастворимый фибрин, а затем в холодильник (Liebherr LKUv 1610, Германия) на 16-18 часов при 4°C для стабилизации образовавшегося фибринового сгустка.
4. Удаление фибринового сгустка из ЛТ.
Сгусток отделяли и центрифугировали (Eppendorf 5810R, Германия) при 280g в течение 10 минут при комнатной температуре с последующим декантированием супернатанта в стеклянный или пластиковый флакон.
5. Фильтрация.
Супернатант ЛТ после центрифугирования (п. 4) пропускали через сито с диаметром отверстий 40 мкм (BD, США).
6. Приготовление полной ростовой среды, содержащей ЛТ без фибриногена.
Фильтрат объемом 10 мл вводили в среду, формируя ПРС, указанную в табл. 5.

7. Оценка функциональной активности полной ростовой среды с ЛТ.
Для исследования были взяты линии аденокарциномы молочной железы человека MCF-7 и карциномы гортани НЕр-2. Состав полной ростовой среды соответствовал таковому в табл. 6; в контроле 10% ЛТ был заменен на 10% ЭТС в этой же ПРС.
Культивирование проводили при исходной плотности посева клеток 1,5×104 клеток/см2. Жизнеспособность клеток была оценена по изменению OD раствора формазана в МТТ-тесте на 1-14-е сутки в 4-х повторах. Параллельно в 96-луночных планшетах с помощью системы для прижизненного мониторинга клеток in vitro IncuCyte® ZOOM™ (Essen Bioscience, США) визуально оценивали состояние клеточного монослоя и количественно - степень конфлюентности последнего.
Как ЭТС, так и ЛТ обеспечивали пролиферацию клеток при их культивировании в течение 7 суток. В то же время, для НЕр-2 значения OD в МТТ-тесте при использовании ЛТ были значимо выше, в сравнении с таковыми для ЭТС на 3-й сутки (0,556±0,013 vs 0,432±0,005) и значимо ниже - на 7-е сутки (0,664±0,017 vs 0,726±0,009) - табл. 6.
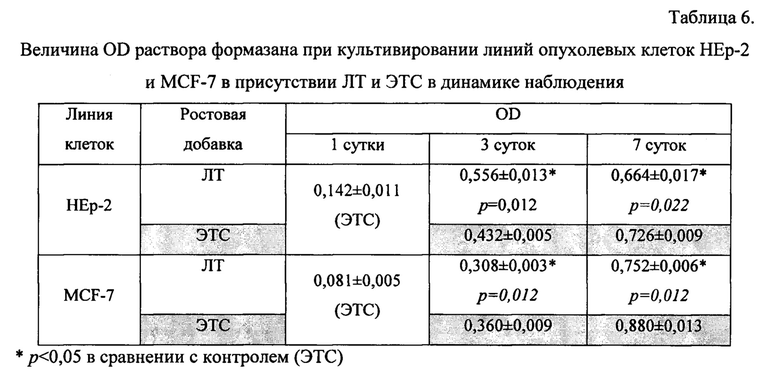
Представленные данные свидетельствуют о том, что в присутствии 10% ЛТ клетки НЕр-2 начинают пролиферировать активнее, чем в присутствии 10% ЭТС, быстрее достигают предконфлюентного монослоя, замедляя пролиферацию вследствие контактного торможения.
ЛТ и ЭТС поддерживали и пролиферацию клеток MCF-7. В то же время значения OD в присутствии ЛТ были значимо ниже в сравнении с ЭТС на 3-й и 7-е сутки (0,308±0,003 vs 0,360±0,009 и 0,752±0,006 vs 0,880±0,013) (Табл. 6).
Визуально определяли нарастание плотности монослоя клеток обеих линий уже через 3 суток культивирования в присутствии обеих ростовых добавок: средняя степень конфлюентности для ЛТ и ЭТС составила 99,7% и 99,5% для НЕр-2, соответственно, и ~ 100% для обеих ростовых добавок для MCF-7. Клетки в среде с ЛТ сохраняли характерную для них морфологию (Фиг. 2, Фиг. 3).
Таким образом, среда для культивирования линий опухолевых клеток НЕр-2 и MCF-7, содержащая в качестве ростовой добавки ЛТ, полученный растворением лиофилизата ЛТ, и не содержащий фибриногена и гепарина, поддерживает пролиферацию ММСК in vitro в сходной с ЭТС степени.
Пример конкретного исполнения №5.
1. Получение лиофилизированного ЛТ.
Лиофилизированный, стандартизованный по функциональной активности ЛТ был получен в соответствии с пп. 1-8 «Примера конкретного исполнения №1».
2. Оценка регенеративной активности ЛТ при накожном применении.
Нами был апробирован способ накожного применения 10% раствора лиофилизированного ЛТ у крыс с эксцизионной раной кожных покровов для ускорения заживления последних.
Перед операцией крысам под наркозом (дроперидол 2,5 мг/мл, внутрибрюшинно по 0,5 мл, кетамин 5% раствор, внутримышечно по 0,25 мл) выбривали шерсть на спине и в области лопаток формировали с помощью пинцета и ножниц плоскостной полнослойный кожный дефект площадью 0,2-0,3 см2. Область раны закрывали стерильной 4-х слойной салфеткой Medicomp (Hartmann AG, Германия) и гипоаллергенным воздухопроницаемым пластырем Fixopore S (Matorat, Польша). На 4-е сутки животных освобождали от повязок и далее кожные раны вели открытыми. Содержание животных после операционного вмешательства было одиночным. Всего было сформировано три группы животных по 6 голов в каждой: 1 - контроль (ежедневная обработка раны 0,9% раствором NaCl); 2 - опыт (ежедневная обработка области раны 20% раствором ЛТ; 3 - опыт (ежедневная обработка области раны 100% раствором ЛТ). Объем средства (0,9% раствор NaCl / 20% раствор ЛТ / 100% раствор ЛТ) для однократной обработки одной раны составлял 70 мкл.
На 7-е и 13-е сутки из каждой группы выводили по 3 животных из эксперимента путем передозировки эфирного наркоза и осуществляли забор биологического материала для гистологического исследования. Из иссеченных фрагментов изготавливали парафиновые блоки. Окрашенные гематоксилин-эозином гистологические срезы изучали с помощью световой микроскопии. Эксперимент завершили, когда в группе 3 кожный дефект закрылся полностью (13-е сутки после операции).
В норме эпидермис межлопаточной области представлен плоским ороговевающим эпителием. Кератиноциты базального слоя кубической формы, расположены в один ряд, в зернистом и шиповатом слоях насчитывается по 2-3 ряда клеток, роговой слой достаточно узкий. Малоклеточная дерма представлена сосочковым и сетчатым слоями, в которых определяются равномерно расположенные волосяные фолликулы и сальные железы (Фиг. 5, А, Б).
На 7-е сутки после операции в контрольной группе животных область раны была заполнена богато васкуляризированной молодой грануляционной тканью с хаотично расположенными фиброб ластами. На поверхности неэпителизированной раны определялся слой фибрина, под которым визуализировалась тонкая «полоска» лимфоидной инфильтрации. С краев раны - гипертрофированный отечный эпителий, представленный 9-10 рядами рыхло расположенных клеток (Фиг. 5, В, Г).
На 13-й день после формирования дефекта кожный регенерат был покрыт сплошным многослойным (8-10 слоев) рыхлым эпителием. Дерма представлена еще васкуляризованной грануляционной тканью, однако зрелые фибробласты ближе к поверхности раны располагались более разреженно параллельно поверхности кожи. Признаков отека и воспаления не обнаружено (Фиг. 5, Д, Е).
Во 2-й группе (20% ЛТ) уже на 7-е сутки была выявлена полная эпителизация раневой поверхности: сглаженный эпителий из 6-8 слоев над кратерообразной раной и гипертрофированный (отечный) в области ее краев. Незрелая грануляционная ткань пронизана большим количеством сосудов, однако фибробласты и соединительнотканные волокна располагались в ближайшей к ране области уже параллельно поверхности кожи, что косвенно свидетельствует о начале фиброзной трансформации грануляционной ткани, т.е. ее созревании (Фиг. 6, А, Б). На 13 сутки процесс формирования кожного регенерата продолжался. Это выражалось, с одной стороны, в формировании сплошного широкого многорядного эпителия с вертикальной анизоморфностью, запустевании сосудов в сосочковом отделе дермы, в упорядочении ориентации соединительнотканных волокон в области дефекта и уменьшении количества фибробластов, появлении зачатков волосяных фолликулов (Фиг. 6, В, Г). Наблюдаемая в присутствии ЛТ быстрая эпителизация является протектором рубцовых образований.
В третьей группе животных обработка раневой поверхности 100% ЛТ в течение 7 дней привела к полной эпителизации раны: за это время в зоне кожного дефекта был сформирован многослойный (8-12 слоев) разреженный эпителий с четкой поляризацией клеток базального слоя. Под эпителием располагалась гиперплазированная дерма с сосудами, над ним - слой фибрина (Фиг. 7, А, Б)
Через 13 суток толщина эпителия кожного регенерата в этой группе животных и его строение, в целом, соответствовало эпителию межлопаточной области кожи спины интактных крыс, за исключением более сглаженного рисунка. В эти сроки были выявлены, как и в предыдущей опытной группе, признаки созревания грануляционной ткани: запустевание кровеносных сосудов и снижение их количества, обеднение клеточного состава дермы за счет снижения количества фибробластов, появление кожных дериватов в области регенерата и ориентация соединительнотканного компонента параллельно поверхности кожи (Фиг. 7, В, Г).
Таким образом, ЛТ стимулирует эпителизацию кожного дефекта и ускоряет формирование грануляционной ткани, причем, этот эффект нарастает с возрастанием концентрации ЛТ с 20% до 100%.
Пример конкретного исполнения №6.
1. Получение фибринового гидрогеля из ЛТ
Гидрогель на основе фибрина был получен из лиофилизированного ЛТ, согласно п.п. 1-2 «Примера конкретного исполнения №3». К ростовой среде состава: среда F12 (ПанЭко, Россия), глютамин (ПанЭко, Россия) 0,44 мг/мл, гентамицин (ПанЭко, Россия) 1,25 мкг/мл, буферный раствор HEPES 1 мМ (ПанЭко, Россия) 1 мл/100 мл среды, добавляли 10-15% растворенного ЛТ. Полученную ПРС использовали сразу после приготовления.
2. Культивирование микроорганов (фрагментов щитовидной железы) и клеток (тиреоцитов) в фибриновом гидрогеле на основе ЛТ.
В пробирку со свежеприготовленной ПРС (~ 1,0 мл) в асептических условиях вносили взвесь (50,0-100,0 мг) фрагментов ткани измельченной механическим способом нормальной щитовидной железы (ЩЖ, операционный материал после тиреоидэктомии), осторожно перемешивали, переносили в полупроницаемые мембраны Transwell (Corning, США) и помещали в 6-луночные планшеты (Corning, США). Планшеты помещали в СО2-инкубатор (Sanyo MCO-20AIC, Япония) на 4 ч для формирования гидрогеля при 37°C, 5% СО2. Затем на дно лунки 6-луночного планшета вносили по 1 мл ПРС состава: среда F12 (ПанЭко, Россия), глютамин (ПанЭко, Россия) 0,44 мг/мл, гентамицин (ПанЭко, Россия) 1,25 мкг/мл, буферный раствор HEPES 1 мМ (ПанЭко, Россия) 1 мл/100 мл среды, 5% ЭТС (Gibco, США). Планшеты помещали в CO2-инкубатор (Sanyo MCO-20AIC, Япония) и поддерживали микрокультуру при 37°C, 5% СО2. В процессе культивирования периодически производили добавление ПРС состава, указанного в п. 1, для формирования гидрогеля на основе ЛТ, с параллельным отбором такого же количества жидкой фазы со дна лунки планшета. Оценку состояния клеток в гидрогеле осуществляли методом световой микроскопии.
На Фиг. 4 показано спонтанное формирование фолликулов ЩЖ из одиночных тиреоцитов через 2,5 месяца культивирования.
Таким образом, гидрогель на основе ЛТ человека способствует формированию органоспецифических структур ЩЖ при долгосрочном культивировании.
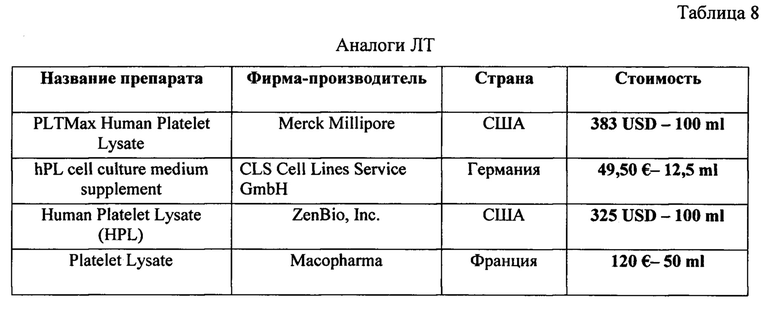
Важно отметить, что замена ЭТС на ЛТ человека в качестве ростовой добавки для культивирования исключает трансмиссию бактериальных, вирусных, прионных и иных неиндентифицированных инфекционных агентов, а также аллергические реакции на ксеногенные компоненты при производстве биомедицинских клеточных продуктов, предназначенных для введения в организм человека. В этом плане экономический эффект определяется производством ЛТ в качестве импортозамещающего аналога имеющихся на рынке препаратов (табл. 8), отличающегося от них рядом значимых признаков и преимуществ, в соответствии с формулой изобретения.
Анализ источников показал, что описанный способ получения лиофилизированного лизата тромбоцитов крови человека и 4-х продуктов на его основе, в том числе гидрогеля, не имеет аналогов.
Полученные таким образом продукты на основе ЛТ предназначены для:
- культивирования клеток (стволовых, дифференцированных, опухолевых) клеточных ассоциатов (сфероидов) и микроорганов в 2D и 3D вариантах.
- формирования тканеинженерных 3D конструкций и 3D биопечати.
- накожного применения в целях регенеративной медицины: заживление хронических ран, трофических язв, предотвращения рубцевания, а также для создания косметических средств ухода за кожей и против морщин.
Гидрогель на основе ЛТ, представленный в настоящей заявке, является оригинальным продуктом. Использование гидрогеля на основе лиофилизированного ЛТ человека (который представляет собой смесь в физиологических соотношениях биоактивных молекул плазмы крови и тромбоцитов) облегчит, а в ряде случаев сделает возможным тканеинженерное органотипическое конструирование эквивалентов органов и тканей in vitro.
И, наконец, ЛТ человека, сделанный по представленному методу, проявил выраженные свойства регенератора дефектов кожных покровов. Использование его в этом аспекте будет способствовать трудовой и социальной реабилитации больных с плохо заживающими после оперативных вмешательств кожными ранами (например, у пожилых людей, у онкологических больных после лучевой терапии с последующим оперативным вмешательством), при трофических язвах (при диабете, критической ишемии нижних конечностей).
При производстве ЛТ из ТМ может быть использована тромбоцитарная масса с истекающим сроком годности, который составляет лишь несколько дней и обусловлен разрушением тромбоцитов, которое препятствует ее клиническому использованию, но является первым этапом получения ЛТ. Таким образом, может быть произведена реутилизация биологического материала с формированием новых высокоактивных продуктов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РОСТОВОЙ ДОБАВКИ НА ОСНОВЕ ЛИЗАТА ТРОМБОЦИТОВ ИЗ ТРОМБОЦИТАРНОЙ МАССЫ ДОНОРОВ К СРЕДЕ ДЛЯ НАРАЩИВАНИЯ КЛЕТОЧНОЙ МАССЫ СТВОЛОВЫХ, ПРОГЕНИТОРНЫХ, ДИФФЕРЕНЦИРОВАННЫХ И ОПУХОЛЕВЫХ КЛЕТОК | 2016 |
|
RU2648162C2 |
| Способ получения аутологичного лизата тромбоцитов в качестве основы для клеточных биомедицинских препаратов ветеринарной медицины | 2020 |
|
RU2732150C1 |
| Роботизированная медицинская система и манипулятор для 3D-биопечати для полнослойного закрытия кожного дефекта | 2023 |
|
RU2814949C1 |
| СПОСОБ СОЗДАНИЯ БИОРЕЗОРБИРУЕМОГО КЛЕТОЧНОГО СКАФФОЛДА НА ОСНОВЕ ФИБРИНА ПЛАЗМЫ КРОВИ | 2017 |
|
RU2653434C1 |
| Биотрансплантат для лечения дисплазии суставов и способ его получения | 2017 |
|
RU2659204C1 |
| СПОСОБ ПРОФИЛАКТИКИ ОСТРОЙ РЕАКЦИИ ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА ПОСЛЕ ТРАНСПЛАНТАЦИИ АЛЛОГЕННОГО КОСТНОГО МОЗГА | 2010 |
|
RU2454247C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ЛИЗАТА ТРОМБОЦИТОВ С ВЫСОКИМ СОДЕРЖАНИЕМ ФАКТОРОВ РОСТА | 2020 |
|
RU2739515C1 |
| СЫВОРОТОЧНАЯ ФРАКЦИЯ ОБОГАЩЕННОГО ТРОМБОЦИТАМИ ФИБРИНА | 2014 |
|
RU2711330C2 |
| Способ лечения остеоартроза коленного сустава | 2017 |
|
RU2688176C2 |
| Среда для культивирования клеток костного мозга, предназначенных для клеточной терапии | 2020 |
|
RU2756926C1 |


Изобретение относится к области клеточной биологии и биотехнологии, в частности к получению культуральной ростовой добавки для культивирования опухолевых клеток. Способ включает нормирование образца тромбоцитарной массы (ТМ) по содержанию тромбоцитов путем центрифугирования ТМ при 3130 g в течение 40 минут при 20°C и ресуспендирование осадка в супернатанте заданного объема до концентрации тромбоцитов 1,75×109 клеток/мл, 3-кратный температурный лизис тромбоцитов путем замораживания на сутки до -80°C и размораживания при +37°C. Далее осуществляется осаждение клеточного дебриса путем центрифугирования при 3130 g, 40 минут, 20°C, сбор супернатанта, микроскопический контроль (×200) на наличие в поле зрения не более 3-х фрагментов тромбоцитов, стандартизация путем пулирования равных по объему образцов, полученных из ТМ не менее 12 доноров обеих тендерных групп, далее центрифугирование пулированного ЛТ при 3130 g, 40 минут, 20°C и фильтрация образца на фильтрах 0,45 мкм и 0,22 мкм, наконец, разливание по аликвотам требуемого объема и лиофилизация. Изобретение позволяет осуществить больший прирост опухолевых клеток линии НТ-29, MCF-7 и MG-63 и сходный прирост опухолевых клеток линии HCT-116 и HEp-2. 7 ил., 9 табл., 6 пр.
Способ получения культуральной ростовой добавки для культивирования опухолевых клеток, включающий нормирование образца тромбоцитарной массы (ТМ) по содержанию тромбоцитов путем центрифугирования ТМ при 3130 g в течение 40 минут при 20°C и ресуспендирование осадка в супернатанте заданного объема до концентрации тромбоцитов 1,75×109 клеток/мл, 3-кратный температурный лизис тромбоцитов путем замораживания на сутки до -80°C и размораживания при +37°C, осаждение клеточного дебриса путем центрифугирования при 3130 g, 40 минут, 20°C, сбор супернатанта, микроскопический контроль (×200) на наличие в поле зрения не более 3-х фрагментов тромбоцитов, и далее его стандартизацию путем пулирования равных по объему образцов, полученных из ТМ не менее 12 доноров обеих тендерных групп, далее центрифугирование пулированного ЛТ при 3130 g, 40 минут, 20°C и осуществление фильтрации образца на фильтрах 0,45 мкм и 0,22 мкм, наконец разливание по аликвотам требуемого объема и лиофилизация.
| СПОСОБ ПОЛУЧЕНИЯ РОСТОВОЙ ДОБАВКИ НА ОСНОВЕ ЛИЗАТА ТРОМБОЦИТОВ ИЗ ТРОМБОЦИТАРНОЙ МАССЫ ДОНОРОВ К СРЕДЕ ДЛЯ НАРАЩИВАНИЯ КЛЕТОЧНОЙ МАССЫ СТВОЛОВЫХ, ПРОГЕНИТОРНЫХ, ДИФФЕРЕНЦИРОВАННЫХ И ОПУХОЛЕВЫХ КЛЕТОК | 2016 |
|
RU2648162C2 |
| GUDRUN W., et al | |||
| "Human Platelet Lysate Gel Provides a Novel Three Dimensional-Matrix for Enhanced Culture Expansion of Mesenchymal Stromal Cells", Tissue Engineering Part C: Methods | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| ТЕХНОЛОГИЯ ЛИОФИЛИЗАЦИИ ОБОГАЩЕННОЙ ТРОМБОЦИТАМИ ПЛАЗМЫ С СОХРАНЕНИЕМ ЖИЗНЕСПОСОБНОСТИ ФАКТОРОВ TGF PDGF VEGF | 2012 |
|
RU2506946C1 |
| Способ получения искусственной кожи | 1978 |
|
SU826966A3 |
Авторы
Даты
2018-08-17—Публикация
2017-08-18—Подача