Область техники
Данное изобретение относится к химии органических соединений, фармакологии и медицине и касается терапии заболеваний, связанных с аберрантной активностью клеток иммунной системы, предпочтительно терапии заболеваний органов брюшной полости, в частности терапии перитонитов, нефропатий, болезни Крона и язвенного колита посредством применения соединения, обладающего эффективностью в модулировании фермента глутаминилциклазы, вовлеченной, в частности, в процессы посттрансляционной модификации хемокинов и хемотаксиса клеток иммунной системы.
Уровень техники
Хемотаксис или направленное движение клеток иммунной системы по градиенту концентрации некоторых эндогенных и экзогенных веществ (хемоаттрактантов) является одной из важнейших составных частей функционирования клеток иммунной системы. Избыточный приток клеток иммунной системы, как правило, вызывает избыточную активность клеток иммунной системы и повреждению окружающих органов и тканей. Понимание участников и процессов, связанных с процессом хемотаксиса, на молекулярном уровне может привести к новых эффективным подходам в лечении и профилактике целого ряда заболеваний, связанных с аберрантной активностью клеток иммунной системы.
Хемокины семейства CCL (CCL2, CCL7, CCL8, CCL13), являющиеся лигандами рецептора ССR2, являются наиболее мощными факторами хемотаксиса моноцитов и макрофагов в организме млекопитающих (Biochem J. 2012 Mar 1; 442(2):403-12). Хемокины семейства CCL составляют важный класс цитокинов, необходимых для активации нейтрофилов и моноцитов и привлечения этих клеток в очаг воспаления. Однако высокие концентрации хемокинов как правило вызывают избыточный приток клеток иммунной системы. Аберрантная активность клеток иммунной системы может привести к серьезным повреждением окружающих органов и тканей. Например, в ряде случаев продукты окисления липидов могут активировать клетки эндотелия сосудов (интиму), что приводит к выделению CCL2, привлечению макрофагов, которые, в свою очередь выделяют маркеры воспаления, провоцирующие повреждение артериальной стенки и развитие атеросклероза (Mol Cell. 1998 Aug;2(2):275-81; Nature. 1998 Aug 27;394(6696):894-7). Известна роль хемокинов семейства CCL в патофизиологии целого ряда аутоиммунных и аллергических состояний, опосредованных аберрантной активностью моноцитов CCR2+, CD14+ и CD16lo (ревматоидный артрит, рассеянный склероз). Кроме того, хемокины семейства CCL (в частности CCL2) вовлечены в патогенез метаболического синдрома, хронической боли, фиброза и некоторых форм рака.
Подавление аберрантной активности клеток иммунной системы, за счет ингибирования CCL-опосредованного хемотаксиса, может быть крайне востребовано для терапии целого круга заболеваний, таких как болезнь Крона, язвенный колит, перитониты и нефропатии. Например, в случае диабетической нефропатии воздействие высоких концентраций глюкозы приводит к увеличению секреции CCL2 тубулярными клетками почек, что в свою очередь вызывает миграцию моноцитов (Kidney Int. 2006 Jan;69(1):73-80). Увеличение концентрации моноцитов в тканях почек и их созревание в макрофаги, вызывает развитие аберрантного ответа ассоциированного с выделением большего количества хемокинов (ROS, TNFα, IL-1, IL-6) и активных форм кислорода, повреждающих окружающие клетки почек (Mediators Inflamm. 2012;2012:146154). Повреждение ткани почек приводит к развитию и сохранению аберрантной активности клеток иммунной системы и дальнейшему разрушению тканей почек. В in vivo моделях диабетической нефропатии блокада взаимодействия CCL2/CCR2 низкомолекулярными антагонистами показала значительную эффективность (Nephrol Dial Transplant. 2013 Jul;28(7):1700-10).
Члены семейства CCL (CCL2, CCL7, CCL8, CCL13), а также ряда других гормонов и секретируемых белков, содержат остаток пироглутаминовой кислоты (pE), роль которого заключается в защите от деградации аминопептидазами (Chem Immunol. 1999;72:42-56; Biochemistry. 1999 Oct 5;38(40):13013-25). Пироглутаминирование N-концевого остатка глутамина является посттрансляционной модификацией белка, и катализируется ферментами глутаминилциклазой (QPCT или QC) (J Biol Chem. 2003 Dec 12;278(50):49773-9) и изо-глутаминилциклазой (QPCTL или isoQC) (J Mol Biol. 2008 Jun 20;379(5):966-80). Обе изоформы фермента представляют собой близкие по структуре и субстратной специфичности белки с различной локализацией: глутаминилциклаза является секретируемым белком, в то время как изоглутаминилциклаза находится внутри клетки и закреплена в аппарате Гольджи (J Mol Biol. 2008 Jun 20;379(5):966-80).
В ходе экспериментальных исследований было показано, что ингибирование глутаминилциклаз приводит к резкому снижению хемоаттракторной активности непироглутаминированных форм хемокинов CCL2, CCL7, CCL8 и CCL13 (Biochem. J. (2012) 442, 403-412). Таким образом, пироглутаминирование хемокинов семейства CCL, является необходимым этапом CCL-опосредованного хемотаксиса моноцитов, а стратегия, направленная на ингибирование глутаминилциклазы является стратегией модулирования аберрантной активности клеток иммунной системы.
К настоящему времени известны ингибиторы глутаминилциклазы, включающие сульфолипиды (WO 2017/046256), производные флаваноидов (Bioorg Med Chem. 2016 May 15;24(10):2280-6), производные пиридина (US 2015/0291632) и некоторые небольшие молекулы, описанные в работах последнего времени (J Med Chem. 2017 Mar 23;60(6):2573-2590; WO 2014/193974, US 2015/0291557). Наиболее близкие аналоги, соединения, являющегося предметом настоящего изобретения, приведены в публикациях компании Probiodrug Aktiengesellschaft (J Biol Chem. 2003 Dec 12;278(50):49773-9). В данной работе описаны ингибиторы глутаминилциклазы на основе производных имидазола. Однако, в структурах соединений, опубликованных компанией Probiodrug Aktiengesellschaft, имидазол содержит алифатический заместитель на одном из атомов азота. Введение алифатического заместителя снижает метаболическую стабильность соединений. Кроме того, введение алифатического заместителя увеличивает гидрофобность соединений и облегчает проникновение соединения через гемато-энцефалический барьер, что не требуется для подавления аберрантной активности клеток иммунной системы и потенциально может привести к возникновению побочных эффектов.
На сегодняшний день нет ни одного препарата, действующего как ингибитор глутаминилциклазы, который бы применяли в терапии заболеваний, связанных с аберрантной активностью клеток иммунной системы, поэтому сохраняется потребность в создании и внедрении в клинику новых эффективных лекарственных средств на основе ингибиторов глутаминилциклазы.
Данное изобретение касается применения соединения, обладающего эффективностью в модулировании глутаминилциклазы, в терапии заболеваний, связанных с аберрантной активностью клеток иммунной системы, предпочтительно терапии заболеваний органов брюшной полости, в частности терапии перитонитов, заболеваний почек (в том числе являющиеся осложнениями других заболеваний (диабетическая нефропатия) или побочным эффектом применения лекарственных препаратов), болезни Крона, язвенного колита, а так же других заболеваний органов брюшной полости, связанных с аберрантной активностью клеток иммунной системы.
Раскрытие изобретения
Задачей настоящего изобретения является разработка нового модулятора глутаминилциклазы, более конкретно, ингибитора внутриклеточной и/или секретируемой изоформ глутаминилциклазы, и эффективного для лечения заболеваний, связанных с аберрантной активностью клеток иммунной системы, в особенности заболеваний органов брюшной полости, таких как болезнь Крона, язвенный колит, перитониты и нефропатии а так же прочих заболеваний связанных с аберрантной активностью клеток иммунной системы.
Техническим результатом данного изобретения является разработка и получение эффективного модулятора глутаминилциклазы, в частности соединения, обладающего высокой ингибирующей активностью по отношению к внутриклеточной и/или секретируемой изоформам глутаминилциклазы и хорошими фармакокинетическими характеристиками (в частности, существенным превышением экспозиции ингибитора в органах-мишенях (почки, селезенка) по сравнению с плазмой крови), позволяющих использовать данное соединение для лечения заболеваний, связанных с аберрантной активностью клеток иммунной системы, в особенности заболеваний органов брюшной полости, таких как болезнь Крона, язвенный колит, перитониты и нефропатии (в частности диабетической нефропатии), а так же прочих заболеваний связанных с аберрантной активностью клеток иммунной системы, в частности с аберрантным хемотаксисом клеток иммунной системы.
Указанный технический результат достигается путем применения соединения N,N'-бис[2-(1H-имидазол-4-ил)этил]изофталамида формулы
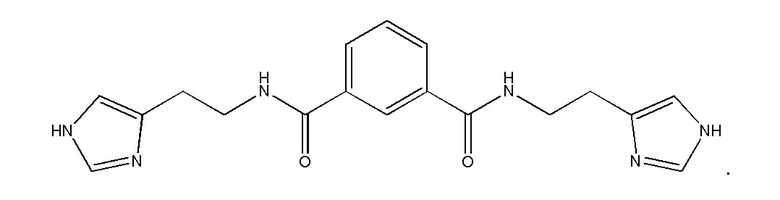
или его фармацевтически приемлемой соли, гидрата, сольвата в качестве модулятора, в частности, ингибитора внутриклеточной и/или секретируемой изоформ глутаминилциклазы.
Указанный технический результат достигается также посредством применения соединения N,N'-бис[2-(1H-имидазол-4-ил)этил]изофталамида или его соли, гидрата, сольвата для изготовления лекарственного средства для предупреждения и/или лечения расстройства, опосредованного активностью глутаминилциклазы.
Указанный технический результат достигается также посредством применения соединения N,N'-бис[2-(1H-имидазол-4-ил)этил]изофталамида или его соли, гидрата, сольвата для изготовления лекарственного средства для предупреждения и/или лечения расстройства, связанного с аберрантной активностью клеток иммунной системы, в частности с аберрантным хемотаксисом клеток иммунной системы.
В рамках изобретения находится лекарственное средство, включающее соединение формулы
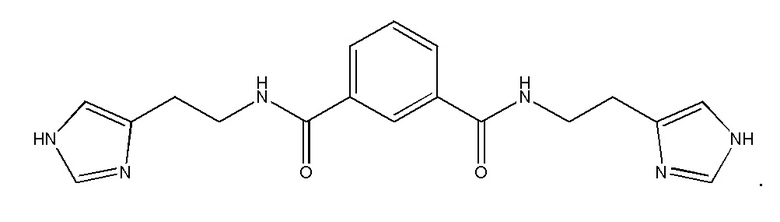
или его фармацевтически приемлемую соль.
Кроме того, изобретение предусматривает фармацевтические композиции для предупреждения и/или лечения расстройства, связанного с активностью глутаминилциклазы и/или с аберрантной активностью клеток иммунной системы, в частности с аберрантным хемотаксисом клеток иммунной системы, и характеризующиеся тем, что они содержит эффективное количество соединения по изобретению и, по меньшей мере, одно фармацевтически приемлемое вспомогательное вещество. В некоторых вариантах воплощениях изобретения вспомогательное вещество представляет собой фармацевтически приемлемый носитель и/или эксципиент.
Изобретение также включает способ предупреждения и/или лечения расстройства, связанного с активностью глутаминилциклазы в организме, включающий введение в указанный организм лекарственного средства по изобретению. Такое расстройство, связанное с активностью глутаминилциклазы, представляет собой заболевание, связанное с аберрантной активностью клеток иммунной системы, в частности с аберрантным хемотаксисом клеток иммунной системы, в особенности заболевание органов брюшной полости. В некоторых неограничивающих вариантах воплощения изобретения заболевание органов брюшной полости представляет собой болезнь Крона, язвенный колит, перитонит, нефропатию (в частности диабетическую нефропатию). В частных случаях воплощения изобретения организм представляет собой человека или животного.
Соединение N,N'-бис[2-(1H-имидазол-4-ил)этил]изофталамид описано в заявке на изобретение RU 2013/116822.
Подробное раскрытие изобретения
Получение Соединения 1, медицинское применение которого являющегося предметом настоящего изобретения, описано в заявке на изобретение RU 2013/116822. В указанной патентной заявке описаны производные бисамидов дикарбоновых кислот, обладающие способностью к комплексообразованию или хелатированию ионов металлов, а также их применение в качестве средства для профилактики и/или лечения вирусного гепатита, ВИЧ-инфекции, онкологических, нейродегенеративных, сердечнососудистых, воспалительных заболеваний, диабета, геронтологических заболеваний, заболеваний, вызываемых токсинами микроорганизмов, а также алкоголизма, алкогольного цирроза печени, анемии, поздней порфирии, отравлений солями переходных металлов.
В ходе исследований специфической фармакологической активности Соединения 1 в моделях различных заболеваний неожиданно было установлено, что применение Соединения 1 достоверно снижает приток клеток иммунной системы. Таким образом, было показано, что Соединение 1 влияет на хемотаксис клеток иммунной системы. Снижение притока клеток иммунной системы может применяться в терапии целого ряда заболеваний, связанных с аберрантной активностью клеток иммунной системы, в частности заболеваний органов брюшной полости, таких как болезнь Крона, язвенный колит, перитониты и нефропатии (частности диабетической нефропатии). Поскольку влияние на хемотаксис не может быть предсказано или объяснено способностью соединения к комплексообразованию или хелатированию ионов металлов, была предпринята попытка поиска возможных терапевтических мишеней Соединения 1.
Поиск возможных терапевтических мишеней, с использованием методов вычислительной химии, молекулярного моделирования и in vitro испытаний на ферментном препарате позволил обнаружить, что наблюдаемый терапевтический эффект Соединения 1 связан со способностью данного соединения ингибировать активность глутаминилциклазы.
В ходе дальнейших исследований фармакокинетики Cоединения 1 оказалось, что в результате перорального применения вещества наибольшие концентрации наблюдаются в печени, почках и других органах брюшной полости.
Таким образом, Соединение 1 является новым ингибитором глутаминилциклазы, который влияет на хемотаксис клеток иммунной системы и может применяться для терапии заболеваний, связанных с аберрантной активностью клеток иммунной системы, предпочтительно заболеваний органов брюшной полости, таких как болезнь Крона, язвенный колит, перитониты, нефропатии, в частности диабетической нефропатии, а так же других заболеваний органов брюшной полости, связанных с аберрантной активностью клеток иммунной системы.
Термины и определения
Термин «Соединение 1» относится к N,N'-бис[2-(1H-имидазол-4-ил)этил]изофталамиду, представленному структурной формулой:
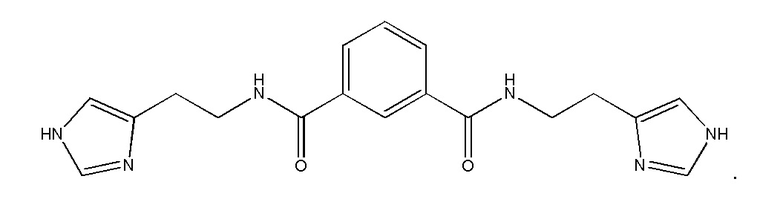
Термин «С», когда он используется со ссылкой на температуру, означает температурную шкалу Цельсия.
Термин «IC50» означает концентрацию тестируемого соединения, при которой достигается полумаксимальное ингибирование фермента.
Термин «фармацевтически приемлемые соли» или «соли» включает соли соединения 1, которые получены взаимодействием с относительно нетоксичными кислотами. Примерами фармацевтически приемлемых солей могут служить соли, образованные неорганическими кислотами, такими как соляная, бромоводородная, фосфорная, серная и хлорная кислоты, или органическими кислотами, такими как уксусная, щавелевая, малеиновая, винная, янтарная, лимонная или малоновая кислоты, или полученные другими методами, используемыми в данной области, например, с помощью ионного обмена. К другим фармацевтически приемлемым солям относятся адипинат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептанат, гексанат, гидройодид, 2-гидрокси-этансульфонат, лактобионат, лактат, лаурат, лаурил сульфат, малат, малеат, малонат, метансульфонат (мезилат), 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, полуфумарат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат (тозилат), ундеканат, валериат и подобные.
Термин «сольват» используют для описания молекулярного комплекса, содержащего соединение по изобретению и одну или более молекул фармацевтически приемлемого растворителя, например этанола. Термин «гидрат» используется, когда указанным растворителем является вода.
Термин «аберрантная активность» клеток иммунной системы в настоящем документе означает активность, существенно отличающуюся от базового уровня активности клеток иммунной системы в организме при отсутствии патологии. Аберрантная активность может быть вызвана избыточным притоком клеток иммунной системы к органу или ткани, нарушением процессов, приводящих к активации клеток иммунной системы, дерегулированием процессов связанных с гибелью клеток иммунной системы, а также другими факторами.
Термин «вспомогательное вещество» означает любое фармацевтически приемлемое вещество неорганического или органического происхождения, входящее в состав лекарственного препарата или используемое в процессе производства, изготовления лекарственного препарата для придания ему необходимых физико-химических свойств.
Термин «AUC» (area under the curve) означает фармакокинетический параметр, характеризующий суммарную концентрацию лекарственного препарата в плазме крови в течение всего времени наблюдения. Математически определяется как интеграл от 0 до ∞ функции концентрации препарата (фармакокинетической кривой) в плазме крови от времени и равен площади фигуры, ограниченной фармакокинетической кривой и осями координат.
Термин «среда RPMI» (англ. Roswell Park Memorial Institute medium) означает среду для культур клеток и тканей. RPMI традиционно используется для выращивания лимфоидных клеток человека. Среда содержит значительное количество фосфата и имеет состав для выращивания в атмосфере с содержанием углекислого газа 5%.
Термин «глутаминилциклаза» означает фермент аминоацилтрансферазу, участвующую в преобразовании N-концевой группы глутамина в пироглутамин в различных пептидных субстратах. Образование N-концевого пироглутамата защищает биологически активные пептиды, гормоны и хемокины (например, тиреотропин-высвобождающий гормон, β-хемокиновый лиганд-2) от деградации экзопептидазами и в некоторых случаях может увеличивать аффинность лигандов к их рецепторам.
Термин «секретируемая глутаминилциклаза» означает одну из изоформ фермента глутаминилциклазы, содержащая секреторный N-концевой домен и преимущественно секретируемая клетками человека. Секретируемая глутаминилциклаза преимущественно экспрессируются в клетках нервной и иммунной систем.
Термин «внутриклеточная глутаминилциклаза» означает одну из изоформ фермента глутаминилциклазы, содержащая якорный N-концевой домен и преимущественно связанная с аппаратом Гольджи. Внутриклеточная глутаминилциклаза распространена повсеместно в клетках млекопитающих и человека.
Термин «хемотаксис» означает направленное движение клеток в ответ на химический раздражитель. В основе хемотаксиса лежит способность клетки отвечать на градиент концентрации хемотаксического медиатора. Хемотаксис является тем процессом, благодаря которому клетки иммунной системы покидают сосудистое русло и мигрируют в поврежденную ткань. Ведущую роль в хемотаксисе играют хемотаксические вещества (хемоатрактанты). Одним из наиболее мощных хемоатрактантов для моноцитов и макрофагов является хемокин CCL2.
Термины «лечение», «терапия» охватывают лечение патологических состояний у млекопитающих, предпочтительно у человека, и включают: а) снижение, б) блокирование (приостановку) течения заболевания, в) облегчение тяжести заболевания, т.е. индукцию регрессии заболевания, г) реверсирование заболевания или состояния, к которому данный термин применяется, или одного или более симптомов данного заболевания или состояния.
Термин «профилактика», «предотвращение» охватывает устранение факторов риска, а также профилактическое лечение субклинических стадий заболевания у млекопитающих, предпочтительно у человека, направленное на уменьшение вероятности возникновения клинических стадий заболевания. Пациенты для профилактической терапии отбирают на основе факторов, которые, на основании известных данных, обуславливают увеличение риска возникновения клинических стадий заболевания по сравнению с общим населением. К профилактической терапии относится а) первичная профилактика и б) вторичная профилактика. Первичная профилактика определяется как профилактическое лечение у пациентов, клиническая стадия заболевания у которых еще не наступила. Вторичная профилактика - это предотвращение повторного наступления того же или близкого клинического состояния заболевания.
Соединение 1 перспективно для лечения заболеваний, связанных с аберрантной активностью клеток иммунной системы, в особенности заболеваний связанных с аберрантным хемотаксисом клеток иммунной системы, предпочтительно терапии заболеваний органов брюшной полости, таких как болезнь Крона, язвенный колит, перитониты, нефропатии, в частности диабетической нефропатии, имеющих как системный, так и локальный характер, в том числе, обусловленных первичными патологическими изменениями в этих тканях, или связанных с различными заболеваниями или длительным приемом некоторых лекарственных препаратов. В некоторых частных вариантах соединения по изобретению могут быть использованы для лечения других заболеваний органов брюшной полости, связанных с аберрантной активностью клеток иммунной системы.
Способ терапевтического применения соединений
Предмет данного изобретения также включает способ лечения, подразумевающий введение субъекту, нуждающемуся в соответствующем лечении, терапевтически эффективного количества соединения 1. Под терапевтически эффективным количеством подразумевается такое количество соединения, вводимого или доставляемого пациенту, при котором у пациента с наибольшей вероятностью проявится желаемая реакция на лечение (профилактику). Точное требуемое количество может меняться от субъекта к субъекту в зависимости от возраста, массы тела и общего состояния пациента, тяжести заболевания, методики введения препарата, комбинированного лечения с другими препаратами и т.п.
Соединение по изобретению может быть введено в организм пациента в любом количестве (предпочтительно, суточная доза действующего вещества составляет до 0,5 г на пациента в сутки, наиболее предпочтительно, суточная доза составляет 5-50 мг/сутки) и любым путем введения (предпочтительно, пероральный путь введения), эффективным для лечения или профилактики заболевания.
После смешения соединения 1 с конкретным подходящим фармацевтически приемлемым носителем в желаемой дозировке, композиции, составляющие предмет изобретения, могут быть введены в организм человека или других животных перорально, парентерально, местно и другими традиционными понятными специалисту способами.
Введение может осуществляться как разово, так и несколько раз в день, неделю (или любой другой временной интервал), или время от времени. Кроме того, соединение может вводиться в организм пациента ежедневно в течение определенного периода дней (например, 2-10 дней), а затем следует период без приема (например, 1-30 дней).
В том случае, когда соединение 1 используют в составе режима комбинированной терапии, доза каждого из компонентов комбинированной терапии вводится в течение требуемого периода лечения. Соединения, составляющие комбинированную терапию, могут вводиться в организм пациента как единовременно, в виде дозировки, содержащей все компоненты, так и в виде индивидуальных дозировок компонентов.
Фармацевтические композиции
Изобретение также относится к фармацевтическим композициям, которые содержат соединение 1 или его фармацевтически приемлемую соль, гидрат или сольват (или пролекарственную форму или другое фармацевтически приемлемое производное) и один или несколько фармацевтически приемлемых носителей, адъювантов, растворителей и/или наполнителей, таких, которые могут быть введены в организм пациента совместно с соединением, применение которого составляет предмет данного изобретения, и которые не влияют на фармакологическую активность этого соединения, и являются нетоксичными при введении в дозах, достаточных для доставки терапевтического количества соединения.
Фармацевтические композиции, заявляемые в данном изобретении, содержат соединение 1 или его фармацевтический приемлемую соль совместно с фармацевтически приемлемыми носителями, которые могут включать в себя любые растворители, разбавители, дисперсии или суспензии, поверхностно-активные вещества, изотонические агенты, загустители и эмульгаторы, консерванты, вяжущие вещества, скользящие материалы и т.д., подходящие для конкретной формы дозирования. Материалы, которые могут служить фармацевтически приемлемыми носителями, включают, но не ограничиваются, моно- и олигосахаридами, а также их производными; желатин; тальк; эксципиенты, такие как какао-масло и воск для суппозиториев; масла, такие как арахисовое, хлопковое, сафроловое, кунжутное, оливковое, кукурузное и соевое масло; гликоли, такие как пропиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные вещества, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический раствор, раствор Рингера; этиловый спирт и фосфатные буферные растворы. Также в составе композиции могут быть другие нетоксичные совместимые скользящие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, пленкообразователи, подсластители, вкусовые добавки и ароматизаторы, консерванты и антиоксиданты.
Предметом данного изобретения являются также лекарственные средства, под которыми подразумевают фармацевтические композиции, состав которых оптимизирован для определенного пути введения в организм в терапевтически эффективной дозе, например, для введения в организм орально, местно, ингаляционно, например, в виде ингаляционного спрея, или внутрисосудистым способом, интраназально, подкожно, внутримышечно, а также инфузионным способом, в рекомендованных дозировках.
Лекарственныесредства данного изобретения могут содержать составы, полученные методами включения в липосомы, методами микрокапсулирования, методами приготовления наноформ препарата, или другими методами, известными в фармацевтике.
При получении композиции, например в форме таблетки, соединение 1 или его фармацевтически приемлемую соль смешивают с одним или несколькими фармацевтическими эксципиентами, такими как желатин, крахмал, лактоза, стеарат магния, тальк, кремнезем, аравийская камедь, маннит, микрокристаллическая целлюлоза, гипромеллоза или аналогичные соединения.
Таблетки могут быть покрыты сахарозой, целлюлозой или ее производным или другими веществами, подходящими для создания оболочки. Таблетки могут быть получены различными способами, такими как непосредственное сжатие, сухое или влажное гранулирование или горячее сплавление в горячем состоянии.
Фармацевтическая композиция в форме желатиновой капсулы может быть получена смешиванием соединения 1 или его фармацевтически приемлемой соли с другими компонентами и заполняя полученной смесью мягкие или твердые капсулы.
Для введения парентеральным путем используются водные суспензии, изотонические солевые растворы или стерильные растворы для инъекций, которые содержат фармакологически совместимые агенты, например пропиленгликоль или бутиленгликоль.
Примеры фармацевтических композиций
Для профилактики и/или лечения болезней человека, или животных используют, в частности, следующие составы (под «Веществом» подразумевают соединение 1 или его фармацевтически приемлемая соль):
Таблетка I мг/таблетка
Вещество 0.5
Микрокристаллическая целлюлоза 66.5
Карбоксиметилкрахмал натрия 2,3
Магния стеарат 0,7
Таблетка II мг/таблетка
Вещество 5.0
Микрокристаллическая целлюлоза 62.0
Карбоксиметилкрахмал натрия 2,3
Магния стеарат 0.7
Таблетка III мг/таблетка
Вещество 50
Микрокристаллическая целлюлоза 620
Карбоксиметилкрахмал натрия 23
Магния стеарат 7
Таблетка IV мг/таблетка
Вещество 50
Лактоза 223.75
Кроскармеллоза натрия 6.0
Кукурузный крахмал 15
Поливинилпироллидон (5% м/об. паста) 2.25
Стеарат магния 3.0
Таблетка V мг/таблетка
Вещество 200
Лактоза 182.75
Кроскармеллоза натрия 12.0
Кукурузный крахмал (5% м/об паста) 2.25
Стеарат магния 3.0
Капсула мг/капсула
Вещество 10
Лактоза 488.5
Магнезия 1.5
Состав для инъекций I (50 мг/мл)
Вещество 5.0% м/об
1M раствор гидроксида натрия 15.0% м/об
1M раствор соляной кислоты до pH 7.6
Полиэтиленгликоль 400 4.5% м/об
Вода для инъекций до 100%
Мазь 1 мл
Вещество 40 мг
Этанол 300 мкл
Вода 300 мкл
1-додецилазациклогептанон 50 мкл
Пропиленгликоль до 1 мл
Данные составы могут быть приготовлены в соответствии со стандартными фармацевтическими методиками. Таблетки (I)-(II) могут быть покрыты кишечнорастворимой оболочкой с использованием, например, фталата ацетата целлюлозы.
Применение Соединения 1 в комбинированной терапии
Несмотря на то что Соединение 1 по данному изобретению может быть введено в качестве индивидуального активного агента, его также можно использовать в сочетании с одним или несколькими другими агентами, в частности, другой агент может представлять собой антибиотик, нестероидное противовоспалительное средство (НПВС) или другое противовоспалительное средство, антигипертензивные средство, α-блокатор, цитостатический препарат и т.д. При совместном приеме внутрь терапевтические агенты могут представлять собой разные лекарственные формы, которые вводят одновременно или последовательно в разное время, либо терапевтические агенты могут быть объединены в одну лекарственную форму.
Фраза «комбинированная терапия» в отношении соединения данного изобретения в сочетании с другими активными агентами, означает одновременный или последовательный прием всех агентов, который так или иначе обеспечит благоприятное воздействие комбинации агентов. Совместное введение подразумевает, в частности, совместную доставку, например, в одной таблетке, капсуле, инъекции или в другой форме, имеющих фиксированное соотношение активных агентов, так же как и одновременную доставку в нескольких, отдельных лекарственных формах для каждого соединения соответственно.
Таким образом, введение соединения 1 или его фармацевтически приемлемой соли данного изобретения может быть осуществлено в сочетании с дополнительными методами лечения, известными специалистам в области профилактики и лечения соответствующих заболеваний, включающими применение антибактериальных, цитостатических и цитотоксических препаратов, препаратов для подавления симптомов или побочных эффектов одного из лекарств.
Если лекарственная форма представляет собой фиксированную дозу, такая комбинация использует соединение 1 или его фармацевтически приемлемую соль в приемлемом дозовом диапазоне. Соединение 1 по данному изобретению или его фармацевтически приемлемая соль также может быть введено в организм пациента последовательно с другими агентами, в том случае, когда совместное введение комбинаций указанных агентов невозможно. Изобретение не ограничено последовательностью введения; соединение данного изобретения может быть введено в организм пациента совместно, до или после введения другого препарата.
Примеры
1) Получение соединения по изобретению
Получение Соединения 1 описано в заявке на изобретение RU 2013/116822. В той же заявке описана способность Соединения 1 к комплексообразованию или хелатированию ионов металлов.
2) Характеристика биологической активности соединения по изобретению
Биологическая активность Соединения 1 была изучена в различных in vitro и in vivo экспериментах. В частности, при изучении активности Соединения 1 в различных in vitro и in vivo моделях было показано ингибирующее действие Соединения 1 на хемотаксис моноцитов, макрофагов и других клеток иммунной системы. Данное биологическое действие Соединения 1 не может быть предсказано или объяснено на основе предшествующих знаний о способности Соединения 1 к хелатированию ионов металлов.
Исследования биологической активности Соединения 1 in vitro позволили установить, что Соединение 1 является ингибитором фермента глутаминилциклазы и, таким образом, действие Соединения 1 на хемотаксис клеток иммунной системы может быть опосредованно ингибированием активности глутаминилциклазы.
2.1) Исследование влияния Соединения 1 на ферментативную активность внутриклеточной глутаминилциклазы человека in vitro.
В ходе исследований влияния Соединения 1 на ферментативную активность внутриклеточной глутаминилциклазы in vitro впервые было обнаружено прямое ингибирующее действие Соединения 1 на рекомбинантную внутриклеточную глутаминилциклазу человека.
Активность глутаминилциклазы при различных концентрациях Соединения 1 изучалась при 25°C с использованием флуоресцентного субстрата L-глутаминил-2-нафтиламида (Gln-bNA) (Anal Biochem. 2002 Apr 1;303(1):49-56). Реакционная смесь объемом 100 мкл содержала 50 мкМоль флуорогенного субстрата; ~0,2 единицы пироглутаминиламинопептидазы человека (1 единицу определяют как количество, гидролизующее 1 микромоль pGlu-bNA в минуту), и аликвоту рекомбинантной внутриклеточной глутаминилциклазы человека (gQC) в 50 мM трисаминометан-HCl и 5% глицерине, pH 8,0. Реакцию инициировали добавлением к реакционной смеси аликвоты глутаминилциклазы, инкубированной с Соединением 1 в течение 5 минут. Дальнейшее протекание реакции отслеживали спектрофотометрически (длина волны возбуждения и эмиссии составляли 320 и 410 нм). Ферментативную активность определяли по количеству выделившегося 2-нафтиламида (bNA), рассчитанному по калибровочной кривой. Значения IC50 рассчитывали с помощью нелинейной регрессии кривой ʺконцентрация ингибитораʺ-ʺферментативная активностьʺ. В качестве вещества сравнения использовали известный ингибитор глутаминилциклаз -- соединение PBD150 (J Med Chem. 2006 Jan 26;49(2):664-77).
В результате эксперимента было установлено, что Соединение 1 ингибирует активность внутриклеточной глутаминилциклазы с IC50=4,7 мкМ.
2.2) Исследование влияния Соединения 1 на ферментативную активность секретируемой глутаминилциклазы человека in vitro.
В лунки 96-луночного ПЦР планшета (Bio-Rad) добавляли по 25 мкл раствора Соединения 1. В каждую лунку, содержащую Соединение 1, помещали 25 мкл 320 мкМ раствора (2S)-2-амино-N-(4-метил-2-оксо-хромен-7-ил)пентандиамида (Q-AMC) в 25 мМ HEPES, pH 7.0 и перемешивали. В каждую лунку (кроме контролей холостого гидролиза) помещали 50 мкл раствора секретируемой глутаминилциклазы (QPCT) с концентрацией 0,2 мкг/мл в буфере (25 мМ HEPES, pH 7.0), либо аналогичный буферный раствор (контроль холостого гидролиза). Планшет инкубировали при комнатной температуре в течение 20 минут, затем помещали в термостат, нагревали при 100°C в течение 5 минут и затем охлаждали во льду в течение 3 минут. В каждую лунку добавляли 100 мкл раствора пироглутаминилпептилазы (PGPEP) с концентрацией 1 мкг/мл в буфере (0.1 мМ трисаминометан, 5 мМ дитиотреитол, pH 9.0) и инкубировали при комнатной температуре в течение 10 минут. Из каждой лунки отбирали 2 раза по 90 мкл раствора, помещали в 3 лунки планшета для флуориметрии Greiner Bio и определяли флуоресценцию (возбуждение - 355 нм, испускание - 460 нм). Полученную кривую ингибирования (зависимости I от концентрации вещества) аппроксимировали дозозависимой кривой (Dose-response curve) c нижней асимптотой=0 и верхней асимптотой =1 с помощью программного обеспечения Origin Pro 8.0, что позволяло получить значение IC50.
В результате эксперимента было установлено, что Соединение 1 ингибирует активность секретируемой глутаминилциклазы с IC50=2,9 мкМ.
2.3) Исследование влияния Соединения 1 на миграцию моноцитов in vitro
Влияние Соединения 1 на миграцию моноцитов in vitro было изучено с использованием клеток линии U937, концентрации (2-3)×106 клеток/мл на среде RPMI 1640 с добавлением 10% термоинактивированной фетальной коровьей сыворотки (Biochem J. 2012 Mar 1;442(2):403-12). Примерно 1×107 клеток U937 инкубировали с различными концентрациями Соединения 1 (всего 7 значений концентрации) при 37◦C в течение 2 часов и затем обрабатывали липополисахаридом E.coli (O111:B4). Супернатант (кондиционированная среда) использовали для изучения миграции моноцитов.
Свежую порцию клеток U937 окрашивали флуоресцентным красителем Calcein AM в течение 1 часа при 37◦C. После этого аликвоту окрашенных клеток помещали в верхнее отделение лунок планшета BD FalconTM HTS FluoroBlok, ячейки которого разделены полупроницаемыми оптически непрозрачными мембранами. В нижнее отделение лунок планшета помещали кондиционированную среду, полученную после инкубирования клеток с ингибитором и липополисахаридом. Планшеты инкубировали 2 часа при 37◦C, количество (% относительно эксперимента без ингибитора) клеток, мигрировавших в нижний отсек лунок определяли флуориметрически. В качестве сравнения использовали известный ингибитор глутаминилциклаз -- соединение PBD150 (J Med Chem. 2006 Jan 26;49(2):664-77).
Данные по влиянию Соединения 1 на миграцию моноцитов in vitro приведены в таблице 1.
Таблица 1 - Влияние Соединения 1 на миграцию перевиваемой культуры моноцитов линии U937 in vitro
В результате эксперимента было установлено, что Соединение 1 ингибирует миграцию моноцитов с IC50=2.9 мкМ.
2.4) Исследование влияния Соединения 1 на хемотаксис макрофагов in vivo на модели каррагенинового мешочка
Для оценки эффективности действия лекарственного препарата на активность клеток иммунной системы на доклиническом этапе исследований, как правило, используются различные модели острого воспалительного процесса. На сегодняшний день наиболее часто используют модели, в которых паталогический процесс развивается в ограниченной полости. Данные модели позволяют достаточно близко сымитировать заболевание, при котором аберрантная активность клеток иммунной системы локализуется в определенной полости (перитонит, холангит, артрит) (J Pharmacol Toxicol Methods. 1994 Nov;32(3):139-47). Модель каррагенинового мешочка часто используется на доклиническом этапе исследований для исследования паталогических процессов, связанных с аберрантной активностью клеток иммунной системы, локализованной в изолированной полости. В этой модели изолированный мешочек формируют подкожной инъекцией воздуха во внутрикапсульную область спины мыши или крысы. Подкожная инъекция воздуха в область спины, за несколько дней приводит к морфологическим изменениям в клеточной выстилке мешочка. Мешочек состоит главным образом из макрофагов и фибробластов и хорошо васкуляризирован. На шестой день от момента формирования воздушного мешочка в полость воздушного мешочка вводят раствор λ-каррагенина. Каррагенин взаимодействует с рецепторами TLR4 на поверхности макрофагов, выстилающих внутрикапсульную область мешочка, что вызывает их активацию и последующий синтез хемокинов и других медиаторов (IL-1; IL-6; TNFα, IL-8, простагландинов и лейкотриенов, NO) и так же к миграцию клеток иммунной системы внутрь мешочка.
Исследование активности Соединения 1 выполняли на мышах-самцах линии Balb/c по стандартной методике (Curr Protoc Pharmacol. 2012 Mar;Chapter 5:Unit5.6). Опытным группам животным внутрижелудочно вводили Соединение 1 в дозе 3 мг/кг сразу перед введением каррагенина и затем каждые 10-12 ч. Последнее введение - за 12 ч до забоя.
Спустя 48 часов после инъекции λ-каррагенина отдельные группы животных подвергались эвтаназии ингаляцией СО2. Сразу же после эвтаназирования внутрь мешочка стерильным шприцом 25G вводили 1 мл физиологического раствора, содержащего 5,4 мМоль EDTA (Этилендиаминтетрауксусной кислоты), комнатной температуры. После легкого массажа области воздушного мешочка делали саггитальный разрез поперек мешочка и дозатором собирали экссудат в стерильные пробирки объемом 15 мл. В экссудате с помощью камеры Горяева определяли абсолютное количество клеточных элементов на 1 мкл смыва (цитоз). Затем экссудат центрифугировали при 200 ◦С в течение 10 минут. Из осадка клеток готовили мазки, которые в дальнейшем фиксировали в метаноле (5 мин) и окрашивали по методу Романовского-Гимзе (40 мин при t 20-22 ◦С). На мазках рутинным способом под микроскопом Olympus bx51 (на увеличении 100) подсчитывали количество макрофагов. Подсчет клеток производили до 100 шт.
В таблице 2 продемонстрировано количество клеток иммунной системы в экссудате из каррагенинового мешочка при исследовании активности Соединения 1 на модели хемотаксиса макрофагов.
Таблица 2 - Влияние Соединения 1 на миграцию лейкоцитов и макрофагов в каррагениновый мешочек (M±m, n=10)
(3 мг/кг)
Проведенные исследования показали, что применение Соединения 1 в 10 раз снизило приток лейкоцитов и макрофагов (до уровня интактного контроля). Таким образом, Соединение 1 потенциально пригодно для терапии широкого круга заболеваний, таких как болезнь Крона, язвенный колит, перитониты и артриты.
2.5) Исследование влияния Соединения 1 на хемотаксис макрофагов in vivo на модели тиогликолятного перитонита
Исследование выполнено на мышах-самцах линии balb/c по стандартной методике (J Leukoc Biol. 2009 Aug;86(2):361-70). Мышам контрольной группы внутрибрюшинно вводили 2 мл 3% тиогликолевой среды, хранившейся в течение 1 месяца. Интактным животным внутрибрюшинно вводили 2 мл физиологического раствора. Опытным группам животным внутрижелудочно вводили Соединение 1 за 1 ч до введения тиогликолята, 24 и 48 ч после введения тиогликолята в дозе 1 мг/кг. Через 72 ч животных эвтаназировали в CO2-камере, область брюшины смачивали 70% спиртом, аккуратно срезали кожу на брюшной полости, шприцом внутрибрюшинно вводили 5 мл холодного фосфатно-солевого буфера, содержащего 0.1% ЭДТА. После легкого массажа брюшной полости экссудат собирали шприцом в пробирки, определяли объем собранного экссудата.
Количество клеток иммунной системы в экссудате из брюшной полости при исследовании активности Соединения 1 на модели хемотаксиса макрофагов (тиогликолятный перитонит) продемонстрировано в таблице 3.
Таблица 3 - Влияние Соединения 1 на миграцию лейкоцитов и моноцитов в перитонеальную полость мышей на модели тиогликолятного перитонита M±m, n=10)
В экссудате с помощью камеры Горяева определяли абсолютное количество клеточных элементов на 1 мкл смыва (цитоз). Затем эксудат центрифугировали при 200 °С в течение 10 минут. Из осадка клеток готовили мазки, которые в дальнейшем фиксировали в метаноле (5 мин) и окрашивали по методу Романовского-Гимзе (40 мин при t 20-22 °С). На мазках рутинным способом под микроскопом Olympus bx51 (на увеличении 100) подсчитывали количество моноцитов/макрофагов. Подсчет клеток производили до 100 шт.
Проведенные исследования показали, что применение Соединения 1 снижает тиогликолят-индуцированный приток макрофагов в перитонеальную полость мышей и оказывает противовоспалительное действие. Таким образом, Соединение 1 потенциально пригодно в терапии перитонитов, болезни Крона и язвенного колита.
2.6) Исследование активности Соединения 1 на модели каррагенинового отека
Для оценки влияния Соединения 1 на функциональный статус иммунной системы была использована модель каррагенин-индуцированного отека лапы крыс. Эксперименты выполнены на белых нелинейных крысах самцах массой 250-270 г. Острое воспаление лапы у крыс вызывали интраплантарным введением (подкожно) в объеме 0,1 мл в правую лапу 1.5% раствора каррагенина. Исследуемое соединение вводили внутрижелудочно за 1 час до введения каррагенина. Действие Соединения 1 и контрольного вещества (диклофенак) оценивали по степени снижения отека лапы в сравнении с интактной левой лапой. Объем лапы оценивали до введения Соединения 1 и через 2 ч после введения каррагенина.
Влияние Соединения 1 на прирост отека лапы крыс (относительно контроля) в модели каррагенин-индуцированного отека продемонстрировано в таблице 4.
Таблица 4 - Влияние Соединения 1 на прирост отека лапы крыс (относительно контроля) в модели каррагенин-индуцированного отека лапы крыс
Из приведенных результатов видно, что Соединение 1 обладает прямым тормозящим действием на прирост отека лапы и может быть использовано для лечения широкого круга заболеваний, связанных с активностью клеток иммунной системы.
2.7) Изучение активности Соединения 1 в модели диабетической нефропатии у крыс
Модель диабетической нефропатии у крыс индуцировали длительным содержанием животных на рационе высокожировой диеты и однократным или двукратным внутрибрюшинным введением стрептозотоцина в дозе 30 мг/кг (Int J Clin Exp Med. 2015 Apr 15;8(4):6388-96).
Животных содержали на высокожировой диете в течение 16 недель, на 9-ой неделе крысам внутрибрюшинно вводили стрептозотоцин двукратно (2 дня подряд) в дозе 30 мг/кг. Через 7 дней после введения стрептозотоцина начинали введение Соединения 1. Субстанцию вводили ежедневно внутрижелудочно один раз в день в дозе 50 мг/кг.
В таблице 5 приведен биохимический анализ мочи после 6 недели внутрижелудочного введения Соединения 1 крысам в модели диабетической нефропатии, индуцированной высокожировой диетой и введением стрептозотоцина (15 недель высокожировой диеты)
Таблица 5 - Влияние внутрижелудочного введения Соединения 1 в течение 6 недель на биохимический анализ мочи крыс на модели диабетической нефропатии, индуцированной высокожировой диетой и введением стрептозотоцина
Таким образом, проведенные исследования показали, что Соединение 1 обладает эффективностью в ингибировании фермента глутаминилциклазы (IC50=4,7 мкМ для внутриклеточной глутаминилциклазы и IC50=2,9 мкМ для секретируемой глутаминилциклазы) и ингибирует хемотаксиса макрофагов in vitro (IC50=2,9 мкМ). В модели каррагенинового мешочка и тиогликолятного перитонита Соединение 1 ингибирует хемотаксиса макрофагов in vivo. В модели диабетической нефропатии действие Соединения 1 приводит к снижению хемотаксиса моноцитов и макрофагов в ткани почек, остановки локального патологического процесса в клубочках почек и нормализации функциональных характеристик почек.
2.8) Исследование фармакокинетики Соединения 1 при однократном пероральном введении
Для анализа применимости Соединения 1 в качестве лекарственного препарата были исследованы фармакокинетические параметры этого соединения. Поскольку соединение оказывает выраженное действие на хемотаксис клеток иммунной системы, для достижения максимального терапевтического эффекта представляется разумным достичь высоких концентраций Соединения 1 в органе-мишени. В то же время с точки зрения минимизации возможных негативных эффектов, связанных с системным подавлением хемотаксиса клеток иммунной системы представляется обоснованным стараться создать по возможности низкие концентрации Соединения 1 в системном кровотоке. Таким образом, органы обеспечивающие «накопление» Соединения 1 будут наиболее благоприятными органами-мишенями. В качестве меры «накопления» Соединения 1 была выбрана характеристика «тканевая биодоступность» определяемая отношением значения площади под фармакокинетической кривой, которая рассчитывается от момента введения до конкретной временной точки (AUC0-t) в ткани к соответствующей величине AUC0-t в плазме крови.
Фармакокинетика Соединения 1 была изучена после однократного внутрижелудочного введения Соединения 1 крысам в дозе 18 мг/кг. Определение концентрации Соединения 1 при фармакокинетических исследованиях было проведено методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (ВЭЖХ-МС/МС).
При изучении фармакокинетики Соединения 1 оказалось, что наиболее высокие концентрации Соединения 1 наблюдаются в органах брюшной полости - селезенке, печени, почках (см таблицу 5). Таким образом применение Соединения 1 потенциально пригодно для лечения заболеваний органов брюшной полости.
В таблице 6 оценена тканевая биодоступность Соединения 1 при однократном внутрижелудочном введении крысам дозы 18 мг/кг.
Таблица 6 - Тканевая биодоступность Соединения 1 при однократном внутрижелудочном введении крысам дозы 18 мг/кг.
ность
Несмотря на то что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ ИНГИБИТОР ГЛУТАМИНИЛЦИКЛАЗ И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2791703C2 |
| НОВЫЙ ИНГИБИТОР ГЛУТАМИНИЛЦИКЛАЗ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЛЕГКИХ И ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2017 |
|
RU2662559C1 |
| НОВЫЙ ЦИНКОВЫЙ КОМПЛЕКС, ЕГО ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ ДЛЯ ТЕРАПИИ ЗАБОЛЕВАНИЙ ЧЕЛОВЕКА И ЖИВОТНЫХ | 2018 |
|
RU2697580C1 |
| Композиция для лечения инфекционного перитонита кошек | 2021 |
|
RU2780097C1 |
| СПОСОБ ИММУНОКОРРЕКЦИИ ПРИ ГНОЙНОМ ПЕРИТОНИТЕ | 1992 |
|
RU2026678C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ИНГИБИТОР РЕНИНА, БЛОКАТОР КАЛЬЦИЕВЫХ КАНАЛОВ И ДИУРЕТИК | 2003 |
|
RU2316318C2 |
| СВЯЗЫВАЮЩАЯ МСР-1 НУКЛЕИНОВАЯ КИСЛОТА И ЕЕ ПРИМЕНЕНИЕ | 2008 |
|
RU2542973C2 |
| СОДЕРЖАЩИЙ G-CSF АГЕНТ ДЛЯ ПРЕДУПРЕЖДЕНИЯ И ЛЕЧЕНИЯ ДИАБЕТИЧЕСКОЙ ПЕРИФЕРИЧЕСКОЙ НЕЙРОПАТИИ | 2007 |
|
RU2448726C2 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНОГО ГЛУТАРИМИДА ДЛЯ ТЕРАПИИ ЗАБОЛЕВАНИЙ, АССОЦИИРОВАННЫХ С АБЕРРАНТНОЙ АКТИВНОСТЬЮ ИНТЕРЛЕЙКИНА-6 | 2020 |
|
RU2774928C2 |
| СЛИТЫЕ БЕЛКИ RAGE | 2008 |
|
RU2513695C2 |
Изобретение относится к медицине, в частности к фармацевтической композиции для модулирования активности глутаминилциклазы, а также для лечения расстройства, связанного с активностью глутаминилциклазы, содержащей эффективное количество соединения N,N'-бис[2-(1H-имидазол-4-ил)этил]изофталамида.
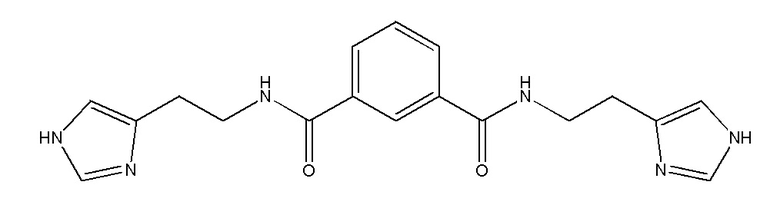
Осуществление изобретения позволит получить эффективный модулятор глутаминилциклазы, обладающий высокой активностью по отношению к внутриклеточной и/или секретируемой изоформам глутаминилциклазы и хорошими фармакокинетическими характеристиками. 2 н. и 9 з.п. ф-лы, 10 пр., 6 табл.
1. Фармацевтическая композиция для модулирования активности глутаминилциклазы, содержащая фармацевтически эффективное количество соединения формулы
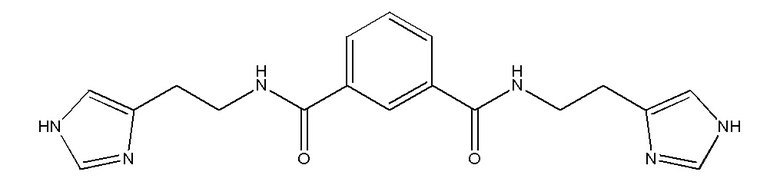
или его фармацевтически приемлемой соли, гидрата или сольвата и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
2. Фармацевтическая композиция по п.1, отличающаяся тем, что вспомогательное вещество представляет собой носитель и/или эксципиент.
3. Фармацевтическая композиция по п.1 или 2, где модулирование активности глутаминилциклазы представляет собой ингибирование внутриклеточной и/или секретируемой глутаминилциклазы.
4. Фармацевтическая композиция по п.1 или 2, дополнительно включающая другой активный агент.
5. Фармацевтическая композиция по п.4, где другой активный агент выбран из группы, включающей антибактериальные, цитостатические, цитотоксические средства, средства подавления симптомов или побочных эффектов активных агентов и их комбинации.
6. Фармацевтическая композиция для лечения расстройства, связанного с активностью глутаминилциклазы, содержащая фармацевтически эффективное количество соединения формулы
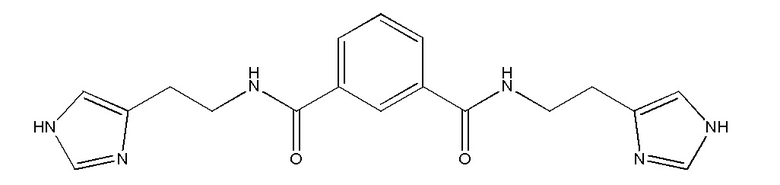
или его фармацевтически приемлемой соли и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
7. Фармацевтическая композиция по п.6, отличающаяся тем, что вспомогательное вещество представляет собой носитель и/или эксципиент.
8. Фармацевтическая композиция по п.6 или 7, отличающаяся тем, что расстройство, связанное с активностью глутаминилциклазы, представляет собой заболевание органов брюшной полости.
9. Фармацевтическая композиция по п.8, отличающаяся тем, что расстройство представляет собой болезнь Крона, язвенный колит, перитонит, нефропатию, в частности диабетическую нефропатию, или заболевание почек, которое является побочным эффектом применения лекарственных средств.
10. Фармацевтическая композиция по п.6 или 7, дополнительно включающая другой активный агент.
11. Фармацевтическая композиция по п.10, где другой активный агент выбран из группы, включающей антибактериальные, цитостатические, цитотоксические средства, средства подавления симптомов или побочных эффектов активных агентов и их комбинации.
| WO 2010026212 A1, 11.03.2010 | |||
| Identification of human glutaminyl cyclase as a metalloenzyme | |||
| Potent inhibition by imidazole derivatives and heterocyclic chelators / Stephan Schilling, André J | |||
| Niestroj, Jens-Ulrich Rahfeld, Torsten Hoffmann, Michael Wermann, Katrin Zunkel, Claus Wasternack, and Hans-Ulrich Demuth // The journal of biological chemistry | |||
| Vol | |||
| ПАРОВАЯ ИЛИ ГАЗОВАЯ ТУРБИНА | 1914 |
|
SU278A1 |
| Устройство для выпрямления многофазного тока | 1923 |
|
SU50A1 |
| Способ обработки зернистой икры | 1935 |
|
SU49773A1 |
| Cиндром низкой толерантности к гистамину | |||
| Обзор литературных данных | |||
| Часть I / О.А | |||
| Наумова // Клiнiчна iмунологiя | |||
| Алергологiя | |||
| Iнфектологiя | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| RU 2013116822 A, 20.10.2014. | |||
Авторы
Даты
2018-09-03—Публикация
2017-05-26—Подача