Изобретение относится к области медицины, конкретно к способу диагностики генетических нарушений, ведущих к бесплодию супружеских пар. Способ включает в себя комплексное определение мутаций в генах F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1, MTHFR, MTR, MTRR и исследование специфичностей локусов А, В, DRB1, DQA1, DQB1 системы HLA. Способ обеспечивает раннюю и точную диагностику генетических причин нарушения процессов репродукции человека.
Изобретение относится к области медицины, а именно к лабораторной диагностике, основанной на анализе генетических факторов, свидетельствующих об иммуногенетическом характере нарушений репродуктивной функции человека.
Цель изобретения - разработать способ оценки иммуногенетических факторов при анализе мутаций в генах F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1, MTHFR, MTR, MTRR и генов HLA-системы у супругов.
Бесплодный брак - отсутствие наступления беременности у женщины репродуктивного возраста в течение одного и более года регулярной половой жизни без использования контрацептивных средств [1, 2]. Бесплодие возникает вследствие хромосомных, генетических, анатомических, эндокринных и инфекционных нарушений. Одним из приоритетных направлений развития медицины является разработка современных высокоэффективных программ лечения репродуктивных расстройств, в том числе методом экстракорпорального оплодотворения (ЭКО) [3, 4]. Несмотря на то, что технология выполнения ЭКО хорошо изучена, результативность данного метода в мире и в Российской Федерации составляет менее 30%, без тенденции к возрастанию в последние годы [5, 6]. Дифференциальная диагностика причин, вызывающих бесплодие и/или неудачные попытки ЭКО, является основой для назначения терапии и определения прогноза при проведении вспомогательных репродуктивных технологий [3].
Патогенез нарушений, препятствующих наступлению беременности или приводящих к ее прерыванию на ранних сроках, связан с генетическими особенностями системы гемостаза у женщины или особенностями генотипов системы HLA у супружеской пары. В первом случае речь идет о полиморфизме генов тромбофилии и фолатного цикла, мутации которых ассоциированы с патологическим синтезом факторов системы свертывания крови и гомоцистеина. Во втором - о совпадении генотипов супругов по системе HLA, основанном на предопределяющем значении генов иммунного ответа HLA для выработки блокирующих антител, необходимых для имплантации яйцеклетки и развития беременности. Комплексный анализ генов F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1, MTHFR, MTR, MTRR, HLA локусов А, В, DRB1, DQA1, DQB1 позволяет клиницисту персонифицировать терапию бесплодия, в том числе при проведении процедуры ЭКО.
Известен способ определения факторов врожденного иммунитета при установлении причин бесплодия [7]. Метод основан на оценке комплекса иммунологических механизмов (Th-1, Th-2, IL-1, TNF-α, IL-6, IL-8, АФС, TLR-рецепторы), действующих во время беременности и необходимых для успешной имплантации эмбриона и его дальнейшего развития. Недостатком способа является отсутствие информации о роли HLA-антигенов при репродуктивных расстройствах, а также данных о влиянии мутаций генов системы гемостаза и фолатного обмена на фертильность.
Известен способ оценки полиморфизма генов F2, F5 и MTHFR при определении причин нерезультативных процедур ЭКО [8], однако исследование мутаций только в трех генах недостаточно для установления связи генетических факторов с неудачными попытками ЭКО.
Известен способ оценки генов системы HLA при мужском бесплодии, причем внимание уделяется не совпадению супругов по HLA-генотипам, а значению отдельных антигенов HLA в развитии инфертильности. Недостатком является также отсутствие данных о влиянии мутаций в генах тромбофилии и фолатного цикла на возникновение бесплодия [9].
Наиболее близко к предлагаемому изобретению - изучение HLA-антигенов класса II, аллелей генов MTHFR, F2, F5 при ранних репродуктивных потерях [10]. Этот способ охватывает несколько вариантов генетического тестирования супругов, но не включает оценку данных факторов при бесплодии и идентификацию аллелей генов F7, F13, FGB, ITGA2, ITGB3, PAI-1, MTR, MTRR, HLA класса I при невынашивании беременности.
Техническим результатом заявляемого изобретения является создание способа оценки генетических особенностей супругов при анализе мутаций в генах F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1, MTHFR, MTR, MTRR и количества общих аллелей HLA класса I и II.
Для достижения результата в соответствии с прототипом (Веропотвелян Н.П., 2011) проводят типирование аллелей у супругов и выявляют специфичности, позволяющие дать оценку влияния иммуногенетических факторов на возникновение репродуктивных неудач. В отличие от аналога, в котором проводится ПЦР только нескольких полиморфизмов генов, в данном способе осуществляется комплексная оценка генов тромбофилии, фолатного обмена (F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1 MTHFR, MTR, MTRR) и HLA-антигенов класса I и II и определение риска бесплодия и неудачных попыток ЭКО в соответствии с разработанной балльной шкалой.
В процессе проведения патентно-информационного поиска не выявлено источников, порочащих новизну предполагаемого изобретения.
Заявляемое изобретение разработано в лаборатории иммуногематологии ФГБУН КНИИГиПК ФМБА России в соответствии с планом научно-исследовательской работы.
Способ осуществляется следующим образом: Этап 1. Полиморфизм генов F2, F5, F7, F13, ITGA, ITGB, FGB, PAI-1, MTHFR, MTR, MTRR в образцах крови женщин исследуют в соответствии с инструкцией к наборам реагентов методом ПЦР с детекцией результатов в режиме реального времени.
Этап 2. Проводят типирование генов системы HLA классов I и II у обоих супругов методом ПЦР в режиме реального времени с целью выявления общих специфичностей у супругов.
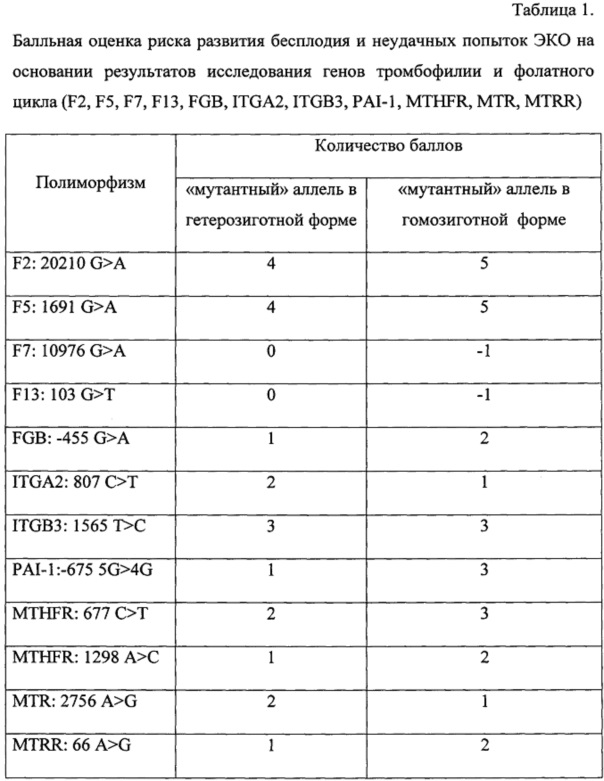
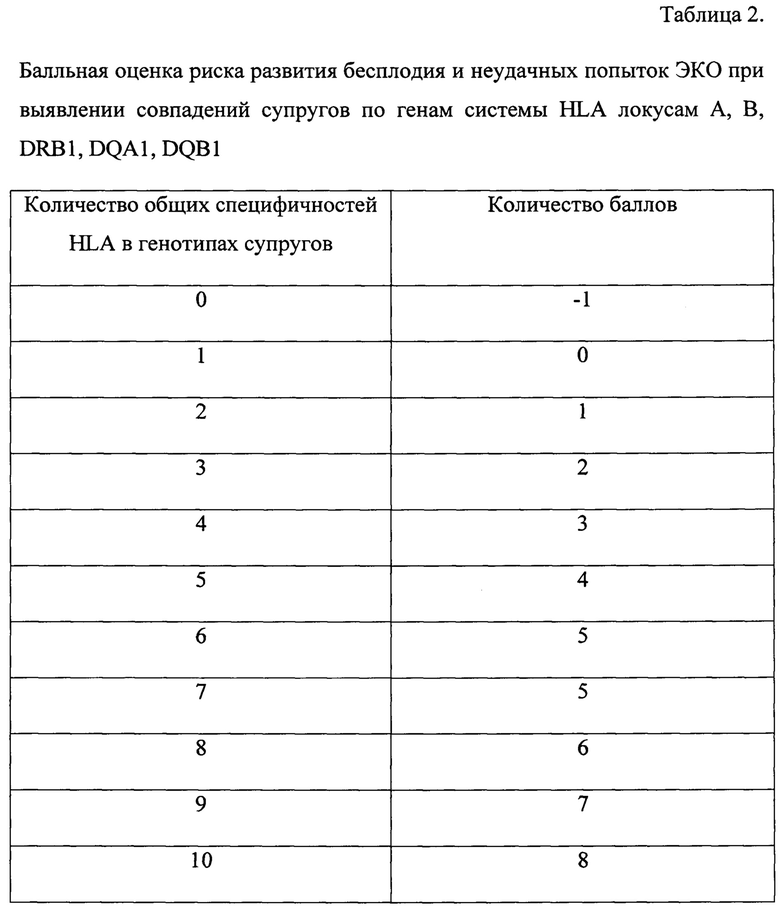
Этап 3. Осуществляют оценку генотипов супругов, присваивая выявленным полиморфизмам генов F2, F5, F7, F13, ITGA, ITGB, FGB, PAI-1, MTHFR, MTR, MTRR и общим специфичностям генов HLA определенный балл в зависимости от их корреляции с репродуктивными расстройствами (таблицы 1, 2).
Заключение о том, что бесплодие с высокой вероятностью ассоциировано с генетическими причинами делают при суммарном количестве баллов 18 и более, вероятность выше среднего - 14-17 баллов, бесплодие не детерминировано генетическими факторами - 13 баллов и менее; заключение о благоприятном прогнозе при проведении вспомогательных репродуктивных технологий делают при суммарном количестве баллов 13 и менее.
Клинические примеры подтверждают возможность использования и эффективность предлагаемого способа при оценке иммуногенетических факторов как причины репродуктивных нарушений.
Пример 1.
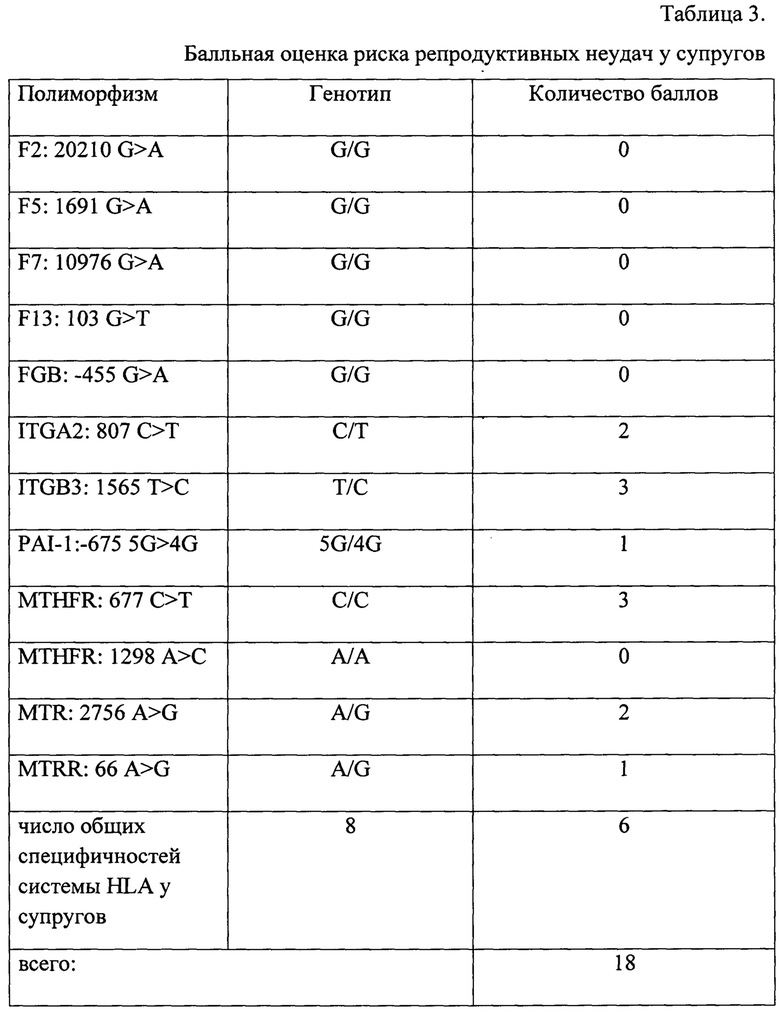
Супружеская пара М., репродуктивного возраста с диагнозом: Первичное бесплодие. В анамнезе 3 попытки ЭКО, закончившиеся неудачей. Инфекционные заболевания, эндокринная патология и отягощенная наследственность исключены, спермограмма в норме, делеции в локусе AZF не выявлены. В таблице 3 представлены результаты типирования полиморфизмов генов тромбофилии и фолатного цикла. В генотипе женщины выявлены полиморфизмы генов ITGA2: 807 С/Т, ITGB3: 1565 Т/С, PAI-1:-675 5G/4G, MTHFR: 677 С/С, MTR: 2756 A/G, MTRR: 66 A/G в гомо/ и гетерозиготных формах. У супругов обнаружено 8 общих специфичностей HLA. Количество баллов, характеризующих риск развития репродуктивных нарушений, - 18 (таблицы 1, 2). Заключение: Генетически обусловленный риск возникновения бесплодия и неудачных попыток ЭКО высокий (таблица 3).
Пример 2.
Супружеская пара Д., репродуктивного возраста с диагнозом: Первичное бесплодие. ЭКО не проводилось. Назначена комплексная диагностика факторов, ассоциированных с репродуктивными нарушениями, в том числе проведение типирования супругов по системе HLA и генам тромбофилии и фолатного цикла. Результаты исследования представлены в таблице 4. В генотипе женщины выявлены полиморфизмы генов ITGA2: 807 С/Т, PAI-1: -675 5G/4G, MTHFR: 1298 С/С, MTR: 2756 A/G, MTRR: 66 A/G в гомо/ и гетерозиготных формах. У супругов обнаружена 1 общая специфичность HLA. Количество баллов, характеризующих риск развития репродуктивных нарушений, - 13 (таблицы 1, 2). Заключение: Генетически обусловленный риск возникновения бесплодия и неудачных попыток ЭКО не выявлен (таблица 4).
СПОСОБ ДИАГНОСТИКИ ГЕНЕТИЧЕСКИХ НАРУШЕНИЙ ПРИ ПАТОЛОГИИ ПРОЦЕССА РЕПРОДУКЦИИ ЧЕЛОВЕКА

Список литературы:
1. Терентьева Л.С., Асымбекова Г.У., Аскеров А.А., Ташбулатова Н.К. Диагностика и лечение бесплодия: методическое пособие. - Бишкек: Изд-во КРСУ, 2005. 37 с.
2. Витязева И.И., Бармина И.И. Причины отказов пациентам, направленным на лечение бесплодия методом ЭКО за счет федерального бюджета // Материалы XXI международной конференции Российской Ассоциации Репродукции Человека «Репродуктивные технологии сегодня и завтра», Санкт-Петербург, 2011: 17-18.
3. Валиев Р.К., Рыбина А.Н. Первый опыт проведения бюджетных программ экстракорпорального оплодотворения // Материалы XXI международной конференции Российской Ассоциации Репродукции Человека «Репродуктивные технологии сегодня и завтра», Санкт-Петербург, 2011: 16-17.
4. Киселева А.Н., Бутина Е.В., Зайцева Г.А., Попонина Е.А., Игнатьев С.В., Ярыгин Д.Н., Белоус И.А. Роль генетических полиморфизмов, ассоциированных с тромбофилией, протромботическими состояниями и нарушениями фолатного цикла, у женщин с репродуктивными расстройствами // Тромбоз, гемостаз и реология. - 2017. - №2(70). - С. 52-57.
5. Радзинский В.Е., Алеев И.А. Бесплодие и экстракорпоральное оплодотворение в свете контраверсий (по данным VII всемирного конгресса "Противоречия в акушерстве, гинекологии и фертильности"). Акушерство и гинекология. 2006; 1: 60-2.
6. Вартанян Э.В., Айзикович И.В., Антонов А.Р. Причины неудач ЭКО (обзор литературы). Проблемы репродукции. 2010; 3: 57-61.
7. Сухих Г.Т., Ванько Л.В. Иммунные факторы в этиологии и патогенезе осложнений беременности // Акушерство и гинекология. -2012. - №1. - С. 143-147.
8. Husseinei N.F., Rezk A.U., Odah М.М., Rahman S.M., Ali A.I. Thrombophilic genes mutations in momen with repeated // American Medical Journal. - 2011. - 2(1). - P. 7-12.
9. Van der Ven, K., Fimmers R., Engels G. et al. Evidence for major histocompatibility complex-mediated effects on spermatogenesis in humans // Hum Reprod. - 2000. - Vol. 15(1). - P. 189-196.
10. Веропотвелян, Н.П., Погуляй Ю.С., Кодунов Л.О. Особенности распределения полиморфных генов системы HLA II класса, фолатного обмена, факторов свертываемости крови у супружеских пар с привычным невынашиванием беременности //  ,
, 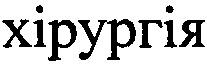 та перинатальна медицина. - 2011. - Т. 1 (1). - С. 82-85.
та перинатальна медицина. - 2011. - Т. 1 (1). - С. 82-85.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования клинического течения гемофилии с уровнем активности факторов VIII, IX | 2019 |
|
RU2698453C1 |
| Способ определения посттрансплантационного химеризма при анализе точечных мутаций замены оснований в генах F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1 | 2017 |
|
RU2667006C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ АСПИРИНОРЕЗИСТЕНТНОСТИ | 2015 |
|
RU2602664C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОТСЛОЙКИ ХОРИОНА В ПЕРВОМ ТРИМЕСТРЕ БЕРЕМЕННОСТИ | 2014 |
|
RU2566729C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ МУЛЬТИФАКТОРНОЙ ПАТОЛОГИИ У ДЕТЕЙ, РОЖДЕННЫХ С ПОМОЩЬЮ ВСПОМОГАТЕЛЬНЫХ РЕПРОДУКТИВНЫХ ТЕХНОЛОГИЙ | 2011 |
|
RU2456911C1 |
| Способ прегестационного прогнозирования рецидива ранних репродуктивных потерь и первичной плацентарной недостаточности | 2019 |
|
RU2709246C1 |
| Способ оценки риска образования анти-HLA антител при трансфузиях компонентов крови | 2022 |
|
RU2793843C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЫСОКОЙ СТЕПЕНИ РИСКА ТЯЖЕЛОГО ТЕЧЕНИЯ COVID-19 | 2022 |
|
RU2787517C1 |
| Способ прогнозирования неразвивающейся беременности при нормальном кариотипе эмбриона | 2021 |
|
RU2766750C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ФОРМИРОВАНИЯ СУБ- И ДЕКОМПЕНСИРОВАННОЙ ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ В СЕМЬЯХ С ТРОМБОФИЛИЕЙ ОБОИХ РОДИТЕЛЕЙ | 2017 |
|
RU2637873C1 |
Изобретение относится к области биотехнологии. Изобретение представляет собой способ диагностики генетических нарушений, являющихся причиной бесплодия супружеских пар, включающий в себя комплексное определение мутаций в генах тромбофилии, фолатного цикла и аллелей HLA, где оценку генов в гомозиготном и гетерозиготном состояниях проводят в соответствии с разработанной балльной шкалой, присваивая генетическим факторам в образцах крови женщин следующие значения: F2 G/A - 4 балла, F2 А/А - 5 баллов, F5 G/A - 4 балла, F5 А/А - 5 баллов, F7 G/A - 0 баллов, F7 А/А - -1 балл, F13 G/T - 0 баллов, F13 Т/Т - -1 балл, FGB G/A - 1 балл, FGB А/А - 2 балла, ITGA2 С/Т - 2 балла, ITGA2 Т/Т - 1 балл, ITGB3 Т/С - 3 балла, ITGB3 С/С - 3 балла, PAI-1 5G/4G - 1 балл, PAI-1 4G/4G - 3 балла, MTHFR:677 С/Т - 2 балла, MTHFR:677 Т/Т - 3 балла, MTHFR: 1298 А/С - 1 балл, MTHFR: 1298 С/С - 2 балла, MTR A/G - 2 балла, MTR G/G - 1 балл, MTRR A/G - 1 балл, MTRR G/G - 2 балла; при наличии у супругов одной общей специфичности системы HLA - 0 баллов, двух - 1 балл, трех - 2 балла, четырех - 3 балла, пяти - 4 балла, шести или семи - 5 баллов, восьми - 6 баллов, девяти - 7 баллов, десяти - 8 баллов, общих специфичностей нет - -1 балл; заключение о том, что бесплодие с высокой вероятностью ассоциировано с генетическими причинами, делают при суммарном количестве баллов 18 и более, вероятность выше среднего - 14-17 баллов, бесплодие не детерминировано генетическими факторами -13 баллов и менее; заключение о благоприятном прогнозе при проведении вспомогательных репродуктивных технологий делают при суммарном количестве баллов 13 и менее. Способ обеспечивает раннюю и точную диагностику генетических причин нарушения процессов репродукции. 4 табл., 2 пр.
Способ диагностики генетических нарушений, являющихся причиной бесплодия супружеских пар, включающий в себя комплексное определение мутаций в генах тромбофилии, фолатного цикла и аллелей HLA, отличающийся тем, что оценку генов в гомозиготном и гетерозиготном состояниях проводят в соответствии с разработанной балльной шкалой, присваивая генетическим факторам в образцах крови женщин следующие значения: F2 G/A - 4 балла, F2 А/А - 5 баллов, F5 G/A - 4 балла, F5 А/А - 5 баллов, F7 G/A - 0 баллов, F7 А/А - -1 балл, F13 G/T - 0 баллов, F13 Т/Т - -1 балл, FGB G/A - 1 балл, FGB А/А - 2 балла, ITGA2 С/Т - 2 балла, ITGA2 Т/Т - 1 балл, ITGB3 Т/С - 3 балла, ITGB3 С/С - 3 балла, PAI-1 5G/4G - 1 балл, PAI-1 4G/4G - 3 балла, MTHFR:677 С/Т - 2 балла, MTHFR:677 Т/Т - 3 балла, MTHFR: 1298 А/С - 1 балл, MTHFR: 1298 С/С - 2 балла, MTR A/G - 2 балла, MTR G/G - 1 балл, MTRR A/G - 1 балл, MTRR G/G - 2 балла; при наличии у супругов одной общей специфичности системы HLA - 0 баллов, двух - 1 балл, трех - 2 балла, четырех - 3 балла, пяти - 4 балла, шести или семи - 5 баллов, восьми - 6 баллов, девяти - 7 баллов, десяти - 8 баллов, общих специфичностей нет - -1 балл; заключение о том, что бесплодие с высокой вероятностью ассоциировано с генетическими причинами, делают при суммарном количестве баллов 18 и более, вероятность выше среднего - 14-17 баллов, бесплодие не детерминировано генетическими факторами -13 баллов и менее; заключение о благоприятном прогнозе при проведении вспомогательных репродуктивных технологий делают при суммарном количестве баллов 13 и менее.
| ВЕРОПОТВЕЛЯН Н.П., и др., Особенности распределения полиморфных генов системы HLA II класса, фолатного обмена, факторов свертываемости крови у супружеских пар с привычным невынашиванием беременности, Неонантологiя, хiрургия та перинатальная медицина, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| КИСЕЛЕВА А.Н., и др., Особенности полиморфизма генов системы HLA при нарушениях процессов репродукции, Международный научно-исследовательский журнал, Екатеринбург, 2015, с | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
Авторы
Даты
2018-09-04—Публикация
2017-09-27—Подача