Родственная заявка
Согласно настоящей заявке испрашивается приоритет в соответствии с предварительной заявкой на выдачу патента США №61/819699, поданной 6 мая 2013 г. Все идеи вышеуказанной заявки(заявок) включены в настоящий документ ссылкой.
Предшествующий уровень техники настоящего изобретения
Существует растущая потребность в альтернативных источниках щелочных металлов, таких как, помимо прочего, калий. Хлорид калия (традиционное калийное удобрение) получают в ограниченном числе географических местоположений, удаленных от Южного полушария, причем стоимость транспортировки вносит значительный вклад в рыночную стоимость, что делает местное производство калийного удобрения все более заманчивым. Поскольку население растет, сельское хозяйство также должно расти и развиваться с ним, в частности, в пригодных для этого регионах в Южном полушарии. Среди прочего, современное развитие сельского хозяйства в этих регионах требует выращивания сельскохозяйственных культур на почвах, которые часто полностью лишены питательных макроэлементов, структурных элементов, например, кремния в виде, усвояемом растениями (монокремниевая кислота), или кальция, и структурообразующих минералов, таких как глинистые минералы (филлосиликаты). Другими словами, эти почвы являются не наилучшими для выращивания сельскохозяйственных культур из-за отсутствия соответствующей структуры и источников необходимых элементов. С точки зрения удобрения почв традиционные удобрения, такие как нитрат калия и хлорид калия, являются не наилучшими из-за их чрезмерного выщелачивания, отсутствия удержания их соответствующих ионов и их неспособности обеспечивать соответствующую структуру почве. Калий и другие питательные элементы, вносимые в почву в виде этих сильно растворимых солей, таким образом, тратятся напрасно с сильными отрицательными воздействиями на окружающую среду, например, загрязнением хлоридом. Таким образом, новые источники калия и лучшие средства доставки питательных веществ требуются для обеспечения высокой продуктивности и роста сельского хозяйства в пригодных для этого регионах Южного полушария. В идеале, эти источники могут одновременно обеспечивать необходимые элементы, такие как кальций и усвояемый растениями кремний, и ускорять образование структурных минералов.
Породообразующие минералы, такие как калиевые полевые шпаты (KAlSi3O8), могут таким образом рассматриваться как часто встречающиеся на Земле альтернативы традиционным источникам на основании относительно высокого содержания K2O в них (более 15 масс. % K2O в чистом KAlSi3O8). Ряд научно-исследовательских работ, посвященных экстракции иона калия (K+) из породообразующих минералов, был проведен в последние десятилетия. Среди таких предложений представлены способы полного разложения калийсодержащих силикатов и алюмосиликатов, направленных на экстракцию K+ в виде сильно растворимой соли, такой как, помимо прочего, KCl. Эти экстракционные способы обычно основаны на осаждении растворимой в воде калиевой соли из водного раствора, полученного после разложения сырьевых минералов. В способах разложения, в свою очередь, обычно используют относительно высокие температуры (>1000°С) и/или агрессивные кислотно-щелочные обработки, неизбежно создающие большие объемы жидких и/или твердых отходов, включая сложные и дорогостоящие техники разделения ("Обработка для разложения калиевого полевого шпата посредством выбора низкотепературного полусухого способа для полной утилизации", CN 103172074 А; Нао Zhang и соавт. (2012). The Extraction of Potassium from Feldspar by Molten Salt Leaching Method with Composite Additives. Advanced Materials Research, 524-527, 1136; и патентная заявка WO 2013061092 A1, выданная Pedro Lucas Gervasio Ladiera на калийный продукт и способ. Идеи из них всех включены в настоящий документ ссылкой во всей их полноте.).
Также были сделаны попытки использовать неизмененную каменную муку (раздробленную породу) в качестве альтернативного источника калия для удобрения и источника усвояемого растениями кремния (Anne Kjersti Bakken, Harvard Gautneb, Kristen Myhr (1997) Plant available potassium in rocks and mine tailings with biotite, nepheline and K-feldspar as K-bearing minerals. Acta Agriculturae Scandinavica, Section В - Soil & Plant Science. Vol. 47; и Y. Tokunaga, Potassium silicate (1991). A slow-release potassium fertilizer. Fertilizer Research. 30, 55-59. Идеи из них всех включены в настоящий документ ссылкой во всей их полноте.). Однако, природное химическое разрушение этой раздробленной породы является очень медленным процессом, и преимущества, такие как высвобождение питательных веществ и образование филлосиликата из раздробленных первоначальных минералов, проявляются только с течением времени, которое значительно превышает - несколько лет, возможно десятилетий - временные рамки выращивания и сбора сельскохозяйственных культур в современном сельском хозяйстве.
Таким образом, существует потребность в получении источника ионов калия, который высвобождает питательное вещество со средней скоростью, меньшей, чем бесконечная скорость растворения традиционных солей, но большей, чем скорость, обычно проявляемая природными минералами. В идеале, этот источник, получаемый из часто встречающихся на Земле K-содержащих силикатных пород, может обеспечивать структурные компоненты (такие как кремний в виде монокремниевой кислоты и/или кальций) и может ускорять образование глинистых минералов (филлосиликатов). Также существует потребность в способе получения источника таких материалов, который минимизирует вышеуказанные проблемы.
Краткое раскрытие настоящего изобретения
Настоящее изобретение в общем относится к способу получения источника ионов щелочного металла и источнику ионов щелочного металла, полученному согласно способу.
Согласно одному варианту осуществления способ настоящего изобретения для получения источника ионов щелочного металла предусматривает объединение первого компонента, который содержит содержащий ионы щелочного металла каркасный силикат в виде частиц, со вторым компонентом, который содержит по меньшей мере одно из оксида и гидроксида по меньшей мере одного из щелочноземельного металла и щелочного металла, с образованием твердой смеси. Мольное отношение кремния первого компонента к по меньшей мере одному из щелочноземельного и щелочного металла второго компонента находится в диапазоне от приблизительно 1,0:0,1 до приблизительно 1,0:0,3. Проводят необязательное влажное совместное измельчение или сухое совместное измельчение смеси, или компоненты отдельно измельчают и смешивают после измельчения. В случае, когда проводят влажное совместное измельчение твердой смеси, общее количество жидкости находится в массовом отношении жидкости к твердому веществу в диапазоне от приблизительно 0,05:1 до приблизительно 5:1. Смесь затем подвергают воздействию повышенной температуры и давления в течение периода времени, достаточного для образования геля, который содержит кремний и щелочной металл первого компонента, таким образом образуя источник щелочного металла. Массовое отношение фазы тоберморита к непрореагировавшим фазам содержащего ионы щелочного металла каркасного силиката источника ионов щелочного металла может составлять от приблизительно 1:1 до приблизительно 0:1. Массовое процентное содержание геля K(Na)-A-S-H в источнике ионов щелочного металла может составлять от приблизительно 10% до приблизительно 100%. Удельная площадь поверхности источника ионов щелочного металла может составлять от приблизительно 8 м2/г до 50 м2/г.
Согласно другому варианту осуществления способа настоящего изобретения источник ионов щелочного металла получают путем дробления содержащего ионы щелочного металла каркасного силиката в виде частиц, пока по меньшей мере приблизительно 50 масс. % частиц не будут иметь диаметр равный или меньший 5 мкм, что измерено лазерной дифракцией при помощи лазерного дифракционного анализатора размеров частиц в жидком режиме (например, в водной среде).
Согласно одному варианту осуществления источник ионов щелочного металла настоящего изобретения получают из содержащего ионы щелочного металла каркасного силиката в виде частиц посредством способа настоящего изобретения, чтобы таким образом получить источник щелочного металла, который содержит не менее 10 масс. % содержащего ионы щелочного металла силикатного геля, характеризуется удельной площадью поверхности (БЭТ) от приблизительно 8 м2/г до приблизительно 50 м2/г и высвобождает не менее 1 г калия на 1 кг источника ионов щелочного металла и не менее 1 масс. % кремниевой кислоты в течение 24 часов при воздействии водного раствора, который ненасыщен по калию и диоксиду кремния.
Согласно одному варианту осуществления источник ионов щелочного металла настоящего изобретения получают из содержащего ионы щелочного металла каркасного силиката в виде частиц посредством способа настоящего изобретения, чтобы таким образом получить источник щелочного металла, характеризующийся удельной площадью поверхности по Брунауэру-Эмметту-Теллеру (БЭТ) от приблизительно 3 м2/г до приблизительно 10 м2/г.
Настоящее изобретение имеет множество преимуществ. Например, способ настоящего изобретения для получения источника ионов щелочного металла из калийсодержащей породы не требует сильных кислот или избыточного количества жидкости, и его можно осуществлять при относительно умеренных температурах (≤350°С). Способ настоящего изобретения также позволяет регулировать скорость высвобождения щелочного металла из готового продукта без необходимости в сложных промежуточных стадиях путем подгонки количества образованного геля относительно других содержащих ионы щелочного металла компонентов содержащего ионы щелочного металла каркасного силиката в виде частиц. Также высвобождение калия из продукта связано с введением в почву веществ, которые составляют гель (кремниевой кислоты и гидроксида алюминия), и их осаждением во вторичной фазе, полезной для почвы (а именно, филлосиликаты). Это обеспечивает несколько основных элементов в одном материале и необходимые структурные компоненты для почв таким образом, который описан выше. Кроме того, способ настоящего изобретения предотвращает образование твердых и жидких отходов, которые в противном случае будет необходимо отделять, рециркулировать и складировать перед использованием продукта, например, если продукт используют в качестве удобрения.
Состав и структура материала настоящего изобретения обеспечивают регулирование состава почвы путем регулируемого высвобождения необходимых элементов. Например, в случае очень кислых почв (pH<5) pH можно безопасно повышать при помощи ионов кальция, высвобождаемых из продукта. Кроме того, наличие фазы тоберморита предотвращает полное высвобождение ионов кальция, что может, таким образом, предупреждать повышение pH почвы свыше 7. Силикатный гель обеспечивает усвояемый растениями кремний, который является структурным и защитным элементом для многих растений, в виде мономеров и низкомолекулярных олигомеров кремниевой кислоты, что также принимает участие в осаждении фазы филлосиликата in-situ. Средняя скорость высвобождения калия предупреждает мгновенную утечку калия при орошении. Исходные фазы, когда содержатся в продукте, обеспечивают колонизацию корней растений и длительное медленное высвобождение всех его элементов.
Краткое описание фигур
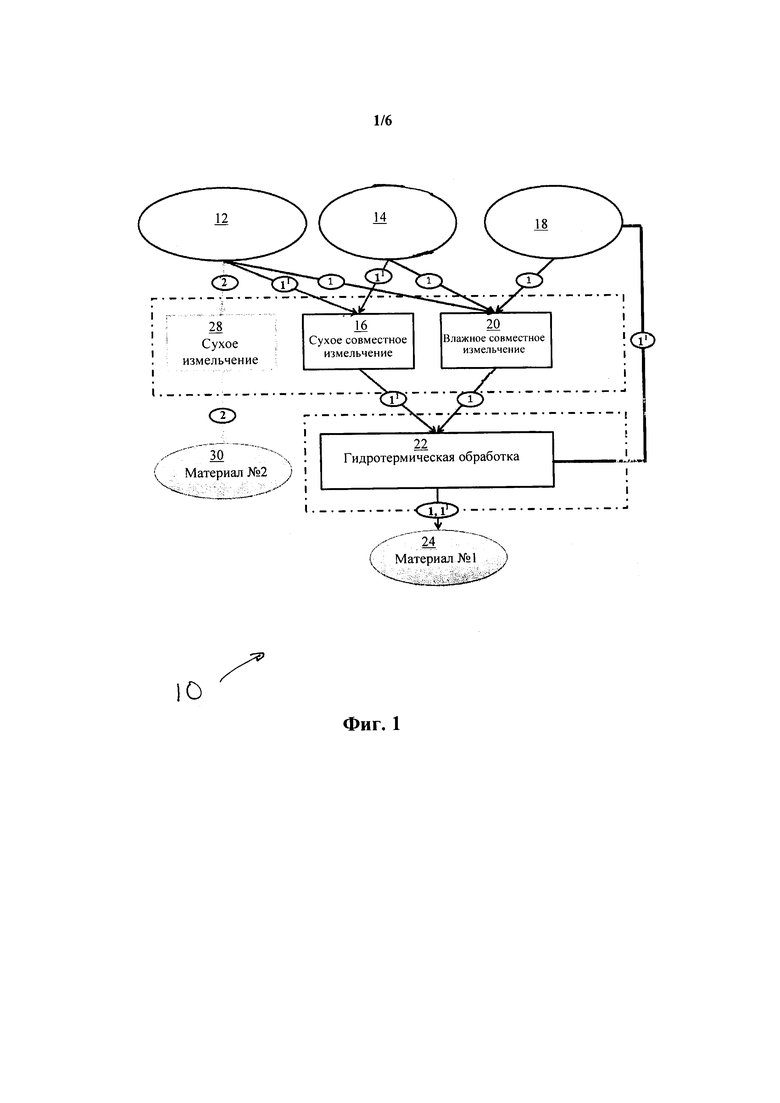
На фиг. 1 показано схематическое изображение последовательности стадий некоторых вариантов осуществления способа согласно настоящему изобретению для получения вариантов продуктов настоящего изобретения.
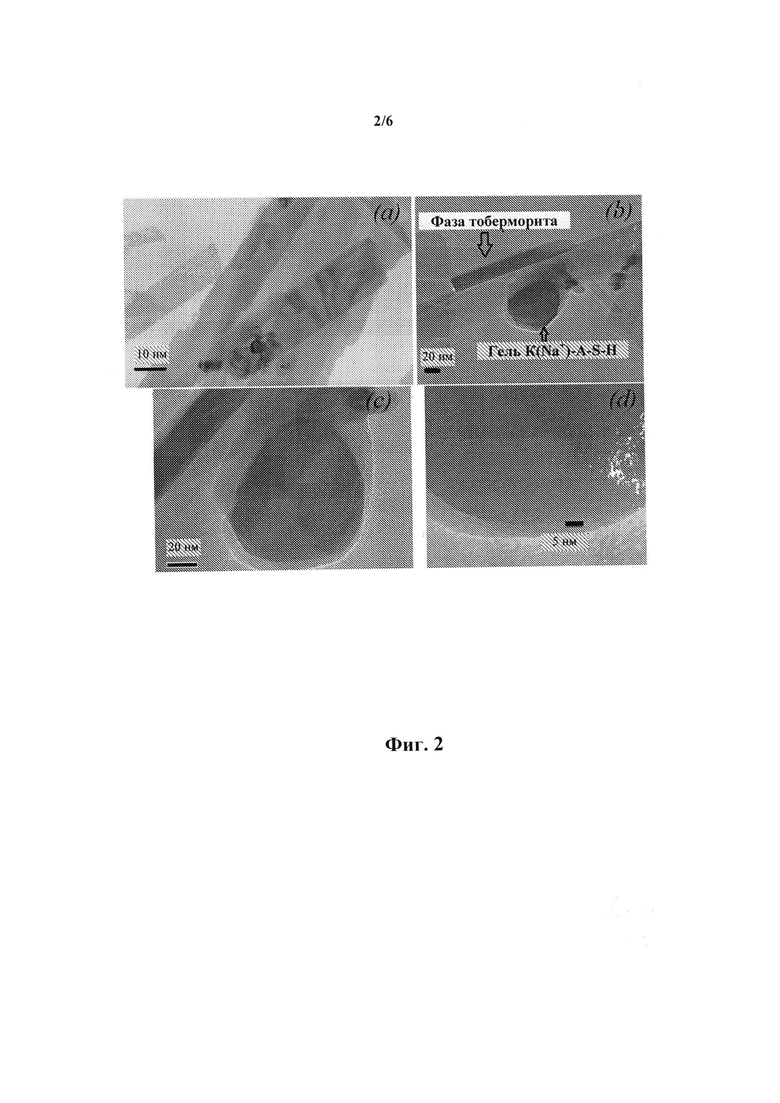
На фиг. 2A-2D представлены изображения трансмиссионной электронной микроскопии (ТЕМ), показывающие аморфный компонент (гель), совместно образованный и стабилизированный вместе с фазой тоберморита, согласно одному варианту осуществления продукта настоящего изобретения, указанный как материал №1.
На фиг. 3A-3D представлены изображения при помощи вторичных электронов для одного варианта осуществления настоящего изобретения.
На фиг. 4А представлено изображение обратного излучения электронов одного варианта осуществления настоящего изобретения; на фиг. 4В представлена композиционная карта согласно энергодисперсионной рентгеновской спектроскопии одного варианта осуществления настоящего изобретения, показывающая распределение калия (светло-серый цвет) в основном материале.
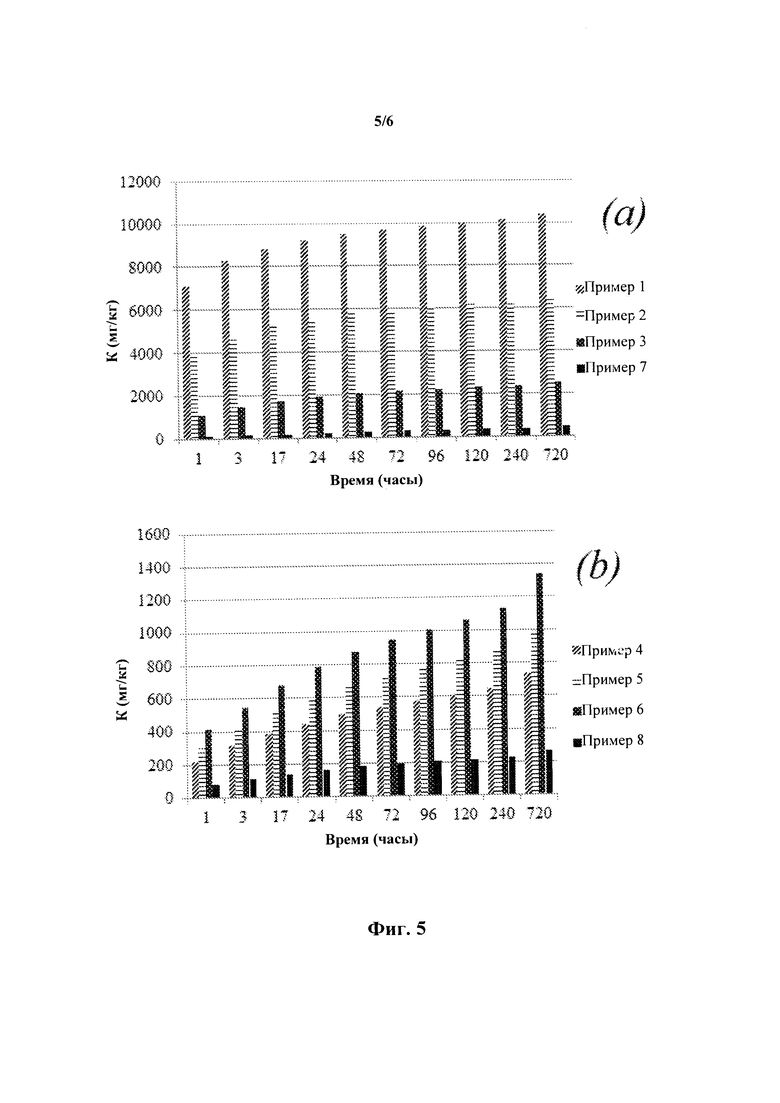
На фиг. 5А-5В представлена динамика суммарных скоростей высвобождения калия (K) вариантов осуществления настоящего изобретения, описанных ниже, и сравнение этих скоростей с контрольными образцами, также описанными ниже.
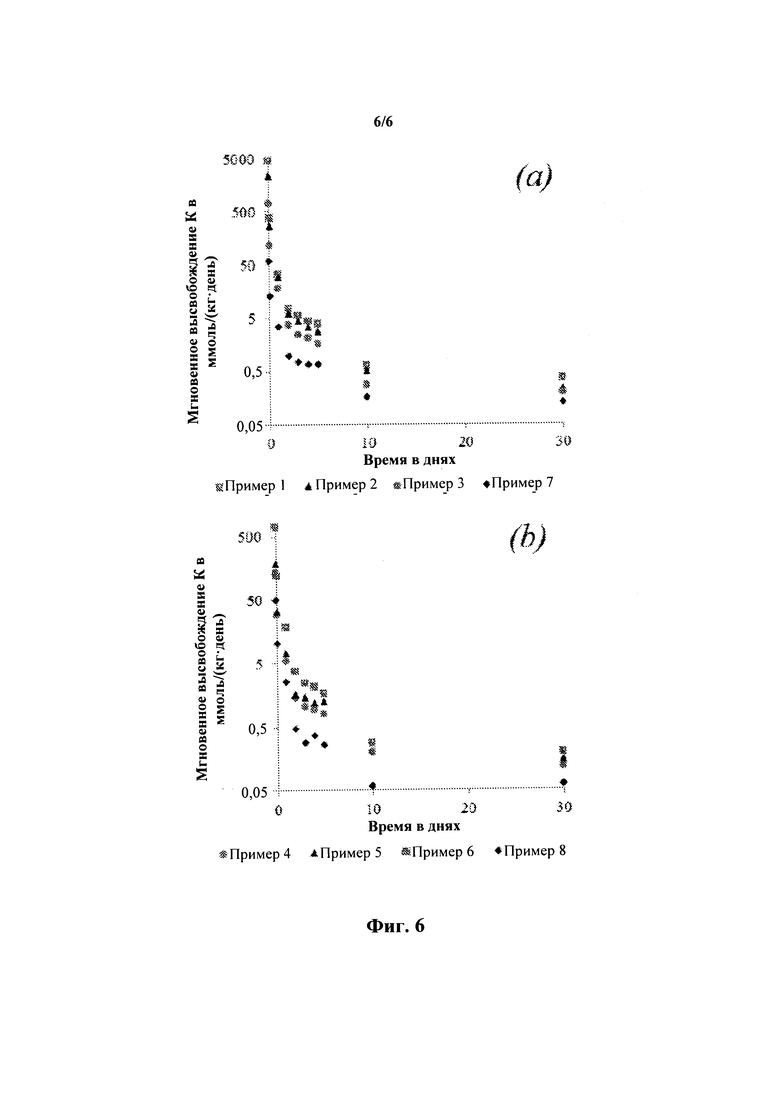
На фиг. 6А и 6В представлены мгновенные скорости высвобождения калия вариантов осуществления настоящего изобретения, описанных ниже, и сравнение этих скоростей с контрольными образцами, также обсуждаемыми ниже.
Подробное раскрытие настоящего изобретения
Вышеуказанное будет очевидно из следующего более подробного описания примера вариантов осуществления настоящего изобретения, как показано на сопутствующих графических материалах, на которых подобные номера позиций относятся к подобным элементам на всех различных видах. Графические материалы не обязательно представлены в масштабе, акцент вместо этого сделан на изображение вариантов осуществления настоящего изобретения.
Настоящее изобретение в общем относится к способу получения источника ионов щелочного металла и источнику ионов металла, полученному посредством способа настоящего изобретения. Источник ионов щелочного металла настоящего изобретения имеет множество применений, например, если щелочной металл представляет собой калий, удобрение для выращивания сельскохозяйственных культур На фиг. 1 представлена схема 10, показывающая некоторые варианты осуществления способа настоящего изобретения. Стадии трех возможных вариантов осуществления способа настоящего изобретения представлены на фиг. 1 как "1" для "процесса 1," "1I" для "процесса 1I" и "2" для "процесса 2". Первый компонент 12, показанный на фиг. 1, представляет собой содержащий ионы щелочного металла каркасный силикат в виде частиц. Следует понимать, что "силикат" в выражении "содержащий ионы щелочного металла каркасный силикат в виде частиц" включает алюмосиликаты.
Согласно одному варианту осуществления способа настоящего изобретения, представленного на фиг. 1, первый компонент 12 получают из подходящей руды, содержащей щелочной металл, которую дробят подходящим способом, известным специалистам в данной области, таким как размол. Например, размер частиц подходящей руды можно уменьшать до среднего размера частиц, равного или меньшего приблизительно 5 мм, что измерено, например, ситовым анализом (способ стандартного тестирования ASTM С136-06 для ситового анализа тонкодисперсных и крупных агрегатов, положения которого включены в настоящий документ ссылкой во всей их полноте). Примеры подходящих щелочных металлов для использования в способе настоящего изобретения для получения источника ионов щелочного металла включают, например, по меньшей мере один элемент из группы, состоящей из лития (Li), натрия (Na) и калия (K). Пример подходящего источника лития включает петалит (LiAlSi4O10). Примеры подходящих источников натрия включают альбит (NaAlSi3O8) и нефелин (Na3KAl4Si4O16). Примеры подходящих источников калия включают калиевый полевой шпат (KAlSi3O8), лейцит (KAlSi2O6), кальсилит (KAlSiO4) и нефелин (Na3KAl4Si4O16). Примеры подходящих источников калия включают руды, такие как сиенит, нефелиновый сиенит и гранит.
Согласно особенно предпочтительному варианту осуществления щелочной металл представляет собой калий, и предпочтительный содержащий ионы щелочного металла каркасный силикат представляет собой калиевый полевой шпат (KAlSi3O8), причем подходящая руда содержит по меньшей мере приблизительно 5 масс. % эквивалентного количества оксида калия (K2O).
Согласно одному варианту осуществления второй компонент содержит, по меньшей мере один из щелочного металла и щелочноземельного металла. Предпочтительно щелочноземельные металлы второго компонента 14 включают по меньшей мере один элемент из группы, состоящей из бериллия (Be), магния (Mg), кальция (Са) и стронция (Sr). Предпочтительно щелочноземельный металл второго компонента включает кальций. Наиболее предпочтительно щелочноземельный металл второго компонента объединяют с первым компонентом, когда щелочноземельный металл находится в виде оксида кальция (СаО) или гидроксида кальция (Са(ОН)2).
Согласно другому варианту осуществления второй компонент содержит щелочной металл. Предпочтительно щелочной металл второго компонента включает по меньшей мере один элемент из группы, состоящей из лития (Li), натрия (Na) и калия (K).
Согласно одному варианту осуществления мольное отношение кремния первого компонента 12 к по меньшей мере одному из щелочноземельного металла и щелочного металла второго компонента 14 находится в диапазоне от приблизительно 1,0:0,1 до приблизительно 1,0:0,3. Согласно предпочтительному варианту осуществления второй компонент 14 содержит кальций в качестве элемента-щелочноземельного металла второго компонента 14 в виде оксида кальция или гидроксида кальция. Исходя из количества оксида кальция, находящегося в твердой смеси первого компонента 12 и второго компонента 14, концентрация оксида кальция предпочтительно находится в диапазоне от приблизительно 5 масс. % до приблизительно 30 масс. % объединенных первого и второго компонентов.
В процессе 1 первый компонент 12 объединяют со вторым компонентом 14 и жидкой водой 20 с образованием смеси жидкости и твердого вещества. Согласно одному варианту осуществления количество присутствующей жидкой воды находится в массовом отношении жидкости к твердому веществу в смеси жидкости и твердого вещества в диапазоне от приблизительно 0,05:1 до приблизительно 5:1, предпочтительно в диапазоне от приблизительно 2:1 до приблизительно 3:1.
Согласно предпочтительному варианту осуществления объединенную смесь жидкости и твердого вещества подвергают влажному совместному измельчению 20, чтобы таким образом уменьшить средний размер частиц содержащего ионы щелочного металла каркасного силиката в виде частиц, пока массовое процентное содержание частиц содержащего ионы щелочного металла каркасного силиката в виде частиц с диаметром 5 мкм или менее не станет по меньшей мере приблизительно 50%. Измельчение смеси жидкости и твердого вещества предпочтительно, но не обязательно. Альтернативно, смесь твердого вещества и жидкости можно обрабатывать гидротермически, как описано ниже, но сначала проводить стадию влажного совместного измельчения.
Смесь жидкости и твердого вещества гидротермически обрабатывают 22 путем подвергания действию повышенной температуры и давления, чтобы таким образом получить содержащий ионы щелочного металла силикатный гель, основной компонент "материала №1" 24. Гель содержит щелочной металл первого компонента, таким образом формируя источник ионов щелочного металла. Согласно предпочтительному варианту осуществления смесь жидкости и твердого вещества подвергают воздействию как температуры в диапазоне от приблизительно 100°С до приблизительно 350°С, так и давления от приблизительно 100 фунтов/кв. дюйм (фунтов силы на квадратный дюйм) до приблизительно 500 фунтов/кв. дюйм, чтобы таким образом получить содержащий ионы щелочного металла силикатный гель. Согласно конкретному варианту осуществления смесь жидкости и твердого вещества подвергают воздействию повышенной температуры и давления до тех пор, пока по существу весь щелочной металл первого компонента не станет компонентом силикатного геля.
В процессе 1I, также представленном на фиг. 1, первый компонент 12 объединяют со вторым компонентом 14 с образованием твердой смеси и необязательно измельчают 16 всухую. В процессе 1I второй компонент 14 содержит по меньшей мере один из оксида и гидроксида по меньшей мере одного из щелочного металла и щелочноземельного металла. Необязательно щелочной металл второго компонента 14 может быть таким же, как щелочной металл первого компонента 12.
Твердую смесь процесса 1I затем гидротермически обрабатывают, как в процессе 1, но с дополнительной водой, при необходимости, чтобы таким образом получить такое же массовое отношение жидкости к твердому веществу, как в процессе 1. Как и в процессе 1, гидротермическая обработка вызывает образование содержащего ионы щелочного металла силикатного геля, основного компонента материала №1.
Согласно одному варианту осуществления материал №1, образованный посредством способа процесса 1 или процесса 1I настоящего изобретения, объединяют с почвой с образованием смеси. Предпочтительно массовое отношение силикатного геля к почве находится в диапазоне от приблизительно 0,0001:1 до приблизительно 0,01:1.
Согласно другому варианту осуществления способ настоящего изобретения, представленный на фиг. 1 как "процесс 2," предусматривает образование источника ионов щелочного металла посредством дробления содержащего ионы щелочного металла каркасного силиката в виде частиц путем сухого измельчения, пока по меньшей мере приблизительно 50 масс. % частиц не будут иметь диаметр равный или меньший приблизительно 5 мкм, что измерено лазерной дифракцией при помощи лазерного дифракционного анализатора размеров частиц в жидком режиме (вода), чтобы таким образом получить "материал №2" 30. Примеры подходящих способов дробления содержащего ионы щелочного металла каркасного силиката в виде частиц включают размол на шаровой мельнице и тонкое измельчение. Примеры подходящих источников содержащего ионы щелочного металла каркасного силиката в виде частиц для использования с данным вариантом осуществления способа являются такими, как описано выше. Согласно предпочтительному варианту осуществления содержащий ионы щелочного металла каркасный силикат в виде частиц представляет собой руду, такую как сиенит, включая, например, нефелиновый сиенит, и гранит, и предпочтительный способ дробления сиенита включает влажный размол на шаровой мельнице.
Согласно одному варианту осуществления настоящее изобретение представляет собой источник ионов щелочного металла, полученный из содержащего ионы щелочного металла каркасного силиката в виде частиц посредством способа настоящего изобретения. Примеры подходящих содержащих ионы щелочного металла каркасных силикатов в виде частиц, из которых получают источник ионов щелочного металла со средней скоростью высвобождения ионов настоящего изобретения, перечислены выше. Согласно одному варианту осуществления источник ионов щелочного металла получают из калиевого полевого шпата, и он имеет удельную площадь поверхности по Брунауэру-Эмметту-Теллеру (БЭТ) в диапазоне от приблизительно 8 м2/г до приблизительно 50 м2/г и удельную площадь поверхности микропор (площадь поверхности пор, полостей и дефектов с глубиной от 4 до 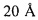 ) в диапазоне от приблизительно 1 м2/г до приблизительно 10 м2/г.
) в диапазоне от приблизительно 1 м2/г до приблизительно 10 м2/г.
Следующие примеры представлены как варианты осуществления настоящего изобретения и не являются ограничивающими.
Пояснение на примере
Механо-гидротермальное изменение калийсодержащих породообразующих минералов
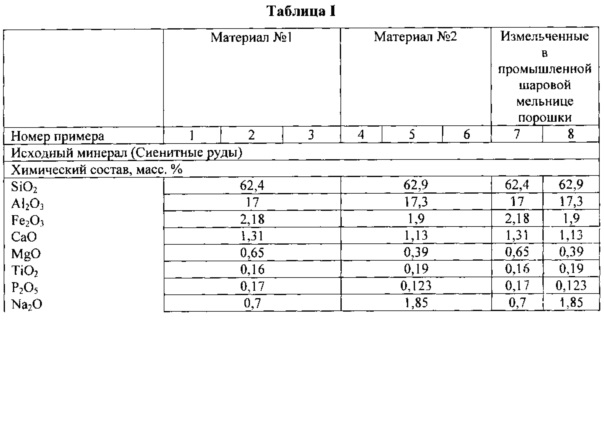
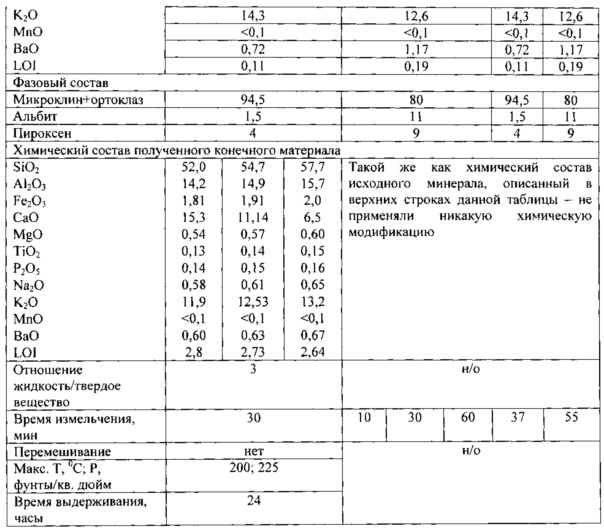
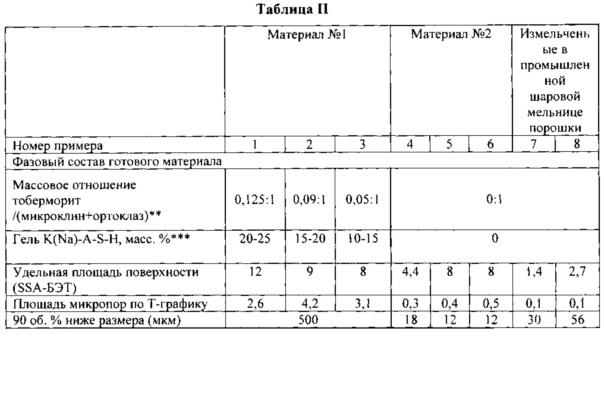
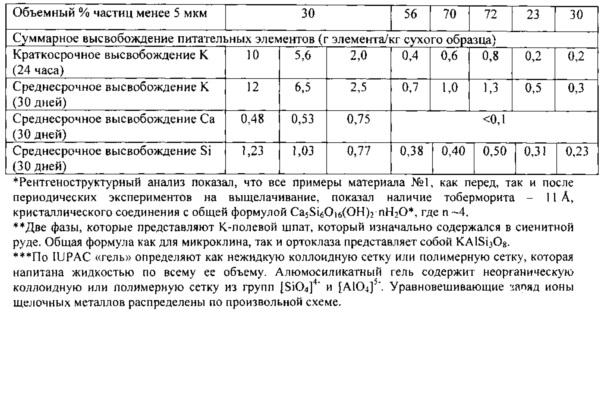
Следующие неограничивающие примеры двух вариантов продуктов настоящего изобретения (материал №1 и материал №2) и измельченных в промышленной шаровой мельнице минеральных порошков представлены в таблицах I и II. Согласно настоящему изобретению в таблице I представлены примеры смесей химических (в оксидах) и минеральных (фазовых) составов исходного минерала (сиенитной руды) и составы продуктов, полученных в конечном итоге. В таблице II представлены некоторые физические свойства продуктов настоящего изобретения, полученных из смесей, описанных в таблице I.
Примеры
10 г грубо перемолотого сырьевого материала (перемолотая сиенитная руда с крупными кристаллическими частицами с неровной поверхностью с размером <5 мм) и состав, указанный в таблице I, смешивали с сухим порошкообразным Са(ОН)2 (Sigma-Aldrich, сорт: ≥96,0%, ≤3,0% карбоната кальция) в течение 5-10 минут перед добавлением воды. Дистиллированную воду добавляли в смесь согласно количеству, указанному в таблице I. Суспензию помещали в камеру мельницы для тонкого помола McCrone, произведенную McCrone Microscope & Accessories из Уэстмонта, Иллинойс, и измельчали в течение 30 минут (массовое отношение между перемалывающими элементами (агатовыми шариками) и образцом составляло приблизительно 4). После измельчения суспензию переносили в емкость высокого давления периодического действия, коммерчески доступную от Parr Instrument Со. из Молина, Иллинойс, и выдерживали при температуре приблизительно 200°С и давлении приблизительно 225 фунтов/кв. дюйм в течение приблизительно 24 часов без перемешивания. После реакции полученную твердую фазу, содержащую остаточную жидкость, сушили в течение ночи при приблизительно 110°С. Конечные составы материала указаны как примеры 1, 2 и 3 в таблице I. Примеры 4, 5 и 6 таблицы I получали только посредством сухого измельчения. Измельчение проводили в мельнице для тонкого помола McCrone; массовое отношение между перемалывающими элементами и образцом минерала составляло приблизительно 67. Данное измельчение не имело заметного влияния на фазовый состав, но обеспечивало положительное воздействие, содействующее увеличению скоростей высвобождения калия, включая увеличение доступной площади поверхности, объем ультратонких частиц и внесение нарушений в структуру кристаллической решетки. Пример 7 (контрольные образцы в эксперименте) готовили только при помощи измельчения в промышленной шаровой мельнице из той же сиенитной руды, что и примеры 1, 2 и 3. Пример 8 (контрольный образец в эксперименте) готовили только при помощи измельчения в промышленной шаровой мельнице из той же сиенитной руды, что и примеры 4, 5 и 6. Параметры измельчения указаны в таблице I, а свойства полученных материалов указаны в таблице II. Следующие аналитические техники использовали для того, чтобы охарактеризовать свойства основных материалов и показатели.
Удельную площадь поверхности согласно Брунауэру-Эмметту-Теллеру (SSA-БЭТ) определяли для каждого из синтезированных образцов. Анализ проводили при помощи анализатора площади поверхности и пористости, используя азот в качестве адсорбирующего газа. В этом испытании изотермы сорбции азота получали на анализаторе площади поверхности и пористости ASAP 2020 Micrometric, доступном от Micrometrics Co., Норкросс, Джорджия, при 77 K. Образцы дегазировали под низким вакуумом при 110°С в течение ~24 часов. Расчет SSA по модели Брунауэра-Эмметта-Теллера (БЭТ) применяли к абсорбционной ветви изотермы. Для оценки площади микропор (площади пор и шероховатости поверхности с глубиной 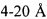 ), применяли модель с Т-графиком.
), применяли модель с Т-графиком.
Анализ распределения частиц по размерам (PSD) проводили для порошкообразных образцов при помощи способа лазерной дифракции, используя лазерный дифракционный анализатор размеров частиц LS 13 320 (Beckman Coulter, Inc.) в жидком режиме (в водной среде). Дифрактограмму получали после предварительной обработки ультразвуком суспензии, направленной на устранение случайной погрешности, вызванной агрегацией.
Фазовый состав согласно порошковой рентгеновской дифракции: Графики порошковой рентгеновской дифракции образцов перед и после экспериментов по выщелачиванию получали при помощи дифрактометра PANalytical X'Pert Pro, доступного от PANalytical, Со. Использовали скорость сканирования 150 с/шаг и оптику падающего/отраженного пучка, рекомендованные для медленного сканирования сложных плохо кристаллизованных образцов. Фазовый состав кристаллической части и количество аморфной части (геля K(Na)-A-S-H) в материале №1 определяли количественным анализом профиля линий рентгенограмм, проводимым при помощи программного обеспечения High-Score plus, доступного от PANalytical, Со.
Микроструктуру материалов изучали при помощи сканирующей электронной микроскопии (SEM) и трансмиссионной электронной микроскопии (ТЕМ). Изучение при помощи сканирующей электронной микроскопии (SEM) проводили при помощи микроскопа JEOL 6610LV, доступного от JEOL USA, Inc., как в режиме с низким вакуумом (30 Па), так и в режиме с высоким вакуумом (<10-3 Па). В режиме с высоким вакуумом использовали ускоряющее напряжение 15-20 кВ, размер пятка 40-50 и рабочее расстояние 1015 мм для изображения при помощи вторичных электронов (SE) для изучения микроструктуры частиц и для определения шероховатости поверхности, топографии, включений и пористости на микронном/субмикронном уровне. Природные дефекты и "искусственные" дефекты, вызванные дроблением, лучше всего различались в этом режиме. Изображение обратнорассеянных электронов (BSE) использовали для определения различных фаз на основании атомного числа для сопоставления размера частиц, формы и их минералогии (если возможно). Энергодисперсионный рентгено-спектральный анализ (EDX) использовали для составления композиционной карты.
Высвобождение питательных элементов (показатели материалов) изучали следующим образом. "Значение краткосрочного суммарного высвобождения K" таблицы II соответствует сумме грамм (г) калия (K), высвобожденного в 3 порции из материала №1, материала №2 и двух контролей - примеров 7 и 8 при помощи свежего раствора с pH=5, проводимого в течение 24 часов (массовое отношение твердого вещества к жидкости = 1:10, pH входящего потока = 5, t=22°С). "Значение среднесрочного суммарного высвобождения K" таблицы II соответствует сумме грамм калия, высвобожденного в 10 порций (каждая порция является заменой старого входящего потока на свежий входящий поток, сохраняя то же самое отношение твердого вещества к жидкости), проводимое в течение 10 дней (массовое отношение твердого вещества к жидкости = 1:10, pH входящего потока = 5, t=22°С). Концентрацию элементов во входящем потоке измеряли путем использования индуктивно-связанно-плазменного масс-спектрометра, предоставленного Agilent Technologies, Inc., США. Высвобождение таких элементов, как кальций Са и Si, анализировали таким же способом, что использовали для измерения скорости высвобождения K.
В дополнение к данным рентгеновской дифракции образование аморфного геля K(Na)-A-S-H в материале №1 вследствие гидротермической обработки подтверждали трансмиссионной электронной микроскопией, и изображения показаны на фиг. 2. Сканирующая электронная микроскопия показала микроструктуру материала №1 на субмикронном/микронном уровне (пример 1, показанный на фиг. 3a-3d). Совместное существование аморфного геля вместе с мелкими кристаллами тоберморита и остаточным кристаллическим K-полевым шпатом в материале №1 показано посредством изображений при помощи вторичных электронов с высоким разрешением (фиг. 2a-2d). Составление композиционной карты при помощи EDX материала №1 (пример 1) показало распределение калия (K показан светло-серым цветом) в основном материале (фиг. 4).
Суммарное высвобождение калия для материала №1 и материала №2, описанное выше, показано на гистограммах и фиг. 5а-5b. Динамика мгновенного высвобождения калия показана на графике на фиг. 6.
При pH≤5 и температуре и давлении окружающей среды как материал №1, так и материал №2 высвобождают K+ и другие ионы посредством двух основных химических механизмов: ионный обмен на поверхности материала-жидкости и гидролиз связей Al-O-Si и Si-O-Si. Как можно увидеть на фиг. 5 и 6, начальное растворение сильно ненасыщенного по K+ входящего потока приводит к быстрому и значительному высвобождению в течение 24 часов как для материала №1, так и материала №2. Дальнейшее высвобождение ограничено скоростью гидролиза, который по существу медленнее, чем начальный ионный обмен.
Доступная удельная площадь поверхности (SSA-БЭТ), концентрация аморфной части (параметр соответствует только материалу №1 и выражен как масс. % геля K(Na)-A-S-H, смотри таблицу II) и поверхностная концентрация дефектов на субнанометровом уровне (параметр соответствует как материалу №1, так и материалу №2 и оценен по площади микропор по Т-графику, смотри таблицу II) вносят вклад в регулирование динамики высвобождения K. Как можно видеть на фиг. 5а для материала №1, чем выше SSA, концентрация аморфной части (геля) и площадь микропор (площадь по Т-графику), тем выше скорость высвобождения K+. Например: материал №1 примера 1 характеризуется наибольшим содержанием геля, SSA-БЭТ и площадью по Т-графику; таким образом, он показывает наибольшее (24-кратное увеличение относительно контрольного образца 7). Пример 2 находится посередине как в отношении свойств материала, описанных выше, так и высвобождения K (13-кратное увеличение относительно контрольного образца). Материал №1 примера 3 также следует этой тенденции и имеет наименьшее (5-кратное) увеличение. Массовое отношение тоберморит/(микроклин + ортоклаз), в свою очередь, вносит вклад в быстродоступное количество Са: чем больше это отношение, тем меньше доступность Са из-за его закрепления в кристаллической структуре тоберморита.
Для материала №2 SSA-БЭТ, площадь микропор и объемная концентрация частиц микронного размера вносят вклад в динамику высвобождения ионов. При других таких же параметрах, материалы примеров 4, 5 и 6 показали 2-кратное, 3-кратное и 4-кратное увеличение высвобождения K относительно контрольного образца 8, соответственно. Сравнивая характеристики высвобождения K материала №1 и материала №2, целесообразно сделать вывод, что, в общем, влияние только механической обработки значительно ниже, чем влияние механо-химической обработки.
Идеи всех патентов, опубликованных заявок и ссылок, цитируемых в настоящем документе, включены ссылкой во всей их полноте.
Хотя настоящее изобретение было подробно показано и описано со ссылками на примерные варианты его осуществления, специалистам в данной области будет понятно, что различные изменения в его форме и деталях можно осуществить, без отклонения от объема настоящего изобретения, охваченного приложенной формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СМЕШАННЫЙ ТЕМПЛАТНЫЙ СИНТЕЗ Cu-CHA С ВЫСОКИМ СОДЕРЖАНИЕМ ДИОКСИДА КРЕМНИЯ. | 2014 |
|
RU2703462C1 |
| СИНТЕЗ ЦЕОЛИТА AEI | 2014 |
|
RU2744763C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ ЗАГРЯЗНЯЮЩИХ МЕТАЛЛОВ ИЗ ПОТОКОВ ЖИДКОСТЕЙ | 1998 |
|
RU2176155C2 |
| ПОЛУЧЕННЫЕ ИЗ ТРИГИДРАТА ОКСИДА АЛЮМИНИЯ КОМПОЗИТЫ ОКСИДА АЛЮМИНИЯ С БОЛЬШИМ ОБЪЕМОМ ПОР И БОЛЬШОЙ ПЛОЩАДЬЮ ПОВЕРХНОСТИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2000 |
|
RU2259232C2 |
| ЦЕОЛИТНЫЕ КАТАЛИЗАТОРЫ, СОДЕРЖАЩИЕ МЕТАЛЛЫ | 2013 |
|
RU2634899C2 |
| СИНТЕТИЧЕСКИЙ ЦЕОЛИТ, СОДЕРЖАЩИЙ КАТАЛИТИЧЕСКИЙ МЕТАЛЛ | 2017 |
|
RU2740186C2 |
| ВЫСОКОКРЕМНЕЗЕМНЫЙ ЦЕОЛИТ AEI | 2017 |
|
RU2746017C2 |
| КАТАЛИЗАТОР ДЛЯ ОБРАБОТКИ ВЫХЛОПНЫХ ГАЗОВ | 2014 |
|
RU2675821C2 |
| УПРАВЛЕНИЕ ВРЕМЕНЕМ СХВАТЫВАНИЯ У ГЕОПОЛИМЕРНЫХ КОМПОЗИЦИЙ, СОДЕРЖАЩИХ РЕАКЦИОННОСПОСОБНЫЕ АЛЮМОСИЛИКАТНЫЕ МАТЕРИАЛЫ, ХАРАКТЕРИЗУЮЩИЕСЯ ВЫСОКИМ УРОВНЕМ СОДЕРЖАНИЯ Ca | 2018 |
|
RU2795134C2 |
| КАТАЛИЗАТОР ДЛЯ ОБРАБОТКИ ВЫХЛОПНЫХ ГАЗОВ | 2014 |
|
RU2771714C2 |


Группа изобретений относится к неорганической химии и может быть использовано в сельском хозяйстве. Источник ионов щелочного металла получают посредством способа, который предусматривает: а) объединения содержащего ионы щелочного металла каркасного силиката с оксидом или гидроксидом щелочноземельного или щелочного металлов с образованием твердой смеси; b) подвергания твердой смеси гидротермической обработке с образованием геля, который содержит кремний и щелочной металл. Мольное отношение кремния к щелочноземельному или щелочному металлу находится в диапазоне от приблизительно 1,0:0,1 до приблизительно 1,0:0,3. Гидротермическая обработка включает подвергание твердой смеси воздействию температуры в диапазоне от 100 до 350°С для образования геля. Обеспечивается повышение эффективности и увеличение скорости высвобождения ионов щелочного металла. 2 н. и 56 з.п. ф-лы, 8 пр., 2 табл., 6 ил.
1. Способ получения источника ионов щелочного металла, предусматривающий стадии:
a) объединения содержащего ионы щелочного металла каркасного силиката в виде частиц первого компонента со вторым компонентом, который содержит по меньшей мере один из оксида и гидроксида по меньшей мере одного из щелочноземельного металла и щелочного металла, с образованием твердой смеси, причем мольное отношение кремния к по меньшей мере одному из щелочноземельного металла и щелочного металла второго компонента в твердой смеси находится в диапазоне от приблизительно 1,0:0,1 до приблизительно 1,0:0,3; и
b) подвергания твердой смеси гидротермической обработке с образованием геля, который содержит кремний и щелочной металл из первого компонента, таким образом получая источник ионов щелочного металла,
при этом гидротермическая обработка включает подвергание твердой смеси воздействию температуры в диапазоне от 100 до 350°С для образования геля.
2. Способ по п. 1, в котором щелочной металл первого компонента включает по меньшей мере один элемент из группы, состоящей из лития, натрия и калия.
3. Способ по п. 2, в котором щелочной металл первого компонента включает калий.
4. Способ по п. 3, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц представляет собой алюмосиликат.
5. Способ по п. 4, в котором содержащий ионы щелочного металла каркасный алюмосиликат включает по меньшей мере один элемент, выбранный из группы, состоящей из калиевого полевого шпата (KAlSi3O8), лейцита (KAlSi2O6), кальсилита (KAlSiO4) и нефелина (Na3KAl4Si4O16).
6. Способ по п. 4, в котором первый компонент содержит по меньшей мере приблизительно 5 масс. % эквивалентного количества K2O.
7. Способ по п. 1, в котором второй компонент содержит щелочной металл.
8. Способ по п. 7, в котором щелочной металл второго компонента включает по меньшей мере один элемент из группы, состоящей из лития (Li), натрия (Na) и калия (K).
9. Способ по п. 1, в котором второй компонент содержит щелочноземельный металл.
10. Способ по п. 9, в котором щелочноземельный металл второго компонента включает по меньшей мере один элемент из группы, состоящей из бериллия (Be), магния (Mg), кальция (Са), стронция (Sr).
11. Способ по п. 10, в котором щелочноземельный металл второго компонента включает кальций (Са).
12. Способ по п. 11, в котором кальций второго компонента находится в виде гидроксида кальция (Са(ОН)2).
13. Способ по п. 12, в котором количество гидроксида кальция находится в объединенной твердой смеси в диапазоне от приблизительно 5 масс. % до приблизительно 30 масс. %.
14. Способ по п. 1, дополнительно предусматривающий стадию объединения смеси с жидкой водой с образованием смеси жидкости и твердого вещества перед гидротермической обработкой.
15. Способ по п. 14, в котором количество жидкости, находящейся в смеси жидкости и твердого вещества, находится в массовом отношении жидкости к твердому веществу в диапазоне от приблизительно 0,05:1 до приблизительно 5:1.
16. Способ по п. 15, дополнительно предусматривающий стадию измельчения твердой смеси, чтобы таким образом уменьшить средний размер частиц первого компонента так, чтобы объемный процент указанных частиц с диаметром 5 мкм или менее составлял по меньшей мере приблизительно 30%.
17. Способ по п. 16, дополнительно предусматривающий стадию измельчения твердой смеси, чтобы таким образом уменьшить средний размер частиц первого компонента так, чтобы объемный процент указанных частиц с диаметром 5 мкм или менее составлял по меньшей мере приблизительно 50%.
18. Способ по п. 16, в котором жидкую воду добавляют перед стадией измельчения.
19. Способ по п. 16, в котором жидкую воду добавляют после стадии измельчения.
20. Способ по п. 16, в котором гидротермическая обработка предусматривает подвергание смеси жидкости и твердого вещества воздействию температуры в диапазоне от приблизительно 100°С до приблизительно 350°С в течение периода времени, вполне достаточного для образования геля, который содержит диоксид кремния и щелочной металл из первого компонента, в количестве не менее 10 масс. %.
21. Способ по п. 20, в котором щелочной металл первого компонента представляет собой калий.
22. Способ по п. 1, дополнительно предусматривающий стадию образования первого компонента путем уменьшения размера частиц до размера частиц равного или меньшего приблизительно 5 мм.
23. Способ по п. 22, дополнительно предусматривающий стадию объединения источника ионов щелочного металла с почвой.
24. Способ по п. 1, в котором твердую смесь подвергают воздействию повышенной температуры и давления до тех пор, пока по существу весь щелочноземельный металл первого компонента не станет компонентом геля.
25. Способ по п. 1, в котором массовое отношение фазы тоберморита к фазам непрореагировавшего содержащего ионы щелочного металла каркасного силиката источника ионов щелочного металла составляет от приблизительно 1:1 до приблизительно 0:1.
26. Способ по п. 1, в котором массовое процентное содержание геля K(Na)-A-S-H источника ионов щелочного металла составляет от приблизительно 10% до приблизительно 100%.
27. Способ по п. 1, в котором удельная площадь поверхности источника ионов щелочного металла составляет от приблизительно 8 до 50 м2/г.
28. Способ по п. 1, дополнительно предусматривающий стадию уменьшения размера частиц содержащего ионы щелочного металла каркасного силиката, пока по меньшей мере приблизительно 50 масс. % частиц не будут иметь диаметр равный или меньше 5 мкм, что измерено лазерным анализом распределения частиц по размерам.
29. Способ по п. 28, в котором щелочной металл первого компонента включает по меньшей мере один элемент из группы, состоящей из лития, натрия и калия.
30. Способ по п. 29, в котором щелочной металл содержащего ионы щелочного металла каркасного силиката включает калий.
31. Способ по п. 30, в котором силикат содержащего ионы щелочного металла каркасного силиката в виде частиц представляет собой алюмосиликат.
32. Способ по п. 31, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц включает по меньшей мере один элемент, выбранный из группы, состоящей из калиевого полевого шпата (KAlSi3O8), лейцита (KAlSi2O6), кальсилита (KAlSiO4) и нефелина (Na3Kal4Si4O16).
33. Способ по п. 32, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц содержит по меньшей мере приблизительно 5 масс. % эквивалентного количества K2O.
34. Способ по п. 33, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц включает по меньшей мере один элемент из группы, состоящей из сиенита и гранита.
35. Способ по п. 1, в котором источник ионов щелочного металла имеет удельную площадь поверхности по Брунауэру-Эмметту-Теллеру (БЭТ) от приблизительно 3 м2/г до приблизительно 10 м2/г.
36. Способ по п. 35, в котором щелочной металл содержащего ионы щелочного металла каркасного силиката в виде частиц включает по меньшей мере один элемент из группы, состоящей из лития, натрия и калия.
37. Способ по п. 36, в котором щелочной металл содержащего ионы щелочного металла каркасного силиката в виде частиц включает калий.
38. Способ по п. 37, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц представляет собой алюмосиликат.
39. Способ по п. 38, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц включает по меньшей мере один элемент, выбранный из группы, состоящей из калиевого полевого шпата (KAlSi3O8), лейцита (KAlSi2O6), кальсилита (KAlSiO4) и нефелина (Na3KAl4Si4O16).
40. Способ по п. 39, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц содержит по меньшей мере приблизительно 5 масс. % эквивалентного количества K2O.
41. Способ по п. 35, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц включает по меньшей мере один элемент из группы, состоящей из сиенита, нефелинового сиенита и гранита.
42. Способ по п. 1, в котором гидротермическая обработка дополнительно включает подвергание твердой смеси воздействию давления от 100 до 500 фунтов/кв. дюйм в течение по меньшей мере части периода времени, в который твердую смесь подвергают воздействию температуры от 100 до 350°С.
43. Источник ионов щелочного металла, полученный посредством способа, предусматривающего стадии:
а) объединения содержащего ионы щелочного металла каркасного силиката в виде частиц первого компонента со вторым компонентом, который содержит по меньшей мере один из оксида и гидроксида по меньшей мере одного из щелочноземельного металла и щелочного металла, с образованием твердой смеси, причем мольное отношение кремния к по меньшей мере одному из щелочноземельного металла и щелочного металла второго компонента находится в диапазоне от приблизительно 1,0:0,1 до приблизительно 1,0:0,3; и
b) подвергания твердой смеси гидротермической обработке с образованием геля, который содержит диоксид кремния и щелочной металл из первого компонента, таким образом получая источник ионов щелочного металла, состоящий из содержащего ионы щелочного металла силикатного геля в количестве не менее 10 масс. %, причем источник ионов щелочного металла характеризуется удельной площадью поверхности (БЭТ) от приблизительно 8 м2/г до приблизительно 50 м2/г, причем источник ионов щелочного металла высвобождает не менее 1 г калия на 1 кг источника ионов щелочного металла и не менее 1 масс. % кремниевой кислоты в течение 24 часов при воздействии водного раствора, который ненасыщен по калию и диоксиду кремния,
при этом гидротермическая обработка включает подвергание твердой смеси воздействию температуры в диапазоне от 100 до 350°С для образования геля.
44. Источник ионов щелочного металла по п. 43, дополнительно содержащий стадию объединения смеси с жидкой водой с образованием смеси жидкости и твердого вещества перед гидротермической обработкой.
45. Источник ионов щелочного металла по п. 44, в котором количество жидкости, находящееся в смеси жидкости и твердого вещества, находится в массовом отношении жидкости к твердому веществу смеси в диапазоне от приблизительно 0,05:1 до 5:1.
46. Источник ионов щелочного металла по п. 45, дополнительно содержащий стадию измельчения твердой смеси.
47. Источник ионов щелочного металла по п. 46, в котором жидкая вода добавлена в твердую смесь перед стадией измельчения.
48. Источник ионов щелочного металла по п. 47, в котором жидкая вода добавлена в твердую смесь после стадии измельчения.
49. Источник ионов щелочного металла по п. 43, в котором щелочной металл содержащего ионы щелочного металла каркасного силиката в виде частиц включает по меньшей мере один элемент из группы, состоящей из лития, натрия и калия.
50. Источник ионов щелочного металла по п. 49, в котором щелочной металл содержащего ионы щелочного металла каркасного силиката в виде частиц включает калий.
51. Источник ионов щелочного металла по п. 50, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц представляет собой алюмосиликат.
52. Источник ионов щелочного металла по п. 51, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц включает по меньшей мере один элемент, выбранный из группы, состоящей из калиевого полевого шпата (KAlSi3O8), лейцита (KAlSi2O6), кальсилита (KAlSiO4) и нефелина (Na3KAl4Si4O16).
53. Источник ионов щелочного металла по п. 52, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц содержит по меньшей мере приблизительно 5 масс. % эквивалентного количества K2O.
54. Источник ионов щелочного металла по п. 52, в котором содержащий ионы щелочного металла каркасный силикат в виде частиц включает по меньшей мере один элемент из группы, состоящей из сиенита, нефелинового сиенита и гранита.
55. Источник ионов щелочного металла по п. 43, у которого массовое отношение фазы тоберморита к сумме фаз микроклина плюс ортоклаза источника ионов щелочного металла составляет от приблизительно 0,1:1 до приблизительно 0:1.
56. Источник ионов щелочного металла по п. 43, у которого массовое процентное содержание геля K(Na)-A-S-H источника ионов щелочного металла составляет от приблизительно 10% до приблизительно 100%.
57. Источник ионов щелочного металла по п. 43, у которого удельная площадь поверхности источника ионов щелочного металла составляет от приблизительно 8 м2/г до 50 м2/г.
58. Источник ионов щелочного металла по п. 43, в котором гидротермическая обработка дополнительно включает подвергание твердой смеси воздействию давления от 100 до 500 фунтов/кв. дюйм в течение по меньшей мере части периода времени, в который твердую смесь подвергают воздействию температуры от 100 до 350°С.
| CN 102408256 A, 11.04.2012 | |||
| Способ получения метасиликата кальция | 1981 |
|
SU986852A1 |
| Способ получения пористых гранул | 1988 |
|
SU1640129A1 |
| US 20110002870 A1, 06.01.2011 | |||
| CN 102583429 A, 18.07.2012 | |||
| Способ количественного определения антрахинона | 1961 |
|
SU142802A1 |
| BIAO ZHANG et al | |||
| Study on thermal treatment schedule of leucite microcrystallizatin to reinforce dental glass ceramics, Zhonghua kouqiang yixue zazhi - Chinese journal of stomatology, 2003, vol | |||
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПРЕПАРАТА ЖИДКОГО ЗОЛОТА | 1922 |
|
SU1002A1 |
Авторы
Даты
2018-10-02—Публикация
2014-05-06—Подача