Изобретение относится к медицине и физиологии, а именно к способам определения степени активации стресс-системы у пациентов по параметрам кожной проводимости, и может быть использован в комплексной оценке стресса, в том числе болевого, у новорожденных, детей грудного и раннего возраста, а также у пациентов других возрастных групп, с которыми невозможен или затруднен вербальный контакт, или находящихся в бессознательном состоянии.
Известно, что стресс является пусковым механизмом в развитии сложной защитной реакции вегетативного типа и сопровождается напряжением функциональных систем организма: дыхания, кровообращения, гормональной регуляции, метаболизма и гомеостаза. Состояние функционального напряжения (реакция напряжения) представляет собой начальную стадию ответной реакции организма на воздействие стрессорных факторов. Это состояние характеризуется мобилизацией - повышением уровня функционирования физиологических систем и адаптационных резервов организма, обеспечивающих приспособительный эффект (см. публикацию Г. Селье, 1956).
Мобилизация энергетических ресурсов, выраженная при стресс-реакции достаточно сильно, обеспечивает срочную адаптацию организма к стрессорной ситуации и является положительным адаптивным фактором. В противоположность этому, при затянувшейся и/или чрезмерно интенсивной стресс-реакции, когда не происходит формирования структурных следов адаптации, интенсивная мобилизация энергетических ресурсов организма перестает быть адаптивным фактором и приводит к прогрессирующему истощению физиологических резервов организма. Состояние неудовлетворительной адаптации характеризуется понижением уровня функционирования и развитием утомления. Это состояние, как правило, является результатом истощения физиологических резервов.
Эффективность адаптивной реакции на стрессоры и вероятность возникновения стрессорных повреждений в значительной мере определяются, помимо интенсивности и продолжительности действия стрессора, состоянием стресс-системы: ее базальной (исходной) активностью и реактивностью, т.е. степенью активации при стрессе, (см. публикацию Мороз Б.Б. с соавт., 2001).
Устойчивость к стрессовым воздействиям в основном определяется взаимодействием стресс-системы и стресс-лимитирующих систем, которые обусловлены как генетическими особенностями организма, так и возможностью их совершенствования в процессе жизнедеятельности под воздействия различных стрессирующих факторов. В результате взаимодействия стресс-системы и системы, специфически ответственной за адаптацию, достигается восстановление гомеостаза (т.е. адаптация к данному стрессору) и соответственно завершается стресс-реакция. Однако при прочих равных условиях эта схема реализуется только в тех случаях, когда сила и продолжительность действия стресс-фактора умеренны, т.е. тогда, когда реализуются положительные, т.е. адаптивные эффекты стресс-реакции. Чрезмерно сильное стрессорное воздействие, превышающее функциональные резервы организма, сопровождается снижением адаптационных возможностей и вызывает превращение этих эффектов в повреждающие, приводя к нарушению функций, повреждениям органов и тканей. В условиях реакции напряжения, каждый из механизмов стрессового ответа имеет компенсаторный предел и, если воздействие стрессора не прекращается, наблюдается кумулятивный эффект, нарастает напряжение, что закономерно может привести к перенапряжению и дистрессу, и, соответственно, к дисфункциональным и патологическим состояниям (см. публикацию Ф.З Меерсон с соавт., 1981, 1988).
Интенсивность (сила) воздействия факторов стресса не отражает в полной мере состояние напряжения в организме, т.к. величина ответной реакции физиологических систем определяется не только интенсивностью, но и продолжительностью действия стрессоров и накопительным эффектом негативных последствий от действия повторяющихся стрессовых стимулов. Кратковременный сильный стресс вызывает срочную кратковременную ответную реакцию, и после прекращения действия стрессора физиологические параметры быстро возвращаются к исходному уровню. В противоположность этому, менее интенсивный, но продолжительный стресс приводит к истощению функциональных резервов организма. С позиций физиологии, продолжительность стресса имеет большее значение, чем его интенсивность. Чем дольше действуют факторы стресса, тем вероятнее наступление стадии истощения и, соответственно, вероятнее развитие дистресса.
Вегетативная нервная система (ВНС), посредством взаимодействия симпатической и парасимпатической подсистем, обеспечивает реактивность функционирования, осуществляя срочную регуляцию, координацию и адаптацию деятельности в состоянии относительного покоя, а также в ответ на действие факторов стресса. Динамическое равновесие функционирования симпатического и парасимпатического звеньев ВНС отражает адекватную реакцию в ответ на воздействие различных внутренних и внешних факторов на организм, в противоположность этому, вегетативный дисбаланс, в котором одна ветвь вегетативной нервной системы преобладает над другой, связан с отсутствием динамического равновесия. Симпатическая гиперактивность в сочетании с парасимпатической гипоактивностью может являться патологическим механизмом, ведущим к повышенному риску неблагоприятных исходов. Несмотря на диагностическую значимость оценки вегетативной реактивности у пациентов, принятые для этой цели пробы (холодовая и тепловая пробы, кардиоваскулярные вегетативные рефлексы, проба с глубоким дыханием, изометрическим напряжением и т.д.) не могут быть использованы для оценки реактивности у пациентов в отделениях реанимации и интенсивной терапии.
Одним из потенциальных неинвазивных маркеров, отражающим симпатическую активность является кожная проводимость (см. публикации McEwen B.S., 2007; Chida Y., Steptoe A., 2010; Lovallo W.R., 2011). Записи кожной проводимости представляют собой следующие друг за другом в определенном ритме волны колебаний. Характер ответа кожной проводимости зависит от стимула. Так, например, при стимуляции глубоким вдохом преимущественно формируется парасимпатический ответ, а при электрокожной стимуляции - симпатический. Возможна одновременная активация механизмов тормозящих и усиливающих потоотделение.
Известно, что определение параметров кожной проводимость (ЭДА) является объективным чувствительным индикатором функционирования ВНС. Изучение потенциалов кожи в условиях клиники показало зависимость кожной проводимости от состояния вегетативной нервной системы и возможность суждения по электрическим показателям кожи о целом ряде различных особенностей протекания патологических процессов. Кожная проводимость быстро реагируют на любые изменения психо-эмоционального и функционального состояния пациента, и параметры кожной проводимости способны объективно и оперативно отражать величину и направленность реакции напряжения. Однако практически во всех работах отмечается существенная зависимость физиологических норм от индивидуальных особенностей пациента, что позволяет надежно диагностировать только резко выраженные изменения состояния, такие как шок, гипоксия и т.д. В этой связи наибольшую диагностическую значимость может иметь изменение параметров кожной проводимости в динамике, что позволит составить представление о состояние пациента с учетом его индивидуальных особенностей. Детальное изучение функциональной реактивности с помощью переменных, характеризующих деятельность вегетативной нервной системы, в частности кожной проводимости как показателя симпатической активности, в условиях действия различных стресс-факторов, может предоставить важную информацию о стрессе (см. публикацию Visnovcova Z., et al, 2013)
Актуальным для клинической практики до настоящего времени остается вопрос разработки диагностических критериев, позволяющих дифференцировать состояния функционального напряжения и повреждающие эффекты стресса для своевременного выявления негативной динамики и предотвращения дальнейшего ухудшения состояния пациента и предотвращения стадии истощения.
За последние годы в многочисленных литературных источниках раскрыта и подтверждена правомерность использования параметров кожной проводимости в оценке болевого стресса, и наиболее надежным (информативным) критерием стресс-реакции является количество (частота) колебаний (флуктуации) кожной проводимости (пик/сек.) (см. публикации Hellerud В.С, Storm Н., 2002; Anand К.J.S., et al, 2007; Т. Ledowski et al, 2007; J. Brinkmeyer, 2008; A Elfering, 2011; Н.И. Мельникова с соавт.. 2011; Ю.В. Жиркова с соавт., 2011; О.Ю. Терлякова с соавт., 2013; В. Kikhia et al, 2016).
Из уровня техники известны различные способы определения стресса, в том числе болевого, основанные на измерении, регистрации и анализе параметров кожной проводимости (US 8512240, А61В 5/00, опубл. 20.08.2013; KR 20130016708, А61В 5/05, опубл. 18.02.2013; US 2015018707, А61В 5/053, опубл. 15.01.2015). Однако известные способы не могут обеспечить достоверную оценку степени активации стресс-системы у пациента, поскольку полученные данные не являются результатом всестороннего анализа проявления стресс-реакций.
Известен также способ мониторинга для оценки стресса и интенсивности боли, включающий выборку и сохранение пороговых данных, пошаговый процесс мониторинга, включающий в себя: непрерывное или дискретное во времени измерение проводимости кожи, сохранение в памяти результатов измерения, получение результатов анализа текущих и предшествующих измерений проводимости; указанные результаты анализа состоят из флуктуации частоты и амплитуды сигнала проводимости во временном интервале, содержащем недавно истекшие моменты времени, где результаты анализа в отношении частоты получаются посредством подсчета максимальных значений, содержащихся в указанном временном интервале, сравнение полученных результатов анализа с пороговыми данными и определение повышенной болевой реакции пациента по показателям частоты и амплитуды кожной проводимости (US 6571124, А61В 5/053, опубл. 27.05.2003).
Исследования по клиническому применению данного способа выявили как положительные (см. публикации Ledowski Т et al., 2006; Ledowski et al., 2007; Hullett et al., 2009), так и отрицательные результаты (см. публикации Е.К. Choo et al., 2010; Е.К. Choo, 2013, Savino F et al, 2013; Ledowski T, et al., 2009; Czaplik M, et al., 2012; Gunther A., 2016). При этом положительные результаты были получены авторами в тех случаях, когда частота пиков в секунду усреднялась за 5-15 секунд, а в противоположность этому, усреднение значений частоты пиков за 30-60 секунд приводили к отрицательным результатам. Противоречивость результатов клинического применения предложенного способа оценки интенсивности боли может быть объяснена тем, что данный способ определения интенсивности боли может быть эффективен только для оценки кратковременных болевых стимулов при болезненных манипуляциях, например укол скарификатором при взятии проб крови. Кроме того, метод позволяет оценить только интенсивность (силу) болевых стимулов, но не учитывает их продолжительность и возможный кумулятивный эффект, что не позволяет составить представление о напряжении компенсаторных систем организма в динамике, т.е. оценить степень активации стресс-системы.
Задачей заявленного изобретения является разработка способа определения степени активации стресс-системы, отражающей реакцию напряжения организма, у невербальных пациентов разных возрастных групп в сознательном и бессознательном состоянии, лишенного недостатков вышеуказанных аналогов, а также расширение арсенала средств указанного назначения.
Техническим результатом заявленного изобретения является повышение объективности неинвазивного способа определения степени активации стресс-системы, отражающей реакцию напряжения организма, у невербальных пациентов разных возрастных групп или находящихся в бессознательном состоянии.
Выявление степени активации стресс-системы необходимо для оптимизации тактики ведения пациентов с учетом их индивидуальных особенностей с целью своевременной профилактики перенапряжения функциональных систем организма и предотвращения развития дистресса.
Технический результат достигается тем, что способ определения степени активации стресс-системы у пациентов включает измерение параметров кожной проводимости и по параметрам кожной проводимости определяют степень активации стресс-системы путем вычисления отношения показателя кумулятивного эффекта стресса к показателю вегетативной реактивности, при этом кумулятивный эффект стресса определяют путем вычисления суммы всех значений интенсивности стресс-реакции, превышающих 0,01 пик/сек, интенсивность стресс-реакции определяют путем усреднения значений частоты флуктуаций кожной проводимости за установленный временной интервал, а показатель вегетативной реактивности определяют по значению вариабельности частоты флуктуаций кожной проводимости путем вычисления отношения среднего квадратичного отклонения значений частоты флуктуаций кожной проводимости к среднему значению частоты флуктуаций кожной проводимости за установленный временной интервал, причем значение показателя степени активации стресс-системы меньше 15 усл. ед. соответствует нормальной степени активации стресс-системы, а значение показателя степени активации стресс-системы больше 15 усл. ед. отражает увеличение степени активации стресс-системы.
Повышение объективности определения степени активации стресс-системы у пациентов достигается за счет использования для ее определения таких расчетных показателей, как интенсивность стресс-реакции, вегетативная реактивность и кумулятивный эффект стресса.
В заявленном способе определения степени активации стресс-системы измеряют параметры кожной проводимости пациента и одновременно по параметрам кожной проводимости в динамике рассчитывают и оценивают качественно (графически) и количественно (по соответствующей шкале) за период непрерывного мониторирования показатели: интенсивность стресс-реакции, кумулятивный эффект стресса, вегетативная реактивность и интегральный показатель - степень активации стресс-системы.
Непрерывно в режиме реального времени в течение всего периода мониторирования регистрируют и автоматически усредняют частоту флуктуаций кожной проводимости времени и рассчитывают вариабельность частоты флуктуаций кожной проводимости за установленный временной интервал. Выбор интервала времени зависит от поставленных медицинским персоналом задач при мониторировании. Усредненные значения частоты кожной проводимости отражают интенсивность стресс-реакции. Рассчитанные значения вариабельности частоты отражают вегетативную реактивность.
В качестве показателя вегетативной реактивности используется значение вариабельности частоты флуктуаций кожной проводимости. Рассчитывают отношение среднего квадратичного отклонения к среднему значению частоты флуктуаций кожной проводимости за установленный интервал времени.
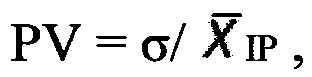
где: PV - показатель вегетативной реактивности, пик/сек;
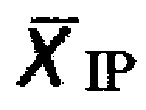 - значение средней частоты флуктуаций кожной проводимости за установленный интервал времени, пик/сек;
- значение средней частоты флуктуаций кожной проводимости за установленный интервал времени, пик/сек;
σ - среднее квадратичное отклонение значений частоты флуктуаций кожной проводимости.
В качестве показателя кумулятивного эффекта стресса рассчитывают сумму всех значений частоты флуктуаций кожной проводимости, превышающих 0,01 пик/сек (значений интенсивности стресс-реакции) за период непрерывного мониторирования.
DIS=(IP1+IP2+IP3+…IPn),
где: DIS - показатель кумулятивного эффекта стресса, усл. ед.;
IP1…IPn - интенсивность стресс-стимулов, превышающих 0,01 пик/сек.;
В качестве интегрального показателя степени активации стресс-системы, вычисляют отношение показателя кумулятивного эффекта стресса к показателю вегетативной реактивности:
DASS=DIS/PV,
где: DASS - показатель степени активации стресс-системы, усл. ед.;
DIS - показатель кумулятивного эффекта, усл. ед.;
PV - показатель вегетативной реактивности за установленный временной интервал, пик/сек.
Для определения степени активации стресс-системы пациента разработаны оценочные шкалы интенсивности стресс-реакции (IP), вегетативной реактивности (PV), кумулятивного эффекта (DIS) и степени активации стресс-системы (DASS). Степень активации стресс-системы в вербальных характеристиках определяют по соответствующему числовому значению показателя степени активации стресс-системы (DASS).
Значение показателя степени активации стресс-системы меньше 15 усл. ед. соответствует нормальной степени активации стресс-системы, а значение показателя степени активации стресс-системы больше 15 усл. ед. отражает увеличение степени активации стресс-системы.
Для разработки шкал были обследованы 63 взрослых пациентов, из них 36 мужчин, 27 женщин, а также 101 пациент грудного возраста и новорожденные на 1 - 6 сутки после рождения. В качестве стандартизированного временного интервала, в течение которого осуществлялось непрерывное мониторирование, был взят 60-минутный период. Полученные данные показали отсутствие статистически значимых среднегрупповых отличий между минимальными, максимальными и средними значениями исследуемых показателей в зависимости от пола и возраста.
Пример 1
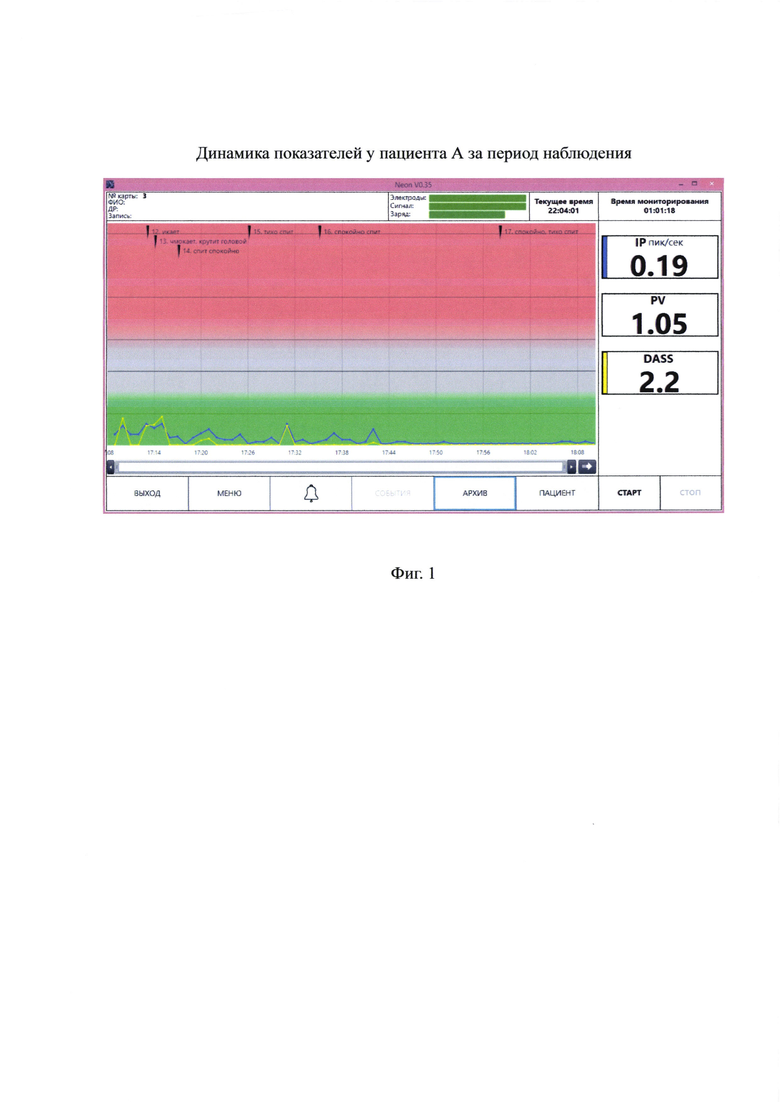
Пациент А, девочка, роды срочные оперативные на 38-39 неделе. Возраст - 3 суток, вес при рождении - 2700 г, рост - 47 см, по шкале Апгар - 8/9. Диагноз: ЗВУР II ст. На протяжении 60-минутного мониторирования проводилось непрерывное визуальное наблюдение: пациентка спала и периодически просыпалась по причине голода, после кормления снова засыпала. Абсолютные значения показателей по завершению 60-минутного периода мониторирования составили: интенсивность (IP) - 0,19 пик/сек., обобщенный показатель реактивности (PV) - 1,05 и показатель степени активации стресс-системы (DASS) - 2,2 усл. ед. На Фиг. 1 представлена динамика показателей за весь период мониторирования и значения показателей на момент отключения пациента А от устройства, реализующего заявленный способ. Как видно из представленных данных, динамика и абсолютное значение показателя степени активации стресса находились в пределах нормы.
Пример 2
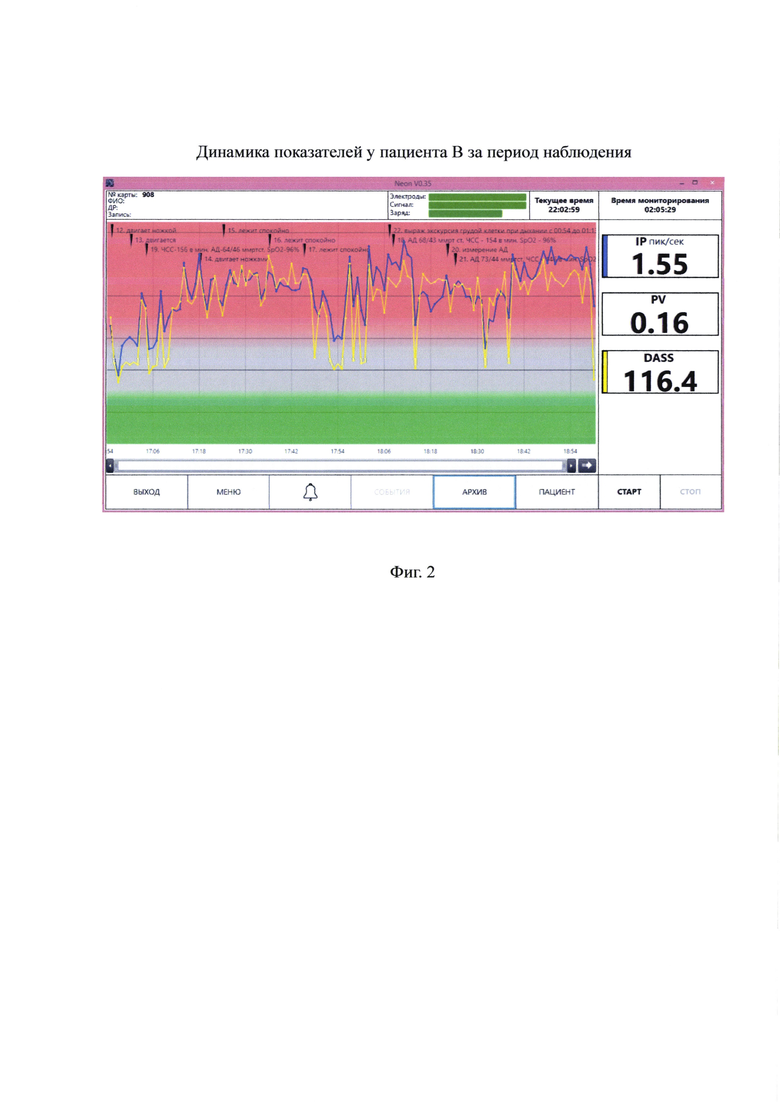
Пациент В, мальчик, возраст - 1 сутки. Роды преждевременные оперативные в головном предлежании. При рождении вес - 2040 г. рост - 44 см. По шкале Апгар - 7/8. Состояние при рождении - тяжелое. Закричал на 2'. В родильном зале проведена санация ВДП, ингаляция кислородной маской. Гемолитическая болезнь новорожденных по Rh-фактору под вопросом. Внутриутробная гипотрофия I ст. Синдром ДР 1 ст. Гипоксия при рождении. Недоношенность 32 недели. Отечный синдром. По результатам нейросонографии - 2-х сторонняя СЭК (субэпендимальная киста), перивентрикулярная ишемия II ст, повышенная резистентность мозговых сосудов, ЭХОКГ - данных за ВПС нет. ООО - 3,5 мм, ОАП - 2,7 мм с лево-правым шунтированием, сократимость несколько снижена, тахикардия. Через 30' после рождения состояние ухудшилось. Учитывая нарастание неврологической симптоматики и СДР ребенок, переведен на ИВЛ. Лечение - оксигенотерапия, АБ и инфузионная терапия. На момент мониторирования состояние очень тяжелое. ЧСС - 154 уд/мин, АД - 64/41 мм. рт. ст, SaO2 - 97%. Тяжесть состояния обусловлена проявлениями ДН II-III ст. на фоне РДС 1 ст., перинатального поражения ЦНС II-III ст гипоксически-ишемического генеза на фоне течения ГБН по Rh-конфликту у недоношенного ребенка. По данным непрерывного визуального наблюдения пациент бодрствовал на протяжении всего 60-минутного периода и не проявлял видимых проявлений стресс-реакции, т.е. лежал спокойно, не плакал, несколько раз спокойно двигал ножками, мимика была спокойной. Результаты анализа параметров кожной проводимости по завершению 60-минутного периода мониторирования выявили: интенсивность (IP) - 1,55 пик/сек., показатель реактивности (PV) - 0,16, показатель степени активации стресс-системы (DASS) - 116,4 усл. ед. На Фиг. 2 представлена динамика показателей за весь период мониторирования и значения показателей на момент отключения пациента В от устройства, реализующего заявленный способ. Как следует из полученных данных, новорожденный пациент В находился в состоянии очень высокого стрессового напряжения: очень высокие значения частоты кожной проводимости в сочетании с очень низкими значениями вариабельности привели к высокой степени (чрезмерной) активации стресс-системы.
Для качественной оценки состояния пациента на дисплее устройства, реализующего данный способ, может графически отображаться в режиме "on-line" динамика показателей, что позволяет в условиях длительного мониторирования своевременно выявлять уровень напряжения и негативную стресс-реакцию, предотвращая тем самым состояние перенапряжения и развитие повреждающего стресса у пациента.
Источники информации
1. Меерсон Ф. 3. Адаптация, стресс и профилактика. М.: Наука, 1981. 278 с.
2. Меерсон Ф.З. Пшенникова М.Г. Адаптация к стрессовым ситуациям и физическим нагрузкам. М.: Медицина, 1988. 252 с.
3. Мельникова Н.И., Дземешко Е.Ю., Строганов И.А., Воробьев В. В. Определение болевой чувствительности у новорожденных детей с хирургической патологией. Анестезиология и реаниматология, 2011, №1. с. 51-52.
4. Мороз Б.Б. Актуальные проблемы патофизиологии, 2001, 424 с.
5. Жиркова Ю.В., Степаненко СМ., Кучеров Ю.И. Послеоперационное обезболивание введением местного анестетика через раневой оросительный катетер постоянного действия у новорожденных. Анестезиология и реаниматология, 2011, №I. с. 55-58.
6. Овсянников В.Г. Патологическая физиология, типовые патологические процессы, 1987.
7. Терлякова О.Ю., Байбарина Е.Н., Ионов О.В., Антонов А.Г., 81 Балашова Е.Н., Крючко Д.С. Оценка боли у детей с очень низкой и экстремально низкой массой тела при заборе капиллярной крови и применение нефармакологических методов обезболивания. Акушерство и гинекология, 2013, №10. с. 81-85.
8. Anand К.J.S., Stevens В. J., McGrath P. J. Pain in Neonates and Infants. - 3rd Ed. Pain Research and Clinical Management, 2007.
9. Choo EK. The painful truth: A review of the clinical use of skin conductance monitoring for postoperative pain assessment. Pediatric Pain Letter, 2013, 15(3). p. 29-33.
10. Czaplik M., Hiibner С, Копу M., Kaliciak J., Kezze F., Leonhardt S., et al. Acute pain therapy in postanesthesia care unit directed by skin conductance: a randomized controlled trial. PLoS ONE, 2012, 7 41758.
11. В. Kihia, TG Stavropoulos, S. Fndreadis, N. Karvjnen, Utilizing a Wristband Sensor to Measure the Stress Level for People with Dementia, Sensors 16(12), 198.
12. Ledowski Т., Ang B, Schmarbeck T, Rhodes J. Monitoring of sympathetic tone to assess postoperative pain: skin conductance vs surgical stress index. Anesthesia 2009, 64:727-731.
13. Ledowski Т., Bromilow J., Paech J, Storm H. and Schug S. A. The assessment of postoperative pain by monitoring skin conductance: results of a prospective study, Anaesthesia, 2007, 62, p. 989-993.
14. 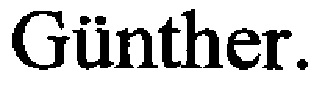 A. et al. Pain Rather Than Induced Emotions and ICU Sound Increases Skin Conductance Variability in Healthy Volunteers, Acta Anaesthesiol Scand 60 (8), 1111-1120. 9 2016
A. et al. Pain Rather Than Induced Emotions and ICU Sound Increases Skin Conductance Variability in Healthy Volunteers, Acta Anaesthesiol Scand 60 (8), 1111-1120. 9 2016
15. Savino F., Vagliano L., Ceratto S., Viviani F., Miniero R., Ricceri F. Pain assessment in children undergoing venipuncture: the Wong-Baker faces scale versus skin conductance fluctuations, Peer J, 2013, 137.
16. Storm H. The Capability of Skin Conductance to Monitor Pain Compared to Other Physiological Pain Assessment Tools in Children and Neonates, 2013.
17. Visnovcova Z, Heart Rate Variability and Electrodermal Activity as Noninvasive Indices of Sympathovagal Balance in Response to Stress, Published Online: 2013-05-14 I DOI: https://doi.org/10.2478/acm-2013-0006.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОНИТОРИНГА УРОВНЯ СТРЕССА У ПАЦИЕНТА | 2015 |
|
RU2622607C2 |
| СПОСОБ МОНИТОРИНГА СОСТОЯНИЯ ПАЦИЕНТА | 2019 |
|
RU2713942C1 |
| СПОСОБ ДИАГНОСТИКИ СТРЕССА В РАННЕМ НЕОНАТАЛЬНОМ ПЕРИОДЕ | 2022 |
|
RU2790755C1 |
| Способ оценки адекватности анестезии | 2022 |
|
RU2807285C1 |
| СПОСОБ ПСИХОТЕРАПЕВТИЧЕСКОГО ВОЗДЕЙСТВИЯ | 2006 |
|
RU2315633C1 |
| СПОСОБ МЕДИКО-ПСИХОЛОГИЧЕСКОЙ ПРОФИЛАКТИКИ СТРЕССА | 2013 |
|
RU2503412C1 |
| СПОСОБ МЕДИКО-ПСИХОЛОГИЧЕСКОЙ АДАПТАЦИИ РАБОТНИКОВ ЖЕЛЕЗНОДОРОЖНОГО ТРАНСПОРТА | 2013 |
|
RU2503402C1 |
| Способ бальнеотерапии больных остеоартритом с сопутствующей гипертонической болезнью | 2021 |
|
RU2817309C2 |
| Способ реабилитации пациентов с вибрационной болезнью | 2021 |
|
RU2773413C1 |
| СПОСОБ ОЦЕНКИ СТРЕСС-РЕАКТИВНОСТИ ОРГАНИЗМА | 2018 |
|
RU2697884C1 |
Изобретение относится к медицине, а именно к физиологии. По параметрам кожной проводимости определяют степень активации стресс-системы путем вычисления отношения показателя кумулятивного эффекта стресса к показателю вегетативной реактивности. При этом кумулятивный эффект стресса рассчитывают путем вычисления суммы всех значений интенсивности стресс-реакции, превышающих 0,01 пик/сек. Интенсивность стресс-реакции определяют усреднением значений частоты флуктуаций кожной проводимости за установленный временной интервал. Показатель вегетативной реактивности определяют по значению вариабельности частоты флуктуаций кожной проводимости путем вычисления отношения среднего квадратичного отклонения значений частоты флуктуаций кожной проводимости к среднему значению частоты флуктуаций кожной проводимости за установленный временной интервал. При значении показателя степени активации стресс-системы меньше 15 усл.ед. диагностируют нормальную степень активации стресс-системы. При значения показателя больше 15 усл.ед. - повышение степени активации стресс-системы. Способ позволяет повысить эффективность диагностики, что достигается за счет последовательности выполнения указанных выше приемов способа. 2 ил., 2 пр.
Способ определения степени активации стресс-системы у пациентов, включающий измерение параметров кожной проводимости, характеризующийся тем, что по параметрам кожной проводимости определяют степень активации стресс-системы путем вычисления отношения показателя кумулятивного эффекта стресса к показателю вегетативной реактивности,
при этом кумулятивный эффект стресса определяют путем вычисления суммы всех значений интенсивности стресс-реакции, превышающих 0,01 пик/сек,
интенсивность стресс-реакции определяют путем усреднения значений частоты флуктуаций кожной проводимости за установленный временной интервал,
а показатель вегетативной реактивности определяют по значению вариабельности частоты флуктуаций кожной проводимости путем вычисления отношения среднего квадратичного отклонения значений частоты флуктуаций кожной проводимости к среднему значению частоты флуктуаций кожной проводимости за установленный временной интервал,
причем значения показателя степени активации стресс-системы меньше 15 усл.ед. соответствуют нормальной степени активации стресс-системы, а значения показателя степени активации стресс-системы больше 15 усл.ед. отражают увеличение степени активации стресс-системы.
| US 6571124 B1, 27.05.2003 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ СТРЕССА | 2013 |
|
RU2531443C1 |
| RU 2073484 С1, 20.02.1997 | |||
| US 2013079602 A1, 28.03.2013 | |||
| КОВАЛЕВ В.В | |||
| Стрессовое состояние человека и реакция мозга на стресс | |||
| Развитие профессионализма | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Схема обмотки ротора для пуска в ход индукционного двигателя без помощи реостата, с применением принципа противосоединения обмоток при трогании двигателя с места | 1922 |
|
SU122A1 |
| ЖИРКОВА Ю.В | |||
| и др | |||
| Мониторинг кожной проводимости и интенсивной терапии | |||
| Анестезиология и реаниматология | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| HARRISON D | |||
| et al | |||
| Skin conductance as a measure of pain and stress in hospitalised infants | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Машина для разделения сыпучих материалов и размещения их в приемники | 0 |
|
SU82A1 |
Авторы
Даты
2018-10-02—Публикация
2017-12-25—Подача