Изобретение относится к медицине, в частности к анестезиологии, реаниматологии, интенсивной терапии и реабилитологии и может быть использовано при мониторинге адекватности анальгезии.
Термин «анестезия» используют для определения состояния, искусственно вызванного фармакологическими средствами, характеризующегося отсутствием боли с одновременной потерей или сохранением других видов чувствительности у больного, подвергающегося лечению. Если потеря чувствительности у больного достигается путем влияния средств общего действия на ЦНС, ее определяют терминами «общая анестезия» или «наркоз». При местном устранении болевых стимулов и болевой чувствительности с помощью местных анестетиков, действующих на те или иные структуры периферической нервной системы, состояние определяют термином «местная анестезия».
Международная ассоциация по изучению боли (IASP) определяет боль как "неприятное сенсорное и эмоциональное переживание, связанное с фактическим или потенциальным повреждением тканей или описываемое в терминах такого повреждения". Ноцицепция, в отличие от перцепции (восприятия) боли, является не субъективным ощущением, а физиологическим кодированием и обработкой болевых стимулов.
Мониторинг ноцицепции остается проблемой при попытках снизить частоту возникновения острой послеоперационной боли и перейти к более автоматизированному подходу к обезболиванию и анестезии (Ledowski T., 2019). Вместе с тем анестезия и интенсивная терапия являются областями, подверженными человеческим ошибкам (Schulz C.M. et al., 2017). Визуальное внимание, как основной процесс ситуационной осведомленности у анестезиологов, направлено на монитор пациента, что предъявляет требования к качеству отображения информации на экране монитора и ее информативности. Дизайн когнитивной эргономики мониторинга пациента может уменьшить ошибки человеческого фактора в условиях высокой нагрузки в критических ситуациях анестезии. В этой связи визуализация мониторинга в режиме реального времени при кратковременном или долговременном воздействии стрессирующих факторов у анестезированных хирургических и терапевтических пациентов представляется особенно актуальной (Roche T.R. et al., 2022). Хороший когнитивно-эргономичный дизайн устройств мониторинга улучшает осведомленность анестезиолога о ситуации и значительно снижает ошибки человеческого фактора в условиях высокого стресса (Andrade E. et al. 2020). Необходимость непрерывного мониторинга пациента отражает динамическую природу боли, возбуждения и седации, которые постоянно меняются в процессе лечения. Кроме того, клинический мониторинг способствует динамическому контролю ответа пациента на терапию, что облегчает принятие врачебного решения для устранения боли и возбуждения, что предотвращает чрезмерную седацию.
С позиции теории функциональных систем П.К.Анохина ЦНС и ВНС находятся на высшей ступени генетической управляющей системы, которые посредством взаимодействия с нижележащими управляющими системами: эндокринной управляющей системой, системой управления автоматизмом жизненно важных органов, генетической управляющей системой клетки и метаболической управляющей системой регулирует и координирует деятельность организма на интегративном уровне. При этом более старшие по рангу системы задают настройку более младшим (Анохин П.К., 1975, Судаков К.В., 2011, 2012).
Основу диагностики состояния ВНС составляют исследования ее тонуса, реактивности и вегетативной деятельности. Текущий тонус отражает уровень напряжения функциональных систем и висцеральных органов в конкретный момент жизнедеятельности организма в зависимости от интенсивности воздействия внешних и внутренних стрессоров. Реактивность, являясь динамической характеристикой процессов интегративной системы вегетативных функций, отражает ответную реакцию организма на воздействие внешних и внутренних раздражителей и определяет скорость реакции на внешние и/или внутренние раздражители. Вегетативное обеспечение деятельности - способность к поддержанию реактивности на должном уровне в соответствии с текущей потребностью организма. При исследовании вегетативной реактивности необходимо учитывать "закон исходного уровня", согласно которому чем выше исходный уровень, тем в более деятельном и напряженном состоянии находится система или орган, тем меньший ответ возможен при действии возмущающих стимулов. В целом, вегетативный тонус и реактивность дают возможность составить представление о степени напряжения адаптационных механизмов в условиях текущей ситуации. Паттерны активации ВНС отличаются у людей, отражая тип вегетативной регуляции и использование физиологических измерений для регистрации индивидуальных вариаций вегетативного обеспечения деятельности имеет решающее значение для эффективного лечения (Berntson G.G. et al., 1991; Berntson G.G., Cacioppo J.T., 2004; Giuliano R.J., Karns C.M. et al., 2017).
В условиях действия внешних или внутренних факторов стресса, ВНС контролирует функционирование организма посредством реципрокного взаимодействия двух ее отделов: симпатической нервной системы - стресс-реализующей (СНС) и парасимпатической нервной системы - стресс-лимитирующей (ПСНС). Одной из адаптивных особенностей реципрокных режимов управления является доминирование одного из двух отделов ВНС (Cohen & Randall 1984; Weise, Heydenreich, Runge, 1987; Berntson et al., 1991), и, в случае реципрокного режима контроля, достаточно количественной оценки влияния доминирующего отдела ВНС, поскольку реципрокные изменения в другом подразделении будут очевидными (Berntson and Cacioppo, 1991, 1999).
Ключевая роль, которую играет симпатическая нервная система в интеграции физиологических процессов, была отражена в работах Валин и Чаркоудиан, они писали: "В эпоху, когда важность интегративной системной физиологии вновь становится в центре внимания биомедицинской науки, симпатическая нервная система может рассматриваться как окончательный интегратор системной физиологии...". (Wallin B.G., Charkoudian N., 2007). Со времени первых записей активности симпатического нерва стало очевидно, что активность СНС организована в виде колебаний, и эти колебания довольно сложны и зависят от физиологического состояния субъекта и ситуации. Для определения колебательных характеристик СНС используется метод спектрального анализа мощности, основанный на быстром преобразовании Фурье, так как было показано преимущество анализа в частотной области по сравнению с анализом во временной области для точной количественной оценки сигнала с несколькими частотными компонентами. Наряду с этим анализ в частотной области точно отражает "общий объем активности" в различных частотных диапазонах (Miller W.L., Sigvardt K.A., 1998; Barman S.M. and Yate В.J. 2017).
Известно, что боль и возбуждение усиливают симпатическую реакцию на стресс, потенциально приводя к негативным острым и долгосрочным последствиям. Вместе с тем передозировка анальгетиками и седативными препараторами часто связана с худшими клиническими исходами, включая более длительное пребывание на искусственной вентиляции легких, длительное пребывание в отделении интенсивной терапии и усиление мозговой дисфункции (делирий и кома). Чтобы оптимизировать уход за пациентами, безопасность и комфорт при минимизации негативных последствий, связанных с фармакотерапией, медицинские работники должны достичь правильного баланса между назначением обезболивающих и седативных препаратов.
Для определения симпатического возбуждения широко применяется электродермальная активность (ЭДА/кожная проводимость). Существует доказательства иннервации потовых желез исключительно симпатическим отделом ВНС (Tower и Richter, 1932). ЭДА является единственной физиологической переменной, не подверженной влиянию парасимпатического отдела ВНС, так потовые железы эккринной системы получают только возбуждающие симпатические нервные импульсы (Fowles, 1986; Boucsein W., 2012; Freeman R. and Chapleau M. W., 2013). ЭДА зависит от количества пота, выделяемого потовыми железами в подкожной клетчатке пальцев, ладонной и подошвенной областей. Терморегуляторные процессы в этих зонах оказывают минимальное влияние на потоотделение (Richter, C. P.,1927; Groscurth P., 2002). Комплекс ЭДА включает в себя две составляющие: уровень проводимости кожи (SCL), который характеризует медленно изменяющуюся в пределах нескольких минут компоненту и фазический отклик кожной проводимости (SCR), которая характеризует быстро меняющуюся компоненту ЭДА.
ЭДА, являясь признанным количественным функциональным маркером судомоторной активности, позволяет дать объективную оценку симпатической функции на интегративном уровне. (Healey J.A. et al., 2005; Benedek M., Kaernbach С., 2010; Ellaway P.H. et al., 2010; Setz C. et al.,2010) и, как периферическая мера активности симпатической нервной системы, нашла широкое применение в практике (Cacioppo J.T. et al., 2007; Boucsein W. et al., 2012). В отличие от этого количественного аспекта, качественная сторона, такая как его валентность (положительный / отрицательный) или какой стресс-фактор присутствует (физический или психоэмоциональный) не отражены в ЭДА и должны быть выведены из других возможных причин.
ЭДА используется в качестве объективного показателя при различных стрессовых состояниях, в том числе таких, как боль, эмоции, депрессия, беспокойство и т.д. (McEwen B.S., 2007; Mobascher A. et al, 2009; Lovallo W.R., 2011; Sano A. and Picard R.W., 2013; Doberenz S. et al., 2011; Hernandez J., 2011; Mestanik M. et al., 2014; Nickel M.M. et al., 2017; Geuter S. et al., 2017; Posada-Quintero H.F. et al., 2018; Aslanidis T. et al. 2018).
Существует большое количество методов оценки интенсивности боли, основанных на оценочных шкалах наблюдателя и самоотчета (Sessler C.N. et al, 2008) Поскольку боль является субъективным восприятием, самооценка остается золотым стандартом для пациентов с сознанием, точным пониманием и вербальным выражением, включая визуально аналоговую шкалу (VAS), числовую шкалу оценки (NRS), вербальную шкалу оценки (VRS) и шкалу оценки боли в лице, хотя стандартный метод все еще является предметом дискуссий. Показано, что высокая дисперсия и несогласованность показателей VAS приводят к снижению эффективности классификации болевых ощущений, при этом три уровня боли (нет, низкий и высокий) могут быть количественно определены с хорошей точностью и физиологическими доказательствами того, что симпатические реакции, регистрируемые ЭДА, в большей степени коррелируют с интенсивностью применяемых стимулов, чем с ощущением боли, о котором сообщает субъект (Posada-Quintero H.F. et al., 2021).
Клинический мониторинг адекватности анестезии включает ряд физиологических параметров, используемых для измерения адекватности анестезии и определения выбора анестетика и титрования дозы. Используются показатели артериального давления, частоты сердечных сокращений, изменения характера дыхания, соматической и скелетной двигательной активности, потоотделения, слезотечения, диаметра зрачка и вазомоторных кожных рефлексов (Guinard B., 2006). Однако, в зависимости от клинического состояния пациента и используемых лекарств, эти параметры могут плохо отражаться при оценке адекватности анестезии (Nunes R.R., 2003). Наличие движения в ответ на болевые раздражители было одним из методов оценки эффективности анестезирующих средств. Хотя двигательная реакция опосредуется спинальными рефлексами, ее наличие является важным признаком неадекватной анестезии, что делает пациента восприимчивым к риску интраоперационного пробуждения и осознания ((Nunes R.R., 2015).
Как правило, изменения частоты сердечных сокращений и артериального давления используются в качестве признаков усиления ноцицепции во время седации, но их специфичность и чувствительность не очень высоки (Luginbuhl M. et al., 2007). Для клинической пользы объективный показатель ноцицепции должен быть надежным, постоянно чувствительным к обезболивающим вмешательствам и простым в использовании в различных клинических ситуациях. Хотя объективный подход к ноцицепции может быть возможен, оценка и последующее лечение боли остаются субъективными и часто неоптимальными, даже при использовании определенных протоколов и рекомендаций (Fallon M. et al, 2018).
С целью повышения объективности оценки течения анестезии за последние годы было разработано много методов оценки боли, возбуждения - седации, и возможности мониторинга значительно возросли. Вместе с тем стандарты мониторинга пока еще недостаточно разработаны. В частности, многие предложенные способы мониторинга адекватности анестезии, многообещающие вначале, позже не подтвердили свою надежность, что в свою очередь диктует необходимость их дальнейшего совершенствования (Zhaosheng Jin et al., 2019; Довбыш Н.Ю., с соавт., 2020). Кроме того, широко используемые для оценки состояния ВНС физиологические показатели, отражают частные механизмы вегетативной регуляции. При этом в комплексных исследованиях показано, что оценка функционального состояния организма по показателям отдельных методов исследования является неоднозначной, так как вегетативный тонус в различных функциональных системах может быть различным (Вейн А.М. и сотр., 2000). В этой связи, поскольку активность потовых желез контролируется только симпатическими нервами, измерение ЭДА считается идеальным способом мониторинга активности вегетативной регуляции на уровне целостного организма.
На основании передовых методов функциональной магнитно-резонансной томографии, нейровизуализации, ЭЭГ и машинного обучения была подтверждена правомерность и эффективность применения фазической составляющей кожной проводимости с целью мониторинга баланса ноцицепция/антиноцицепция. Результаты показали, что параметры кожной проводимости зависимы от активности мозга, связанной с интенсивностью стимула (альфа- и бета-ритмы сенсомоторной области) и с интенсивностью боли (гамма-ритмы медиальной префронтальной коры) (Gross J. et al., 2007; Zhang Z.G. et al., 2012; Tiemann L. et al., 2015: Tiemann L. et al., 2018; Lee I.S. et al., 2020; Posada-Quintero, et al., 2021). Эти исследования подтвердили концепцию боли, в которой сенсорные, мотивационные и автономные процессы частично самостоятельно вносят вклад в окончательную оценку боли (Nickel М.М. et al., 2017; Posada-Quintero, et al., 2021). Утверждается, что ноцицепция постоянно происходит в отсутствие восприятия боли, и это фундаментальный физиологический процесс (Baliki M.N. et al., 2015). Одновременно с этим было отмечено, что изменчивость ЭДА, связанная с возбуждением симпатической нервной системы, представляет собой важный индивидуальный фактор (Fenning R.M. et al., 2010). Существенных взаимосвязей между вариабельностью сердечного ритма (ВСР) и интенсивностью стимулов или интенсивностью боли обнаружено не было (Mobascher A. et al, 2009; Nickel M.M. et al.,2017). Несомненно, сердечно - сосудистая система играет ведущую роль в обеспечении адекватной адаптации организма. Однако оценка функционального состояния всего организма на основе показателей какой - либо одной анатомо - физиологической системы вряд ли может быть исчерпывающей. Если исследуются только показатели сердечно - сосудистой системы, можно судить не об общем тонусе вегетативной нервной системы, а о вегетативном тонусе в сердечно - сосудистой системе (Вейн А.М., 1981).
Из уровня техники известны различные способы определения уровня ноцицепции/боли, возбуждения - седации и стресса, исходными данными для исследования которых служили записи множества физиологических сигналов и анализ переменных, полученных с помощью электроэнцефалографии (ЭЭГ), электромиограмиографии лица (ЭМГ), электрокардиографии и импедансной кардиографии для расчета частоты сердечных сокращений (ЧСС) и вариабельности сердечного ритма (ВСР), артериального давления (АД), слуховых вызванных потенциалов (СВП), электроокулографии (ЭОГ) и электродермальной активности (ЭДА/КГР/кожная проводимость) (RU2712850 опубл. 31.01.2020; US20150374285 опубл. 31.12.2015; US8914102 опубл. 16.12.2014; WO2017012622 опубл. 26.01.2017; WO2002032305 опубл.24.05.2002; US20020117176 опубл. 29.08.2002; US20060217615 опубл. 24.03.2005; US9498138 опубл. 22.11.2016; EP3232917 опубл. 18.09.2018; US20050143665 опубл. 03.10.2002; US7215994 опубл. 08.05.2007; US8512240 опубл. 20.08.2013; KR20130016708, опубл. 18.02.2013; US2015018707 опубл.15.01.2015; US6571124 опубл.27.05.2003; WO2016095918 опубл. 23.06.2016; WO2014199093 опубл. 18.12.2014; RU2622607 опубл. 16.06.2017; RU2668698 опубл. 02.10.2018; RU2718544 опубл. 08.04.2020; RU2713942 опубл. 11.02.2020).
Однако известные способы не могут обеспечить надежную оценку состояния пациента, поскольку полученные данные не являются результатом всестороннего анализа показателей, отражающих проявления боли и возбуждения у пациента, а также не имеют визуального способа представления данных в реальном режиме времени непрерывного мониторинга, что снижает эффективность управления анестезией с учетом индивидуальных особенностей пациента
Наиболее близким к заявляемому способу является способ мониторинга состояния пациента, включающий регистрацию и временной анализ фазической компоненты ЭДА, отражающей симпатическое возбуждение, при этом определяют вариабельность параметров фазической ЭДА и осуществляют оценку состояния пациента по обобщенному показателю путем вычисления частного от деления суммы значений показателя частоты колебаний, коэффициента осцилляции, коэффициента вариации и индекса ритма фазической ЭДА на количество слагаемых параметров. Дополнительно оценивают сочетание значений частоты колебаний фазической ЭДА и индекса ритма фазической ЭДА и оценивают состояние пациента по обобщенному показателю по 7-балльной шкале (RU2713942 опубл.11.02.2020). Однако данный способ не обеспечивает визуальный контроль соответствия адекватности анальгезии и седации потребности пациента при хирургический агрессии, интенсивной терапии.
Известен способ визуального отображения и оценки адекватности анальгезии и седации у пациента (RU2718544 опубл.08.04.2020), предназначенный для комплексной оценки и визуализации на мнемосхеме текущего состояния пациента во время седации и общей анестезии, включающий анализ сигналов электроэнцефалограммы, электрокардиограммы, содержания кислорода в крови, уровня анестезии по ограниченному числу параметров. Основным существенным недостатком этого известного способа является то, что способ рассматривает только периодическую оценку и визуализацию на мнемосхеме текущего состояния пациента во время седации и общей анестезии, что недостаточно, так как не учитывает динамическую природу боли и седации, которые постоянно меняются в процессе периоперационного периода.
Задачей изобретения является разработка способа визуализации состояния пациента в реальном режиме времени для контроля адекватности анестезии с учетом потребности пациента при хирургических вмешательствах, интенсивной терапии, при проведении лечебных и диагностических мероприятий, а также на этапах медицинской реабилитации для поддержки принятия клинического решения в целях повышения качества и безопасности анестезиологической помощи за счет снижения рабочей врачебной нагрузки, лишенного недостатков вышеуказанных аналогов, а также расширение арсенала средств указанного назначения.
Технический результат изобретения заключается в облегчении и ускорении процесса принятия врачебного решения для устранения боли и возбуждения пациента, тем самым предотвращая чрезмерную или недостаточную анестезию за счет достижения правильного баланса между назначением обезболивающих и седативных препаратов.
Технический результат достигается тем, что способ визуализации состояния пациента для контроля адекватности анестезии включает регистрацию кожной проводимости, определение частоты флуктуаций фазической компоненты кожной проводимости по 5-секундным эпохам за установленный интервал времени, расчет вариабельности частоты флуктуаций фазической компоненты кожной проводимости, определение по частоте флуктуаций фазической компоненты кожной проводимости индекса симпатического доминирования, отражающего текущий симпатический тонус в качестве показателя анальгезии, определение по вариабельности частоты флуктуаций фазической компоненты кожной проводимости индекса симпатической реактивности, отражающего возбуждение-седацию, и графическое отображение в режиме реального времени значений индекса симпатического доминирования и индекса симпатической реактивности в виде точечной проекции данных на плоскости квадрантов диаграммы рассеяния, оси которых центрированы относительно пороговых значений индексов, при этом каждая пара анализируемых параметров отображаться на графике одной точкой.
Визуальный контроль адекватности анальгезии и седации индивидуальной потребности пациента осуществляется в режиме реального времени с помощью графического отображения числовых значений индексов симпатического доминирования и симпатической реактивности в виде точечной проекции данных на плоскости диаграммы рассеяния в координатной плоскости, разделенной на 4 квадранта, оси которых центрированы относительно пороговых значений симпатического доминирования, характеризующего интенсивность действия болевых стимулов и симпатической реактивности, отражающей восприятие пациентом стрессирующих стимулов. Расположение точек по квадрантам определяет соответствие анальгезии и седации индивидуальной текущей потребности пациента. Каждая пара числовых значений индексов симпатического доминирования и симпатической реактивности отображается в одной точке на графике, что обеспечивает визуальную связь показателей и является объективным способом анализа динамической системы - клинического мониторинга с непрерывным режимом реального времени.
В предложенном способе визуальной оценки адекватности анестезии непрерывно регистрируют и рассчитывают в пределах установленного 1-минутного интервала частоту колебаний фазической компоненты кожной проводимости и по параметрам фазической кожной проводимости вычисляют и отображают на диаграмме рассеяния показатели, характеризующие соответствие анальгезии и седации индивидуальной потребности анестезированного пациента.
Непрерывно в режиме реального времени в течение всего периода мониторирования регистрируют и автоматически усредняют частоту колебаний фазической компоненты кожной проводимости, рассчитывают индекс симпатического доминирования и индекс симпатической реактивности, при этом индекс симпатического доминирования характеризует анальгезию, а индекс реактивности характеризуют возбуждение-седацию. Полученные значения индексов отображаются на плоскости квадрантов двумерной диаграммы рассеяния путем их совмещения и по проекции точек визуально оценивают адекватность анальгезии и седации текущей потребности пациента в динамике.
Непрерывно в режиме реального времени в течение всего периода мониторирования регистрируют кожную проводимость, автоматически усредняют частоту колебаний фазической компоненты кожной проводимости. Запись делят на 5-секундные отрезки (эпохи). В каждой эпохе отдельно подсчитывают число пиков за эпоху, затем переводят в пики в секунду (делением на длительность эпохи), после чего число пиков/секунду за эпоху усредняется за 12 эпох (минуту).
Для расчет индексов используются следующие формулы:
Частоту колебаний фазической компоненты кожной проводимости вычисляют как:
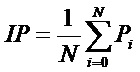
где:
IP - усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости;
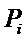 - пик/секунду за i-ю эпоху (кол-во пиков за эпоху, деленное на длительность эпохи в секундах);
- пик/секунду за i-ю эпоху (кол-во пиков за эпоху, деленное на длительность эпохи в секундах);
N - количество эпох за минуту, N=12.
В качестве индекса вегетативной реактивности вычисляют вариабельность частоты колебаний фазической компоненты кожной проводимости:
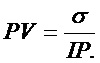
где:
PV - вариабельность фазической компоненты кожной проводимости;
σ - среднеквадратичное отклонение;
IP - усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости.
В качестве индекса симпатической реактивности вычисляем обратную величину
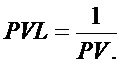
где:
PVL - индекс симпатической реактивности.
В качестве индекса симпатического доминирования рассчитывают натуральный логарифм обратного среднего значения колебаний фазической компоненты кожной проводимости за установленный интервал времени:
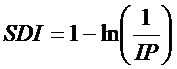
где:
SDI - индекс симпатического доминирования;
IP - усредненное за 1-минутный интервал значение спектральной мощности кожной проводимости;
ln - натуральный логарифм.
Оценку соответствия анальгезии и седации индивидуальной потребности пациента осуществляют в режиме реального времени с помощью графического отображения на мониторе числовых значений индекса симпатического доминирования (SDI) и индекса реактивности (PVL) в виде точечной проекции данных на декартовой координатной плоскости, при этом декартову плоскость разделяют на 4 квадранта, оси которых центрируют относительно пороговых значений симпатического доминирования, характеризующего анальгезию и индекса реактивности, характеризующего восприятие - седацию. Пороговое значения индексов SDI и PVL определяют по оценочным шкалам, разработанным с учетом циклов сна и бодрствования, нозологической формы заболевания, возрастной группы пациентов и анестезиологического пособия.
Построение диаграммы рассеяния осуществляют следующим образом: две взаимно перпендикулярные координатные оси наносятся на плоскость с общим началом в точке их пересечения и одинаковой масштабной единицей, образуя декартову прямоугольную систему координат на плоскости. Квадрант - это одна из четырех зон на декартовой плоскости, каждый квадрант имеет комбинацию положительных и отрицательных значений для абсциссы (x) и для ординаты (y), при этом значения индекса симпатической реактивности всегда наносятся по абсциссе, а значения индекса симпатического доминирования по ординате. Прямолинейные оси квадрантов ограничивают расположение точек в пространстве в зависимости от положительных или отрицательных знаков координат по отношению к точке пересечения пороговых значений индексов SDI и PVL, являющейся началом координат для каждого из 4 квадрантов.
В заявленном способе визуальной оценки адекватности анестезии построение диаграммы рассеяния осуществляют следующим образом: при построении прямолинейных и круговой координат предпочтительной масштабной единицей являются целые числа, определяющие границы диапазонов уровней (коридоров), полученных путем разработки оценочных шкал числовых значений индексов SDI и PVL, соответственно отрицательным и положительным значениям по отношению к началу координат, т.е. точке пересечения пороговых значений. Круговая масштабная шкала ограничивает диапазон средних значений. Качественную оценку величин индексов, соответственно диапазонам разброса точек, осуществляют соответственно следующим статистическим уровням индексов: предельно низкий (<-4), очень низкий (-4), низкий (-3), пониженный (- 2), пороговый (0±1), повышенный (+2), высокий (+3), очень высокий (+4) и чрезмерно высокий (>+4).
В качестве стандартизированного временного интервала, в пределах которого производится усреднение числовых значений индексов SDI и PVL, остающегося неизменным в процессе всего периода мониторирования, предпочтительным является 1-минутный интервал. В случаях относительно устойчивых состояний могут быть использованы также и другие временные интервалы, выбор которых зависит от поставленных медицинских задач и клинической ситуации. Для каждого установленного временного периода необходима разработка специальных шкал.
Динамический визуальный анализ соответствия анальгезии и седации текущей потребности пациента в периоперационном периоде при общей, местной анестезии и интенсивной терапии с помощью графического отображения сводится к нижеследующему:
Нижний левый квадрант (I).
При общей анестезии расположение точек в пространстве визуализируется на плоскости левого нижнего квадранта, т.е. значения индексов SDI и PVL ниже пороговых значений. Этот тип течения анестезии указывает на отсутствие как ноцицептивных стимулов, так и отсутствие восприятия каких-либо внешних раздражителей. Данный тип течения анестезии специфичен для общей анестезии и указывает на соответствие анальгезии и седации текущей потребности пациента.
Нижний правый квадрант (II).
При общей анестезии расположение точек в пространстве визуализируется на плоскости правого нижнего квадранта, т.е. значения индекса SDI ниже порогового уровня, а значения PVL выше пороговых значений. В интраоперационном периоде этот тип течения анестезии свидетельствует об отсутствии ноцицептивных стимулов, при этом повышение индекса PVL указывает на вероятность интранаркозного пробуждения. Значения индексов SDI и PVL до операции и после пробуждения, как правило, располагаются в правом верхнем квадранте.
Верхний правый квадрант (III).
При местной анестезии расположение точек в пространстве визуализируется на плоскости левого нижнего и правого верхнего квадрантов, т.е значения индексов SDI и PVL могут быть как ниже, так и выше пороговых значений. Этот вариант течения анестезии является характерным для местной анестезии и визуализация расположения точек позволяет непрерывно контролировать соответствие анальгезии и седации индивидуальной потребности пациента.
Верхний левый квадрант (IY).
Этот вариант расположения точек в пространстве, визуализируемый на плоскости левого верхнего квадранта, отличается сочетанием числовых значений индекса SDI выше порогового уровня со значениями индекса PVL ниже порогового, является негативным как у пациентов в сознании, так и в бессознательном состоянии. В случаях одиночных выбросов значений индекса SDI в эту зону, может свидетельствовать о болевых стимулах у пациентов в бессознательном состоянии. У пациентов в сознании, при наличии нескольких точек со значениями SDI выше+3 может указывать на тенденцию к перенапряжению адаптационных возможностей организма. Самым неблагоприятным вариантом, свидетельствующем о состоянии дистресса, является сочетание значений SDI выше+4 при PVL ниже -4.
В целом способ визуального контроля адекватности анестезии и интенсивной терапии с учетом индивидуальной потребности пациента по расположению точек в пространстве квадрантов диаграммы рассеяния, сводится к следующему: левый нижний - анестезия, анальгезия, седация; правый нижний - сон, покой, зона комфорта; правый верхний - активное бодрствование, сочетанный физический и эмоциональный стресс; верхний левый - боль, стресс.(Фиг. 1)
Предложенный способ визуализации состояния пациента для контроля адекватности анестезии и интенсивной терапии реализован в приборе для мониторинга состояния пациента с помощью разработанного специального программного обеспечения. Отображение в режиме реального времени значений индекса симпатического доминирования и индекса симпатической реактивности в виде точечной проекции данных на плоскости квадрантов диаграммы рассеяния осуществляется на мониторе.
Осуществление изобретения поясняется приведенными ниже примерами:
Пример 1. Больной П., 66 лет.Искривление носовой перегородки. Вазомоторный ринит.Септопластика в условиях общей анестезии. План анестезии: севоран, индукция фентанил 0,2+0,2 мг, пропофол 250 мг, эсмерон 50 мг, преднизолон 2 мг/кг.Мониторинг проведен в периоперационном периоде, продолжительность операции 1 ч 35 мин. До операции распределение точек на плоскости III квадранта (верхний правый) совпадало по времени с проведением интубации, при этом значения индекса SDI находились в диапазоне от+1 до+2, т.е. на уровне повышенных значений, при этом индекс PVL находился в границах от+2 до+3, т.е. на уровне повышенных и высоких значений. К началу операции уровень индексов SDI и PVL были ниже пороговых значений. В процессе хирургического вмешательства было отмечено 5 случаев фазического отклика кожной проводимости на плоскости I квадранта (нижний левый), все остальное время операция была проведена при базальном уровне кожной проводимости, т.е. при нулевых значениях фазического отклика, что указывало на отсутствие как болевых стимулов, так и вероятности интранаркозного пробуждения. Мониторинг был завершен до восстановления адекватного спонтанного дыхания, сознания и до экстубации. Следовательно, визуальный контроль подтвердил адекватность общей анестезии с учетом индивидуальной потребности пациента по течению всего периоперационного периода. (Фиг. 2)
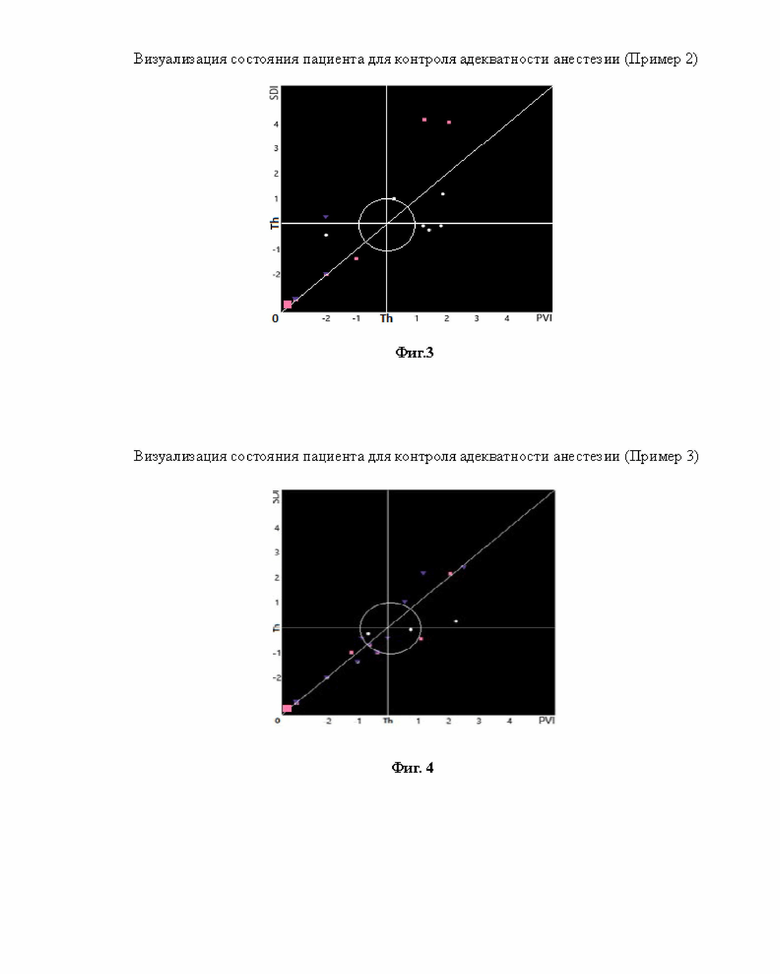
Пример 2. Больная С., 47 лет.Деформация наружного носа. Ринопластика в условиях общей анестезии. Анестезия - севофлуран, пропофол 250 мг, фентанил 0,2+0,1+0,1+0,1 мг, эсмерон 50 мг, кетопрофен 100 мг.Мониторинг проведен в периоперационном периоде, продолжительность операции 2 часа 18 мин. До операции величины индексов SDI и PVL были в пределах порогового и ниже порогового уровня. В интраоперационном периоде соотношение индексов SDI и PVL соответствовало I квадранту (нижний левый), т.е. ниже пороговых значений за исключением 2 точек на плоскости III квадранта (верхний правый), что совпало по времени с фиксацией лоскута в области 2 ветви тройничного нерва, при этом величина индекса SDI соответствовала+4, т.е. на уровне очень высоких значений, при этом индекс PVL находился в пределах от+1 до+2, т.е. на повышенном уровне, что указало на действие ноцицептивных стимулов на протяжении двух минут операции. Данное событие совпало по времени с наиболее травматичным этапом операции - фиксацией лоскута в области тройничного нерва. В дальнейшем, как в интраоперационном периоде, так при пробуждении пациента все точки находились в I квадранте. Таким образом, визуальный контроль подтвердил соответствие анестезии индивидуальной потребности пациента, за исключением этапа фиксации лоскута в области тройничного нерва. (Фиг. 3)
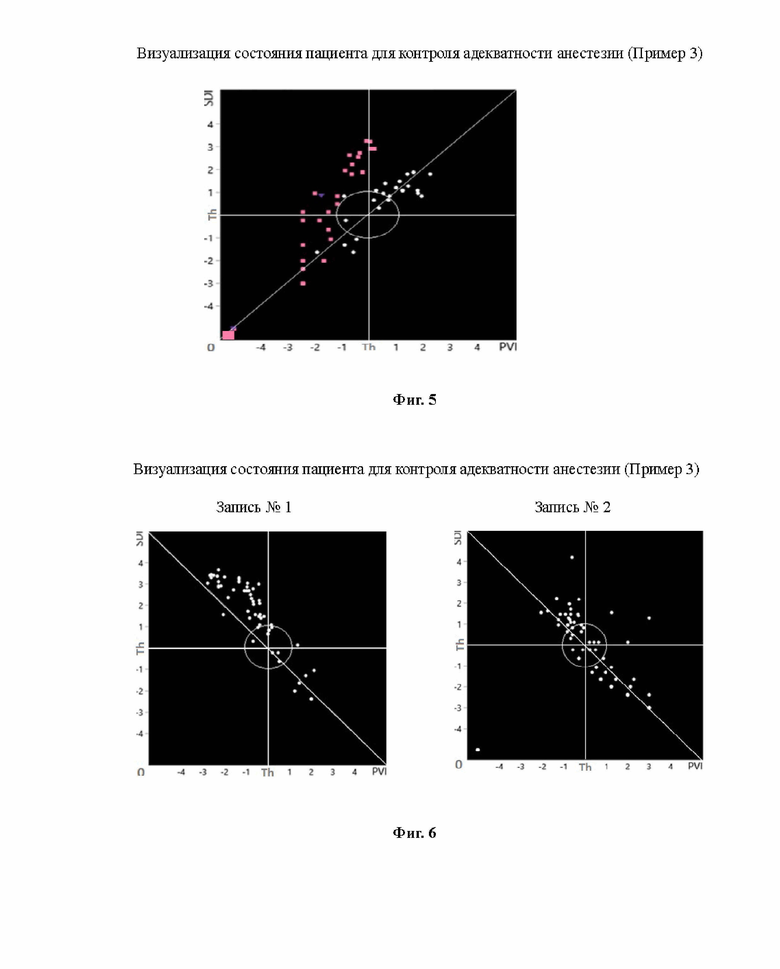
Пример 3. Больная П., 57 лет.Киста яичника. Аднексэктомия. Эндоскопическая операция в условиях общей анестезии. Анестезия - пропофол 150 мг, фентанил 100 мкг, эсмерон 50 мг, севофлуран 1 МАС, поток 0,7 л, FiO2 0,5, преднизолон 60 мг в/в. Мониторинг проведен в периоперационном периоде, продолжительность операции 21 мин. В предоперационном периоде отмечено 3 случая фазического отклика кожной проводимости. Величина индекса SDI находилась в диапазоне от -1 до+1, т.е в пределах пороговых значений и индекс PVL соответствовал диапазону значений от -1 до+2, т.е. на уровне пороговых - выше пороговых значений. В начале операции появление точки на плоскости II квадранта (правый нижний) совпало по времени с введением эндоскопа, что указывало на дискомфорт при отсутствии ноцицептивных стимулов. В процессе хирургического вмешательства был выявлен 1 случай фазического отклика с проекцией точки на плоскость III квадранта (верхнего правого), при этом величины индексов SDI и PVL соответствовали+2 как в одном, та и в другом случае, т.е. находились на повышенном уровне. Повышение величин SDI и PVL было связано с наложением пневмоперитонеума. В дальнейшем, вплоть до окончания операции анестезия была адекватна потребности пациента при общей анестезии. По окончанию интраоперазионного периода наблюдался процесс постепенного пробуждения, на что указывало повышение соотношения SDI и PVL до повышенного и высокого уровня, т.е. в диапазоне величин. от+2 до+3. Таким образом, визуальный контроль зафиксировал эпизод повышения симпатического возбуждения при введении эндоскопа и наложении пневмоперитонеума. В целом было подтверждена адекватность общей анестезии индивидуальной потребности пациента в течение остального периоперационного периода. (Фиг. 4)
Пример 4. Пациент Н., 60 лет. Деформирующий коксартроз. Эндопротезирование тазобедренного сустава. В условиях местной анестезии: лидокаин 80 мг., ропивакаин 20 мг, атропин, реланиум 5 мг.Мониторинг проведен в периоперационном периоде, продолжительность операции 2 ч.20 мин. До операции расположение точек в пространстве визуализировалось на плоскости III квадранта (правый верхний). Величины индексов SDI и PVL находились в диапазоне от+1 до+2, т.е в пределах пороговых и повышенных значений, что указывало на средне выраженный эмоциональный стресс.После постановки эпидурального катетера и проведения спинальной анестезии на протяжении 25 минут до начала операции пациент находился в состоянии сна. В интраоперационном периоде, начиная с 27 минуты мониторинга, были выявлены 3 эпизода смещения точек на плоскость IY квадранта, индекс SDI увеличивался от+1 до+3, т.е от выше пороговых до высоких, при этом величина индекса PVL находился в предела от -1 до -2, т.е. на уровне пониженных и низких значений, что указывало на действие ноцицептивных стимулов. Жалоб от пациента на восприятие боли не было. В дальнейшем, вплоть до окончания операции анестезия была адекватна потребности пациента, что подтверждалось рассеянием точек на плоскости I квадранта. (Фиг. 5)
Пример 5. Больная А., 2 мес.Двухсторонняя бронхопневмония. Бронхолегочная дисплазия. Ребенок в тяжелом состоянии находился в отделении реанимации и интенсивной терапии (ОРИТ). Тяжесть состояния обусловлена дыхательной недостаточностью, микроциркуляторными и метаболическими нарушениями. На ИВЛ, в кювезе. Терапия - медикаментозная седация Дормикум 0,5% -1,0 кап., антибактериальная и инфузионная терапия. Беспокоен, беззвучно плачет, сильный тремор. Мониторинг проводился дважды, первичный мониторинг продолжался 60 минут, продолжительность повторного - 120 минут.При первичном и повторном мониторировании ребенок находился в ОРИТ, состояние ребенка было тяжелым. При повторном обследовании был экстубирован, дышал самостоятельно. Визуальный сравнительный динамический анализ изменений в рассеянии точек по квадрантам выявил тенденцию к снижению симпатического тонуса в сочетании с повышением реактивности, что отражалось в уменьшении количества точек соотношения индексов SDI и PVL в IY квадранте и увеличении их количества в III и II квадранте за счет действия седативного препарата и увеличение продолжительности состояния сна. Вместе с тем существенного снижения тяжести состояния за истекший 8-дневный период выявлено не было, что может расцениваться как тенденцию к некоторому улучшение состояния пациента в процессе лечения. (Фиг. 6)
Источники информации:
Анохин П.К. Очерки по физиологии функциональных систем. М., 1975 -448 с
Вейн А.М. Вегетативные расстройства: клиника, лечение, диагностика / Под ред. A.M. Вейна. М.Медицинское информационное агентство, 2000. - 752 с
Вейн A.M. Вегетососудистая дистония / A.M. Вейн, А.Д. Соловьева, О.А. Колосова. М., Медицина, 1981. - 320 с.
Судаков К.В. Функциональные системы. - М.: Изд-во РАМН, 2011.
Судаков К.В., Андрианов В.В. Теория функциональных систем как основа формирования системного мировоззрения студентов медиков. Сеченовский вестник №1 (7) 2012, с.29-33
Довбыш Н.Ю., Бичурин Р.А, Грицан А.И. Интраоперационная оценка адекватности анальгезии. Сибирское медицинское обозрение. 2020;(6):97-100
Andrade E., Quinlan L., Harte R., Byrne D., Fallon E., Kelly M., et al. Novel Interface designs for patient monitoring applications in critical care medicine: human factors review. JMIR human factors. 2020;7(3):e15052
Aslanidis T., Grosomanidis V., Karakoulas K., and Chatzisotiriou A. Electrodermal Activity during Blood Pooling for Arterial Blood Gases Analysis in Sedated Adult Intensive Care Unit Patients. Med Sci (Basel). 2018 Mar; 6(1): 20.
Aslanidis T., Grosomanidis V., Karakoulas K., and Chatzisotiriou A. Electrodermal Activity Monitoring During Painful Stimulation in Sedated Adult Intensive Care Unit Patients: a Pilot Study. Acta Medica (Hradec Králové) 2018; 61(2): 47-52.
Baliki MN, Apkarian AV. Nociception, Pain, Negative Moods, and Behavior Selection. Neuron. 2015 Aug 5;87(3):474-91. doi: 10.1016/j.neuron.2015.06.005. PMID: 26247858; PMCID: PMC4529956.
Barman S.M., and Yate В.J. (2017). Deciphering the Neural Control of Sympathetic Nerve Activity: Status Report and Directions for Future Research. Front. Neurosci., https://doi.org/10.3389/fnins.2017.00730
Benedek M.; Kaernbach C. (2010).A continuous measure of phasic electrodermal activity.J. Neurosci.Methods 2010,190,80-91
Berntson G.G, Cacioppo J.T., and Quigley K.S. (1991).Autonomic Determinism: The Modes of Autonomic Control, the Doctrine of Autonomic Space, and the Laws of Autonomic Constraint. Psychological Review Copyright 1991 by the American Psychological Association~ Inc. 1991, Vol.98, No. 4, 459-487
Bouscein W. (2012). Electrodermal activity. New York: Springer Science+Business Media
Boucsein W., Fowles D. C., Grimnes S., Ben-Shakhar G., Roth W. T., Dawson M. E. (2012). Publication Recommendations for Electrodermal Measurements, Psychophysical Psychophysology, vol. 49, no. 8, pp.1017-1034, 2012
Cacioppo J.T., Tassinary L. G. and Berntson G., (2007) Handbook of Psychophysiology, Cambridge: Cambridge Up, 2007.
Cohen, D. H., & Randall, D. C. (1984). Classical conditioning of cardiovascular responses. Annual Review of Physiology, 46, 187-197.
Doberenz S., Roth W. T., Wolburgh E., Maslowski N. I. and S. Kim. (2011). Methodological considerations in ambulatory skin conductance monitoring, International Journal of Psychophysiology, vol. 80, no. 2, pp.87-95, 2011.
Ellaway, P.H.; Kuppuswamy, A.; Nicotra, A.; Mathias, C.J. (2010).Sweat production and the sympathetic skin response: Improving the clinical assessment of autonomic function. Auton. Neurosci. 2010, 155, 109-114.
Hernandez J., Morris R.R. and Picard R.W., (2011). Call Center Stress Recognition with Person-specific Models, Springer, 2011, pp.125-134.
Geuter S, Boll S, Eippert F, Büchel C. Functional dissociation of stimulus intensity encoding and predictive coding of pain in the insula. Elife. 2017 May 19;6:e24770. doi: 10.7554/eLife.24770. PMID: 28524817; PMCID:
Groscurth P. (2002). Anatomy of sweat glands. Curr Probl Dermatol. 2002;30:1-9
Gross J, Schnitzler A, Timmermann L, Ploner M. Gamma oscillations in human primary somatosensory cortex reflect pain perception. PLoS Biol. 2007 May;5(5):e133. doi: 10.1371/journal.pbio.0050133. PMID: 17456008; PMCID: PMC1854914
Guinard B. Monitoring analgesia. Best Pract Res Clin Anaesthe-siol. 2006;20:161-1680
Giuliano R. J., Karns C.M., et al. (2017). Parasympathetic and Sympathetic Activity Are Associated with Individual Differences in Neural Indices of Selective Attention in Adults. bioRxiv preprint doi: https://doi.org/10.1101/173377.
Fallon M., Walker J., Colvin L.Pain management in cancer center inpatients: a cluster randomized trial to evaluate a systematic integrated approach-the Edinburgh Pain Assessment and Management Tool. J Clin Oncol. 2018;36:1284-1290.
Fenning R.M., Baker J.K., Baucom B.R., Erath S.A., Howland M.A., Moffitt J.
Electrodermal Variability and Symptom Severity in Children with Autism Spectrum Disorder. Autism Dev Disord. 2017 Apr; 47(4):1062-1072. doi: 10.1007/s10803-016-3021-0.
Fowles D.C. (1986). The eccrine system and electrodermal activity. In Psychophysiology, ed. MGH Coles, E Donchin, SW.Porges, pp.51-96, Guilford Press, New York.
Freeman R. (2006). Assessment of cardiovascular autonomic function. Clinical Neurophysiology.
https://doi.org/10.1016/j.clinph.2005.09.027
Ledowski T. Objective monitoring of nociception: a review of current commercial solutions. Br J Anaesth. 2019 Aug;123(2):e312-e321. doi: 10.1016/j.bja.2019.03.024. Epub 2019 Apr 30. PMID: 31047645; PMCID: PMC6676047
Lee I.S., Necka E.A., Atlas LY. Distinguishing pain from nociception, salience, and arousal: How autonomic nervous system.activity can improve neuroimaging tests of specificity. Neuroimage. 2020 Jan 1;204:116254. doi:.10.1016/j.neuroimage.2019.116254. Epub 2019 Oct 8. PMID: 31604122; PMCID:
Lovallo W.R. (2011). Do low levels of stress reactivity signal poor states of health? Biol Psychol. 2011 Feb;86(2):121-8.
Luginbuhl M, Ypparila-WoltersH, Rufenacht M, Petersen-Felix S, Korhonen I. Heart rate variability does not discriminate betweendifferent levels of hemodynamic responsiveness during surgical anesthesia. Br J Anesth. 2007; 98: 728-736.
McEwen BS Physiology and neurobiology of stress and adaptation: central role of the brain.
Physiol Rev. 2007 Jul; 87(3): 873-904.
Mestanik M, Visnovcova Z, Tonhajzerova I. (2014).The assessment of the autonomic response to acute stress using electrodermal activity. ACTA MEDICA MARTINIANA 2014 14/2, рр. 5-9
Miller WL, Sigvardt KA. (1998).Spectral analysis of oscillatory neural circuits. J Neurosci Methods. 1998;80(2):113-128. doi:10.1016/s0165- 0270(97)00185-4
Mobascher A. et al. Fluctuations in electrodermal activity reveal variations in single trial brain responses to painful laser stimuli - A fMRI/EEG study. NeuroImage, Volume 44, Issue 3, 1 February 2009, Pages 1081-1092. Naga Y. et al.
Nickel MM et al. Autonomic responses to tonic pain are more closely related to stimulus intensity than to pain intensity. Pain. 2017 Nov;158(11):2129-2136.
Nunes RR, Fonseca NM, Simões CM, Rosa DM, Silva ED, Cavalcante SL, Lopes CG, Stefani LC. Brazilian consensus on anesthetic depth monitoring. Braz J Anesthesiol. 2015 Nov-Dec;65(6):427-36. doi: 10.1016/j.bjane.2015.10.001. Epub 2015 Nov 3. PMID: 26614137.
Nunes RR. Componentes da atividade anestésica-uma novavisão. Rev Bras Anestesiol. 2003;53:145--9.
Posada-Quintero H.F., Reljin N., Mills C., Mills I., Florian J.P., VanHeest J.L., et al. (2018). Time-varying analysis of electrodermal activity during exercise. (2018) PLoS ONE 13(6): e0198328.
Posada-Quintero, H.F.; Kong, Y.; Chon, K.H. Objective Pain Stimulation Intensity and Pain Sensation Assessment Using Machine Learning
Classification and Regression Based on Electrodermal Activity. Am. J. Physiol.-Regul. Integr.
Comp.Physiol. 2021, 321, R186-R196.
Richter, C. P. (1927). A study of the electrical skin resistance and the psychogalvanic reflex in a case of unilateral sweating. Brain, 50, 216-224.
Roche, T.R., Maas, E.J.C., Said, S. et al. Anesthesia personnel’s visual attention regarding patient monitoring in simulated non-critical and critical situations, an eye-tracking study. BMC Anesthesiol 22, 167 (2022).
Sano A. and Picard R. W., (2013).Stress Recognition using Wearable Sensors and Mobile Phones, in Humaine Association Conference on Affective Computing and Intelligent Interaction (IEEE), 2013.
Schulz CM, Burden A, Posner KL, Mincer SL, Steadman R, Wagner KJ, et al. Frequency and type of situational awareness errors contributing to death and brain damage: a closed claims analysis. Anesthesiology. 2017;127(2):326-37. https://doi.org/10.1097/ALN.0000000000001661
Sessler, C.N., Grap, M.J. & Ramsay, M.A. Evaluating and monitoring analgesia and sedation in the intensive care unit. Crit Care 12, S2 (2008). https://doi.org/10.1186/cc6148
Setz, C.; Arnrich, B.; Schumm, J.; La Marca, R.; Tröster, G.; Ehlert, U. (2010). Discriminating stress from cognitive load using a wearable EDA device. IEEE Trans. Inf. Technol. Biomed. 2010, 14, 410-417.
Tiemann L, May ES, Postorino M, Schulz E, Nickel MM, Bingel U, Ploner M. Differential neurophysiological correlates of bottom-up and top-down modulations of pain. Pain. 2015 Feb;156(2):289-296. doi: 10.1097/01.j.pain.0000460309.94442.44. PMID: 25599450
Tiemann, L., Hohn, V.D., Ta Dinh, S. et al. Distinct patterns of brain activity mediate perceptual and motor and autonomic responses to noxious stimuli. Nat Commun 9, 4487 (2018). https://doi.org/10.1038/s41467-018-06875-x
Tower, S. S., & Richter, C. P. (1932). Injury and repair within the sympathetic nervous system II. The postganglionic neurons. Archives of Neurology and Psychiatry, 28, 1139-1150.
Zhang Z.G., Hu L., Hung Y.S., Mouraux A., Iannetti G.D. Gamma-band oscillations in the primary somatosensory cortex--a direct and obligatory correlate of subjective pain intensity. J Neurosci. 2012;32(22):7429-7438. doi:10.1523/JNEUROSCI.5877
Zhaosheng Jin, et al. Anesthesia Monitoring-Why Not a Standard of Care? APSF.ORG Newsletter the official journal of the anesthesia patient safety foundation. Circulation 122,210, Volume 34, No 2. 2019.
Wallin BG, Charkoudian N. (2007).Sympathetic neural control of integrated cardiovascular function: Insights from measurement of human sympathetic nerve activity. Muscle Nerve. 2007;36:595-614
Weise, E, Heydenreich, E, & Runge, U. (1987). Coni~ibutions of sympathetic and vagal mechanisms to the genesis of heart rate fluctuations during orthostatic load: A spectral analysis. Journal of the Autonomic Nervous System, 21, 127-134.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОНИТОРИНГА СОСТОЯНИЯ ПАЦИЕНТА | 2019 |
|
RU2713942C1 |
| Способ комплексной оценки и визуализации состояния пациента во время седации и общей анестезии | 2019 |
|
RU2718544C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ АКТИВАЦИИ СТРЕСС-СИСТЕМЫ У ПАЦИЕНТОВ | 2017 |
|
RU2668698C1 |
| СПОСОБ ПРЕМЕДИКАЦИИ ПЕРЕД ОПЕРАТИВНЫМИ ГИНЕКОЛОГИЧЕСКИМИ ВМЕШАТЕЛЬСТВАМИ, ВЫПОЛНЯЕМЫМИ В УСЛОВИЯХ ОБЩЕЙ АНЕСТЕЗИИ | 2014 |
|
RU2549474C1 |
| СПОСОБ ОЦЕНКИ АДЕКВАТНОСТИ БЛОКА ПРИ ПРОВОДНИКОВОЙ АНЕСТЕЗИИ | 2008 |
|
RU2357660C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УРОВНЯ РАННЕЙ ПОСЛЕОПЕРАЦИОННОЙ БОЛИ У ПАЦИЕНТОВ ПОСЛЕ ВМЕШАТЕЛЬСТВ НА БРЮШНОМ ОТДЕЛЕ АОРТЫ | 2022 |
|
RU2793546C1 |
| Способ восстановления микроциркуляции вне зоны кожной анестезии при выполнении продлённой эпидуральной анестезии | 2021 |
|
RU2773274C1 |
| Способ прогнозирования и коррекции ожидаемого болевого синдрома после проведения обширных абдоминальных операций на нижнем этаже брюшной полости | 2016 |
|
RU2636901C1 |
| Способ обезболивания при витреоретинальной и эписклеральной хирургии | 2018 |
|
RU2713133C1 |
| СПОСОБ КОНТРОЛЯ АНАЛГЕЗИИ ПРИ ДЕЙСТВИИ БОЛЕВОГО ФАКТОРА | 2004 |
|
RU2279249C2 |

Изобретение относится к медицине, в частности к анестезиологии, реаниматологии, интенсивной терапии и реабилитологии, и может быть использовано для оценки адекватности анестезии. Проводят регистрацию кожной проводимости. Определяют частоты флуктуаций фазической компоненты кожной проводимости по 5-секундным эпохам за интервал времени. Определяют вариабельность фазической компоненты кожной проводимости по формуле 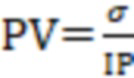 , где PV - вариабельность фазической компоненты кожной проводимости; σ - среднеквадратичное отклонение; IP - усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости. После чего вычисляют индекс симпатической реактивности
, где PV - вариабельность фазической компоненты кожной проводимости; σ - среднеквадратичное отклонение; IP - усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости. После чего вычисляют индекс симпатической реактивности  , где PVL - индекс симпатической реактивности. Вычисляют индекс симпатического доминирования
, где PVL - индекс симпатической реактивности. Вычисляют индекс симпатического доминирования 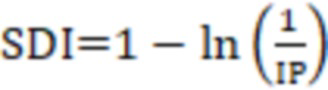 , где SDI - индекс симпатического доминирования, IP – усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости. Графически отображают значения PVL и SDI в режиме реального времени, при этом значениям PVL соответствует ось ординат, а SDI – ось абсцисс. По расположению точек, соответствующих парным значениям PVL и SDI, в системе координат оценивают адекватность анестезии. Если точки находятся в левом нижнем квадранте, то ноцицептивные стимулы и восприятие внешних раздражителей отсутствуют, анальгезия и седация соответствуют текущей потребности пациента. Если точки находятся в правом нижнем квадранте, то ноцицептивные стимулы отсутствуют, возможно интранаркозное пробуждение. Расположение точек в правом верхнем квадранте соответствует активному бодрствованию. Расположение точек в левом верхнем квадранте соответствует болевым стимулам у пациента в бессознательном состоянии. Способ обеспечивает предотвращение чрезмерной или недостаточной анестезии за счет оценки адекватности анестезии путем определения PVL и SDI. 6 ил., 5 пр.
, где SDI - индекс симпатического доминирования, IP – усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости. Графически отображают значения PVL и SDI в режиме реального времени, при этом значениям PVL соответствует ось ординат, а SDI – ось абсцисс. По расположению точек, соответствующих парным значениям PVL и SDI, в системе координат оценивают адекватность анестезии. Если точки находятся в левом нижнем квадранте, то ноцицептивные стимулы и восприятие внешних раздражителей отсутствуют, анальгезия и седация соответствуют текущей потребности пациента. Если точки находятся в правом нижнем квадранте, то ноцицептивные стимулы отсутствуют, возможно интранаркозное пробуждение. Расположение точек в правом верхнем квадранте соответствует активному бодрствованию. Расположение точек в левом верхнем квадранте соответствует болевым стимулам у пациента в бессознательном состоянии. Способ обеспечивает предотвращение чрезмерной или недостаточной анестезии за счет оценки адекватности анестезии путем определения PVL и SDI. 6 ил., 5 пр.
Способ оценки адекватности анестезии, заключающийся в том, что проводят регистрацию кожной проводимости, определяют частоты флуктуаций фазической компоненты кожной проводимости по 5-секундным эпохам за интервал времени, определяют вариабельность фазической компоненты кожной проводимости по формуле 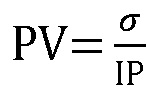 , где PV - вариабельность фазической компоненты кожной проводимости; σ - среднеквадратичное отклонение; IP - усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости;
, где PV - вариабельность фазической компоненты кожной проводимости; σ - среднеквадратичное отклонение; IP - усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости;
после чего вычисляют индекс симпатической реактивности 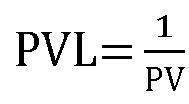 , где PVL - индекс симпатической реактивности;
, где PVL - индекс симпатической реактивности;
вычисляют индекс симпатического доминирования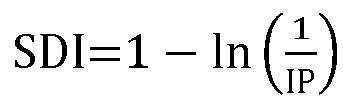 , где SDI - индекс симпатического доминирования, IP – усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости;
, где SDI - индекс симпатического доминирования, IP – усредненное за 1-минутный интервал значение частоты колебаний фазической компоненты кожной проводимости;
графически отображают значения PVL и SDI в режиме реального времени, при этом значениям PVL соответствует ось ординат, а SDI – ось абсцисс,
по расположению точек, соответствующих парным значениям PVL и SDI, в системе координат оценивают адекватность анестезии:
если точки находятся в левом нижнем квадранте, то ноцицептивные стимулы и восприятие внешних раздражителей отсутствуют, анальгезия и седация соответствуют текущей потребности пациента;
если точки находятся в правом нижнем квадранте, то ноцицептивные стимулы отсутствуют, возможно интранаркозное пробуждение;
расположение точек в правом верхнем квадранте соответствует активному бодрствованию; расположение точек в левом верхнем квадранте соответствует болевым стимулам у пациента в бессознательном состоянии.
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ АКТИВАЦИИ СТРЕСС-СИСТЕМЫ У ПАЦИЕНТОВ | 2017 |
|
RU2668698C1 |
| СПОСОБ МОНИТОРИНГА СОСТОЯНИЯ ПАЦИЕНТА | 2019 |
|
RU2713942C1 |
| СПОСОБ МОНИТОРИНГА УРОВНЯ СТРЕССА У ПАЦИЕНТА | 2015 |
|
RU2622607C2 |
| WO 2018141850 A1, 09.08.2018 | |||
| ASLANIDIS T | |||
| et al | |||
| Electrodermal activity: Applications in perioperative care | |||
| International Journal of Medical Research & Health Sciences | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Ручной прибор для отделки верхних концов лопаток на роторах и цилиндрах паровых турбин | 1925 |
|
SU687A1 |
| TSENG B | |||
| et al | |||
| Tonic Electrodermal Activity is a Robust Marker of | |||
Авторы
Даты
2023-11-13—Публикация
2022-09-08—Подача