Изобретение относится к области фармации и касается способа получения средства, обладающего антигипоксической активностью.
В практике народной медицины с большим успехом применяются многокомпонентные лекарственные препараты, включающие в среднем от 3 до 5 ингредиентов. Считается, что их высокая фармакотерапевтическая эффективность обусловлена гармоничным сочетанием содержащихся биологически активных веществ в исходных видах растительного сырья. В Государственный реестр лекарственных средств входит около 40 различных многокомпонентных сборов и количество их постоянно увеличивается [7, 13].
Основываясь на данные литературы о химическом составе, фармакологическом действии лекарственных растений нами предлагается способ получения средства, обладающего антигипоксической активностью на основе травы серпухи васильковой, травы эхинацеи пурпурной, плодов шиповника, корневищ с корнями девясила высокого, листьев бадана толстолистного черных в виде экстракта сухого.
Фенологликозиды обладают широким спектром фармакологической активности, они проявляют противовоспалительное, противомикробное, антисептическое, мочегонное, противогрибковое, противовирусное, антигельминтное, адаптогенное и тонизирующее действия [2, 8]. Известно, что в опытах in vivo на белых крысах отвары толокнянки проявляют антигипоксическое действие: под их влиянием увеличивался процент выживания животных в условиях гипоксии. Это действие связывают с содержанием в них гидрохинона, который относится к веществам с лабильным водородом и повышает активность окислительно-восстановительных реакций. Он обладает способностью блокировать О-метилтрансферазу, что способствует увеличению периода действия адреналина. В эксперименте гидрохинон влияет на метаболические процессы, поглощение кислорода тканями, содержание в крови глюкозы, калия, глутатиона, корригирует диабетический кетоацидоз, проявляет гипертензивный эффект в экспериментальных шоковых ситуациях. Фенологликозиды содержатся в черных листьев бадана, а также в траве серпухи васильковой.
Спектр фармакологических свойств флавоноидов очень разнообразен, они оказывают: капилляроукрепляющее, спазмолитическое, антистрессовое, противовоспалительное, антигрибковое, антитоксическое, антибактериальное, антиаллергическое, противовирусное, антиаритмическое, антиканцерогенное,
антигипертензивное, антиатеросклеротическое, иммуномодулирующее,
гепатопротекторное, нефропротекторное [3, 4, 6]. Одним из ключевых свойств флавоноидов является их антиоксидантная активность, в том числе способность подавлять процессы перекисного окисления липидов, белков, нуклеиновых кислот и других соединений, тормозить процессы пероксидации. Флавоноиды содержатся в траве серпухи васильковой, эхинацеи пурпурной, в плодах шиповника и черных листьях бадана.
В качестве прототипа данного изобретения принят - экстракт левзеи сафлоровидной жидкий, который изготовлен из корневищ с корнями левзеи сафлоровидной в соотношении сырье и экстрагент 1:1 на 70% этаноле [5]. Данный экстракт применяется в качестве средства, повышающего работоспособность при умственном и физическом переутомлении. Основными действующими веществами экстракта являются экдистероиды [5].
Недостатками указанного средства являются слабо выраженная антигипоксическая активность по сравнению со средством, полученным по предлагаемому способу.
Технический результат изобретения - расширение ассортимента лекарственных средств, обладающих антигипоксической активностью, за счет использования широко распространенного растительного сырья, имеющего надежную и обеспеченную сырьевую базу, повышение выхода экстрактивных веществ, арбутина и суммы флавоноидов.
Для этого растительный материал, состоящий из высушенной измельченной растительной смеси следующего состава (мас. части) - серпухи васильковой (травы) - 30, эхинацеи пурпурной (травы) - 20, шиповника (плодов) - 20, девясила высокого (корневищ с корнями) - 20, бадана толстолистного черные (листьев) - 10 - экстрагируют трехкратно при соотношении 1 мас. ч. сырья : 12 об. ч экстрагента. При первом и втором контакте фаз используется экстрагент 30% этиловый спирт, при третьем контакте фаз - экстракция 70% этиловым спиртом. Экстрагирование при каждом контакте фаз выполняется в течение 90 минут. Спиртовые извлечения после экстракций упаривают до 1/3 первоначального объема. Объединенные кубовые остатки от трех извлечений сепарируют. Полученный продукт доупаривают приблизительно до 1/5 и высушивают в вакуум-сушильном шкафу. Выход готового продукта составляет 40,09% от массы растительного материала. Экстракт сухой, представляет собой аморфный порошок от коричневого до темно - коричневого цвета со специфическим запахом, сладковатого вкуса, потеря в массе при высушивании не более 5%. Гигроскопичен, комкуется. Данный способ получения достаточно прост, не требует сложной схемы очистки, позволяет получить продукт постоянного состава.
Изучены факторы, которые оказывают влияние на процесс экстрагирования растительного материала - природа экстрагента, степень измельчения, соотношение сырье: экстрагент, температурный режим и длительность экстракции.
Количественная оценка велась по выходу экстрактивных веществ [1], количественному содержанию арбутина и суммы флавоноидов в пересчете на лютеолин-7-гликозид. Результаты исследования представлены в таблице 1.
Количественное содержание арбутина проводили
хроматоспектрофотометрическим методом. Для этого аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм.
Около 1,0 г (точная навеска) сбора помещают в колбу со шлифом вместимостью 250 мл, прибавляют 50 мл спирта 30%, взвешивают с погрешностью ±0,01. Колбу присоединяют к обратному холодильнику и экстрагируют на кипящей водяной бане в течение 60 мин. После экстракции колбу с содержимым охлаждают до комнатной температуры, взвешивают и доводят спиртом 30% до первоначальной массы. Извлечение фильтруют через бумажный складчатый фильтр (раствор А испытуемого раствора).
2,0 мл раствора А помещают в стеклянную колонку диаметром 1,5 см на слой алюминия оксида, сформированного в спирте 30%, массой 3,0 г, элюируют 20 мл спиртом 30% в мерную колбу на 25 мл, доводят объем раствора тем же растворителем до метки и перемешивают (раствор Б). В качестве раствора сравнения используют спирт 30%. Определяют оптическую плотность раствора на спектрофотометре при длине волны л***= 285 нм в кювете с толщиной слоя 10 мм.
Параллельно измеряют оптическую плотность раствора Б СО арбутина. В качестве раствора сравнения используют спирт 30%.
Содержание арбутина и абсолютно сухое сырье в процентах (X) вычисляют по формуле:
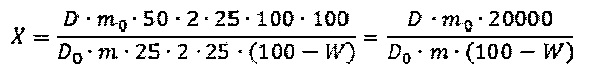
где D - оптическая плотность испытуемого раствора Б; Do - оптическая плотность раствора СО арбутина; m - навеска сырья, г; m0 - навеска СО арбутина, г; W - влажность сырья, %.
Приготовление СО арбутина: около 0,025 г (точная навеска) СО арбутина, предварительно высушенного при температуре 105-110°С в течение 2 ч, помещают в мерную колбу вместимостью 25 мл, растворяют в небольшом количестве спирта 95%, доводят объем раствора до метки спиртом 95% и перемешивают (раствор А СО арбутина).
Срок годности раствора не более 30 сут при хранении в прохладном, защищенном от света месте.
2 мл раствора А СО арбутина помещают в стеклянную колонку диаметром 1,5 см на слой алюминия оксида, сформированного в спирте 30%, массой 3,0 г, элюируют 20 мл спиртом 30% в мерную колбу на 25 мл, доводят объем раствора тем же растворителем до метки и перемешивают (раствор Б СО арбутина).
Количественное содержание флавоноидов проводили спектрофотометрическим методом с добавлением комплексообразующего реактива - спиртового раствора алюминия хлорида.
Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм.
Около 1,0 г (точная навеска) измельченного сырья помещают в колбу со шлифом вместимостью 250 мл, прибавляют 50 мл спирта 70%. Колбу взвешивают с погрешностью ±0,01 г, присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 60 минут. После охлаждения до комнатной температуры, колбу вновь взвешивают и доводят до первоначальной массы спиртом 70%. Извлечение фильтруют через бумажный складчатый фильтр «красная лента», отбрасывая первые 10 мл фильтрата (раствор А).
2 мл раствора А помещают в мерную колбу вместимостью 25 мл, прибавляют 3 мл алюминия хлорида спиртового раствора 3% и доводят объем раствора спиртом 70% до метки и перемешивают (раствор Б). В качестве раствора сравнения используют раствор, состоящий из 1 мл раствора А, доведенного спиртом 70% до метки в мерной колбе вместимостью 25 мл.
Через 45 мин измеряют оптическую плотность раствора Б на спектрофотометре при длине волны 395 нм в кювете с толщиной слоя 10 мм. Параллельно в тех же условиях измеряют оптическую плотность раствора СО лютеолин-7-гликозида.
Содержание суммы флавоноидов в пересчете на лютеолин-7-гликозида и абсолютно сухое сырье в процентах (X) вычисляют по формуле:
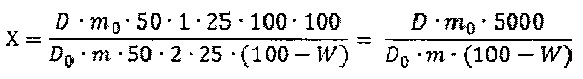
где D - оптическая плотность испытуемого раствора; D0 - оптическая плотность раствора Б СО лютеолин-7-гликозида; m - навеска сырья, г; m0 - навеска СО лютеолин-7-гликозида, г; W - влажность сырья, %.
Приготовление РСО лютеолин-7-гликозида:
Около 0,05 г (точная навеска) РСО лютеолин-7-гликозида, предварительно высушенного при температуре 100-105°С в течение 2 часов, растворяют в небольшом количестве 70% спирта в мерной колбе на 25 мл и доводят объем раствора до метки 70% спиртом (раствор А).
1 мл раствора А помещают в мерную колбу вместимостью 25 мл, приливают 2 мл 3% спиртового раствора алюминия хлорида и доводят объем раствора до метки 70% спиртом (раствор Б).
Результаты анализа влияния типа экстрагента на извлечение биологически активных веществ представлены в таблице 1.
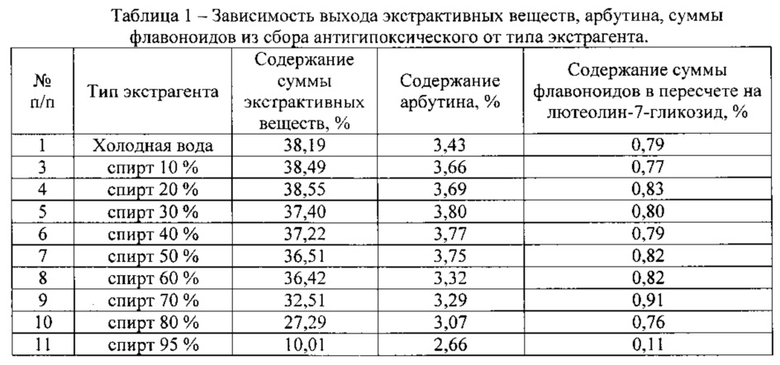
Из данных таблицы следует, что 30% этанол обеспечивает максимальный выход арбутина, 70% этанол - флавоноидов, а сумму экстрактивных веществ максимально извлекает 20% этанол. Таким образом, нами предлагается использовать два экстрагента для полного истощения сырья - 30 % этанол в первой и второй экстракции и 70% этанол -в третьей экстракции, которые позволят увеличить выход биологически активных веществ из исходного сырья. Для полного извлечения экстрактивных веществ предлагаем использовать многократную экстракцию.
Изучено влияние различных типов экстрагента при трехкратной экстракции на извлечение экстрактивных веществ. По данным таблиц видно, что наибольшее истощение сырья и максимальный выход экстрактивных веществ наблюдается при экстракции первом контакте фаз - спиртом 30%, при втором - 30% и третьем - 70% (таблицы 2).
На процесс экстракции, качество вытяжки и полноту выхода биологически активных веществ большое влияние оказывает характер измельчения растительного
сырья. Исходное сырье подвергалось измельчению до размера частиц 0,5; 1; 2; 3 и 5 мм. Данные анализа представлены в таблице 3.
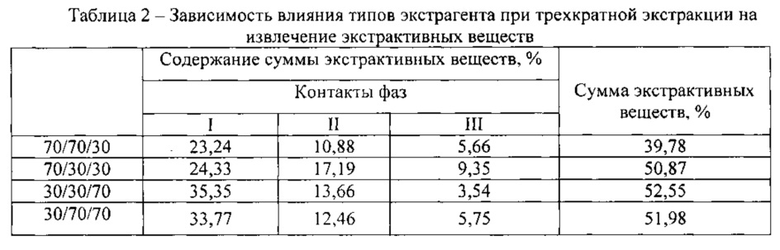
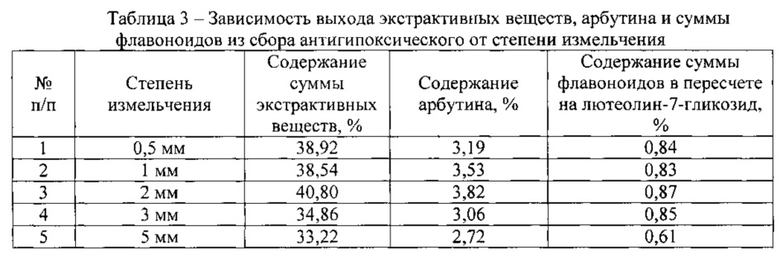
Наиболее оптимальным измельчением растительного сырья является степень измельчения 1-2 мм. Так как дальнейшее измельчение растительного материала нецелесообразно из-за затруднения экстрагирования (очень мелкий порошок образует с растворителем тестообразную массу, что затрудняет процесс фильтрации) и более крупное измельчение не рационально, так как в сырье замедляется процесс экстракции биологически активных веществ.
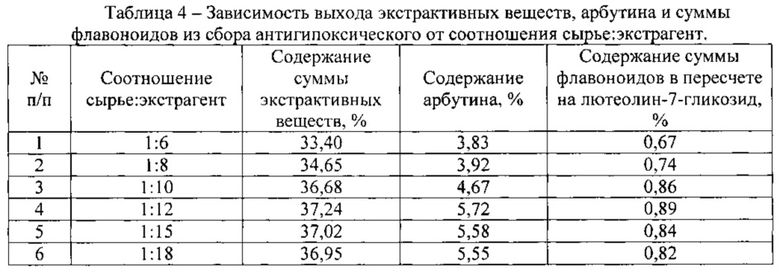
Изучена зависимость выхода суммы экстрагируемых веществ в различных соотношениях к количеству сырья (таблица 4). Экспериментальные данные свидетельствуют о том, что оптимальное соотношение сырья и экстрагента является 1:12 для однократного залива. Дальнейшее увеличение соотношения нецелесообразно ввиду незначительного повышения выхода действующих веществ, а также в связи с увеличением расхода экстрагента. Коэффициент водопоглощения сбора антигипоксического 3.
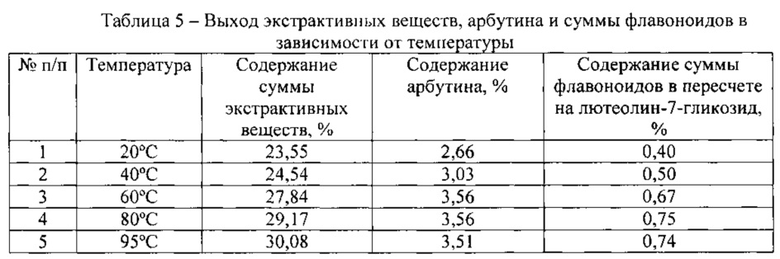
Изучено влияние температурного режима на выход экстрактивных веществ и биологически активных веществ. По данным таблицы 5 видно, что повышение
температуры увеличивает выход веществ, но для получения экстракта сухого выбрана температура при 60°С, так как повышение температуры с одной стороны может привести к разрушению термолабильных веществ, ухудшению растворения или испарению некоторых веществ (например, эфирных масел), переходу в извлечение большого количества балластных веществ, с другой стороны - увеличивает энергозатратность производства готового продукта.
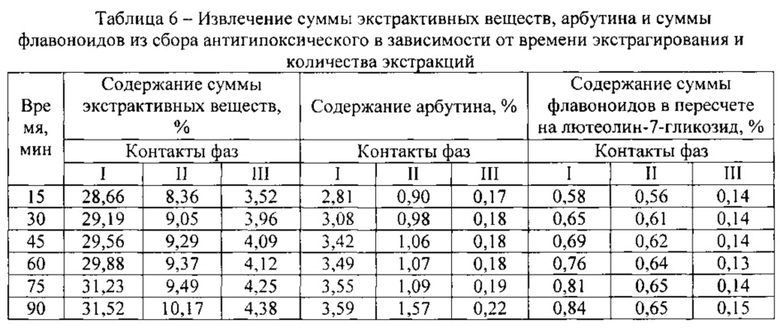
С целью определения продолжительности и кратности числа экстракций было изучено время наступления равновесной концентрации в системе сырье-экстрагент при трехкратной экстракции разными типами экстрагента. Для этого массу навески сырья экстрагировали последовательно спиртом 30%, 30% и 70% в соотношении 1:12 на водяной бане при температуре 60°С при постоянном перемешивании с обратным холодильником. Через заданные промежутки времени (15, 30, 45, 60, 75, 90 мин.) извлечения фильтровали (1-ый контакт фаз), определяя содержание суммы экстрактивных веществ, арбутина и флавоноидов. Затем проводили две последующие экстракции отжатого сырья при тех же промежутках времени, заливая во 2-ом контакте фаз - 30% спирт, а в 3-ем контакте - 70% спирт равных объему слитых извлечений. Извлечения также анализировали на сумму
экстрактивных веществ, арбутина и флавоноидов. По результатам данных таблицы 6 видно, что равновесное состояние наступает при 1-ом, 2-ом и 3-ем контакте фаз через 90 мин.
Все подобранные оптимальные параметры процесса экстракции были положены в основу первой серии балансовых загрузок, на основании которой была разработана технологическая схема получения средства, обладающего антигипоксической активности, в виде экстракта сухого.
Пример способа получения экстракта сухого: 0,30 кг серпухи васильковой травы, 0,20 кг девясила высокого корневищ с корнями, 0,20 кг эхинацеи пурпурной травы, 0,20 кг шиповника плодов, 0,10 кг бадана толстолистного листьев черных измельчают на мельнице до размера частиц диаметром 1,0-2,0 мм. Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 15 л спиртом 30 % в соотношении сырье: экстрагент 1:12 (с учетом коэффициента водопоглощения = 3). Первую экстракцию выполняют при температуре 60°С в течение 90 мин при постоянном перемешивании. Извлечение фильтруют через серошинельное сукно в сборник. Вторую экстракцию выполняют в течение 90 мин при температуре 60°С, подавая в экстрактор 12,9 л спирта 30 %. Третью экстракцию выполняют спиртом 70 % в течение 90 мин при той же температуре, объем экстрагента 11 л. В результате экстракции получаем извлечения в количестве 12,9 л (1-ый слив); 11 л (2-ой слив); 11 л (3-ий слив). Объединенные водно-спиртовые извлечения после экстрагирования последовательно порциями упаривают примерно до 1/3 первоначального объема. Объединенные кубовые остатки от трех извлечений подвергают очистке сепарированием. Очищенный экстракт доупаривают до 1/5 первоначального объема и сушат на нержавеющих противнях в
вакуумной сушилке при 65-70°С 8 ч. Получают 400,9 г готового продукта, что составляет 40,09 % сухого экстракта от веса исходного сырья.
Средство, обладающее антигипоксической активностью, представляет собой экстракт сухой - аморфный порошок от коричневого до темно - коричневого цвета со специфическим запахом, сладковатого вкуса, потеря в массе при высушивании не более 5%. Гигроскопичен, комкуется.
Исследование острой токсичности средства, обладающего антигипоксической
активностью.
Опыты проведены на крысах-самцах линии Wistar массой 170-190 г. Острую токсичность средства оценивали с использованием метода Кербера [9] при однократном внутрибрюшинном введении экстракта сухого в дозах от 300 до 5000 мг/кг и внутрижелудочном введении в диапазоне доз от 500 до 6000 мг/кг. Все испытанные дозы доводили дистиллированной водой до конечного объема, составляющего 1,0 мл/100 г массы животного. Наблюдение за общим состоянием подопытных крыс и их поведением осуществляли в течение 14 дней. В первый день после введения указанных средств животные находились под постоянным наблюдением. Регистрировали видимые признаки интоксикации: общее состояние животных, поведение, двигательную активность, характер дыхательных движений, состояние волосяного и кожного покрова, окраску слизистых оболочек, потребление корма и воды, количество и консистенцию фекальных масс, частоту мочеиспускания и окраску мочи. Также регистрировали сроки развития интоксикации и гибели животных. На 14 сутки эксперимента осуществляли эвтаназию под эфирным наркозом и проводили макроскопический осмотр внутренних органов с помощью бинокулярной лупы, а также осуществляли патоморфологическое исследование жизненно важных органов.
Установлено, что при внутрижелудочном и внутрибрюшинном введении во всех исследованных дозах гибели животных в течение всего периода наблюдения не отмечалось. При внутрибрюшинном введении наиболее высоких доз испытуемого фитоэкстракта (3000 -5000 мкг) в течение 1-2 суток наблюдали видимые признаки интоксикации животных в виде гиподинамии, снижения потребления корма, учащения дыхания. Вскрытие животных, осуществленное через 14 суток показало, что визуально внутренние органы не отличались от таковых у интактных крыс. При патоморфологическом исследовании у животных, получавших фитоэкстракт в высоких дозах, отмечали нарушения гемодинамики в виде полнокровия сосудов, а также единичные мелкоточечные кровоизлияния в слизистой оболочке желудка.
Таким образом, полученные данные позволяют отнести средство, обладающее антигипоксической активностью, к группе практически нетоксичных веществ по классификации К.К.Сидорова [12].
Исследование влияния средства, обладающего антигипоксической активностью, на устойчивость животных к кислороддефицитным состояниям.
Эксперименты проведены на крысах линии Wistar массой 170-190 г. Антигипоксическую активность средства исследовали с использованием модели острой гемической, гистотоксической и нормобарической гипоксии с гиперкапнией. Модель гемической гипоксии воспроизводили путем однократного внутрибрюшинного введения нитрита натрия в дозе 70 мг/кг (LD50); гистотоксической гипоксии - однократным введением нитропруссида натрия 20 мг/кг (DL100); нормобарической гипоксии с гиперкапнией - путем помещения животных в герметически закрытые банки объемом 200 см3 [10]. Животным опытных групп испытуемое средство в виде водного раствора вводили внутрижелудочно в дозах 50, 100 и 200 мг/кг в объеме 10 мл/кг профилактически в течение 7 дней до тестирования. Крысам контрольной группы вводили эквиобъемное количество дистиллированной воды. В качестве препарата сравнения использовали использовали деалкоголизированный раствор экстракта левзеи сафлоровидной жидкий в изоэффективной дозе 5,0 мл/кг. С целью оценки антигипоксической активности регистрировали резервное время жизни и количество выживших животных в условиях гипоксии. Общая продолжительность наблюдения за животными составила две недели; в первые сутки после введения гипоксантов животные находились под непрерывным наблюдением. Значимость различий между указанными параметрами среди контрольной и опытных групп оценивали с помощью непараметрического критерия Манна-Уитни. Различия считались существенными при Р<=0,05 [11]. Полученные данные приведены в таблице 7.
Установлено, что комплексное средство оказывает антигипоксическое действие, увеличивая продолжительность жизни и выживаемость животных при кислороддефицитных состояниях различного генеза. При гемической гипоксии курсовое введение испытуемого средства в дозах 100 и 200 мг/кг время жизни животных увеличилось соответственно на 36 и 45% по сравнению с данными крыс контрольной группы. При этом в указанных группах из 6 животных погибло по 1 крысе, что составило 16% при 100% гибели в контрольной группе. Препарат сравнения оказывал аналогичное действие в дозе 100 мг/кг по показателю продолжительности жизни, но уступал по количеству погибших животных. Как следует из приведенной таблицы, испытуемое средство в исследованных дозах, как и экстракт левзеи
сафлоровидной, не оказывали влияния на резервное время жизни животных, при этом в группах крыс, получавших новое средство, отмечалось увеличение выживаемости животных. При нормобарической гипоксии с гиперкапнией введение средства, обладающее антигипоксической активностью, в дозах 100 и 200 мг/кг сопровождалось увеличением продолжительности жизни животных в среднем на 23-25%, а также выживаемости на 50 и 17% по сравнению с аналогичными показателями крыс контрольной группы. Антигипоксическое действие препарата сравнения при гиперкапнической гипоксии уступало таковому у заявленного средства.
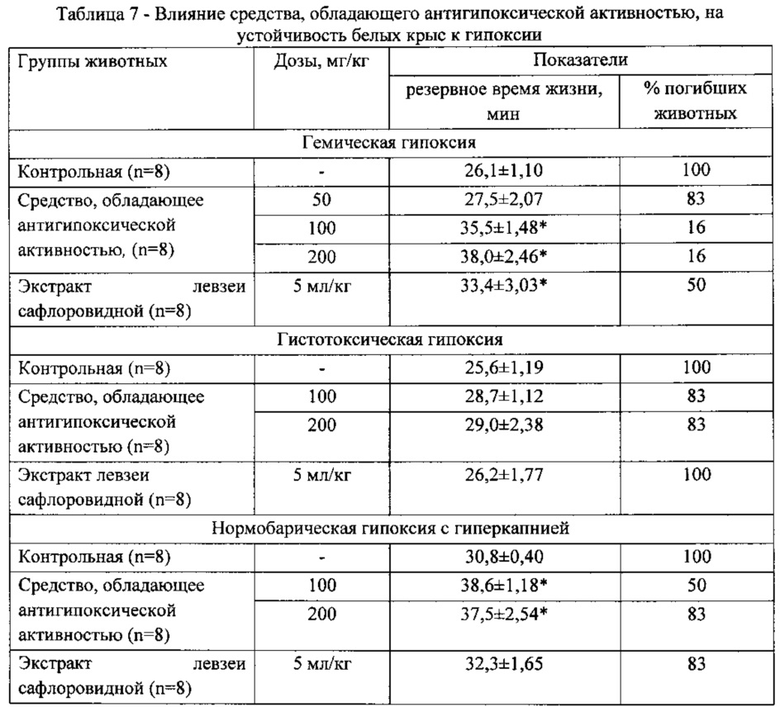
Примечание: * - здесь и далее различие достоверно по сравнению с данными в контрольной группе животных при Р <= 0,05.
Таким образом установлено, что курсовое введение средства, обладающего антигипоксической активностью, в дозах 100 и 200 мг/кг повышает устойчивость
лабораторных животных к гемической гипоксии и нормобарической гипоксии с гиперкапнией, существенно повышая выживаемость животных и резервное время их жизни. При этом антигипоксическая активность заявленного средства в указанных дозах была выше таковой у препарата сравнения - экстракта левзеи сафлоровидной.
Литература
1. Государственная фармакопея СССР XI издание. Т. 1. - Москва, 1987. - С. 295
2. Дугаржапов A.M. Экспериментальная фармакотерапия экстрактом толокнянки обыкновенной повреждений почек. - автореф. дисс. ... к.м.н. - Улан-Удэ, 2000. - 23 с.
3. Корулькин Д.Ю., Абилов Ж.А., Музычкина Р.А., Толстиков Г.А. Природные флавоноиды. - Новосибирск: Академическое издательство «Гео», 2007. - 232 с.
4. Макарова М.Н., Макаров В.Г. Молекулярная биология флавоноидов (химия, биохимия, фармакология): руководство для врачей. - СПб., 2010. - 428 с.
5. Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - 1216 с.
6. Муравьева Д.А., Самылина И.А., Яковлев Г.П. Фармакогнозия: учебник. -М.: Медицина, 2002. - 656 с.
7. Муравьев И.А. Технология лекарств. Том 1. - М.: Медицина, 1980. - 704 с.
8. Нагаслаева Л.А. Разработка технологии и состава таблеток с сухим экстрактом толокнянки / Л.А. Нагаслаева, В.И. Глызин, В.Ф. Охотникова // Тибетская медицина. Состояние и перспективы исследований. - Улан-Удэ, 1994. - С. 158-163.
9. Руководство по проведению доклинических исследований лекарственных средств. - М., - 2012. - 944 с.
10. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М., 2005. - С. 308-320
11. Сергиенко В.И., Бондаренко И.Б. Математическая статистика в клинических исследованиях. - Москва, 2006. - 256 с.
12. Требования по доклиническому изучению общетоксического действия новых фармакологических веществ. - М., 1984. - 49 с.
13. Яковлев Г.П. Лекарственное сырье растительного и животного происхождения. Фармакогнозия: учебное пособие / под ред. Г.П. Яковлева. - СПб.: СпецЛит, 2006. - 845с: ил.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения средства, обладающего стресспротективной и антиоксидантной активностью | 2016 |
|
RU2619856C1 |
| Средство, обладающее антигипоксическим и адаптогенным действием | 2021 |
|
RU2771555C1 |
| Композиции для получения бальзама | 2022 |
|
RU2797913C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО СТРЕССПРОТЕКТИВНОЙ И АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2582282C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО СРЕДСТВА, ОБЛАДАЮЩЕГО НЕЙРОПРОТЕКТИВНЫМ ДЕЙСТВИЕМ | 2022 |
|
RU2805653C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И АНТИБАКТЕРИАЛЬНЫМ ДЕЙСТВИЕМ | 2009 |
|
RU2413527C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУММЫ ЭКСТРАКТИВНЫХ ВЕЩЕСТВ, ОБЛАДАЮЩИХ АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2076727C1 |
| Способ получения средства, обладающего тиреотропной активностью | 2016 |
|
RU2619863C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2135198C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2259840C2 |
Изобретение относится к фармацевтической промышленности, а именно к способу получения средства, обладающего антигипоксической активностью. Способ получения средства, обладающего антигипоксической активностью, для этого измельченный растительный материал, состоящий из серпухи васильковой травы, девясила высокого корневищ с корнями, эхинацеи пурпурной травы, шиповника плодов, бадана толстолистного листьев черных, взятые в определенном соотношении, экстрагируют трехкратно при определенных условиях, далее объединенные водно-спиртовые извлечения фильтруют, упаривают, очищают сепарированием, доупаривают, затем высушивают в вакуум-сушильном аппарате. Средство, полученное вышеописанным способом, обладает повышенной антигипоксической активностью. 7 табл.
Способ получения средства, обладающего антигипоксической активностью, для этого растительный материал, состоящий из серпухи васильковой травы, девясила высокого корневищ с корнями, эхинацеи пурпурной травы, шиповника плодов, бадана толстолистного листьев черных в соотношении компонентов в мас. ч.- 3:2:2:2:1, измельченный до размеров частиц диаметром 1,0-2,0 мм, экстрагируют трехкратно при температуре 60°С при отношении 1 мас. ч. растительного материала: 12 об.ч экстрагента, первый и второй контакт фаз 30%-ым этиловым спиртом, третий контакт фаз 70% этиловым спиртом в течение 90 мин каждый, далее объединенные водно-спиртовые извлечения фильтруют, упаривают, очищают сепарированием, доупаривают, затем высушивают в вакуум-сушильном аппарате.
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства., 16-е издание, М.: Новая волна, 2012,1216 с | |||
| КОМПОЗИЦИЯ ИНГРЕДИЕНТОВ "АДАПТОВИТ", ОБЛАДАЮЩАЯ АНТИГИПОКСАНТНЫМ ДЕЙСТВИЕМ | 1997 |
|
RU2114628C1 |
| СБОР, ОБЛАДАЮЩИЙ АНТИГИПОКСИЧЕСКИМ И ГИПОТЕНЗИВНЫМ ДЕЙСТВИЯМИ | 2013 |
|
RU2587722C2 |
| Приспособление для просекания язычков в мундштучной ленте на гильзовых машинах | 1925 |
|
SU5345A1 |
Авторы
Даты
2018-10-11—Публикация
2017-06-13—Подача