Изобретение относится к области фармации и касается способа получения средства из растительного сырья, обладающего нейропротективным действием. Экстракты, субстанции и биологически активные вещества, получаемые из растительных видов рода Серпуха, используются в качестве эффективных лекарственных средств, обладающих нейропротективным, адаптогенным, стресс-протективным действием [1]. Для получения лекарственных средств из видов серпухи наиболее часто используемым является серпуха венценосная, для которой были разработаны способы получения растительных сборов, экстрактов и субстанций, а также серпуха васильковая.
Известны способы получения растительных сборов, содержащих траву серпухи венценосной, в том числе для лечения сердечно-сосудистых заболеваний [2], для лечения злокачественных новообразований [3], для лечения оперированных онкобольных [4], для лечения цирроза печени [5], для лечения эпилепсии [6], для восстановления полового влечения у мужчин [7].
Известен способ получения препарата для оздоровления сердечно-сосудистой системы, обладающий кардиопротекторным, седативным и гипотензивным действием, представляющего собой водно-спиртовый экстракт из растительной смеси из 21 компонента, включая траву серпухи венценосной [8].
Известен способ получения экдистероидсодержащей субстанции из надземной части серпухи венценосной, представляющей смесь 20-гидоксиэкдизона и 25S-инокостерона, используемой для лечения инсулиннезависимого диабета (диабета II типа) [9], а также для коррекции нарушений липидного обмена с целью профилактики и лечения дислипидемий, ишемической болезни сердца [10] и обладающей тонизирующим, актопротекторным [11], антиагрегационным, стресс-лимитирующим действием [12] и противолучевым действием [13].
Лекарственные средства, содержащие серпуху васильковую немногочисленны. Известен способ получения средства, обладающего антигипоксической активностью, представляющего собой сухой экстракт их растительной, состоящей из серпухи васильковой травы, девясила высокого корневищ с корнями, эхинацеи пурпурной травы, шиповника плодов, бадана толстолистного листьев черных, взятые в определенном соотношении [14].
Наиболее близким к заявляемому можно считать способ получения сухого экстракта из травы серпухи васильковой, заключающийся в трехкратной экстракции сырья 70%, 40% и 20% спиртом этиловым при температуре 60°С в течение 90, 60 и 60 мин, соответственно [15]. Выход готового продукта составляет 37% от массы растительного материала. Недостатками заявляемого способ получения являются низкий выход готового продукта, что обусловлено использованием всей надземной части растения, включая стебли, которые содержат мало экстрактивных соединений и обладают плохой измельчаемостью [16], длительность экстракционного процесса (3,5 часа) и применение токсичного экстрагента - этанола. Контроль качества готового продукта ведется по содержанию экдистероидов, которые обладают низкой стресс-протективной и антиоксидантной активностью, и не учитывается содержание действующей группы веществ - кофеилхинных кислот, который оказывают ведущую роль в формировании биологического действия лекарственного средства.
Для устранения недостатков способа-прототипа предложено использование листьев серпухи васильковой, в качестве сырья, ввиду высокого содержания действующей группы соединений - кофеилхинных кислот, высокой экстрактивности и хорошей измельчаемости. В качестве экстрагента выбрана вода по причине низкой токсичности и высокой экстракционной силы по отношению к метаболитам листьев серпухи васильковой. С целью интенсификации процесса экстракции предложено применение ультразвуковой ванны, сокращающей длительность процесса более чем в 2 раза.
Задачей изобретения является создание суммарного растительного препарата, содержащего кофеилхинные кислоты, уменьшение времени экстракции, устранение токсичного экстрагента, а также повышение нейропротективного действия средства за счет высокого содержания действующих веществ. Техническим результатом изобретения является повышенное нейропротективное действие средства из листьев серпухи васильковой, полученного заявленным способом.
Для достижения указанного технического результата измельченный растительный материал (листья серпухи васильковой) экстрагируют водой очищенной в соотношении сырье: экстрагент 1:(15-17) с ультразвуковой обработкой частотой 50 кГц при 90-94°С в течение 50-70 мин, после чего проводят экстракцию водой в тех же условиях в течение 20-40 мин. Водный экстракты концентрируют в вакууме, объединяют остатки после концентрирования в единый экстракт, высушивают его вакуум-сушильном шкафу при температуре 55-65°С и давлении 0,1 атм в течение 5-6 часов и измельчают на мельнице пропеллерного типа. Выход готового продукта (сухого экстракта) составляет 42-46%) от массы растительного сырья.
Выявленные отличительные признаки позволяют сделать вывод о соответствии предлагаемого технологического решения критерию "новизна". Предложенный способ позволяет получить сухой экстракт (далее - средство) в виде рассыпчатого негигроскопичного порошка коричневого цвета с горьким вкусом и специфическим запахом. Потеря массы при высушивании 3,5-4%.
Способ иллюстрируется нижеследующими примерами.
Пример 1. 5,24 кг листьев серпухи васильковой с влажностью 4,8% измельчают на мельнице до размера частиц диаметром 2-3 мм. Измельченные листья серпухи васильковой (5 кг) загружают в экстракционный аппарат с мешалкой и внешним паровым обогревателем и заливают 75 л воды (плотность 0,997 г/см3). Полученную смесь перемешивают, вносят стержневой ультразвуковой процессор и обрабатывают смесь ультразвуком мощностью 50 кГц в импульсном режиме при температуре 90°С в течение 60 мин. После этого ультразвуковой процессор удаляют, смесь фильтруют через сукно в сборник, остаток на фильтре дополнительно промывают 5 л воды очищенной. В результате получено 70 л водного экстракта с плотностью 1,021 г/см3, который концентрируют в вакууме до объема 4 л (плотность концентрата 1,421 г/см3). Отгон воды объемом 66 л (плотность 0.997 г/см3) далее может быть повторно использован на стадии экстракции растительного сырья. Остаток сырья после первой экстракции водой переносят в экстракционный аппарат, заливают 65 л воды и экстрагируют в указанных условиях 30 мин. Смесь фильтруют через сукно в сборник. В результате получено 62 л водного экстракта с плотностью 1,004 г/см3, который концентрируют в вакууме до объема 2 л (плотность концентрата 1,207 г/см3). Отгон воды объемом 60 л (плотность 0,997 г/см3) далее может быть повторно использован на стадии экстракции растительного сырья.
Полученные концентраты после первой и второй водной экстракций объединяют (объем объединенного концентрата 6 л, плотность 1,401 г/см3), сушат в вакуум-сушильном шкафу при температуре 65°С и давлении 0,1 атм в течение 6 часов и измельчают на мельнице пропеллерного типа. Получают 2,1 кг продукта, что составляет 42% от массы растительного сырья. Средство представляет собой рассыпчатый негигроскопичный порошок, коричневого цвета, с горьким вкусом и специфическим запахом. Потеря массы при высушивании составляет 3,5%. Шрот растительного сырья массой 24,2 кг и влажностью 88% далее не используют и направляют в отвал.
Пример 2. 5,22 кг листьев серпухи васильковой с влажностью 5,0% измельчают на мельнице до размера частиц диаметром 2-3 мм. Измельченные листья серпухи васильковой (5 кг) загружают в экстракционный аппарат с мешалкой и внешним паровым обогревателем и заливают 80 л воды (плотность 0,997 г/см3). Полученную смесь перемешивают, вносят стержневой ультразвуковой процессор и обрабатывают смесь ультразвуком мощностью 50 кГц в импульсном режиме при температуре 92°С в течение 50 мин. После этого ультразвуковой процессор удаляют, смесь фильтруют через сукно в сборник, остаток на фильтре дополнительно промывают 5 л воды очищенной. В результате получено 75 л водного экстракта с плотностью 1,023 г/см3, который концентрируют в вакууме до объема 4 л (плотность концентрата 1,429 г/см3). Отгон воды объемом 71 л (плотность 0.997 г/см3) далее может быть повторно использован на стадии экстракции растительного сырья. Остаток сырья после первой экстракции водой переносят в экстракционный аппарат, заливают 70 л воды и экстрагируют в указанных условиях 40 мин. Смесь фильтруют через сукно в сборник. В результате получено 68 л водного экстракта с плотностью 1,008 г/см, который концентрируют в вакууме до объема 2 л (плотность концентрата 1,211 г/см3). Отгон воды объемом 66 л (плотность 0,997 г/см3) далее может быть повторно использован на стадии экстракции растительного сырья.
Полученные концентраты после первой и второй водной экстракций объединяют (объем объединенного концентрата 6 л, плотность 1,409 г/см3), сушат в вакуум-сушильном шкафу при температуре 60°С и давлении 0,1 атм в течение 5,5 часов и измельчают на мельнице пропеллерного типа. Получают 2,2 кг продукта, что составляет 44% от массы растительного сырья. Средство представляет собой рассыпчатый негигроскопичный порошок, коричневого цвета, с горьким вкусом и специфическим запахом. Потеря массы при высушивании составляет 3,8%. Шрот растительного сырья массой 22 кг и влажностью 87% далее не используют и направляют в отвал.
Пример 3. 5,20 кг листьев серпухи васильковой с влажностью 5,2% измельчают на мельнице до размера частиц диаметром 2-3 мм. Измельченные листья серпухи васильковой (5 кг) загружают в экстракционный аппарат с мешалкой и внешним паровым обогревателем и заливают 85 л воды (плотность 0,997 г/см3). Полученную смесь перемешивают, вносят стержневой ультразвуковой процессор и обрабатывают смесь ультразвуком мощностью 50 кГц в импульсном режиме при температуре 94°С в течение 70 мин. После этого ультразвуковой процессор удаляют, смесь фильтруют через сукно в сборник, остаток на фильтре дополнительно промывают 5 л воды очищенной. В результате получено 81 л водного экстракта с плотностью 1,027 г/см3, который концентрируют в вакууме до объема 4 л (плотность концентрата 1,433 г/см3). Отгон воды объемом 77 л (плотность 0.997 г/см3) далее может быть повторно использован на стадии экстракции растительного сырья. Остаток сырья после первой экстракции водой переносят в экстракционный аппарат, заливают 78 л воды и экстрагируют в указанных условиях 20 мин. Смесь фильтруют через сукно в сборник. В результате получено 75 л водного экстракта с плотностью 1,011 г/см3, который концентрируют в вакууме до объема 2 л (плотность концентрата 1,214 г/см3). Отгон воды объемом 73 л (плотность 0,997 г/см3) далее может быть повторно использован на стадии экстракции растительного сырья. Полученные концентраты после первой и второй водной экстракций объединяют (объем объединенного концентрата 6 л, плотность 1,414 г/см3), сушат в вакуум-сушильном шкафу при температуре 55°С и давлении 0,1 атм в течение 5 часов и измельчают на мельнице пропеллерного типа. Получают 2,3 кг продукта, что составляет 46% от массы растительного сырья. Средство представляет собой рассыпчатый негигроскопичный порошок, коричневого цвета, с горьким вкусом и специфическим запахом. Потеря массы при высушивании составляет 4,0%. Шрот растительного сырья массой 24 кг и влажностью 86% далее не используют и направляют в отвал.
Химический состав средства, количественный анализ и показатели качества средства
С применением метода ВЭЖХ [17] изучен химический состав разработанного средства, в котором установлено присутствие таких фитокомпонентов как 1-O-кофеилхинная кислота, 4-О-кофеилхинная кислота, 5-О-кофеилхинная кислота, 1,3-ди-О-кофеилхинная кислота, 1,5-ди-О-кофеилхинная кислота, 3,4-ди-О-кофеилхинная кислота, 3,5-ди-О-кофеилхинная кислота, 4,5-ди-О-кофеилхинная кислота, а также арбутин, апигенин-7-О-глюкуронид, хризоэриол-7-О-глюкуронид, 20-гидроксиэкдизон и инокостерон.
Для осуществления химической стандартизации средства разработаны методика количественного анализа лютеолин-7-О-глюкуронида, розмариновой кислоты и пулегона в средстве методом ВЭЖХ-УФ.
Методика количественного анализа 5-О-кофеилхинной кислоты в средстве методом ВЭЖХ. Испытуемый раствор. 20 мг средства помещают в пластиковую пробирку типа Эппендорф вместимостью 2 мл, прибавляют 1 мл 80% этанола и растворяют в ультразвуковой ванне при 30°С в течение 15 мин. Охлаждают и центрифугируют при 3000 об/мин 10 мин. Надосадочную жидкость фильтруют через мембранный фильтр с диаметром пор 0.45 мкм.
Раствор сравнения. 1 мг 4-О-кофеилхинной кислоты и 1 мг 5-О-кофеилхинной кислоты растворяют в метаноле и доводят до объема 5 мл этим же растворителем.
Условия хроматографирования:
- колонка длиной 75 мм и внутренним диаметром 2 мм, заполненная силикагелем октадецилсилильным для хроматографии с размером частиц 5 мкм;
- температура: 35°С;
- подвижная фаза:
- подвижная фаза А: 21 г/л лития перхлората раствор в 1 г/л кислоте перхлорной;
- подвижная фаза В: ацетонитрил;
- спектрофотометрический детектор, длина волны 330 нм;
- время уравновешивания системы: 3 мин перед каждым вводом (5% В);
- объем вводимой пробы: 1 мкл.
- программа градиентного режима элюирования представлена в таблице 1.

Результаты: на хроматограмме должен быть один основной пик, совпадающий по подвижности с веществом в растворе сравнения (5-О-кофеилхинная кислота).
Порядок выхода пиков раствора сравнения: 4-О-кофеилхинная кислота → 5-О-кофеилхинная кислота.
Пригодность хроматографической системы. Хроматографическая система считается пригодной, если выполняются следующие условия: разрешение между пиками 4-O-кофеилхинной кислоты и 5-О-кофеилхинной кислоты не менее 2.
Расчет: содержание соединения в средстве в процентах (X) вычисляют по формуле:
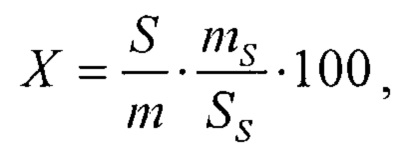 t
t
где S - площадь пика соединения в исследуемом растворе; m - масса навески средства, г; SS - площадь пика соединения в растворе сравнения; mS - масса навески соединения, г.
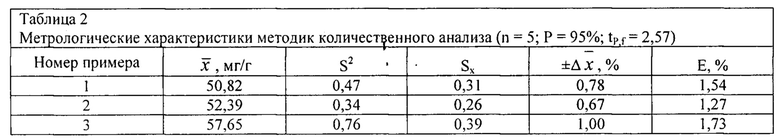
Метрологический анализ разработанных методик показал, что относительная ошибка определения 5-О-кофеилхинной кислоты методом ВЭЖХ не превышает 2% (таблица 2). Полученные результаты свидетельствуют об удовлетворительных валидационных параметрах методик, что указывает на возможность их использования в практике фармакопейного анализа для определения показателей качества разработанного средства.
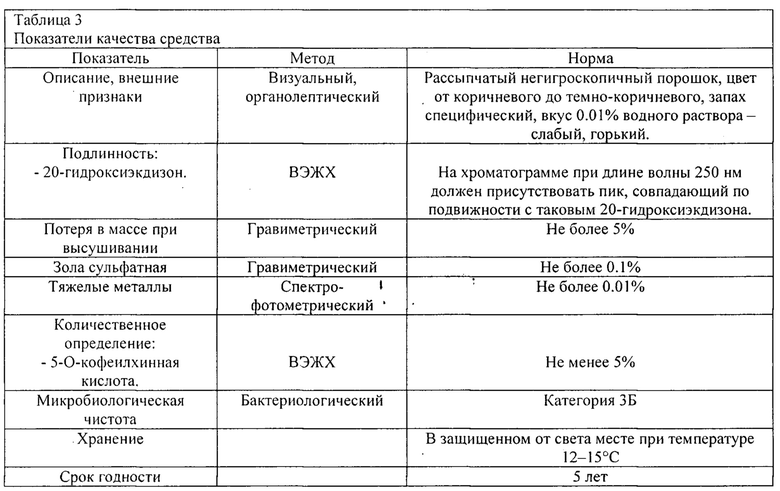
По данным проведенных исследований определены общие показатели качества средства, обобщенные в таблице 3. Для стандартизации средства было предложено определение внешнего вида, подлинности (присутствие 20-гидроксиэкдизона), потери в массе при высушивании, золы сульфатной, тяжелых металлов, количественное определение 5-О-кофеилхинной кислоты (ВЭЖХ) и микробиологической чистоты.
Предлагаемый. способ, по сравнению с известным, позволяет получить препарат постоянного состава с более выраженной активностью за счет более высокого содержания действующих веществ (кофеилхинных кислот).
Рассчитать экономическую целесообразность предлагаемого способа в настоящее время не представляется возможным, однако вышеуказанные преимущества в сочетании с простой схемой получения способствуют рациональному использованию лекарственного растительного сырья и определяют перспективность внедрения данного способа в фармацевтическую промышленность.
Фармакотерапевтические свойства средства.
Исследования выполнены на 48 белых крысах линии Wistar обоего пола массой 160-180 гр. Содержание животных соответствовало «Правилам надлежащей лабораторной практики» (GLP) и Приказу МЗ РФ №199Н от 01.04.2016 г. «Об утверждении Правил надлежащей лабораторной практики». Экспериментальную работу осуществляли в соответствии с Правилами, принятыми в Европейской конвенции по защите позвоночных животных (Страсбург, 1986 г.). Животных, соответствующих критериям эксперимента, разделяли на 4 группы с учетом принципа рандомизации: интактная, контрольная и две опытных. Холинергический дефицит у животных контрольной и опытных групп вызывали введением скополамина гидрохлорида (1 мг/кг, внутрибрюшинно) в течение 21 дня [18]. Далее на протяжении 14 дней животные I и II опытных групп получали исследуемые объекты в дозе 100 мг/кг - экстракт сухой серпухи васильковой (далее средство) и танакан (BEAUFOUR IPSEN INDUSTRIE, Франция) соответственно. На 31 сутки у животных вырабатывали условный рефлекс пассивного избегания (УРПИ), который проверяли через 1 час, 24 и 72 часа. На 35 сутки для проведения биохимических и морфологических исследований животных декапитировали под эфирным наркозом. На гистологических срезах коры больших полушарий и гиппокампа, окрашенных по Нисслю, определяли количество (%) нормохромных, резко гиперхромных, резко гипохромных нейронов и «клеток-теней». Состояние про- и антиоксидантной систем характеризовали по концентрации малонового диальдегида (МДА) [19], активности каталазы [20], глутатионпероксидазы и глутатионредуктазы [21] в гомогенате головного мозга.
Обработку результатов осуществляли с помощью пакета программ Statistica for Windows 6.0. Статистические различия между выборками оценивали с помощью t-критерия Стьюдента, данные представлены в виде среднего и стандартного отклонения (M±SD). Различия считались достоверными при достижении уровня значимости р≤0,05.
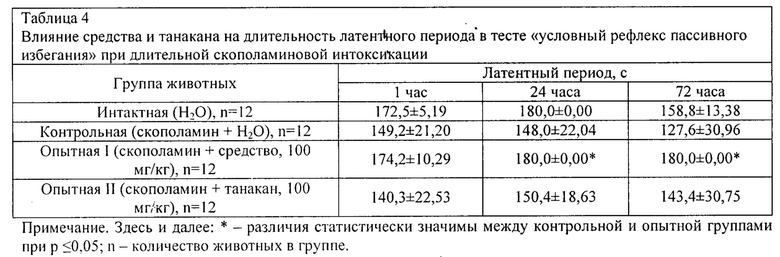
Результаты исследований показали, что в контрольной группе условный рефлекс выработался у 75% животных, и на 3 сутки он сохранился только у 58%) животных, и, как следствие, латентный период во все сроки наблюдения был значимо ниже показателя у интактных животных (таблица 4). При этом в I опытной группе УРПИ сформировался у 100% животных, а во II опытной группе - только у 75% животных. При проверке сохранности УРПИ через 24 и 72 часа установлено, что рефлекс сохранился у 100% животных (р≤0,05), получавших средство, а латентный период выше такового показателя в контроле в 1,3 и 1,5 раза соответственно срокам тестирования.
Результаты патоморфологических исследований показали, что на фоне скополаминовой интоксикации в коре больших полушарий развиваются структурные изменения, характеризующиеся увеличением числа гиперхромных нейронов в 5,3 раза, а также «клеток-теней» в 2,0 раза в сравнении с результатами у животных интактной группы (Таблица 5).
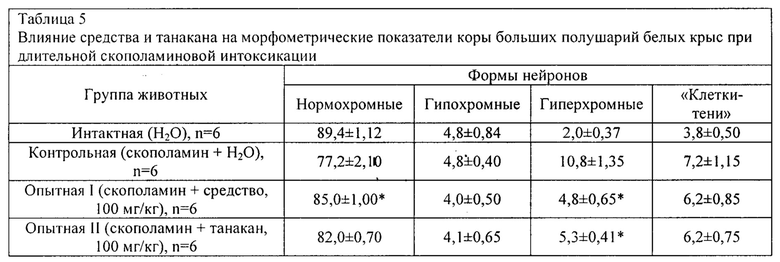
На микропрепаратах животных контрольной группы отмечаются нейроны, уменьшенные в размерах с дистрофическими изменениями в виде истончения дендритов, нечеткости ядерных компонентов на фоне гомогенной цитоплазмы. Гиперхромные клетки выявляются преимущественно во II и III слоях, «клетки-тени» располагаются диффузно во всех слоях коры больших полушарий. Наблюдается периваскулярный отек, а также явления нейронофагии. Кроме того, в нейронах при холинергическом дефиците отмечается вакуолизация нейропиля, гиперхроматические и сморщенные ядра, а также измененная форма апикальных дендритов - в форме «штопора» и слияние мембраны с перикариальной цитоплазмой.
На фоне введения животным средства и танакана количество «клеток-теней» уменьшается в среднем на 14%, а количество гиперхромных пикнотических нейронов -на 55 и 50% соответственно по сравнению с данными у животных контрольной группы (таблица 5). Гиперхромные нейроны у животных опытных групп не образуют скопления, встречаются одиночно; явления нейронофагии и сателлитоза не выявляются. У животных, получавших исследуемый экстракт, также отмечалось статистически значимое снижение количества гиперхромных нейронов (на 24%) в гиппокампе относительно контрольного показателя (таблица 6).
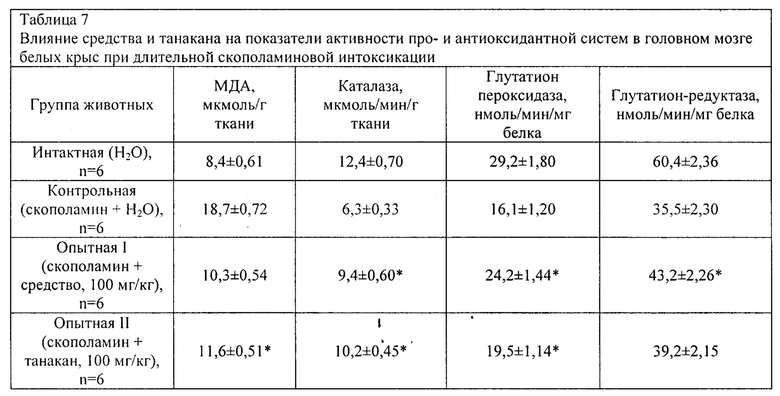
На фоне длительного введения скополамица в гомогенате головного мозга животных контрольной группы наблюдаются повышение содержания МДА в 2,2 раза, снижение активности каталазы, глутатионпероксидазы и глутатионредуктазы на 49, 45 и 41% соответственно по сравнению с таковыми у интактных животных (таблица 7).

Применение средства способствует ингибированию реакций свободно-радикального окисления и повышению активности ферментов антиоксидантной системы в головном мозге белых крыс. В частности, на это указывает снижение концентрации МДА на 45%, увеличение активности каталазы и глутатионпероксидазы в среднем в 1,5 раза и глутатионредуктазы - на 22% по сравнению с данными у контрольных животных. Введение препарата сравнения увеличивало активность каталазы (на 62%) и глутатионпероксилазы (на 21%) относительно контрольных показателей.
Таким образом, средство в дозе 100 мг/кг оказывает нейропротективное действие на фоне холинергического дефицита, нормализуя когнитивные функции, снижая количество регрессивных форм нейронов в коре больших полушарий и гиппокампе, а также ингибируя реакции свободно-радикального окисления и активируя активность антиоксидантных ферментов в головном мозге.
Источники информации
1. Оленников Д.Н., Кащенко Н.И. Фитоэкдистероиды родов Serratula L. и Klasea Cass. (Asteraceae): Хеморазнообразие, методы выделения и анализа // Химия растительного сырья. - 2017. -№4. - С.123-135. DOI:10.14258/jcprm.2017042016.
2. Лекарственный сбор для лечения сердечно-сосудистых заболеваний. Патент РФ 2484843 С1. Опубликовано: 20.06.2013. Бюл. №17.
3. Онкологический растительный сбор для лечения рака. Патент РФ 2246963 С1. Опубликовано: 27.02.2005. Бюл. №6.
4. Онкологический растительный сбор "Биалан-2" для лечения оперированных онкобольных. Патент РФ 2003115035 А. Дата публикации заявки: 27.11.2004.
5. Фитокомплекс для лечения цирроза печени и способ лечения с его применением. Патент РФ 2606835 С1. Опубликовано: 10.01.2017. Бюл. №1.
6. Сбор лекарственных растений для лечения эцилепсии. Патент РФ 2016104048 А. Дата публикации заявки: 11.08.2017. Бюл. №23.
7. Способ восстановления полового влечения (либидо) у мужчин путем применения биологически активной добавки к пище для восстановления полового влечения (либидо) у мужчин. Патент РФ 2496491 С1. Опубликовано: 27.10.2013. Бюл. №30.
8. Препарат для оздоровления сердечно-сосудистой системы, обладающий кардиопротекторным, седативным и гипотензивным действием. Патент РФ 2704323 С1. Опубликовано: 28.10.2019. Бюл. №31.
9. Противодиабетическое средство с гиполипидемической активностью для лечения и профилактики сахарного диабета II типа. Патент РФ 2337698 С1. Опубликовано: 10.11.2008. Бюл. №31.
10. Гиполипидемическое и противоишемическое средство "Серпистен". Патент РФ 2337701 С1. Опубликовано: 10.11.2008. Бюл. №31.
11. Тонизирующее и актопротектроное средство "Серпистен". Патент РФ 2276991 С1. Опубликовано: 27.05.2006. Бюл. №15.
12. Антиагрегационное и стресс-лимитирующее средство. Патент РФ 2375071 С1. Опубликовано: 10.12.2009. Бюл. №34.
13. Противолучевое средство. Патент РФ 2326672 С2. Опубликовано: 20.06.2008. Бюл. №17.
14. Способ получения средства, обладающего антигипоксической активностью. Патент РФ 2669365 С1. Опубликовано: 11.10.2018. Бюл. №29.
15. Способ получения средства, обладающего стресспротективной и антиоксидантной активностью. Патент РФ 2619856 С1. Опубликовано: 18.05.2017. Бюл. №14.
16. Olennikov, D.N., Kashchenko, N.I. Phytoecdysteroids of Serratula centauroides herb from Cisbaikalia // Russian Journal of Bioorganic Chemistry. - 2019. - Vol.45. - P. 913-919. DOI: 10.1134/S1068162019070094.
17. Shantanova L.N., Olennikov D.N., Matkhanov I.E., Gulyaev S.M., Toropova A.A., Nikolaeva I.G., Nikolaev S.M. Rhaponticum uniflorum and Serratula centauroides extracts attenuate emotional injury in acute and chronic emotional stress //Pharmaceuticals. - 2021. -Vol.14.-No 1186. DOI:10.3390/ph14111186.
18. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. Под ред. А.Н. Миронова. - М.: Гриф и К, 2012: 944 с.
19. Камышников B.C. Справочник по клинико-биохимическим исследованиям и лабораторной диагностике. - М., 2009. - 890 с.
20. Королюк М.А. Метод определения активности каталазы // Лабораторное дело. - 1988. -№1.-С.16-19.
21. Pinto R.E., Bartley W. The effect of age and sex on glutathione reductase and glutation peroxidase activities and aerobic glutathione oxidation in rat liver homogenates // Biochemical Journal. - 1969. - Vol.112(1).-P. 109-115.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО СРЕДСТВА, ОБЛАДАЮЩЕГО АНКСИОЛИТИЧЕСКИМ И АНТИДЕПРЕССИВНЫМ ДЕЙСТВИЕМ | 2018 |
|
RU2678586C1 |
| Способ получения средства, обладающего стресспротективной и антиоксидантной активностью | 2016 |
|
RU2619856C1 |
| Способ получения средства, обладающего антигипоксической активностью | 2017 |
|
RU2669365C1 |
| Способ получения средства, обладающего нейропротективной, иммуномодулирующей активностью | 2022 |
|
RU2784435C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО СРЕДСТВА, ОБЛАДАЮЩЕГО ИММУНОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2016 |
|
RU2639132C1 |
| Способ получения иммуностимулирующего средства из шрота ягод брусники обыкновенной | 2021 |
|
RU2775065C1 |
| Способ получения растительного средства, обладающего гастропротекторным действием | 2023 |
|
RU2812531C1 |
| Композиции для получения бальзама | 2022 |
|
RU2797913C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОИШЕМИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2603465C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2173161C1 |
Изобретение относится к области фармацевтической промышленности и касается способа получения средства, обладающего нейропротективным действием. Способ получения средства, обладающего нейропротективным действием, из листьев серпухи васильковой путем экстрагирования растительного материала, в котором измельченный до размера частиц диаметром 2-3 мм растительный материал смешивают с водой в соотношении сырье : экстрагент 1:(15-17), подвергают смесь ультразвуковой обработке с частотой 50 кГц при 90-94°С в течение 50-70 мин, смесь фильтруют и промывают на фильтре дополнительным объемом воды, составляющим 1:1 от массы измельченного растительного сырья, экстракцию повторяют в тех же условиях в течение 20-40 мин, водные извлечения концентрируют в вакууме до 1/17,5-1/37,5 от первоначального объема, сконцентрированные извлечения объединяют, высушивают, измельчают. Вышеописанный способ обеспечивает получение суммарного растительного средства, содержащего кофеилхинные кислоты, обладающего повышенным нейропротективным действием за счет высокого содержания действующих веществ. 7 табл., 3 пр.
Способ получения средства, обладающего нейропротективным действием, из листьев серпухи васильковой путем экстрагирования растительного материала, отличающийся тем, что измельченный до размера частиц диаметром 2-3 мм растительный материал смешивают с водой в соотношении сырье : экстрагент 1:(15-17), подвергают смесь ультразвуковой обработке с частотой 50 кГц при 90-94°С в течение 50-70 мин, смесь фильтруют и промывают на фильтре дополнительным объемом воды, составляющим 1:1 от массы измельченного растительного сырья, экстракцию повторяют в тех же условиях в течение 20-40 мин, водные извлечения концентрируют в вакууме до 1/17,5-1/37,5 от первоначального объема, сконцентрированные извлечения объединяют, высушивают, измельчают.
| Способ получения средства, обладающего стресспротективной и антиоксидантной активностью | 2016 |
|
RU2619856C1 |
| РАЗУВАЕВА Я.Г | |||
| и др | |||
| Влияние экстракта сухого Serratula centauroides на поведение белых крыс в тестах с положительным подкреплением // Фитофармакология, том 19, N2, 2021, стр | |||
| Прибор для корчевания пней | 1921 |
|
SU237A1 |
| ОЛЕННИКОВ Д.Н | |||
| и др | |||
| Фитоэкдистероиды надземной части Serratula Centauroudes, произрастающей в Прибайкалье // Химия растительного сырья | |||
Авторы
Даты
2023-10-23—Публикация
2022-07-27—Подача